Занятие №16 Основные положения мкт. Масса и размеры молекул. Мкт- молекулярно- кинетическая теория
| Вид материала | Задача |
- Молекулярная физика и термодинамика. Лекция №1 Молекулярно-кинетическая теория Основные, 10053.18kb.
- Тема: Молекулярно-кинетическая теория, 131.48kb.
- Молекулярная структура вещества. Скорости газовых молекул, 140.08kb.
- Эртильская средняя общеобразовательная школа №1 «Молекулярно – кинетическая теория, 233.1kb.
- Тема урока: «Основные положения молекулярно-кинетической теории», 62.02kb.
- Ох, уж эти молекулы, 53.23kb.
- Молекулярно-кинетическая теория, 37.31kb.
- Молекулярно-кинетическая теория газов, 97.72kb.
- Программа «мкт-администратор» предназначена для обеспечения взаимодействия всех программных, 253.93kb.
- Контрольная работа "Молекулярно-кинетическая теория идеального газа. Газовые законы., 9.92kb.
Занятие №16
Основные положения МКТ. Масса и размеры молекул.
МКТ- молекулярно- кинетическая теория. Теория, объясняющая тепловые явления и свойства тел, на основании того, что вещества состоят из молекул, которые непрерывно движутся.
Основные положения МКТ:1. Все вещества состоят из молекул. 2. Молекулы непрерывно движутся. 3. Молекулы взаимодействуют друг с другом.
Молекула-это наименьшая частица вещества.
О
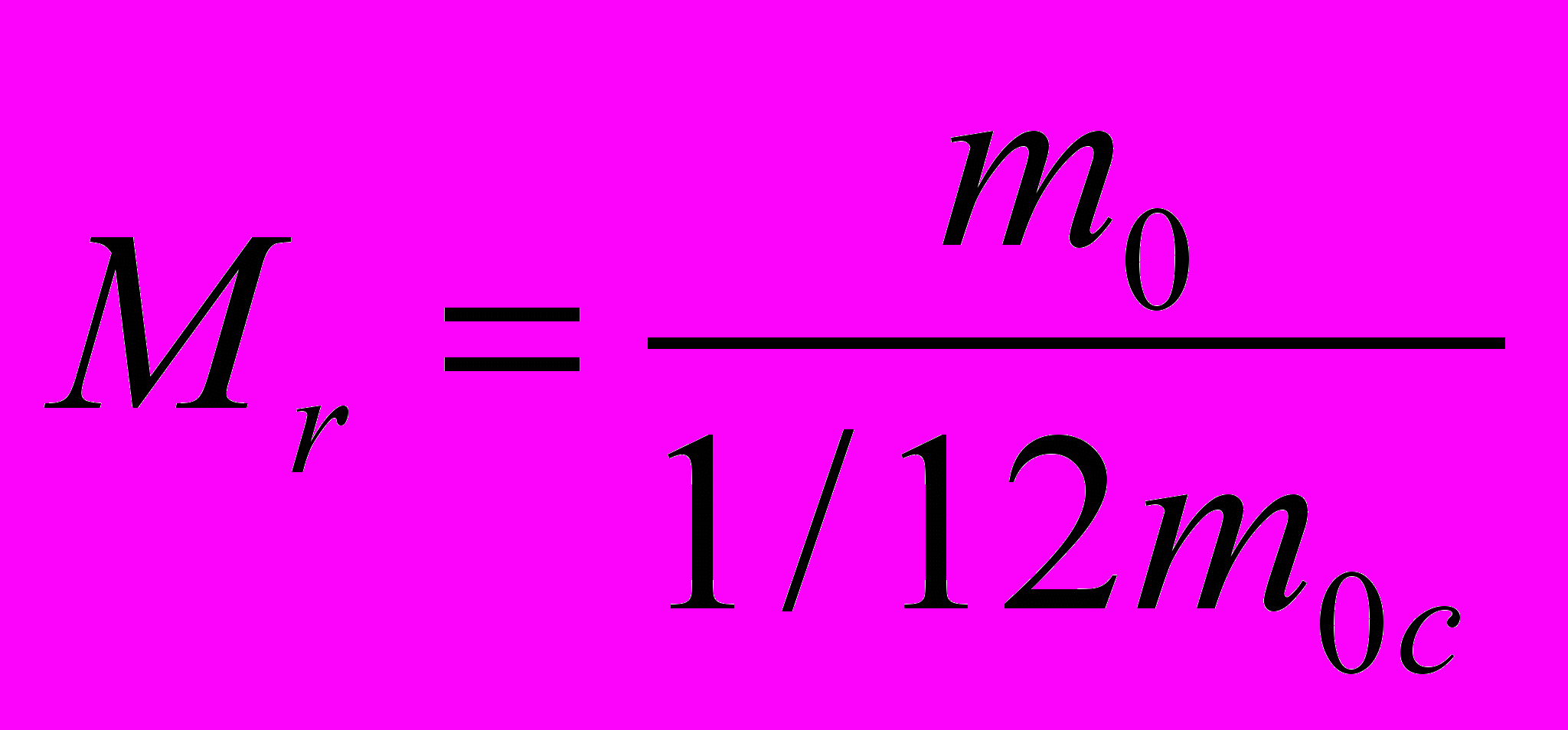 тносительная молекулярная масса - отношение массы одной молекулы данного вещества к 1/12 массы атома углерода.
тносительная молекулярная масса - отношение массы одной молекулы данного вещества к 1/12 массы атома углерода.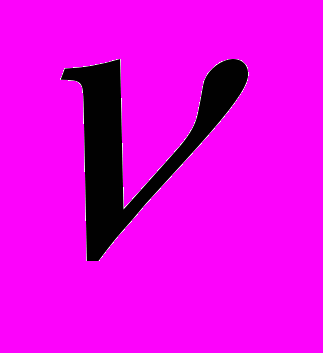
Количество вещества ( ) - это отношение числа частиц, содержащихся в теле к числу частиц, содержащихся в 0,012 кг углерода. В СИ измеряется в моль.
1 моль – это такое количество вещества в котором число молекул равно числу атомов углерода в
0,012 кг. Один моль содержит: NА- число Авогадро. NА=6,02.1023 1/моль.
М
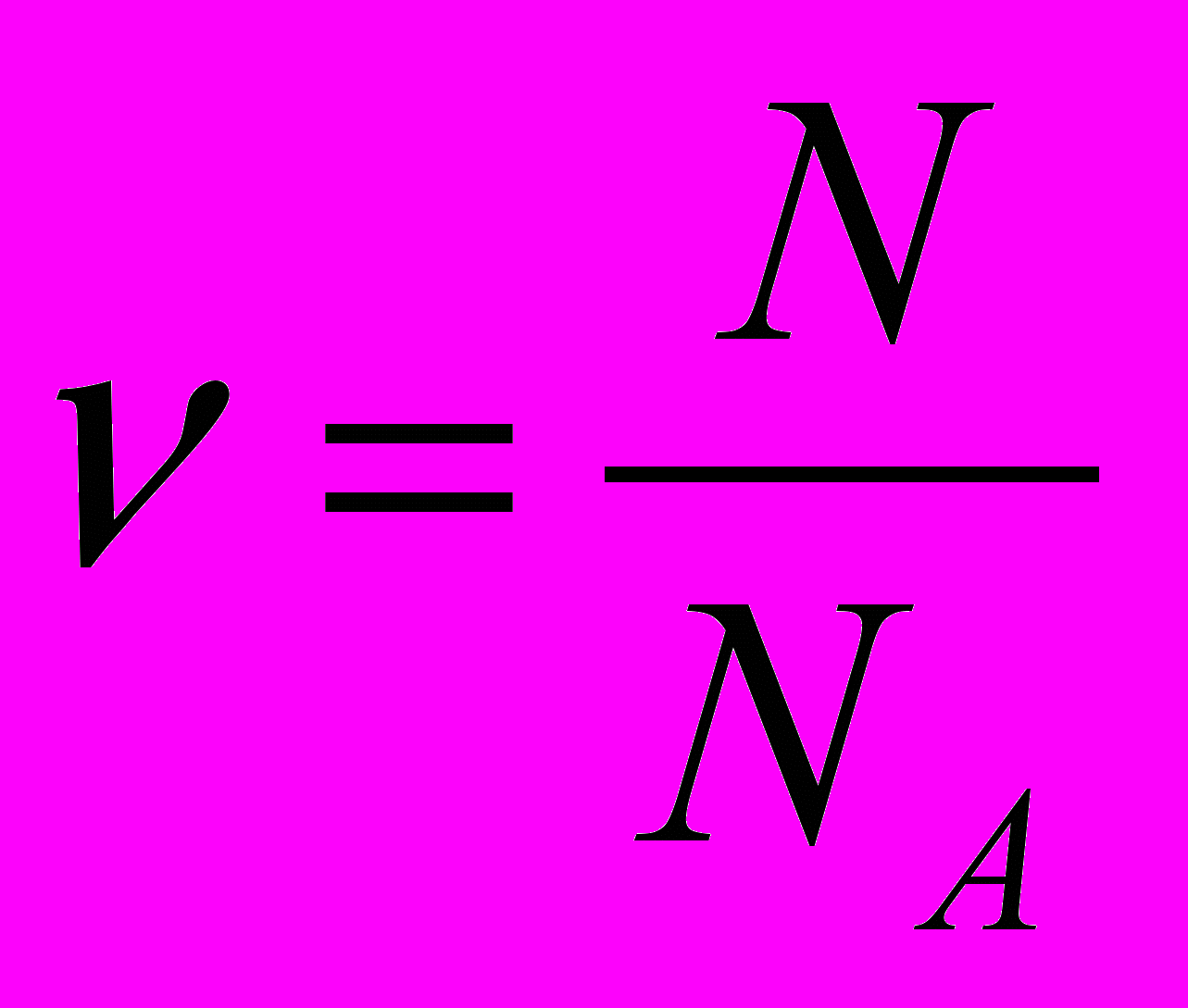
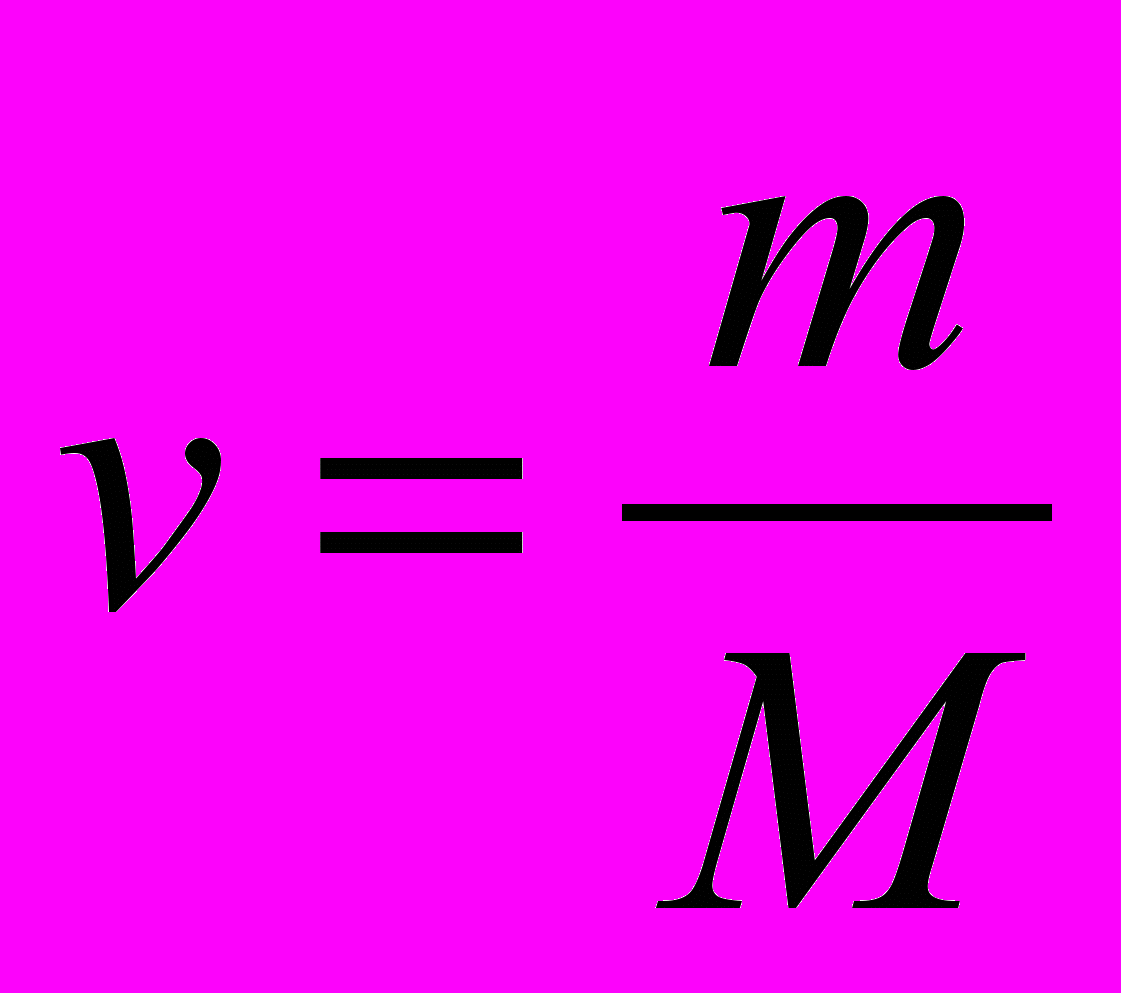 олярная масса – это масса 1 моль вещества.
олярная масса – это масса 1 моль вещества.Измеряется в килограммах на моль.
М=Мr .10-3 [кг/моль]
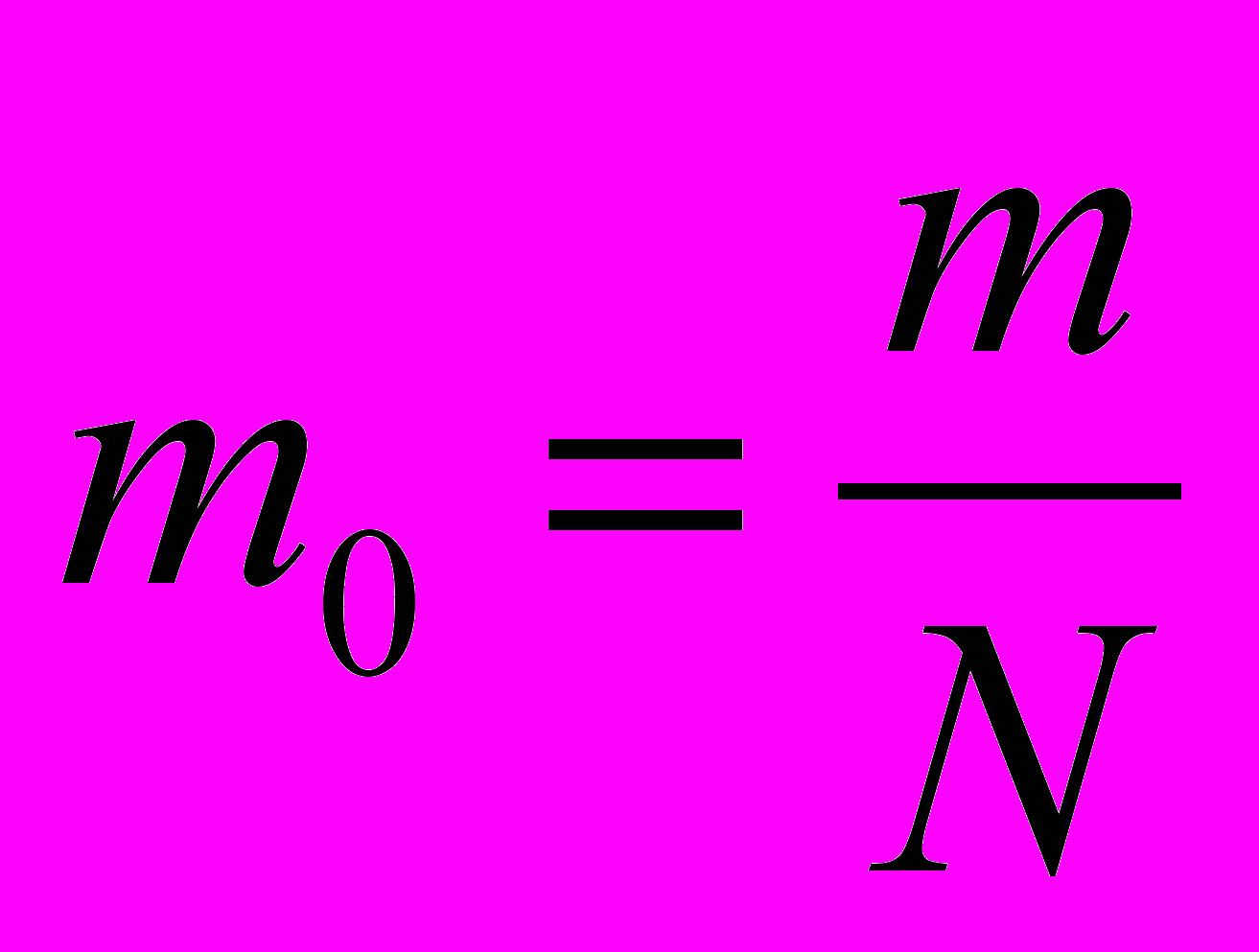
Масса одной молекулы
Задача №1.Какое количество вещества содержится в алюминиевой отливке массой 5,4 кг?
Задача №2. В сосуде находится 0,5 моль водорода Н2. Сколько молекул водорода в сосуде?
Домашнее задание. Выучить конспект. Решить задачу:№455. Какова масса 500 моль углекислого газа?
Занятие №17
Давление идеального газа. Основное уравнение МКТ. Шкала Кельвина. Температура в МКТ.
И
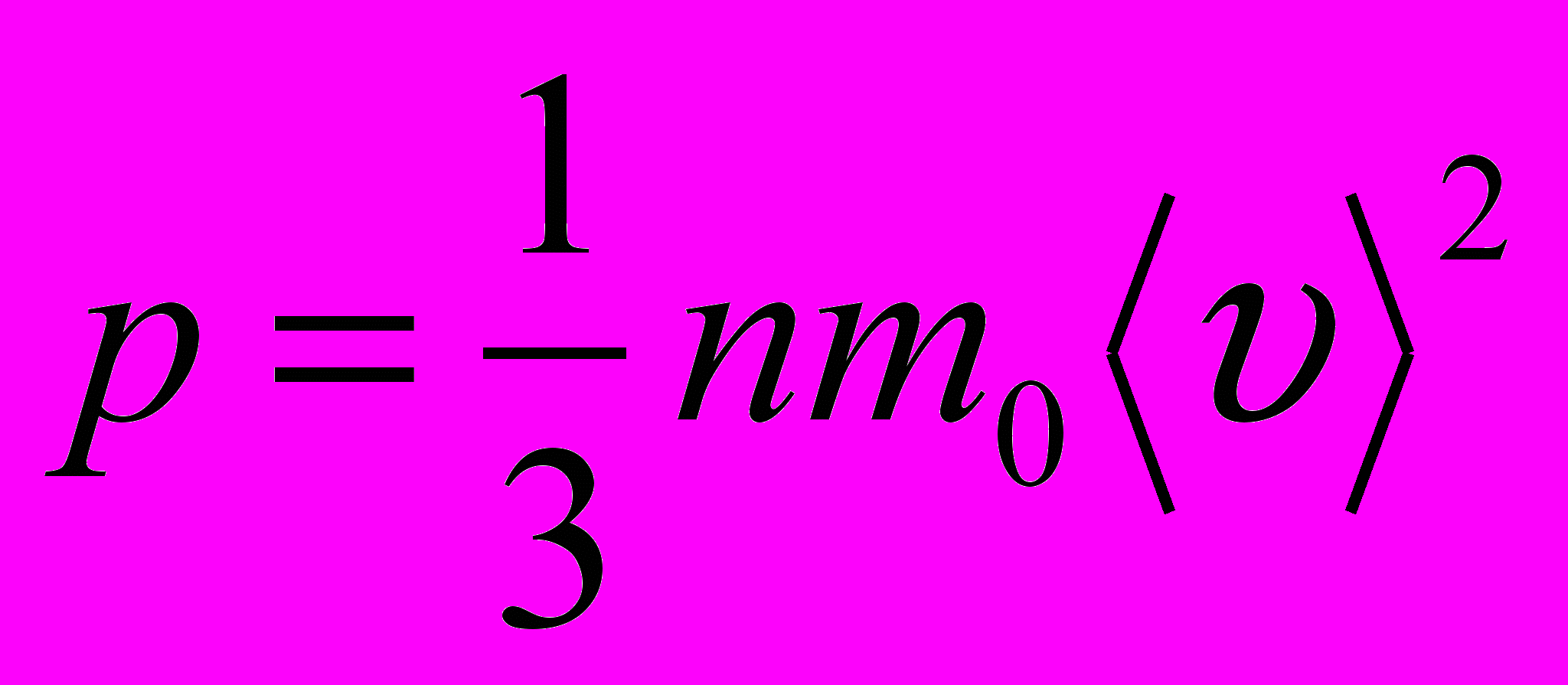 деальный газ- это теоретическая модель газа, в которой не учитываются размеры молекул.
деальный газ- это теоретическая модель газа, в которой не учитываются размеры молекул.Основное уравнение МКТ идеального газа
Анализ основного уравнения кинетической теории газов.
1. Вычисленное давление газа на внесённую в него пластину одинаково с обеих её сторон (согласно закону Паскаля); такое же давление испытывают стенки сосуда в котором находится газ.
2.Давление – это параметр газа в целом. Для отдельной молекулы этот параметр смысла не имеет.
3.Давление численно равно 2/3 кинетической энергии.
Максвелловское определение температуры.
Температура характеризует состояние теплового равновесия макроскопической системы: во всех частях системы, находящихся в состоянии теплового равновесия, температура имеет одно и тоже значение.
Абсолютная температура
(термодинамическая температура) (T)– это температура, введенная в 1848 г. английским физиком Томсоном (Кельвином) и связанная с температурой по шкале Цельсия соотношением T = (t + 273,15 0С). Измеряется в кельвинах (К). Отсчитывается от абсолютного нуля, для всех обычных тел положительна: Т > 0.
Перевод из шкалы Цельсия в шкалу Кельвина: Т=t+273
Т-Температура по шкале Кельвина
t- Температура в градусах Цельсия.
Абсолютный нуль – это температура, при которой средняя кинетическая энергия молекул равна нулю, т.е. прекращается тепловое движение молекул.
Задача №1. Сравнить давления кислорода и водорода при одинаковых концентрациях молекул и равных средних квадратичных скоростях их движения.
Задача №2. Найти концентрацию молекул кислорода, если при давлении 0,2 МПа средняя квадратичная скорость его молекул равна 700 м/с.
Домашнее задание. Учить конспект. Решить задачу: перевести в Кельвины: 16 оС, 25 оС, 38 оС.
Занятие №18
У
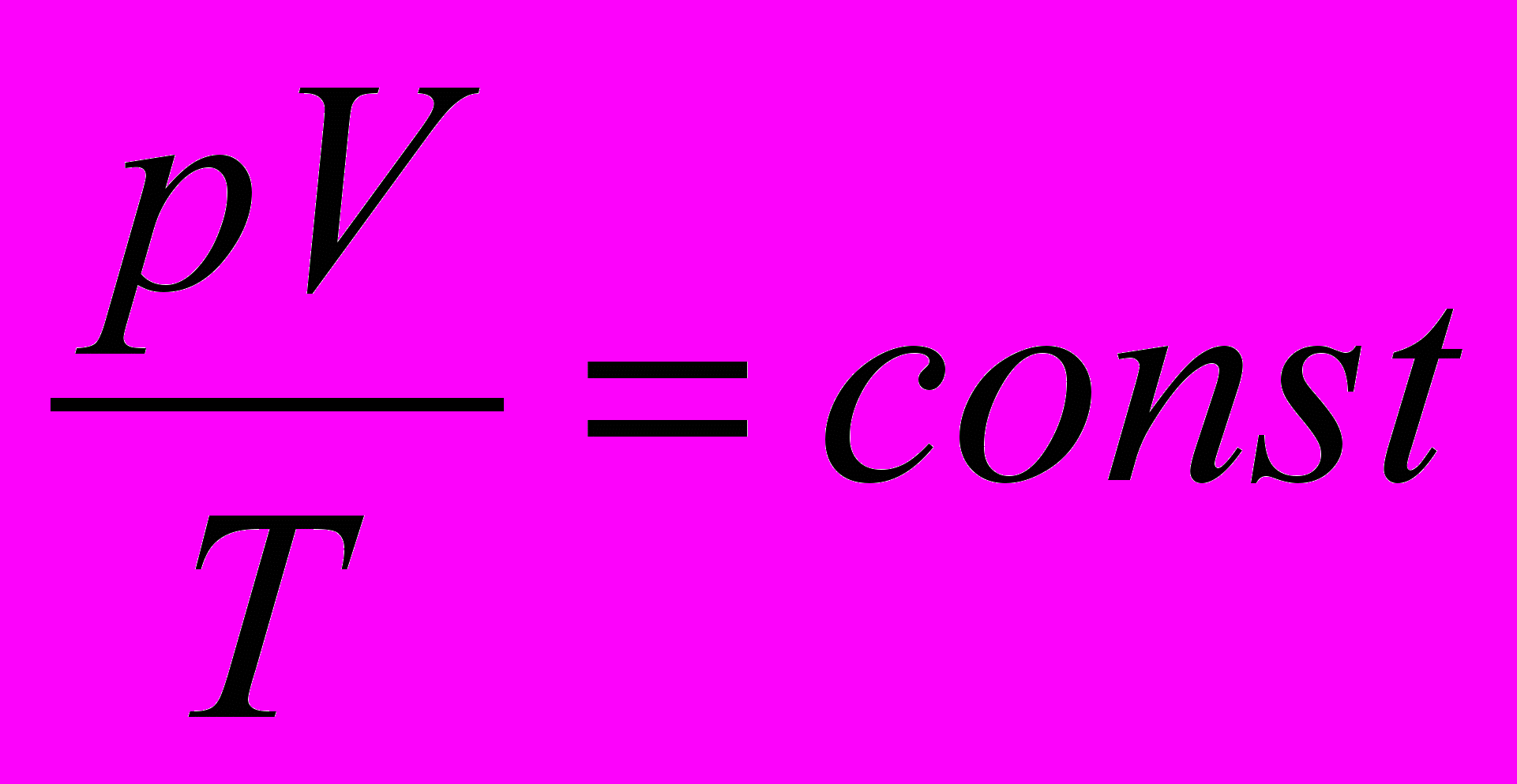 равнение Менделеева- Клапейрона. Изопроцессы.
равнение Менделеева- Клапейрона. Изопроцессы.Уравнение Клапейрона:
У
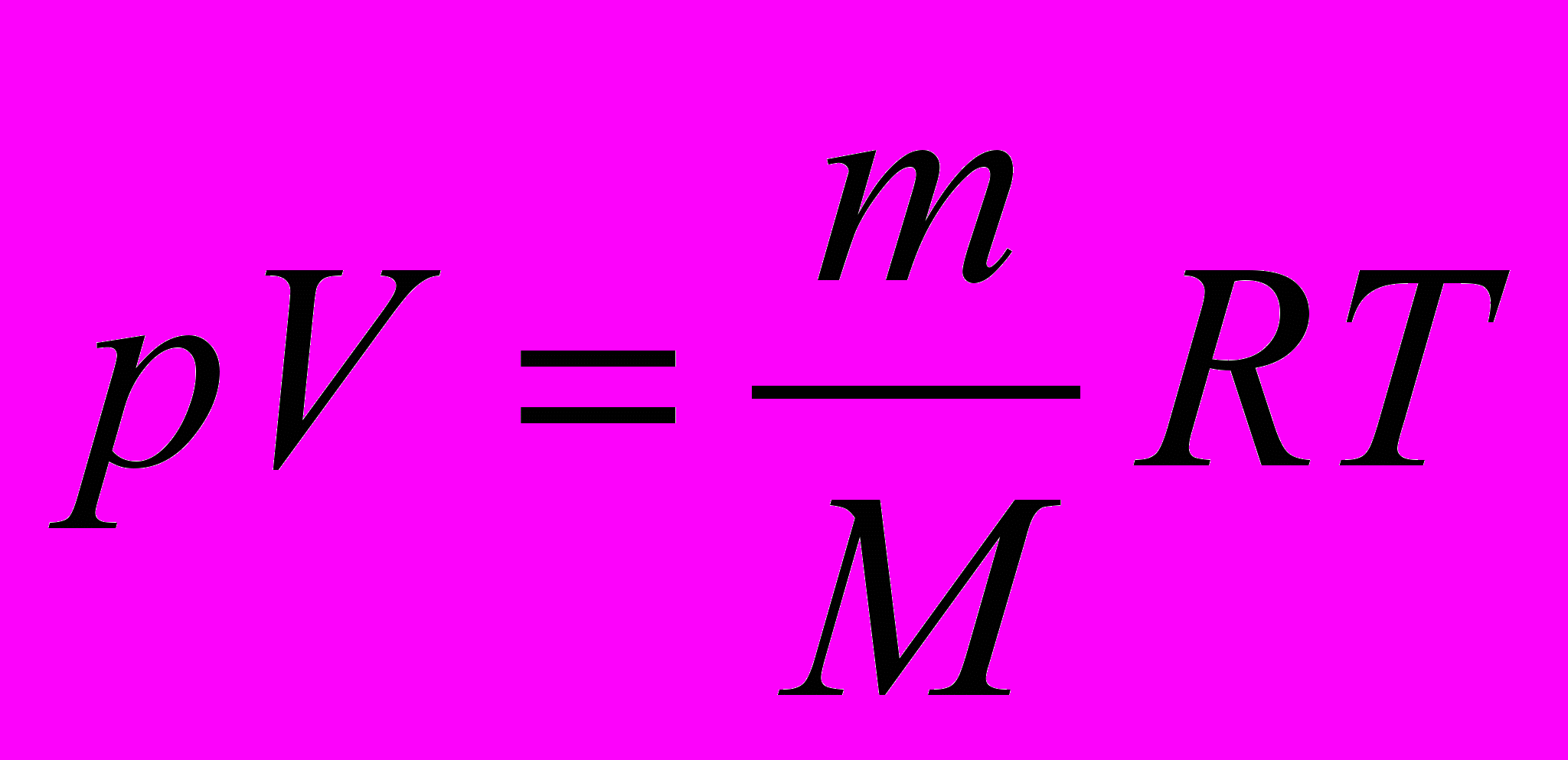 равнение Менделеева- Клапейрона. P- давление газа [Па]; V- объём газа [м3]; m- масса газа [кг]; М- молярная масса [кг/моль]; R-универсальная газовая постоянная R=8,31[Дж/(моль.К)]; R=NA.k;
равнение Менделеева- Клапейрона. P- давление газа [Па]; V- объём газа [м3]; m- масса газа [кг]; М- молярная масса [кг/моль]; R-универсальная газовая постоянная R=8,31[Дж/(моль.К)]; R=NA.k; T- температура газа [K].
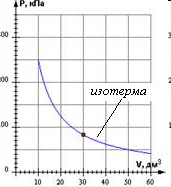
Изотермический процесс
T=const; p1V1=p2V2 Закон Бойля- Мариотта.
Изобарный процесс
P
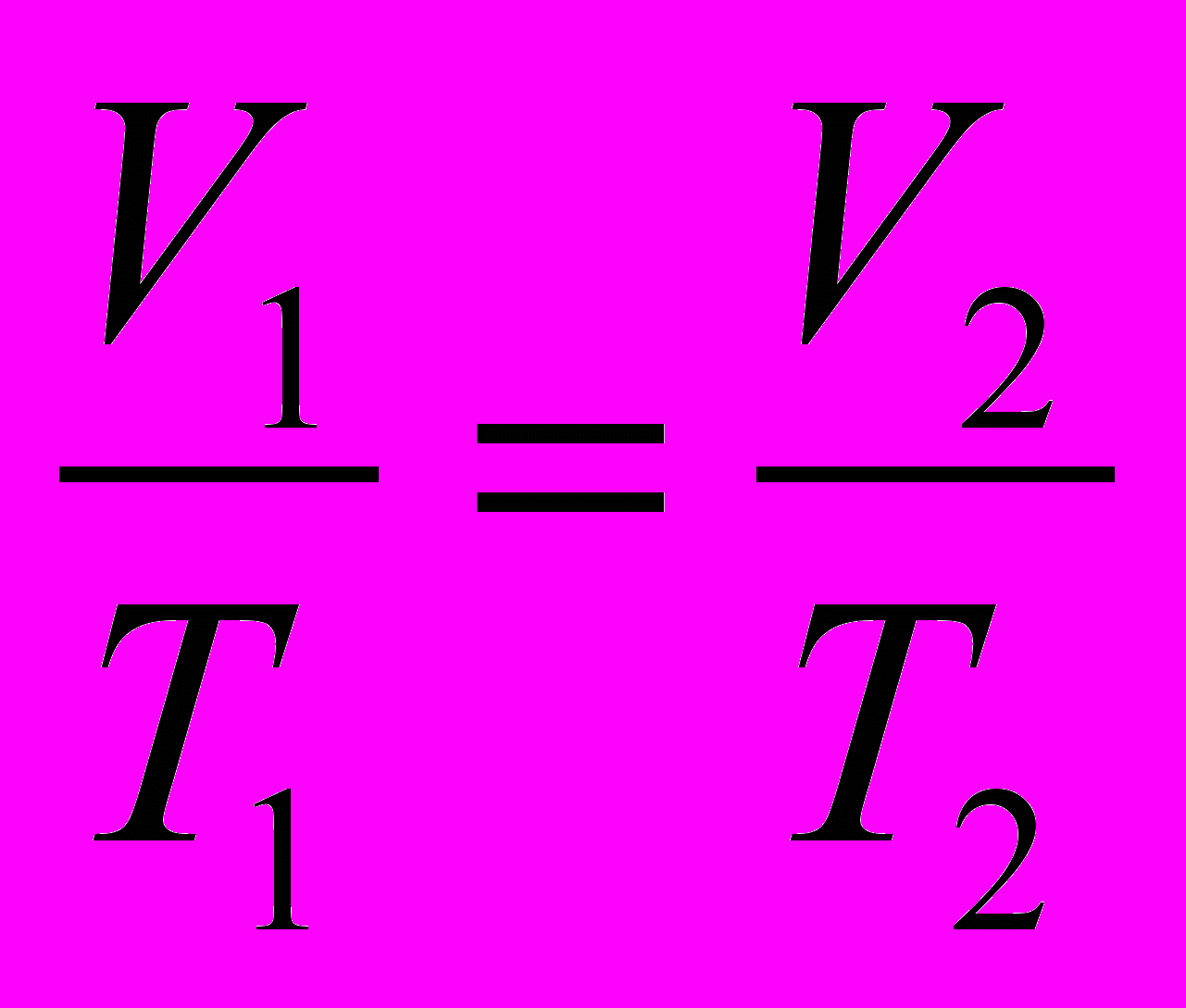 =const; Закон Гей- Люссака.
=const; Закон Гей- Люссака. 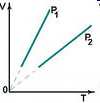
И
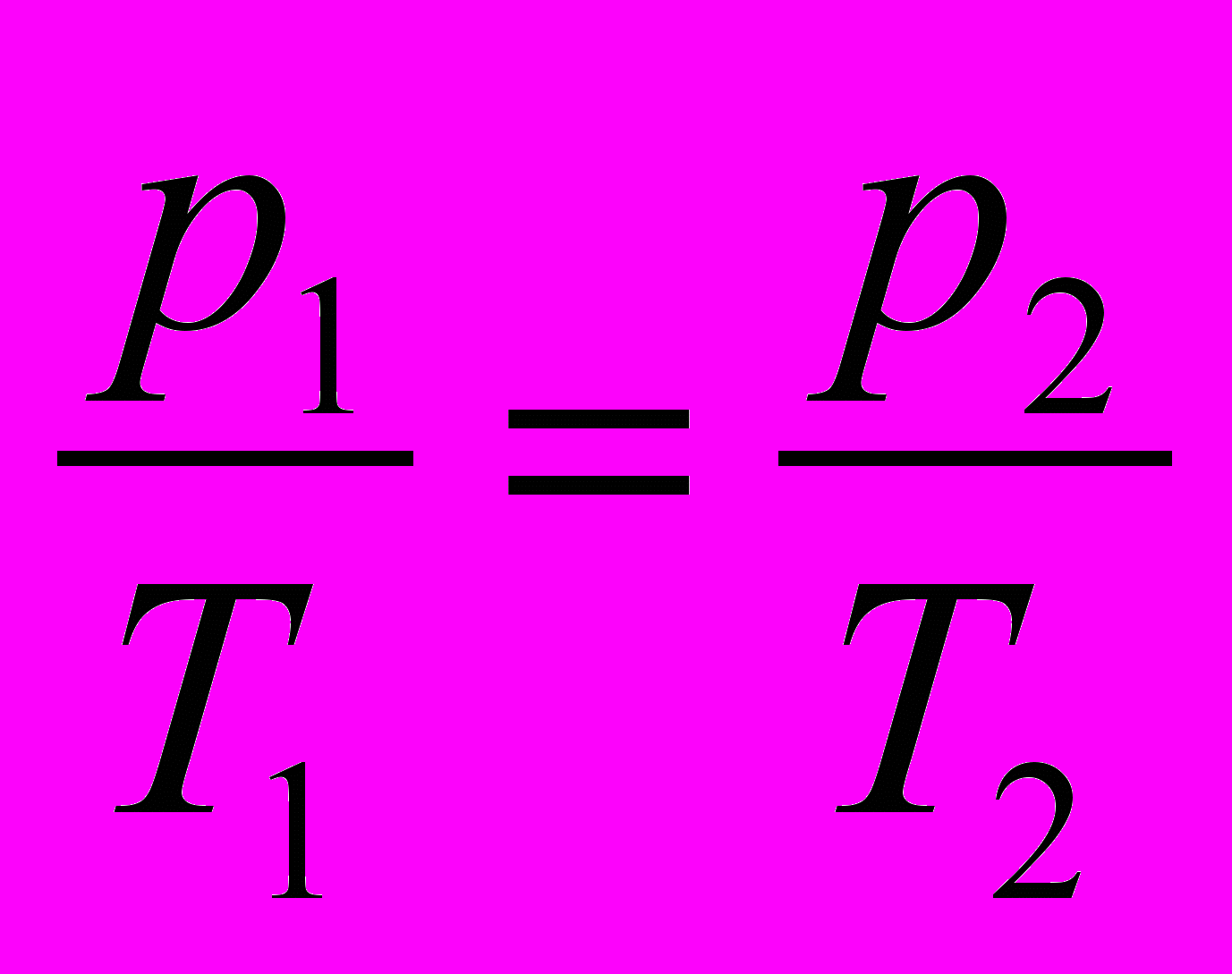 зохорный процесс
зохорный процессV=const;
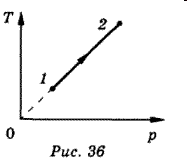 Закон Шарля.
Закон Шарля.Задача №1. Баллон объёмом 0,02 м3, содержащий воздух под давлением 4.105 Па, соединяют с баллоном объёмом 0,06 м3, из которого воздух выкачан. Найти давление, которое установится в баллонах. Ответ выразить в килопаскалях (кПа).
Задача №2. Газ изотермически сжат от объёма 6л до объёма 3л. Давление его при этом повысилось до 2.105 Па. Каково первоначальное давление газа? Ответ выразить в мегапаскалях (МПа).
Домашнее задание: 1. Учить конспект. 2. Решить задачу: №527.
Какой объём займёт газ при температуре 770С, если при температуре 270С его объём был 6л?
Занятие №20
Фазы вещества. Испарение, кипение.
Твёрдая фаза (лёд) имеет и объём и форму.
Жидкая фаза (вода) имеет объём, но не имеет формы.
Газообразная фаза (пар) не имеет ни объёма, ни формы.
Испарение – это переход вещества из жидкого состояния в газообразное (парообразование), происходящий на свободной поверхности жидкости.
Скорость испарения зависит от сорта жидкости, увеличивается с возрастанием температуры жидкости, площади ее свободной поверхности и при наличии ветра (который уносит вылетевшие из жидкости молекулы, не давая им возвращаться в жидкость).
Кипение – это процесс интенсивного парообразования, происходящий как со свободной поверхности жидкости, так и по всему объему жидкости внутри образующихся в ней пузырьков пара.
Н
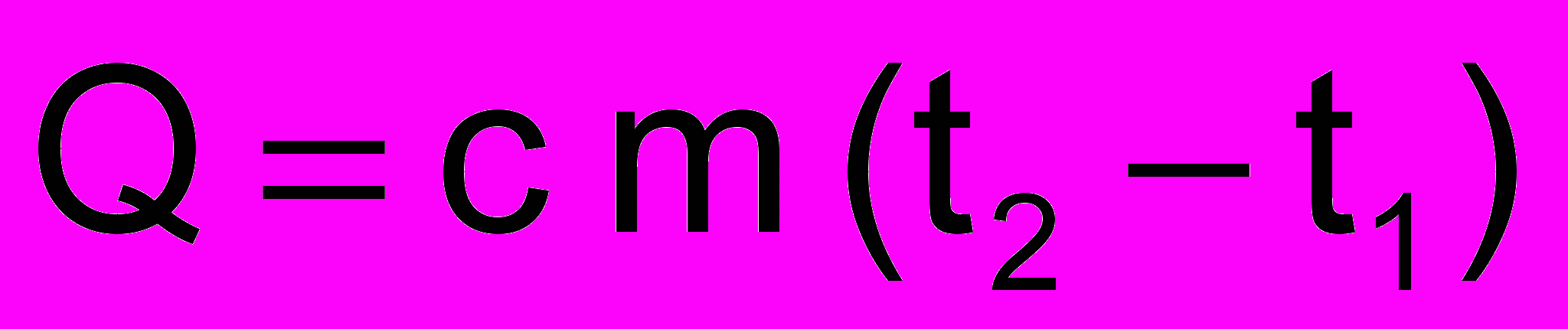 агревание или охлаждение
агревание или охлаждениеc- удельная теплоёмкость
[Дж/(кг .К)]
П
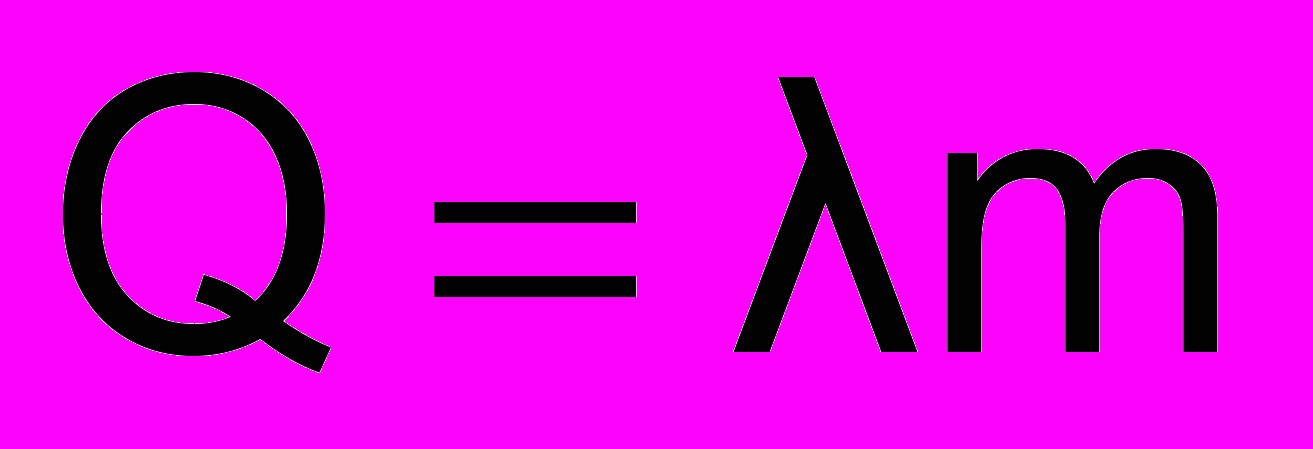 лавление или кристаллизация
лавление или кристаллизацияλ- удельная теплота плавления
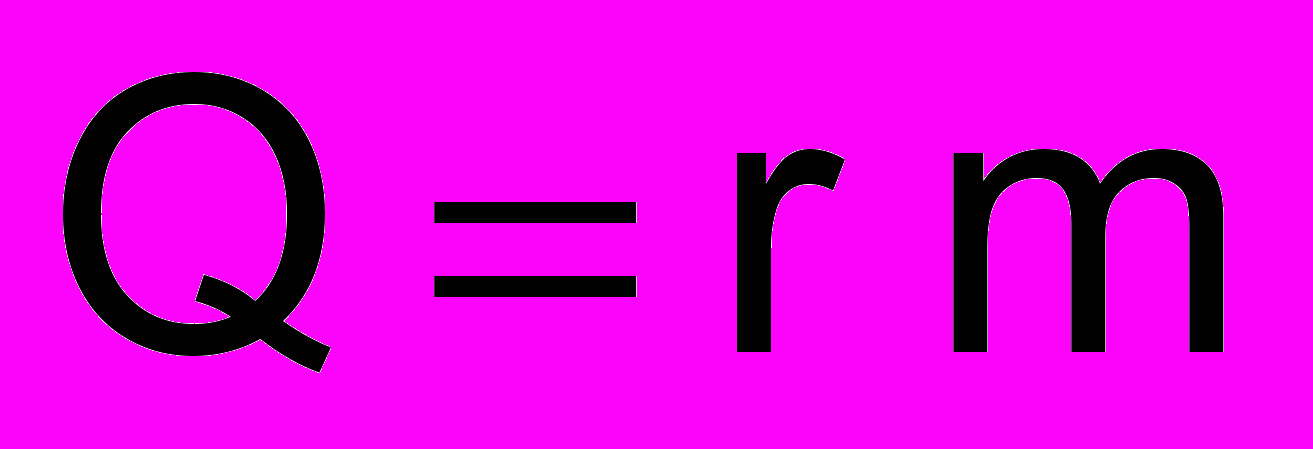 [Дж/кг]
[Дж/кг] Парообразование или конденсация
r- удельная теплота парообразования
[Дж/кг]
Задача №1. На сколько градусов нагреется 2 кг воды, получив 126 кДж теплоты? Удельная теплоёмкость воды 4200 Дж/(кг . К).
Задача №2.Какова масса стального слитка, если при его отвердевании выделилось 205 МДж теплоты? Удельная теплота плавления стали 82 кДж/кг. Ответ выразить в тоннах.
Домашнее задание. Выучить конспект. Решить задачу: Какое количество теплоты необходимо для нагревания 5 кг воды от10 до 900С? Удельная теплоёмкость воды 4200 Дж/(кг . К). Ответ выразить в мегаджоулях (МДж).
Занятие №21
Насыщенный пар. Влажность. Точка росы.
Насыщенный пар – пар, находящийся в динамическом равновесии со своей жидкостью.
Ненасыщенный пар - это пар, не достигший динамического равновесия со своей жидкостью.
Влажность воздуха – физическая величина, характеризующая содержание в воздухе водяного пара. Влажность воздуха (относительная влажность воздуха) – это отношение парциального давления водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного пара при той же температуре, выраженное в процентах.
О
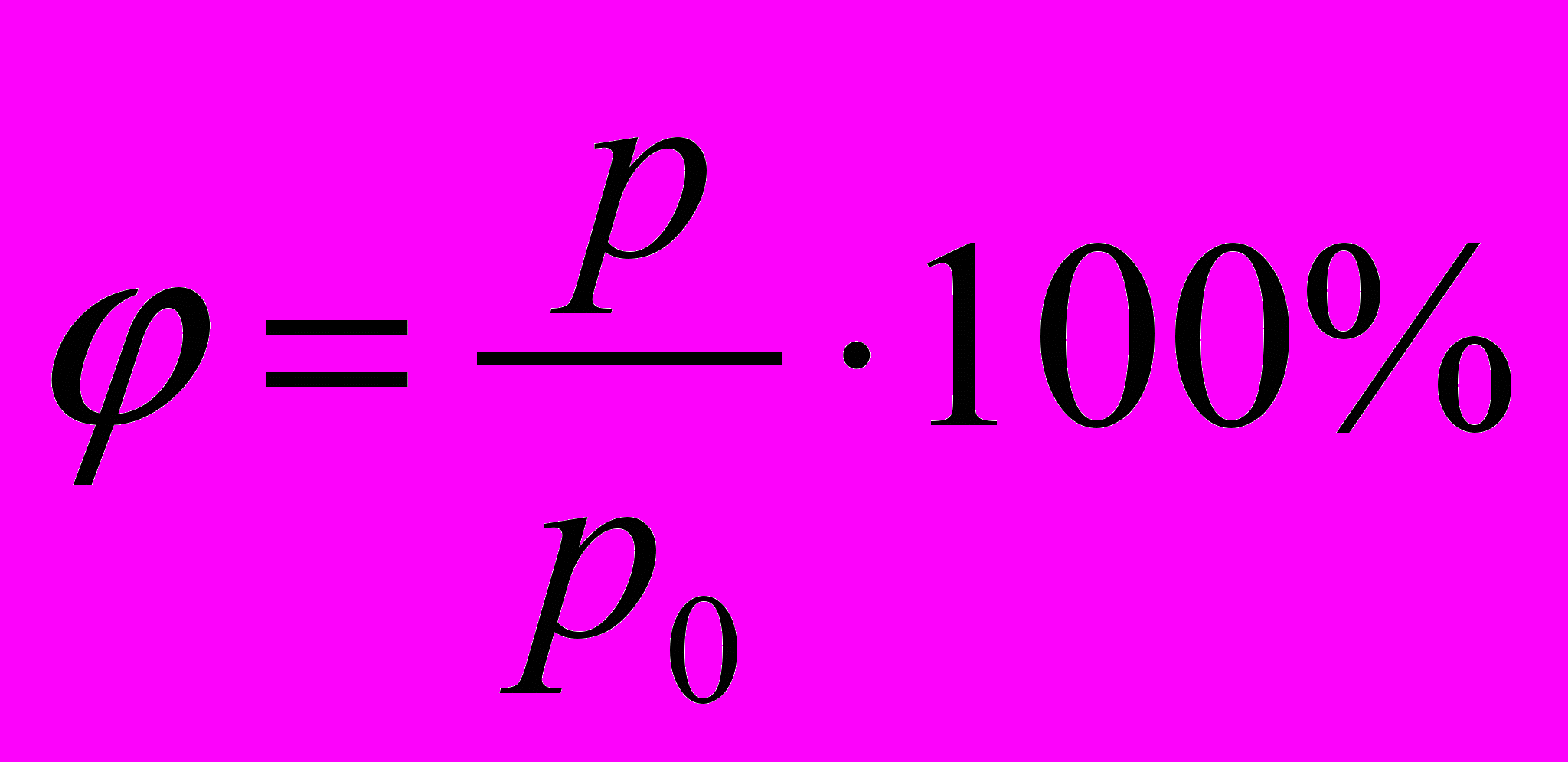 тносительная влажность воздуха показывает, насколько водяной пар в данных условиях близок к насыщению. Именно от этого зависит интенсивность испарения воды и потеря влаги живыми организмами. Для человека наиболее благоприятна относительная влажность 40–60%.
тносительная влажность воздуха показывает, насколько водяной пар в данных условиях близок к насыщению. Именно от этого зависит интенсивность испарения воды и потеря влаги живыми организмами. Для человека наиболее благоприятна относительная влажность 40–60%.φ- относительная влажность воздуха [%];
р- парциальное давление [Па];
р0- давление насыщенного пара [Па].
Парциальное давление– это давление, которое имел бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре.
Точкой росы называют температуру, при которой пар, находящийся в воздухе, становится насыщенным.
Это температура, до которой нужно, не меняя давления, охладить водяной пар в воздухе, чтобы он стал насыщенным. Начиная с этой температуры, охлаждение воздуха сопровождается появлением капелек росы, влаги на окнах и т. д. Парциальное давление водяного пара при температуре, большей точки росы, совпадает с давлением насыщенного пара в точке росы. При температуре воздуха, равной точке росы, относительная влажность воздуха составляет 100% .
Домашнее задание. Выучить конспект. Подготовиться к лабораторной работе. Решить задачу:№561. Почему запотевают очки, когда человек с мороза входит в комнату?
Занятие №23
Жидкости. Поверхностное натяжения. Смачивание, капиллярность.
Жидкость– это агрегатное состояние вещества. Жидкости присущи некоторые свойства твердого тела (сохраняет свой объем, образует свободную поверхность, обладает определенной прочностью на разрыв) и газа (принимает форму сосуда, в котором находится).
Поверхностное натяжение– это явление, проявляющееся в стремлении поверхности жидкости к уменьшению своей площади.
Объясняется тем, что любая молекула, находящаяся на поверхности жидкости, притягивается молекулами, находящимися внутри жидкости. Под действием этих сил молекулы с поверхности жидкости уходят внутрь жидкости, и число молекул, находящихся на поверхности, уменьшается до тех пор, пока площадь свободной поверхности жидкости не достигнет минимально возможного значения. Это явление выглядит таким образом, будто жидкость покрыта тонкой растянутой упругой пленкой, стремящейся к сокращению. Так как шар имеет минимальную поверхность при заданном объёме, то это объясняет факт образования шаровой формы жидкости.
Смачивание – это явление, проявляющееся в большем или меньшем растекании жидкости по поверхности твердого тела.
Жидкость, которая растекается тонкой плёнкой по твёрдому телу, называется смачивающей (силы притяжения между молекулами жидкости и твёрдого тела больше сил притяжения между молекулами самой жидкости).
Жидкость, которая не растекается, а наоборот свёртывается в каплю, называется несмачивающей (преобладают силы притяжения между молекулами самой жидкости).
Капилляр- это узкая трубка или сосуд с диаметром около миллиметра и менее.
Капиллярные явления– это явления изменения высоты уровня жидкости в капиллярах, опущенных одним концом в жидкость.
Поверхность жидкости, искривлённая на границе с твёрдым телом, называется мениском (выпуклый- если не смачивает, вогнутый- если смачивает).
Задача №1. Весной землю пашут и боронуют. Почему это способствует сохранению влаги в почве?
Задача №2. Почему трудно вытереть мокрые руки шерстяной тряпкой?
Домашнее задание. Учить конспект. Решить задачу:№585. Как объяснить происхождение поговорки «Как с гуся вода»? Выполнить экспериментальное задание: В таз с водой опустить вырезанную из картона «лодочку». Макнуть около одного конца этой «лодочки» мылом. Объясните, почему движется «лодочка»?
Занятие №25
Кристаллические и аморфные тела. Механические свойства твёрдых тел.
Кристаллы это твердые тела, обладающие трехмерной периодической атомной или молекулярной структурой. Обычно имеют форму правильного симметричного многогранника.
Поликристалл – это агрегат мелких монокристаллов различной ориентации (кристаллических зерен).
Анизотропия твердых тел – это зависимость физических свойств твердого тела от направления внутри него.
Все кристаллы анизотропны (по разным направлениям в кристалле различны механическая прочность, теплопроводность, электропроводность и т. п.). Поликристаллические материалы, состоящие из огромного числа случайно ориентированных мелких монокристаллов, в обычных условиях в целом изотропны.
Жидкие кристаллы - это вещества, находящиеся в состоянии, промежуточном между жидким состоянием и твердым кристаллическим. Подобно жидкостям, обладают текучестью. Однако в отличие от них характеризуются анизотропией свойств, присущей обычным кристаллам.
Аморфное состояние - это твердое некристаллическое состояние вещества, характеризующееся изотропией физических свойств и отсутствием определенной температуры плавления.
Деформация тела – изменение формы или размеров тела.
Виды деформаций: Деформация сжатия и растяжения (испытывают колонны и фундаменты зданий, стены домов, устои мостов; деформацию растяжения испытывают тросы, балки строительных ферм).
Деформация сдвига (испытывают соединительные стержни, заклёпки, болты, шпонки и т.д.).
Деформация изгиба (испытывают фермы мостов, провода электропередач).
Деформация изгиба сводится к двум деформациям: сжатия и растяжения. Средние слои не деформируются, поэтому часто используют полые стержни (трубки). В процессе эволюции приобрели трубчатую форму многие кости человека, животных и птиц, стебли некоторых растений (бамбук, злаки).
Д
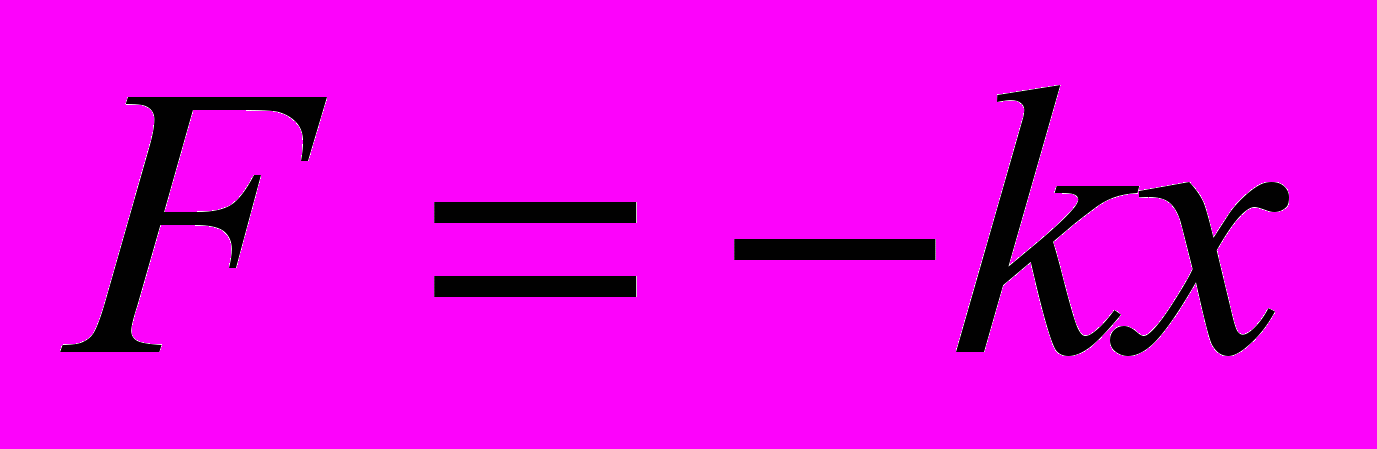 еформация кручения (испытывают валы машин, винты, свёрла).
еформация кручения (испытывают валы машин, винты, свёрла).Закон Гука:
F- сила упругости [H]; k- коэффициент упругости [Н/м]; x- величина деформации [м].
Задача №1. Определите удлинение пружины, если на неё действует сила 6,2 Н, а жёсткость пружины 0,5 кН/м. Ответ выразить в миллиметрах.
Домашнее задание. Выучить конспект. Прочитать: § 7.4. Решить задачу: Определите модуль силы упругости, возникающей в пружине жёсткостью 520 Н/м, если под действием внешней силы её длина уменьшилась на 4,5 см.
Занятие №27
Количество теплоты. Работа газа в термодинамике. Первое начало термодинамики, применение к изопроцессам.
Внутренняя энергия (U )– энергия физической системы, зависящая от ее внутреннего состояния. Внутренняя энергия включает кинетическую энергию хаотического (теплового) движения микрочастиц системы (молекул, атомов и т. д.) и потенциальную энергию взаимодействия этих частиц друг с другом.
Изменение внутренней энергии может происходить двумя способами: совершением работы и теплопередачей.
Теплопередача – это теплообмен между двумя теплоносителями (жидкими или газовыми средами), осуществляющийся через разделяющую их твердую стенку или через поверхность раздела между ними.
Количество теплоты(Q)– это часть внутренней энергии, переданная от одного тела к другому при теплообмене.
Работа А (в термодинамике)– это изменение внутренней энергии системы, связанное с изменением ее объема и расположения ее частей относительно друг друга.
А = р∆V А - работа (Дж); р - давление (Па); ∆V – изменение объёма (м3).
ПЕРВЫЙ ЗАКОН (первое начало) ТЕРМОДИНАМИКИ – изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе.
I закон термодинамики: ∆U=Q+A A-работа над газом; ∆U=Q-A′ А′- работа газа.
Изотермическое сжатие. Первый закон термодинамики выглядит так: 0 = -Q + A
Над газом совершается работа, при этом газ выделяет тепло во внешнюю среду ( внутренняя энергия не изменяется).
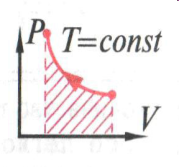
Изотермическое расширение. Первый закон термодинамики выглядит так: Q = A. Газ совершает работу за счет поглощения тепла из внешней среды ( внутренняя энергия не изменяется).
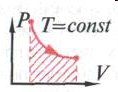
Изобарное нагревание. Первый закон термодинамики выглядит так: Q = U – A. Газ получает тепло из внешней среды. Полученная таким образом энергия тратится на увеличение внешней энергии и на совершение работы.
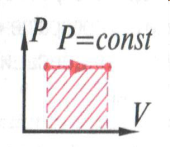
Изобарное охлаждение. Первый закон термодинамики выглядит так: U = -Q + A. Над газом совершается работа, при этом газ выделяет тепло во внешнюю среду, а его внутренняя уменьшается.
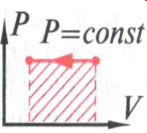
Изохорное нагревание. Первый закон термодинамики выглядит так: U=Q. Газ увеличивает свою внутреннюю энергию за счет теплоты, полученной из внешней среды.
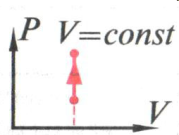
Изохорное охлаждение. Первый закон термодинамики выглядит так: - U = -Q. Газ выделяет тепло во внешнюю среду; при этом его внутренняя энергия уменьшается.
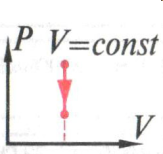
Адиабатное сжатие. Первый закон термодинамики выглядит так: U=A. Над газом совершается работа, при этом внутренняя энергия газа увеличивается.
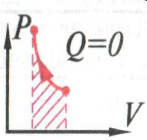
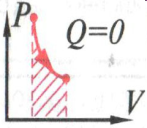
Адиабатное расширение. Первый закон термодинамики выглядит так: 0= - U+A. Газ совершает работу только за счет своей внутренней энергии. ( Внутренняя энергия при этом уменьшается).
Задача №1. Какую работу совершает газ, расширяясь изобарически при давлении 2.105 Па от объёма 1,6 л до объёма 2,5 л?
Задача №2. Внешние силы совершили над газом работу 300 Дж, при этом внутренняя энергия газа увеличилась на 500 Дж. Какое количество теплоты было передано газу?
Домашнее задание. Выучить конспект. Решить задачу: как изменяется внутренняя энергия идеального газа при адиабатном сжатии: а)не изменяется; б) увеличивается; в)уменьшается. Ответ обосновать.
Занятие №29,30
Принцип действия тепловых двигателей. КПД теплового двигателя.
ТД и охрана природы.
Т


 ЕПЛОВОЙ ДВИГАТЕЛЬ - это машина, преобразующая внутреннюю энергию топлива в механическую энергию.
ЕПЛОВОЙ ДВИГАТЕЛЬ - это машина, преобразующая внутреннюю энергию топлива в механическую энергию.
 Нагреватель (Q н) Рабочее тело (А) Холодильник (Q х)
Нагреватель (Q н) Рабочее тело (А) Холодильник (Q х)В термодинамике рассматриваются только тепловые машины, работающие циклически. Работа любого теплового двигателя состоит из повторяющихся циклов, каждый из которых включает в себя получение рабочим телом энергии от нагревателя, расширение рабочего тела и совершение им работы, передачу части энергии холодильнику и возвращение рабочего тела в исходное состояние.
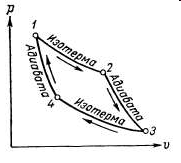
ЦИКЛ КАРНО – это циклический обратимый процесс, состоящий из двух изотермических и двух адиабатных процессов.
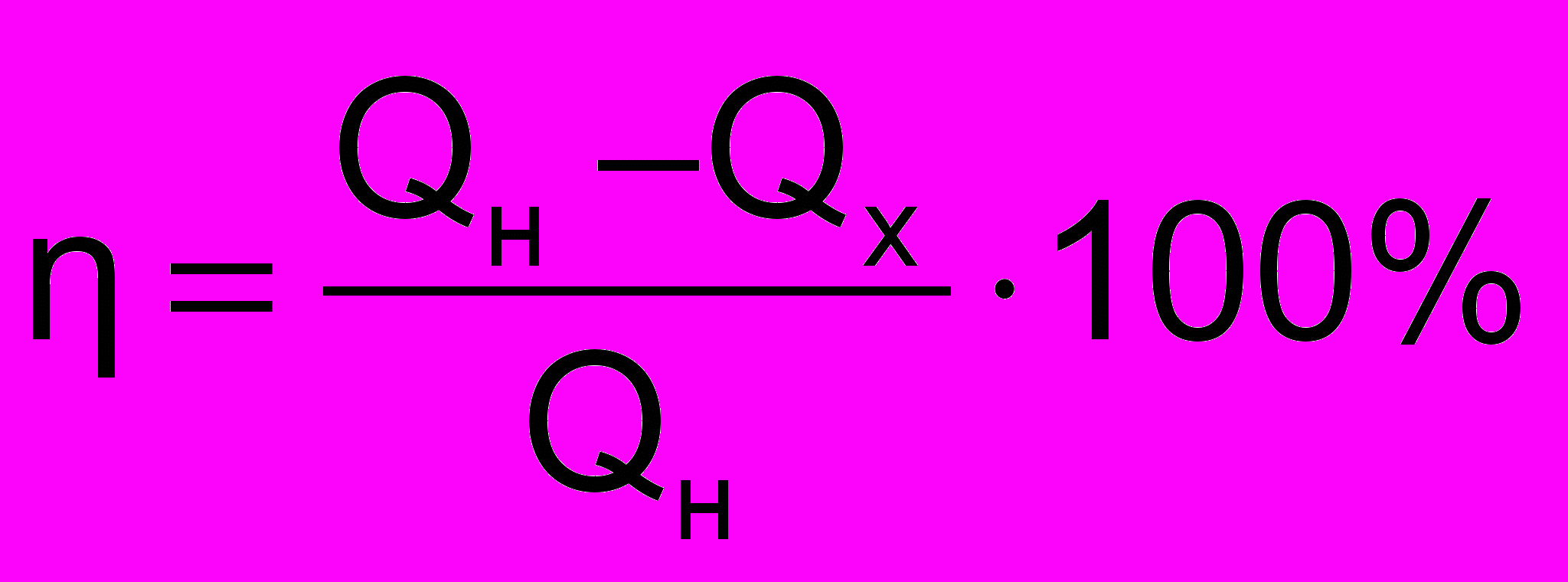
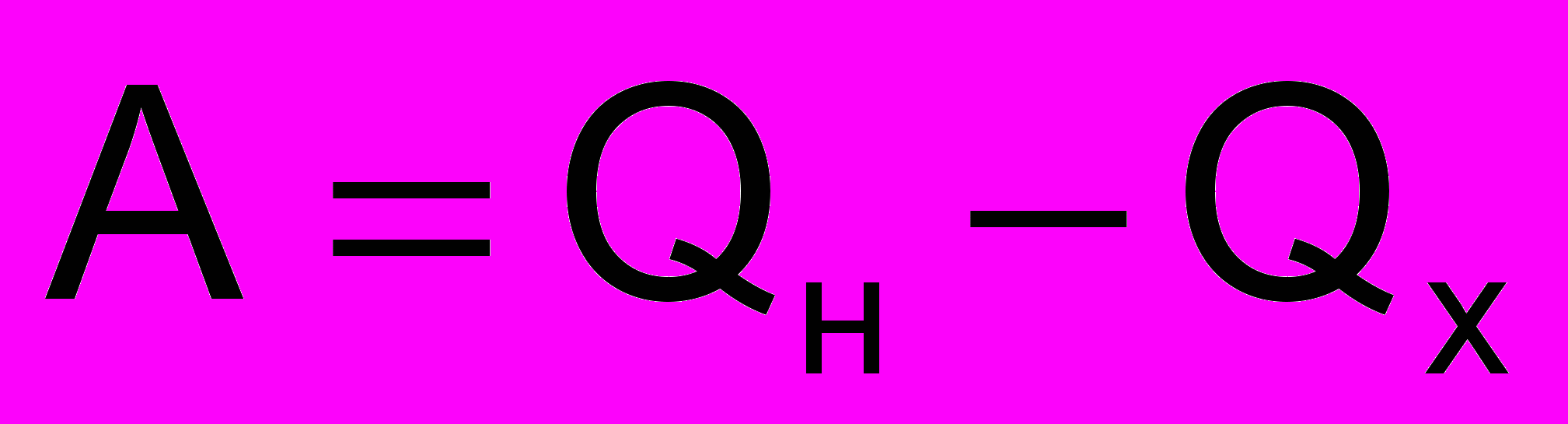
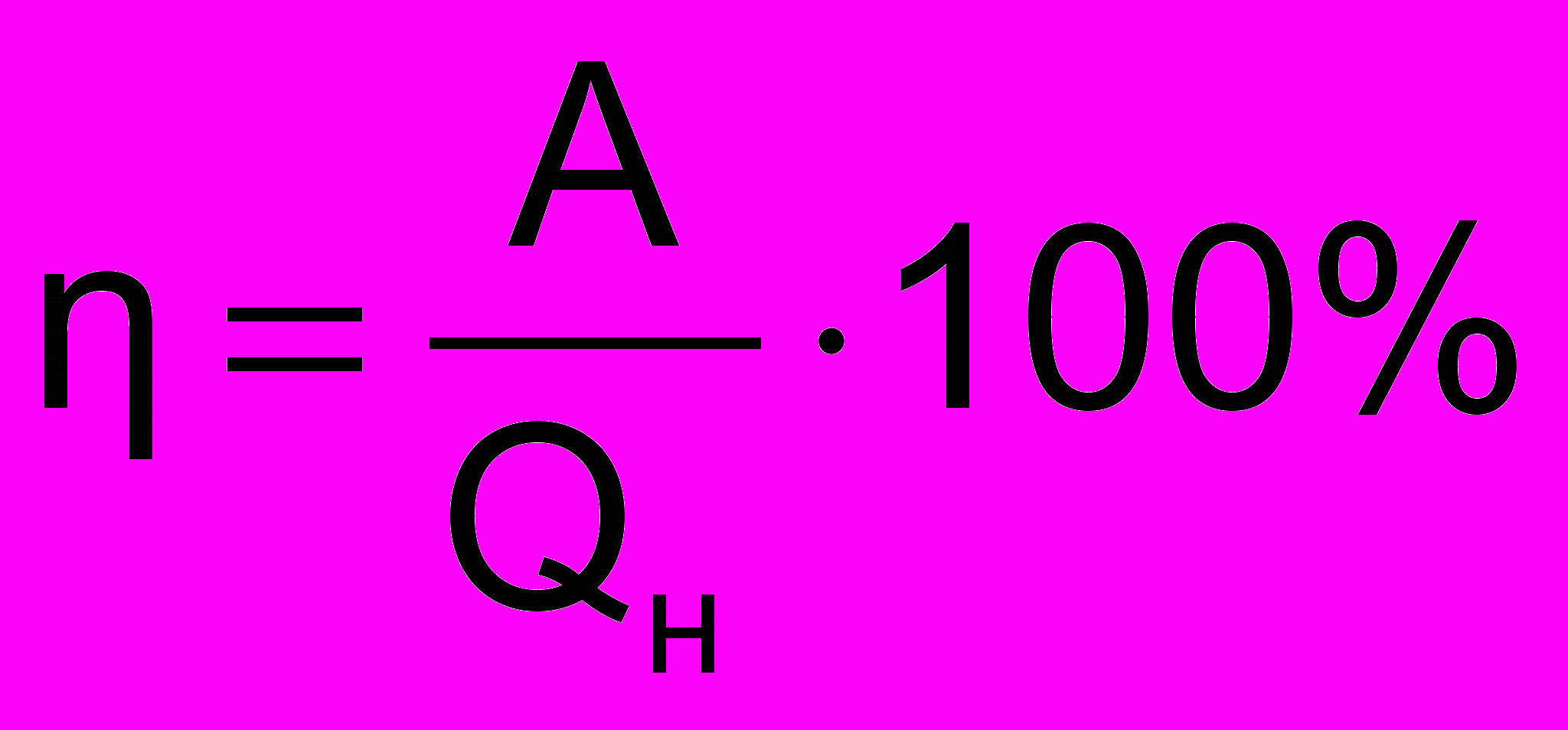
К
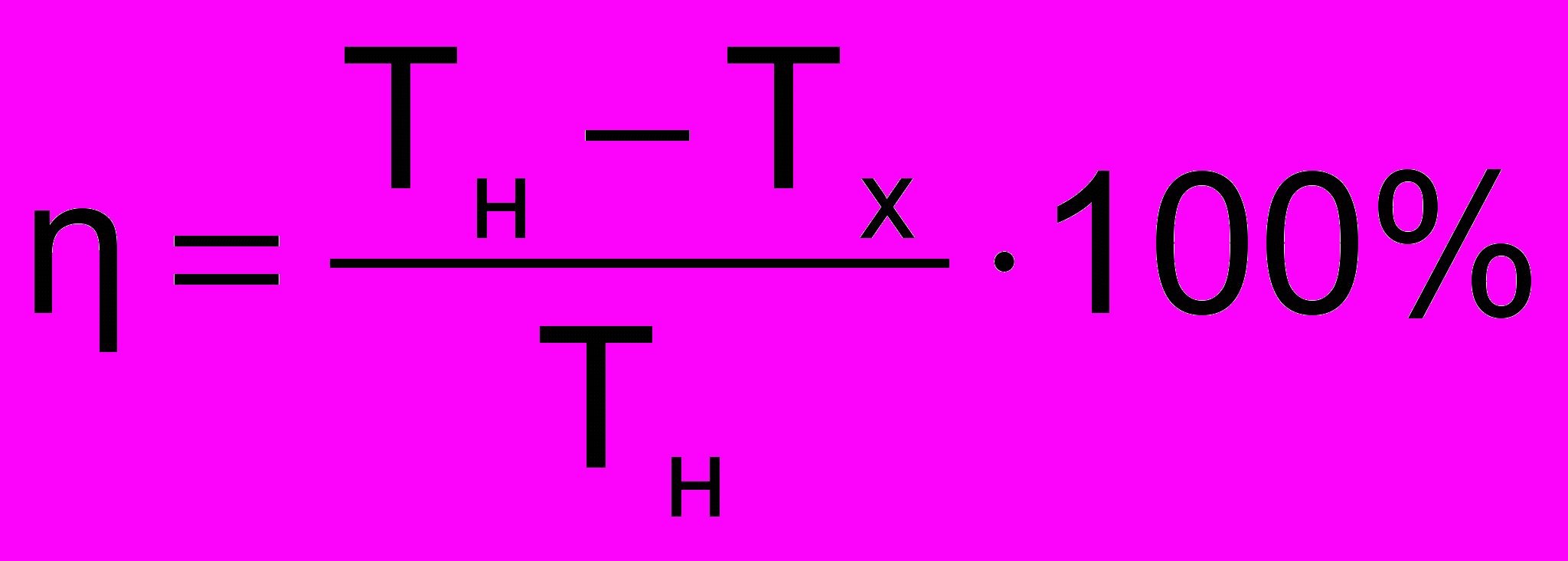 ПД тепловой машины:
ПД тепловой машины:КПД идеальной тепловой машины, работающей по циклу Карно:
Задача №1. Тепловой двигатель получает от нагревателя за некоторое время 7200 кДж теплоты, а отдаёт холодильнику 6400 кДж. Чему равна работа двигателя за это время? Ответ выразить в мегаджоулях (МДж).
Задача №2. Тепловой двигатель получил от нагревателя 600 кДж теплоты и совершил при этом работу 240 кДж. Определить КПД двигателя.
Домашнее задание. Учить конспект. Прочитать: § 6.3. Решить задачу: №677.
В идеальной тепловой машине за счёт каждого килоджоуля энергии, получаемой от нагревателя, совершается работа 300 Дж. Определить КПД машины и температуру нагревателя, если температура холодильника 280 К.
