Инструкция по применению Учреждения разработчики
| Вид материала | Инструкция |
- Инструкция по применению Учреждения-разработчики, 918.08kb.
- Инструкция по применению Учреждения-разработчики, 377.56kb.
- Инструкция по применению Сертификат соответствия № росс ru. Oc03. H00280, 894.98kb.
- Инструкция по применению и испытанию средств защиты, используемых в электроустановках, 1601.52kb.
- Инструкция №6/04 по применению средства дезинфицирующего «Мистраль», 475.49kb.
- Инструкция по применению средства для дезинфекции Самаровка ООО «Дезинфекция для Вас», 346.95kb.
- Инструкция №05-2/07. по применению дезинфицирующего средства "Оксилизин", 203.08kb.
- Методические рекомендации по порядку отражения в бухгалтерском учете входящих остатков, 246.68kb.
- Инструкция №17/07 по применению средства дезинфицирующего "Бриллиантовый миг-2" производства, 197.57kb.
- Инструкция №05/Б-09 по применению моющее дезинфицирующего средства «Централь» (ооо, 757.08kb.
Приложение 1
к Инструкции Организация и проведение мониторинга антибиотикорезистентности
клинически значимых микроорганизмов к антибактериальным лекарственным средствам в организациях здравоохранения
Республики Беларусь
Микробиологический мониторинг и эпидемиологический анализ
антибиотикорезистентности микроорганизмов с использованием
компьютерной программы WHONET
Анализ результатов тестирования микроорганизмов на антибиотикорезистентность/антибиотикочувствительность имеет большое значение для проведения эпидемиологической диагностики в госпитальных условиях.
Центральным вопросом в этом направлении деятельности является анализ спектра активности антибиотиков по отношению к ведущим возбудителям в стационаре.
В микробиологических лабораториях ежегодно формируется база данных микробиологических исследований. Для обработки информации требуется внедрение программного продукта.
Всемирной Организацией Здравоохранения рекомендуется к использованию компьютерная аналитическая программа WHONET (разработчики профессор T.O’Brien и доктор J.Stelling, Бостон США).
WHONET 5 - это программное обеспечение базы данных для обработки результатов микробиологических лабораторных исследований.
Основными задачами этого программного обеспечения являются:
- повысить возможность использования лабораторных данных на местах; и
- способствовать сотрудничеству центров посредством обмена данными.
Программное обеспечение было разработано для обработки результатов рутинных лабораторных исследований, но также использовалось для научных исследований. Программное обеспечение было разработано для анализа данных, особенно результатов тестов на чувствительность к антимикробным препаратам.
Аналитические возможности WHONET облегчают:
- подбор антимикробных препаратов;
- идентификацию вспышек внутрибольничной инфекции;
- определение проблем контроля качества при лабораторных исследованиях.
- уйти от «ручной» обработки результатов.
К тому же обзор результатов антимикробного тестирования позволяет определить:
- механизмы развития резистентности;
- эпидемиологию резистентных штаммов.
Для внедрения в работу данной программы требуются следующие условия:
- оснащение рабочих мест микробиологов, эпидемиологов, врачей лечебного звена компьютерной техникой;
- проведение обучения всех заинтересованных специалистов;
- обеспечение электронной почтой микробиологической лаборатории, организаций здравоохранения и санитарно-эпидемиологической службы.
Если в микробиологической лаборатории используется другая компьютерная система, то для перевода данных из вашей системы в WHONET потребуется программное обеспечение BacLink.
BacLink - это компьютерное программное обеспечение, которое позволяет импортировать данные из существующей информационной системы и автоматизированных анализаторов определения чувствительности в WHONET. В настоящее время существует только версия DOS.
WHONET имеет следующие три основных компонента
Лабораторная конфигурация
Система может быть адаптирована для вашей лаборатории путем ввода конкретной информации, как например, протестированные антибиотики и локализации больных, обслуживаемые вашей лабораторией. К тому же вы можете указать какие данные вы хотите включить в файл. Эта конфигурация может быть изменена в последующем.
Ввод данных
WHONET позволяет вводить результаты тестов на чувствительность, а также сохранять, исправлять и распечатывать клинические записи. Возможно немедленное получение ответа по фенотипу штамма. Если данные конвертируются из существующей лабораторной системы, то повторное введение данных непосредственно в WHONET не требуется.
Анализ данных
В настоящее время возможные анализы включают отчеты по культурам в виде построчного перечня и резюме, сведение в таблицы статистических данных по резистентности, диаметр зоны и гистограммы MIC, диаграммы и кривые регрессии по антибиотикам, построчные и суммарные профили резистентности антибиотиков.
Начальный экран WHONET
Каждый раз, когда вы начинаете работать с WHONET, вы увидите начальный экран WHONET (рисунок 1). Это перечень лабораторий, имеющихся в базе данных WHONET.
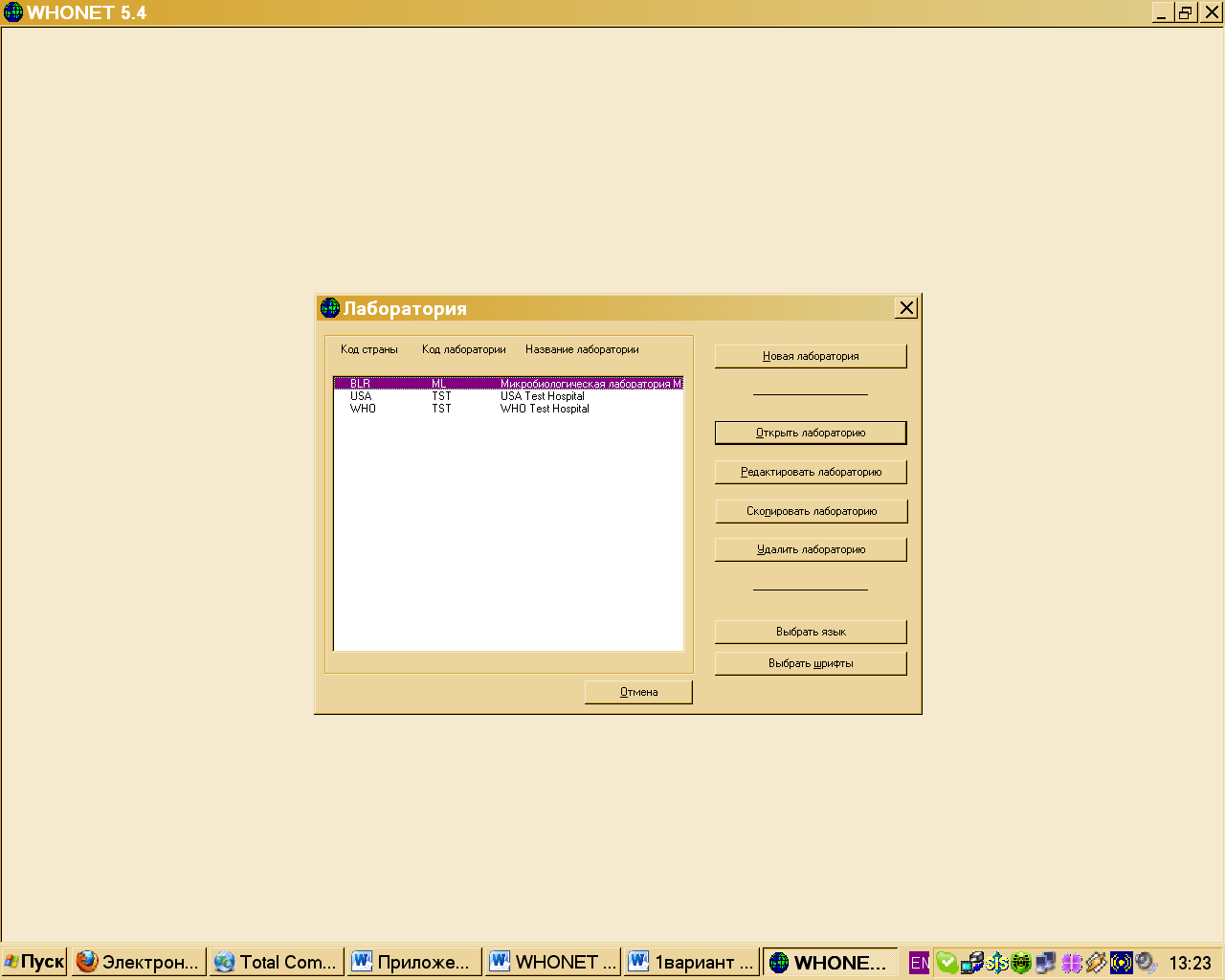
Рис.1. Начальный экран
Основной экран WHONET
Когда вы открываете лабораторию, появляется основной экран WHONET (рисунок 2). Заметьте, что название лаборатории появляется в левом верхнем углу экрана.
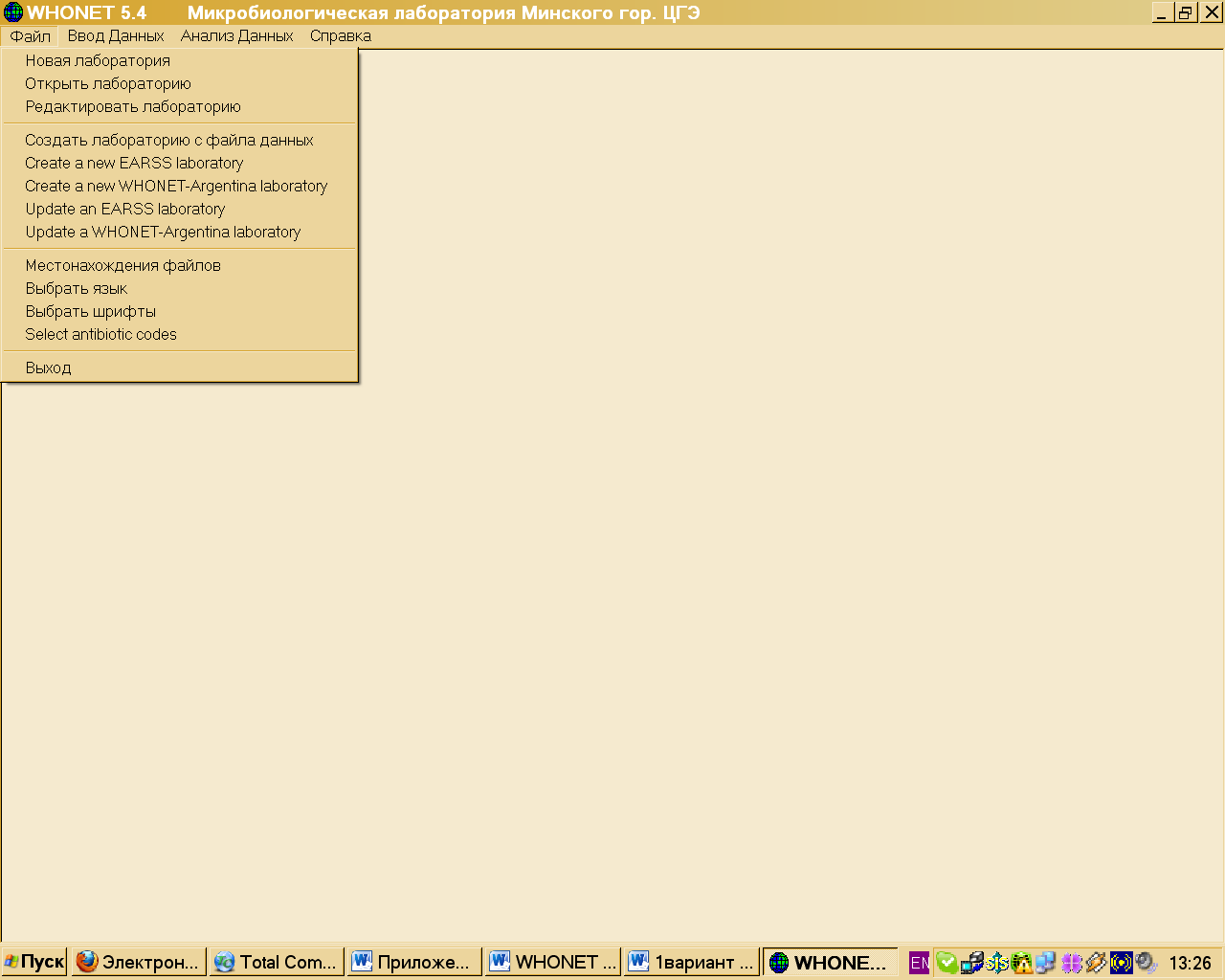
Рис. 2. Основной экран
Анализ данных проводится по различным параметрам с выбором определенных критериев (рис. 3).
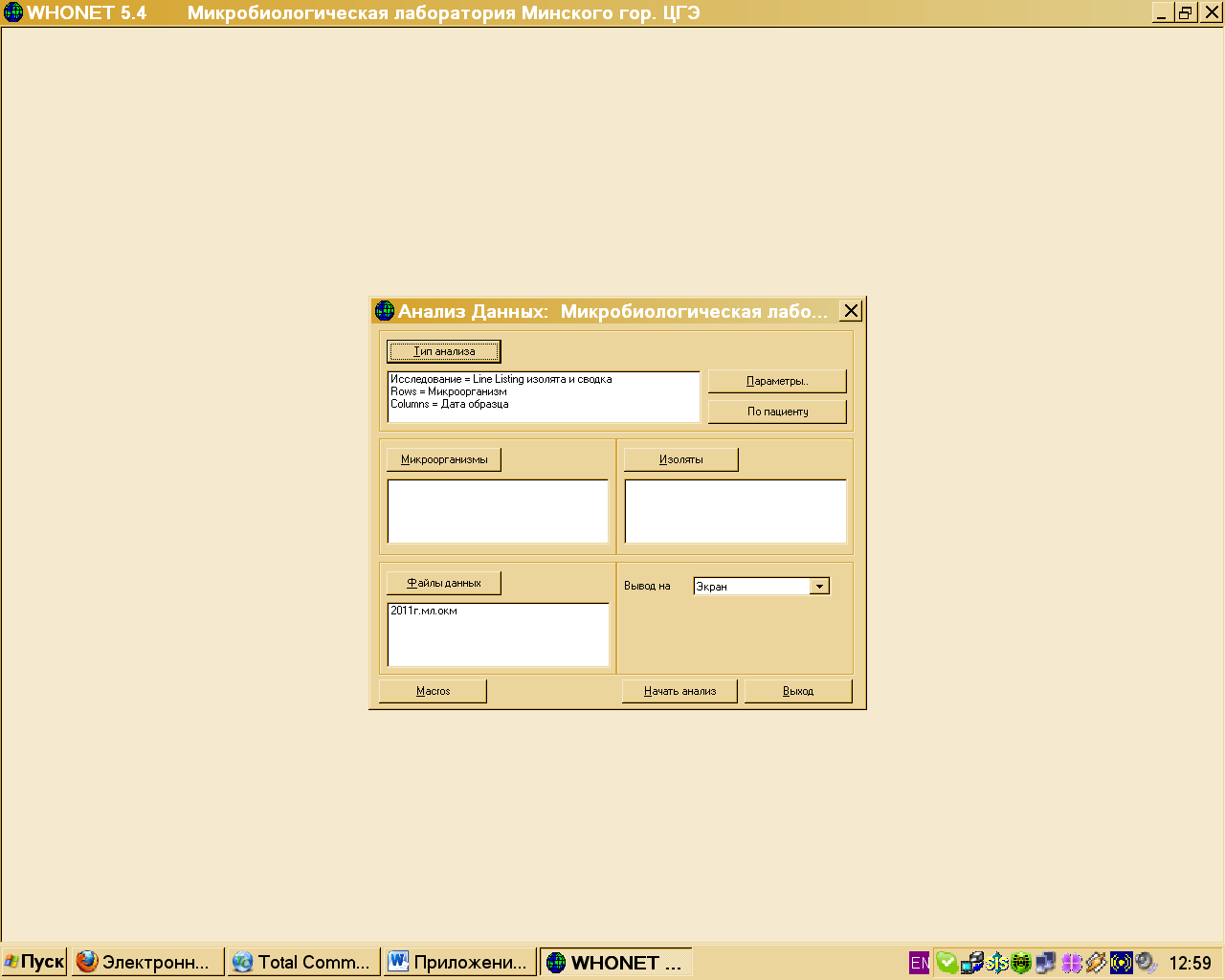
Рис.3. Экран Анализа данных
Введенные данные могут быть просмотрены в виде таблиц.
- Проведение анализа с использованием типа анализа «Построчный анализ» (Line-listing)
Построчный список представляет собой результаты исследования всего клинического материала.
Каждый результат исследования располагается на отдельной строке, где отмечаются идентификационный номер пациента (номер истории болезни), номер образца, палата (отделение), дата взятия образца, образец (код материала), возбудитель (код микроорганизма) и результаты исследования в соответствии с каждым протестированным антибиотиком. Каждый антибиотик отмечается тремя буквами (трехбуквенный код) (рис.4).
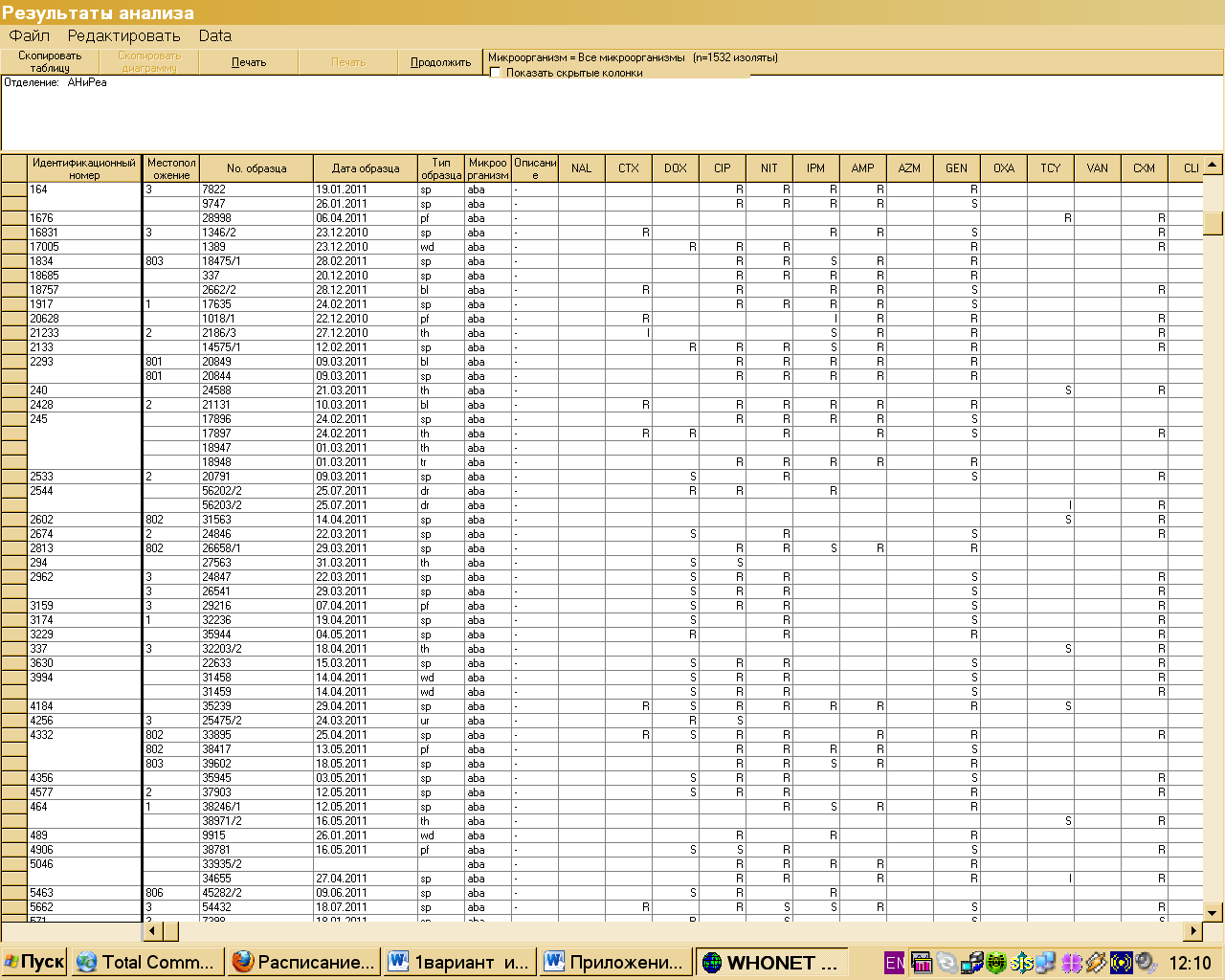
Рис.4. Простой построчный анализ (Line-listing)
Данная таблица может рассматриваться как электронная версия журнала микробиолога, содержащая всю необходимую информацию для проведения эпидемиологического анализа.
- Сводная таблица изолятов (рис.5).
Анализ тестирования микроорганизмов на чувствительность/резистентность к антимикробным препаратам начинается с выявления ведущих, эпидемиологически наиболее значимых видов возбудителей в данном стационаре, подразделении стационара, среди группы больных, видов материалов, откуда произведено выделение.
Данный формат является сводной таблицей, которая позволяет:
• проводить необходимую группировку материалов,
• выявлять ведущие микроорганизмы по частоте выделения (на 100 исследований) от пациентов в анализируемом отделении.
Изучаемые данные могут в зависимости от поставленной задачи суммироваться по:
• видам штаммов микроорганизмов,
• виду материалов, взятых для исследования,
• палатам,
• отделениям,
• полу,
• возрасту пациентов,
• диагнозам пациентов,
• по любым другим критериям, занесенным в раздел "Комментарии".
Сводная таблица, помимо указания общего числа протестированных изолятов, включает число пациентов по месяцам.
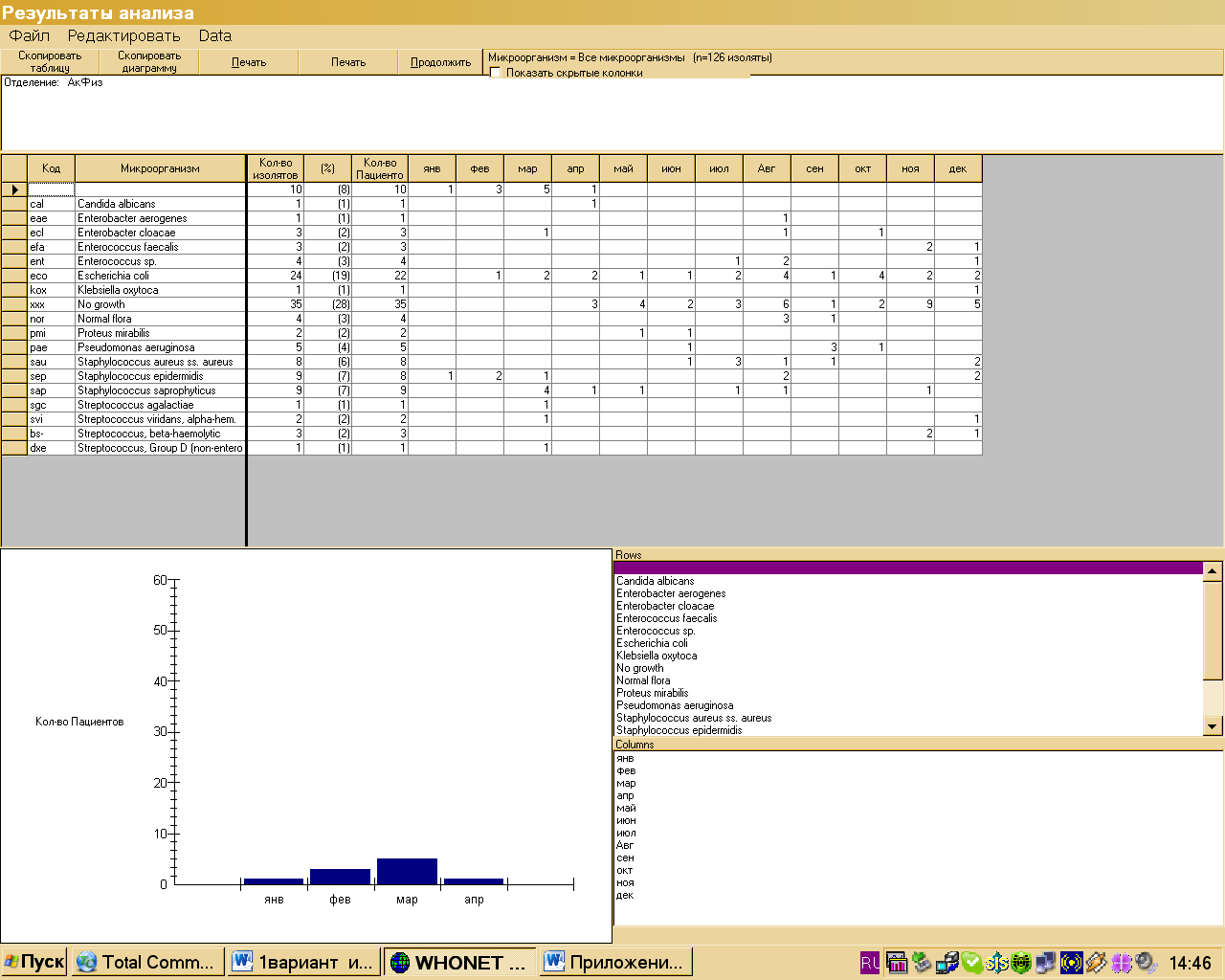
Рис.5.Сводная таблица изолятов "Частота выделений микроорганизмов
с учетом распределения по месяцам"
На рисунке 5 образец сводной таблицы изолятов представляет собой пример распределения микроорганизмов, полученных от пациентов акушерско-физиологического отделения, сгруппированных по виду. В таблице представлены данные об изолятах по каждому виду микроорганизма (в абсолютных числах и доле), о количестве пациентов, у которых были выделены данные изоляты и распределение этих данных по месяцам.
Из таблицы, представленной на рисунке 2, видно, что ведущими микроорганизмами по частоте выделения (на 100 исследований) от пациентов в данном отделении является Escherichia coli.
В помесячном распределении число штаммов Escherichia coli практически одинаково, в августе и октябре отмечается наибольшее количество изолятов. Для более корректных выводов требуется расчет интенсивных показателей выделения микроорганизмов и проведение эпидемиологического расследования.
На рисунке 6 представлено распределение микроорганизмов, выделенных из клинического материала пациентов, в разрезе отделений.
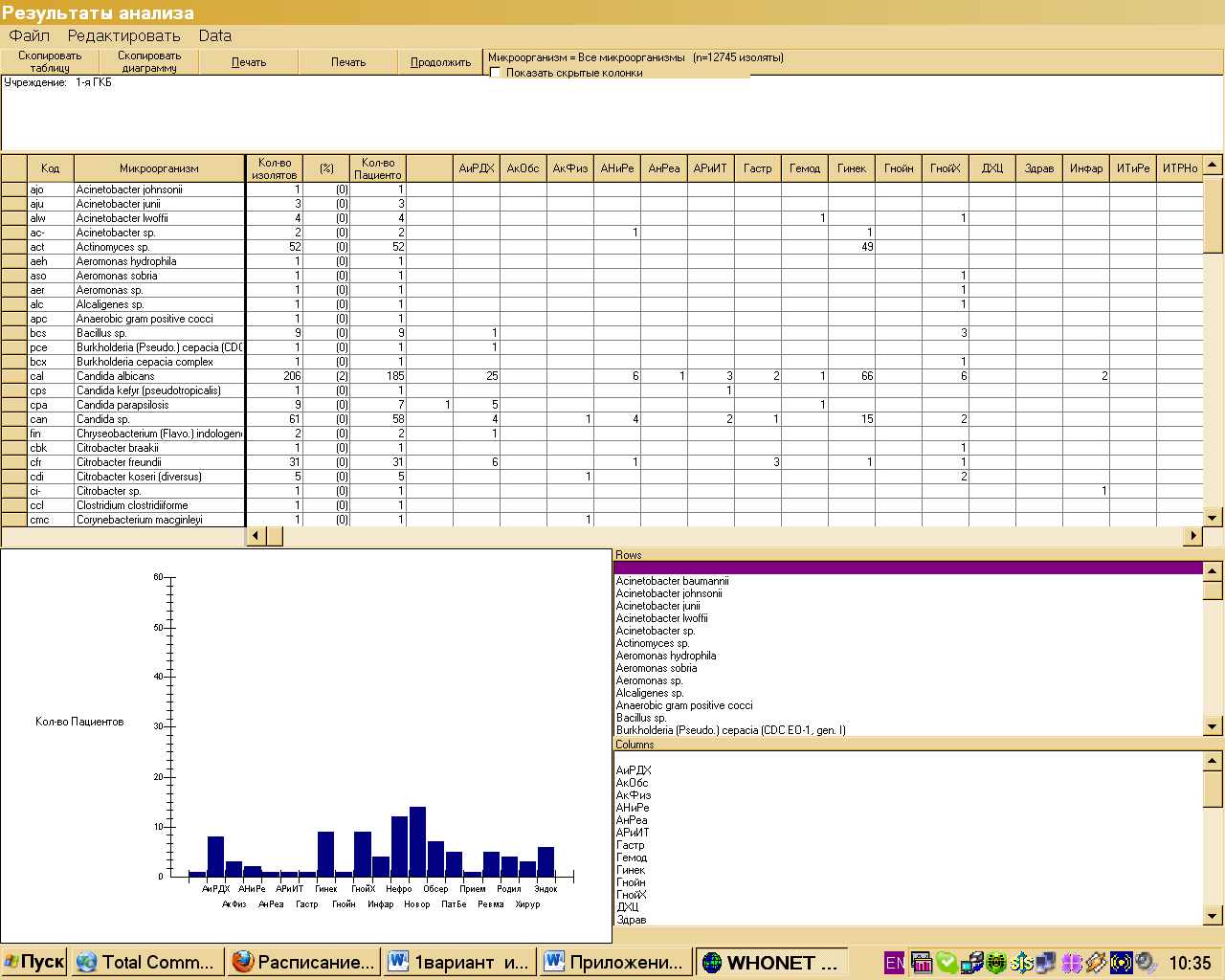
Рис.6.Распределение микроорганизмов в разрезе отделений за год.
На рисунке 7 представлены данные бактериологических исследований различного клинического материала пациентов отделения.
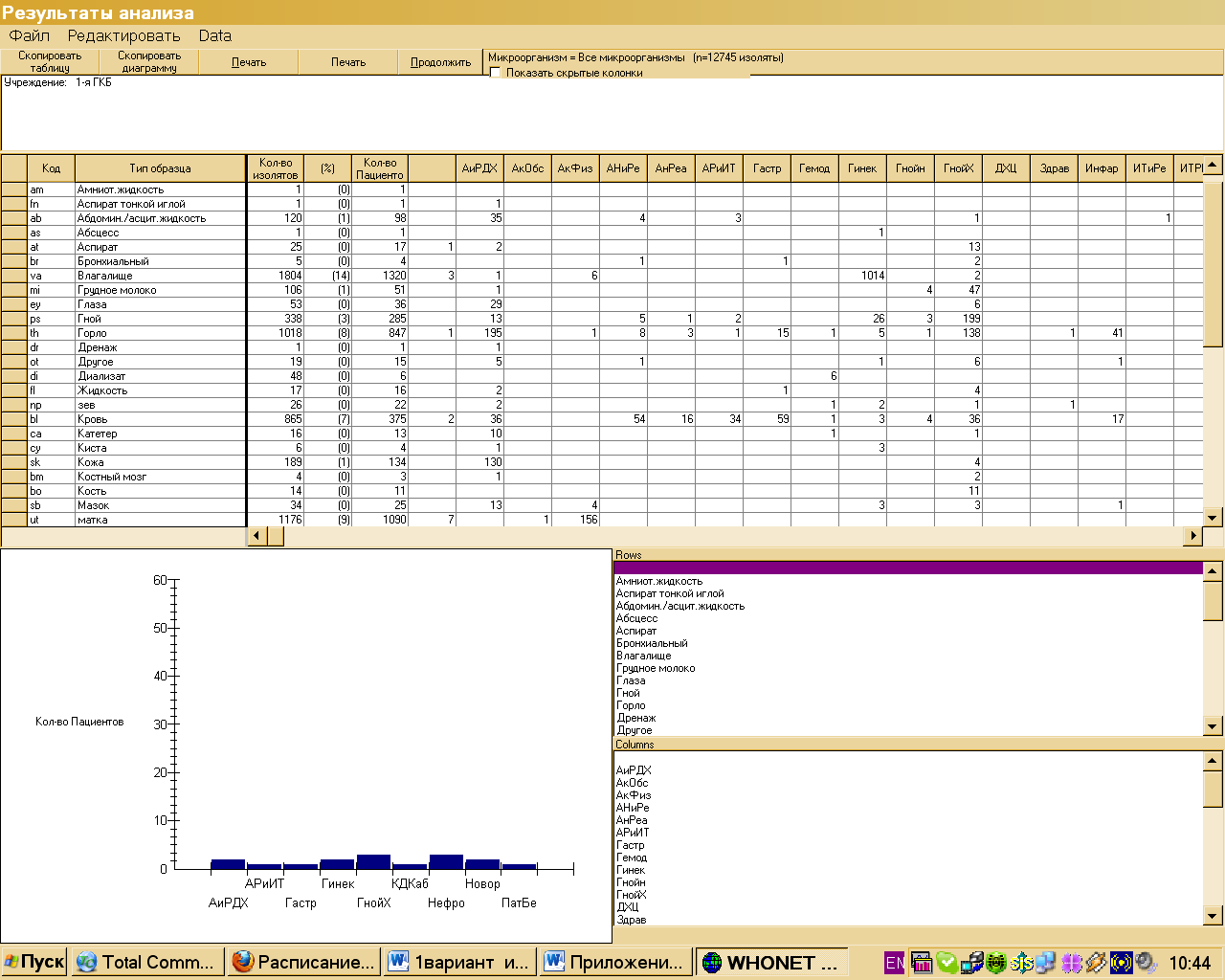
Рис.7. Распределение частоты встречаемости
микроорганизмов по субстрату выделения
- Анализ спектра активности антибиотиков по отношению к ведущим возбудителям в стационаре (рис.8).
Распределение по доли резистентных (R), промежуточных (умеренно чувствительных) (I) и чувствительных штаммов (S) микроорганизмов.
Данное распределение может быть представлено в нескольких вариантах (в виде таблицы и гистограммы):
Таблица распределения %R, %I и %S - представляет распределение микроорганизмов, основанное на интерпретации результатов измерения диаметров зон задержки роста культур (в миллиметрах) вокруг диска или, если используется тест МПК (определение минимальных подавляющих концентраций) - диаметр зон МПК.
Цель составления таблиц распределения %R, %I и %S - установление соотношения долей чувствительных, устойчивых и промежуточных (умеренночувствительных) микроорганизмов к изучаемым антибиотикам. Эти сведения могут быть в дальнейшем использованы для анализа антимикробной активности каждого антибиотика.
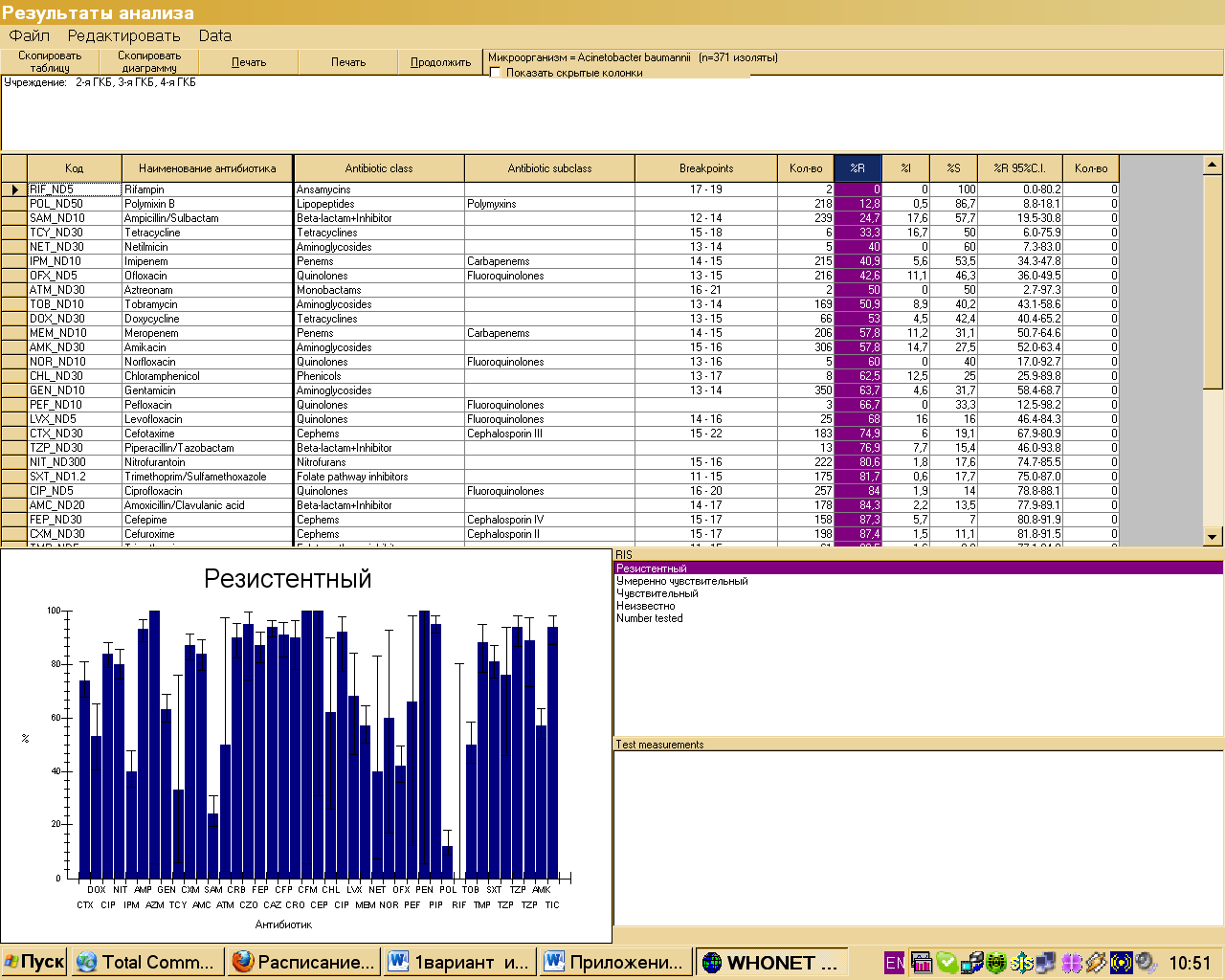
Рис.8. Пример таблицы распределения доли R, I и S
На рисунке 8 в таблице последовательно представлены: трехбуквенный код антибиотика, латинское название антибиотика, антимикробные контрольные точки (зоны задержки роста микроорганизмов на чашке при постановке диск-диффузионного метода, выраженные в мм - breakpoints), количество протестированных изолятов (штаммов), доля резистентных, промежуточных (умеренно/чувствительных), чувствительных штаммов.
- Пример таблицы в формате Line-listing «Распределение построчного анализа профилей резистентности микроорганизмов»
WHONET позволяет создавать профили резистентности, известные также под названиями образцы, фенотипы или антибиотипы. Это очень полезный эпидемиологический инструмент для идентификации штаммов вспышки инфекции, механизмов резистентности, трансмиссивных плазмид и фенотипов невозможной резистентности.
При создании профилей резистентности выделяются первичные и вторичные антибиотики. Первичные антибиотики используются для определения профилей резистентности. Хотя вы можете включить столько антибиотиков, сколько хотите, обычно разумным (и зачастую предпочтительным) считается включить только 5-10 наиболее важных типов антибиотиков. Включение вторичных антибиотиков остается на ваше усмотрение - они появятся при построчном печатании профиля, но не используются при определении профиля резистентности.
Анализ профилей антибиотикорезистентности микроорганизмов позволяет оценить действие на бактерии нескольких антибиотиков одновременно. Изоляты с одинаковыми профилями резистентности перечисляются вместе. В начале списка представляются изоляты, чувствительные ко многим антибиотикам, множественно резистентные показаны в конце списка.
В таблице может быть произведена группировка по интересующему врача признаку, например, по группам пациентов с одинаковым диагнозом, помещенных в одном отделении, палате и т.д. В пределах одной группы пациентов они представляются в соответствии с нумерацией пациентов и датой анализа (рис.9).
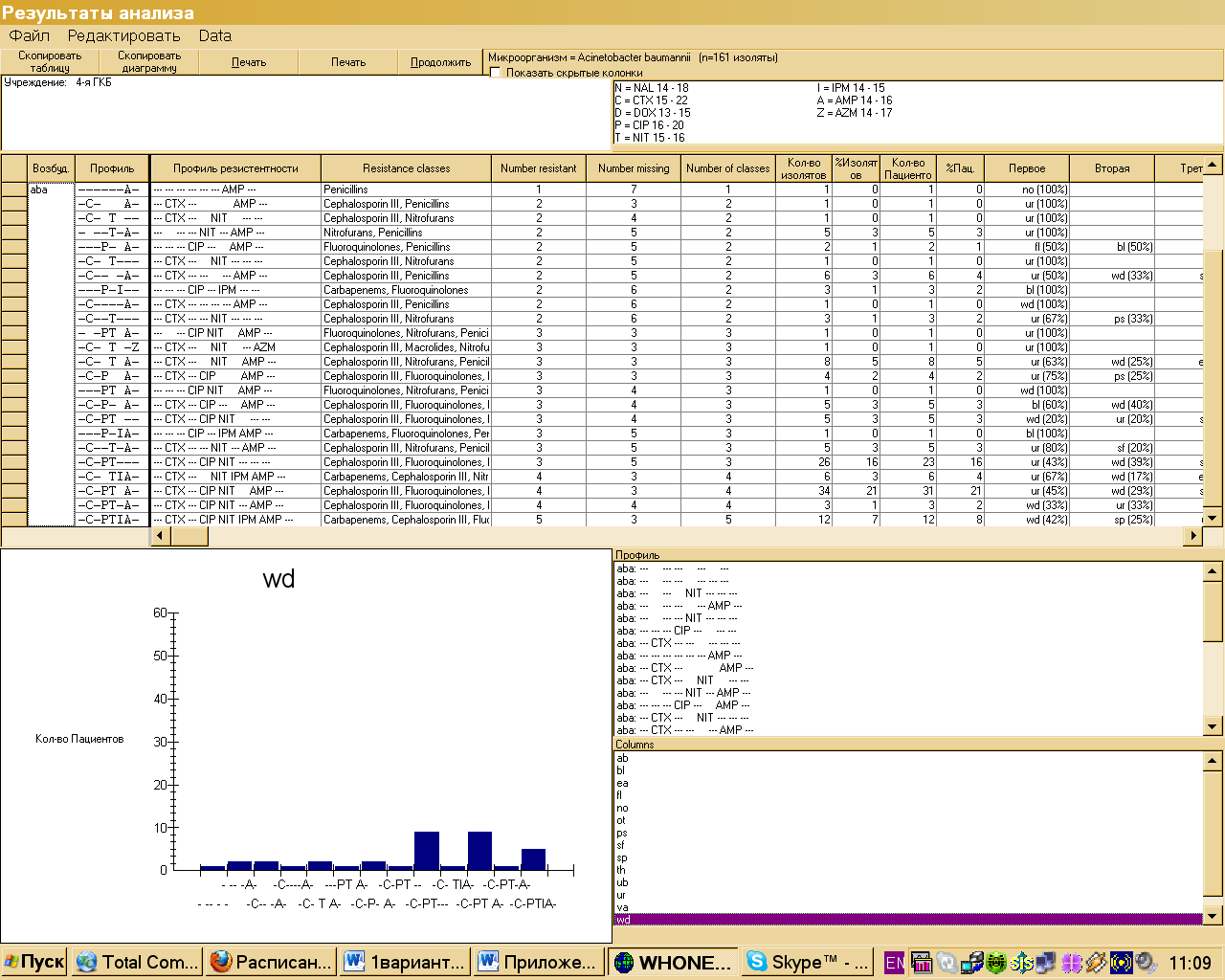
Рис.9. Пример распределения профиля резистентности.
В сводной таблице представлены результаты построчного анализа о количестве изолятов микроорганизма каждого профиля резистентности. В данном случае обнаружено 24 варианта профилей резистентности Acinetobacter baumanii по отношению к 8 антибиотикам, что может быть использовано как внутривидовая метка при проведении эпидемиологического анализа.
Часто наблюдается выделение нескольких идентичных по профилю резистентности изолятов от пациента, в том числе полученных из разных биосубстратов. В сводных таблицах эта информация может быть суммирована с указанием числа изолятов и количества пациентов для каждого профиля резистентности.
Кроме того, количество пациентов с каждым из профилей может быть, по желанию, представлено по месяцам и с указанием отделения (палат), в которых такие профили микроорганизмов встречались наиболее часто. Такие данные значительно облегчают расследование вспышек.
Особое внимание необходимо уделять обнаружению новых множественно резистентных штаммов и особые усилия следует направлять на предотвращение распространения таких штаммов.
Приложение 2
к Инструкции Организация и проведение мониторинга антибиотикорезистентности
клинически значимых микроорганизмов к антибактериальным лекарственным средствам в организациях здравоохранения
Республики Беларусь
АНКЕТА организации здравоохранения за 20_____ г.
Мероприятия по мониторингу резистентных микроорганизмов и рациональному применению антибиотиков
ЧАСТЬ I. Для всех организаций здравоохранения
- Информация о лечебном учреждении:
а) Наименование учреждения___________________________________________________
б) ФИО главного врача________________________________________________________
в) почтовый адрес_____________________________________________________________
г) адрес электронной почты (если есть)___________________________________________
2. Информация о лице, отвечающем на анкету:
Фамилия, имя, отчество________________________________________________________
Должность __________________________________________________________________
Адрес, телефон, адрес электронной почты (если не совпадают с п.1)__________________
__________________________________________________________________________________
3. Наличие в штате госпитального эпидемиолога: да нет
4. Использование компьютера для регистрации микробиологических исследований да нет
5. Наличие электронной базы данных о выделенных микроорганизмах и их свойствах да нет
6. Если электронная база данных есть то:
а) С какого времени ___________________________________________________________________
б) Какая программа используется для хранения и обработки данных________________________
7.Общее количество коек в УЗ____________
Количество коек пульмонологического ____, хирургического____,терапевтического____,
отд. интенсивной терапии____, ЛОР____, гастроэнтерологического____, урологического____ профилей.
8. Наличие плана мероприятий по профилактике ВБИ в клинике да нет
9. Осуществляется ли регистрация случаев ВБИ? да нет
10. Какие шаги были предприняты для достижения максимальной эффективности использования антимикробных препаратов
а) ограничение применения малоэффективных антибиотиков (какие___________________)
б) отказ от использования малоэффективных антибиотиков (какие___________________)
в) введение в практику новых антимикробных средств (какие_________________________)
г) смена перечня антибиотиков каждые 3-6 мес.
д) определение резерва антимикробных препаратов
е)___________________________________________________________________________
11. Соответствует ли назначение антибиотиков протоколам лечения заболеваний, утвержденных Министерством Здравоохранения?
соответствует на 25% на 50% на 75% на 100% не соответствует
12. Введены ли формуляры для эмпирического применения антимикробных средств (в отделениях и общебольничные)? Да (приложите Ваши формуляры к анкете) нет
13. Приобретение антибиотиков
Перечень и количество закупленных и использованных антибиотиков в I полугодии 2009 г.
Приложить к анкете в виде таблицы в соответствии с образцом
Образец заполнения
| № п/п | Наименование антимикробного препарата | Количество, граммы действующего вещества | Страна производитель |
| 1 | Ципрофлоксацин 0,25 №25 | 168 уп. (840 гр.) | РБ |
| 2 | Сумамед 0,5 №5 | 102 фл. | Хорватия |
ЧАСТЬ II. Для организаций здравоохранения, имеющих бактериологическую лабораторию
1. Наличие в баклаборатории микробиологического анализатора да нет
2. При наличии анализатора укажите его марку (модель)________________________________
Укажите дату начала использования анализатора_______________________________
Наличие компьютерной базы данных о тестированных микроорганизмах да нет
Просим предоставить базу данных по электронному адресу: leonidtitov@tut.by или ermakova_riem@mail.ru
Для предоставивших базу данных, заполнять следующий раздел нет необходимости.
1. Контроль за резистентностью бактерий к антимикробным препаратам:
а) Какие микроорганизмы наиболее часто выделялись от больных в 2010 г.:
| Вид (род) микроорганизма | Количество (абс. число) |
| 1. | |
| 2. и т.д. | |
б) Резистентные формы бактерий в вашем ЛПО (в абсолютных числах):
Приложение 3
к Инструкции Организация и проведение мониторинга антибиотикорезистентности
клинически значимых микроорганизмов к антибактериальным лекарственным средствам в организациях здравоохранения
Республики Беларусь
Научное сопровождение микробиологического и эпидемиологического мониторинга антибиотикорезистентности бактерий
На базе лаборатории клинической и экспериментальной микробиологии ГУ РНПЦ ЭМ по заказу министерства здравоохранения выполняются научно-исследовательские работы по теме: «Микробиологический и эпидемиологический мониторинг резистентности к антимикробным препаратам стафилококков, энтеробактерий и неферментирующих грамотрицательных бактерий».
Целью данной работы является разработка методологических подходов и рекомендаций к осуществлению микробиологического и эпидемиологического мониторинга, снижению циркуляции и уровней антибиотикорезистентности микроорганизмов – стафилококков, энтеробактерий, неферментирующих грамотрицательных бактерий в Республики Беларусь.
Задачи:
Определить удельный вес стафилококков, энтеробактерий, неферментирующих грамотрицательных бактерий в этиологической структуре бактериальных инфекций в медицинских учреждениях различного профиля. Получить данные о биологических свойствах клинически значимых возбудителей в организациях здравоохранения РБ.
Создать коллекцию клинически значимых штаммов бактерий. Провести фенотипирование выделенных штаммов, изучить уровни и спектр антибиотикорезистентности.
Изучить некоторые биологические свойства клинически значимых бактерий: уровни и спектры антибиотикорезистентности, факторы патогенности, молекулярно-генетические характеристики.
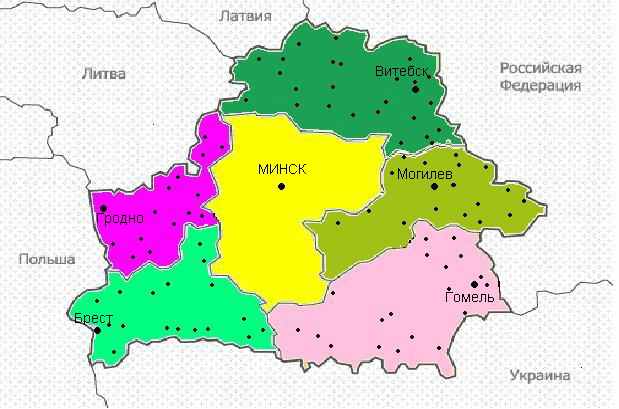
Рис. 1. Территориальное распределение УЗ участников системы микробиологического и эпидемиологического мониторинга антибиотикорезистентности бактерий в Республике Беларусь.
Структура системы мониторинга антибиотикорезистентности клинически значимых микроорганизмов к антибиотикам, антисептикам и дезинфектантам представлена ниже:
| | | | | | | ВОЗ | | | | | | |
| | | | | | |  | | | | | | |
| ESCMID | | FEMS |  | МАКМАХ | | МЗ РБ | | НОЭМП | | РЦГиОЗ | | |
| | | | |  | | | |  | |  | | |
| | |  | | ГУ НИИ ЭМ Референс-центр мониторинга антибиотикорезистентности бактерий | | | | | ||||
 | | | |   | |   | |   | | | | |
| О   порная база МН порная база МН | | Опорная база ВИ | | Опорная база ГР | |     | | Опорная база ГО | | Опорная база МО | | Опорная база БР |
| | | | | | |     | | | | | | |
| Лаб. ОЗ | | Лаб. ОЗ | | Лаб. ОЗ | |       | | Лаб. ОЗ | | Лаб. ОЗ | | Лаб. ОЗ |
| | | | | | |  | | | | | | |
| Лаб. ЦГЭиОЗ | | Лаб. ЦГЭиОЗ | | Лаб. ЦГЭиОЗ | |         | | Лаб. ЦГЭиОЗ | | Лаб. ЦГЭиОЗ | | Лаб. ЦГЭиОЗ |
| | | | | | | | | | | | | |
| Микробиолог | | Микробиолог | | Микробиолог | | | | Микробиолог | | Микробиолог | | Микробиолог |
| | | | | | | | | | | | | |
| Эпидемиолог | | Эпидемиолог | | Эпидемиолог | | | | Эпидемиолог | | Эпидемиолог | | Эпидемиолог |
Рис. 1 Структура системы мониторинга антибиотикорезистентности клинически значимых микроорганизмов к антибиотикам, антисептикам и дезинфектантам
