IV. свойства неорганических веществ
| Вид материала | Документы |
- Рабочая программа по дисциплине "Химическая технология неорганических веществ " Направление:, 112.47kb.
- Задачи урока: Образовательные: Закрепить на практике знания о классах неорганических, 211.06kb.
- Методические указания к выполнению лабораторной работы по курсу «Основные направления, 102.41kb.
- Получение топлив из угля, 241.18kb.
- Рабочая программа дисциплины приборы и методы исследования в технологии неорганических, 249.27kb.
- «показатели качества воды и их определение» введение, 948.44kb.
- Гоу впо «Московский государственный открытый университет», 483.26kb.
- Лабораторная работа №2 Важнейшие классы неорганических соединений, 88.03kb.
- Реферат по курсу технологии неорганических веществ на тему: Технология неконцентрированной, 289.65kb.
- Технология переработки отходов производств, использующих высокочистый кремний 05. 17., 277.13kb.
4.9. Переходные металлы
К переходным металлам относятся химические элементы побочных подгрупп периодической системы химических элементов. Для атомов этих элементов характерно заполнение электронами d-орбитали предпоследнего электронного уровня. Валентные электроны атомов этих элементов размещаются на последнем и предпоследнем электронном уровнях. Эти элементы располагаются в периодической системе, начиная с четвертого периода, между s-элементами и р-элементами.
К переходным элементам относят химические элементы с порядковыми номерами 21-30, 39-48, 57, 72-80, 89, 104-111. Найдите эти элементы в периодической системе, выпишите химические знаки знакомых элементов. Сделайте о них краткие сообщения. Что вы знаете об элементах последней группы?
Медь. Серебро
Медь и серебро, как и золото, относятся к элементам IБ подгруппы. Их атомы, в отличие от атомов щелочных металлов, имеют на предпоследней электронной оболочке не 8, а 18 электронов (n-1/s2p6d10); на последнем энергетическом уровне – один электрон (ns1). Такое строение электронной оболочки и более высокий заряд ядра приводит к относительно меньшим атомным радиусам меди, серебра и золота, по сравнению с атомами щелочных металлов. Это приводит к повышению потенциалов ионизации, что, в свою очередь, обусловливает малую химическую активность этих металлов и выраженные окислительные свойства их катионов.
Для меди наиболее характерны степени окисления +2, +1; для серебра - +1; для золота - +3, +1.
Опыт 1. Физические свойства меди. Рассмотрите образец чистой меди (из коллекции) и опишите ее внешние признаки. Значения физических констант возьмите из справочников. Исключительную теплопроводность меди можно показать на следующем опыте. Возьмите одинаковые по длине и толщине пластинки меди и другого металла или сплава. Укрепите их в двух штативах. На один край пластинок капните по капле раствора поваренной соли, а с других краев нагрейте пластинки пламенем горелок, стараясь, чтобы пламя было в обоих случаях одинаковым.
На какой пластинке капля раствора выпарится быстрее?
Опыты 2-11. Химические свойства меди. а) Внесите медную пластинку или медную проволоку в пламя горелки. При температуре около 150 оС металл покрывается темно-красной пленкой оксида меди (I):
4Cu + О2 = 2Cu2O.
б) При более высокой температуре медь окисляется до оксида меди (II) черного цвета:
2Cu + О2 = 2CuO.
в) Опустите медную проволоку в иодную воду (иодную настойку). Поверхность металла покрывается белым налетом иодида меди (I):
2Cu + I2 = 2CuI.
г) Разотрите в ступке порошок меди с порошком серы. Наблюдайте изменение окраски:
Cu + S = CuS.
Опишите ваши наблюдения реакций между медью и неметаллами и запишите уравнения реакций этого металла с другими неметаллами.
д) Металлическая медь реагирует с азотной кислотой, с концентрированной серной кислотой при нагревании, с солями аммония и железа (III):
Cu + 4HNO3(конц.) = Cu(NO3)2 + 2H2O + 2NO2;
3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 4H2O + 2NO;
Cu + 2H2SO4(конц.) = CuSO4 + 2H2O + SO2;
Cu + 2NH4NO3 = Cu(NO3)2 + 2NH3 + H2;
Cu + Fe2(SO4)3 = CuSO4 + 2FeSO4.
е) В присутствии кислорода воздуха медь реагирует и с растворами кислот-неокислителей, например, с уксусной кислотой, образуя оснóвный ацетат меди (ярь-медянку):
2Cu + 2CH3COOН + О2 = Cu(CH3COO)2×Cu(OH)2.
Проведите эти реакции, опишите внешние признаки и классифицируйте их по различным критериям.
Опыты 12-18. Свойства гидроксида меди. а) Прилейте к раствору (5%) сульфата меди раствор (5%) щелочи, произойдет известная реакция с образованием гидроксида меди (II):
CuSO4 + 2NaOH = Cu(OH)2¯ + Na2SO4.
б) Разделите полученную суспензию на 5 частей. Одну часть слегка нагрейте. Гидроксид меди легко разлагается на оксид меди и воду:
Cu(OH)2
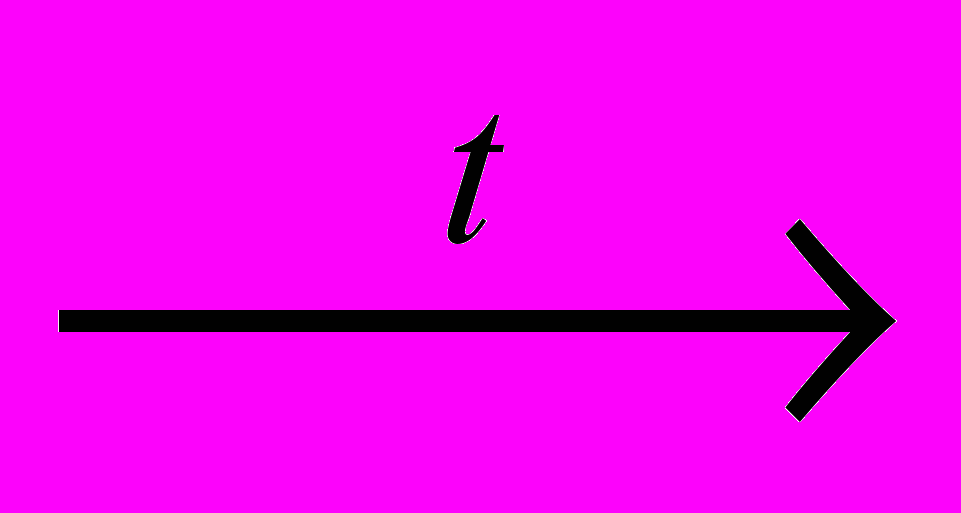 CuO + H2O.
CuO + H2O.в) Ко второй части добавьте маленькими порциями раствор кислоты. Осадок быстро растворится:
Cu(OH)2 + 2HCl = CuCl2 + H2O.
г) К третьей части прилейте равный объем концентрированного раствора щелочи. Происходят ли изменения при обычных условиях? Нагрейте смесь, осадок постепенно растворится с образованием тетрагидроксокупрата натрия:
Cu(OH)2 + 2NaOH = Na2[Cu(OH)4].
д) К четвертой части прилейте раствор (10%) аммиака. Осадок вновь растворится с образованием комплексного соединения:
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2.
е) К пятой части суспензии гидроксида меди добавьте раствор (10%) глюкозы и слегка нагрейте. Наблюдайте образование желтого осадка CuОН, который при дальнейшем нагревании разлагается с образованием красного осадка оксида меди (I):
2Cu(OH)2 + С6Н12О6 = 2CuОН¯ + С6Н12О7 + H2O;
2CuОН
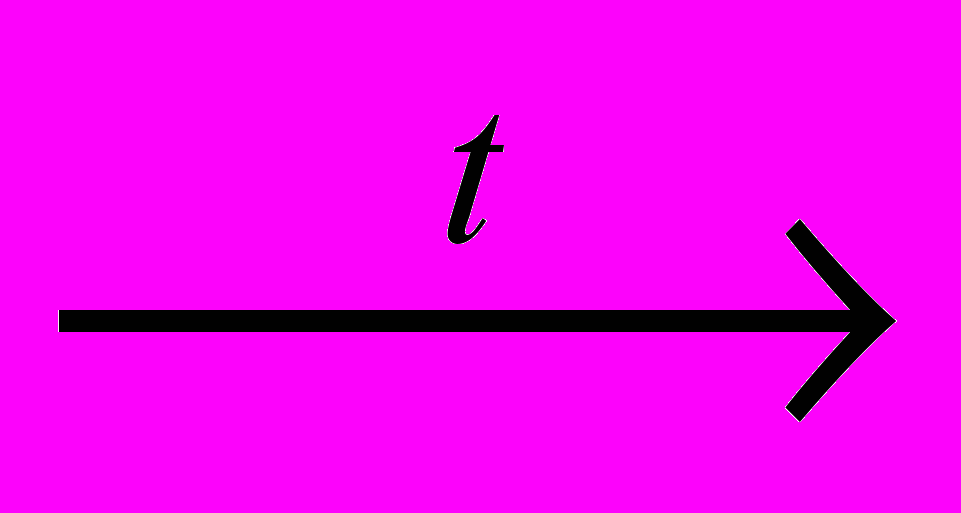 Cu2O + H2O.
Cu2O + H2O.ж) Нагрейте растворы (5%) сульфата меди и гидроксида натрия и слейте их в горячем виде. В этих условиях гидроксид меди не образуется, а сразу же выпадает осадок оксида меди (II):
CuSO4(горячий) + NaOH(горячий) = Na2SO4 + CuO¯ + H2O.
Проанализируйте свойства гидроксида меди, проявленные в этих реакциях, сделайте выводы. Дайте этому веществу полную физико-химическую характеристику.
Опыты 19-22. Свойства оксида меди (II). а) Оксид меди легко восстанавливается водородом, углем, магнием, алюминием и другими восстановителями. Некоторые из этих реакций описаны ранее. Получите медь из оксида несколькими способами и проведите их сравнение.
б) Поместите немного порошка оксида меди (II) (лучше всего для опытов подходит оксид, полученный разложением малахита) в три пробирки; добавьте в них растворы (10%) серной кислоты, соляной кислоты и гидроксида натрия. Что вы наблюдаете? Нагрейте смеси. Какие выводы вы можете сделать о свойствах оксида меди (II)? Почему полученный раствор хлорида меди зеленого цвета, а раствор сульфата меди – синего? Прилейте к зеленому раствору хлорида меди достаточный объем воды. Раствор становится голубым. Почему? Добавьте к полученному раствору насыщенный раствор хлорида калия или натрия. Раствор вновь становится зеленым. Почему? Какое свойство проявляет в этих изменениях цвета хлорид меди?
в) Насыпьте в пробирку порошок оксида меди и залейте раствором (10%) аммиака. Закройте пробирку пробкой и отставьте на некоторое время. Реакция протекает во времени:
CuO + 4NH3×H2O ® [Cu(NH3)4](OH)2 + 3H2O.
Каковы признаки этой реакции? К какому типу она относится?
Опыты 23-30. Свойства солей меди. а) Опустите в раствор соли меди железный гвоздь, гранулу цинка или другие металлы и сплавы. Сделайте выводы о наличии или отсутствии тех или иных взаимодействий. Напишите уравнения реакций. Проведите электролиз растворов солей меди и запишите уравнения процессов.
б) К раствору (5%) сульфата меди прилейте раствор (5%) иодида калия. Раствор становится бурым вследствие выделения иода:
2CuSO4 + 4KI = 2CuI + 2K2SO4 + I2¯.
в) Прилейте к раствору (5%) сульфата меди раствор (10%) аммиака. Наблюдайте образование осадка, который переходит в раствор аммиаката меди ярко-голубого цвета:
2CuSO4 + 2NH3×H2O = (CuОН)2SO4¯ + (NH4)2SO4;
(CuОН)2SO4 + (NH4)2SO4 + 6NH3×H2O = 2[Cu(NH3)4]SO4 + 8H2O.
г) Прилейте к раствору (5%) сульфата меди сероводородную воду. Образуется осадок сульфида меди черного цвета:
CuSO4 + H2S = CuS¯ + H2SO4.
д) Если к суспензии сульфида меди прилить раствор (5%) нитрата серебра, то цвет раствора станет голубым в результате реакции:
CuS + 2AgNO3 = Cu(NO3)2 + Ag2S¯.
Эта реакция доказывает, что абсолютно нерастворимых веществ нет, однако сульфид серебра еще менее растворим в воде, чем сульфид меди.
е) К раствору (5%) сульфата меди прилейте раствор (5%) карбоната натрия. Выпадает осадок гидроксокарбоната меди, средняя соль (карбонат меди) не образуется:
2CuSO4 + Na2CO3 + H2O = (CuOH)2CO3¯ + 2NaHSO4.
ж) Аналогично получите другие нерастворимые соли меди (фосфаты, силикаты). Напишите соответствующие уравнения реакций. Опишите ваши наблюдения. Примечание. Полученные вещества не выбрасывайте, постарайтесь их выделить в чистом виде и использовать для других опытов.
Опыт 31. Физические свойства серебра. Рассмотрите изделие из серебра или серебряную монету и опишите внешние признаки этого металла. Физические константы серебра найдите в справочниках.
Сравните физические свойства меди и серебра.
Примечание. Соединения серебра имеют относительно высокую стоимость, поэтому в опытах расходуйте минимальные объемы растворов и минимальные количества веществ. В тех случаях, когда это возможно, проведите с данной порцией вещества ряд последовательных реакций или осуществите регенерацию реактива.
Опыты 32-37. Получение металлического серебра и его свойства. Серебро легко восстанавливается из растворов солей в виде серебристого металла или черного осадка. а) Капните на пластинки из алюминия, цинка, железа, меди по капле раствора нитрата серебра. Опишите ваши наблюдения и запишите уравнения реакций.
б) Прибавьте к раствору сульфата железа (II) несколько капель раствора нитрата серебра. Наблюдайте выпадение осадка:
3AgNO3 + 3FeSO4 = Fe(NO3)3 + Fe2(SO4)3 + 3Ag¯.
в) Добавьте к осадку в пробирке немного концентрированной азотной кислоты. Осадок растворяется:
3Ag + 4HNO3 = 3AgNO3 +2H2O + NO.
Опыты 38-51. Свойства соединений серебра. а) Нагрейте в пробирке несколько кристалликов нитрата серебра. Наблюдайте образование металлического серебра и появление облачка бурого газа:
2AgNO3
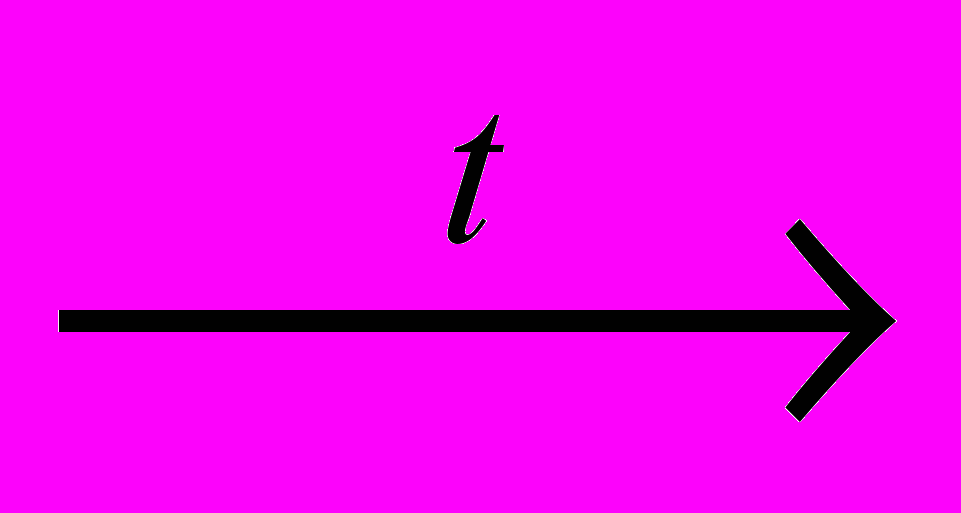 2Ag + 2NO2 + О2.
2Ag + 2NO2 + О2.б) К раствору щелочи добавьте несколько капель раствора нитрата серебра. Обратите внимание на образование осадка:
2AgNO3 + 2NaOH = Ag2O¯ + 2NaNO3 + H2O.
в) В четыре пробирки налейте растворы фторида, хлорида, бромида и иодида натрия. В каждую пробирку добавьте по 2-3 капли раствора нитрата серебра. В первой пробирке нет признаков реакции. Почему? Во второй, третьей и четвертой пробирках выпадают, соответственно, белый, желтоватый и желтый осадки галогенидов серебра:
AgNO3 + NaCl = AgCl¯ + NaNO3;
AgNO3 + NaBr = AgBr¯ + NaNO3;
AgNO3 + NaI = AgI¯ + NaNO3.
г) К первому осадку добавьте по каплям концентрированный раствор аммиака. Осадок растворяется:
AgCl + 2(NH3×H2O) = [Ag(NH3)2]Cl + 2H2O.
д) Ко второму осадку добавьте небольшими порциями раствор тиосульфата натрия. Осадок также растворяется:
AgBr + 2Na2SO3S = Na3[Ag(SO3S)2] + NaBr.
е) К осадку иодида серебра добавьте концентрированный раствор иодида калия. Осадок вновь растворяется:
AgI + 3KI = К3[AgI4].
Какое характерное свойство проявляет серебро в этих трех реакциях? Как называются полученные соединения? К какому классу веществ относятся продукты этих реакций?
ж) К растворам (5%) карбоната, сульфата, роданида, сульфида, ортофосфата натрия или калия прибавьте по 2-3 капли раствора (1%) нитрата серебра. Образуются нерастворимые или трудно растворимые соли серебра:
2AgNO3 + Na2CO3(разб.) = Ag2CO3¯ + 2NaNO3;
2AgNO3 + Na2SO4(конц.) = Ag2SO4¯ + 2NaNO3;
AgNO3 + KSCN = AgSCN¯ + KNO3;
2AgNO3 + Na2S = Ag2S¯ + 2NaNO3;
3AgNO3 + K3PO4 = Ag3PO4¯ + 3KNO3.
Опишите характер полученных осадков и выскажите предположения о возможности использовать эти реакции для идентификации карбонатов, сульфатов, роданидов, сульфидов, ортофосфатов. Какими реактивами, по вашему мнению, можно перевести полученные осадки в растворимые соединения? Проверьте ваши гипотезы опытным путем.
з) Получите немного осадка хлорида серебра. Отфильтруйте смесь через фильтр, разверните его и выставьте на прямой солнечный свет, предварительно закрыв половину осадка на фильтре черной бумагой. Соль на свету темнеет:
2AgCl = 2Ag + Cl2.
Часть хлорида серебра, защищенная темной бумагой не разложилась. Как называются реакции, протекающие под действием света? Где используются светочувствительные свойства соединений серебра?
