Исследовательская работа по химии на тему: «Чистая вода. Какая она?»
| Вид материала | Исследовательская работа |
- Программа "чистая вода" на 2011 2017 годы паспорт федеральной целевой программы "Чистая, 535kb.
- Жила-была река. Сначала она была маленьким, веселым ручейком, который прятался среди, 36.59kb.
- Xi международный симпозиум и выставка «чистая вода россии», 69.46kb.
- Пенсионные фонды и инфраструктурные проекты на примере программы «чистая вода», 76.43kb.
- Федеральной целевой программы "чистая вода" на 2011-2017 годы, 1780.43kb.
- Реферат по химии на тему "Вода", 58.52kb.
- Исследовательская работа по химии Сравнение состава минеральной воды «Хан-Куль», 363.21kb.
- Федеральная целевая программа «Чистая вода» на 2011 2017 годы паспор тфедеральной целевой, 559.1kb.
- 1. я благодарна бабушке за её теплоту, за то, что она растила, воспитывала меня. Она, 20.41kb.
- Методика, диагностирующая и развивающая экологическую культуру. 18 Карточка «мой проект», 206.82kb.
Муниципальное общеобразовательное учреждение
Ремонтненская гимназия №1
Реферативно - исследовательская работа
по химии на тему:
«Чистая вода. Какая она?».

Выполнил: Ковалев Даниил Юрьевич,
ученик 7 «А» класса.
Руководитель: Богданова Людмила Викторовна,
учитель химии.
с.Ремонтное
2010 год
ОГЛАВЛЕНИЕ:
| I.Введение. | стр. | 1-4 |
| II.Основная часть «Результаты изменения состояния воды в течение года». | | 5-15 |
| 2.1.Цветность, мутность. | стр. | 5-6 |
| 2.2.рН среда, нитраты. | стр. | 6-7 |
| 2.3. Жесткость, хлориды. | стр. | 8-10 |
| 2.4.Сухой остаток. «Состояние воды в зависимости от географического положения села» | | 10-11 |
| 2.5. Антинакипины. | стр. | 12 |
| 2.6.Способы очистки воды. | стр. | 13-14 |
| III. Заключение. | стр. | 15 |
| IV. Список литературы. | стр. | 16 |

-
«В природе нет такой вещи, которая излечивала бы все болезни, но если бы она была, то это бы была вода в правильном использовании»
Доктор Диндлар
Реферат
С древних времен известно, что 999 болезней из 1000, связаны с качеством питьевой воды. Питьевая вода, которая не соответствует установленному стандарту, может содействовать зарождению и развитию хронических заболеваний внутренних органов, ускорять старение организма, вызывать неприятные ощущения и внутренний дискомфорт. Некачественная питьевая вода, по мнению врачей, сокращает продолжительность жизни от 3 до 7 лет.
Человек для нормальной жизнедеятельности должен каждый день употреблять не менее 3 литров воды в виде напитков и в составе разнообразной пищи.
Наиболее полезной, для постоянного употребления, является сырая вода питьевого качества, в которой оптимально уравновешено содержание природных химических элементов и соединений.
Оптимальная по составу питьевая вода имеет такие показатели: кальций и магний - 30 - 50 мг в 1 л воды (кальция должно быть больше магния), натрий и калий - до 80 мг, сульфаты - до 50 мг, хлориды - до 50 мг, бикарбонаты - до 200 мг. Вода подобного состава может без каких-либо ограничений постоянно использоваться в сыром виде при условии ее санитарной безопасности.
Как хорошо жилось нашим предкам, спокойно набиравшим воду прямо из родников и рек. Увы, сегодня это невозможно. По данным областного Управления Роспотребнадзора, чуть ли не все ростовские источники нынче опасны - пить из них категорически не рекомендуется. Что же можно говорить о водопроводной воде, учитывая катастрофическую ветхость систем водоснабжения. Если наполнить стакан водой из-под крана водопровода г. Ростов-на–Дону и оставить на 10 минут, то можно увидеть мутный осадок на дне стакана и ощутить приторный привкус хлора. А теперь только можно представить, как вся эта грязь ежедневно проникает в наш организм, заполняя внутренние органы. Водопроводная вода наполнена сверх всякой нормы многими органическими соединениями. Врачи бьют тревогу: пропуская жидкость, наш организм действует, словно фильтр, оставляя в себе все содержащиеся в воде примеси! А вывести соли тяжелых металлов чрезвычайно сложно, почти невозможно! Нитраты поражают дыхательную систему и сердце, поэтому готовить на водопроводной воде не рекомендуется. Алюминий накапливается в головном мозге и забивает печень. Но коварнее всех хлор, тот самый который добавляют, перед тем как пустить воду по трубам. Чтобы избавиться от запаха мы, как правило, пробуем её кипятить. Однако именно при кипячении хлорированной воды образуются опаснейшие органические соединения, наполняя питьевую воду канцерогенами и токсинами. Соли хлора хорошо выпадают в осадок при замораживании и последующем размораживании, т.е. таким образом можно частично себя обезопасить.
Кроме этого, питьевая вода может быть санитарно- опасной, другими словами, содержать болезнетворные бактерии в случаях недостаточного ее обеззараживания на сооружениях водоподготовки, загрязнения микроорганизмами во внешних и внутренних водопроводных сетях, использования грязной или использованной больными посуды.
Питьевая вода особенно опасна в том случае, когда в водопроводную сеть каким-либо путем попадает сточная вода из канализационной сети. Возможными последствиями этого могут быть заражения воды бактериями брюшного тифа, холеры, паратифа, дизентерии, а также вирусами гепатита.
Для определения качества воды требуется проведение большого числа разнотипных анализов - химических, физико-химических, санитарно- бактериологических. Набор разнохарактерных определений обусловлен сложностью состава примесей воды и большим разнообразием целей, для которых выполняется анализ. Основными задачами, решаемыми на основе анализов, являются:
- оценка санитарно-токсикологического состояния воды;
- определение пригодности воды для конкретного вида потребления;
- определение степени и характера загрязненности воды; выявление возможности применения тех или иных методов очистки воды;
- управление процессами очистки воды и контроль работы сооружений.
При оценке воды есть показатели, общие для всех категорий воды, но есть и специфические, необходимые для характеристики той или иной воды.
Для исследования качества воды питьевой водопроводной, отобранной из водопроводной сети (колонки) с.Ремонтное ул.Гоголя,104 были взяты официальные результаты физико-химических испытаний, проведенных специалистами Роспотребнадзора по Ростовской области в г.Волгодонске, Дубовском, Ремонтненском и Заветинском районах в условиях лаборатории.
Результаты изменения состояния воды в течение года.
Цветность поверхностных вод вызывается присутствием органических соединений, которые образуются в процессе химического и биологического разложения остатков растений.

| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 2,7 | 3,1 | 0,6 | 1,2 | 2,1 | 3,5 | 3,1 | 0 | 0,42 | 1,9 | 1,3 | 2,7 |
Уровень цветности питьевой воды не должен превышать более 20 градусов.
Вывод: наиболее высокий уровень цветности в жаркое время года, т.к. выпадает минимальное количество осадков, растворяющих окрашенные органические вещества.
Мутность воды обусловлена присутствием нерастворимых и коллоидных веществ неорганического (глина, песок) и органического происхождения (ил, планктон).

| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 0,23 | 0,29 | 0,41 | 0,17 | 0,058 | 0,12 | 0,23 | 0 | 0,12 | 0,12 | 0,12 | 0,058 |

При величине допустимого уровня: не более 1,5 мг/дм3.
Вывод: наиболее высокие показатели мутности в период таяния снега, паводка, т.к. дождевая вода просачивается сквозь грунт и увлекает за собой нерастворимые частицы почвы.
Организм человека в значительной степени состоит из воды, среды, в которой перемещаются питательные вещества, кислород и др. важные для организма элементы. Водная среда организма может иметь кислотные или щелочные свойства, которые определяются по специальной шкале, называемой pH-фактором (pH - potential hydrogen - потенциальный водород). Если уровень pH находится в пределах от 1,0 до 6,9, то среда называется кислой, 7,0 - нейтральная среда, а при уровне pH от 7,1 до 14,0 среда является щелочной. Чем ниже pH фактор, тем выше кислотность, чем
выше pH, тем выше щелочность среды.
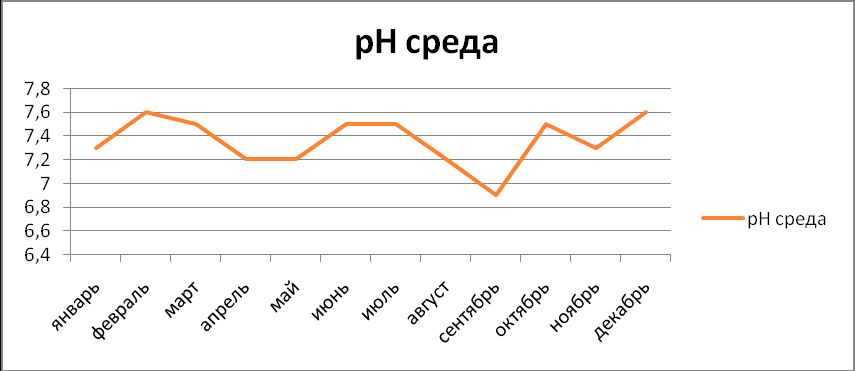
| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 7.3 | 7.6 | 7.5 | 7.2 | 7.2 | 7.5 | 7.7 | 7.2 | 6.9 | 7.5 | 7.3 | 7.6 |
При величине допустимого уровня: в пределах 6,0 - 9,0 ед. рН
Вывод: в отличии от других характеристик рН-фактор соответствует допустимым нормам. Повышение кислотности воды можно связать с кислотной средой осадков, выпадающих в летнее время года («кислотные дожди»).
Нитраты - это соли азотной кислоты, которые накапливаются в продуктах и воде при избыточном содержании в почве азотных удобрений.
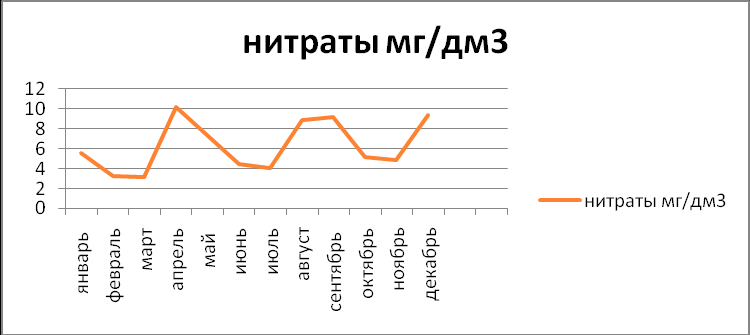
| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 5,5 | 3,2 | 3,1 | 10,2 | 7,4 | 4,4 | 4,0 | 8,9 | 9,2 | 5,1 | 4,8 | 9,4 |
При величине допустимого уровня: не более 45,0 мг/дм3
Жесткость - свойство воды, определенное наличием солей кальция и магния в растворенном виде.
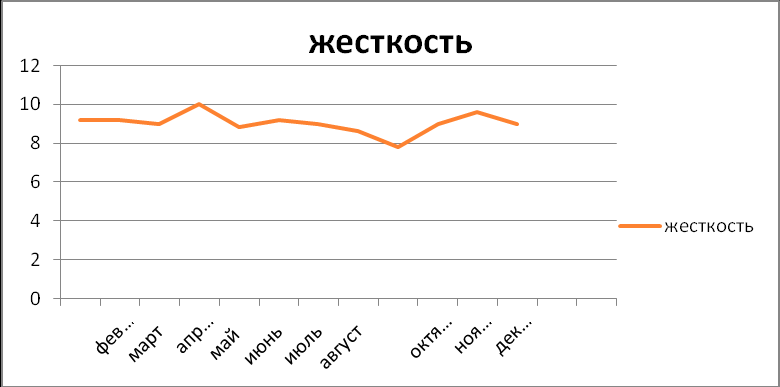
| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 9,2 | 9,2 | 9,0 | 10,0 | 8,8 | 9,2 | 9,0 | 8,6 | 7,8 | 9,0 | 9,6 | 9,0 |
При величине допустимого уровня: не более 7,0 (моль/м3).
Вывод: наша вода очень жесткая и независимо от климатических условий в течение всего года показатели превышают предельно допустимую концентрацию.
Хлориды - это соли соляной кислоты, которые есть почти во всех водах. Не имеют ничего общего с активным хлором. Присутствие хлоридов в воде объясняется наличием в породах наиболее распространенной на Земле соли – хлорида натрия. Она необходима для удержания полезных микроэлементов в организме, при этом обладает лёгкими антисептическими свойствами.

| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 172 | 153,6 | 138,2 | 177,6 | 182,4 | 158,4 | 163,2 | 134,4 | 126,7 | 182,4 | 186,2 | 181,3 |
При величине допустимого уровня: не более 350,0 мг/дм3
Вывод: содержание хлоридов в воде в норме.

Под сухим остатком подразумевается сумма всех примесей воды. Величина сухого остатка характеризует степень общей загрязненности воды


Пояснение: Сухой остаток определяется путем выпаривания литра воды и взвешивания того, что осталось. Сухой остаток характеризует общее содержание в воде минеральных солей, которое рассчитано суммированием концентрации каждой из них, без учёта летучих органических соединений. Пресной считается вода, имеющая общее солесодержание не более 1 г/л.
| январь | февраль | март | апрель | май | июнь | июль | август | сентябрь | октябрь | ноябрь | декабрь |
| 1045,0 | 1037,5 | 1026,0 | 1082,5 | 1156,5 | 998,5 | 1007,0 | 0 | 966,0 | 1095,0 | 1073,5 | 1111,0 |
При величине допустимого уровня: не более 1000,0мг/дм3
Вывод: содержание сухого остатка в воде чуть превышает предельно допустимую концентрацию, особенно в период выпадения осадков. Это связано с составом почвы.
Также, мною, изучено состояние воды в зависимости от географического расположения села.
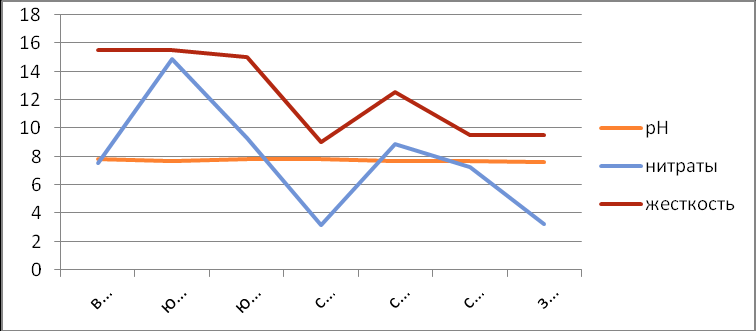

| | Предел допустимого уровня | восток | юг | юго-восток | северо-восток | север | северо-запад | запад |
| рН | 6,5-8,5 | 7,8 | 7,7 | 7,8 | 7,8 | 7,7 | 7,7 | 7,6 |
| Нитраты | 45,0мг/дм3 | 7,6 | 14,9 | 9,3 | 3,2 | 8,9 | 7,3 | 3,3 |
| жесткость | 7,0 моль/м3 | 15,5 | 15,5 | 15,0 | 9,0 | 12,5 | 9,5 | 9,5 |
| хлориды | 350,0 мг/дм3 | 427,2 | 427,2 | 422,4 | 168,0 | 297,6 | 172,8 | 172,8 |
Пробы воды водопроводной (колонки, артезианские скважины) отобраны в середине июля 2009г. (15,07) соответствуют по химическим показателям как хозяйственно - питьевая и культурно - бытовая вода, но не соответствуют нормам (требованиям), предъявляемым к воде как питьевая двум показателям; по жесткости на всей территории села, а по хлоридам на востоке, юге и юго-востоке села (ул. Пушкина, ул. Октябрьская).
Жесткость воды – характеристика соединения солей кальция и магния.
Различают : 1) временную жесткость воды, обусловленную наличием в воде гидрокарбонатов кальция Ca (HCO3)2 и магния Mg (HCO3)2. При кипячении идет разложение на карбонат кальция и гидрооксид магния (CaCO3, Mg(OH)2)c выделением CO2 ;
2) постоянную жесткость воды, обусловленную наличием в воде сульфатов Ca, Mg (СaSO4, MgSO4), хлоридов Ca, Mg (CaCl2, MgCl2) и других солей ((силикатов, нитратов, фосфатов) - Ca, Mg).
| Характеристика воды по жесткости | |
| Очень мягкая | Не более 1,5 |
| Мягкая вода | От 1,5до 4,0 |
| Вода средней жесткости | От 4,0до 8,0 |
| Жесткая вода | От 8,0до 12,0 |
| Очень жесткая вода | Свыше 12,0 |
Общая жесткость водопроводной воды в г. Ростове-на-Дону от 6 до 8 моль/м3 в течение от времени года, воды в черном море 65,5 моль/м3,в с.Ремонтном от 7,8 до 10 моль/м3.

В жесткой воде плохо растворяются продукты питания, плохо и долго растворяется чай. Постоянное употребление жесткой воды приводит к отложению солей в организме человека. В жесткой воде плохо мылится мыло. Также жесткая вода способствует образованию накипи в чайниках, что значительно снижает интенсивность теплообмена, приводит к большому перерасходу электроэнергии, выходу из строя деталей турбин и т.д.
Для устранения, или уменьшения жесткости применяются специальные методы – например, реагентный метод (известково-содовый).
Существуют антинакипины - химические препараты для удаления с внутренних стенок эмалированной посуды накипи, отложений, образующихся при нагревании и кипячении воды вследствие выпадения в осадок содержащихся в ней солей (СаСО3, MgCO3, CaSO4 и др.). Накипь хорошо растворяется минеральными кислотами, которые, однако, быстро разрушают металлические стенки и эмаль, поэтому для удаления накипи в быту, как правило, применяют средства на основе более слабых органических кислот (лимонной, щавелевой). Антинакипины выпускают в виде порошков.
В стиральных машинах накипь появляется не из-за воды, а из-за стирального порошка. Если взять порошок, развести 1/3 столовой ложки в 1 стакане воды и перемешать, то можно увидеть осадок, который будет плавать в стакане и не растворится никогда. Это "утяжелитель" порошка. В России - это пластиковая стружка, в Финляндии - каменная крошка. Добавляется исключительно как маркетинговый ход (реклама). Если положить в стакан железные гвозди, и оставить на 1-2 месяца, то гвозди обрастут ржавчиной, вода станет темно бурого цвета, непрозрачной. Можно представить, что происходит со стиральной машиной.
Общий вывод по характеристике водопроводной воды с. Ремонтного: Вода из водопроводной сети соответствует государственным стандартам технической воды.
А можно ли очисть воду собственными силами, в бытовых условиях?
1 способ – отстаивание:
Если приходится пить воду из-под крана, ее желательно подвергнуть отстаиванию хотя бы в течение суток. Конечно, артезианской она от этого не станет, но зато улетучится хлор. Кроме того, осядут на дно механические примеси типа песка, ила, соединения железа, некоторые микроорганизмы. Чем медленнее вода движется по трубам, тем примесей набирается больше. Быстрее всего вода бежит по трубам вечером, в период максимального водорасхода. А значит, лучше всего набирать воду для питья в вечерние часы и ставить отстояться. Но, конечно, независимо от времени суток, надо еще на эту самую воду и поглядывать. Если она грязно-ржавая и пахнет тиной, значит, в водопроводе произошла какая-то очередная авария. Бытовой фильтр такую ржавчину, конечно, задержит, но это, возможно, будет его последним добрым делом: ресурс фильтрующего картриджа на ржавой воде уменьшится в несколько раз.
2 способ- кипячение:
Позволяет избавиться от временной жесткости, хлора и большей части бактерий. Кипятить следует достаточно долго и с открытой крышкой: есть шанс, что тогда чайник покинет кое-какая летучая вредная органика. Только вот любая вода после кипячения становится абсолютно невкусной. Нагревание удаляет из нее весь кислород, делает как бы "мертвой".
3 способ- замораживание:
При замерзании воды лучше отделяются взвешенные частицы. Особенно, если только слегка приморозить воду и выбросить лед, вобравший песчинки, или прочий мусор, - вода явно станет прозрачнее. Но замораживание не освобождает воду от химических примесей.
4 способ- фильтрование воды через природные материалы:
В природе вода медленно осветляется и очищается, проходя через десятки и сотни метров пористых горных пород в течение многих дней и недель. Попытки достичь того же эффекта в домашних условиях заранее обречены на неудачу. Нужны сотни тонн песка, известняка или глины, чтобы действительно очистить несколько десятков литров воды. Но если из крана идет мутная, ржавая жидкость, то можно попробовать профильтровать ее через слой песка - часть механических примесей удастся задержать.
Общий вывод довольно неутешителен: ни один из домашних методов очистки воды не позволяет избавиться от самых опасных загрязнителей - тяжелых металлов и других вредных химических соединений.
Улучшить качество воды можно одним из следующих способов:
Улучшить качество питьевой воды можно с помощью фильтров.
Если в доме нет очистителей воды, то рекомендуется взять на заметку следующие рецепты:
- в местностях, где воды немного, пить ее следует с небольшим количеством уксуса: 1 л воды – 1-2 чайные ложки яблочного уксуса и меда, 3 - 5 капель 5%-го йода (в такой среде микробы погибают за несколько минут);
- изготовить из шерсти фитиль, опустить один его конец в посуду с водой, а другой - в пустую. Вода станет капать, из полной в пустую посуду уже хорошо очищенной. Это один из лучших способов, - через такую очистку воду можно пропускать несколько раз;
- вскипятить горькую или плохую воду и бросить в нее чистую глину и клубки шерсти, затем вынуть их и отжать. Отжатая вода будет гораздо лучшего качества;
- соленую воду можно пить, добавив в нее ягоды боярышника;
- 10 - 15 листьев рябины на 1 - 3 л воды делают ее чистой через 2 часа (даже болотную, охотники это знают). Листья можно использовать повторно, только надо осторожно промыть чистой водой и затем уже настаивать не менее 3 часов. Листья высушивают в тени и для хранения складывают в деревянный ящик или картонную коробку.
Таким образом, питьевая вода должна быть не только чиста на бактериологическом уровне, и не иметь вредных для человека веществ, но и содержать полезные минералы (из воды они лучше усваиваются организмом, чем из пищи). В последнее время, как для питья, так и для приготовления пищи всё чаще стала использоваться питьевая бутилированная вода, которая не подвергается обработкам и очистке, сохраняя свои натуральные природные свойства. Наиболее полезна для организма натуральная подземная вода, которая добывается из источника и разливается непосредственно в месте добычи с применением современных технологий, исключающих влияние наружной среды и контакт с человеком. Расположенные глубоко в земле такие источники имеют естественную природную защиту в виде пластов глины и кварцевого песка, что исключает попадание в воду загрязнений из внешней среды. Эта вода не только утоляет жажду, но и способствует оздоровлению организма.
Список литературы.
1. «Химия воды и микробиология», Т.А. Карюхина, И.Н.Чурбанова, Москва, Стройиздат, 1983г.
2. «Химическая энциклопедия», ТТ. 1,2,3, издательство «Советская энциклопедия», Москва,1990 год.
3. Для подготовки данной работы были использованы материалы с сайтов интернета: referat.ru; vsereferat.ru; rusreferat.ru; bankofreferat.ru; 5-ballov.ru; www.xumuk.ru.

