Исследование экологического статуса систем «почва-растение» степной зоны при антропогенном воздействии
| Вид материала | Исследование |
- Методические рекомендации по выполнению оценки качества среды по состоянию живых существ, 443.86kb.
- Ические средства контроля и мониторинга экологического статуса компонентов окружающей, 12.92kb.
- Оценка и экологическое обоснование комплексных приемов коррекции поллютантов в системе, 642.86kb.
- Миграция тяжелых металлов в системе «почва-растение» при внесении осадка сточных вод, 640.08kb.
- Морфофункциональные изменения в лимфоидных органах при воздействии экотоксикантов, 865.65kb.
- Задачи и основные принципы экоаудита. Критерии аудита систем экологического менеджмента, 45.12kb.
- Лишайники степной зоны южного урала и прилегающих территорий 03. 00. 24 «Микология», 399.34kb.
- Исследование систем управления Введение Учебный курс "Исследование систем управления", 2314.26kb.
- Внедрение систем экологического менеджмента экономически эффективно для государства, 448.91kb.
- Наименование тем лекционных занятий, их содержание, объем в часах, 15.64kb.
В качестве объектов исследований использовались следующие виды сорных растений: щирица запрокинутая (Amaranthus retroflexus L.), марь белая (Chenopordium album L.), латук дикий (Lactuca serriola L.), молочай Вальдштейна (Euphorbia Waldsteinii), а также культурные растения: кукуруза сорта Кичкасская местная, подсолнечник сорта Скороспелый, баклажан, перец, томат, капуста, входящие в состав агроценозов Оренбургской области.
Надземные органы вегетирующих растений обрабатывались растворами гербицида (раундап) разных концентраций ( 2 %, 4 %, 8%, 10%) с помощью пульверизатора из расчета 2 л/га. Объем раствора гербицида для всех вариантов опыта брался постоянный, обеспечивающий полное, равномерное смачивание всех растений. Контрольные растения аналогичным образом опрыскивали чистой водой. Затем отделенный от растения лист помещали в камеру экспериментальной установки, облучали его источником света и в течение 300 секунд регистрировали количество импульсов (площадь каждого листа была одинаковой). Замедленную флуоресценцию последовательно измеряли у обработанного гербицидом и контрольного растений. При этом учитывалась также продолжительность воздействия гербицида на растения (1, 2, 3, 4 суток).
Для исследования влияния физико-химических свойств почвы на замедленную флюоресценцию растений, растения выращивались на различных типах почв, характерных для Оренбургской области. При изучении влияния тяжелых металлов на замедленную флюоресценцию растения выращивались на черноземе обыкновенном. Растения, выращенные до состояния 4-5 листа, извлекались из земли и погружались корневой системой в растворы солей металлов концентраций 1,5,10,15,20 мг/л на время три часа для установления равновесных концентраций. Затем листья 3-4 ярусов удалялись для проведения измерений. После помещения листьев в измерительную камеру, листья адаптировались к темноте в течение пяти минут. Для этих экспериментов использовались культурные растения томат, баклажан, капуста, перец, подсолнечник, кукуруза.
В наших исследованиях строго учитывалось возрастное состояние исследуемых листьев. Для определения использовали листья одного яруса (3 - 4 лист). Все измерения выполняли в 10-кратной повторности.
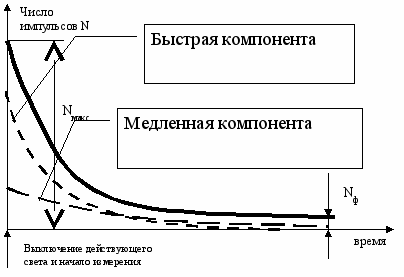
Рисунок 2. Характерная кривая кинетики замедленной флюоресценции растений.
На рисунке 2 приведена характерная кривая замедленной флюоресценции (ЗФ) растений, регистрируемая при помощи описанного выше устройства. Собственный фон установки Nф вычитался из зарегистрированного числа импульсов флюоресценции. Кривая кинетики ЗФ (выделенная кривая рисунка 2) представлялась в виде суммы экспонент (по методу Левенберга –Макгравта), с целью выявления быстрых Nб и медленных Nм компонент флуоресценции (рисунок 2 пунктирные кривые). Быстрые и медленные компоненты отличаются амплитудами G и D, а также постоянными a и b, характеризующими интенсивность затухания ЗФ.
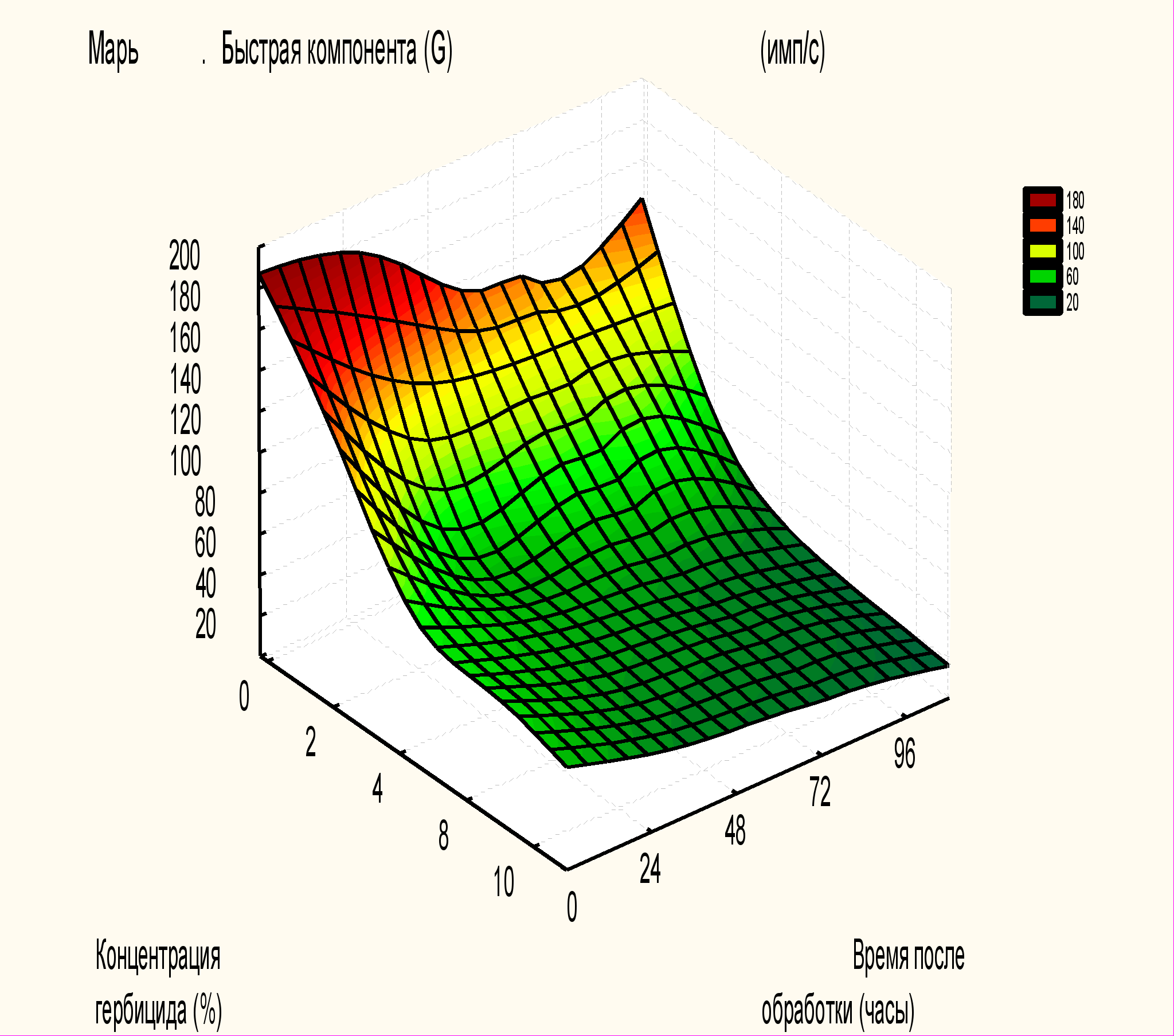
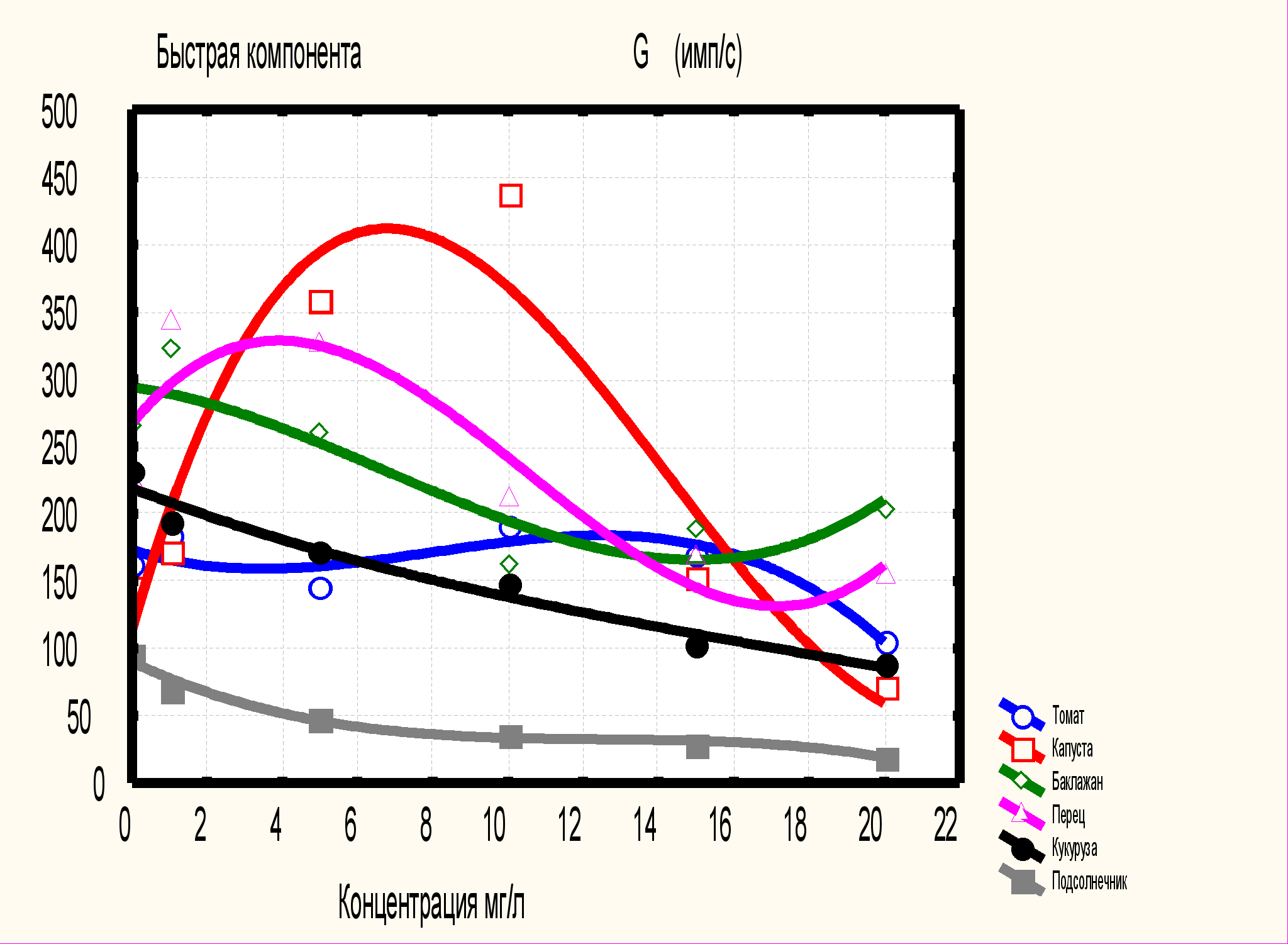
На рисунке 3 представлен результаты экспериментальных исследований влияния различных концентраций гербицида раундап на параметры замедленной флюоресценции (для примера приведены результаты влияния гербицида на ростки мари). Анализируя графические зависимости, представленные на рисунках, видно, что амплитуда быстрого компонента (G) у контрольных образцов растений понижается с течением времени. У контрольных образцов молочая и щирицы амплитуда быстрого компонента достигает максимума на третьи и вторые сутки после обработки гербицидом. Обработка растений гербицидом приводит к резкому снижению интенсивности быстрой компоненты у всех опытных образцов растений. При этом максимальное снижение интенсивности быстрой компоненты отмечено у латука на четвертые сутки после обработки 10%-ным раствором раундап. У латука, подсолнечника отмечается повышение быстрой компоненты при обработке гербицидом на третьи сутки с последующим снижением. Аналогичная зависимость отмечается у молочая, щирицы и кукурузы на вторые сутки после обработки гербицидом. Следует отметить нелинейную зависимость быстрой компоненты от концентрации гербицида.
а б
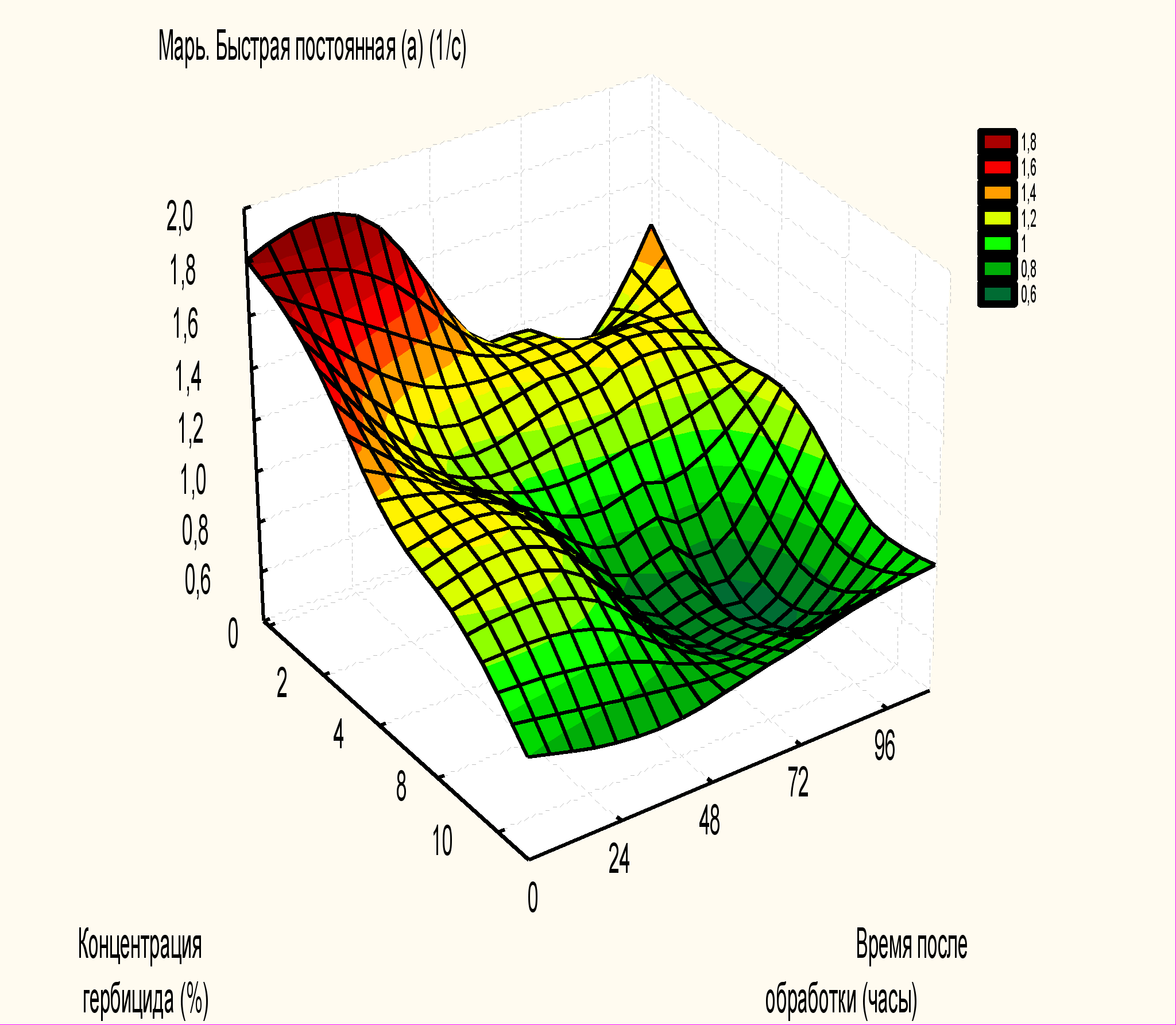
Рисунок 3. Зависимость быстрой компоненты G(имп/с) (а) и быстрой постоянной а(1/с) (б) от концентрации гербицида и времени после обработки .
По графическим зависимостям видно, что у контрольных образцов всех растений отмечается тенденция к снижению амплитуды медленного компонента (D) как с течением времени после обработки гербицидом, так и при увеличении концентрации гербицида. Анализ графических и табличных данных показывает, что быстрая постоянная (а) снижается как с течением времени после обработки, так и с увеличением концентрации гербицида. У молочая, например, при концентрации гербицида 10% происходит увеличение быстрой постоянной с течением времени после обработки гербицидом.
Из анализа корреляции видно, что наиболее сильная отрицательная корреляционная связь параметров ЗФ и концентрации гербицида (раундап) отмечается у баклажана, капусты, кукурузы, мари, перца, подсолнечника, томата. Рассмотрим действие на параметры ЗФ солей тяжелых металлов.
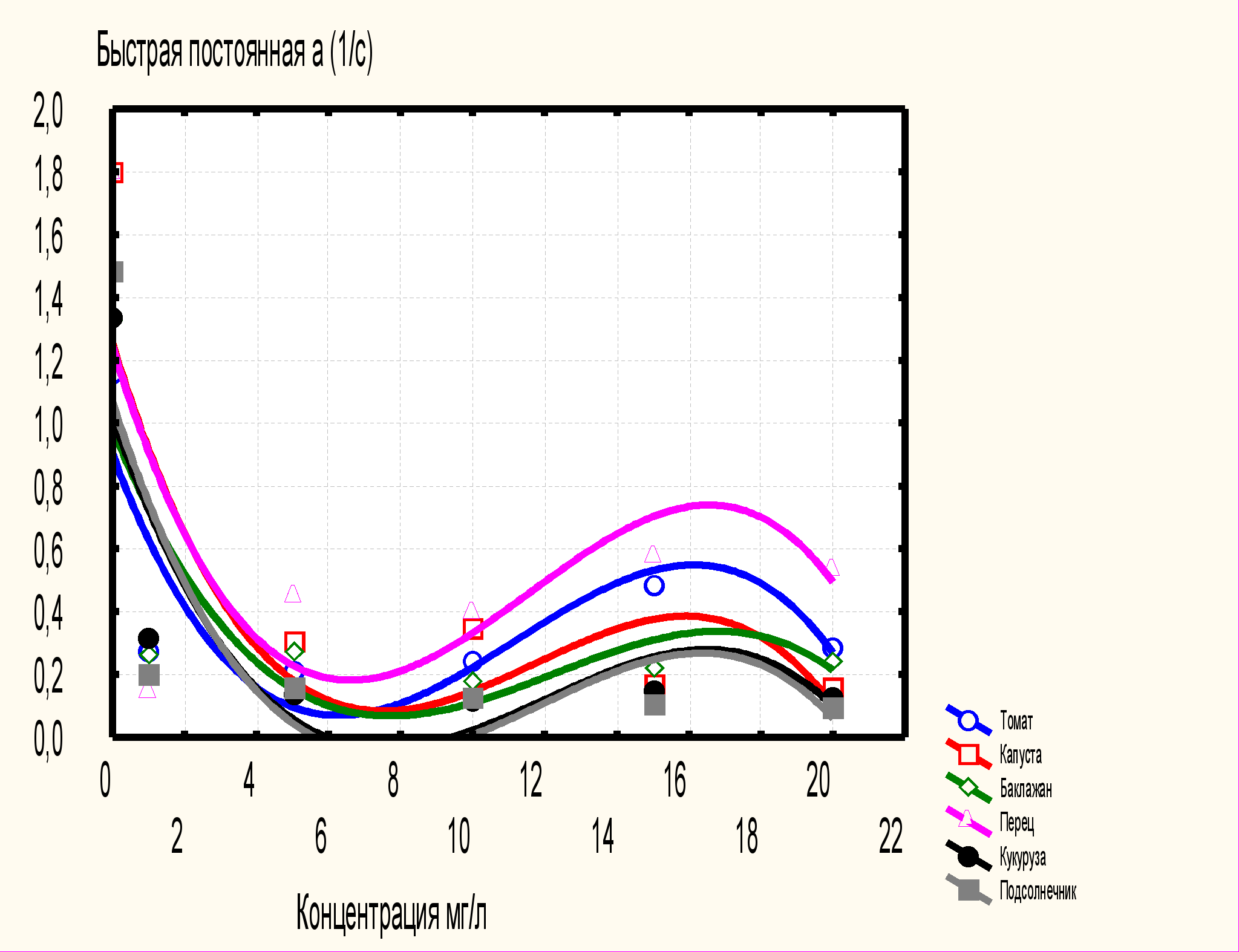
Марганец. Анализируя графические зависимости (рисунок 4), можно сделать вывод, что с увеличением концентрации марганца, у баклажана отмечается тенденция понижения быстрого компонента, вместе с тем, максимальное его значение наблюдается при концентрации 1мг/л, минимальное - при концентрации 10мг/л.
а б
Рисунок 4. Зависимость быстрой компоненты G(имп/с) (а) и быстрой постоянной а(1/с) (б) от концентрации марганца
С увеличением концентрации марганца у баклажана, томата, перца, капусты, кукурузы и подсолнечника отмечается тенденция понижения медленного компонента. По графическим зависимостям видно, что с увеличением концентрации металла у всех растений отмечается понижение быстрой и медленной постоянной, при этом у томата, капусты, баклажана, перца повышается быстрая постоянная при концентрациях марганца 5-15мг/л. Следует отметить, что максимальные значения параметров отмечено у контрольных образцов.
Кобальт. У баклажана наблюдается тенденция к снижению быстрого компонента с увеличением концентрации кобальта, при этом минимальное его
значение наблюдается при концентрации 20мг/л, а максимальное – при концентрации 15мг/л. У капусты происходит возрастание быстрого компонента при концентрациях металла от 0 до 15мг/л, а при концентрации 20мг/л значение быстрого компонента снижается (минимальное значение). Из всех растений подсолнечник характеризуется наименьшим значением быстрого компонента.
Медь. С увеличением концентрации меди у баклажана происходит понижение быстрого компонента, при этом максимальное его значение наблюдается у контрольного образца, минимальное - при концентрации 20мг/л. У капусты четкой зависимости не наблюдается: так при концентрации 1мг/л и 15мг/л отмечаются низкие значения быстрого компонента, при концентрации 5 и 10мг/л – высокие. У перца при концентрации 10-20 мг/л быстрый компонент достигает максимального значения. Медленная постоянная характеризуется повышением величины, начиная с концентрации 1мг/л до концентрации 15мг/л, с последующим снижением.
Свинец. С увеличением концентрации свинца у баклажана, капусты, подсолнечника и перца отмечается тенденция снижения быстрого компонента с
максимальными значениями для контрольных образцов и незначительным увеличением параметра при концентрациях 1мг/л (для баклажана), 10мг/л (для
капусты) и 5мг/л (для перца и подсолнечника). У томата и кукурузы также отмечается тенденция снижения быстрого компонента, вместе с тем максимальное его значение отмечается при концентрации 5мг/л (для томата) и 10мг/л (для кукурузы).
Хром. Анализируя графические зависимости можно сделать вывод, что у баклажана, подсолнечника и томата отмечается тенденция снижения быстрого компонента с увеличением концентрации хрома. У капусты, перца и кукурузы отмечается, при общем снижении, увеличение параметра при концентрациях 10мг/л (томат, перец), 5мг/л (капуста ), 1мг/л (кукуруза). Медленная постоянная снижается по сравнению с контрольным образцом при концентрации хрома 1мг/л.
Цинк. С увеличением концентрации цинка отмечается тенденция понижения быстрого компонента. При этом следует отметить резкое увеличение параметра у всех опытных растений при концентрациях 1-10мг/л. Динамика медленной компоненты характеризуется значительным увеличением
по сравнению с контрольными образцами. Быстрая и медленная постоянные снижаются с ростом концентрации металла.
а б
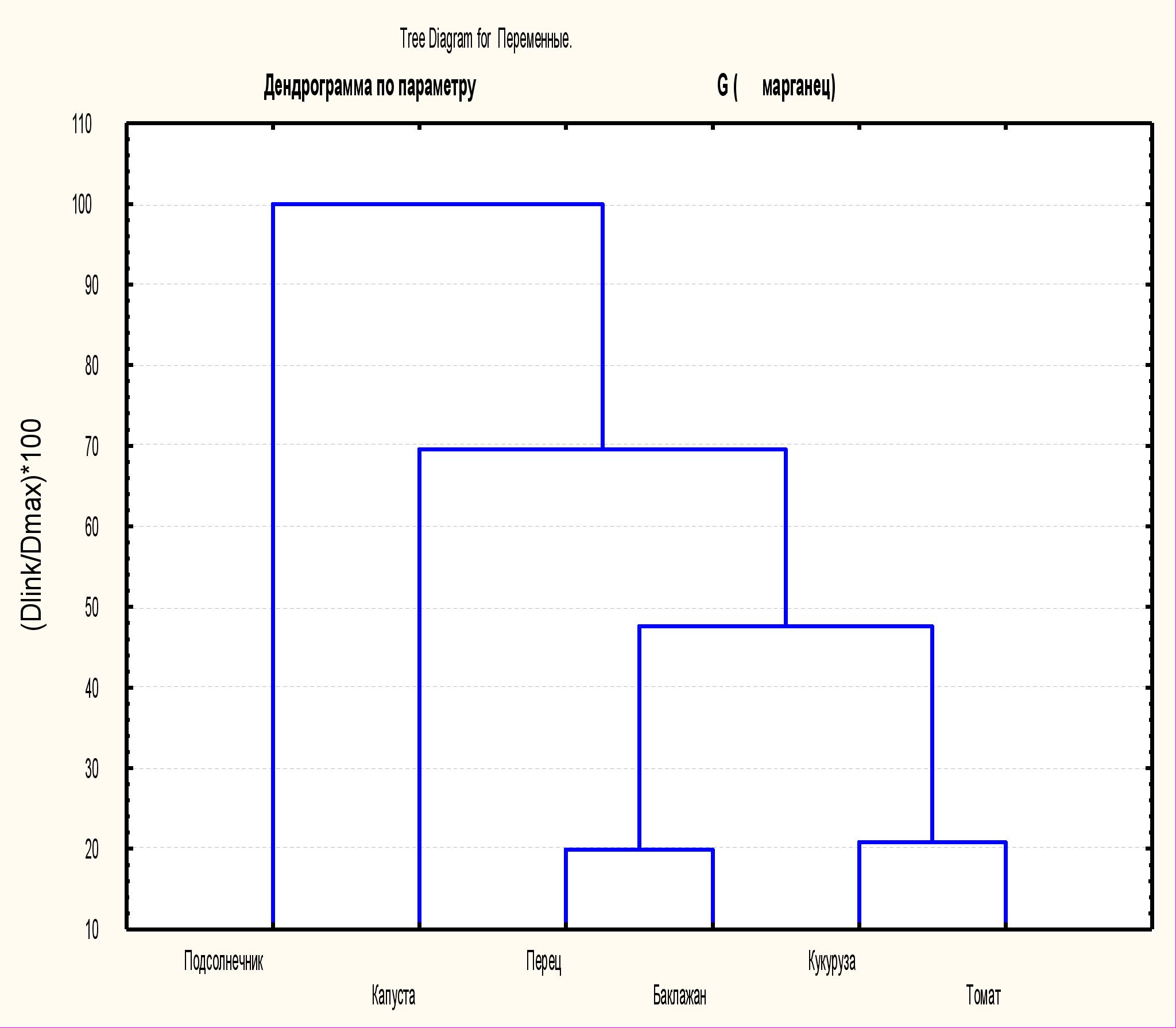
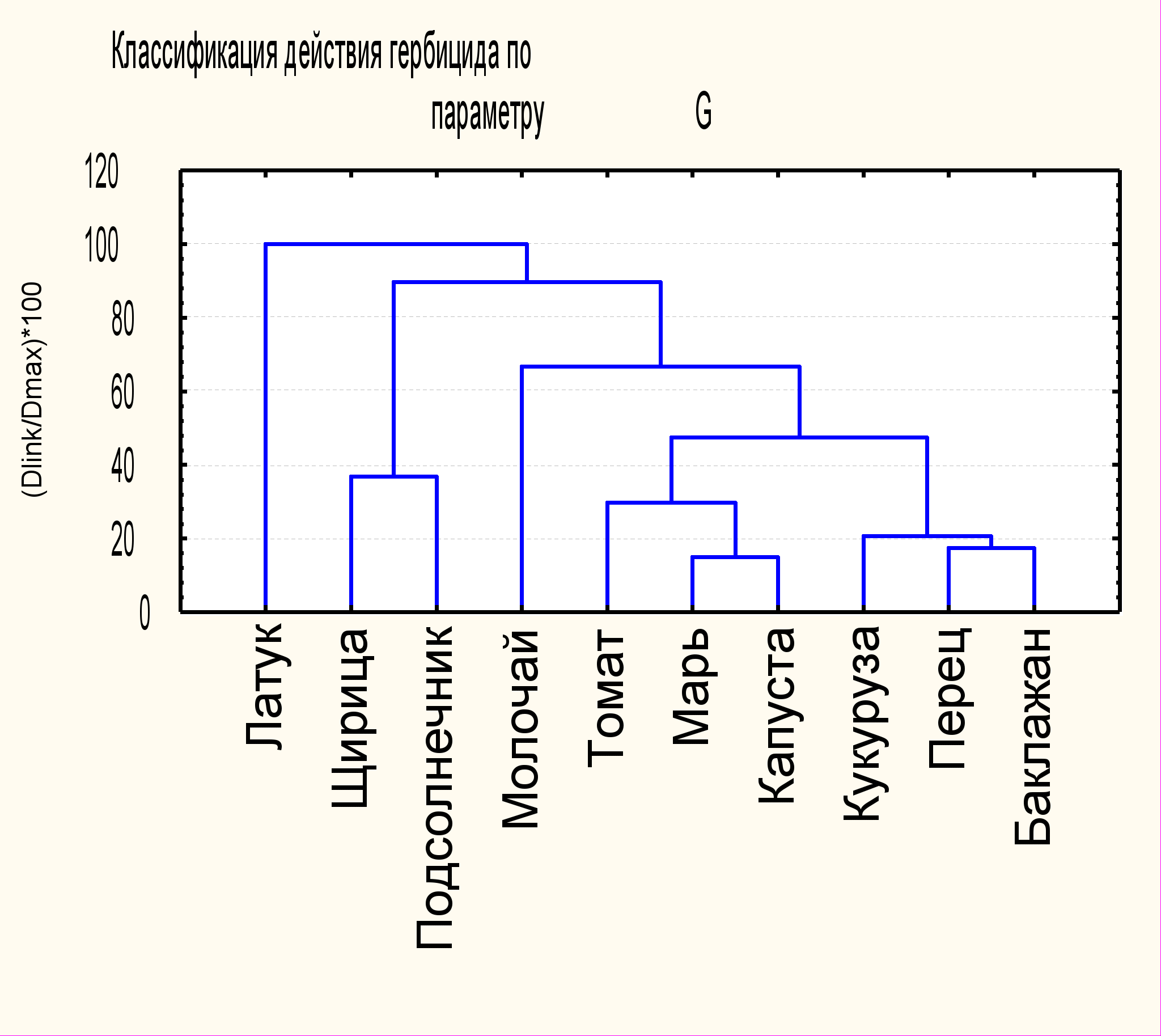
Рисунок 5. Дендрограмма растений по действию тяжелых металлов (а) и гербицида (раундап) (б) на параметры кинетики замедленной флуоресценции G.
Рассматривая параметры кинетики замедленной флуоресценции как величины, описывающие растения в пространстве состояний, можно классифицировать растения по действию на них факторов окружающей среды. На дендрограммах показаны примеры подобной классификации по параметрам замедленной флуоресценции. Объединение в кластер растений показывает на идентичность реакции фотосинтетического аппарата растений на внешнее воздействие. Как следует из результатов кластерного анализа можно выделить на уровне связи более 70% следующие кластеры:
по марганцу
(по параметру G): 1 кластер-подсолнечник; 2 кластер- капуста, перец, баклажан, кукуруза, томат;
(по параметру «а»): 1 кластер- перец, капуста; 2 кластер – подсолнечник, кукуруза, баклажан, томат. Аналогичная классификация проведена и по другим металлам.
Классифицируя растения по действию фосфорорганических гербицидов (раундап) и уровню связи более 70% можно отметить: (по параметру G) 1 кластер – латук; 2 кластер – щирица, подсолнечник; 3 кластер – молочай, томат, марь, капуста, кукуруза, перец, баклажан.
Рассматривая данную классификацию можно отметить, например, что подсолнечник и кукуруза одинаково реагируют на влияние большинства исследованных тяжелых металлов. Это может свидетельствовать об идентичности процессов, протекающих в этих растениях.
ГЛАВА 6. Исследование кинетики замедленной флуоресценции почв Оренбургской области. В главе рассмотрены методики и результаты исследования кинетики замедленной флуоресценции почвенных образцов при различных температурах. В последнее время, в почвоведении, развивается направление по разработке методов создания почв с заранее известными физико-химическими свойствами, а также методов их определения. Одним из таких методов является термический. В связи с этим, актуальным является изучение замедленной флуоресценции и химических свойств почв при термическом воздействии.
Для исследования замедленной флюоресценции отобраны следующие типы почв: черноземы (типичный и выщелоченный, южный, обыкновенный) и темно-каштановая почва. Отбор проб почв осуществлялся методом конверта по профилю (горизонта) А -0-20; АВ -20-40; ВС- 40-90 см. Из проб удаляются растительные остатки, производится механическое разрыхление, тщательное перемешивание и доведение до воздушно-сухого состояния. Пробы разделялись на контрольные (пробы почв, высушенные до воздушно-сухого состояния при температуре 20 ºС) и опытные группы.
Опытные пробы почв подвергались термической обработке при температурах 200°С, 400°С, 600°С и 800°С с выдержкой при каждой температуре в течение 30 минут и последующим охлаждением до комнатной температуры. Исследование контрольных и опытных групп проб производилось на установке для регистрации замедленной флуоресценции. Образец почвы помещали в светонепроницаемую камеру установки, выдерживали в темноте 5 мин., облучали световым импульсом мощностью 19 Вт длительностью 10 мс и регистрировали с помощью фотоэлектронного умножителя число импульсов замедленной флуоресценции. Экспериментально установлено, что для всех исследованных типов почв независимо от режимов температурного воздействия на них выполняется экспоненциальный закон затухания флуоресценции. Экспериментальные данные описывались уравнением регрессии экспоненциального вида (метод Левенберга-Макгравта). Характер изменения флуоресценции описывался экспоненциальной зависимостью вида

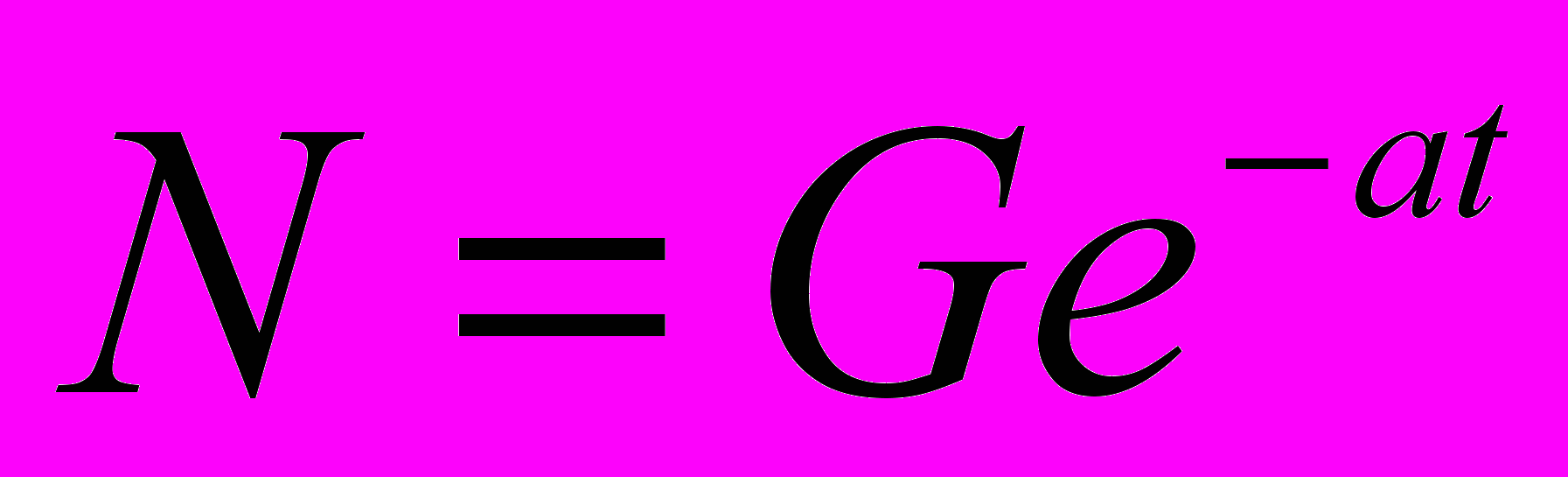 , где а - показатель экспоненты, характеризующий скорость затухания флуоресценции (постоянная быстрой компоненты); G- начальная интенсивность свечения (амплитуда быстрой компоненты). Параметры D и b при представлении кинетики затухания в виде суммы двух экспонент равны нулю и в дальнейшем рассматриваются только параметры быстрой компоненты. Контрольные и опытные группы почвы подвергались химическому анализу на содержание основных агрохимических показателей: определение лабильного органического вещества, гумуса, подвижных форм фосфора и калия, рН солевого, плотного остатка.
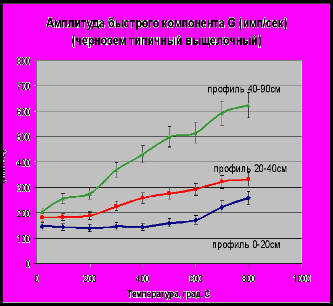
, где а - показатель экспоненты, характеризующий скорость затухания флуоресценции (постоянная быстрой компоненты); G- начальная интенсивность свечения (амплитуда быстрой компоненты). Параметры D и b при представлении кинетики затухания в виде суммы двух экспонент равны нулю и в дальнейшем рассматриваются только параметры быстрой компоненты. Контрольные и опытные группы почвы подвергались химическому анализу на содержание основных агрохимических показателей: определение лабильного органического вещества, гумуса, подвижных форм фосфора и калия, рН солевого, плотного остатка. Чернозем типичный выщелочный. Амплитуда быстрого компонента (G) возрастает с ростом температуры аналогично другим типам почв. Наиболее значительный рост интенсивности компонента отмечается у третьего слоя почв
при температуре 800С.
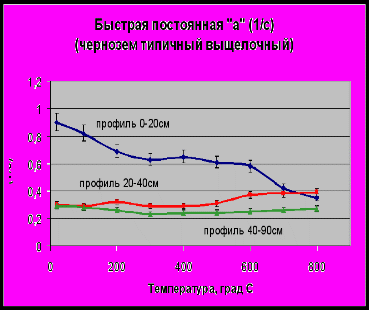
Постоянная быстрого компонента (а) характеризуется значительным снижением с ростом температуры (для первого слоя) прокаливания. Вместе с тем постоянная второго и третьего слоев практически не изменяется.
а б
Рисунок 6. Зависимость параметров ЗФ G (а) и а (б) чернозема типичного выщелочного от температуры прокаливания.
Постоянная а коррелирует с pH, гумусом, подвижным калием, ЛОВ (р0,2).
рН солевой. Значение рН не изменяется до температуры прокаливания 400C и увеличивается до величины 12 при температуре 800С для всех 3-х слоев почв. При этом ход зависимости рН коррелирует с гумусом, постоянной быстрой компоненты, ЛОВ, плотным остатком (р0,2).
Подвижные фосфор и калий. Содержание подвижных форм фосфора и калия достигает максимального значения при температуре прокаливания 400-600С для всех исследованных слоев почвы. При этом наибольшее увеличение
фосфора и калия происходит во втором слое почв (до 5 раз).
Чернозем южный. Амплитуда быстрой компоненты (G) для чернозема южного увеличивается с ростом температуры (для первого слоя). Для второго и третьего слоев динамика величины G носит немонотонный характер, при этом интенсивность амплитуды второго слоя почвы меньше амплитуды третьего слоя. Отмечена сильная корреляционная связь амплитуды и pH солевого плотного остатка, ЛОВ.
Постоянная быстрого компонента (а) увеличивается при температуре 200 0С (1 слой) и снижается при дальнейшем увеличении температуры прокаливания образцов почвы. Выявлены корреляции между величиной а и pH, гумусом, ЛОВ, подвижным фосфором (второй слой), калием (третий слой).
pH солевой увеличивается с ростом температуры для первого, второго, третьего слоев почвы, достигая максимального значения при температуре прокаливания почвы 8000С.
Подвижные фосфор и калий. Динамика подвижных форм фосфора и калия характеризуется значительным подъемом при температуре прокаливания почв 400-600 0С и дальнейшим снижением при температуре 8000С.
Аналогичный анализ проведен для чернозема обыкновенного и темно-каштановой почвы.
По данным термического анализа почв в интервале 200-400˚С происходит обезвоживание образца. Одновременно начинается частичное обугливание органических веществ почвы. В результате возрастает доля поглощенной световой энергии. При нагревании до 400˚С изменяется степень окисленности образца и частично разрушается органическое вещество. Одновременно происходит процесс окисления почвенного пигмента – соединений железа. Прокаливание при 600-800˚С сопровождается разрушением кристаллических решеток таких минералов, как каолинит и монтмориллонит, при этом увеличивается интенсивность свечения флуоресценции. Для всех типов и подтипов почв выявляется общая закономерность возрастания амплитуды быстрого компонента с ростом температуры прокаливания. Исследуемые почвы отличаются по показателям замедленной флуоресценции. Выявляется общая закономерность изменения замедленной флуоресценции в интервале температур прокаливания 400-6000С, выраженная в увеличении интенсивности свечения черноземов обыкновенного и южного, темно-каштановой почвы. Быстрая постоянная а исследуемых почв, выдержанных при различных температурах прокаливания уменьшается при температуре 8000С по сравнению с исходным состоянием образцов почвы (увеличивается длительность свечения); в интервале температур прокаливания 200-6000С быстрая постоянная, как правило, возрастает по сравнению с исходным состоянием образцов почв (длительность свечения уменьшается – происходит тушение флуоресценции). Содержание подвижных форм фосфора и калия увеличивается и достигает максимум при температурах 500-600С. Это явление связано, по всей видимости, с тем, что при такой температуре происходит сублимация фосфора и калия. При температуре 800С снижение содержания фосфора и калия связано с испарением этих элементов из почвы.
ГЛАВА 7. Системное моделирование как основной метод представления природных систем. В главе получены математические зависимости параметров кинетики замедленной флуоресценции (G) и (а) растений от физико-химических свойств почв на основании применения алгоритмов метода группового учета аргументов (МГУА).
Алгоритмы, реализующие МГУА, воспроизводят схему массовой селекции. В них есть генераторы усложняющихся из ряда в ряд комбинаций и пороговые самоотборы лучших из них. Так называемое полное описание объекта
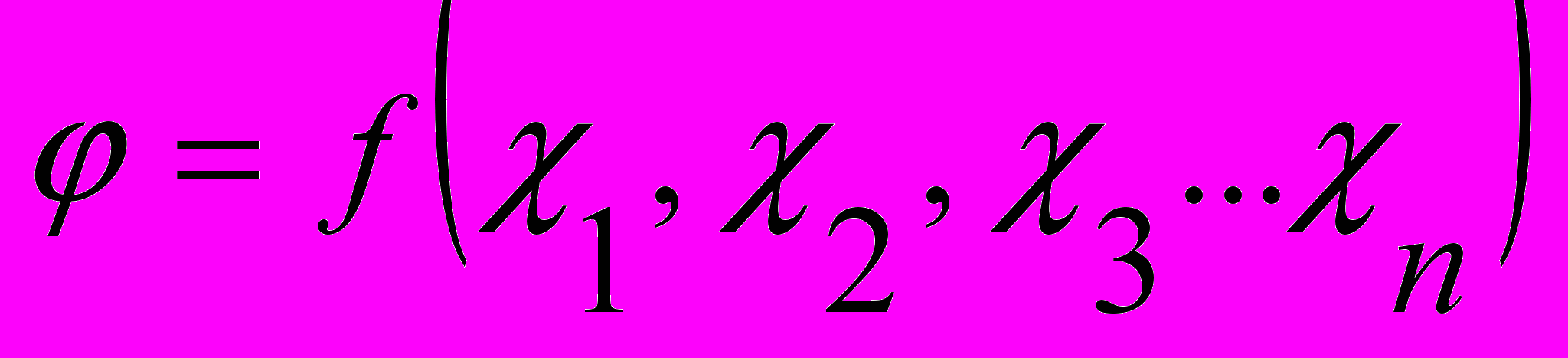
заменяется несколькими рядами частных описаний:
Ряды селекции наращиваются до тех пор, пока критерий несмещенности решений падает
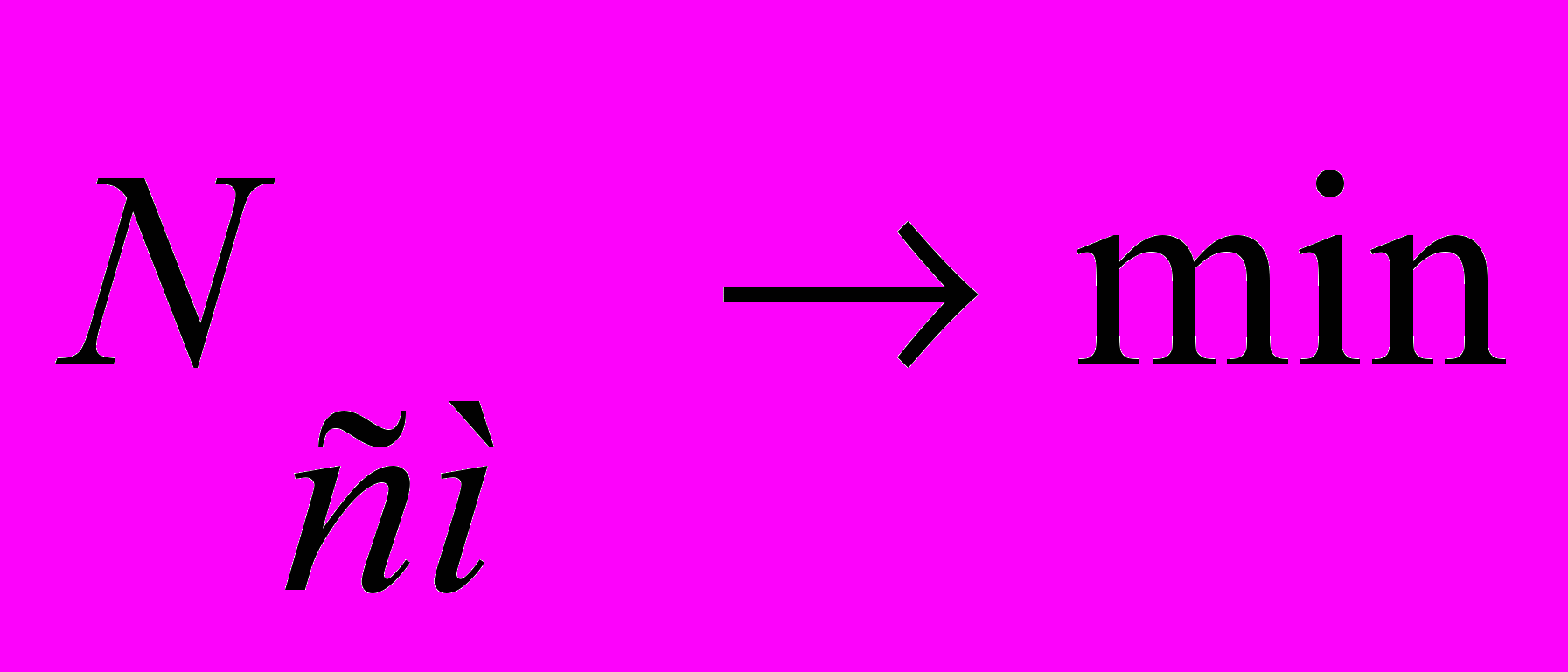 . Нулевое значение оценки несмещенности достигается только при отсутствии помех в исходных данных и при решении задачи открытия законов и идентификации. На основании рассмотренного алгоритма разработана программа, реализующая метод группового учета аргумента.
. Нулевое значение оценки несмещенности достигается только при отсутствии помех в исходных данных и при решении задачи открытия законов и идентификации. На основании рассмотренного алгоритма разработана программа, реализующая метод группового учета аргумента. 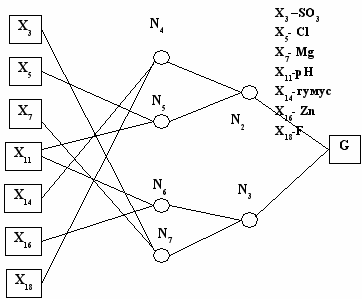
Рисунок 7. Регрессионная зависимость параметра G замедленной флуоресценции листьев томата от химических свойств почв (по методу МГУА)
Учитывая, что почвенные факторы влияют на фотосинтетический аппарат растений, представляет значительный интерес моделирование влияния факторов почвенной среды на растения. Для определения исходных данных для моделирования растения выращивались на почвах с различными химическими показателями. Экспериментально определялись параметры кинетики замедленной флуоресценции растений (быстрая компонента (G) и быстрая постоянная (а)) и химические показатели почвы (Xi). Почвенные показатели принимались в качестве независимых параметров. Параметры кинетики флуоресценции (G и а) - в качестве зависимых от Xi величин. На рисунке 7 приведены результаты регрессионного анализа по методу МГУА для томата. Отмечены факторы влияющие на параметры ЗФ томата, это- сульфаты, хлориды, рН, ионы магния, цинка, фтор, гумус. Полученные результаты позволяют по заданным химическим свойствам почв, прогнозировать состояние фотосинтетического аппарата растений и соответственно урожайность посевов.
ГЛАВА 8. Моделирование процессов миграции тяжелых металлов в почвенно-растительных системах. В главе рассмотрены вопросы моделирования систем почва-растение. Теоретически получена линейная зависимость содержания тяжелых металлов в растениях и почве при стационарных процессах миграции. На основании вероятностного моделирования и применения теории стационарных марковских цепей получены зависимости для оценки риска загрязнения почвенно-растительных систем, получен и проанализирован комплексный коэффициент, характеризующий миграционные способности почвенно-растительных систем и проведена их классификация.
В процессе взаимодействия компонентов системы почва - корневая система - надземная часть растений друг с другом происходит перенос материи и энергии. Определим начальные условия следующим образом: 1) в начальный момент времени в систему (например, через атмосферу) введена С0 концентрация загрязняющего вещества; 2) между компонентами системы существует обмен веществом с различными интенсивностями: λ1 - интенсивность перехода вещества из почвы в корневую систему; λ2 - интенсивность перехода вещества из корневой системы в надземную часть растения; λ3 - интенсивность перехода вещества из надземной части растения в почву.
Будем характеризовать состояние системы вероятностями Р нахождения загрязняющего вещества в составных частях системы: Рп – вероятность нахождения загрязнителя в почве, Рк – вероятность нахождения загрязнителя в корневой системе растений, Рн – вероятность нахождения загрязнителя в надземной части растений. Сформулируем задачу следующим образом: определить концентрацию загрязняющего вещества, установившуюся в каждом из компонентов системы при условии стационарности интенсивностей перехода загрязняющего вещества из одного компонента в другой, при стремлении времени наблюдения в бесконечность.
Получим для Рп:
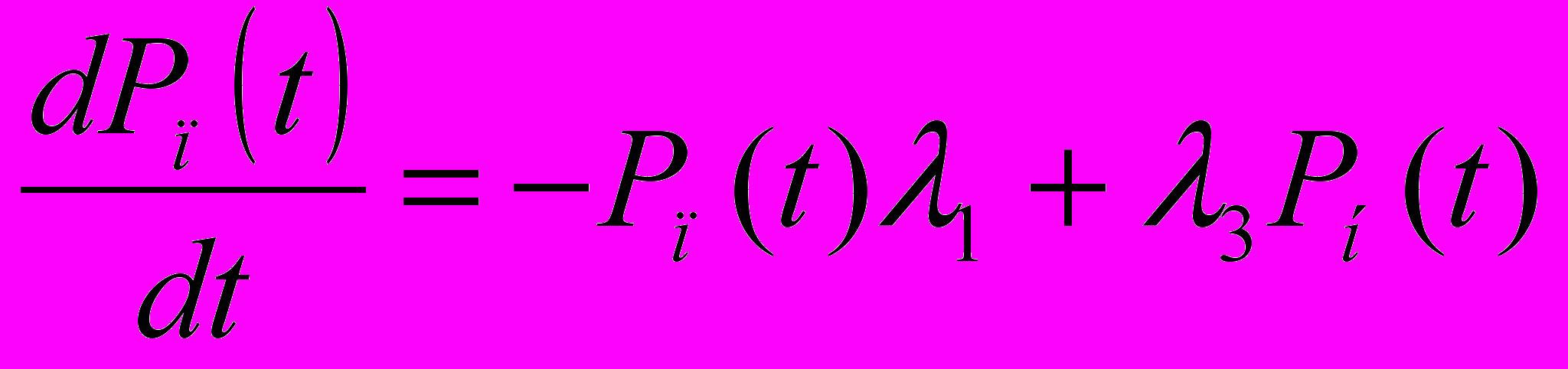 (5)
(5)Аналогично, для состояний систем Рк(t) и Рн(t) запишем уравнения
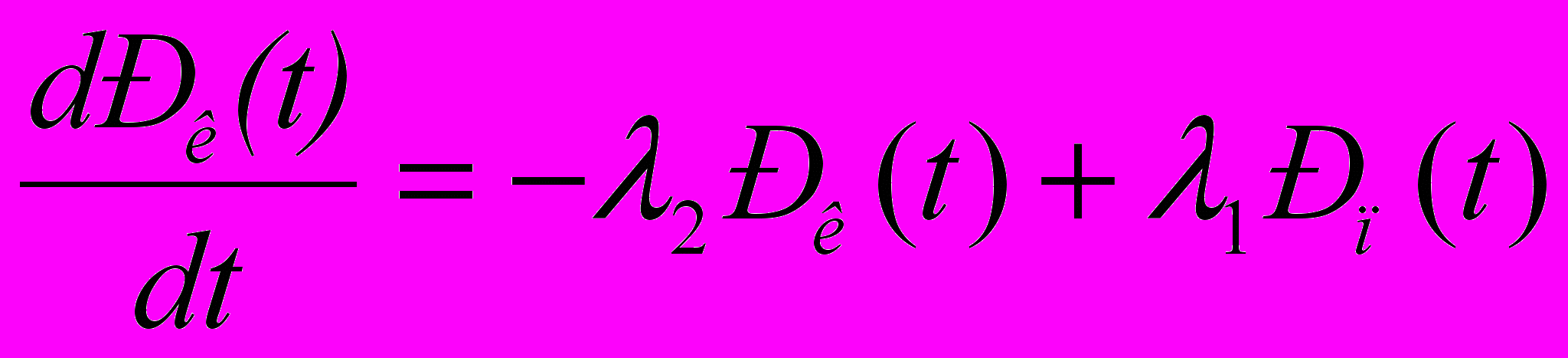 (6)
(6)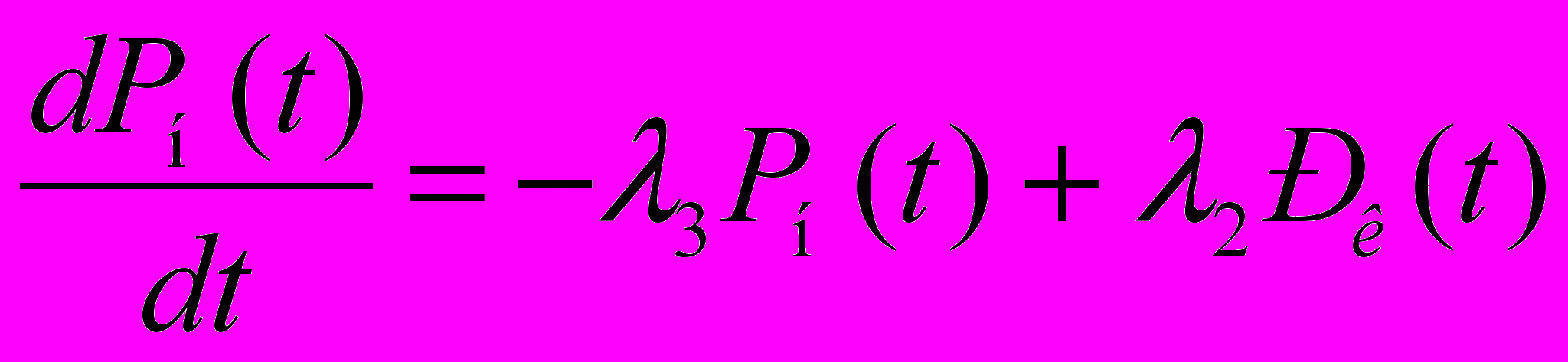 (7)
(7)Совокупность уравнений 5, 6, 7 образуют систему уравнений Колмогорова, в котором в качестве неизвестных величин фигурируют вероятности Рп, Рк, Рн. Как отмечалось выше, их можно интерпретировать как вероятности нахождения загрязняющих веществ в корневой системе, надземной части растений, почве. За перенос загрязнения из одной среды в другую отвечает различные процессы, такие как диффузия, сорбция, сухое, влажное осаждение и т.д. С течением времени, т.е. при t → ∞ в компонентах системы устанавливаются концентрации загрязняющих веществ в соответствии с финальными вероятностями Рп, Рк, Рн. После ряда преобразований, переходя от вероятностей к концентрациям получим:
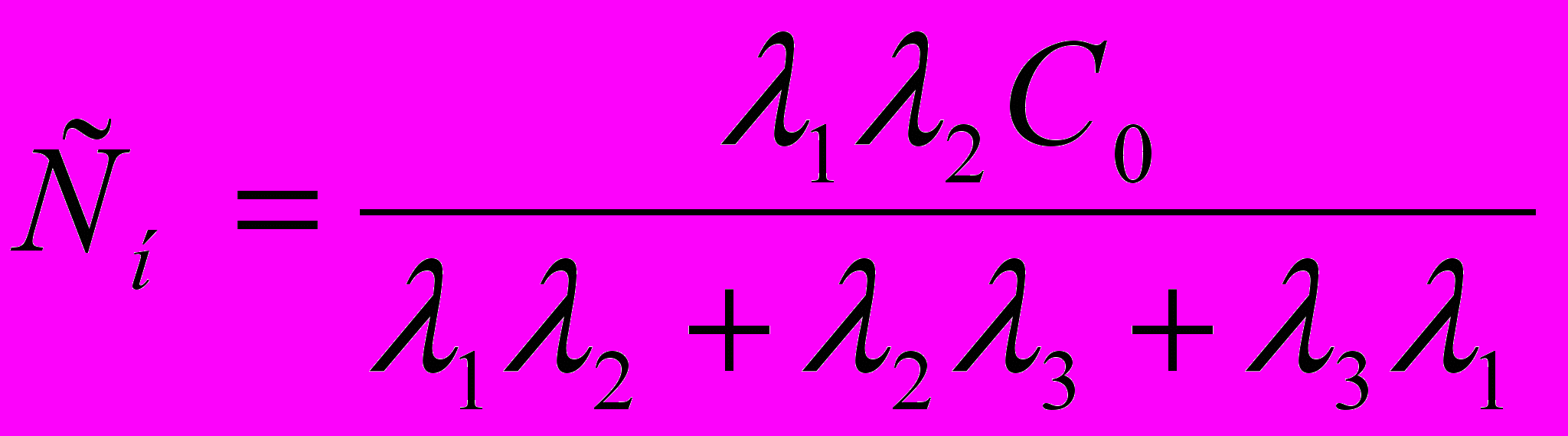 ;
;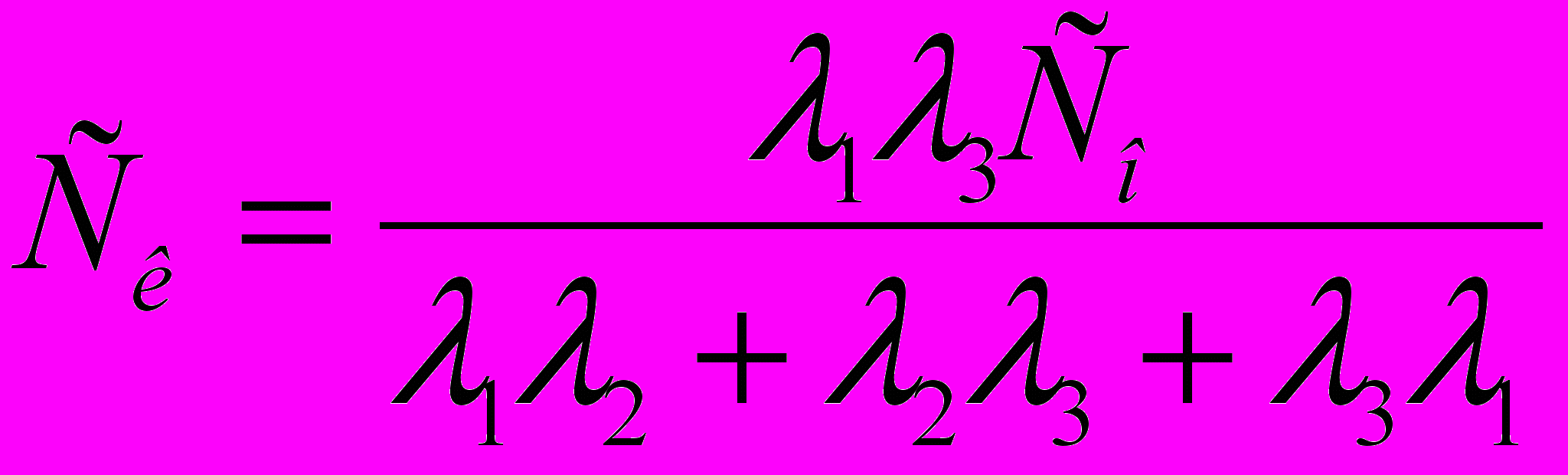 ;
;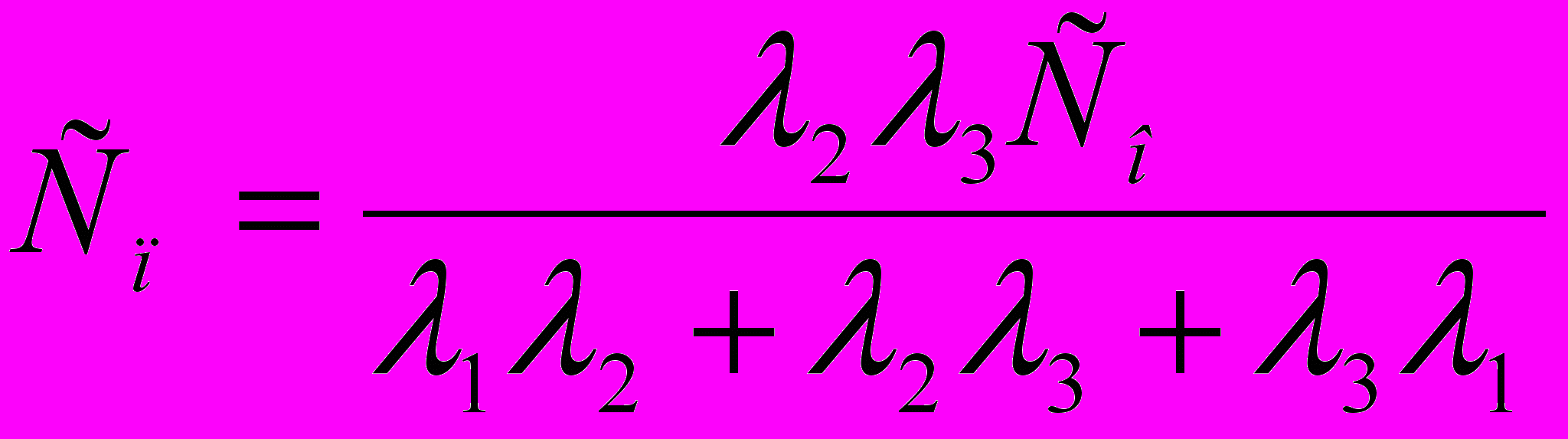 . (8)
. (8) Полученные соотношения позволяют по известным интенсивностям переходов веществ в системе почва-растение определять преимущественное распределение веществ в подсистемах. Следует отметить, что интенсивности переходов определяются свойствами почв и растений.
Для интегральной оценки почвенно-растительных комплексов предложен показатель, учитывающий физико-химические свойства почв и растений. В качестве такого критерия выбран знаменатель в уравнениях (8).
Расчет интенсивностей переходов, характеризующий соотношение между содержаниями изучаемого химического элемента в растениях и в почве, показал, что интенсивность поглощения микроэлементов зависит от разновидностей растений. В результате теоретического моделирования процессов взаимодействия в системе почва-растение ранее были предложены системы уравнений для оценки риска загрязнения компонентов системы:
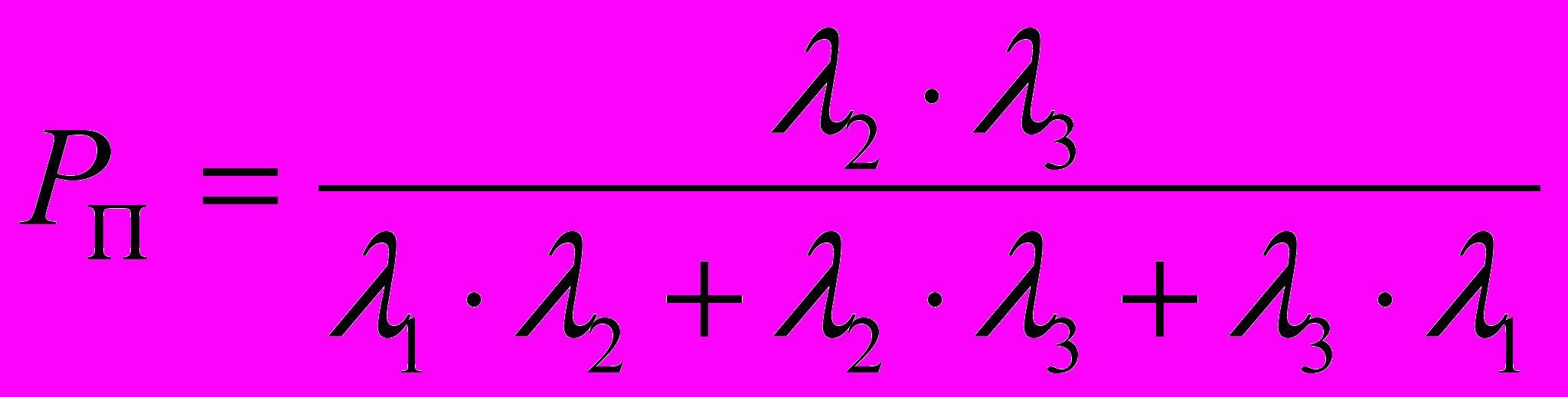 ;
; 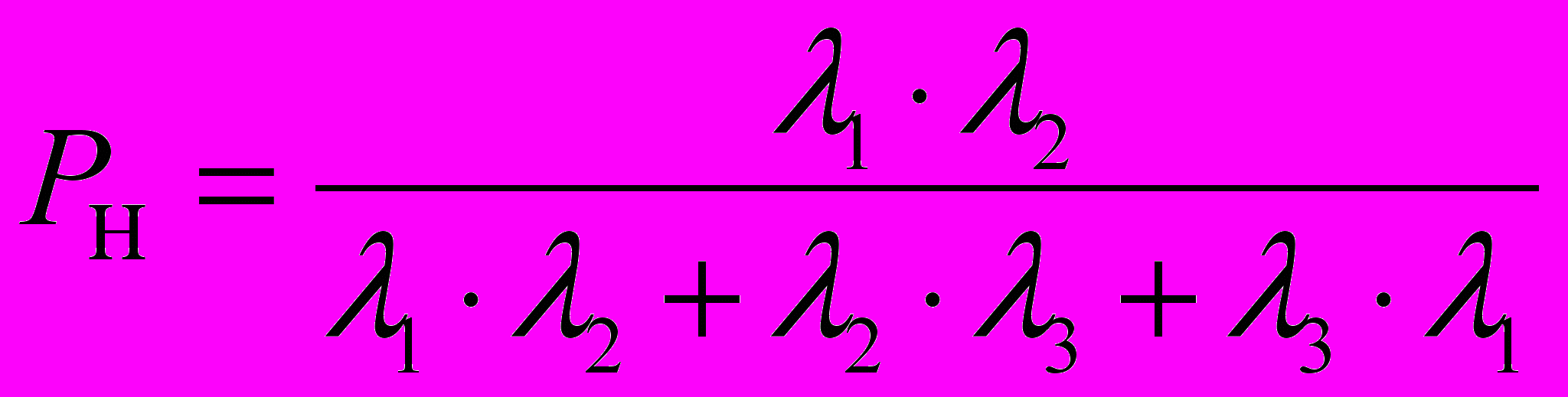 ;
; 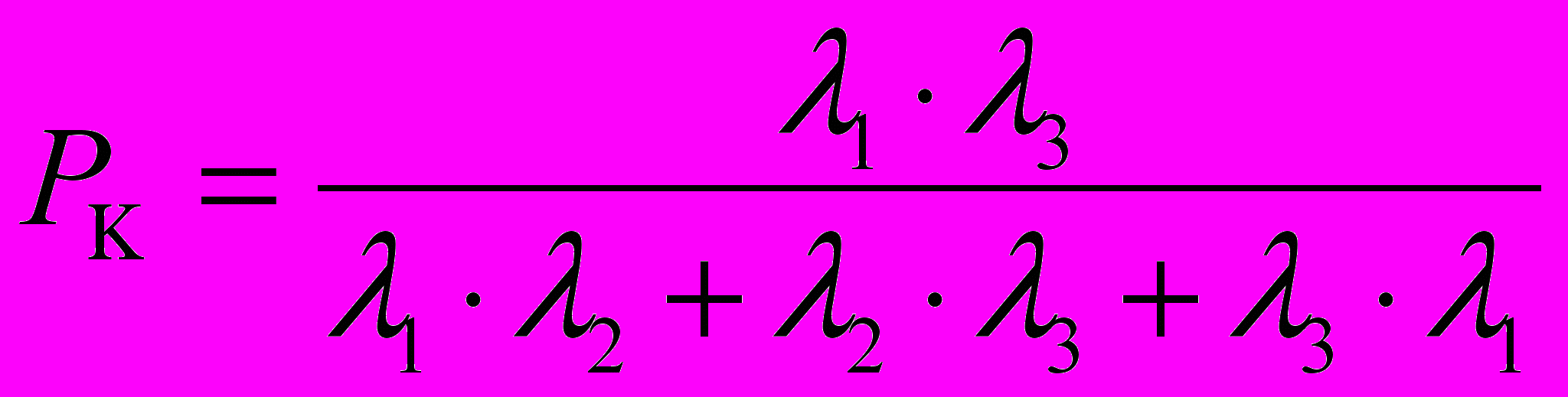
Результаты расчет риска загрязнения компонентов системы почва-растение представлены в таблицах 1, 2, 3 (фрагменты). Наибольший риск загрязнения медью надземной части растений наблюдается у татарника – 0,21 (почва темно-каштановая неполноразвитая), на других типах почв риск загрязнения татарника медью на порядок ниже. Минимальное значение риска загрязнения медью наблюдается у шалфея (чернозем южный), тысячелистника (чернозем типичный) и солодки (чернозем обыкновенный). Максимальное значение риска загрязнения цинком у полыни обыкновенной- 0,07 (чернозем обыкновенный), на других типах почв риск загрязнения ниже в 7 раз. Риск загрязнения цинком клевера лугового на всех исследуемых типах почв практически равен 0.
Таблица 1. Риск загрязнения надземной части растений тяжелыми металлами (фрагмент)
| почва | растения | Cu | Zn | Pb | Ni | Cr | V | Ti | Mo | Ag | Ga | Ba | Zr | Mn |
| черно-зем южный | шалфей | 0,01 | 0,01 | 0,0006 | 0,002 | 0,00015 | 0,00018 | 0,00005 | 0,03 | 0,0011 | 0,0009 | 0,0009 | 0 | 0,002 |
| татарник | 0,05 | 0,01 | 0,003 | 0,005 | 0,00011 | 0,00013 | 0,00005 | 0,04 | 0,0148 | 0,001 | 0,001 | 0 | 0,004 | |
| цикорий | 0,04 | 0,02 | 0,07 | 0,016 | 0,017 | 0,0019 | 0,00077 | 0,11 | 0,4068 | 0,003 | 0,001 | 0 | 0,0002 | |
| полынь обыкновенная | 0,03 | 0,01 | 0,004 | 0,008 | 0,0072 | 0,0006 | 0,00004 | 0,02 | 0,0931 | 0,0008 | 0,0007 | 0 | 0,005 | |
| тысячелистник | 0,02 | 0,01 | 0,003 | 0,004 | 0,00019 | 0,001 | 0,00007 | 0,03 | 0,3723 | 0,0006 | 0,001 | 0 | 0,0005 | |
| одуванчик | 0,03 | 0,01 | 0,008 | 0,006 | 0,00009 | 0,0009 | 0,00005 | 0,05 | 0,0447 | 0,001 | 0,0009 | 0 | 0,0006 | |
| клевер луговой | 0,03 | 0 | 0,001 | 0,004 | 0,00018 | 0,0005 | 0,00011 | 0,65 | 0,0107 | 0,0003 | 0,0005 | 0 | 0,001 | |
| солодка | 0,02 | 0 | 0,001 | 0,005 | 0,00008 | 0,00009 | 0,00002 | 0,1 | 0,015 | 0,0006 | 0,0004 | 0 | 0,002 |
подчеркнуто минимальное значение риска загрязнения,
Риск загрязнения свинцом максимален у тысячелистника – 0,033 (почва темно-каштановая неполноразвитая), на других типах почв – на порядок ниже. Наибольший риск загрязнения молибденом наблюдается у клевера лугового на всех исследуемых типах почв.
Максимальное и минимальное значения риска загрязнения барием наблюдается у солодки на разных типах почв (чернозем типичный и южный).
Анализ риска загрязнения корневой системы растений (таблица 2) показал, что наибольший риск загрязнения медью наблюдается у шалфея – 0,94 (чернозем южный). По данным результатам анализа видно, что основная масса меди из почве аккумулируется в корневой системой растений. Максимальное и минимальное значения риска загрязнения цинком наблюдается у цикория – 0,63 (чернозем обыкновенный) и 0,06 (чернозем типичный). Риск загрязнения свинцом наиболее высок у солодки 0,69 (чернозем типичный), на других типах почв риск загрязнения солодки снижается в 2 раза.
Таблица 2. Риск загрязнения корневой системы растений тяжелыми металлами (фрагмент)
| почва | растения | Cu | Zn | Pb | Ni | Cr | V | Ti | Mo | Ag | Ga | Ba | Zr | Mn |
| чернозем южный | шалфей | 0,94 | 0,45 | 0,33 | 0,37 | 0,7549 | 0,26 | 0,05 | 0,78 | 0,99 | 0,25 | 0,31 | 0,09 | 0,12 |
| татарник | 0,59 | 0,19 | 0,17 | 0,26 | 0,8404 | 0,57 | 0,59 | 0,89 | 0,72 | 0,21 | 0,47 | 0,25 | 0,05 | |
| цикорий | 0,46 | 0,46 | 0,11 | 0,11 | 0,3001 | 0,07 | 0,07 | 0,54 | 0,34 | 0,08 | 0,33 | 0,08 | 0,32 | |
| полынь обыкновенная | 0,79 | 0,23 | 0,47 | 0,47 | 0,3994 | 0,75 | 0,42 | 0,93 | 0,32 | 0,57 | 0,45 | 0,22 | 0,11 | |
| Тысячелистник | 0,69 | 0,29 | 0,29 | 0,33 | 0,8317 | 0,54 | 0,27 | 0,65 | 0,38 | 0,36 | 0,34 | 0,11 | 0,16 | |
| Одуванчик | 0,81 | 0,53 | 0,36 | 0,24 | 0,9042 | 0,41 | 0,40 | 0,65 | 0,49 | 0,36 | 0,64 | 0,11 | 0,11 | |
| клевер луговой | 0,67 | 0,14 | 0,34 | 0,11 | 0,6517 | 0,27 | 0,10 | 0,20 | 0,91 | 0,31 | 0,19 | 0,09 | 0,05 | |
| Солодка | 0,55 | 0,11 | 0,30 | 0,51 | 0,8385 | 0,72 | 0,32 | 0,89 | 0,48 | 0,22 | 0,23 | 0,15 | 0,17 |
подчеркнуто минимальное значение риска загрязнения,
Риск загрязнения корневой системы растений хромом, ванадием, титаном имеет большой разброс, так: по хрому – 0,01-0,91;по ванадию – 0,005-0,76;по титану – 0,007-0,59. Значения риска загрязнения почвы представлены в таблице 3. Разброс в значениях риска загрязнения можно объяснить влиянием почвенных факторов, характерных для каждого типа почв. Максимальное значение риска загрязнения молибденом наблюдается у полыни обыкновенной 0,94 (чернозем южный).
