Особенности фазовых состояний сегнетоэлектрических baTiO 3, knbO 3 и твердых растворов ba(Ti 1-х Мn Х )O 3 при разных условиях их приготовления 01. 04. 07 физика конденсированного состояния
| Вид материала | Автореферат |
| Второй синтез |
- Учебно-методический комплекс по дисциплине Физика Конденсированного Состояния Для специальности, 322.8kb.
- Паспорт специальности 01. 04. 07 – физика конденсированного состояния, 1004.81kb.
- Влияние электромагнитных полей на фазовый состав и структуру жидко-твердых сплавов, 820.51kb.
- Рабочая программа учебной дисциплины «Физика конденсированного состояния, термодинамика,, 223.9kb.
- Фазы, фазовые состояния и морфотропные области в n компонентных системах сегнетоэлектрических, 528.08kb.
- Ён Викторович Методы визуализации кинетики зарождения и роста углеродных наноструктур, 219.01kb.
- Министерство образования Российской Федерации международный университет природы, общества, 1374.95kb.
- Кинетика старения медно-бериллиевых сплавов в постоянном магнитном поле 01. 04., 427.06kb.
- Рабочая программа дисциплины «нелинейные уравнения математической физики» Рекомендовано, 163.22kb.
- Эволюция структурно-фазовых состояний при термомеханическом упрочнении балочного профиля, 23.3kb.
В разделе 2.1 анализируются перовскитовые и гексагональные фазы в системе Ва(Тi1-хМnх)О3.
Среди двойных оксидов с общей формулой АВО3 выделяется соединение ВаМnО3, которое кристаллизуется в ряде гексагональных фаз с различными вариантами чередования (с) и (h) слоев упаковки вдоль оси z.
Одной из задач работы являлось приготовление гексагонального BaMnO3 и твердых растворов Ва(Тi1-хМnх)О3 с изучением возможных эффектов изменений структуры при режимах низкотемпературного синтеза. Исходные составы были получены из смесей α-титановой кислоты и нитрата марганца. После отжига гель-смеси BaMnO3 при температуре Т= 500 оС в течение двух часов рентгенографически была обнаружена гексагональная фаза, аналогичная фазе гексагонального BaТiO3, с параметрами ячейки аh = 5.738 Å, сh = 14.022 Å.
При данных условиях синтеза (500 оС, 2 часа) при приготовлении составов системы Ва(Тi1-хМnх)О3 (0.1 ≤ х ≤ 0.9) все образцы имели структуру перовскитового типа. Полученные структуры составов Ва(Тi1-хМnх)О3 характеризуются как нанокристаллические, об этом свидетельствуют относительно большие величины параметров ячеек и полуширины основных дифракционных отражений (табл.6, рис.4).
При малых концентрациях Мn (от 0.1 ≤ х ≤ 0.4) при комнатной температуре реализуется тетрагональная фаза, а в составах 0.5 ≤ х ≤ 0.9 – кубическая.
Отжиг при Т = 600 оС (в течение двух часов) составов системы Ва(Тi1-хМnх)О3, привел к образованию гексагональной фазы во всех составах системы (табл.7), кроме чистого ВаТiО3.
Таким образом, низкотемпературный синтез (при 500 оС) титаната бария и его твердых растворов приводит к образованию наноразмерной перовскитовой фазы с увеличенным объемом ячейки и пониженной спонтанной деформацией (с/а-1). По мере развития процесса кристаллизации с увеличением размера кристаллитов в результате отжига при Т = 600 оС образуется гексагональная фаза титаната бария с более плотной структурой . На рис.4 показаны изменения полуширин дифракционных отражений типа 110 от х в перовскитовой и гексагональной фазах.
В разделе 2.2 описаны фазовые состояния составов системы ВаТi1-хSnхО3. Образцы получали по гель-технологии из растворов титановой и оловянной кислот, взятых в эквивалентных отношениях, с отжигом Тотж=500 0С в течение 2 часов.
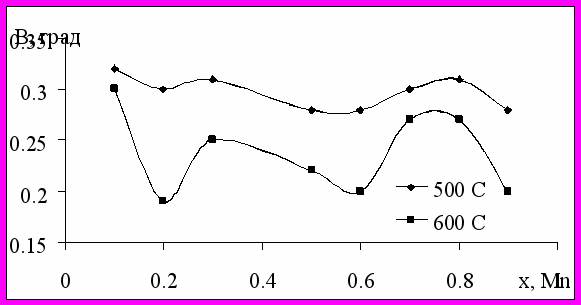 | | ||||||||||
| Рисунок 4. Полуширины отражений 110 ВаМn1-хТiхО3 (10 ≤ х ≤ 90 %), отожженных при температуре 500 и 600 оС. | | ||||||||||
| Таблица 6. Параметры ячеек, величины спонтанной деформации, объемы ячеек, средние длины связей В-О составов системы Ва(Тi1-хМnх)О3, при 500 оС | | ||||||||||
| х, Мn | а, Å | с, Å | с/a-1 | V, Å3 | L(В-О), Å | | |||||
| 0 | 4.058 | --- | 0 | 66.82 | 2.029 | | |||||
| 0.1 | 4.064 | 4.106 | 0.010 | 67.81 | 2.039 | | |||||
| 0.2 | 4.081 | 4.107 | 0.006 | 68.40 | 2.045 | | |||||
| 0.3 | 4.082 | 4.098 | 0.004 | 68.28 | 2.044 | | |||||
| 0.5 | 4.078 | 4.088 | 0.002 | 67.98 | 2.041 | | |||||
| 0.6 | 4.080 | --- | 0 | 67.92 | 2.040 | | |||||
| 0.7 | 4.084 | --- | 0 | 68.12 | 2.042 | | |||||
| 0.8 | 4.078 | --- | 0 | 67.82 | 2.034 | | |||||
| 0.9 | 4.086 | --- | 0 | 68.22 | 2.043 | | |||||
| Таблица 7. Структурные параметры Ва(Тi1-хМnх)О3, отожженного при 600 оС | |||||||||||
| х, Мn | аh, Å | сh, Å | VАВО3, Å3 | h, Å | |||||||
| 0*) | 5.738 | 14.022 | 66.63 | 2.337 | |||||||
| 0.1 | 5.743 | 14.058 | 66.92 | 2.343 | |||||||
| 0.2 | 5.733 | 14.029 | 65.55 | 2.338 | |||||||
| 0.3 | 5.739 | 14.034 | 66.710 | 2.339 | |||||||
| 0.4 | 5.749 | 14.108 | 67.295 | 2.351 | |||||||
| 0.5 | 5.750 | 14.109 | 67.323 | 2.352 | |||||||
| 0.6 | 5.761 | 14.102 | 67.548 | 2.350 | |||||||
| 0.7 | 5.784 | 14.107 | 68.113 | 2.351 | |||||||
| 0.8 | 5.783 | 14.156 | 68.325 | 2.359 | |||||||
| 0.9 | 5.783 | 14.232 | 68.692 | 2.372 | |||||||
| 1 | 5.783 | 14.072 | 67.322 | 2.346 | |||||||
| *) Для х=0 приведены параметры для (h)- ВаТiО3, приготовленного закалкой от 1460 оС. | |||||||||||
В составах с 0.1 х 0.6 при комнатной температуре наблюдается тетрагональная фаза с увеличенными (относительно (Т) – BaTiO3) параметрами решетки. При увеличении концентрации атомов Sn уменьшается спонтанная деформация ячейки (с/а-1). Характер зависимости (с/а-1) от х в данной системе твердых растворов выявил max (с/а-1) для состава с х = 0.3.
В третьей главе приведены результаты исследований синтеза KNbO3 и изменений его структуры при фазовых переходах.
В разделе 3.1 анализируются условия образования и основные характеристики KNbO3, многочисленные результаты исследований структуры и физических свойств ниобата калия.
В разделе 3.2 приведены результаты изучения особенностей синтеза KNbO3.
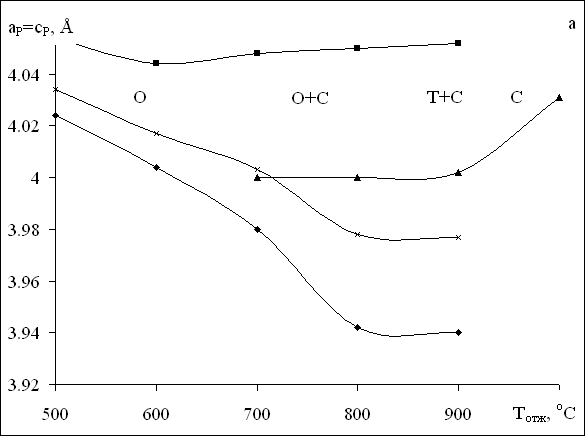
При первом синтезе KNbO3 приготовленный порошок из смеси K2СO3 и Nb2O5 (образец № 1) последовательно отжигался при температурах 300 ≤ Тотж ≤ 1000 оС в течение одного часа. После каждого отжига проводилось рентгенографическое исследование образца. Результаты исследования представлены в табл.8 и на рис.5. Отжиг при температуре Тсин = 300 и 400 оС не приводит к образованию перовскитовых фаз KNbO3, а при температуре 500 и 600 оС в течение 1 часа приводит к образованию (при комнатной температуре) орторомбической фазы KNbO3.
В результате отжига при Тотж = 700 оС образовалось 16% второй фазы KNbO3 – кубической, которая зафиксирована одновременно с орторомбической. Дальнейшее повышение температуры отжига привело к увеличению концентрации второй (кубической) фазы. После отжига при 900 оС при комнатной температуре наблюдаются тетрагональная и кубическая фазы. В результате последнего отжига при температуре 1000 оС зафиксирована одна кубическая фаза с параметром а2 = 4.031 Å. Увеличение параметра а2 может свидетельствовать о процессах разложения (размельчения) кристаллитов при высоких температурах отжига.
Уширение дифракционного максимума 200 после отжига при температуре 1000 оС также свидетельствует об уменьшении областей когерентного рассеяния.
Второй синтез KNbO3. Твердофазный синтез KNbO3 был проведен повторно из смеси K2СO3 и Nb2O5 (образец № 2) при температурах отжига от 600 ≤ Тотж ≤ 900 оС. Он также привел к образованию орторомбической фазы при комнатной температуре после отжига при 600 ≤ Тотж ≤ 800 оС. Отжиг KNbO3 при 900 оС привел к образованию тетрагональной фазы при комнатной температуре.
Для контроля процесса твердофазного синтеза KNbO3 нами был проведен следующий эксперимент. Стехиометрическую смесь нагревали в температурной камере на дифрактометре. Температура в камере постепенно повышалась, начиная от комнатной до 900 оС. Результаты температурных изменений структурных параметров образовавшегося KNbO3 в режиме нагрева представлены в табл.9.
| Таблица 8. Структурные параметры KNbO3 (образец № 1) при нормальных условиях, синтезированного при разных температурах | |||||||
| Тсин, оС | 500 | 600 | 700 | 800 | 900 | 1000 | |
| Структурные параметры | |||||||
| Фаза | Орторомбическая | орт+куби-ческая | орт+ куби-ческая | Тетра-гональная+ куби-ческая | куби-ческая | ||
| Параметры ячейки, Å | Ао*)=4.024 Во*)=5.690 Со*)=5.714 | Ао*)=4.004 Во*)=5.690 Со*)=5.710 | Ао*)=3.980 Во*)=5.694 Со*)=5.718 аС=4.000 | Ао*)=3.942 Во*)=5.690 Со*)=5.720 аС=4.000 | аТ=3.940 сТ=4.052 аС=4.002 | аС=4.031 | |
| Параметры приведенной (перовскитовой) ячейки | аР=сР=4.054 bР=4.024 βР=90.24о | аР=сР=4.044 bР=4.004 βР=90.20о | аР=сР=4.048 bР=3.980 βР=90.24о | аР=сР=4.050 bР=3.942 βР=90.30о | | | |
| Объем приведенной ячейки, Å3 | VО=66.13 | VО=65.48 | VО=65.00 VС=64.00 | VО=64.66 VС=64.00 | VТ=62.90 VС=64.10 | VС=65.50 | |
| %, фаза 1 | 100 | 100 | 84 | 48 | 23 | 0 | |
| %, фаза 2 | 0 | 0 | 16 | 52 | 77 | 100 | |
| RP, % | 6.15 | 5.42 | 4.9 | 5.13 | 4.81 | 5.89 | |
| В022, град | 0.89 | 0.42 | 0.38 | 0.37 | 0.26 | --- | |
| В200, град | 0.45 | 0.34 | 0.3 | 0.36 | 0.36 | --- | |
| В200, , о С-фаза | --- | --- | 0.26 | 0.27 | 0.24 | 0.67 | |
| *) Ао= bР, Во= аР+сР, Со= аР - сР; RP, % - фактор недостоверности | |||||||
  аP=сР, Å  
bP, Å 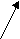 аС, Å   | |
| Рисунок 5. Зависимости параметров ячеек KNbO3 от температур отжига |
При всех температурах синтеза KNbO3 на рентгенограммах четко фиксируются дифракционные отражения, соответствующие двум кубическим фазам (ΙС и ΙΙС) с параметрами а1 и а2. Образовавшаяся фаза ΙС имеет меньшие параметры ячейки по сравнению с фазой ΙΙС и характеризуется большими полуширинами отражений 110 и 200.
| Таблица 9. Структурные параметры KNbO3 (образец № 5), при температурах синтеза | ||||
| Тсин, оС | 600 | 700 | 800 | 900 |
| а1, Å | 3.9705 | 3.9774 | 3.9816 | 3.9903 |
| С1, % | 51 | 55 | 57 | 63 |
| В110 (а1), град | 0.47 | 0.35 | 0.34 | 0.32 |
| В200 (а1), град | 0.5 | 0.48 | 0.46 | 0.4 |
| а2, Å | 4.0271 | 4.0193 | 4.0187 | 4.0229 |
| С2, % | 49 | 45 | 43 | 37 |
| В110 (а2), град | 0.27 | 0.26 | 0.26 | 0.25 |
| В200 (а2), град | 0.25 | 0.3 | 0.28 | 0.28 |
| RР, % | 7.80 | 6.16 | 6.35 | 7.04 |
Нами изучены зависимости структурных параметров KNbO3 от времени синтеза при температурах 550 и 600 оС. Кубическая фаза с параметром а = 4.046 Å образуется за время τ = 10 минут. При дальнейшей выдержке этот параметр ячейки не изменяется при данной температуре в течение двух часов.
После охлаждения до комнатной температуры эта фаза оставалась кубической с параметром решетки а = 4.046 Å. Затем этот же образец был нагрет до 600 оС и последовательная съемка рентгенограмм показала, что через 10 минут после установления температуры 600 оС фиксируются две кубические фазы с параметрами а1 и а2, которые в зависимости от времени отжига при этой температуре изменяются нелинейно. Первые 30 минут наблюдается увеличение параметров решетки, с течением времени значение этих параметров уменьшаются и сближаются (табл.10).
-
Таблица 10. Временная зависимость структурных параметров KNbO3 при 600 0С в камере (№ 7)
τ, мин
%, фаза (а2)
%, фаза (а1)
а1, Å
а2, Å
15
36
64
4.0334
3.9869
30
25
75
4.052
4.0401
45
22
78
4.000
3.989
60
14
86
3.997
3.96
90
3
97
3.993
3.979
В разделе 3.3 приведены результаты изучения изменений структуры KNbO3 в интервале температур 20≤ Т ≤ 900 оС.
В части 3.3.1 рассматриваются различные модели KNbO3 как сегнетоэлектрика типа смещения или типа порядка/беспорядка.
В части 3.3.2 рассматривается возможность установления рентгеновскими дифракционными методами истинной модели для кубической, тетрагональной и орторомбической фаз KNbO3. Для этого проведены расчеты структурных амплитуд и интегральных интенсивностей рефлексов в предположении двух моделей и различных величин смещения атомов. В результате расчетов выявлены группы рефлексов наиболее чувствительных как к той или другой структурной модели KNbO3, так и к величинам атомных смещений.
Часть 3.3.3 посвящена изучению фазовых переходов в KNbO3 в интервале температур 20≤ Т ≤ 900 оС на рентгеновском дифрактометре с целью: определить особенности температурных зависимостей структурных параметров в орторомбической, тетрагональной сегнетоэлектрических и в кубической параэлектрической фазах, и проверить по данным рентгеноструктурного анализа, какая структурная модель является предпочтительной для этих фаз – типа смещения или типа порядок/беспорядок.
Эксперимент по изучению температурных изменений структуры KNbO3 проведен дважды. Температура фазового перехода из орторомбической фазы в тетрагональную фазу совпадает с литературными данными, а из тетрагональной фазы в кубическую оказалась несколько ниже.
На рис.6 показана температурная зависимость величин смещения атомов Nb (вместе с данными [10]) из идеальной позиции в структуре перовскита (в модели типа смещения).
   Тетрагональная фаза Орторомбическая фаза [10] [10] 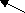 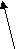 | |
| Рисунок 6. Зависимости смещений атомов ниобия δz от температуры в КNbO3 | |
 l2(Nb-О) l 1(Nb-О)  | |
| Рисунок 7. Зависимости длин связей l (Nb-O) от температуры в KNbO3 | |
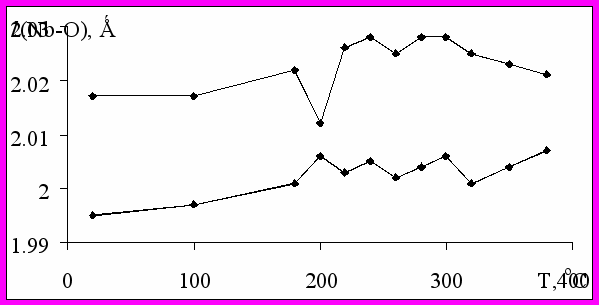
 Рѕ Ріѕ | |
| Рисунок 8. Расчетные температурные зависимости спонтанной поляризации (Рs) и ее ионной составляющей (Рis) в тетрагональной фазе KNbO3. | |
Характер температурных изменений δz(Nb) в тетрагональной фазе KNbO3 совпадает с зависимостью этих смещений, предсказанных в [9]. Отметим, что полученные нами данные хорошо согласуются с данными, полученными методом дифракции нейтронов [10].
В длинах межатомных связей lI(Nb-O) и lII(Nb-O) (рис.7) наблюдается монотонное их увеличение и в орторомбической и в тетрагональной фазе. Особенность возникает лишь при температуре фазового перехода 200 оС, когда длины этих связей сближаются. Это означает, что переход от смещений Nb по оси второго порядка (вдоль направления типа [110] в орторомбической фазе) при переходе в тетрагональную фазу смещениям вдоль оси четвертого порядка (по направлению типа [001]) происходит через состояние, в котором связи lI(Nb-O) и lII(Nb-O) становятся близкими.
На рис. 8 представлены расчетные температурные зависимости спонтанной поляризации (Рs) и ее ионной составляющей (Рis) в тетрагональной фазе KNbO3. Ионная составляющая рассчитана по формуле
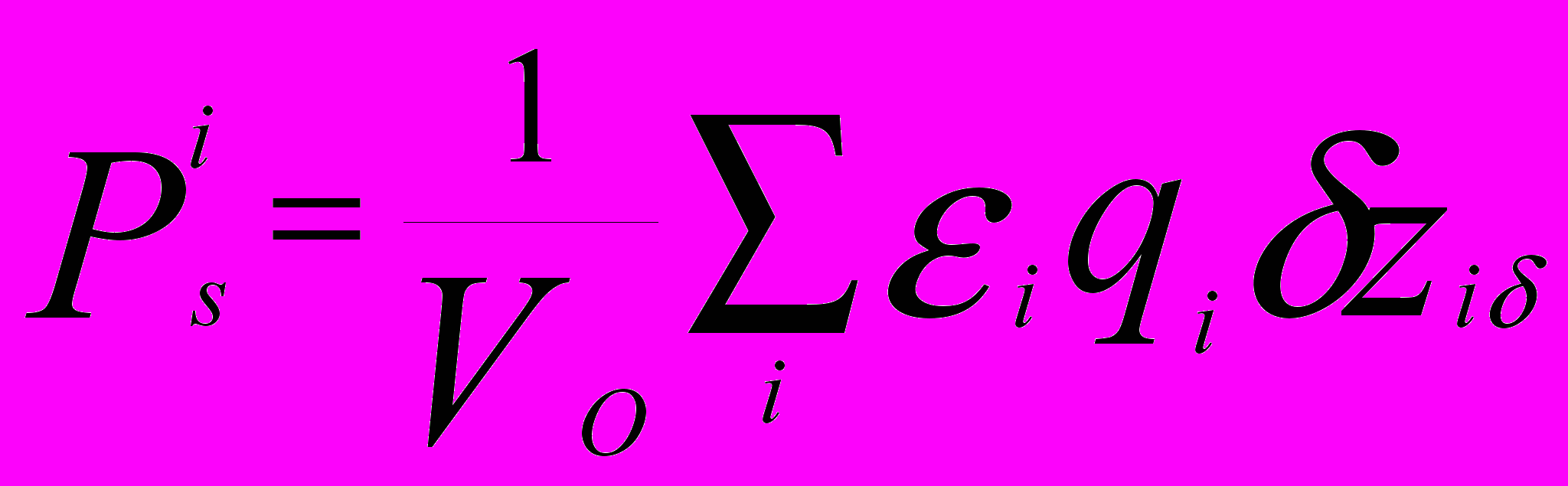 , где VО-объем ячейки; εi - число атомов i–го сорта; qi- заряд атомов i–го сорта; δzi-смещение атома i–го сорта из идеальной позиции. Рs рассчитана по величине спонтанной деформации δ:
, где VО-объем ячейки; εi - число атомов i–го сорта; qi- заряд атомов i–го сорта; δzi-смещение атома i–го сорта из идеальной позиции. Рs рассчитана по величине спонтанной деформации δ: 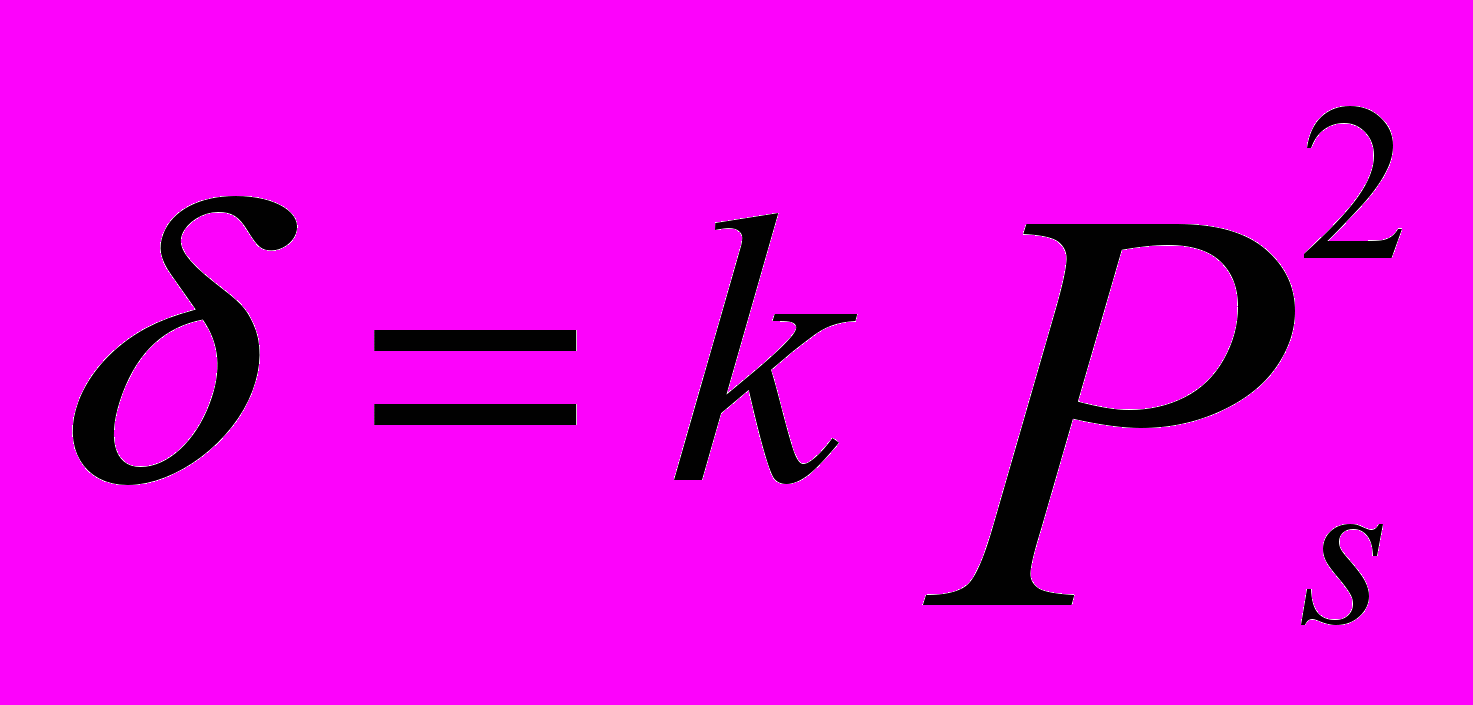 .
.В заключении сформулированы основные результаты и выводы диссертации:
1. При синтезе BaTiO3 из гель-смеси при низких температурах отжига (450 ≤ Тсин ≤ 650 оС) образуется перовскитовая кубическая фаза. С увеличением температуры отжига (750 ≤ Тсин ≤ 1200 оС) при комнатной температуре наблюдается тетрагональная фаза BaTiO3, степень тетрагональности которой увеличивается с увеличением Тсин.
2. Установлено, что интенсивное механическое воздействие и его длительность приводят к структурным изменениям BaTiO3 при комнатной температуре: с увеличением времени интенсивного механического воздействия степень тетрагональности ячейки BaTiO3 уменьшается вплоть до образования кубической фазы.
3. Обнаружено, что при температурном фазовом переходе в BaTiO3 при температуре 80 оС происходит скачкообразное изменение параметров ячейки (а,с, Ǻ), спонтанной деформации (с/а-1) и уширение рефлексов.
4. Определены коэффициенты теплового расширения для гексагональной фазы BaTiO3 в интервале температур 20 ≤ Т ≤ 900 оС: α(аh)=1.1*10-5; α(сh)=1.1*10-5.
5. Предложена кристаллохимическая трактовка высокотемпературного фазового перехода из кубической фазы BaTiO3 в его гексагональную модификацию.
6. Получено, что низкотемпературный синтез (при 500 оС) твердых растворов Ва(Тi1-хМnх)О3 0.1 ≤ х ≤ 0.9 приводит к образованию наноразмерной перовскитовой фазы с увеличенным объемом ячейки и пониженной спонтанной деформацией (с/а-1). По мере развития процесса кристаллизации в результате отжига при Т = 600 оС образуется гексагональная фаза с более плотной структурой.
7. Установлено, что при отжиге стехиометрической смеси К2СО3 и Nb2О5 при 500 ≤ Тсин ≤ 800 оС при комнатной температуре наблюдается орторомбическая фаза KNbO3. По мере увеличения Тсин объем ячейки этой фазы уменьшается. Начиная с Тсин = 700 оС в образце при комнатной температуре наблюдается образование кубической фазы KNbO3, параметр ячейки которой увеличивается с увеличением Тсин. После отжига при 900 оС в образце при комнатной температуре наблюдается смесь тетрагональной и кубической фаз.
8. По температурным зависимостям структурных параметров KNbO3 при фазовом переходе из орторомбической фазы в тетрагональную (200 оС), установлено, что длины связей (Nb-О) в кислородном октаэдре сближаются. Это означает, что переход от смещений Nb по оси второго порядка в орторомбической фазе к смещениям Nb вдоль оси четвертого порядка в тетрагональной фазе происходит не скачкообразным изменением направлений смещений Nb, а через минимум этих смещений.