Использование четвертичных аммониевых солей для защиты стали от коррозии в сернокислых растворах
| Вид материала | Документы |
- Методические указания для курсового и дипломного проектирования Москва 2009, 305.78kb.
- Vi методы защиты от коррозии металлов и сплавов, 783.92kb.
- Защиты от коррозии и старения, 844.02kb.
- Защиты от коррозии и старения, 1104.68kb.
- Методическая разработка урока химии по теме: «понятие о коррозии металлов, способы, 159.91kb.
- Реверсивное потенциометрическое титрование в анализе щелочных растворов солей карбоновых, 81.35kb.
- «Электрохимические методы защиты металлов от коррозии», 282.48kb.
- «Вызов», 86.73kb.
- Эффект электроиндуцированного селективного дрейфа катионных аквакомплексов в водных, 268.92kb.
- Эффект электроиндуцированного селективного дрейфа катионных аквакомплексов в водных, 268.96kb.
ИСПОЛЬЗОВАНИЕ СОВРЕМЕННЫХ ИНФОРМАЦИОННЫХ ТЕХНОЛОГИЙ ДЛЯ РЕШЕНИЯ КОРРОЗИОННЫХ ПРОБЛЕМ
Таранцева К.Р.*, Пахомов В.С.**
Пензенская государственная технологическая академия*, г. Пенза, kr@pgta.ac.ru; Московский государственный университет инженерной экологии**, г. Москва
Вопросы корректного выбора коррозионно-стойких материалов и способов противокоррозионной защиты для оборудования различных производств приобретают в последнее время особую актуальность в связи с острой нехваткой специалистов по коррозии и резким устареванием производственных фондов.
В условиях явной нехватки специалистов по коррозии на предприятиях помощь конструкторам при выборе конструкционных материалов могут оказать современные информационные технологии, в частности, экспертные системы. История развития глобальных или многомодульных экспертных систем по коррозии в других странах показывает, что создание их требует привлечения большого количества специалистов из различных областей знаний, координации их усилий на уровне государственной или отраслевой программы и вложения больших средств. В России в ближайшее время реально создание лишь локальных или отраслевых экспертных систем по коррозии. Для их создания и последующего успешного объединения в глобальную экспертную систему по коррозии необходимо решение ряда теоретических и прикладных задач. К теоретическим задачам, в первую очередь, нужно отнести разработку стратегии представления знаний по коррозии в той или иной ее области. Главной прикладной задачей является пересмотр практики бессистемного, хаотичного накопления экспериментальных данных по коррозии в отдельных областях, не позволяющей интегрировать получаемые данные для создания качественных банков данных.
Процесс создания экспертных систем достаточно длительный, поэтому существенную помощь предприятиям на первом этапе могут оказать узкоспециализированные автоматизированные системы выбора коррозионно-стойких материалов, разработанные на основе баз данных и баз знаний для конкретных производств. Такая попытка разработать прототип автоматизированной системы выбора коррозионно-стойких материалов для оборудования химико-фармацевтических производств (АСТЭАК) была предпринята авторами. С учетом существующих потоков данных в состав автоматизированной системы технико-экономического анализа и выбора коррозионно-стойких материалов нами были включены автоматизированное рабочее место конструктора (АРМ ОГК) и автоматизированное рабочее место экономиста (АРМ ПЭО). АРМ инженера-конструктора информационно связано с САПР «Компас», имеющей в своем составе базу данных материалов в формате СУБД Access. Это обеспечивает возможность ввода и вывода данных из базы проектируемого АРМ в базу данных САПР «Компас», получившей широкое применение в практике отечественных конструкторских разработок.
Информация в базе данных справочно-информационной системы АСТЭАК представлена по блокам: «Материалы», «Способы формообразования», «Вид термообработки», «Свойства материалов», «Условия эксплуатации», «Характеристика среды», «Стоимость». Для формирования отчетных документов разработаны алгоритмы формирования результатов, запросы на выборку, при этом для формирования требуемых результатов использованы взаимосвязанные запросы на языке SQL (Structured Query Language). Алгоритмы формирования и обработки данных реализованы на основе запросов, которые созданы в визуальном режиме средствами СУБД Access.
В настоящее время работа над наполнением базы данных АСТЭАК продолжается. Предварительная апробация АСТЭАК для выбора коррозионно-стойких материалов для аппаратурного оформления процессов получения лекарственных средств в конструкторских разработках научно-исследовательского и технологического института антибиотиков показали дружественность ее интерфейса и высокую надежность.
НАЧАЛЬНЫЕ СТАДИИ ПАССИВАЦИИ ЖЕЛЕЗОХРОМОВЫХ СПЛАВОВ В КИСЛЫХ СУЛЬФАТНЫХ СРЕДАХ
Трофимова Е.В., Подобаев А.Н., Реформатская И.И.
Ордена Трудового Красного Знамени Научно-исследовательский физико-химический институт имени Л.Я.Карпова, 105064, г. Москва, ул. Воронцово поле, д. 10,
E-mail: reform@cc.nifhi.ac.ru.
Изучены начальные стадии пассивации Cr и сплавов Fe-x%Cr (8,65£х£60 мас.%) в кислых сульфатных средах методом скачка потенциала. Предложено понятие максимального критического потенциала пассивации сплава Епасмакс - наиболее положительного потенциала, при котором сплав еще может находиться в состоянии активно-пассивного перехода. Показано, что для сплавов с содержанием СCr 27,78% при pH1,2 накопление частиц-пассиваторов при Епасмакс происходит благодаря избирательному растворению атомов Fe, при большем содержании СCr и в менее кислых растворах состав поверхности сплава во времени практически не меняется, и в пассивационном процессе участвуют только поверхностные атомы Cr. Накопление на электродной поверхности Cr(O)ads протекает по реакции:
Cr + H2O Cr(O)ads + 2H+ +2e (1)
Cr(O)ads + 2H+ Cr2+ads + H2O (2)
Количество атомных слоев (n), растворившихся до стабилизации скорости растворения сплава при Епасмакс, зависит от CCr и pH (n приближенно рассчитывали, интегрируя i(t)-кривые при Епасмакс). При расчетах полагали период кристаллической решетки сплавов равным 2,4910-10 м, а количество электронов, переносимых при ионизации атома сплава, равным 2. В интервале pH сернокислых растворов 0,48-0,9 зависимости n-CCr одинаковы для растворов различной ионной силы. Во всех случаях, когда n 1, с момента переключения потенциала до момента стабилизации скорости растворения при Епасмакс имеет место накопление частиц–пассиваторов на поверхности сплавов. В интервале CCr 8,65-22,4% при pH<1,2 это, очевидно, результат преимущественного растворения атомов Fe. В области CCr = 26,28–100 %, n, независимо от CCr, составляет ~ 60% Cr, т.е. стабилизация скорости растворения даже чистого Cr происходит только после растворения указанного количества монослоев. Это свидетельствует о том, что реакция (2) в указанном интервале pH протекает в прямом направлении со значительной скоростью. В менее кислых растворах сплавы с CCr = 25,2–100 % самопассивируются непосредственно в момент переключения потенциала. В интервале CCr 8,65- 12,8% повышение pH сопровождается снижением n, тем большим, чем меньше CCr. Скорость растворения железа из сплава при этом не должна сильно меняться, поскольку повышение pH одновременно сопровождается разблагороживанием Епасмакс, поэтому в накоплении частиц пассиваторов на поверхности сплава преимущественную роль должно играть равновесие (2), смещающееся влево при подщелачивании раствора. С повышением CCr в сплаве влияние pH на n ослабевает и, начиная с CCr =17,38%, практически прекращается. Резкое изменение поведения n при pH1,2, вероятно, связано с изменением природы частицы–пассиватора. Сделано заключение, что при pH<1,2 пассиваторами сплавов Fe-Cr являются кислородсодержащие соединения двухвалентного хрома, а при более высоких pH – трехвалентного, что согласуется с термодинамическими данными.
КОРРОЗИОННО-ЭЛЕКТРОХИМИЧЕСКОЕ ПОВЕДЕНИЕ СИЛИЦИДОВ ПЕРЕХОДНЫХ МЕТАЛЛОВ В ЭЛЕКТРОЛИТАХ РАЗЛИЧНОГО СОСТАВА
Шеин А.Б., Ракитянская И.Л.
Пермский государственный университет
614990, г. Пермь, ул. Букирева, 15, ashein@psu.ru
Одной из актуальных задач современной науки является создание материалов, обладающих высокими эксплуатационными характеристиками, в том числе высокой коррозионной стойкостью. Особое место занимают интерметаллические и металлоподобные соединения, являющиеся в ряде случаев основой для создания новых коррозионностойких сплавов. Вместе с тем, основные закономерности механизмов и кинетики парциальных электродных процессов на таких материалах изучены недостаточно.
С применением комплекса электрохимических, аналитических и структурных методов выполнено систематическое исследование основных закономерностей анодного растворения и катодного поведения силицидов металлов подгруппы железа, силицидом марганца, молибдена в кислых и щелочных электролитах. Детально изучено влияние внешних и внутренних факторов на механизм и кинетику анодного процесса. Показано, что механизмы анодного растворения силицидов в кислых и щелочных средах, а также во фторид-содержащих электролитах существенно различаются. В кислых электролитах, как правило, происходит селективное растворение металла из подрешетки в силициде, а кремний остается на поверхности и образует пленку SiO2, обладающую высокой стойкостью в бесфторидных средах. Далее процесс контролируется диффузией атомов металла из объема в приповерхностный слой силицида и окисленного металла через пленку гидратированного диоксида кремния. В щелочных электролитах растворимость кремния и диоксида кремния резко возрастают, а кинетика анодного процесса определяется образованием защитных пленок оксидов и гидроксидов металлического компонента силицидов, которые пассивируют поверхность и делают силициды стойкими в щелочах.
Установлено, что стойкость силицидов металлов подгруппы железа в кислых и щелочных электролитах в области потенциалов активного растворения, активно-пассивного перехода и в пассивной области существенно (на 2-6 порядков величины плотности анодного тока) выше, нежели соответствующих чистых металлов (М) и она зависит от соотношения количества «металл : кремний» в силицидах. Высокое химическое сопротивление силицидов обусловлено большой прочностью ковалентных связей М – Si, обусловленных сильной донорной способностью атомов М, приводящей к уменьшению вероятности отрыва поверхностных атомов от матрицы при контакте с агрессивной средой, и участием части нелокализованных электронов М в стабилизации электронной конфигурации кремния. Следует учитывать и прочные Si – Si связи, а также защитные свойства образующихся поверхностных оксидов.
На примере системы Сo, Co2Si, CoSi, CoSi2 CoSi2-Si (эвтектический сплав), Si изучено влияние соотношения количества металлической и неметаллической компоненты на анодное поведение силицидов кобальта. Установлено, что при повышении содержания кремния скорость реакции выделения водорода на силицидах в кислотах резко уменьшается. Но на низших силицидах кобальта (Co2Si, CoSi) в катодном процессе наблюдается электрокаталитический эффект.
Также детально исследованы анодные и катодные процессы на силицидах молибдена и марганца различного состава.
КОРРОЗИЯ И ПРОТИВОКОРРОЗИОННАЯ ЗАЩИТА ВНУТРЕННЕЙ ПОВЕРХНОСТИ НЕФТЯНЫХ РЕЗЕРВУАРОВ
Шишканов Б.А., Бегишев И.Р., Ащеулова И.И., Реформатская И.И.
Ордена Трудового Красного Знамени Научно-исследовательский физико-химический институт имени Л.Я.Карпова, 105064, г. Москва, ул. Воронцово поле, д. 10,
E-mail: reformir@yandex.ru; reform@cc.nifhi.ac.ru
Углеродистые и низколегированные стали являются основным конструкционным материалом для изготовления резервуаров, цистерн и др. тары для хранения нефти и нефтепродуктов. К настоящему времени резервуарный парк по хранению сернистых нефтей, выработал плановый ресурс на 69-70%. До 70% отказов приходится на коррозионные повреждения внутренней поверхности резервуаров. Наиболее сильно страдают от коррозии верхние и нижние пояса резервуаров, контактирующие соответственно с парогазовой фазой и подтоварной водой. Коррозия верхних поясов, протекающая с образованием пирофорных соединений, представляет опасность и сточки зрения пожаровзрывоопасности резервуарного парка.
Парогазовая фаза нефтяных резервуаров всегда содержит влагу, испаряющуюся из нефти или проникающую внутрь резервуара из окружающей среды. Конденсация влаги на внутренней поверхности резервуаров интенсифицируется в зимний период, когда разница температур на внутренней и внешней поверхности резервуара может достигать ~ 80 0. В зависимости от времени года и обводненности содержащейся в резервуаре нефти на внутренней поверхности кровли резервуара конденсируется 103-106 монослоев влаги, представляющей собой водный раствор, содержащий хлорид ионы и сероводород. Это позволяет сделать заключение об электрохимической природе процесса коррозионного процесса. Согласно основному уравнению диффузионной кинетики указанная толщина слоя воды сравнима или несколько меньше толщины диффузионного слоя, что позволяет сделать заключение о неограниченной диффузии газа к поверхности металла.
Предложен новый способ противокоррозионной защиты внутренней поверхности резервуаров с сернистой нефтью, заключающийся в изменении состава их естественной газофазной среды. Показано, что введение в газофазную среду азота не только снижает скорость коррозии металлических поверхностей, но и приводит к изменению состава коррозионных отложений, определяющих пожаровзрывобезопасность нефтяного резервуарного парка.
Определена критическая концентрация кислорода в газофазной среде резервуаров, при которой происходит изменение химического состава коррозионных отложений – от инертного моносульфида до пирофорного дисульфида железа. Изменение скорости коррозии, роста коррозионных отложений и их пирофорных свойств объяснены изменением скорости деполяризующей коррозионной реакции с изменением концентрации O2 в смесях O2+N2 и сменой основного деполяризатора процесса - O2, на H2S при переходе к естественной газофазной среде резервуаров с сернистой нефтью.
ВЛИЯНИЕ РЕЖИМОВ КАТОДНОЙ ЗАЩИТЫ НА СТЕПЕНЬ ПОДАВЛЕНИЯ КОРРОЗИИ И НАВОДОРОЖИВАНИЕ СТАЛИ 17ГС
В.И. Хижняков
(Томский политехнический университет)
Коррозионное растрескивание подземных стальных трубопроводов под напряжением (КРН) с внешней катодно защищаемой стороны в настоящее время является основной причиной аварийных ситуаций на газопроводах. Доля аварий на газопроводах по этой причине достигает 41,93% от общего количества.
Экспериментально установлено, что при плотности тока катодной защиты, равной плотности предельного тока по кислороду, остаточная скорость коррозии ферритно-перлитных сталей трубного сортамента в грунтах с рН 5,5…7,5 не превышает 0,01… 0,015 мм/год. При режимах катодной защиты, когда плотность тока катодной защиты превышала плотность предельного тока по кислороду в 8…10 раз, остаточная скорость коррозии уменьшалась незначительно, до значений 0,007…0,01 мм/год. Дальнейшее увеличение плотности тока катодной защиты не оказывает практического значения на степень подавления коррозии стали 17ГС. Однако степень превышения плотности тока катодной защиты над плотностью предельного тока по кислороду оказывает существенное влияние на процесс катодного наводороживания трубной стали. Экспериментально установлено, что максимальное количество поглощенного катодно защищаемой поверхностью водорода (
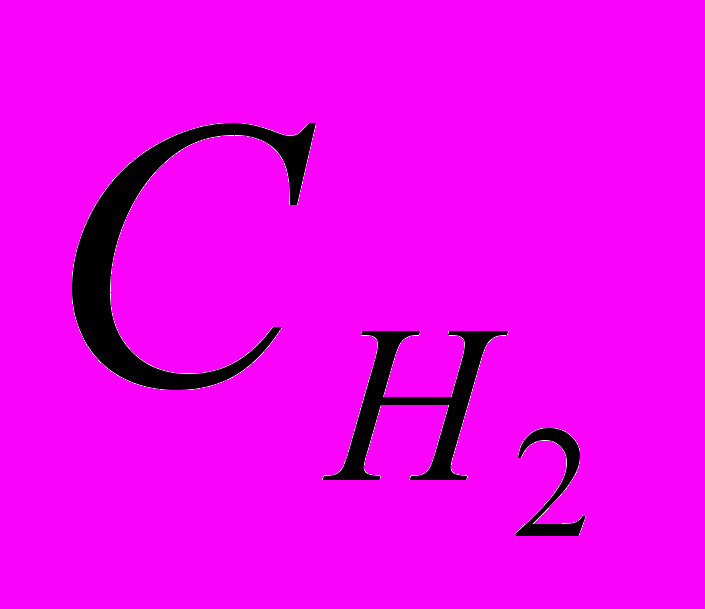 ) находится в пропорциональной зависимости от степени превышения плотности тока катодной защиты над плотностью предельного тока по кислороду, характеризуемого отношением (
) находится в пропорциональной зависимости от степени превышения плотности тока катодной защиты над плотностью предельного тока по кислороду, характеризуемого отношением (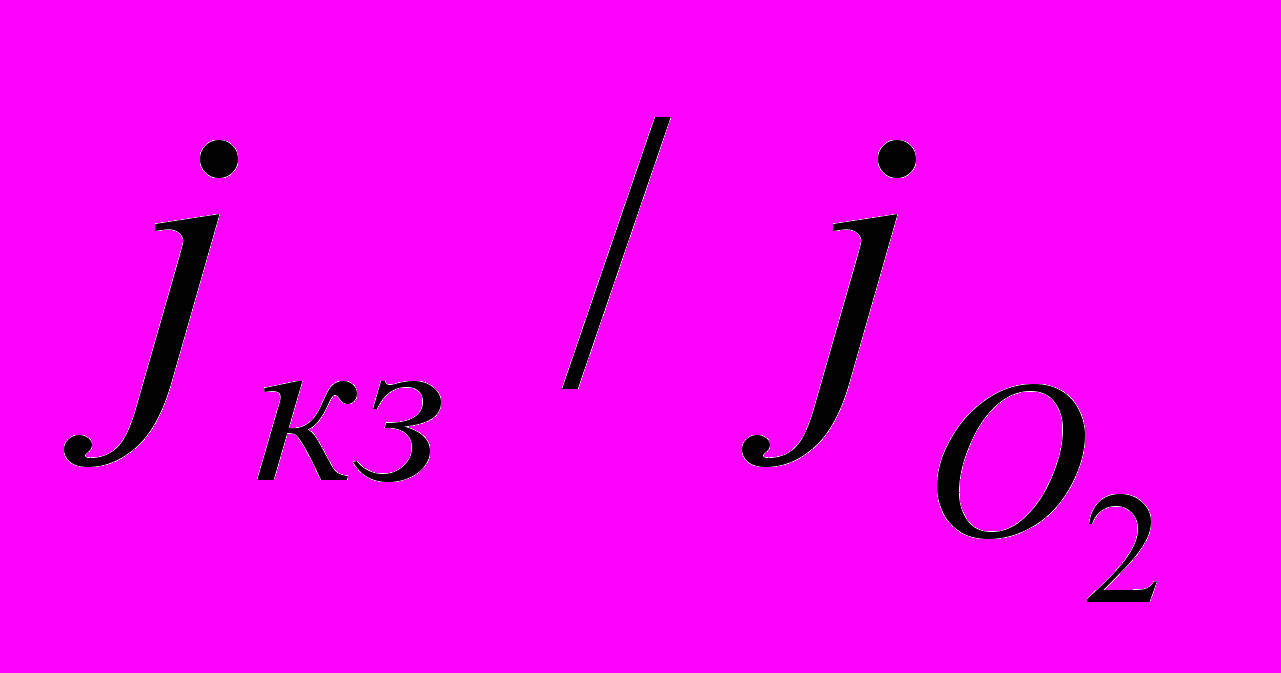 ):
): 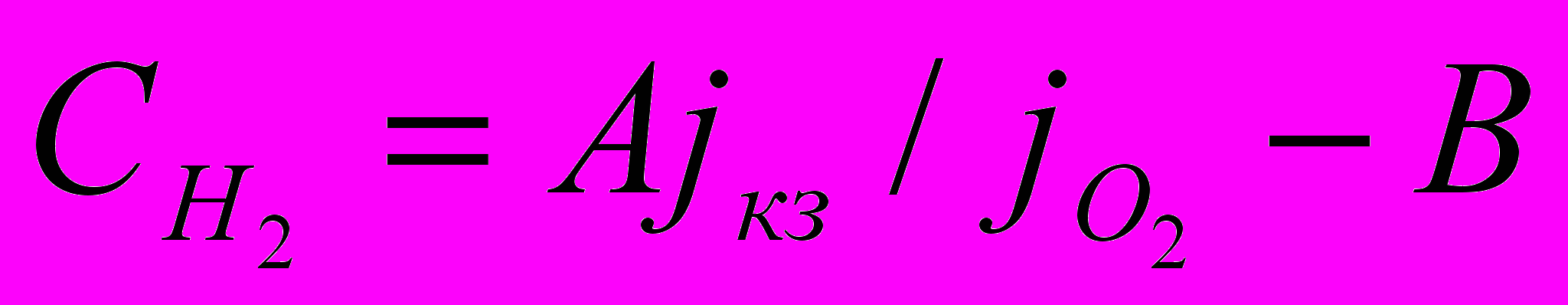 (1)
(1)Коэффициенты А и В в уравнении (1) зависят от внутренних напряжений в образцах. Однако, когда механические напряжения в образце не превышали
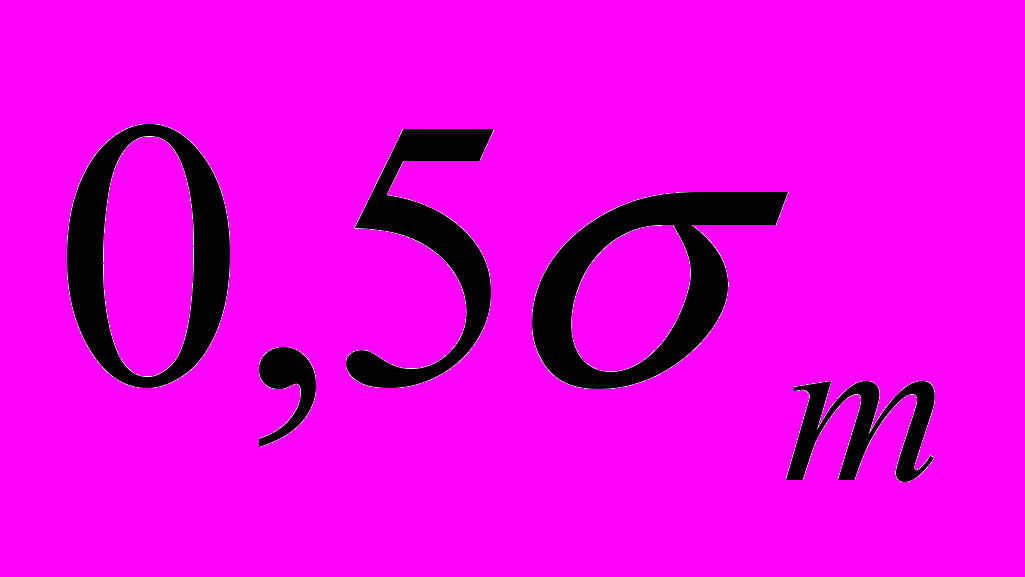 , их степень наводороживания на фоне разброса экспериментальных результатов практически не отличается от ненапряженных образцов. Степень наводороживания заметно увеличивается при режиме катодной защиты, когда
, их степень наводороживания на фоне разброса экспериментальных результатов практически не отличается от ненапряженных образцов. Степень наводороживания заметно увеличивается при режиме катодной защиты, когда и при напряжениях в образцах более
и при напряжениях в образцах более 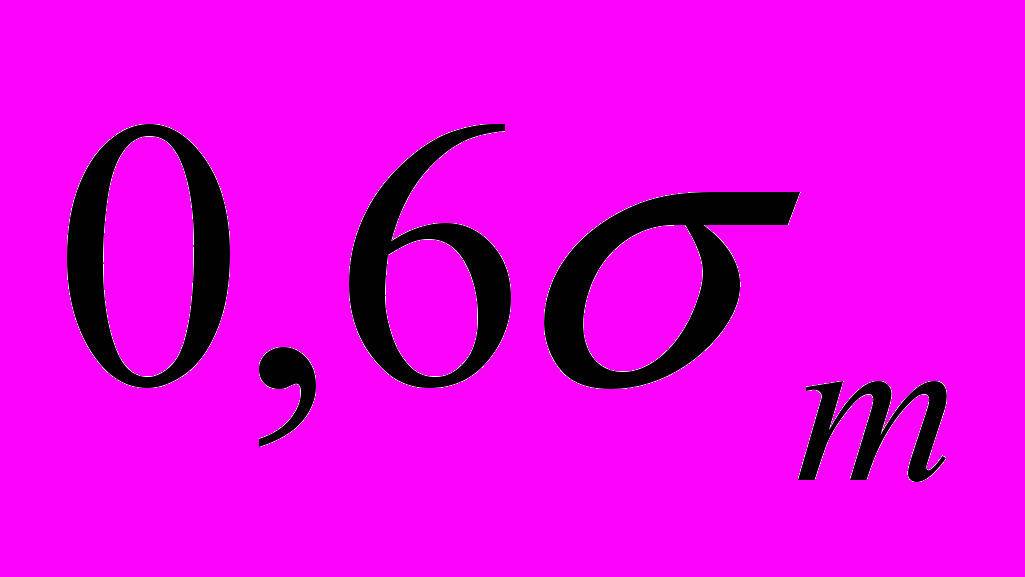 . Прямые (1) не проходят через начало координат и, практически, независимо от внутренних напряжений в образце, отсекают от оси абсцисс отрезок, когда плотность тока катодной защиты превышала плотность предельного тока кислорода в 5…8 раз. Это означает, что, независимо от внутренних напряжений, когда плотность тока катодной защиты превышает плотность предельного тока по кислороду не более, чем в 5…8 раз, количество выделившегося водорода из исследуемых образцов не превышает «родословного» - содержания водорода в образцах, не подверженных катодной поляризации.
. Прямые (1) не проходят через начало координат и, практически, независимо от внутренних напряжений в образце, отсекают от оси абсцисс отрезок, когда плотность тока катодной защиты превышала плотность предельного тока кислорода в 5…8 раз. Это означает, что, независимо от внутренних напряжений, когда плотность тока катодной защиты превышает плотность предельного тока по кислороду не более, чем в 5…8 раз, количество выделившегося водорода из исследуемых образцов не превышает «родословного» - содержания водорода в образцах, не подверженных катодной поляризации. ВЫСОКОТЕМПЕРАТУРНЫЕ ЭЛЕКТРОХИМИЧЕСКИЕ ТЕХНОЛОГИИ ПОЛУЧЕНИЯ НАНОСТРУКТУР КАРБИДОВ, БОРИДОВ И СИЛИЦИДОВ ТУГОПЛАВКИХ МЕТАЛЛОВ
Малышев В.В.
Национальный технический университет Украины «Киевский политехнический институт»,
г. Киев, 03056, пр. Победы, 37, корп.4.
Открытый международный университет развития человека «Украина»,
г. Киев, 04071, ул. Хорива. 1г, e-mail: malyshev@vmurol.com.ua
Повышенный интерес к вопросам разработки новых эффективных методов получения тугоплавких соединений– карбидов, боридов, силицидов, сплавов и интерметаллидов металлов IV-VI В групп как в виде покрытий на металлических, полупроводниковых и диэлектрических материалах, так и в виде наноструктур – продиктован их использованием для нужд современной техники, которые беспрестанно расширяются. Сравнительный анализ существующих методов синтеза металлоподобных тугоплавких соединений показал, что одним из очень перспективных, но пока мало изученных является метод высокотемпературного электрохимического синтеза в ионных расплавах.
В основе высокотемпературного электрохимического синтеза (ВЭС) лежат многоэлектронные процессы электровыделения металлов и неметаллов из ионных расплавов. Отсутствие информации о теоретических основах и принципах управления как многоэлектронными процессами, так и процессами ВЭС не давала возможность осуществлять электросинтез на практике.
В данной работе представлены теоретические основы метода ВЭС, обобщены результаты практической реализации новых технологических процессов электросинтеза наиболее важных в прикладном отношении соединений металлов IV-VI В групп с углеродом, кремнием и бором. Они базируются на результатах термодинамического анализа химических и электрохимических реакций и принципах управления многоэлектронными процессами выделения тугоплавких металлов и неметаллов.
Решение поставленных задач осуществлено при помощи:
- проведения термодинамического обоснования возможности высокотемпературного электросинтеза тугоплавких металлов и их соединений, на основании которого определялись возможные варианты и режимы электросинтеза, а также подбирались компоненты для синтеза;
- установления механизма электровосстановления сложных комплексных анионов тугоплавких металлов и неметаллов, разработки принципов реализации и управления многоэлектронными процессами;
- разработки способов сближения и нахождения условий совмещения потенциалов разных процессов выделения компонентов синтеза;
- определения способов управления формой (порошки, дендриты, покрытие, монокристаллы) катодных осадков.
1 Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований:
проект № 07-08-00631
