Учебно-методическое пособие для студентов естественных специальностей Павлодар
| Вид материала | Учебно-методическое пособие |
Содержание1.4 Природные и промышленные канцерогены Наименование фактора 2 Химические вещества и организм |
- Учебно-методическое пособие для студентов естественных специальностей Павлодар, 1215.72kb.
- Учебное пособие для студентов естественных специальностей Павлодар, 2290.94kb.
- Методика обучения техники легкоатлетических прыжков учебно-методическое пособие для, 695.99kb.
- Методика проведения круговой тренировки учебно-методическое пособие для студентов всех, 493.53kb.
- История зарубежной социологии Учебно-методическое пособие для студентов всех специальностей, 725.22kb.
- Республики казахстан, 1486.93kb.
- Учебно-методическое пособие для учителей и студентов Павлодар, 666.39kb.
- Учебно-методическое пособие по дипломному проектированию для студентов специальности, 532.3kb.
- Учебно-методическое пособие для студентов филологических специальностей Павлодар, 1306.55kb.
- Учебно-методическое пособие Рекомендовано методической комиссией финансового факультета, 556.98kb.
1.4 Природные и промышленные канцерогены
Канцерогенные вещества (от лат. cancer,- рак и греч. genes,- рождающий, рожденный), бластомогенные вещества, канцерогены, карциногены – представляют собой химические соединения, способные при воздействии на биохимические структуры организма вызывать рак и другие злокачественные опухоли, а также доброкачественные новообразования.
Среди канцерогенов можно найти как вещества встречающиеся в естественной среде, так и вещества, появившиеся в результате деятельности человека. Иногда это новые, ранее не встречавшиеся вещества, а иногда речь идет о природных веществах, но поступающих в окружающую среду в больших концентрациях, благодаря техногенезу.
Известно несколько сот таких веществ принадлежащих к разным классам химических соединений. В таблице 11 приведены химические элементы, которые могут служить причиной появления опухолей у человека, а также структуры организма (органы-мишени), которые в наибольшей степени подвержены канцерогенному действию того или иного вещества. Как видно из таблицы, наиболее уязвимым органом являются легкие, в которых бластомогены могут задерживаться достаточно долго.
Таблица 11 - Канцерогенные соединения, в отношении которых имеются убедительные доказательства их причинной роли в происхождении опухолей у человека (группа 1 по классификации МАИР) и органы-мишени
| Наименование фактора | Органы-мишени |
| Бериллий и его соединения | Легкие (центральная нервная система) |
| Кадмий и его соединения | Легкие, предстательная железа |
| Мышьяк и его соединения | Легкие, кожа |
| Никель и его соединения | Полость носа, легкие |
| Радон и продукты его распада | Легкие |
| Сажа | Кожа, легкие |
| Хром шестивалентный и его соединения | Легкие (полость носа) |
2 Химические вещества и организм
Ниже рассмотрено содержание химических элементов в живом организме и их значение для здоровья. Химические элементы рассмотрены в порядке их расположения в таблице Д.Менделеева.
2.1 Водород
Значение водорода в организме трудно переоценить. С одной стороны – это элемент, входящий в состав воды, содержание которой в живом организме достигает 90 и более процентов. С другой стороны – его ион, обуславливает рН среды. Это имеет важнейшее значение в регуляции процессов, протекающих в организме, т.к. активность ферментов специфична к кислотности среды. Благодаря этому в клетках и тканях организма возможно сохранение строгой последовательности химических превращений различных веществ. Кроме того, именно ион водорода играет важнейшую роль в окислительно-восстановительных процессах, тканевом дыхании и многих других биологически значимых процессах.
Биологическое окисление как процесс, протекающий в организме животных и человека очень сложен. В нем принимает участие сотни различных ферментов, в результате чего потенциальная энергия, запасенная растениями в молекулах органических молекул или преобразованная в организме – высвобождается. За счет этой энергии осуществляются все жизненно важные процессы – синтез веществ, деление клеток, мышечное сокращение, секреция, мышление и др.
В процессах биологического окисления еще много белых пятен, так как до сих пор еще не изучены все детали биохимических реакций в клетках. Однако точно установлено, что в цепи биологического окисления принимают участие четыре группы коферментов:
1) коферменты пиридиновой природы – никотинамидадениндинуклеотид (НАД+) и никотинамидадениндинуклеотидфосфат (НАДФ+);
2) коферменты флавиновой природы (флавинаденинмононуклеотид – ФМН , флавинадениндинуклеотид – ФАД);
3) убихинон КоQ и цитохромные системы (b, c, a), представленные комплесом геминовых ферментов;
4) цитохромоксидазы.
Все четыре группы коферментов способствуют переносу протонов (ионов водорода) и электронов от окисляемых органических веществ на кислород, как это показано на схеме – рисунок 4.
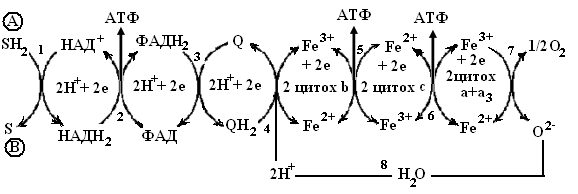
 - восстановленный субстрат,
- восстановленный субстрат,  - окисленный субстрат, 1-8 – ступени переноса протона и электрона (объяснение в тексте)
- окисленный субстрат, 1-8 – ступени переноса протона и электрона (объяснение в тексте) Рисунок 4 – Схема переноса протонов и электронов в процессе окисления
Как видно из представленной схемы, процесс тканевого дыхания протекает ступенчато, при этом перенос ионов водорода и электронов от органических веществ, подвергающихся окислению, осуществляется коферментами. Как показано на схеме цифрами:
1) пиридинзависимыми дегидрогеназами, коферментом которых является НАД;
2) флавинзависимыми дегидрогеназами, простетической группой которых является ФАД;
3) ФМН и кофермент Q;
4) - 6) цитохромами, содержащих железопорфириновые системы (цитохромы b, c, a) и цитохромоксидазой (а3).
Связующим звеном в цепи переноса протонов и электронов является кофермент Q, который передает на систему цитохромов только электроны, а ионы водорода – протоны поступают в среду и воздействуют с восстановленным кислородом, образуя воду. Эта вода называется эндогенной.
Цитохромы являются переносчиками электронов от молекул окисляемого органического вещества к молекулярному кислороду. В процессе биологического окисления – переноса протонов и электронов на кислород освобождается энергия, которая аккумулируется в пирофосфатных связях АТФ. При переброске двух протонов и двух электронов от субстрата (органического вещества) на конечный акцептор – кислород, образуется три молекулы АТФ.
