Кристаллоэнергетика как основа оценки свойств твердотельных материалов
| Вид материала | Документы |
- Исследование электрофизических свойств сельскохозяйственных продуктов и материалов, 83.47kb.
- Ознакомление с основными марками цветных сплавов и композиционных материалов, их свойствами, 385.05kb.
- Cx-x электроразрядная обработка порошков твердых сплавов с целью изменения структуры, 33.2kb.
- Вопросы вступительных экзаменов в докторантуру PhD по специальности «Материаловедение, 27.1kb.
- Тема: Основные группы свойств стоматологических материалов: адгезия и адгезионные свойства,, 288.13kb.
- Данилов А. М., Гарькина И. А. Общая методология идентификации систем: опыт моделирования, 48.43kb.
- Новыe приборы для неразрушающего контроля и технической диагностики материалов, 137.79kb.
- Методические указания по выполнению и варианты контрольной работы (задания) для студентов, 96.95kb.
- Бухгалтерский баланс как основа оценки финансово-экономического состояния предприятия, 540.21kb.
- Строение и свойства металлических материалов лекция 2 Строение и свойства металлов, 103.5kb.
3.3. Физико-химические процессы при твердении магнезиального цементаБольшинство физико-химических исследований в области твердения вяжущих веществ посвящено механизму гидратации и изучению продуктов гидратации. Обсуждение механизмов и различных схем твердения цементов приводится в книге (Теория цемента, 1991). Несмотря на приводимые в ней весьма серьезные исследования по этой проблеме, единой и общепринятой теории твердения цемента до сих пор не разработано. В отношении магнезиального вяжущего известно, что, согласно классификации вяжущих веществ по типам твердения (Кузнецова, Сычев и др., 1997), цемент Сореля можно условно обозначить как магний-хлоридный. Известно (Пащенко, 1986), что процесс гидратации порошка MgO в воде происходит чрезвычайно медленно вследствие того, что образующаяся пленка Mg(OH)2 препятствует диффузии воды вглубь зерен MgO. Процесс резко ускоряется, если в воде растворена соль-электролит, например, MgCl2. При этом гидратация основной фазы MgO сопровождается фазовыми изменениями в системе MgO-MgCl2-H2O с образованиемгидроксихлоридов магния. Общие принципы твердения магнезиальных цементов рассматривались в ряде зарубежных и отечественных публикаций (Смирнов, Соловьева, Сегалова, 1967). Например, первые исследователи магнезиального цемента считали, что твердение этого цемента обусловлено образованием оксихлоридов магния типа хMgO∙MgCl2∙yH2O, где, по данным разных авторов, х изменяется от 1 до 10, а у - от 5 до 21. Однако другая группа исследователей сводила химическую сторону процесса твердения лишь к гидратации окиси магния: MgO + H2O → Mg(OH)2 или к образованию твердых растворов гидроокиси и хлорида магния. Некоторые исследователи полагали, что при твердении магнезиального цемента наряду с гидроокисью магния образуется оксихлорид магния или твердый раствор гидроокиси и оксихлорида магния. Гидроксид и оксихлорид магния образуются преимущественно в виде коллоидных частиц на стадии гидролиза соли MgCl2 путем непрерывного связывания воды затворителя в оксигруппы гидроксида магния и в оксигруппы оксихлорида магния до момента затвердевания системы. Кристаллизация же коллоидных частиц происходит практически мгновенно. Детальному изучению продуктов твердения магнезиального цемента посвящена работа (Смирнов, Соловьева, Сегалова, 1967), в которой в результате применения химического, термографического и рентгенофазового методов анализа получены следующие данные.
На рис. 3.7 из этой статьи воспроизведены термограммы твердых фаз, образующихся при взаимодействии MgO с растворами MgCl2 разной концетрации. Как видно, в обоих случаях конечной стабильной фазой, согласно этим данным, явялется соединение 3MgO∙MgCl2∙11H2O. 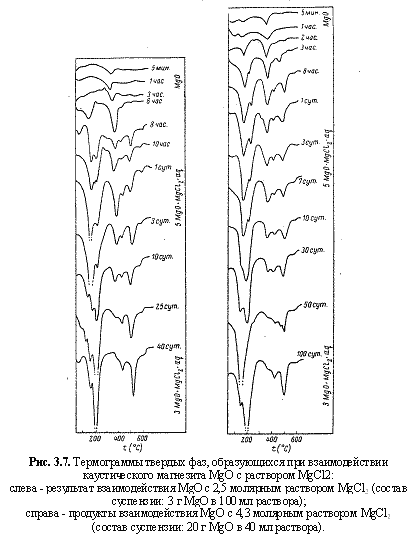 Другие, несколько отличающиеся данные о конечных продуктах твердения магнезиального цемента приводятся в более поздней, уже цитированной выше работе (Корнеев, Медведева и др., 1997), в которой авторы использовали комплекс различных методов анализа, включая рентгенофазовый, метод инфракрасной спектроскопии, дифференциально-термический, термогравиметрический, петрографический и др. Согласно данным этой работы (таблица 3.3), при взаимодействии каустического магнезита с бишофитом образуется преимущественно 5MgO∙MgCl2∙13H2O.ссылка скрыта При этом было установлено, что достижение максимальной прочности цемента в ранние сроки твердения имеет место при соотношении фаз 3MgO∙MgCl2∙11H2O : 5MgO∙MgCl2∙13H2O = 1 : 6 при суммарном их содержании 35-37%. Такой состав новообразований обеспечивает через 6 часов твердения на воздухе прочность >35 МПа. В более поздние сроки твердения от 7 до 28 суток указанное соотношение фаз практически не меняется. Таблица 3.3 Результаты исследования изменения процентного состава новообразований магнезиального вяжущего во времени твердения по данным (Корнеев, Медведева и др., 1997)
На основании выше изложенного можно сделать следующие выводы. С одной стороны, имеются данные, согласно которым при затворении MgO концентрированным раствором MgCl2 в начале гидратации кристаллизуется неустойчивое метастабильное соединение 5MgO∙MgCl2∙13H2O, которое постепенно переходит в конечную устойчивую фазу 3MgO∙MgCl2∙11H2O. Высокая прочность этого соединения обусловлена его текстурой, отличающейся взаимным прорастанием спиралевидных трубчатых нитевидных агрегатов (Маткович, Рогич, 1974), наблюдаемых в сканирующем электронном микроскопе (Установка Geolco JSM, США университет штата Иллинойс). С другой стороны, имеется фактический материал, согласно которому в быстротвердеющем магнезиальном цементе в составе собственно вяжущего доминирует соединение 5MgO∙MgCl2∙13H2O с подчиненным количеством фазы 3MgO∙MgCl2∙11H2O. Впрочем, как показано в разделе 3.5, обе эти фазы являются весьма близкими по структуре и свойствам. Кроме концентрационного фактора, на процесс структурообразования магнезиального вяжущего огромное влияние оказывает влажностный фактор (водоцементное соотношение). Влияние влажностного фактора подробно анализируется в работах Б. В. Дерягина, Л. И. Хейфеца, И. Н. Ахвердова, Е. И. Шмитько и других исследователей на дисперсных системах «вода-цемент. Результаты этих исследований можно использовать не только для управления плотностью прессованных материалов, но и при отработке технологических приемов при укладке напольных покрытий. Например, соблюдение общих законов по обеспечению кинетической устойчивости цементных растворов для самовыравнивающихся составов позволяет избежать таких неприятных последствий, как водоотделение и разупрочнение (деструктуризация) в цементно-водной дисперсии и приводит к изменению основных характеристик цементного теста: подвижности, плотности, устойчивости во времени, склонности к явлениям водоотделения и седиментации, схватывания и отвердевания. В конечном счете все эти процессы и явления находят отражение в структуре и свойствах цементного камня.  [1] Это подтверждается и нашими данными - по результатам рентгенофазового анализа продукта месячного твердения (таблица 3.2) магнезиальный цемент представлен в основном фазой 5MgO∙MgCl2∙13H2O. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
