Cols=2 gutter=151> Марина карпинская людмила луцкая марина карпинская людмила луцкая
| Вид материала | Документы |
СодержаниеПодходы к проведению реабилитационных мероприятий. |
- Насилие в отношении женщин в России Теневой доклад в работе над текстом Доклада принимали, 791.38kb.
- Насилие в отношении женщин в России Теневой доклад в работе над текстом Доклада принимали, 793.11kb.
- Cols=2 gutter=83> литература маркс К., Энгельс, 345.97kb.
- Элиасберг Наталия Ильинична, Барышников Евгений Николаевич, Захарченко Марина Владимировна,, 768.14kb.
- Кандалина Людмила Георгиевна / / Валиева Замиля Камиловна Протокол №1 от Пескарева, 499.65kb.
- Тупицына Марина Алексеевна Пименова Марина Николаевна (авторские коллектив) Самарская, 63.51kb.
- Методические материалы по проведению уроков естественнонаучного цикла Сборник подготовлен, 984.81kb.
- Сказочное в поэме «Руслан и Людмила». Цели, 72.62kb.
- Дичковская Людмила Николаевна Кравченко Людмила Савватьевна методические рекомендации, 361.68kb.
- Gutter=47> Власова Людмила Ивановна мои личные данные, 126.68kb.
Подходы к проведению реабилитационных мероприятий.
При планировании реабилитационных мероприятий должны исходить из того, что существенное количественное изменение факторов среды обитания в сложившихся социально-экономических условиях не представляется возможным.
Одним из путей является развитие системы здравоохранения. Однако, согласно позиции Всемирной организации здравоохранения, «идеальное здравоохранение» способно снизить заболеваемость не более чем на 10% (заболеваемость зависит на 50% от экономических, на 20% - от генетических и 20% от экологических причин). Иллюстрацией являются данные по Свердловской области.
Свердловская область характеризуется выраженной отрицательной динамикой показателей здоровья населения. Так, по данным годовых статистических отчетов Министерства здравоохранения Свердловской области, рост заболеваемости жителей отслеживается не только на протяжении последних трех-четырех лет, а как минимум, последнего десятилетия. Это подтверждают данные, представленные на рисунке 2.
| Классы болезней | Дети | Подростки | |||||||||||
| | 1996 | 1997 | 1998 | 1999 | 2000 | 2001 | 2002 | 1997 | 1998 | 1999 | 2000 | 2001 | 2002 |
| Болезни крови и кроветворных тканей | 6.5 | 7.3 | 8.0 | 9.9 | 10.9 | 12.5 | 15.6 | 2.3 | 2.8 | 3.1 | 3.2 | 2.9 | 5.6 |
| Болезни эндокринной системы | 7.7 | 7.8 | 10.3 | 8.9 | 8.2 | 9.1 | 10.7 | 6.1 | 8.8 | 12.4 | 15.1 | 11.6 | 13.6 |
| Психические расстройства | 7.0 | 5.2 | 6.0 | 6.3 | 6.0 | 6.3 | 7.0 | 7.2 | 12.2 | 12.6 | 11.1 | 9.4 | 8.8 |
| Болезни системы кровообращения | 3.6 | 3.5 | 2.5 | 3.1 | 2.6 | 2.5 | 5.0 | 4.0 | 4.7 | 5.6 | 6.1 | 6.2 | 12.8 |
| Болезни костно-мышечной системы | 13.7 | 14.2 | 18.3 | 16.9 | 17.9 | 19.4 | 25.6 | 17.4 | 20.5 | 23.2 | 24.6 | 19.6 | 27.4 |
| Осложнения беременности и родов | - | - | 0.1 | - | - | 0.1 | 0.1 | 7.6 | 9.4 | 8.5 | 9.6 | 8.7 | 10.0 |
| Болезни перинатального периода | 11.9 | 12.5 | 16.1 | 17.2 | 21.6 | 42.6 | 44.6 | - | - | | | - | |
| Врожденные аномалии | 3.3 | 3.3 | 3.4 | 2.7 | 2.3 | 2.7 | 3.3 | 1.1 | 1.0 | 1.1 | 0.9 | 1.0 | 1.8 |
| Новообразования | 1.5 | 1.9 | 2.0 | 1.9 | 1.6 | 1.9 | 2.5 | 1.3 | 1.3 | 1.1 | 1.4 | 1.5 | 2.2 |
| Неточно обозначенные состояния | 12.0 | 15.2 | 16.3 | 16.0 | 15.7 | 20.5 | 18.6 | 8.5 | 10.5 | 12.6 | 8.4 | 9.1 | 10.4 |
 5.0
5.0 30.0 4
Злокачественные образования на 10000 жителей (с впервые установленным диагнозом)
—it— Общая
25.0
заболеваемость болезнями
эндокринной системы (на 1000 жителей)
—*— Общая
20.0
заболеваемость
болезнями крови и
кроветворных
органов (на 1000
жителей) -Ж-Общая
заболеваемость
врожденными
аномалиями(на 1000
жителей)
1990 1992 1994 1996 1998 2000 2002
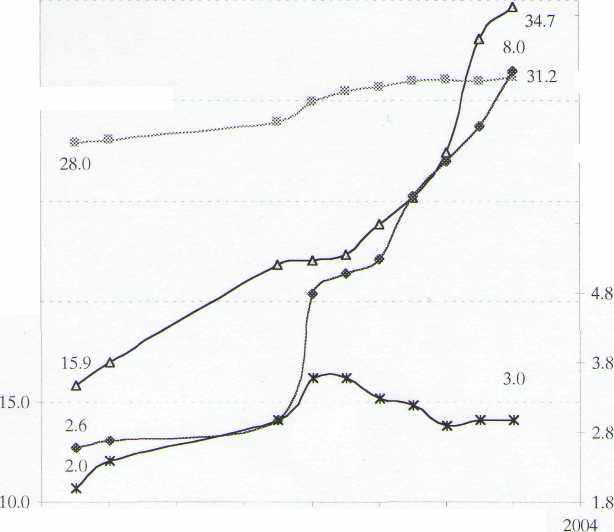
Рисунок 2. Динамика некоторых показателей заболеваемости населения Свердловской области.
В частности, отмечается увеличение злокачественных новообразований - с 28,0 в 1989 г. до 31,2 в 2001 г. (на 10000 жителей с впервые установленным диагнозом, рост в среднем на 1,1% в год), болезней эндокринной системы - с 15,9 до 34,7 за 13 лет (показатель на 1000 жителей, рост в среднем на 7,6% в год), болезней крови и кроветворных органов - с 2,6 до 8,0 (на 1000 жителей, рост в среднем на 16% в год), врожденных аномалий - с 2,0 до 3,0 (на 1000 жителей, ежегодный рост 3,9% в среднем за 13 лет).
Таблица 10.
Первичная заболеваемость детей и подростков по классам заболеваний на 1000 жителей, соответствующей возрастной группы.
Важно отметить, что увеличение заболеваемости происходит в том числе за счет младших возрастных групп населения (табл. 10). Так, с 1996 по 2002 гг. частота болезней крови и кроветворных органов выросла у детей и подростков в 2,4 раза, эндокринной системы - в 1,4 и 2,2 раза, системы кровообращения - в 1,4 и 3,0 раза, костно-мышечной системы - в 1,9 и 1,6 раз, новообразований - в 1,7 раза у детей и подростков области соответственно. Кроме этого, болезни перинатального периода, характерные для детского возраста, возросли в 3,7 раза, а осложнения беременностей и родов, а также врожденные аномалии, возросли в 1,3 и 1,6 раза соответственно. Неблагоприятная динамика роста патологии превосходит таковую на других территориальных образованиях Уральского Федерального округа, несмотря на неуклонное ежегодное возрастание подушевого финансирования областного здравоохранения с 148 рублей в 1994 г. до 1744 рублей в 2002 г. (консолидированный бюджет в расчете на одного жителя области, ежегодный прирост - 200 рублей на одного жителя в среднем в год), что по темпам финансирования превосходит любую из территорий округа (табл. 11).
Наиболее простым объяснением регистрируемого роста заболеваемости при увеличении финансирования могло бы стать возрастание диагностических возможностей лечебно-профилактических учреждений области. Однако основные показатели медицинской помощи населению за последние годы существенно не изменилась (табл. 12).
Результирующим проявлением развития неблагоприятных тенденций является ежегодное снижение средней продолжительности жизни с 70,2 лет в 1988 г. до 63,7 в 2002 г. и численности населения области с 4 млн. 743 тыс. человек в 1988 г. до 4 млн. 545 тыс. человек в 2002 г. (убыль в среднем на 14,1 тысяч жителей в год, а с учетом мигрантов - 25-28 тыс. в
год для коренного населения) (рис. 3).
Таблица 11.
Расходы на здравоохранение в Свердловской области.
| Бюджет | ТФОМС | Внебюджетные | Консолидированные средства | ||||
| Сумма, млн. руб. | Hal жителя, руб. | Сумма, млн. руб. | Hal жителя, в руб. | Сумма, млн. руб. | Hal жителя, в руб. | Сумма, млн. руб. | Hal жителя, в руб. |
| 438.7 | 94 | 245.9 | 53 | 14.0 | 3 | 698.6 | 148 |
| 1006.4 | 214 | 466.3 | 99 | 54.6 | 12 | 1527.3 | 325 |
| 1346.6 | 287 | 634.7 | 135 | 97.6 | 21 | 2078.9 | 444 |
| 1737.2 | 372 | 880.7 | 189 | 166.2 | 36 | 2784.1 | 596 |
| 1529.5 | 329 | 885.4 | 191 | 202.6 | 44 | 2617.5 | 563 |
| 2349.8 | 506 | 1294.9 | 279 | 318.8 | 69 | 3963.5 | 854 |
| 2813.0 | 610 | 1959.2 | 425 | 521.2 | ИЗ | 5293.4 | 1148 |
| 3869.3 | 844 | 2382.8 | 520 | | | 6252.1 | 1364 |
| 4956.1 | 1090 | 3168.1 | 697 | | | 8124.2 | 1744 |
Представленные данные дают основание считать, что рост финансовых вложений в здравоохранение не улучшает состояния здоровья населения области в целом и не изменяет негативных тенденций.
Таблица 12.
Некоторые показатели медицинской помощи, оказываемой населению
Свердловской области.
| Годы | Число посещений врачей (в поликлинике и на дому) на 1 жителя | Охват диспансерным наблюдением (в процентах) | Уровень госпитализации населения на 1000 жителей | Доля лиц, которым в условиях стационара поставлен диагноз(в процентах от числа госпитализированных) |
| 1996 | 6.7 | 23.3 | 239.5 | 95.16 |
| 1997 | 6.5 | 23.4 | 237.6 | 96.42 |
| 1998 | 6.5 | 23.6 | 239.3 | 96.53 |
| 1999 | 6.7 | 23.0 | 225.9 | 89.95 |
| 2000 | 6.5 | 21.7 | 219.9 | 86.30 |
| 2001 | 6.5 | 22.7 | 221.0 | 87.91 |
| 2002 | 6.4 | 19.5 | 215.6 | 84.00 |
—Ф—Численность населения, тыс. чел. 4720.0

Консолидированные расходы на 1 жителя, в руб.
 Рисунок 3.
Рисунок 3.Расходы на здравоохранение в расчете на 1 жителя и численность населения Свердловской области.
Последний момент может свидетельствовать о неэффективности использования финансовых средств и о необходимости определения направления для целевого развития. Важным направлением может считаться биопрофилактика в первую очередь групп жителей, характеризующихся признаками нестабильности генома с целью его стабилизации, тем самым предотвращающим возможность развития патологии.
В ходе выполненных нами исследований показано, что наблюдаемый у жителей Карпинска симптомокомплекс может быть обусловлен накоплением в организме сублетально пораженных клеток, в геноме которых произошла мутация, приведшая не только к гибели клетки путем апоптоза или ее злокачественной трансформации, а к изменению химической структуры синтезируемых клеткой биологически активных веществ (БАВ). При этом, образующиеся вещества приобретают новые свойства, важнейшим из которых является способность изменять чувствительность прочих клеток к регуляторным воздействиям, что приводит к нарушению функционирования нейроэндокринной и иммунной систем, а в конечном итоге - к снижению резистентности организма и появлению новых сублетально поврежденных клеток в результате воздействия как эндогенных, так и экзогенных факторов.
В настоящее время известно более 500 соединений, у которых обнаружены антимутагенные свойства при испытаниях в той или иной тест-системе. Многие из этих соединений отличает узкий дозовый диапазон, смена направленности эффекта за его пределами на про-мутагенный и побочное, в том числе токсическое действие. Поэтому не случайно, что для защиты генома человека апробированы только единицы из них.
Широкий спектр неблагоприятных для здоровья эффектов хронической экспозиции комплекса неорганических соединений металлов и неметаллов ионизирующего излучения и стойкость загрязнения ими среды обитания делают высоко актуальной задачу поиска таких средств, которые, будучи безвредными даже при длительном применении, способствовали бы, с одной стороны, уменьшению задержки токсических веществ в организме и способствовали бы их выведению, а с другой - ослаблению вызываемых ими патологических изменений и, в первую очередь, генотоксического эффекта.
Ослаблению и полной элиминации последствий воздействия мутагенов способствует система репарации повреждений ДНК в клетках организма, включающая следующие разновидности: фотореактивация, эксцизионная репарация, пострепликативная репарация.
Повреждение ДНК сопровождается развитием генетической нестабильности, проявляющейся повышением частоты возникновения спонтанных и индуцированных мутагенами генетических изменений - генных мутаций, хромосомных транслокаций, анэуплоидий и т.д.
Наиболее характерными проявлениями нестабильности генома являются геном-обус-ловленные заболевания, развитие онкопатологии и апоптоз.
Развитие онкопатологии является наиболее клинически значимым эффектом нестабильности генома после геном-обусловленных заболеваний.
В процессе роста и жизнедеятельности на все организмы популяции, вида воздействуют всевозможные неблагоприятные факторы окружающей среды, в том числе физические, химические и биологические мутагены.
Мутационный процесс сопровождается не только повреждением индивидуальных геномов органелл клетки (митохондрий), но и тотальным повреждением ее генома.
Повреждения могут затрагивать всевозможные гены, но наиболее значимым является повреждение ключевых генов, ответственных за регуляцию клеточного цикла, ферментативных систем клетки и многих других.
Например, дезактивация протеина р53 при мутировании гена приводит к сбою в работе репаративных систем клетки и невозможности адекватной корректировки первичных повреждений ДНК. В свою очередь, такая клетка получает селективное преимущество перед другими и может при необратимых изменениях генома продолжать пролиферацию, что в конечном итоге приведет к неопластической трансформации и развитию опухолевого процесса.
Наиболее ярко генетическая нестабильность проявляется в клетках с дефектным р53 из-за сбоя в работе репаративных систем, где достоверно повышается частота мутирования протоонкогенов (B-raf, c-myc, MTS), что еще более усугубляет процесс и способствует трансформации нормальной клетки в опухолевую. С этим эффектом также связывают развитие у опухолевых клеток мультирезистентности к лучевой и химиотерапии, в то время как клетки, содержащие дикий (нормальный) аллель гена, сравнительно легко поддаются лечению.
Повреждение генетического аппарата, сопровождающееся нестабильностью генома клетки, нарушением функционирования генов регуляции пролиферации и ферментативных систем (р53, K-ras, pl6, pl5, BRCA, D-loop мтДНК), впоследствии приводит к неконтролируемой экспрессии генов, ответственных за развитие программируемой клеточной гибели -апоптоза.
Считалось, что нерепарируемые повреждения ДНК, в частности, при лучевом поражении, приводят клетку к гибели в результате нарушения функций всех биохимических систем из-за невозможности полноценной транскрипции генов, содержащих дефекты в матрице ДНК. Исследования привели к формированию новых представлений о механизме гибели клеток, имеющих повреждения ДНК, как о процессе, осуществляемом в соответствии с определенной генетической программой. В индукции этой программы при наличии повреждений в ДНК клетки важная роль принадлежит белку р53. Этот белок с молекулярной массой 53 кДа локализован в ядре клетки и является одним из транскрипционных факторов, повышенная экспрессия которого приводит к репрессии ряда генов, регулирующих транскрипцию и причастных к задержке клеток в фазе клеточного цикла GI. Ключевым событием, способствующим развитию патологии, чаще всего служат соматические мутации, затрагивающие ген р53 (обычно его экзоны 5-8). Уже говорилось, что фактор р53 трансформирует сигнал
о нерепарированных разрывах цепей ДНК в сигнал к развитию апоптоза. Благодаря этому элиминируются клетки с повреждениями генетического аппарата, спонтанными или индуцированными (облученными, например).
Источником апоптогенных факторов является и внешняя среда: когда при экологическом неблагополучии накапливаются факторы, моделирующие или вызывающие развитие апоптоза.
В условиях отсутствия усиления или ослабления апоптоза реализуется такой феномен, как старение.
