Модульный блок «алкины» (6 часов)
| Вид материала | Урок |
- Урок-лекция по теме: Алкины, 28.75kb.
- Модульный курс новосибирск 2002, 283.91kb.
- М. Блок, 179.58kb.
- Контрольные вопросы по дисциплине «модели и алгоритмы обработки информации», 27.51kb.
- 1. Магистрально-модульный принцип построения компьютера, 95.88kb.
- Магистрально-модульный принцип построения компьютера, 132.33kb.
- Спецификация автоматизированного рабочего места в образовательных учреждениях, необходимая, 42.77kb.
- Александр Александрович Блок (1880 1921) биография, 26.49kb.
- Программа элективного предмета по математике, 57.1kb.
- Мозг и психика план: Строение нервной системы (и психика), 172.95kb.
Модульный блок «АЛКИНЫ» (6 часов)
| Номер урока | 0 | 1 | 2 | 3 | 4 | 5 |
| Тема урока | Введение в модуль «Алкины» | УЭ-1. Алкины. Гомологический ряд, изомерия и номенклатура. | УЭ-2. Строение алкинов на примере ацетилена | УЭ-3. Получение и физические свойства алкинов | УЭ-4. Химические свойства и применение алкинов. | УЭ-5. Урок-семинар по теме «Алкины» |
| Вид учебного занятия | Постановочный урок. | Урок изучения нового и первичного усвоения знаний | Урок изучения и первичного усвоения знаний | Урок изучения и первичного усвоения знаний | Урок изучения и первичного усвоения знаний | Урок систематизации и обобщения знаний, умений и навыков |
| Предварительный контроль | Фронтальная беседа | Входной контроль в виде тестовой формы для проверки уровня подготовленности к восприятию нового материала | Входной контроль в виде тестовой формы для проверки уровня подготовленности к восприятию нового материала | Входной контроль в виде тестовой формы для проверки уровня подготовленности к восприятию нового материала | Входной контроль в виде тестовой формы для проверки уровня подготовленности к восприятию нового материала | Фронтальная беседа |
| Что должен знать ученик | Основные понятия блока, темы творческих работ, семинары, количество баллов за работу над каждым элементом модуля | 1. Гомологический ряд ацетилена. 2. Изомерия и номенклатура алкинов. | Строение алкинов, третье валентное состояние атома углерода, sp-гибридизацию. | 1. Нахождение в природе. 2. Получение: В лаборатории; в промышленности. 3. физические свойства | 1. Основные химические свойства и применение полученных из алкинов веществ. 2. Качественные реакции на кислородсодержащие соединения. | 1.Гомологический ряд алкинов. 2. Строение алкинов (на примере ацетилена и пропина). 3.Изомерия. Номенклатура алкинов. 4. Физические и химические свойства алкинов, их применение. 5. Генетические непредельных углеводородов. 6. Качественные реакции на алкины. |
| Что должен уметь ученик | Применять понятия, используемые в модуле | Определять по общей формуле и наличию кратной связи принадлежность вещества в классу алкинов, составлять изомеры и уметь их называть | Объяснять строение молекул алкинов с точки зрения гиридизации атомных орбиталей атома углерода и особенности тройной связи в молекуле | Характеризовать способы получения важнейших алкинов, объяснять изменение в физических свойствах в гомологическом ряду | Записывать уравнения реакций, характеризующих алкины, находить генетическую связь между непредельными углеводородами | Проводить эксперимент, записывать уравнения реакций, объяснять наблюдаемые явления |
| Методы обучения | Урок - беседа | Самостоятельная работа с использованием учебника и раздаточного материала | Самостоятельная работа с использованием учебника и раздаточного материала, практическое задание . | Беседа, самостоятельная работа с использованием учебника и раздаточного материала | Самостоятельная работа с использованием учебника | Урок – коррекция Самостоятельная и групповая работа с использованием учебника, записей и справочной литературы |
| Форма организации познавательной деятельности учащихся | Общеклассная |
|
|
|
|
|
| Эксперимент | | | Л.О.: составление шаростержневых моделей молекул алкинов | Д.: Получение ацетилена из карбида кальция | Д.: Обесцвечивание ацетиленом бромной воды и перманганата калия | |
| Форма конечного контроля на данном уроке | | Составление опорного конспекта, самостоятельная работа (тест) | Обобщающая таблица, самостоятельная работа (тест) | Обобщающая таблица, самостоятельная работа (тест) | Составление опорного конспекта, обобщающей таблицы самостоятельная работа (тест) | Письменные задания, устные ответы |
| Использование ТСО | Компьютер, кодоскоп | Компьютер | Компьютер | Телевизор, компьютер | Телевизор, компьютер | Компьютер |
Урок №1. УЭ-0. Постановочный курс «Алкины»
Цели: познакомить учащихся с содержанием модуля, поставить учебные цели и показать пути их достижения, ознакомить с предполагаемыми результатами данного модуля, возможными способами проверки его усвоения.
На доске записано название модуля “Алкины”. Учитель начинает с актуализации знаний учащихся, постановки учебных целей. Учитель знакомит учащихся с содержанием модуля по карте «Модульный блок-Алкины» (таблица 1), обращает внимание на то, что они должны знать и уметь. После этого учитель предлагает учащимся вспомнить, что они уже знают об алкинах из курса химии 9 класса.
Примерные вопросы для беседы:
- Что такое алкины?
- Кто является первым представителем гомологического ряда этих углеводородов?. Напишите его молекулярную и структурные формулы
- Что вы помните о способах получения и физических свойствах важнейших алкинов? Приведите реакции.
- Какие химические реакции характерны для алкинов?
- Где применяются алкины?
Домашнее задание:
Записи в тетради, подготовиться к работе с модулем «Алкины»
| Содержание | Что нужно знать | Что нужно уметь | Формы к онтроля | Максимальное количество баллов и отметка | Литература |
| УЭ-1 Гомологический ряд, изомерия и номенклатура. | 1. Гомологический ряд ацетилена. 2. Изомерия и номенклатура алкинов | Определять по общей формуле и наличию кратной связи принадлежность вещества к классу алкинов, составлять изомеры и уметь их называть | Входной (в начале темы), текущий, выходной (после изучения этого элемента модуля) | 20 баллов 20-18 «5» 17-14 «4» 13-9 «3» менее 9 «2» | О.С. Габриелян Химия 10. Профильный уровень; Э.Е. Нифантьев Органическая химия 11(10) |
| УЭ-2 Строение алкинов на примере ацетилена | Строение алкинов, третье валентное состояние атома углерода, sp-гибридизацию. | Объяснять строение молекул алкинов с точки зрения гибридизации атомных орбиталей атома углерода и особенности тройной связи в молекуле | Входной (в начале темы), текущий, выходной (после изучения этого элемента модуля) | 20 баллов 20-18 «5» 17-14 «4» 13-9 «3» менее 9 «2» | О.С. Габриелян Химия 10. Профильный уровень; Н.И. Новошинский, Н.С. Новошинская Органическая химия 11 класс |
| УЭ-3 Получение и физические свойства алкинов | 1. Нахождение в природе. 2. Получение: В лаборатории; в промышленности. 3. физические свойства | Характеризовать способы получения важнейших алкинов, объяснять изменение в физических свойствах в гомологическом ряду | Входной (в начале темы), текущий, выходной (после изучения этого элемента модуля) | 23 балла 23-21 «5» 20-17 «4» 14-11 «3» менее 11 «2» | О.С. Габриелян Химия 10. Профильный уровень; Э.Е. Нифантьев Органическая химия 11(10) |
| УЭ-4 Химические свойства и применение алкинов. | 1. Основные химические свойства и применение полученных из алкинов веществ. 2. Качественные реакции на кислородсодержащие соединения. | Записывать уравнения реакций, характеризующих алкины, находить генетическую связь между непредельными углеводородами | Входной (в начале темы), текущий, выходной (после изучения этого элемента модуля) | 37 баллов 37-35 «5» 34-29«4» 28-20 «3» менее 19 «2» | Э.Е. Нифантьев Органическая химия 11(10); Н.И. Новошинский, Н.С. Новошинская Органическая химия 11 класс; |
| УЭ-5 Урок-семинар по теме «Алкины» | 1.Гомологический ряд алкинов. 2. Строение алкинов (на примере ацетилена и пропина). 3.Изомерия. Номенклатура алкинов. 4. Физические и химические свойства алкинов, их применение. 5. Генетические непредельных углеводородов. 6. Качественные реакции на алкины | Проводить эксперимент, записывать уравнения реакций, объяснять наблюдаемые явления | Текущий, выходной (после изучения этого элемента модуля) | 15 баллов 15-14 «5» 13-11«4» 10-8 «3» менее 8 «2» | Н.И. Новошинский, Н.С. Новошинская Органическая химия 11 класс; Э.Е. Нифантьев Органическая химия 11(10) |
Урок №2. СТРОЕНИЕ АЛКИНОВ НА ПРИМЕРЕ АЦЕТИЛЕНА
Цель: организация деятельности учащихся, направленной на прочное усвоение знаний по строению алкинов (на примере ацетилена)
Образовательные задачи
Главная – сформировать представление о структуре молекулы ацетилена на основе модели sp-гибридизации орбиталей атома углерода; строении тройной углерод-углеродной связи и ее характеристикам (энергия, длина).
Сопутствующая – продолжать формирование умений и навыков по предсказанию геометрии молекул. Контролировать и корректировать умения извлекать информацию из учебника (работа с литературой).
Развивающие задачи
1.Развивать у учащихся умения сравнивать и анализировать строение и геометрию молекл алкинов, алкенов с алканами на основе разного типа гибридизации орбиталей атома углерода; выделять главное и существенное.
2.Развивать познавательные способности и интерес у учащихся
Воспитывающие задачи
Продолжить формирование химической картины мира, умение рационально оценивать ответы товарищей, самокритичность, аккуратность
Тип урока: Урок изучения и первичного усвоения знаний
Оборудование: учебник О.С. Габриелян и др. Химия 10. Профильный уровень, таблицы «строение молекулы ацетилена», модульные карты для учащихся, презентации с ключами к вопросам модуля, элементы шаростежневых моделей молекул.
Ход урока:
| № учебного элемента | Деятельность учеников | Деятельность учителя | Затраченное время |
| УЭ - 0 | Каждый ученик читает про себя цель урока, поставив перед собой конкретную задачу. Выполнение, которой он будет отслеживать для себя в течение всего урока. | Направляет деятельность учащихся на чтение цели урока. | 1 мин |
| УЭ – 1 Входной контроль | Прочитывают цель УЭ-1. Отвечают на вопросы модуля и дополнительные вопросы учителя. | Направляет работу учащихся. Проводит фронтальный опрос учащихся по вопросам модуля и по необходимости задает дополнительные и наводящие вопросы, добивается полных развернутых ответов от учащихся. Отмечает ответы учащихся в своем журнале. Следит за самостоятельностью учащихся при выполнении письменных заданий. Выставляет оценку к себе в свой журнал. | 8 мин |
| УЭ -2 Изучение новой темы | Читают цель УЭ-2. Записывают дату и тему урока в тетрадь. Самостоятельно изучают «строение молекулы ацетилена» по предложенной справке, заполняют таблицу (приложение 1) | Направляет работу учащихся. Акцентирует внимание на работе с тетрадью. Оказывает консультативную помощь при решении задачи. Дает разъяснения в случае необходимости. По своему усмотрению может выборочно проверить работы. Выставляет оценку в свой журнал. | 25 мин |
| УЭ – 3 Обобщение и закрепление, выходной контроль | Читают цель УЭ-4 Выполняют тест, ответы записывают на бланке модуля. Для самостоятельной проверки выполнения теста берут ключи у учителя, проверяют правильность выполнения и выставляют оценку в бланк модуля. | Направляет деятельность учащихся. Следит за самостоятельностью выполнения теста. Дает консультации по оцениванию работы. Выставляет оценки в свой журнал. | 9 мин |
| УЭ-4 Подведение итогов урока | Еще раз прочитать цель урока. Обсуждают результаты по модулю. Озвучивают свои оценки. Выставляют оценки в дневник. Выбирают домашнее задание по модулю. Сдают модули учителю, а бланки вклеивают в тетрадь. | Направляет деятельность учащихся. Анализирует ответы учащихся. Учитель выставляет их в свой журнал и комментирует, говорит о своих наблюдениях и объективности оценок. Выставляет итоговые оценки в классный журнал. Отдает на дом модули тем ученикам, кто плохо справился с работой на уроке. | 2 мин |
| | | Расписывается в дневниках учащихся за оценки. Отмечает в своем журнале отсутствующих. | перемена |
УЭ-2. УРОК №2. СТРОЕНИЕ АЛКИНОВ НА ПРИМЕРЕ АЦЕТИЛЕНА
Инструкция по работе с модулем:
Проверить наличие «Бланк учебных достижений»
- При выполнении данной работы необходимо переходить от одного блока модуля к другому последовательно, выполнив все задания блока и оценив свою работу по предложенным критериям.
- Если при выполнении каких либо заданий возникают затруднения – обратись за помощью к учителю.
| № УЭ | Учебный материал с указанием заданий | Рекомендации к выполнению заданий и оцениванию своей работы | ||||||||||||||||
| УЭ 0 (1 мин) | Цель: Выяснить строение алкинов (на примере молекулы ацетилена) в сопоставлении со строением молекул алканов и алкенов. Все новое в науке является простым скоплением уже известных вещей. Л. Мейер, 1867 г. | Внимательно прочитайте цель урока и эпиграф к нему. | ||||||||||||||||
| УЭ 1 (8 мин) | Цель: через повторение учебного материала о строении молекул изученных ранее классов углеводородов подготовиться к работе по новому модулю. Ответьте устно на вопросы:
Выполните письменно тест: 1. Укажите тип гибридизации орбиталей атомов углерода, связанных кратной связью, в пропилене: 1) sp3; 2) sp; 3) sp2; 4) spd2 2. Сколько орбиталей остается негибридными во втором валентном состоянии атома углерода? 1) 1; 2) 2; 3) 3; 4) нет негибридных орбиталей 3. Под каким углом направлены sp3-гибридизованные орбитали углеродных атомов, связанных кратной связью, в этиленовых углеводородах ?: 1) 120о; 2) 180°; 3) 109° 27'; 4) 90о 4. Сколько и π -связей сосредоточено в молекуле пропена? 1) 6 и 1; 2) 7 и 2; 3) 8 и 1; 4) 9 и 2 5. Какова длина и энергия кратной связи С=С в этиленовых углеводородах ?: 1) 0,133 нм; 620 кДж/моль; 2) 0,12 нм; 822 кДж/моль; 3) 0,154 нм; 350 кДж/моль 4) 0,1 нм; 220 кДж/моль; Поменяйтесь работами с соседом по парте. Осуществите взаимопроверку по ключам, приведенных на слайдах. Оцените работу партнера, поставив «+» или 1 за каждый верный ответ . Критерии отметки (баллы): 5 верных ответов-«5», 4 верных ответа-«4» 3 верных ответа-«3», 2 верных ответа-«2» | Работайте вместе с классом 1 балл дополнительно Работайте индивидуально, вписывая ответы в бланк №1. За работу на этом этапе урока максимально 5 баллов Старайтесь быть внимательными и объективными при оценивании своего партнера. Баллы поставьте на бланке №1. | ||||||||||||||||
| УЭ 2 (25 мин) | Цель: Изучить строение алкинов на примере молекулы ацетилена. Прочитав справку «Строение молекулы ацетилена» выполните следующие задания:
Справка Физическими методами исследования установлено, что молекула ацетилена имеет линейное строение (вспомните, что для метана характерна тетраэдрическая структура, молекула этилена-плоская). Также определено, что расстояние между ядрами атомов углерода равно 0,120 нм. Такое строение молекулы ацетилена можно объяснить sp-гибридизацией (третьим валентным состоянием атома углерода). То есть углеродные атомы в молекуле ацетилена находятся в состоянии sp-гибридизации:  Это означает, что каждый атом углерода обладает двумя гибридными sp- орбиталями, оси которых расположены на одной линии под углом 180 друг к другу (максимальное удаление орбиталей друг от друга), а две p (y,z)- орбитали остаются негибридными. По одной из двух гибридных sp-орбиталей каждого атома углерода взаимно перекрываются, приводя к образованию - связи между атомами углерода. Каждая оставшаяся гибридная орбиталь перекрывается с s- орбиталью атома водорода, образуя - связь С–Н (см. рис.1) связь связь связь  Рис.1 Оставшиеся у каждого атома углерода две негибридные р (у,z) орбитали, расположенные перпендикулярно друг другу и перпендикулярно направлению - связей, взаимно перекрываются и образуют две - связи (см. рис.2). 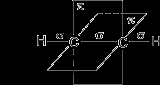 Рис.2. Две - связи между атомами углерода находятся в двух взаимно перпендикулярных плоскостях Рис.2. Две - связи между атомами углерода находятся в двух взаимно перпендикулярных плоскостяхТаким образом, тройная связь характеризуется сочетанием одной - и двух - связей. Их образование приводит к тому, что ядра атомов углерода сближаются, а длина связи между ними уменьшается до 0,120 нм (см. рис.3). 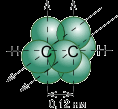 Рис.3 Рис.3(Для сравнения: длина С-С связи 0,154 нм, а длина С=С связи 0,133 нм). Тройная углерод-углеродная связь суммарно прочнее двойной связи и тем более одинарной: СС 814 кДж\моль, энергия связи С=С 620 кДж\моль, С-С 347 кДж\моль. Однако, наличие в молекулах алкинов непрочных -связей обусловливает высокую реакционную активность ацетилена. | Не забудьте записать тему урока Работайте самостоятельно с последующей устной коллективной проверкой. За работу на этом этапе урока максимально 5 баллов (выставить баллы в бланк №2) Заполненное приложение 1 (таблица) после проверки вклеить в тетрадь. | ||||||||||||||||
| УЭ 3 (9 мин) | Цель: обобщить и закрепить изученное на сегодняшнем уроке. Выполните тест: ОБЯЗАТЕЛЬНАЯ ЧАСТЬ (№1-3-по 1 баллу; № 4 - 4 балла)
1) линейная; 2) плоская; 3) тетраэдрическая; 4) зигзагообразная 2. Число связей в молекуле бутин-1 1) 4; 2) 3; 3) 2; 4)1 3.Перечислите тип гибридизации атомов углерода в алкине СНС-СH2-CH3 1) sp2 sp2 sp3 sp; 2) sp sp sp3 sp3 3) sp sp2 sp3 sp; 4) sp2 sp sp3 sp 4. Выберите соответствие:
После выполнения обязательной части самостоятельно сравните ответы с эталоном на слайде. Критерии отметки (баллы): 7 верных ответов-«5»,  6 верных ответов баллов-«4»  , ,5 верных ответов баллов-«3»,  4 и менее верных ответа-«2»   !!!при получении неудовлетворительного результата попросите у учителя данный тест домой с целью проработки его еще раз. !!!при получении неудовлетворительного результата попросите у учителя данный тест домой с целью проработки его еще раз.При хорошем выполнении обязательной части переходите к дополнительной части заданий (если осталось время). ДОПОЛНИТЕЛЬНАЯ ЧАСТЬ Приведите простейшую формулу углеводорода в котором атомы углерода находятся в состоянии sp3 sp sp2 состояниях. Назовите его. Вариант 2. ОБЯЗАТЕЛЬНАЯ ЧАСТЬ
1) sp; 2) sp2 ; 3) sp3 4) spd 2. Число связей в молекуле пентин-2 1) 4; 2) 3; 3) 2; 4)1 3.Перечислите тип гибридизации атомов углерода в алкине H3C-СС--CH3 1) sp2sp2 sp sp; 2) sp sp sp2 sp3 3) sp sp sp3 sp; 4) sp3 sp sp sp3 4. Выберите соответствие:
| Работайте индивидуально, вписывая ответы в бланк №3. Максимально 7 баллов Старайтесь быть внимательными и объективными. Баллы поставьте на бланке №3. 2 балла дополнительно | ||||||||||||||||
| УЭ 4 (3 мин) | Цель: подведение итогов урока. Прочитайте цель урока. Подходит ли эпиграф к теме урока? Достигли Вы цели урока? В какой степени? Какие затруднения возникали у вас при работе на уроке? Почему? Оцените свою работу на уроке по пятибалльной шкале (по средним результатам). Выберите домашнее задание Обязательная часть Стр. 23-24 (читать), упр. №3,4 на стр. 24 (устно) Дополнительная часть (повышенной сложности) В молекуле неизвестного алкина общее число электронов равно 86, а число атомов углерода в третьем валентном состоянии равно числу атомов углерода в первом валентном состоянии. Приведите структурную формулу возможного алкина и изобразите формулы трех его изомеров. | Работайте вместе с классом. Отметку поставьте в бланк №4. Сдайте учителю бланк учебных достижений. Самостоятельно |
БЛАНК УЧЕБНЫХ ДОСТИЖЕНИЙ УЧЕНИКА (ЦЫ):
БЛАНК №1. УЭ-1. ТЕСТ (ВХОДНОЙ КОНТРОЛЬ)
| Вопрос | 1 | 2 | 3 | 4 | 5 | Сумма |
| | | | | | | |
| ответ | | | | | | |
| +/- | | | | | |
Дополнение за устные ответы:
Общий балл:
БЛАНК №2. УЭ-2. РАБОТА НА УРОКЕ
Баллы:
БЛАНК №3. УЭ-3. ТЕСТ (ЗАКРЕПЛЕНИЕ ЗНАНИЙ).
| Вопрос | 1 | 2 | 3 | 4 | Дополнит. часть | Сумма | |||
| | | | | А | Б | В | Г | | |
| ответ | | | | | | | | | |
| +/- | | | | | | | | | |
Баллы:
БЛАНК №4. УЭ-4. ИТОГОВАЯ ОТМЕТКА ЗА УРОК.
Ваша отметка
Отметка учителя
ПРИЛОЖЕНИЕ 1. УЭ-1
| Элементы | Свойства элементов | Связи | Свойства связей | Структура первого представителя алкинов | ||||
| | гибридизация | Электроотрицательность (ЭО) | Разновидность связи (, ) и их число; форма молекулы | Энергия (кДж\моль), длина (нм) | Полярность | Структурная и электронная формула ацетилена | Схема перекрывания орбиталей в ацетилене | |
| Атомы С | | 2,75 2,69 | СС С=С | | | | | Образование связей Образование связей |
| | 2,5 | С-С | | | | |||
| Атомы Н | | 2,1 | С-Н | | | | ||
