«Санкт-Петербургская государственная педиатрическая медицинская академия»
| Вид материала | Автореферат |
- «Санкт-Петербургская государственная педиатрическая медицинская академия», 580.43kb.
- Петербургская Государственная Педиатрическая Медицинская Академия, 194100, улица Литовская,, 26.64kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия Федерального, 682.04kb.
- Поляков Игорь Васильевич Эрман Михаил Владимирович Ведущее учреждение: гоудпо санкт-Петербургская, 348.31kb.
- Петербургская Государственная Педиатрическая Медицинская Академия, 194100, улица Литовская,, 31.72kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия Росздрава», 244.37kb.
- «Санкт-Петербургская государственная педиатрическая медицинская академия», 347.44kb.
- Рабочая программа дисциплины 11 Учебная информация, 1086.73kb.
- Биоактивных наноматериалов при раневом процессе, 438.75kb.
- В периоперационном периоде, 343.13kb.
Таблица 1.
Частота местно-распространенных форм среди больных раком щитовидной железы
| Форма РЩЖ | Общее число наблюдений (1973-2007) | Местно-распространенные формы | |
| Абс. | % | ||
| Папиллярный | 1311 | 196 | 15,0 |
| Фолликулярный | 646 | 169 | 26,1 |
| Медуллярный | 158 | 89 | 56,3 |
| Всего | 2115 | 464 | 21,9 |
Среди 464 пациентов местно-распространенным РЩЖ было 89 (19,2 %) мужчин и 375 (80,8 %) женщин. В общей группе больных РЩЖ этот показатель соответствовал 11,9 % и 88,1 %. То есть, при местно-распространенном РЩЖ удельный вес лиц мужского пола был значительно больше. Соотношение мужчин и женщин составило 1: 4,2, в общей группе больных – 1: 6,4. Таким образом, дифференцированный РЩЖ у мужчин имел более агрессивное течение, так как в обследованной группе их было значительно (р < 0,05) больше, чем женщин с опухолями в стадии Т4. Средний возраст больных был равен 57,7 ± 2,0 г. (при колебании от 17 до 83 лет), что значительно (р < 0,05) превысило аналогичный показатель в общей группе больных РЩЖ (51,6 ± 0,17 года). Около трети больных местно-распространенными формами РЩЖ составили лица старше 60 лет (161 наблюдение или 34,8 %).
В течение 27 лет в клинике при лечении больных РЩЖ применялся органо-сберегательный подход в отношении дифференцированных и спорадических медуллярных форм заболевания. На протяжении последних 8 лет такой вид операций используется лишь при стадии опухоли T1N0M0. Каждая операция у больных РЩЖ с начала 80-х годов дополнялась центральной лимфаденэктомией и биопсией III и IV групп лимфатических узлов шеи. В случае местно-распространенных карцином ЩЖ выполнялись комбинированные, расширенные и паллиативные хирургические вмешательства. Лечебная шейная лимфаденэктомия выполнялась при наличии макроскопически определяемых метастазов в регионарных лимфатических узлах (Романчишен А.Ф. и соавт., 2004). При распространении регионарных метастазов на окружающие структуры производилась операция Крайля. В случаях, когда лимфогенные метастазы располагались в средостении или первичная опухоль была неудалима из шейного доступа, оперативное вмешательство производилось с использованием частичной продольно-поперечной стернотомии, а с 2005 г. – частичной продольной стернотомии.
В 56 случаях (у пациентов из группы «высокого операционного риска») хирургическое вмешательство разделялось на два этапа – сначала производилось вмешательство на первичном очаге, а футлярно-фасциальная диссекция выполнялась через 2 – 3 месяца. Обоснованием такого подхода считали относительно медленное и благоприятное местное течение дифференцированных форм РЩЖ.
Комбинированные, расширенные или паллиативные хирургические вмешательства выполнялись при распространении первичной опухоли за пределы ЩЖ, при распространении регионарных метастазов на лимфатические узлы шеи с двух сторон и в средостение, за пределы лимфатических структур и окружающей клетчатки.
Согласно номенклатуре операций, предложенной Б.Е. Петерсоном (1976), под комбинированной операцией мы понимаем вмешательство, где кроме органа, несущего опухоль, резецируется или удаляется соседний орган, в который вросла карцинома. Расширенной называем операцию, при которой удаляются лимфатические барьеры шире типичных схем. Относительно РЩЖ – это больше, чем односторонняя модифицированная шейная диссекция, когда удаляются 2, 3, 4, 5 и 6 группы шейных лимфоузлов (с одной или двух сторон) и/или средостения. Паллиативной называем операцию, при которой после резекции ЩЖ и/или регионарных лимфоузлов остается часть опухолевой ткани в стенках органов шеи, средостения и/или отдалённые метастазы рака.
Больные с резидуальными папиллярными и фолликулярными карциномами в стенках трахеи, пищевода, сосудов шеи и средостения, других органах (М1) после операций направлялись для терапии радиоактивным йодом (106 наблюдений) и наружного облучения (211 наблюдений). При медуллярном РЩЖ в аналогичных ситуациях проводились химиотерапия и наружное облучение шеи (49 случаев).
В работе анализирована 581 операция, предпринятая у 464 больных дифференцированными и медуллярными опухолями ЩЖ в стадиях T3N1bM0, T4N0M0, T4N1aM0, T4N1bM0 (табл. 2).
Таблица 2
Характер хирургических вмешательств у 464 больных местно-распространенным раком щитовидной железы
| Характер операции | ПР (n = 196) | ФР (n = 169) | МР (n = 89) | Всего |
| Комбинированная | 120 | 112 | 24 | 256 |
| Расширенная | 112 | 102 | 32 | 246 |
| Паллиативная | 58 | 46 | 33 | 137 |
| Всего операций | 290 | 260 | 89 | 581 |
Примечание: ПР – папиллярный рак; ФР – фолликулярный рак; МР – медуллярный рак;
Число операций превышает количество наблюдений, поскольку некоторые больные оперированы повторно или перенесли одновременно комбинированные и расширенные вмешательства.
Среди этих вмешательств 256 (44,1 %) были комбинированными. Из них 60 (23,4 %) операций носили паллиативный характер, так как в итоге операции полностью удалить ткань опухоли не удалось. У 7 (2,7 %) вмешательства выполнялись с использованием трансстернального доступа. Расширенные операции производились в 246 (42,3 %) наблюдениях. Из них 7 (2,7 %) вмешательств оказались паллиативными и 24 (10,2 %) операция выполнены через трансстернальный доступ.
В вышеуказанных группах в 140 (24,1 %) случаях операции носили смешанный характер, то есть, были комбинированными и расширенными одновременно (с резекцией соседних органов и двухсторонней лимфаденэктомией), в том числе у 5 (3,6 %) больных они предпринимались через трансстернальный доступ. Эти вмешательства выполнялись при опухолях T4N1b, и включены в обе вышеперечисленные группы.
Кроме того, были произведены 78 (13,4 %) паллиативных вмешательств у пациентов с первичными опухолями, соответствующими Т4, где была удалена часть опухоли, вызывавшая компрессию органов шеи, в первую очередь, трахеи. В этих случаях попытка комбинированного или расширенно-комбинированного вмешательства, по тем или иным причинам (тяжелое состояние больных, недостаточный опыт хирурга и др.) не предпринималась. В дальнейшем 8 таким больным были произведены повторные операции с успешным полным удалением карцином (после дополнительного обследования, интенсивной подготовки, изменения доступа на расширенный шейно-чрезгрудинный). В итоге эти 8 пациентов были отнесены в группы с соответствующими объемами вмешательств. Таким образом, паллиативных вмешательств без обширного удаления опухолевых масс было 70. Эти пациенты вместе с 67 вышеперечисленными, перенесшими комбинированные и расширенные операции, в результате которых все же оставалась резидуальная опухоль, составили группу из 137 больных. То есть, паллиативными оказались 137 (23,6 %) операций из 581 вмешательства. Это составило 29,5 % по отношению к 464 оперированным больным. Паллиативными эти операции считались, поскольку не полностью были удалены первичная опухоль и/или регионарные метастазы (102 или 21,3 % наблюдений), а также в случаях наличия отдаленных метастазов (35 или 7,5 % наблюдений).
Клиническое обследование пациентов включало традиционные лабораторные и радиоиммунологические тесты. Ультразвуковое исследование выполнялось с использованием аппарата «Aloka - Echodiagnost», датчик 7,5 Мгц в 5-осевом режиме. Пациентам также выполняли обзорную рентгенографию органов шеи и средостения с контрастированием пищевода (при подозрении о врастании в него опухоли) или без него. В течение последних 10 лет применялась спиральная компьютерная томография на аппарате «Siemens Somaton Emotion», магнитно-резонансная томография с использованием аппарата «Siemens». Необходимость в этих исследованиях возникала примерно у каждого второго пациента. При подозрении на врастание опухоли в просвет трахеи и пищевода выполнялись фиброларингоскопия и фиброэзофагоскопия (57 или 12,3 % больных) с использованием эндоскопической аппаратуры фирмы «Olympus».
В обследованной группе больных местно-распространенным РЩЖ изучались непосредственные и отдаленные результаты хирургического лечения. Исследование носило проспективный характер. При оценке показателей выживаемости за точку отсчета принимали дату начала лечения (хирургическое вмешательство). Датой начала наблюдения считали 1.01.1973 г., датой окончания наблюдения – 31.12.2007 г. Подсчитывалось количество человеко-лет наблюдения, которое равнялось 7680,5. При этом, допускалось, что изменение когорты в каждом году наблюдения происходило равномерно (Двойрин В.В., 1975; Mantel N, Haenzel W., 1975).
Показатели выживаемости больных изучались в зависимости от следующих факторов:
- пол и возраст пациентов;
- гистологическое строение опухоли;
- состояние регионарных лимфатических узлов;
- наличие метастазов в лимфатических узлах средостения;
- анатомический вариант инвазии (прорастание различных окружающих структур первичной опухолью или регионарными метастазами);
- характер оперативного вмешательства.
Для установления прогностического значения различных факторов была сформирована контрольная группа. В нее вошли 400 больных дифференцированными формами РЩЖ, у которых опухоли не относились к местно-распространенным. Пациенты выбирались случайным методом и были оперированы в клинике в период с 1980 по 1990 гг. Первичная опухоль у больных контрольной группы соответствовала стадиям Т1-Т3 (при стадии Т3 выбирались только те больные, у которых опухоль не прорастала короткие мышцы шеи). У 107 (26,8 %) больных контрольной группы имелись регионарные метастазы в шейных лимфатических узлах, соответствующие стадии N1a – то есть, ситуации, не требующие расширенных хирургических вмешательств (одностороннее поражение, отсутствие инвазии окружающих тканей, отсутствие поражения медиастинальных лимфатических узлов).
Соотношение мужчин и женщин в контрольной группе соответствовало таковому в основной группе – 1 : 3 (100 или 25,0 % мужчин и 300 или 75,0 % женщин). Возраст больных колебался от 14 до 79 лет (в среднем 55,2 ± 2,6 г.), что также соответствовало показателям в основной группе. Статистическая обработка данных производилась с помощью компьютера на базе Intel Celeron и прикладной программы STATISTICA for Windows версия 6.0.
Возможности диагностики степени распространения РЩЖ.
В анализируемой группе 464 больных местно-распространенным РЩЖ жалобы пациентов и физикальные данные были в основном неспецифичны (табл. 3). У большинства пациентов наблюдалось опухолевидное образование на передней поверхности шеи, ограничено подвижное или несмещаемое. О выходе опухоли за пределы органа можно было достоверно судить при изъязвлении кожи, однако, таких наблюдений было немного. В обследованной группе в основном использовался общепринятый комплекс различных диагностических методов, однако, многие из них не позволяли установить степень и характер распространенности новообразования. Для оценки точности диагностических исследований при местно-распространенном РЩЖ использовался метод построения четырехпольных таблиц (Altman D.G., Bland J.M., 1994). В качестве контроля оценены результаты дооперационного и послеоперационного обследования 400 больных, у которых карцинома ЩЖ не относилась к категории местно-распространенной.
Таблица 3
Жалобы больных местно-распространенными опухолями (464 пациента)
| Жалобы | Число наблюдений | |
| Абс. | % | |
| Опухолевидное образование на шее | 424 | 91,3 |
| Затруднение дыхания | 212 | 45,7 |
| Дисфагия | 133 | 28,7 |
| Дисфония или афония | 167 | 36,0 |
| Синдром верхней полой вены | 119 | 25,6 |
| Кровохарканье | 26 | 5,6 |
| Изъязвление на шее | 8 | 1,7 |
Примечание: Число наблюдений превышает количество больных, поскольку у ряда пациентов отмечалось несколько жалоб.
Ультразвуковое исследование выполнено 379 (81,7 %) пациентам. Этот метод оказался малоэффективным в установлении местного распространения опухоли. Относительно низкие разрешающая способность и различие эхографической плотности соседних структур не позволяли при сонографии отчетливо установить факт прорастания опухоли во внетиреоидные структуры шеи, степень распространения новообразования за грудину. Также при ультразвуковом исследовании была малодоступна для визуализации область средостения. При оценке информативности ультразвукового исследования с помощью четырехпольной таблицы чувствительность метода оказалась невысокой – 20,8 %, специфичность эхографии составила 74,5 %.
Рентгенография шейно-загрудинного пространства с контрастированием пищевода выполнена 447 (96,3 %) пациентам основной группы. В большинстве наблюдений этот метод позволял лишь установить степень распространения опухоли за грудину и наличие компрессии органов шеи и средостения. Визуализация пространства ниже верхней грудной апертуры была преимуществом рентгенологического метода перед ультразвуковым исследованием. Вместе с тем, рентгенография обладала более низкой разрешающей способностью и чрезвычайно малыми различиями в рентгенологической плотности между нормальными и опухолевыми тканями. Наличие инвазии опухолью окружающих органов и тканей при рентгенографическом исследовании установить было практически невозможно. Чувствительность рентгенографии в установлении выхода опухоли за пределы органа была очень низка и составила 10,5 %. О специфичности метода судить было невозможно, поскольку в контрольной группе ни в одном из наблюдений не было высказано предположения о местном распространении новообразования.
Радиоизотопные методы исследования применялись у 105 (22,6 %) больных «запущенным» РЩЖ. В последние десятилетия традиционные методики сцинтиграфии практически не использовались у пациентов с узловыми новообразованиями в ЩЖ. Современные методики с применением различных туморотропных препаратов использовались редко в связи с высокой стоимостью исследований. Традиционное радиоизотопное сканирование позволяло лишь установить локализацию опухоли и степень распространения ее за грудину, в ряде случаев – наличие регионарных метастазов. Также как УЗИ и рентгенография, сканирование не позволяло судить о прорастании опухолью окружающих тканей, поскольку сцинтиграфия не визуализировала окружающие опухоль структуры и имела низкую разрешающую способность.
Компьютерная томография выполнена 132 (28,4 %) больным местно-распространенным РЩЖ. Данное исследование позволяло более точно определять наличие выхода опухоли за пределы органа. Относительно отчетливо выявлялась инвазия окружающих мышц, гортани и трахеи, пищевода, сосудисто-нервного пучка. Исследование позволяло установить наличие или отсутствие капсулы опухоли, метастатическое поражение лимфатических узлов шеи и средостения, уровень распространения опухоли за грудину, отсутствие границы между опухолью и окружающими тканями. Компьютерная томография была недостаточно информативна при относительно небольших размерах новообразования, при дифференциации инвазии и сдавления возвратных гортанных нервов. Чувствительность компьютерной томографии при диагностике местного распространения РЩЖ была равна 71,9 %, специфичность составила 80,0 %.
Магнитно-резонансная томография произведена 89 (19,2 %) больным «запущенным» РЩЖ. Высокая разрешающая способность и отчетливая дифференциация границ тканей обусловливали большую точность и информативность данного исследования по сравнению с компьютерной томографией. Чувствительность магнитно-резонансной томографии при диагностике местного распространения РЩЖ была равна 89,5 %, специфичность составила 90,4 %. Фиброэзофагоскопия выполнена 191 (41,2 %) пациенту, фиброларингоскопия – 114 (24,6 %) больным с местно-распространенными опухолями ЩЖ. Данные исследования производились при клинических признаках инвазии трахеи, гортани и пищевода. При поверхностных степенях инвазии перечисленных органов эндоскопические методы были недостаточно эффективны. Чувствительность фиброэзофагоскопии составила 52,3 %, фиброларингоскопии – 56,1 %. При этом исследования отличались высокой специфичностью – 90,0 % и 92,0 % соответственно.
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ
Комбинированные хирургические вмешательства у больных местно распространенным раком щитовидной железы.
Комбинированные операции выполнены 193 пациентам (исключая пациентов, у которых операции сочетали в себе расширенные и комбинированные – эти больные анализированы отдельно). Среди больных была 141 (73,1 %) женщина и 52 (26,9 %) мужчины. Соотношение мужчин и женщин равнялось 1:2,7. Возраст пациентов варьировал от 17 до 77 лет и в среднем составил 61,2 ± 3,7 г. У большинства (178 или 92,2 %) больных вмешательства производились в плановом порядке. В 15 наблюдениях (7,8 %) операции выполнены по неотложным и срочным показаниям. Более чем в трети случаев (40,4 %) первичная опухоль соответствовала градации Т3 согласно последней редакции классификации TNM (табл. 4) – то есть, наблюдалась инвазия ближайших окружающих мышц. В 51,3 % наблюдений первичные опухоли соответствовали градации Т4a. Более обширная инвазия (T4b) наблюдалась у 8,3 % пациентов.
Таблица 4
Стадии первичной опухоли по TNM у обследованных больных
| Стадия | Число наблюдений | |
| Абс. | % | |
| T3 | 78 | 40,4 |
| T4a | 99 | 51,3 |
| T4b | 16 | 8,3 |
| Всего | 193 | 100,0 |
У 121 (62,7 %) пациента до или во время операции выявлялись метастазы в шейных лимфатических узлах (табл. 5).
Таблица 5
Состояние регионарных лимфатических узлов у больных обследованной группы
| Стадия по TNM | Число наблюдений | |
| Абс. | % | |
| N0 | 72 | 37,3 |
| N1 | 90 | 46,6 |
| N1a | 31 | 16,1 |
| Всего | 193 | 100,0 |
В большинстве этих наблюдений одномоментно производилась шейная лимфаденэктомия – при условии переносимости вмешательства пациентом. В 11 (5,7 %) наблюдениях, у пожилых больных или пациентов, отягощенных тяжелой соматической патологией, операции выполнялись в два этапа – шейная лимфаденэктомия производилась через 2-3 месяца.
Наиболее часто необходимость в комбинированных операциях возникала при медуллярной карциноме – более чем у каждого четвертого пациента (29,6 %), при папиллярном и фолликулярном раке этот показатель составлял соответственно 7,5 % и 8,0 %. У абсолютного большинства пациентов наблюдалось распространение опухоли на ближайшие анатомические структуры (табл. 6) – мышцы шеи и трахею (соответственно 78,8 % и 36,2 %). Реже отмечалась инфильтрация возвратных нервов (24,3 %), еще реже – инвазия гортани, пищевода, кожи, сосудисто-нервного пучка шеи и сосудов средостения. В 154 наблюдениях (79,8 %) опухоль одновременно поражала два и более внетиреоидных анатомических образования.
Таблица 6
Органы и ткани, пораженные опухолью у обследованных больных
| Пораженный орган | Число наблюдений | Удельный вес среди 193 больных (%) |
| Прилежащие мышцы шеи | 152 | 78,8 |
| Мышцы гортани | 17 | 8,8 |
| Гортань | 36 | 18,1 |
| Трахея | 94 | 48,7 |
| Глотка и пищевод | 54 | 27,9 |
| Возвратные нервы | 47 | 24,3 |
| Сонная артерия | 9 | 4,6 |
| Сосуды шеи и средостения | 36 | 18,6 |
| Кожа с подкожной клетчаткой | 11 | 5,7 |
Примечание: Число наблюдений превышает количество больных, поскольку у ряда пациентов отмечалась инвазия нескольких внетиреоидных структур.
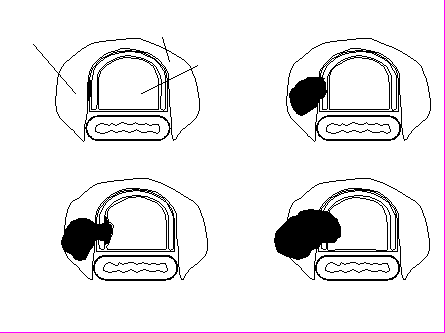
Нами предложено распространить классификацию H.Grillo (1992) и выделять четыре степени инвазии не только трахеи (рис. 1), но и других полых органов шеи – гортани и пищевода. При первой степени опухоль прорастает адвентициальный слой, при второй – опухоль проникает в хрящевой или мышечный слой, при третьей степени инвазия достигает подслизистой оболочки, и при четвертой степени опухоль достигает слизистого слоя и выходит в просвет органа. Схожие классификации разработаны и предложены H.Grillo (1992) и Y.Fujimoto с соавт. (1986) лишь для трахеи.
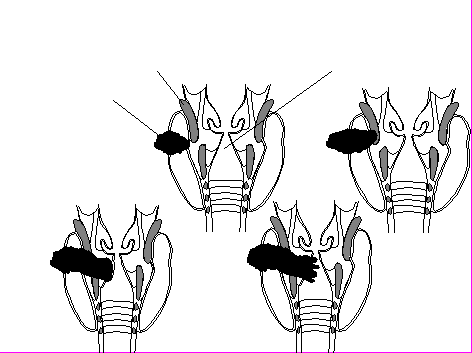
 Щитовидный хрящ Гортань
Щитовидный хрящ ГортаньОпухоль Щитовидная железа Опухоль
Трахея
I степень II степень
I II
III степень IV степень
III IV
а) б)
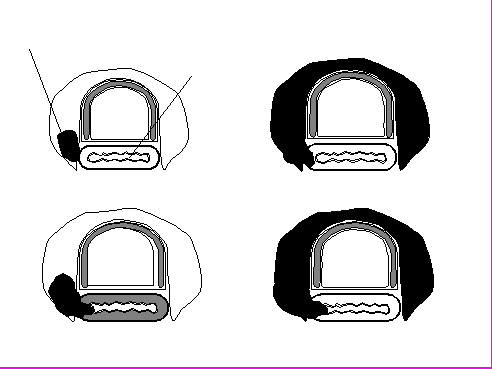
Опухоль
Пищевод
I степень II степень
III степень IV степень
в)
Рисунок 1. Применяемая в клинике классификация степени инвазии а.) трахеи (H.Grillo, 1992), б) гортани и в) пищевода опухолями ЩЖ.
В большинстве случаев (154 или 76,7 %) комбинированные операции были радикальными и у 39 (23,3 %) пациентов полностью удалить опухоль было невозможно. В таких случаях комбинированные операции носили паллиативный характер. У 15 (7,8 %) больных комбинированные вмешательства выполнялись в срочном порядке связи с выраженными расстройствами жизненно важных функций организма, в первую очередь – дыхания. При выраженном сдавлении дыхательных путей, особенно в неотложных ситуациях, интубацию трахеи удавалось выполнить только с помощью фиброэндоскопии.
Расстройства голоса и функции истинных голосовых складок наблюдалось у 43 (22,3 %) пациентов с распространенными карциномами. Причем, субъективные и объективные данные не совпадали в 10 наблюдениях – нарушение функции голосовых складок зарегистрировано лишь при ларингоскопии. В 36 из 47 (76,6 %) наблюдений инвазии опухолью возвратного нерва последний в ходе хирургических вмешательств был относительно легко отделен от опухоли. Это связано с тем, что вокруг опухоли отмечалась, так называемая, «псевдовоспалительная» инфильтрация, или же прорастание было поверхностным. В 11 наблюдениях инвазия возвратного нерва была глубокой и приходилось его резецировать. Во всех случаях резекция произведена на протяжении не более чем 2 см. Восстановление непрерывности нерва после мобилизации выполнено узловыми швами, у 9 больных отмечен положительный эффект через 6-17 месяцев. После прецизионного выделения скальпелем из опухоли 36 возвратных нервов у 29 (80,5 %) больных сохранилась их адекватная функция. При наблюдении в течение более чем 10 лет рецидив опухоли отмечен у 2 (2,9 %) пациентов, у которых возвратный нерв выделялся из опухоли, а не резецировался. Двое из них (в возрасте более 50 лет) погибли вследствие продолженного роста и генерализации фолликулярного «йоднегативного» и медуллярного РЩЖ.
В последнее десятилетие для контроля и сохранения нейропроводящих структур использовался электрофизиологический метод – мониторинг (электронейромиография) возвратного и добавочного нервов. Для идентификации нервных структур шеи при первичных, повторных операциях на ЩЖ и регионарном лимфатическом аппарате шеи, в том числе, с восстановлением возвратных нервов использовался комплект аппаратуры «Nerve Integrity Monitor 2TM» «Xomed Trace». Данный метод основан на регистрации потенциала действия с области голосовых или трапециевидных мышц, вызванного электростимуляцией возвратного или добавочного нервов. Методика апробирована и исследована в клинике (Романчишен Ф.А., 2007), защищена авторским свидетельством № 2006103841/22(004186). После интубации больного и правильной установки трубки в трахее на экране монитора регистрировалась кривая пассивной миографии голосовых связок – потенциал покоя. При стимуляции нерва электродом на экране монитора появлялась характерная кривая, отражающая колебания потенциала действия. Электростимуляцию осуществляли путем непосредственного контакта стимуляционного электрода со стволом искомого нерва (Романчишен А.Ф. и соавт., 2004). Технические особенности операций в последние годы определялись установленными в результате исследований (Романчишен Ф.А., 2007) точками надежной идентификации возвратного нерва. Оптимальным местом начала диссекции нижнего гортанного нерва признан участок трахеопищеводной борозды в надключичной области с дальнейшим выделением нерва снизу вверх. Важным достоинством методики была возможность проверки сохранности нерва в конце операции. Электронейромиография у больных РЩЖ позволяла адекватно иссекать опухоль, инвазировавшую область расположения нервов, а также претрахеальную и паратрахеальную клетчатку с лимфатическими узлами. При иссечении нерва на небольшом протяжении (1,0 – 2,0 см) в связи с врастанием в него РЩЖ концы пересеченных нервов были соединены периневральным швом, нитью 6-0, под оптическим увеличением. Проводимость линии анастомоза проверена с помощью нейромонитора. При стимуляции возвратного гортанного нерва каудальнее линии шва на экране монитора отмечена слабая электрическая активность у каждого из 9 больных. Типичные сокращения мышц гортани при этом отсутствовали. В дальнейшем больные получали нейротропную терапию. Отдаленный результат исследован через 1 – 2 года у 11 больных. Подвижность голосовой связки на стороне нейрорафии восстановилась у 9 больных. Отдаленный результат у двух пациентов неизвестен.
При дооперационных эндоскопических исследованиях гортани, трахеи и пищевода распространение опухоли до слизистой оболочки включительно было обнаружено в 7 наблюдениях (женщины в возрасте 25, 27, 38, 44 и 54 лет). В 5 из них ранее уже предпринимались неудачные попытки хирургического, лучевого и медикаментозного лечения. Но РЩЖ рецидивировал и прогрессировал, вызывая нарушение проходимости дыхательных путей и верхних отделов пищеварительного тракта. У 2 наиболее молодых пациенток была выполнена циркулярная резекция инвазированных опухолью шейных отделов трахеи и пищевода с последующей пластикой последнего кожными лоскутами и полной трахеостомией. Местные изменения тканей на шее после наружного облучения не позволяли использовать для пластики пищевода фрагмент кишки. Пациентки прожили после операций 4,5 и 2,5 года и погибли вследствие генерализации опухолевого процесса. Третьей пациентке, 38 лет, после курса дистанционной лучевой терапии произведена циркулярная резекция гортани и шейных отделов трахеи и пищевода в связи с рецидивом низкодифференцированного папиллярного РЩЖ. Послеоперационный период осложнился формированием свища глотки. После его устранения проведены два курса терапии радиоактивным йодом. Больная продолжила работу в качестве фармацевта и прожила после повторной операции более 5 лет. Двум другим больным (44 и 54 лет) распространенным папиллярным РЩЖ с инвазией всей толщи стенки гортани ранее были предприняты попытки тиреоидэктомии вместе с органосохраняющими боковыми резекциями хрящей гортани и лимфаденэктомиями. В опухолях отсутствовал захват радиоактивного йода, поэтому проводились курсы дистанционного облучения. Через 2 и 3 года выявлены рецидивы рака в стенках гортани, в связи с чем произведены ларингэктомии. Продолжительность жизни пациенток после повторных операций составила соответственно 5 и 6 лет. Вторая пациентка погибла от генерализации РЩЖ, первая – вследствие развития внетиреоидной опухоли (рак яичников).
Еще один пациент 53 лет с папиллярной карциномой перенес удаление гортани с тремя верхними кольцами трахеи в связи с прорастанием опухолью всех слоев этих органов. В настоящее время больной живет без признаков рецидива 10 лет, проводится лишь заместительная терапия левотироксином. Больная 57 лет, с папиллярной карциномой верхнего полюса правой доли ЩЖ, врастающей в гортань, оперирована в клинике дважды. Первоначально выполнена тиреоидэктомия с центральной и боковой лимфаденэктомией и органосохраняющая резекция правой полвины гортани и глотки. Проведена послеоперационная лучевая терапия. Через год после лечения выявлен рецидив опухоли. Повторная операция – ларингэктомия. Через 6 лет произошла генерализация процесса, ставшая причиной смерти пациентки.
Таблица 7
Степень инвазии полых органов шеи и средостения опухолями ЩЖ
| Пораженный орган | I –III степень инвазии (до подслизистого слоя) | IV степень (до слизистой оболочки, проникновение в просвет органа) | ||
| Абс. | % | Абс. | % | |
| Трахея | 88 | 51,8 | 6 | 42,8 |
| Гортань | 32 | 18,8 | 4 | 28,6 |
| Пищевод | 50 | 29,4 | 4 | 28,6 |
| Всего | 170 | 100,0 | 14 | 100,0 |
Таблица 8.
Характер хирургических вмешательств при инвазии полых органов шеи
| Пораженный орган | Характер операции (число наблюдений) | ||
| Органосохраняющая (бреющая) операция | Окончатая (боковая) резекция | Циркулярная резекция | |
| Трахея (94) | 83 (88,3 %) | 5 (5,3 %) | 6 (6,4 %) |
| Гортань (36) | 28 (77,8 %) | 4 (11,1 %) | 4 (11,1 %) |
| Пищевод (54) | 50 (92,6 %) | _ | 4 (7,4 %) |
| Всего (184) | 161 (83,4 %) | 9 (4,9 %) | 14 (8,7 %) |
Примечание: В случае прорастания гортани под циркулярными резекциями подразумевалась ларингэктомия.
Инвазия полых органов шеи (трахеи, гортани, пищевода) I-III степени (до подслизистого слоя органов) наблюдалась у большинства пациентов – 184 наблюдений (табл. 7). Степень инвазии определялась макроскопчески во время операции, в случае резекций органов – подтверждалась при послеоперационном гистологическом исследовании. При I и II степенях инвазии операции были органосохраняющими (табл. 8). При III степени инвазии производились боковые резекции органов, что имело место в 9 наблюдениях. Этим больным выполнены окончатые резекции гортани и трахеи. Дефект в стенке органа укрывался близлежащими мышечными тканями. При IV степени инвазии (в этих случаях всегда наблюдалось поражение органа более чем на треть диаметра) производились циркулярные резекции трахеи (6 наблюдений), пищевода (4 наблюдения), ларингэктомии (4 наблюдения). Технические детали этих операций не отличались существенно от общепринятых соответствующих вмешательств. После удаления гортани формировалась постоянная трахеостома. При глубокой инвазии трахеи во всех случаях потребовалась резекция не более чем трех ее колец. Во всех случаях произведено сшивание концов трахеи отдельными узловыми швами с наложением временной разгрузочной трахеостомы. Глубокая инвазия пищевода в продольном направлении не превышала 4 см. Операция завершалась гастростомией. Окончатых резекций пищевода в наших наблюдениях не было, при прорастании опухоли до мышечного слоя органа производилось ее иссечение с сохранением слизистой оболочки и ушиванием дефекта мышечной оболочки. В некоторых случаях дальнейшее лечение включало лучевую терапию. При папиллярном и фолликулярном РЩЖ, как правило, применялся радиоактивный йод. Реже использовалось наружное облучение (9,8 %) при дифференцированных формах РЩЖ и в 37,1 % наблюдений - при медуллярной карциноме.
С точки зрения онкологической адекватности результаты органосохраняющего, по отношению к инвазированным опухолью ЩЖ соседним органам, хирургического лечения РЩЖ не уступали таковым после циркулярных (обширных) резекций органов (после первых число рецидивов 11,5%, после вторых – 18,5%, послеоперационная летальность составила 11,5% и 18,5% соответственно). У 18 (7,0 %) больных были обнаружены отдаленные метастазы в костях, легких и головном мозге, в связи, с чем операция признана паллиативной. В 25 (9,8 %) наблюдениях, несмотря на большой объем комбинированных резекций ЩЖ, имел место продолженный рост опухолей в стенках полых органов и лимфатических узлах шеи. Проводилась ТТГ-супрессивная и химиолучевая терапия.
В 36 (18,6 %) наблюдений карцинома ЩЖ инвазировала, помимо мышц, гортани и пищевода, крупные сосуды шеи и средостения. Как правило, это были глубокие яремные, подключичные и плечеголовные вены. Истинная инвазия на всю глубину стенки крупных артерий наблюдалась редко (9 или 4,7 % наблюдения). Как правило, удавалось отделить опухоль, частично с адвентициальной оболочкой артерии, а не резецировать ее. Пластическое замещение глубоких яремных вен не требовалось даже при двухсторонних резекциях – постепенная компрессия опухолью этих сосудов приводила к развитию выраженной сети коллатералей, которая обеспечивала достаточный венозный отток. Безопасное и надежное удаление карцином, распространившихся на сосуды и органы средостения в ряде случаев было возможно лишь после частичной продольно-поперечной или продольной стернотомии до уровня 3 или 4 межреберий (5 или 2,0 % наблюдений). У 11 пациентов из группы высокого операционного риска вмешательства были разделены на два этапа – через 2-3 месяца после комбинированного удаления первичной опухоли выполнялась расширенная лимфаденэктомия или после комбинированной операции с односторонней шейной диссекцией производилась лимфаденэктомия с другой стороны. Все эти больные удовлетворительно или хорошо переносили хирургические вмешательства. Случаев послеоперационной летальности не наблюдалось.
Расширенные хирургические вмешательства у больных РЩЖ
Расширенные операции, включающие лимфаденэктомии в объеме, превышающем традиционные схемы (то есть, двухсторонние и\или медиастинальные лимфаденэктомии), выполнены 169 пациентам (пациенты, перенесшие расширенно-комбинированные вмешательства рассматривались отдельно). В эту группу входили больные с опухолями, соответствующими градациям Т1-3 N1b. Среди больных было 130 (77,0 %) женщин и 39 (23,0 %) мужчин. Соотношение мужчин и женщин равнялось 1 : 3,3. Средний возраст пациентов колебался от 13 до 74 лет и в среднем составил 53,7 ± 2,6 г. Чаще всего расширенные вмешательства требовались больным медуллярной карциномой (табл. 9) – почти в каждом пятом наблюдении. Намного реже расширенные вмешательства выполнялись при фолликулярном и папиллярном раке. Так, среди пациентов с медуллярной карциномой необходимость в расширенных операциях отмечена в 18,3 % наблюдений, при фолликулярном раке такие вмешательства потребовались 6,3 %, а при папиллярной карциноме – 7,6 % больных.
Таблица 9
Гистологическая структура опухолей, при которых выполнялись
расширенные операции в период 1973-2007 гг.
| Морфологические формы опухолей | Количество расширенных операций | Удельный вес среди больных данной формой РЩЖ |
| Папиллярный рак (1311) | 99 | 7,6 % |
| Фолликулярный рак (646) | 41 | 6,3 % |
| Медуллярный рак (158) | 29 | 18,3 % |
| Всего (2115) | 169 | 8,0 % |
Среди 1651 пациента с опухолями, не относящимися к местно-распространенным (стадии Т1-Т3), метастазы в регионарных лимфатических узлах обнаруживались в 348 (21,1 %) наблюдениях. При «запущенных» РЩЖ частота метастатического поражения лимфатических узлов шеи и средостения была почти в 2,5 раза больше и составила 50,3 % (233 случая у 464 больных). По мере увеличения степени распространения первичной опухоли возрастала частота и обширность регионарного метастазирования (табл. 10). Так, больные со стадией первичной опухоли Т1 составили всего лишь 2,9 % наблюдений, а более двух третьих представлено опухолями градации Т3.
Таблица 10
Стадии первичной опухоли по TNM в обследованной группе
| Стадия | Число наблюдений | |
| Абс. | % | |
| T1 | 15 | 2,9 |
| T2 | 47 | 27,8 |
| T3 | 107 | 69,3 |
| Всего | 169 | 100,0 |
У большинства больных (154 наблюдения или 91,1 %) операции были радикальными, и лишь у каждого десятого пациента не удавалось полностью удалить метастазы или первичную опухоль. В группу паллиативных операций также включены 18 наблюдений, где выявлялись отдаленные метастазы. Большая часть расширенных вмешательств была представлена двухсторонними лимфаденэктомиями (154 или 91,1 % наблюдений), в остальных 15 наблюдениях производились медиастинальные лимфаденэктомии в сочетании с боковым шейными диссекциями (табл. 11). Случаев изолированного поражения лимфатических узлов средостения без наличия метастазов на шее в обследованной группе не было.
Таблица 11.
Виды расширенных хирургических вмешательств
| Вид операции | Число наблюдений | |
| Абс. | % | |
| Двухсторонняя шейная лимфаденэктомия и тиреоидэктомия | 154 | 91,1 |
| Медиастинальная лимфаденэктомия и односторонняя шейная диссекция, тиреоидэктомия | 11 | 6,5 |
| Медиастинальная лимфаденэктомия и двухсторонняя шейная диссекция, тиреоидэктомия | 4 | 2,4 |
| Всего | 169 | 100,0 |
В большинстве наблюдений для хирургической эрадикации опухолей и регионарных метастазов при расширенных операциях применялся шейный доступ. В последние два десятилетия для шейной лимфаденэктомии в клинике стал применяться зигзагообразный разрез кожи (рис. 2). Такой доступ в большей степени, по сравнению с вертикальным, соответствовал линиям Лангера на шее и передней поверхности груди, что практически во всех случаях обеспечивало хороший косметический результат. Данная методика зигзагообразного кожного разреза разработана в клинике (Романчишен А.Ф., 1992) и защищена авторским свидетельством № 103847201/ 44(003587).
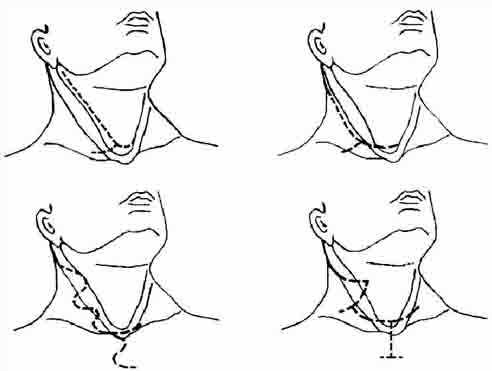
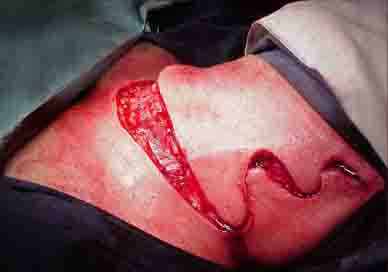
Рисунок 2. Доступы для шейной и медиастинальной лимфаденэктомии, применявшиеся в клинике.
В 15 (8,9 %) случаев при расширенных операциях потребовалось использование стернотомии. В случаях частичной продольно-поперечной стернотомии хирургическое вмешательство начиналось с разреза Микулича на 1 см выше яремной вырезки грудины. Вертикальный разрез кожи проводился по средней линии грудины до 2 или 3 межреберья. Далее кожа рассекалась в поперечном направлении на уровне одного из указанных межреберий до парастернальных линий, послойно рассекались мышцы и надкостница, последняя сдвигалась распатором в продольном и поперечном направлениях. Следующим этапом было выделение и перевязка внутригрудных артерий и вен на уровне 2 или 3 межреберья, что потребовалось в 2/3 наблюдений. В ряде случаев сосуды были сохранены, по крайней мере, с одной стороны, так как проходили латеральнее парастернальной линии, и не препятствовали пересечению грудины в поперечном направлении. Грудина пересекалась в поперечном направлении пилой Джигли, которая проводилась за грудиной зажимом Фёдорова. Вслед за этим, грудина рассекалась в продольном направлении при помощи стернотома. Трудности возникали при повторном рассечении грудины в связи с рецидивами опухоли или метастазов при РЩЖ, что имело место у (4) больных. Края рассечённой грудины разводились лестничным грудным ранорасширителем, при этом, особое внимание уделялось сохранению медиастинальной плевры. При повреждении медиастинальной плевры накладывались швы для герметизации плевральных полостей. Рассекалась внутригрудная фасция, ревизовались сосуды (плечеголовная вена и артериальный ствол, аорта, полая вена), органы средостения (трахея, пищевод, предсердие), удалялись опухоли из переднего и заднего отделов средостения под визуальным контролем блуждающих, возвратных и диафрагмальных нервов. Осуществлялся контроль герметичности медиастинальной плевры с помощью раствора фурациллина, которым заполнялось средостение. Грудина сшивалась двойной капроновой нитью № 5, отверстия в грудине наносились шилом. Загрудинное пространство дренировалось через 2 или 3 межреберье полиэтиленовым дренажом диаметром не менее 10 мм с активной аспирацией, на 2-3 суток. В раннем послеоперационном периоде (сразу после операции и через 1-2 суток) осуществлялось контрольное рентгеновское исследование грудной клетки с целью исключения пневмоторакса. Повреждение медиастинальной плевры отмечалось у 3 пациентов. Послеоперационные пневмонии возникли у 4 больных. Осложнений в виде остеомиелита, патологической подвижности краёв грудины не наблюдалось.
Преимущества продольно-поперечной стернотомии заключались в наиболее высоких клинико-анатомических критериях, рекомендованных для оценки хирургических доступов А.Ю. Созон-Ярошевичем (1954). Экспериментальное исследование, проведенное на трупах (17 операций) показало, что глубина стернотомической раны составила в среднем 7,9 см, угол операционного действия - 690, угол наклонения оси операционного действия - 770, зона доступности - 63 см2. Частичное, а не полное рассечение грудины сохраняло каркасную функцию грудной клетки, предупреждало патологическую подвижность грудины, тем самым обеспечивало лучшие условия для заживления операционной раны.
В последние десятилетия на передней поверхности грудной стенки в клинике также стал применяться зигзагообразный разрез кожи, без поперечного компонента. Эта деталь техники позволила улучшить косметический результат вмешательств. Кроме того, стало применяться частичное рассечение грудины без поперечного компонента или L-образная стернотомия. Отсутствие поперечного пересечения грудины снижало травматичность доступа и улучшало условия заживления раны, при этом, не уменьшая существенно размеры операционной раны и не изменяя угол операционного действия, угол наклонения оси операционного действия и зону доступности. Улучшалось течение послеоперационного периода, меньше был болевой синдром, быстрее отмечалась консолидация краев грудины. К недостаткам стернотомии следует отнести травматичность доступа, пересечение внутригрудных артерий. Применение этого доступа по указанным выше причинам должно быть всегда строго аргументировано.
Двухсторонняя шейная лимфаденэктомия сопряжена с опасностью повреждения нервных структур – добавочного, верхнего гортанного, подъязычного, диафрагмального, возвратного нервов, узлов симпатического ствола. Кроме того, при распространенных опухолях, в процессе операции велик риск повреждения сосудов – яремных и подключичных вен, сонных, подключичных и позвоночных артерий. Частота повреждений указанных образований очень зависит от опыта хирурга, производящего вмешательство. Внедренная в последнее десятилетие методика интраоперационного электрофизиологического мониторинга нервных структур значительно улучшила результаты лимфаденэктомий и позволила снизить частоту осложнений. Проведенные в клинике исследования (Романчишен Ф.А., 2007) определили особенности техники диссекции добавочного нерва. Оптимальным местом идентификации добавочного нерва признана область переднего края верхней трети грудино-ключично-сосцевидной мышцы. Дальнейшее выделение нерва целесообразно проводить сверху вниз, пересечение кивательной мышцы не требуется. Подобная техника в сочетании с электрофизиологическим мониторингом позволяла сохранить добавочный нерв и его ветви, несмотря на значительную анатомическую вариабельность. Важным преимуществом электрофизиологического мониторинга была также возможность проконтролировать целостность нервов в конце операции. За время использования интраоперационного мониторинга иссечение добавочного нерва в связи с врастанием в него опухоли выполнено 4 пациентам. Во всех случая произведена периневральная нейрорафия нитью 6-0, с оптическим увеличением. Проводимость анастомоза проверялась с помощью нейромонитора – во всех случаях зарегистрирована слабая электрическая активность. Отдаленные результаты у этих пациентов пока неизвестны.
Расширенно-комбинированные хирургические вмешательства выполнены 140 пациентам. В эту группу вошли пациенты со стадией опухоли ЩЖ Т4a-bN1b. Среди больных было 105 (75,0 %) женщин и 35 (25,0 %) мужчин. Соотношение мужчин и женщин составило 1:3, то есть практически не отличалось от таковых у пациентов, перенесших только комбинированные и только расширенные операции. Возраст больных колебался от 24 до 67 лет и в среднем составил 51,7 ± 2,3 г.
Таблица 12
Гистологическая структура опухолей, при которых выполнялись расширенно-комбинированные операции в период 1973-2007 гг.
| Морфологические формы опухолей | Количество расширенных операций | Удельный вес среди больных данной формой РЩЖ |
| Папиллярный рак (1311) | 69 | 5,2 % |
| Фолликулярный рак (646) | 43 | 6,7 % |
| Медуллярный рак (158) | 28 | 17,7 % |
| Всего (2115) | 140 | 6,6 % |
Среди всех больных, оперированных в клинике по поводу дифференцированного РЩЖ необходимость в расширенно-комбинированных операциях возникала в 6,6 % (табл. 12). Чаще всего такие вмешательства выполнялись при медуллярной карциноме – в 17,7 % наблюдений, и примерно в три раза реже при папиллярном и фолликулярном раке – соответственно 5,2 % и 6,7 %. Несмотря на значительную распространенность опухолевого процесса, операции были радикальными у75,7 % больных, что практически не отличалось от аналогичного показателя при комбинированных вмешательствах.
Таблица 13
Органы и ткани, пораженные опухолью у больных, перенесших расширенно- комбинированные операции (140 наблюдений)
| Органы и ткани | Число наблюдений | |
| Абс. | % | |
| Мышцы шеи | 131 | 93,6 |
| Трахея | 68 | 48,6 |
| Яремная вена | 35 | 25,0 |
| Пищевод | 29 | 20,7 |
| Гортань | 24 | 17,1 |
| Возвратный нерв | 9 | 6,4 |
| Добавочный нерв | 6 | 4,3 |
| Подчелюстная слюнная железа | 3 | 2,1 |
Примечание: число наблюдений превышает количество больных, поскольку в ряде случаев опухоль инвазировала несколько анатомических образований.
В группе расширенно-комбинированных операций, так же как и в группе комбинированных вмешательств, наиболее часто наблюдалось поражение первичной опухолью мышц шеи – 131 или 93,6 % случаев (табл. 13). Частота инвазии полых органов шеи (гортани, трахеи и пищевода) также практически не отличалась от показателей в группе комбинированных операций. Относительно часто (в каждом четвертом случае) отмечалось прорастание опухолью яремных вен, что требовало их резекции.
Таблица 14
Степень инвазии полых органов шеи и средостения опухолями ЩЖ при расширенно-комбинированных операциях
| Пораженный орган | I –III степень инвазии (до подслизистого слоя) | IV степень (до слизистой оболочки, проникновение в просвет органа) | ||
| Абс. | % | Абс. | % | |
| Трахея | 60 | 49,6 | 8 | 61,5 |
| Гортань | 22 | 18,2 | 2 | 15,4 |
| Пищевод | 26 | 32,2 | 3 | 23,1 |
| Всего | 121 | 100,0 | 13 | 100,0 |
Среди 134 наблюдений инвазии полых органов шеи, у большинства больных прорастание было неглубоким (I-III степень) -121 или 90,3 % (табл. 14). Органосохраняющие операции в отношении полых органов шеи и средостения удалось выполнить в 100 (82,6 %) из 121 наблюдениях. В 13 случаях произведены циркулярные резекции трахеи (8), пищевода (3) и ларингэктомии (2) – табл.15. В 8 наблюдениях производились окончатые резекции трахеи и гортани, наблюдений окончатых резекций пищевода не было. «Расширенный компонент» расширенно-комбинированных операций в большинстве наблюдений (129 или 92,1 %) был представлен двухсторонними боковыми шейными лимфаденэктомиями (табл. 16). У 11 пациентов расширенно комбинированные операции выполнялись с использованием трансстернального доступа, прием в двух случаях стернотомия понадобилась не только для удаления метастазов, но и для эрадикации первичной опухоли. Стернотомия, как правило, планировалась заранее на основании данных предоперационного исследования (рентгенография, компьютерная томография), свидетельствующих о распространении первичной опухоли на органы средостения и о наличии метастазов в лимфатических узлах средостения.
Таблица 15
Характер хирургических вмешательств при инвазии полых органов шеи при расширенно-комбинированных операциях
| Пораженный орган | Характер операции (число наблюдений) | ||
| Органосохраняющая операция | Окончатая резекция | Циркулярная резекция | |
| Трахея (68) | 55 ( 80,9 %) | 5 (7,3 %) | 8 (11,8 %) |
| Гортань (24) | 19 (79,2 %) | 3 (12,5 %) | 2 (8,3 %) |
| Пищевод (29) | 26 (89,6 %) | _ | 3 (10,4 %) |
| Всего (121) | 100 (82,6 %) | 8 (6,6 %) | 13 (10,8 %) |
Таблица 16
«Расширенный компонент» при расширенно-комбинированных операциях
| Вид операции | Число наблюдений | |
| Абс. | % | |
| Двухсторонняя шейная лимфаденэктомия и тиреоидэктомия | 129 | 92,1 |
| Медиастинальная лимфаденэктомия и односторонняя шейная диссекция, тиреоидэктомия | 9 | 6,4 |
| Медиастинальная лимфаденэктомия и двухсторонняя шейная диссекция, тиреоидэктомия | 2 | 1,5 |
| Всего | 140 | 100,0 |
Среди всех наблюдении комбинированных, расширенных и расширенно-комбинированных вмешательств у 74 (16,8 %) пациентов из группы «высокого операционного риска», а также в случаях обширного регионарного распространения (средостение и шея с двух сторон), расширенные операции выполнялись в два этапа. Из 83 пациентов (средний возраст 47,8 ± 1,1 г.), перенесших одноэтапные вмешательства по поводу обширного местного распространения РЩЖ, в раннем послеоперационном периоде погибли 4 (4,8 %). Причинами смерти были острый инфаркт миокарда или тромбоэмболия легочной артерии. В подгруппе из 74 пациентов (средний возраст 63,9 ± 0,9 г.), оперированных в два этапа, послеоперационная летальность отсутствовала, несмотря на более старший возраст (различие в возрасте статистически достоверно при р < 0,05).
В результате проведенных 548 комбинированных и расширенных операций эрадикация опухоли выполнена в 468 (85,4 %) наблюдениях. В раннем послеоперационном периоде погибли 7 (1,3 %) пациентов. Причинами смерти были острый инфаркт миокарда (2 наблюдения), острое нарушение мозгового кровообращения (1 пациент), тромбоэмболия легочной артерии (2 пациента), острая сердечно-сосудистая недостаточность (2 случая). В течение последних 20 лет число послеоперационных осложнений пи комбинированных и расширенных операциях в клинике уменьшилось на 50 %, и в настоящее время, в сумме, составляет 1,5 %. Снижению числа повреждений возвратных гортанных и добавочного нервов в значительной степени способствовало внедрение интраоперационной электрофизиологической визуализации нейропроводящих структур.
