Клинико-иммунологическое обоснование местной интерферонотерапии при респираторных вирусных инфекциях у детей 14. 01. 08 Педиатрия
| Вид материала | Автореферат |
- «Федерального агентства по здравоохранению и социальному развитию», 953.74kb.
- Клинико-диагностическое значение вазоактивных систем при нефропатиях у детей 14. 00., 332.22kb.
- Станицы ленинградской муниципального образования ленинградский район, 78.04kb.
- Диссертационные работы, выполненные в гоу впо тверская гма по специальности «педиатрия», 1153.49kb.
- Комплекс клинико-лабораторных симптомов и сопротивление дыхательных путей при рецидивирующем, 241.6kb.
- Клинико-патогенетические аспекты формирования церебральных нарушений при сахарном диабете, 838.38kb.
- Актуальные вопросы о гриппе и других острых респираторных инфекциях и их профилактике, 284.31kb.
- Адаптация недоношенных новорожденных детей при церебральной ишемии (клинико-функциональное, 394.95kb.
- Клинико-лабораторные особенности ротавирусной инфекции у детей и оптимизация терапии*, 73.79kb.
- Шаповаленко С. А., Рабинович Э. З. (Москва) комплексная терапия вагинального кандидоза, 24.05kb.
На правах рукописи
Курбанова Хадижа Ибрагимовна
КЛИНИКО-ИММУНОЛОГИЧЕСКОЕ ОБОСНОВАНИЕ МЕСТНОЙ ИНТЕРФЕРОНОТЕРАПИИ ПРИ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЯХ У ДЕТЕЙ
14.01.08 - Педиатрия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва - 2012
Работа выполнена в ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздравсоцразвития России
Научный руководитель: доктор медицинских наук, профессор
Захарова Ирина Николаевна
Научный консультант: доктор биологических наук, профессор
Малиновская Валентина Васильевна
Официальные оппоненты: Дегтярева Марина Васильевна
доктор медицинских наук, профессор
заведующая кафедрой неонатологии
факультета усовершенствования врачей
ГБОУ ВПО Российский национальный
исследовательский медицинский
университет имени Н. И. Пирогова
Минздравсоцразвития России
Зайцева Ольга Витальевна
доктор медицинских наук, профессор
заведующая кафедрой педиатрии
Московского Государственного Медико-
стоматологического университета.
Ведущая организация ФГБУ «Московский НИИ педиатрии и детской
хирургии Минздравсоцразвития России»
Защита состоится « 10 » апреля 2012 г. в 13 часов на заседании диссертационного совета Д.208.071.01 в ГБОУ ДПО Российская медицинская академия последипломного образования Минздравсоцразвития России (123955, г. Москва, ул. Баррикадная, д. 2/1).
С диссертацией можно ознакомиться в фундаментальной библиотеке ГБОУ ДПО Российская медицинская академия последипломного образования Минздравсоцразвития России (125445, г. Москва, ул. Беломорская, д.19).
Автореферат разослан "____" ____________________ 2012 г.
| Ученый секретарь диссертационного совета | Зыков В.П |
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Острые респираторные вирусные инфекции занимают ведущее место в структуре общей заболеваемости населения России и являются самой частой инфекционной патологией у детей. Ежегодно в Российской Федерации регистрируется около 25 млн. случаев заболеваний детей и подростков гриппом и ОРВИ [Баранов А.А. (2007, 2008)]. Лечение и профилактика респираторных инфекций у детей находятся в центре внимания педиатров, потому что на их долю, особенно в осенне-зимний период, приходится более 90% всех обращений за амбулаторной помощью [Таточенко В.К.(2004)]. Среди госпитализированных больных дети с данной патологией составляют 35% [Izurieta H.S. (2000)]. Острые респираторные вирусные инфекции занимают одно из ведущих мест в структуре детской и младенческой смертности, хотя эти заболевания излечимы [Ильина Е.С. (2004); Максимова Т.М. (2008); Greskevitch M.(2007)].
Несмотря на то, что заболевания респираторного тракта известны давно, существует много нерешенных проблем в их лечении [Феклисова Л.В. (2009); Чешик С.Г. (2005); Иванова В.В. (2006); Зайцева О.В (2007)]. Применение антибиотиков, химиотерапевтических и противовирусных препаратов может приводить к развитию вторичной «иммунологической недостаточности», сопровождающейся появлением новых устойчивых штаммов микроорганизмов [Малиновская В.В. (1999)]. В настоящее время в терапии острых респираторных заболеваний все чаще применяются препараты рекомбинантного интерферона альфа, в частности ВИФЕРОН. Показано, что противовирусные и иммуномодулирующие свойства ВИФЕРОНА в полной мере проявляются как при ректальном, так и при местном применении [Чеботарева Т.А. (2000); Гатич Р.З. (2004); Ершов Ф. И. (2006); Yu D.X. (2005); Chen Q. (2005); Дегтярева М.В. (2007); Chon T.W. (2010), Зайцева О.В (2011)].
В литературе есть сведения о профилактическом эффекте местной лекарственной формы препарата ВИФЕРОН, мазь в отношении ОРВИ при адаптации к детским организованным коллективам и в период эпидемического подъема гриппа и других ОРВИ у детей всех возрастных групп [Колобухина Л.В. (2004); Макарова Е.С. (2001); Малиновская В.В., (2004); Чеботарева Т.А. (2004); Saito H, (1985)]. Это свидетельствует о целесообразности клинического изучения эффективности местной лекарственной формы «ВИФЕРОН, мазь (интерферон человеческий рекомбинантный α-2β)» при лечении детей с острыми респираторными вирусными инфекциями.
Цель исследования: Оценить эффективность интраназального применения противовирусного и иммуномодулирующего препарата ВИФЕРОН, мазь в комплексной терапии детей раннего возраста с ОРВИ.
Задачи исследования
- Определить этиологическую структуру ОРВИ у наблюдаемых детей.
- Установить особенности местного иммунитета (уровни ИФН-, ИФН-, ИЛ-8, ФНО-, sIgA в назальных смывах) у детей, больных ОРВИ.
- Определить влияние интраназального применения ВИФЕРОН (мази) на состояние местного иммунитета (назальные смывы) при респираторных вирусных инфекциях.
- Оценить клиническую эффективность интраназального применения ВИФЕРОНа (мази) в комплексной терапии детей, больных ОРВИ.
- Оценить безопасность включения в комплексную терапию детей с ОРВИ противовирусного и иммуномодулирующего препарата ВИФЕРОН, мазь.
Научная новизна. Установлена этиологическая структура ОРВИ у ста детей раннего возраста. Уточнена частота, как моно- (риновирусной, аденовирусной, респираторно-синцитиальной и парагриппозной) так и смешанной вирусной инфекции.
Проведена оценка состояния местного иммунитета у больных ОРВИ (исследовались уровни ИФН-, ИФН-, ИЛ-8, ФНО-, sIgA в назальных смывах). Показано, что первые дни заболевания ОРВИ сопровождаются снижением в назальном секрете уровней ИФН-, ИФН- и sIgA с одновременным повышением уровней ИЛ-8 и ФНО-, что обуславливает необходимость проведения местной иммунокоррекции. В связи с недостаточной продукцией эндогенного ИФН-, которая характерна для детей раннего возраста, интраназальное введение экзогенного рекомбинантного ИФН- в виде препарата ВИФЕРОН, мазь, способствует элиминации вирусов со слизистой оболочки верхних дыхательных путей за счет его прямого противовирусного эффекта. Иммуномодулирующее действие препарата ВИФЕРОН, заключающееся в восстановлении цитокинового баланса, проявляется в облегчении клинического течения заболевания благодаря уменьшению катаральных явлений и лихорадки, в развитии которых значительную роль играют провоспалительные цитокины, в частности ФНО-.
Доказано, что интраназальное применение препарата ВИФЕРОН (мазь), в комплексной терапии детей с различными проявлениями ОРВИ приводит к значимому сокращению продолжительности основных клинических симптомов заболевания (интоксикации - на 10 часов, катаральных и респираторных симптомов - на 15 часов). Установлено, что интраназальное применение препарата ВИФЕРОН, мазь приводит к элиминации возбудителей, как при моно-, так и при микстинфекции, и препятствует внутрибольничному суперинфицированию.
Доказано, что клиническая эффективность местной виферонотерапии сопровождается изменениями цитокинового статуса в назальном секрете: продукция ИФН-, ИФН- и sIgA у больных ОРВИ в процессе лечения увеличивалась в 2 раза, что совпадало с элиминацией этиологически значимого вируса со слизистой носа.
Показано, что ВИФЕРОН, мазь является высокоэффективным средством для лечения ОРВИ у детей и его применение характеризуется высокой степенью безопасности.
Практическая значимость исследования. Интраназальное применение противовирусного и иммуномодулирующего препарата рекомбинантного интерферона α-2β ВИФЕРОН, мазь у детей с различными проявлениями ОРВИ оказывает положительное влияние на продолжительность основных клинических симптомов заболевания, сопровождается высокой безопасностью и позволяет повысить эффективность лечения, а также снизить риск внутрибольничного инфицирования.
Апробация работы. Апробация диссертации состоялась на совместном заседании кафедр педиатрии и детских инфекционных болезней ГБОУ ДПО РМАПО Минздравсоцразвития России, располагающихся на клинической базе - Тушинской детской городской больницы г. Москвы 26 декабря 2011 года.
Публикации. По теме диссертации опубликовано шесть работ, в т.ч. шесть - в журналах, рекомендованных ВАК РФ.
Внедрение результатов исследования. Результаты исследований внедрены в практическую деятельность Тушинской детской городской больницы г. Москвы. Основные положения работы включены в программу лекций, семинаров и практических занятий для специалистов, проходящих обучение на кафедре педиатрии ГБОУ ДПО Российская медицинская академия последипломного образования Минздавсоцразвития России.
Объем и структура диссертации. Диссертация изложена на 148 страницах машинописного текста и включает введение, обзор литературы, описание материалов и методов исследования, 6 глав, в которых изложены результаты собственных исследований и наблюдений, заключение, выводы, практические рекомендации и указатель литературы, включающий в себя 154 источника отечественных и 59 иностранных авторов. Работа иллюстрирована 21 рисунком и 30 таблицами.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования. Исследования проводили на базе 3-го инфекционного отделения (зав.отделением Короид Н.В.) Тушинской детской городской больницы города Москвы (главный врач – Куликова О.Е.).
С целью оценки эффективности интраназального применения противовирусного и иммуномодулирующего препарата ВИФЕРОН, мазь в комплексной терапии детей раннего возраста с ОРВИ наблюдались 100 больных респираторными вирусными инфекциями в возрасте от 1 года до 6 лет, среди них 57 мальчиков и 43 девочки. Все дети были госпитализированы в специализированное отделение для острой респираторно-вирусной инфекции в первые 48 часов от начала заболевания. Больные были разделены на две группы. Основную группу составили 60 детей, которые, помимо базисной терапии по поводу ОРВИ, получали препарат ВИФЕРОН (мазь). В группу сравнения вошло 40 больных, которые получали плацебо. Было проведено рандомизированное двойное слепое контролируемое исследование. Объем обследования включал общепринятые клинико-лабораторные, инструментальные, а также специальные методы исследования (табл. 1).
Объем проведенных исследований Таблица 1.
| Методы исследования | Количество | |
| 1 | Анамнез (заболевания, жизни, социальный, генеалогический) | 100 |
| 2 | Клинико-лабораторные исследования | 100 |
| 3 | Клинический анализ крови | 100 |
| 4 | Общий анализ мочи | 100 |
| 5 | Определение в назальных смывах методом ПЦР до лечения | 100 |
| 6 | Определение в назальных смывах методом ПЦР вирусных антигенов после лечения | 100 |
| 7 | Определение ИФН-, ИФН-, ИЛ-8, ФНО-, sIg A методом ИФА в назальных смывах до лечения | 100 |
| 8 | Определение ИФН-, ИФН-, ИЛ-8, ФНО-, sIg A методом ИФА в назальных смывах после лечения | 100 |
| Всего | 800 | |
Этиологическая расшифровка ОРВИ проводилась в лаборатории легионеллеза ГУ НИИ эпидемиологии и микробиологии им Н.Ф. Гамалеи РАМН (зав.лабораторией - д.м.н. Б.И. Маракуша) на основе индикации и идентификации вирусных антигенов и специфических антител к ним с помощью полимеразной цепной реакции (ПЦР) в назальных смывах. Выделение ДНК/РНК для исследования проводилось с использованием комплекта реагентов для выделения нуклеиновых кислот «Проба-НК» производства фирмы «НПФ ДНК-Технология» (Россия). Амплификация и детекция вирусной ДНК осуществлялась с использованием интеркалирующего красителя SYBR-green на амплификаторе для проведения ПЦР в реальном времени ICycler IQ фирмы «Bio-Rad» (США).
Оценка состояния местного иммунитета включала определение ИФН-, ИФН-, ИЛ-8, ФНО- и sIgA с использованием тест-систем ЗАО «Вектор-Бест» (г. Новосибирск). Исследование проводилось в лаборатории «Онтогенеза и коррекции системы интерферона» НИИЭиМ им. Н. Ф. Гамалеи РАМН (зав. лабораторией - д.б.н., проф. В. В. Малиновская).
Статистический анализ данных выполнялся с использованием пакета программ Statistica 6.1 (StatSoft, Inc., США) в соответствии с рекомендациями.
В зависимости от возраста пациенты получали препарат «ВИФЕРОН» или плацебо в следующих дозировках: детям от 1 года до 2-х лет 2500 МЕ (мазь, величиной с горошину диаметром 0,5 см) 3 раза в день, от 2-х до 6 лет 2500 МЕ (мазь, величиной с горошину диаметром 0,5 см) 4 раза в день, распределяя равномерно в оба носовых хода после промывания физиологическим раствором. Длительность терапии составила 5 дней.
Показатели местного иммунитета в назальных смывах исследовали дважды: в острый период заболевания (1–2 день болезни) и в период реконвалесценции (6–7 день болезни).
Критериями оценки терапевтической эффективности препарата являлись сроки и темпы обратного развития основных проявлений болезни (нормализация температуры, исчезновение симптомов интоксикации, катаральных и респираторных симптомов), динамика вирусологических и иммунологических показателей. Критериями переносимости явились возникновение нежелательных явлений, серьезных нежелательных явлений, их связь с приемом препарата.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При оценке тяжести ОРВИ установлено преобладание среднетяжелых форм заболевания – у 79% больных. По группам наблюдения распределение детей по тяжести заболевания было аналогичным: в основной группе - 80% больных, в группе сравнения – 77,5%, р>0,05. Тяжелые формы ОРВИ были диагностированы в 20% и 22,5% случаев (соответственно).
Наиболее часто у детей отмечался ларинготрахеит, который далее у многих из них переходил в круп. Явления ларинготрахеита имели место у 40%, а крупа – у 39% больных. Круп был диагностирован у 41,7% детей основной группы и у 35% детей группы сравнения ( р>0,05).
У одной трети – 30% больных ОРВИ выявлялись признаки фарингита: в основной группе – у 33,3% и в группе сравнения – у 25% детей. Различия не были статистически достоверными (р>0,05). Бронхообструктивный синдром развился у 10% больных. Ларингит и трахеобронхит отмечались у 2% и 3% детей (соответственно).
ОРВИ протекала без осложнений у 29% больных. Неосложненное течение заболевания наблюдалось примерно одинаково часто в основной группе – у 15 25% и в группе сравнения – у 35% больных (р>0,05). Тяжелые осложнения в виде пневмонии, бронхита и отита имели место в 13% случаев. В основной группе на долю этих больных приходилось 13,3%, а в группе сравнения – 12,5%. Следует отметить, что в основной группе преобладала пневмония (5% против 2,5%) и бронхит (6,7% против 5%), а в группе сравнения – отит (5% против 1,7%). Однако различия были достоверными только в отношении отита (р<0,05).
Таким образом, лечение больных ОРВИ проводилось на ранних сроках заболевания и наблюдаемые группы были равноценными по своей клинической характеристике, что является важным условием для получения достоверных результатов исследования.
При наблюдении в клинике оценивалась выраженность и длительность симптомов интоксикации и респираторного синдрома. Основные симптомы ОРВИ были связаны с общей интоксикацией организма (повышение температуры, снижение аппетита, вялость, бледность снижение двигательной активности) и поражением дыхательных путей (ринит, кашель, осиплость голоса, одышка, дыхательная недостаточность). Интоксикация у большинства пациентов проявлялась снижением аппетита – у 90% детей, вялостью – у 89%, бледностью – 89% больных и снижением двигательной активности – у 84%. Лихорадка отмечалась в 93% случаев.
Респираторный синдром с разной выраженностью его компонентов был зарегистрирован при поступлении в стационар у всех больных (100%).
Проявление воспаления слизистой носа отмечалось в виде отека (5%), слизистого ринита в большинстве случаев (94%), ринита с гнойным отделяемым (1%). Гиперемия ротоглотки имела место также во всех случаях (100%). У значительной части больных ОРВИ (88%) наблюдался кашель, который, в основном, характеризовал непродуктивное воспаление: сухой кашель был у 68%, малопродуктивный – у 12% и лающий – у 1 больного. У 7% детей кашель сопровождался отхождением мокроты и у 2 из них выслушивались влажные хрипы в легких. Одышка (чаще экспираторного характера) отмечалась у 22% больных.
Диагноз ОРВИ устанавливался на основании характерных клинических проявлений и эпидемиологических данных, а у 89% детей удалось уточнить этиологию заболевания: аденовирусная инфекция у 12,4%, парагриппозная инфекция – у 6,7%, РС инфекция – у 12,4%, риновирусная инфекция – 18%, смешанная инфекция – у 50,6% больных в различных сочетаниях. У 10% больных удалось доказать участие более 3-х возбудителей (табл. 2).
Вирусную природу заболевания по группам наблюдения удалось подтвердить с одинаковой частотой: в основной группе в 90%, в группе сравнения – в 87,5% случаев. Значимые различия наблюдались при сочетании различных вирусов (р<0,05).
Таблица 2
Этиологическая структура ОРВИ у больных детей (абс./%)
| Вирусы | Всего (n=100) | Основная группа (n=60) | Группа сравнения (n=40) | |||
| абс.ч | % | абс.ч | % | абс.ч | % | |
| Недифференцированное ОРВИ | 11 | 11,0 | 6 | 10,0 | 5 | 12,5 |
| Вирусы: | 89 | 89,0 | 54 | 90,0 | 35 | 87,5 |
| Моноинфекция: | 44 | 49,4 | 33 | 61,1 | 11 | 31,4 |
| Аденовирус | 11 | 12,4 | 8 | 14,8 | 3 | 8,6 |
| Парагрипп | 6 | 6,7 | 6 | 11,1 | - | - |
| РС вирус | 11 | 12,4 | 8 | 14,8 | 3 | 8,6 |
| Риновирус | 16 | 18,0 | 11 | 20,4 | 5 | 14,3 |
| Микстинфекция: | 45 | 50,6 | 21 | 38,9 | 24 | 68,6 |
| РС +Аденовирус | 7 | 7,9 | 2 | 3,7 | 5 | 14,3* |
| РС+Парагрипп | 6 | 6,7 | 5 | 9,3 | 1 | 2,9* |
| Парагрипп + аденовирус | 5 | 5,6 | 1 | 1,9 | 4 | 11,4* |
| РС +риновирус | 7 | 7,9 | 6 | 11,1 | 1 | 2,9* |
| Парагрипп +риновирус | 10 | 11,2 | 4 | 7,4 | 6 | 17,1* |
| РС+ Парагрипп+ аденовирус | 2 | 2,2 | - | - | 2 | 5,7 |
| Риновирус+РС+аденовирус | 3 | 3,4 | - | - | 3 | 8,6 |
| Парагрипп+риновирус+аденовирус | 5 | 5,6 | 3 | 5,6 | 2 | 5,7 |
* межгрупповые различия достоверны, р<0,05
В группе больных, получавших ВИФЕРОН (мазь), средняя продолжительность большинства симптомов интоксикации (вялость, бледность, двигательная активность) была меньше, чем у больных из группы, получавших плацебо – 2,46±1,1 суток против 2,97±0,9 суток, 3,14±0,5 суток против 3,73±1,05 суток и 2,65±1,0 суток против 3,22±1,15 суток, (соответственно). Менее различалась средняя продолжительность снижения аппетита.
Динамика других клинических симптомов ОРВИ (лихорадка, ринит, кашель, гиперемия зева) также происходила по-разному в группах наблюдения. Длительность лихорадки при течении ОРВИ составляла в основной группе - 2,75±0,4 суток, сравнения – 3,25±0,6 суток (р>0,05) (рис.1). Признаки ринита сохранялись продолжительнее, чем лихорадка. Средняя продолжительность ринита также была меньше у больных ОРВИ, в лечение которых был включен ВИФЕРОН, - 3,25±0,98 суток против 3,89±1,0 суток при использовании плацебо, хотя различия были недостоверными (р>0,05).
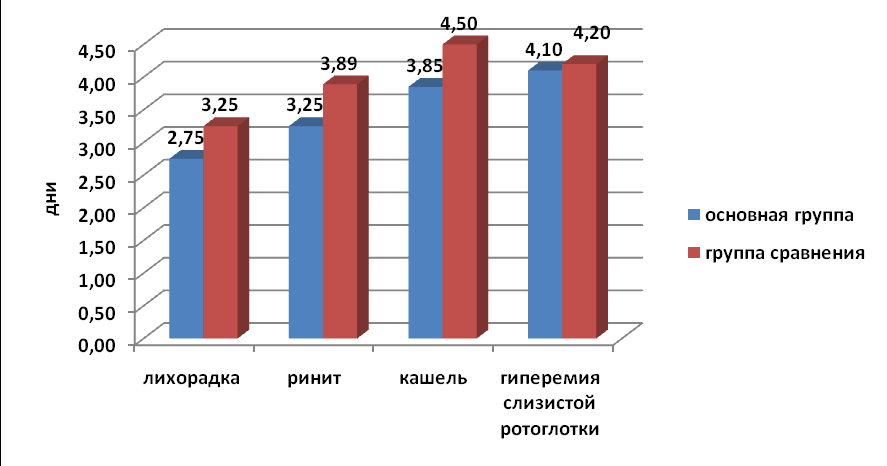
Рис. 1. Средняя продолжительность клинических симптомов у больных ОРВИ в динамике лечения (M±m, дни).
Более продолжительное время сохранялся кашель. Вместе с этим, при использовании ВИФЕРОНА (мази) его продолжительность, в среднем, составляла 3,85±1,1 суток, а при плацебо - 4,5±1,0 суток (р>0,05) (рис.1).
Менее всего ВИФЕРОН (мазь) оказывал влияние на среднюю продолжительность гиперемии в зеве. В основной группе детей продолжительность данного клинического симптома составляла 4,1±0,7 суток, в группе сравнения – 4,2±0,8 суток (р>0,05) (рис.1).
Влияние терапии ВИФЕРОНОМ на среднюю продолжительность респираторного синдрома выражалось в достоверном сокращении длительности сухого кашля – 1,25±0,14 суток в основной группе против 1,95±0,22 суток в группе сравнения (р<0,05). Кроме этого, достоверно быстрее отмечалась трансформация сухого кашля во влажный - 2,2±0,1 суток против 2,98±0,15 суток, соответственно (р<0,05), что в целом, облегчало общее состояние детей, купировался обструктивный синдром - 1,23±0,3 суток против 1,99±0,3 суток (р<0,05) (рис.2)
Особо следует отметить тенденцию положительного влияния препарата ВИФЕРОН на продолжительность осиплости голоса. Купирование данного симптома происходило на 15 часов быстрее, чем в группе сравнения. По средним показателям в основной группе больных продолжительность осиплости голоса была 2,3±0,23 суток и в группе сравнения - 3,0±0,24 суток, p>0,05.


 Рис. 2. Средняя продолжительность респираторных симптомов у больных ОРВИ в динамике лечения (M±m, дни).
Рис. 2. Средняя продолжительность респираторных симптомов у больных ОРВИ в динамике лечения (M±m, дни).Хотя различия не носят достоверный характер, все же это имеет большое практическое значение, так как осиплость голоса является одним из первых предвестников развития такого угрожающего для жизни состояния для детей раннего возраста, как круп.
Для оценки влияния лечения на элиминацию этиологически значимых вирусов из носоглотки оценивалось их исчезновение после терапии (табл. 3).
В основной группе элиминация вирусов была зарегистрирована в 85,2% случаев, в группе сравнения – в 37,1% случаев. Получены достоверные различия в элиминации этиологически значимых вирусов, как при варианте моно- (90,1% против 18,2%), так и при варианте микстинфекции (76,2% против 45,8%). В основной группе больных отмечалась полная (100%) элиминация адено- и РС-вирусов, в 83,3% случаев вирусов парагриппа и в 81,8% случаев риновирусов.
Таблица 3
Динамика вирусной контаминации у больных ОРВИ к 5 дню наблюдения (абс./%)
| Вирусы | Всего (n=100) | Основная группа (n=60) | Группа сравнения (n=40) | |||
| абс.ч | % | абс.ч | % | абс.ч | % | |
| Вирусы: | 89/59 | 66,3 | 54/46 | 85,2* | 35/13 | 37,1 |
| Моноинфекция: | 44/37 | 84,1 | 33/30 | 90,1 | 11/2 | 18,2 |
| Аденовирус | 11/9 | 81,8 | 8/8 | 100,0* | 3/1 | 33,3 |
| Парагрипп | 6/5 | 83,3 | 6/5 | 83,3* | - | - |
| РС вирус | 11/8 | 72,7 | 8/8 | 100,0* | 3/0 | 0,0 |
| Риновирус | 16/10 | 62,5 | 11/9 | 81,8* | 5/1 | 20,0 |
| Микст инфекция: | 45/27 | 60,0 | 21/16 | 76,2* | 24/11 | 45,8 |
| Суперинфицирование: | 36 | 36,0 | 13 | 21,7 | 23 | 57,5* |
| Аденовирус | 16 | 44,4 | 4 | 30,8 | 12 | 52,2* |
| Парагрипп | 9 | 25,0 | 3 | 23,1 | 6 | 26,1 |
| РС вирус | 6 | 16,7 | 3 | 23,1 | 3 | 13,0 |
| Риновирус | 5 | 13,9 | 3 | 23,1 | 2 | 8,7* |
* достоверные межгрупповые различия, p<0,05
У части детей обеих групп при исследовании смывов из носоглотки после проведенной терапии отмечено суперинфицирование. Значительно реже суперинфицирование отмечалось после терапии ВИФЕРОНОМ (мазью) - у 13 (21,7%) из 60 больных, нежели чем у детей, получавших плацебо – у 23 (57,5%) из 49 больных, р<0,05. Выраженный протективный эффект ВИФЕРОНА (мази) выявлен против аденовируса, контаминация данным вирусом происходила в 1,7 раза реже, чем в группе сравнения.
При исследовании уровней цитокинов в смывах со слизистой носа до начала лечения у подавляющего большинства больных ОРВИ – у 90% установлены низкие средние значения ИФН- (4,46±0,6 пкг/мл), ИФН- (4,26±1,16 пкг/мл) и повышенные уровни ИЛ-8 (528,0±158,4 пкг/мл) и ФНО- (26,97±5,5 пкг/мл). Уровень sIg A был снижен незначительно - 8,84±6,6 пкг/мл в общей группе, 8,04±6,8 пкг/мл и 9,64±8,4 пкг/мл по группам наблюдения.
Нами установлено, что при тяжелых формах заболевания отмечалось значительное угнетение выработки ИФН- (3,54±2,89 пкг/мл), ИФН- (3,08±2,1 пкг/мл) и sIg A (4,4±3,6 пкг/мл). Указанные нарушения регистрировались и при среднетяжелых формах ОРВИ, но они не были столь выраженными и достоверно отличались от таковых у тяжелых больных - ИФН- - 6,3±4,33 пкг/мл, ИФН- - 4,77±2,6 пкг/мл и sIg A - 9,75±9,9 пкг/мл (p<0,05). (рис.3)
Явления крупа различной степени тяжести и обструктивный синдром развивались на фоне значительного подавления продукции ИФН- и ИФН-. При крупе эти показатели интерферонового статуса составляли 3,54±2,8 пкг/мл и 3,0±2,11 пкг/мл, (соответственно), при обструктивном синдроме - 3,14±2,12 пкг/мл 2,79±1,55 пкг/мл, (соответственно). При указанных клинических формах ОРВИ значительно нарушалась выработка sIgA.
Рис.3. Показатели местного иммунитета у больных ОРВИ в зависимости от тяжести заболевания (М±m,пкг/мл)
В назальных смывах у больных крупом I-III ст. концентрация sIgA составляла 6,2±8,0 пкг/мл, у больных с проявлениями обструктивного синдрома - 6,6±9,2 пкг/мл. Подавление местного иммунитета при данных формах заболевания сопровождалось подъемом уровня ИЛ-8 - 656,3±172,2 пкг/мл и 690,47±95,2 пкг/мл, соответственно. Можно предположить, что на формирование интерферонового статуса при данных формах респираторного синдрома оказывает влияние тяжесть состояния.
Средние значения иммунологических показателей у детей при остром фарингите составили - ИФН- - 6,45±5,5 пкг/мл, ИФН- - 3,64±3,8 пкг/мл, ИЛ-8 - 528,7±156,3 пкг/мл, ФНО- - 26,66±15,3 пкг/мл и sIgA - 9,8±9,5 пкг/мл; при ларинготрахеите - ИФН- - 5,4±4,34 пкг/мл, ИФН- - 4,76±2,7 пкг/мл, ИЛ-8 - 492,19±144,3 пкг/мл, ФНО- - 24,55±15,3 пкг/мл и sIgA - 8,7±9,0 пкг/мл. Проведенные исследования показали, что на местный интерфероновый статус оказывает влияние присоединение бактериальных осложнений (пневмония, бронхит, отит и др). В первую очередь, это сказывается на выработке ИФН-, ИФН- и sIgA. Возможно, одновременное воздействие вирусов и микробов приводит к более глубоким нарушениям продукции интерферонов и иммуноглобулинов у больных с осложненным течением ОРВИ. При последних достоверно ниже, чем у больных с неосложненными ОРВИ, были уровни ИФН-, (3,5±4,7 пкг/мл, против 5,66±5,0 пкг/мл), ИФН- (2,3±2,2 пкг/мл против 4,66±3,3 пкг/мл) и sIgA (4,1±8,2 пкг/мл против 11,9±9,3 пкг/мл) (p<0,05). Более выраженное угнетение продукции интерферонов отмечалось при ОРВИ с установленной вирусной этиологией, чем при недифференцированном ОРЗ: ИФН-, (4,4±4,3 пкг/мл, против 7,43±5,4 пкг/мл), ИФН- (3,7±2,4 пкг/мл против 4,65±3,6 пкг/мл) и sIgA (8,8±6,3 пкг/мл против 10,6±9,6 пкг/мл), (p<0,05).
Показатели местного иммунитета у больных ОРВИ зависели от этиологии заболевания. Выявлена значительная недостаточность системы интерферона при аденовирусной и риновирусной инфекциях (при воздействии аденовируса продукция ИФН- составляла 4,60±0,5 пкг/мл, ИФН- - 3,3±1,05 пкг/мл и sIgA - 4,7±0,5 пкг/мл, при риновирусной инфекции 4,45±1,1 пкг/мл, 3,63±1,0 пкг/мл и 5,1±1,1 пкг/мл, соответственно). При сравнении интерферонового статуса при парагриппе и РС-вирусе также были выявлены различия. Показано, что РС-вирус оказывает более выраженное воздействие, чем вирус парагриппа, на уровень индуцируемой продукции α- и γ-интерферонов, а также секреторного иммуноглобулина А: ИФН-, - 6,43±2,0 пкг/мл, против 7,4±2,1 пкг/мл, ИФН- - 3,6±0,5 пкг/мл против 4,5±1,3 пкг/мл и sIgA - 6,5±1,1 пкг/мл против 10,8±3,1 пкг/мл, (p<0,05). (рис.4)
Таким образом, показатели местного иммунитета у больных ОРВИ зависят от тяжести и этиологии заболевания.
Рис.4 Динамика показателей местного иммунитета у больных ОРВИ в зависимости от этиологии возбудителя. (М±m,пкг/мл)
Проводилось изучение влияния лечения больных ОРВИ на показатели местного иммунитета. Выявленная клиническая эффективность местной виферонотерапии коррелировала с изменениями местного иммунитета, определяемого в назальных смывах у больных ОРВИ. Уровни α-ИФН у пациентов, получавших мазь ВИФЕРОН, увеличивались в 2,5 раза в динамике (с 4,31±0,47 пкг/мл до 10,75±2,34 пкг/мл) и достоверно отличалась в периоде реконвалесценции по сравнению с детьми, получавшими плацебо (5,91±1,8 пкг/мл и 6,79±2,58 пкг/мл, соответственно), (p<0,05).
Аналогичная ситуация отмечалась в отношении ИФН-. Его динамика была достоверной только в основной группе - с 4,26±1,16 пкг/мл до 9,75± 3,78 пкг/мл (p<0,05).
В группе сравнения хотя и отмечено повышение в назальных смывах уровня ИФН- с 2,98±0,2 пкг/мл до 3,56±0,86 пкг/мл, но указанные изменения не носили достоверный характер ( p>0,05).
В динамике ОРВИ у детей, получавших мазь ВИФЕРОН, концентрация ИЛ-8 в назальных смывах изменялась незначительно (с 506,13±165,7 пкг/мл до 458,13±161,8 пкг/мл (p>0,05), тогда как на фоне плацебо она достоверно увеличивалась (с 549,9±150,3 пкг/мл до 651,48±170,3 пкг/мл (p<0,05). Кроме этого, у детей, получавших мазь ВИФЕРОН, в динамике болезни значимо увеличивалась концентрация секреторного IgА (с 8,04±2,8 пкг/мл до 13,2±4,17 пкг/мл, p<0,05), которая оказалась достоверно более высокой в периоде реконвалесценции по сравнению с детьми, получавшими плацебо (с 9,64±3,4 пкг/мл до 10,29±3,79 пкг/мл, p>0,05).
* достоверные различия между показателями до- и после лечения, p<0,05
Рис. 5. Динамика показателей местного иммунитета у больных ОРВИ по группам наблюдения (M±m, пкг/мл)
Влияние местной виферонотерапии на концентрацию ФНО- в назальных смывах проявлялось в ее снижении с 25,30±6,4 пкг/мл до 9,86±3,84 пкг/мл, p<0,05. У больных ОРВИ, получавших плацебо, этот процесс был менее интенсивным (с 28,64±7,9 пкг/мл до 19,8±8,95 пкг/мл, p>0,05).
У больных ОРВИ основной группы увеличение средних показателей ИФН-, ИФН- и sIg A в назальных смывах было достоверно значимым по сравнению с таковыми в группе больных, получавших плацебо (рис. 5).
Так, средние значения ИФН- к 5 дню лечения ВИФЕРОНОМ, мазью увеличились на 6,44 пкг/мл, в группе сравнения на 0,88 пкг/мл (p<0,05). Соответственно, средние показатели ИФН- выросли на 5,49 пкг/мл и 0,58 пкг/мл, sIg A – на 5,16 пкг/мл и 0,65 пкг/мл (p<0,05).
Изменения показателей ИЛ-8 и ФНО-α характеризовались снижением на 48,0 пкг/мл и 15,44 пкг/мл. Причем эта разница достоверно отличалась от таковой в группе сравнения – 101,58 пкг/мл и 8,84 пкг/мл (p<0,05).
При использовании препарата ВИФЕРОН (мазь) у больных ОРВИ установлена его высокая переносимость, побочных явлений связанных с его применением отмечено не было.
ВЫВОДЫ
- У 100 обследованных больных ОРЗ дошкольного возраста вирусная этиология заболевания отмечена в 89% случаев. На долю риновирусной инфекции приходится 18%, аденовирусной и респираторно-синцитиальной инфекции по 12,4%, парагриппозной инфекции – 6,7%. Смешанная вирусная инфекция в различных сочетаниях выявляется в 50,6% случаев. У 10% больных ОРВИ доказано участие в воспалительном процессе более 3-х видов вирусов.
2. При исследовании состояния местного иммунитета в назальных смывах у больных ОРВИ обнаружены сниженные уровни ИФН-, ИФН- и sIgA – основных факторов, обуславливающих успешную борьбу организма с вирусной инфекцией и резистентность к повторному инфицированию. При этом у больных с ОРВИ отмечаются высокие уровни провоспалительного цитокина ФНО-, участвующего в развитии основных катаральных симптомов.
3. Доказано, что клиническая эффективность местной виферонотерапии сопровождается изменениями цитокинового статуса в назальном секрете: продукция ИФН-, ИФН- и sIgA у больных ОРВИ в процессе лечения увеличивалась в 2 раза, что совпадало с элиминацией этиологически значимого вируса со слизистой носа. Увеличение концентрации sIgА оказалось достоверно более высоким в периоде реконвалесценции по сравнению с детьми, получавшими плацебо.
4. Интраназальное введение ВИФЕРОНа (мази) в составе комплексной терапии детей с различными проявлениями ОРВИ приводит к более значимому сокращению продолжительности клинических симптомов заболевания (интоксикации, катаральных и респираторных симптомов), по сравнению с плацебо. Статистически достоверные различия отмечаются на 3-4 день лечения. При этом ВИФЕРОН (мазь) оказывает значимое влияние на среднюю продолжительность таких симптомов ОРВИ, как осиплость голоса, сухой кашель, обструктивные явления. Получены достоверные различия в элиминации вирусов как при моно-, так и при микстинфекции. ВИФЕРОН (мазь) препятствует внутрибольничному суперинфицированию (особенно аденовирусами).
5. ВИФЕРОН, мазь является высокоэффективным средством для лечения ОРВИ у детей. При использовании препарата ВИФЕРОН (мазь) установлена его высокая безопасность, отсутствие побочных явлений.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Рекомендуется включение противовирусного и иммуномодулирующего препарата ВИФЕРОН (мазь) интраназально в комплексную терапию детей с различными проявлениями ОРВИ в связи с его влиянием на продолжительность основных клинических симптомов заболевания (интоксикация, катаральные и респираторные симптомы) и высокой безопасностью.
- Необходимо учитывать, что у детей раннего возраста при ОРВИ отмечаются исходно низкие уровни ИФН-α в назальных смывах, что обосновывает необходимость лечения препаратом ВИФЕРОН, мазь.
- ВИФЕРОН (мазь) обладает протекторным действием в отношении повторной вирусной контаминации у больных ОРВИ, что можно использовать для предупреждения реинфицирования детей в условиях стационара и в организованных коллективах.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Захарова И.Н., Чебуркин А.В., Малиновская В.В., Торшхоева Л.Б, Курбанова Х.И., Паршина О.В., Гусева Т.С. Значение системы интерферонов в формировании иммунного ответа у детей с острыми респираторными вирусными инфекциями//Вопросы практической педиатрии.–2009.–Т. 4.-№5.–С.38-45.
- Чебуркин А.В., Торшхоева Л.Б, Курбанова Х.И. Особенности иммунореактивности детей раннего возраста в период репарации ОРЗ и профилактика рецидивов заболевания//Вопросы практической педиатрии.–2010.–Т.5.-№1.–С.39-43.
- Малиновская В.В., Захарова И.Н., Исаева Е.И., Торшхоева Л.Б., Курбанова Х.И., Короид Н.В., Глухарева Н.С. Этиологическая структура острых респираторных инфекций у детей раннего возраста//Вопросы практической педиатрии.-2010-Т.5-№5.-С.99-104.
- Малиновская В.В., Захарова И.Н., Коровина Н.А., Курбанова Х.И., Короид Н.В., Глухарева Н.С. Клинико-иммунологическое обоснование местной интерферонотерапии при респираторных вирусных инфекциях у детей. //Вопросы практической педиатрии.–2011.–Т. 6.-№5.–С.21-26.
- Малиновская В.В., Коровина Н.А., Зайцева О.В., Паршина О.В., Чеботарева Т.А., Гусева Т.С., Курбанова Х.И., Локшина Э.Э. Современные возможности использования интерферонов в комплексной терапии острых респираторных инфекций у детей//«Лечащий врач» - 2011. №8. с.116-119.
- Малиновская В.В., Коровина Н.А., Захарова И.Н., Заплатников А.Л., Чеботарева Т.А., Выжлова Е.Н., Курбанова Х.И., Глухарева Н.С., Короид Н.В., Торшхоева Л.Б. Модифицированная интерферонотерапия острых респираторных инфекций у детей раннего возраста: патогенетическое обоснование и эффективность//Российский вестник перинатологии и педиатрии. 2011.-N 3.-С.49-54.
ПЕРЕЧЕНЬ УСЛОВНЫХ ОБОЗНАЧЕНИЙ
ДНК | - дезоксирибонуклеиновая кислота |
ИЛ | - интерлейкин |
ИФН | - интерферон |
| ОРВИ | - острая респираторная вирусная инфекция |
ПЦР | - полимеразная цепная реакция |
РНК | - рибонуклеиновая кислота |
ФНО-α | - фактор некроза опухоли-α |
sIgA | - секреторный иммуноглобулин А |
| | |
