Концепция современного естествознания Глава 1: Предмет естествознания
| Вид материала | Документы |
- Н. И. Константинова концепции современного естествознания учебное пособие, 2191.08kb.
- Экзаменационные вопросы по дисциплине «концепции современного естествознания» Структура, 33.61kb.
- В. М. Найдыш Концепции современного естествознания, 8133.34kb.
- Концепции Современного Естествознания, 274.86kb.
- Учебно-методический комплекс дисциплины концепции современного естествознания Специальность, 187.08kb.
- Программа курса «Концепции современного естествознания», 168.05kb.
- Концепции современного естествознания, 52.76kb.
- Концепции современного естествознания, 232.93kb.
- Программа дисциплины Концепции современного естествознания Специальность/направление, 456.85kb.
- И. А. Кудрова вопросы к зачету по дисциплине «Концепции современного естествознания», 29.77kb.
Специальная теория относительности (С. Т.О.) была создана Эйнштейном в 1905 году.
§1: Постулаты Эйнштейна. Преобразования Лоренса
Во второй половине 19 века Максвелл разработал теорию электромагнитных явлений. В основе теории лежит предположение о том, что скорость распространения магнитных волн, в частности скорости света, является абсолютной величиной, то есть не изменяется при переходе из одной инерциальной системы отсчёта в другую.
Абсолютная величина – величина, которая одинакова в любых инерциальных системах отсчёта.
Физическая величина называется относительной, если она имеет разные значения в разных инерциальных системах отсчёта.
C = 300000 км/с – скорость света в вакууме.
- Правило Галилея нельзя применять к электромагнитным процессам
- Теория электромагнитных излучений неверна
- Обе теории верны, но надо пересмотреть свои взгляды на пространство и время!
C = C’ + V0
C’ = C – V0
V0 = C; C’ = 0
Майкельсон и Морли пытались в 1881 году измерить скорость света. Скорость света оказалась абсолютной.
Масса электрона примерно равна 910-31 кг. Если законы классической механики равны, то нужно разогнать электрон по формуле Eк = mэC2/2, тогда мы получим скорость света = 410-14 Дж.
Eк =3,310-10 Дж.
Но электрон не приобретает скорость света, значит, существует другая физика.
Из существующей теории:
Эйнштейн формирует два постулата:
1 – Постулат о постоянстве скорости света:
Скорость света в вакууме одинакова во всех инерциальных системах отсчёта и не зависит от движения источников и приёмников света.
2 – Принцип относительности:
Все физические явления происходят одинаковым образом во всех инерциальных системах отсчёта.
Эти два постулата составляют основу специальной теории относительности.
Релятивистская теория механики (преобразования Галилеем не удовлетворяют этой теории)
В специальной теории относительности приняты преобразования Лоренса:
x = x’ + V0t’
1-V02/C2
y = y’; z = z’
В разных инерциальных системах отсчёта время течёт по-разному.
t = t’+ (V0/C2)x’
1-V02/C2
x’ = x - V0t
1-V02/C2
t’ = (V0/C2)x
1-V0/C2
Скорость света недостижима!
V, V’, V0 – сонаправлены, тогда следует, что V = V’ + V0
1 + V’V0/C2
V’ = C
V = C + V0 = C
1 + CV0/C2
Относительность одновременности.
Неточность наших представлений о пространстве и времени обусловлена ошибочным предположением о возможности мгновенной передачи взаимодействий и сигналов. Существование конечной скорости передачи взаимодействий заставляет изменить наши взгляды на пространство и время.
Представление об абсолютном времени, которое течёт раз и навсегда с заданным темпом не зависимо от движения материи, оказывается неверным.
С фактором конечной скорости распространения сигналов связана относительность одновременности.
Понятие одновременности событий относительно, поскольку зависит от инерциальной системы отсчёта, в которой находится наблюдатель.
§2: Промежутки времени. Парадокс близнецов.
Рассмотрим некоторую точку, неподвижную относительно движущейся инерционной системы отсчёта K’.
Пусть в этой точке произошло какое-то событие. Длительность этого события относительно движущейся инерционной системы отсчёта K’ = t’ = t2’ – t1’
t = t2 – t1
t1 - начальный момент
t2 - конечный момент
t = t’ .
1-V02/C2
В движущейся системе отсчёта время замедляет свой ход, из чего следует парадокс близнецов.
А В
20 лет 20 лет
t’ < t
t = 80 лет; V0 = 0,99с
t = 80 = 11,3г
1 – 0,992
А В
100 лет 31,3 года
Парадокс:
Дело в том, что братья близнецы в течение всего времени находились в разных условиях. Всё-таки Землю можно с большим основанием считать инерциальной системой отсчёта, чем космический корабль.
Специальная теория относительности справедлива только для инерциальной системы отсчёта. Для неинерциальной системы отсчёта создана общая теория относительности.
§3: Относительность расстояния.
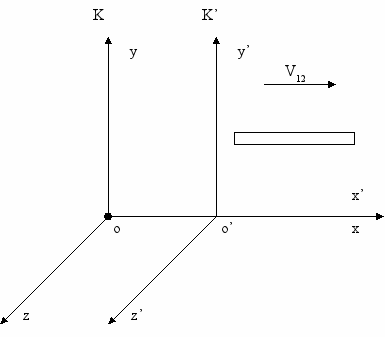
Для наблюдателя системы K’: l0=x’2-x’1
Для наблюдателя системы K: l=x2-x1
l = l01-V02/C2
Линейные размеры движущихся тел сокращаются. Уменьшение размеров движущихся тел обладает удивительным свойством взаимности.
Пространство и время в специальной теории относительности:
1 – Пространство и время не существуют независимо друг от друга. Они связаны между собой единым понятием: пространство-время.
2
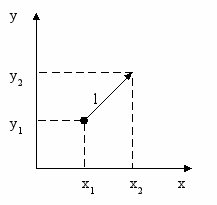
l = (x)2+(y)2
x = x2-x1; y = y2-y1
Время течёт относительно системы отсчёта. Интервал – инвариантная величина.
S = (x)2+(y)2+(z)2-(ct)2
S’=S
l’l
t’t
Эквивалентность массы и энергии. m0 – масса некоторого тела, неподвижного относительно инерциальной системы отсчёта K’(масса покоя).
Для наблюдателя относительно системы K:
m=m0/1-V02/C2
m> m0
Масса движущегося тела увеличивается.
Относительна не только масса, но и энергия тела.
E=mC2
E=m0C2/1-V02/C2
Невозможно всю массу превратить в энергию. Существует закон сохранения тяжёлых частиц: в любых процессах общее количество нуклонов остаётся неизменным.
Основные положения молекулярно-кинетической теории.
Молекулярно-кинетическая теория характеризует свойства веществ и происходящие в природе процессы на основе законов движения молекул. Основные положения в молекулярно-кинетической теории:
1 – Все вещества состоят из мельчайших частиц: атомов и молекул, разделённых меж собой промежутками.
2 – Атомы и молекулы находятся в непрерывном хаотическом движении, которое называется тепловым.
3 – Молекулы взаимодействуют между собой силами притяжения и отталкивания.
Молекула – наименьшая частица вещества, сохраняющая его химические свойства. Молекулы составляют атомы.
Атом – наименьшая частица вещества, обладающая свойствами химических элементов, входящих в его состав.
В естественном состоянии в природе находится только 88 атомов, в то время, как 21 элемент является нестабильным, полученным искусственным путём на современных ускорителях.
d 10-10 м= 1A
He = 2,4 A
Ar = 4 A
M = 10-26 кг
В грамме воды: 3,31022
В см3воздуха: 271019
1 моль – такое количество вещества, которое содержит столько же структурированных элементов (атомов, молекул, ионов), сколько атомов содержится в 0,012кг12С
Na = 6,021023 1/моль
Газ.
Газ занимает объём, значительно больший общего объёма всех молекул, из которых состоит этот газ. Большую часть времени молекулы в газе движутся свободно, не взаимодействуя между собой. Кинетическая энергия больше потенциальной.
Жидкость.
Молекулы в жидкости совершают непрерывные колебательные движения относительно положения равновесия. Несмотря на то, что молекулы в жидкости плотно упакованы, они легко разрывают связи со своими молекулами, совершают прыжок в новое положение равновесия.
10-12-10-13 – время жизни молекулы.
10-11 – период колебания молекулы жидкости.
Чем выше температура жидкости, тем меньше время локализации молекулы.
Твёрдое тело.
Молекулы твёрдо упакованы друг к другу и непрерывно взаимодействуют друг с другом. В отличие от молекул жидкости, молекулы твёрдого тела не разрывают связи со своими соседями. Именно этим объясняется упругость и прочность твёрдого тела. Различают два типа твёрдых тел:
1 – Аморфные твёрдые тела
2 – Кристаллические твёрдые тела.
В аморфных телах молекулы распределяются хаотично.
В твёрдом теле молекулы совершают колебательные движения относительно положению равновесия. Если эти положения равновесия мысленно соединить линиями, то получим структуру, напоминающую упорядоченную кристаллическую решётку, узлами которой являются положения равновесий молекул. Твёрдые тела с упорядоченной решёткой называются кристаллическими. Кристаллические твёрдые тела различаются в зависимости от типа кристаллической решётки. Кинетическая энергия меньше потенциальной.
§4: Динамические и статические описания макроскопических систем.
Различают два вида физических величин:
1 – Микроскопические величины – величины, характеризующие молекулу. Пример: масса, скорость, размер, скорость движения, энергия и т.д.
2 – Макроскопические параметры – объём системы, её масса, давление, температура, концентрация компонентов и т.д.
Существует специальный отдел физики, изучающий микро и макроскопические величины и устанавливающий связь между ними. Это – статическая физика.
Макроскопические величины в статической физике получают в результате статистического усреднения микроскопических величин.
Законы динамики обратимы во времени. Если бы мы повернули время вспять, то молекулы начали бы двигаться в обратном направлении. Макроскопические законы динамики не обратимы во времени.
Каждая отдельная молекула, ударяясь о стенку сосуда, взаимодействует с этой стенкой короткое время и оказывает на эту стенку какое-то действие.
Если просуммировать все эти силы, то мы получим силу давления. Сила давления на стенки сосуда и есть сила давления газа.
[P] = 1Н/м2 = 1 Па
1 мм.рт.ст. = 133,3 Па
1атом = 1, 013105 Па = 760 мм.рт.ст.
Шкала Цельсия построена по двум рёберным точкам.
t1 = 0C
t2 = 100C
Кельвин.
За абсолютный ноль вещества принято такое состояние вещества, при котором прекращается поступательное движение молекул.
T = tC + 270,16C
Шкала Фаренгейта.
32F – t таяния льда
96F – t тела человека
1F = 5/9C
tC/5 = (t-32)F/9
Сравнение температурных шкал:
| Реберные точки | F | C | K |
| Точка кипения воды | 212 | 100 | 373 |
| Точка таяния льда | 32 | 0 | 273 |
| Абсолютный ноль | -459 | -273 | 0 |
Температура – физическая величина, которая является мерой средней кинетической энергии теплового движения молекул.
Eк T
На каждую поступательную степень свободы в среднем должна приходиться энергия ½ kT.
k = 1,3810-23 Дж/k
Eк = 3/2 kT.
Уравнение состояния вещества
Состояние всякой термодинамической системы определяется набором небольшого количества макроскопических параметров.
Уравнением состояния называют соотношение, связывающее между собой термодинамические параметры состояния системы. Это уравнение необходимо для того, чтобы прогнозировать как будут изменяться оставшиеся термодинамические величины, если изменится хоть одна из этих величин. В настоящее время уравнение состояний удалось настроить только для простейшей модели тела: идеального газа.
Законы идеального газа:
1 –
2 – Средняя длина столкновения молекул идеального газа больше средней длины пролёта газа.
3 – Молекулы взаимодействуют между собой только при непосредственном соприкосновении, причём только силами отталкивания.
4 – Силами притяжения между молекулами можно пренебречь.
PV = m/MRT
R = kNa = 8,315 Дж/(kмоль)
Скорости молекул:
Eк = 3/2 kT = moV2/2
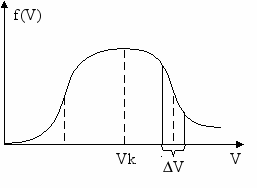
Vk = V2
Vk = 3kT/mo = 3RT/M
T = 273k
Термодинамика – наука о наиболее общих свойствах макроскопических систем, находящихся в состоянии равновесия.
Равновесные системы и процессы.
Система называется равновесной, если термодинамические параметры состояния не изменяются с течением времени и имеют одно и тоже значение во всех частях системы.
Если система не взаимодействует с внешней средой (является изолированной), то с течением времени она обязательно придет в состояние равновесия.
При взаимодействии с внешней средой состояние системы может измениться. Изменение состояния системы называют термодинамическим процессом.
Термодинамический процесс называют равновесным, если при переходе от одного равновесного состояния к другому система проходит промежуточные равновесные состояния.
В природе не существует равновесных процессов. Понятие такого процесса – идеализация.
Вместе с тем, процесс, который протекает достаточно медленно, можно с хорошей степенью точности считать равновесным. Равновесные термодинамические процессы называют обратными.
Первый закон термодинамики (начало).
В середине 19 века физик-экспериментатор Джоуль установил эквивалентность механической работы и теплоты. Обобщая эксперименты Джоуля, немецкий физик Майер сформулировал закон сохранения энергии. Энергия не возникает ни из чего и не исчезает. В различных процессах она только переходит из одного вида в другой в эквивалентных количествах.
Закон сохранения энергии применительно к термодинамике называют первым законом термодинамики (началом).
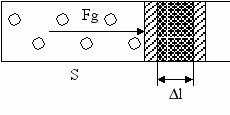
A = Fgl = p Sl = pV
A’ = -A
Работа – передача энергии за счёт движения системы как единого целого.
Количество теплоты характеризует передаваемую энергию электропередач.
[a] = 1Дж
[a] = 1 Кал
Одна калория – такое количество теплоты, которое необходимо сообщить одному грамму дистиллированной воды, чтобы повысить её температуру от 19,5C до 20,5C.
Внутренняя энергия.
Внутренней энергией называют ту часть энергии системы, которая обусловлена собственными параметрами состояния этой системы.
E = Ek + Eп + V
Внутренняя энергия.
Внутренняя энергия складывается из кинетической и потенциальной энергией молекул, из энергии атомов, а так же из энергии элементарных частиц, из которых состоят сами атомы. Существуют только два способа измерения систем:
1 – За счёт механической работы
2 – За счёт теплопередачи
Количество теплоты, переданное системе, расходуется на её внутреннюю энергию и на совершение механической работы над внешней средой.
Q = U+A
Большую роль сыграли создания вечного двигателя.
Вечный двигатель первого рода – машина, которая была бы способна совершить механическую работу, не получая теплоту из внешней среды и не изменяя свою внутреннюю энергию.
Q = 0; U = 0; A 0
Вечный двигатель первого рода не возможен.
Второй закон термодинамики.
Тепловые двигатели.
Тепловым двигателем называют машину, превращающую внутреннюю энергию в механическую работу. Периодическим называют тепловой двигатель, у которого рабочие части периодически возвращаются на исходное место.
3 условия работы движения:
1 – Наличие рабочего тела, которое при нагревании способно расширяться, совершая механическую работу. Обычно вместо тела используется газ или пар.
2 – Наличие замкнутого термодинамического процесса (цикла), т.е. такого процесса, при котором рабочее тело возвращается в исходное термодинамическое состояние.
3 – Наличие нагревателя и холодильника.
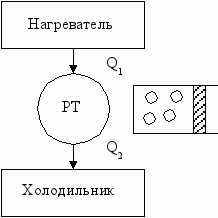
A = Q1 - Q2
Формулировка Кельвина.
Невозможен такой термодинамический процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя в эквивалентную ей работу. Вечный двигатель второго рода – тепловая машина, которая была бы способна превратить всё количество теплоты, полученное от нагревателя в механическую работу.
Вечный двигатель второго рода невозможен.
Глава 4: Квантовая теория.
Основные концепции квантовой теории.
Квантовая теория изучает законы микромира, то есть строение, взаимодействие и движение молекул, атомов, атомных ядер и элементарных частиц.
За все годы существования квантовой физики удалось изучить строение молекул, атомов, атомных ядер, понять природу межмолекулярных взаимодействий и химических связей, объяснить периодические законы химических элементов.
§1: Возникновение квантовой физики.
Тепловое излучение.
Все вещества в природе обладают свойством испускать электромагнитное излучение, называемое тепловым. Тепловым излучением называют испускаемое телом электромагнитное излучение, вырабатываемое за счёт внутренней энергии этого тела.
Атомы твердого тела совершают непрерывные колебательные движения относительно положения равновесия. Атом состоит из отрицательно заряженных электронов и положительно заряженного ядра.
Из законов электродинамики известно, что колебание электрических зарядов приводит к возникновению электрических полей. Таким образом, теплоизлучение обусловлено колебанием атомов в твёрдом теле.
Чем выше температура тела, тем больше интенсивность испускаемого им теплового излучения.
Поскольку атомы-излучатели колеблются с разными частотами, то и тепловое излучение представляет собой набор электромагнитных волн, поэтому важно знать спектральную плотность теплового излучения, приходящуюся на единичный интервал длин волн. (, +).
r = E - Спектральная плотность теплового излучения
Основная задача теории теплового излучения состоит в изучении спектральной плотности.
Теория Релей-Джинса.
Эта теория была основана на законах классической электродинамики, разработанных Максвеллом.
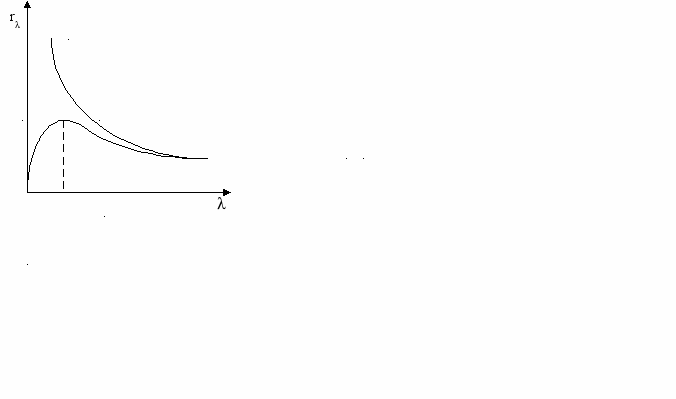
Ультрафиолетовая катастрофа.
Законы классической физики нельзя применять для описания излучения на коротких длинах волн.
В 1900 году немецкий физик Планк пришёл к выводу о том, что теорию можно совместить с экспериментом, если предположить, что всякое тело испускает тепловое излучение не непрерывно, а отдельными порциями (квантами).
Планк предположил, что энергия одного кванта излучения пропорциональна частоте квантового излучения.
E = h
h = 6,62610-34 Джс
Энергия теплового излучения должна быть кратна энергии одного кванта.
§2: Корпускулярно-волновой дуализм.
Фотоэффектом называется явление отрыва электронов с поверхности твёрдого тела под действием света.
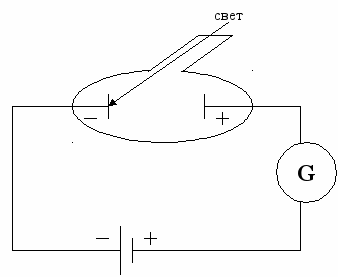
Стрелка гальванометра от света начинает отклоняться.
Величина фототока зависит не от интенсивности света, а от его частоты.
Эйнштейн в 1905 году построил теорию фотоэффекта, используя теорию Планка о тепловом излучении. Катод поглощает свет отдельными квантами.
Свет представляет собой поток квантов. Один квант света – фотон. Положение света – интерференция.
Свет имеет двойственную природу: он является и электромагнитной волной, и потоком частиц. Пока свет распространяется в свободном пространстве, он ведёт себя как электромагнитная волна, но как только он взаимодействует с веществом, он ведёт себя как поток корпускул.
Луи де Бройль выдвинул гипотезу о том, что всякой частице можно поставить в соответствие некоторую длину волны.
§3: Соотношение неопределенностей.
Микрообъекты не являются ни волнами, ни частицами. В их классическом понимании с точки зрения квантовой физики существует некоторая неопределённость в определении местоположения, скорости и энергии частиц.
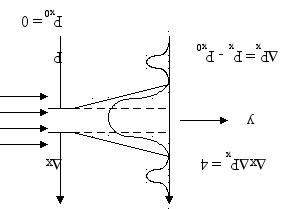
Соотношение неопределённостей Гейзенберга.
Чем более точную информацию мы получаем о координатах частиц, тем меньше мы знаем об их импульсах.
xPx 4
От неопределённости координат импульса можно перейти к неопределённости энергии и времени.
Px = E/c
x = ct
Неопределённость энергии системы.
Чем больше неопределенность энергии системы, тем меньше времени жизни системы.
Важное значение соотношения неопределённостей состоит в том, что оно указывает в какой степени можно пользоваться понятиями классической физики применительно к микрочастицам.
Если в микромире невозможно в любой фиксированный момент времени точно определить координаты и скорости частиц, то нельзя говорить о вероятностях того, что частицы находятся в данной точке и обладают некоторым импульсом.
P = mV
xVx n/m
§4: Строение атомов.
В 1897 году Джордж Томпсон, исследуя электрический заряд, открыл электрон. Обозначение: e-.
Q = Ze
Z = 1,2,3…
Первую модель атома, основанную на классическом цикле, предложил Томпсон. В атоме должен содержаться электрический положительный заряд, по модулю равный общему отрицательному заряду всех электронов в атоме.
Резерфорд исследовал поток - частиц на атомах.
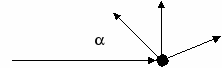
Внутри атома существует массивная маленькая, положительно заряженная частица. Резерфорд предложил планетарную модель атома:
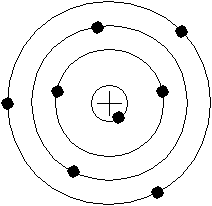
Из классической электродинамики известно, что электрически заряженные частицы, движущиеся с ускорением, испускают электромагнитное излучение. Планетарную модель оказалось невозможным обосновать на основе известных законов классической физики.
Для обоснования планетарной модели выдвигаются два постулата, основанных на квантовых представлениях:
1 – Постулат о стационарных состояниях. Атомная система может находиться только в некоторых состояниях, и в ней возникает электромагнитное излучение. Хотя электроны движутся с ускорением, такие состояния называют стационарными состояниями атомов.
2 – Правило частот Бора. Любое испускание или поглощение энергии атомов происходит при переходе атома из одного стационарного состояния в другое, при этом частота излучения определяется разностью энергий стационарных состояний атомов, между которыми осуществляется переход.
hmn = Em - En
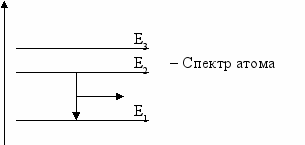
Атом может спонтанно перейти из состояния с высокой энергией в состояние с меньшей энергией, испустив квант света. Бесконечно долго атом может находиться только в состоянии с минимальной энергией E1, оттого его называют основным. Все остальные состояния называют возбуждёнными.
Электронные оболочки
Электроны в атомах располагаются по оболочкам. Разные оболочки находятся на различных состояниях от ядра атома. Электроны, находящиеся в одной оболочке, движутся по разным орбитам. Электроны, находящиеся в одной оболочке, обладают близкими значениями энергий. Чем дальше электроны находится от ядра, тем большей энергией они обладают. Число электронов в каждой оболочке не может быть произвольным.
§5: Строение атомного ядра.
Размер атомного ядра равен 10-13 см.
Почти вся масса атома сосредоточена в ядре
ядра = 1014 гсм3
Ядро имеет положительный электронный заряд, который по модулю равен суммарному электрическому заряду всех электронов в атоме. Если в атоме Ze-, то заряд равен Ze-. В состав ядра входят протоны. Z – Количество протонов в ядре. Сколько протонов, столько и e-. Протон – ядро в атоме водорода.
A = Mя/Mp
Массовым числом ядра называют отношение массы ядра равного элемента к массе протона равного элемента, округлённое до ближайшего целого.
A>Z
В 1932 году Чедвик открыл нейтрон, частицу, не обладавшую электрическим зарядом, но имеющую сходную с протоном массу.
Массовое число – количество нуклонов в ядре.
N = A-Z
Нуклоны удерживаются внутри атомного ядра за счёт сильных (ядерных) взаимодействий. Интенсивность сильных взаимодействий в сто раз превышает кулоновские взаимодействия.
Взаимодействия между нуклонами в ядре характеризуют энергией связи. Энергией связи называют такую энергию, которую необходимо затратить, чтобы разделить ядро на отдельные составляющие, то есть на протоны и нейтроны.
M
Используя принципы эквивалентности массы и энергии, мы можем сказать, что: E = (Zmp+Nmn)c2-Mc2
Химические свойства элементов определяются только количеством протонов в ядре. Все химические элементы имеют несколько разновидностей, из которых они все имеют в ядре одинаковое количество протонов, но разное количество нейтронов.
§6: Явление радиоактивности.
Впервые взаимодействие химических элементов наблюдалось в 1896 году при открытии явления радиоактивности.
Явление радиоактивности состоит в том, что ядра некоторых химических элементов, называемых радиоактивными, могут самопроизвольно (или спонтанно) распадаться, образуя ядра новых химических элементов и испуская излучение, называемое радиоактивным.
224Ra224Ac + e + электромагнитное излучение
81 89
-излучение – поток -частиц.
4He – -частица
2
-излучение – поток ядер He. -излучение обладает малой проникающей способностью.
Проникающая способность -лучей больше, чем у -лучей и есть опасность облучения.
-лучи – высокочастотное магнитное излучение, уничтожающее живые организмы на клеточном уровне. Из космоса на землю идёт мощный поток -излучения.
Каждый изотоп химического элемента может выделять только один вид радиоактивного излучения. Интенсивность радиоактивного распада характеризуют величиной, которая называется периодом полураспада.
Периодом полураспада называют такой промежуток времени, в течение которого распадается половина радиоактивных ядер. У разных изотопов одно и того же химического элемента периоды полураспада различны.
| Уран 238 U 98 | 4,5109 лет |
| Радий 226 Ra 88 | 1622 года |
| Углерод 11 C 6 | 22,4 месяца |
| Полоний 213 Po 84 | 4,210-6 секунды |
