Нарушения когнитивных функций в пожилом возрасте
| Вид материала | Документы |
СодержаниеДиагностические критерии ДЭ |
- Е проблемы обучения, как нарушения письма, чтения, счета, расстройства внимания и других, 116.64kb.
- Вестн. Моск. Ун-та. Сер. 14. Психология, 253.88kb.
- Системная красная волчанка с люпус-нефритом в пожилом возрасте (клиническое наблюдение), 118.27kb.
- С. И. Краюшкин тематический план, 28.14kb.
- Особенности морфологической картины сыворотки крови, эритроцитарного гемолизата и ротовой, 470.47kb.
- Т. А. Воронина Отечественный препарат нового поколения, 449.54kb.
- Шер ирина Игоревна Комплексная пелоидотерапия больных гипертонической болезнью с сопутствующим, 342.36kb.
- Новополоцкая центральная городская больница совет молодых ученых смоленской государственной, 662.95kb.
- Нарушения привязанности как основа формирования психопатологических расстройств в детском, 247.22kb.
- Мотивационная характеристика темы, 400.93kb.
НАРУШЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ В ПОЖИЛОМ ВОЗРАСТЕ
В. Захаров, Н. Яхно,
Кафедра нервных болезней ММА им. И. М. Сеченова
В настоящее время около 15% населения мира составляют лица пожилого и старческого возраста, численность которых – более 400 млн человек. В России, согласно последней переписи населения, проживают свыше 29 млн лиц старше трудоспособного возраста. Ожидается, что в ближайшее время численность лиц старших возрастных групп еще больше возрастет при общем сокращении численности населения страны [2, 14].
Одно из наиболее распространенных неврологических нарушений в пожилом возрасте – ухудшение когнитивных функций (КФ). Под КФ принято понимать наиболее сложные функции головного мозга, с помощью которых осуществляется процесс рационального познания мира и взаимодействия с ним. К КФ относятся:
восприятие (гнозис) – способность распознавать информацию, поступающую от органов чувств;
память – способность запечатлевать, сохранять и в нужный момент воспроизводить усвоенную информацию;
праксис – способность планировать и осуществлять сложные двигательные акты;
речь – способность понимать и выражать мысли с помощью слов;
мышление (интеллект) – способность анализировать информацию, выявлять сходства и различия, выносить суждения и умозаключения;
внимание – способность поддерживать оптимальный для умственной деятельности уровень психической активности.
В 2006 г. были опубликованы результаты одного из первых масштабных исследований распространенности когнитивных нарушений (КН) в амбулаторной неврологической практике в нашей стране. В исследовании принимали участие 132 врача невролога и более 3000 пациентов из 33 городов 30 регионов России. Каждому пожилому пациенту, который приходил на амбулаторный прием к неврологу по какой-либо причине, проводилось короткое исследование КФс использованием наиболее простых психометрических методик: краткой шкалы оценки психического статуса и теста рисования часов. В результате КН были выявлены в 70% случаев, причем в 25% они достигали значительной выраженности (по краткой шкале оценки психического статуса) – рис. 1 [8].
Р
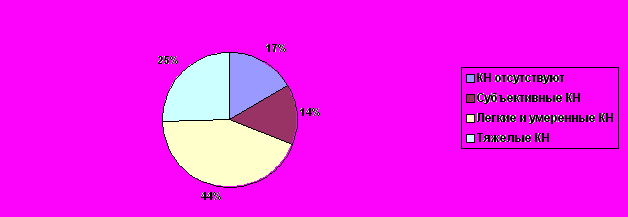
ис. 1. Распространенность КН среди пожилых пациентов на приеме у невролога
Как видно из представленных данных, КН присутствуют у большинства неврологических пациентов пожилого возраста, однако выраженность КН может весьма существенно варьировать. Оценка тяжести и качественных особенностей КН имеет большое значение для определения синдромального, топического и нозологического диагноза, выбора адекватной тактики ведения. Анализ данных литературы и работ, выполненных в клинике нервных болезней им. А. Я. Кожевникова, позволяет предложить следующую классификацию КН по тяжести [21, 23, 25]:
• тяжелые КН: выраженное снижение когнитивных способностей, которое приводит к существенным затруднениям в повседневной жизни (профессиональная деятельность, хобби и увлечения, взаимодействие с другими людьми, быт, самообслуживание);
• умеренные КН: снижение когнитивных способностей, которое явно выходит за рамки среднестатистической возрастной нормы, обращает на себя внимание пациента и/или окружающих его лиц, но не мешает существенно в обычной жизни, хотя может вызывать затруднения в сложных и новых видах деятельности;
• легкие КН: снижение по сравнению с преморбидным уровнем отдельных КФ, которые формально могут оставаться в пределах среднестатистической возрастной нормы или отклоняться от нее незначительно; такие изменения могут вызывать беспокойство пациента, но часто незаметны для окружающих и внешне не влияют на профессиональную, социальную и иную активность.
КН представляют собой полиэтиологический синдром, возможный при разных заболеваниях головного мозга. В пожилом возрасте наиболее частые причины КН – болезнь Альцгеймера (БА), цереброваскулярные заболевания, деменция с тельцами Леви (ДТЛ), лобно-височная лобарная дегенерация, болезнь Паркинсона (БП) и другие нейродегенеративные заболевания с преимущественным поражением подкорковых базальных ганглиев. Перечисленные заболевания лежат в основе около 80% выраженных КН, встречающихся в нейрогериатрической практике [5, 24, 25].
КН, кроме первичных неврологических заболеваний, могут вызывать системные дисметаболические расстройства при соматических и эндокринных заболеваниях, экзогенных интоксикациях. Это делает проблему КН весьма актуальной не только для неврологов, но и для терапевтов, эндокринологов, врачей других специальностей. Важно отметить, что КН преимущественно дисметаболической природы являются потенциально обратимыми при своевременной диагностике и лечении.
БА и смешанные КН. Самая распространенная причина КН в пожилом возрасте – БА, которая отмечается не менее чем у 2% лиц старше 65 лет [2]. По опыту работы лаборатории памяти, которая функционирует на базе Клиники нервных болезней им. А.Я.Кожевникова с 2003 г., БА диагностируется у 30% пациентов, обратившихся по поводу КН [24]. Наиболее характерным проявлением БА являются нарушения памяти на текущие и недавние события, которые развиваются исподволь без видимой причины и выраженность которых постепенно нарастает. Со временем забывчивость распространяется на все более отдаленные события жизни, присоединяются нарушения других КФ, таких как гнозис, праксис, речь и интеллект. В результате постепенно формируется зависимость от посторонней помощи, что свидетельствует о синдроме деменции. При этом очаговая неврологическая симптоматика часто отсутствует вплоть до наиболее поздних стадий болезни. Компьютерная томография или магнитно-резонансная томография (МРТ) головы обнаруживает церебральную атрофию, затрагивающую преимущественно кору височных и теменных долей головного мозга [2, 20, 27].
Патогенез БА связан с отложением в паренхиме головного мозга и церебральных сосудах патологического белка – b-амилоида, который обладает нейротоксическими свойствами. Это приводит к активации тканевых медиаторов воспаления, повышению выброса возбуждающих аминокислот, усилению процессов перекисного окисления липидов. Результатом сложного каскада патохимических реакций становится гиперфосфорилирование одного из основных белков внутренней мембраны нейронов – тау-протеина, что становится непосредственной причиной гибели клеток головного мозга. Длительное время нейродегенеративный процесс протекает бессимптомно, поэтому у многих пожилых людей без КН при морфологическом исследовании выявляются изменения, характерные для начальных стадий БА [27].
Однако наличие сопутствующей цереброваскулярной недостаточности может ускорять темп развития и приближать время клинической манифестации БА. Даже негрубые признаки цереброваскулярной недостаточности увеличивают риск формирования синдрома деменции почти в 2 раза. При этом сочетание дегенеративного и сосудистого процесса вызывает некий кумулятивный эффект: наблюдаемая клиническая картина оказывается более тяжелой, чем можно было бы ожидать при простом суммировании воздействий 2 патологических факторов [32].
В исследовании, проведенном в нашей клинике, было показано, что большинство пациентов пожилого возраста с диагнозом БА имели сопутствующие сердечно-сосудистые заболевания. Однако у части из них клиническая картина не выходила за рамки БА (так называемая БА с сосудистыми факторами риска). У других больных наряду с типичными симптомами БА уже на ранних стадиях деменции выявлялись когнитивные расстройства лобного характера, свидетельствовавшие о значимом васкулогенном характере КН. В этих случаях вероятность смешанной (сосудисто-дегенеративной) этиологии деменции весьма велика (так называемая смешанная деменция). Смешанная деменция (дегенеративно-сосудистая) характеризуется более значительной выраженностью очаговой неврологической симптоматики и большей тяжестью сопутствующих сердечно-сосудистых заболеваний по сравнению с БА с сосудистыми факторами риска [11, 20, 25].
Признаки сочетанного сосудистого и дегенеративного поражения головного мозга могут быть установлены еще до развития у пациента очерченной картины деменции. По нашим данным, умеренные КН выявляются у 56% пациентов с клиническим диагнозом дисциркуляторной энцефалопатии (ДЭ) I или II стадии. При этом в 23% случаев, наряду с типичными для цереброваскулярной недостаточности КН лобного характера выявлялись первичные нарушения памяти, что весьма специфично для ранних стадий дегенеративного процесса. Последующие наблюдения показали, что пациенты этой группы характеризуются более быстрым темпом прогрессирования КН и более высоким риском развития деменции, которая в большинстве случаев оказывалась смешанной (сосудисто-дегенеративной) [21–23].
Сосудистые когнитивные нарушения. Вторая по распространенности причина КН в пожилом возрасте – цереброваскулярные заболевания. По данным эпидемиологических исследований, у 20–25% пациентов, перенесших инсульт, в течение первых 6 мес развиваются выраженные КН [9, 30, 31]. Однако не всегда постинсультные КН непосредственно вызываются острым нарушением мозгового кровообращения (ОНМК). По данным нашей клиники, у 90% пациентов с постинсультными КН ретроспективная оценка выявляет наличие КН до развития инсульта. В этих случаях инсульт приводит к декомпенсации предшествующей когнитивной недостаточности, которая может иметь как сосудистую, так и дегенеративную природу. В пользу последнего предположения свидетельствует наличие у части пациентов первичных нарушений памяти, что, как уже указывалось, обычно связано с сопутствующим дегенеративным процессом. На это же указывает наличие корковой церебральной атрофии у таких больных по результатам нейровизуализационного исследования [9, 12].
КН закономерно развиваются в рамках ДЭ. ДЭ представляет собой синдром хронического поражения головного мозга сосудистой этиологии, который развивается в результате повторных ОНМК и(или) хронической недостаточности кровоснабжения головного мозга.
Диагностические критерии ДЭ:
признаки (клинические, анамнестические, инструментальные) многоочагового и(или) диффузного поражения головного мозга;
признаки острой или хронической церебральной дисциркуляции (клинические, анамнестические, инструментальные);
наличие причинно-следственной связи между нарушениями церебральной гемодинамики и развитием клинической, нейропсихологической, психиатрической симптоматики;
клинические и параклинические признаки прогрессирования сосудистой мозговой недостаточности.
Термин «ДЭ» является более точным, нежели «хроническая ишемия мозга», так как последний игнорирует ОНМК как один из механизмов формирования хронического прогрессирующего сосудистого поражения головного мозга.
В основе формирования КН при ДЭ лежит разобщение связей лобных долей с другими отделами головного мозга в результате диффузных изменений белого вещества – лейкоареоза. Морфологической основой лейкоареоза являются глиоз, демиелинизация, увеличение периваскулярных пространств, пропотевание спинномозговой жидкости из желудочков головного мозга. Причиной формирования лейкоареоза чаще всего является хроническая недостаточность мозгового кровообращения в результате гипертонической микроангиопатии или атеросклеротического поражения церебральных артерий. Выраженность лейкоареоза, выявляемого при МРТ головного мозга, коррелирует с тяжестью КН и другими неврологическими расстройствами при ДЭ. Деафферентация лобных долей головного мозга в результате лейкоареоза ведет к вторичной лобной дисфункции, которая обусловливает наиболее частые симптомы ДЭ. В когнитивной сфере отмечаются снижение активности психических процессов, замедленность мышления (брадифрения), недостаточность концентрации внимания, уменьшение объема оперативной памяти. Выраженность КН при ДЭ коррелирует с другими неврологическими расстройствами, такими как нарушения походки, псевдобульбарные, пирамидные, экстрапирамидные и атактические нарушения [1, 2, 10, 16–18, 25].
ДТЛ представляет собой хроническое прогрессирующее нейродегенеративное заболевание, морфологическая картина которого характеризуется образованием специфических внутриклеточных образований – телец Леви, которые диффузно распространены в корковых и подкорковых отделах головного мозга. Это заболевание было впервые описано японскими невропатологами в 1984 г., однако в течение длительного времени не распознавалось клинически [28]. В настоящее время установлено, что ДТЛ лежит в основе не менее чем 15% деменций в пожилом возрасте [19].
КН при ДТЛ отличаются от таковых при БА и цереброваскулярной недостаточности. По данным исследований И.С.Преображенской и соавт., проведенных в нашей клинике, клиническое ядро образуют КН нейродинамического характера в виде снижения концентрации внимания и истощаемости психической деятельности. Весьма характерны также нарушения зрительно-пространственного гнозиса и праксиса. Нарушения памяти обязательны, но выражены меньше, чем при БА. Снижение интеллекта также типично. Весьма специфическим симптомом ДТЛ являются зрительные галлюцинации, которые отмечаются у 25–50% больных на ранней стадии заболевания и у 80% – на поздней. Галлюцинации носят конкретный характер, обычно – в виде образов людей (нередко – знакомых) или животных. Галлюцинации повторяются и обычно усиливаются в вечернее или ночное время. Критика к ним на начальных этапах болезни сохранна, а затем может ослабляться [13, 19, 20, 25].
Психические нарушения при ДТЛ сочетаются с двигательными нарушениями в виде симметричной брадикинезии, постуральных расстройств и нарушения ходьбы. Характерны также вегетативные расстройства с преобладанием парасимпатической направленности вегетативных реакций. Выраженность периферической вегетативной недостаточности, в частности кардиальной дизавтономии и периферической симпатической денервации, – один из факторов, определяющих продолжительность жизни пациентов с ДТЛ. Периферическая вегетативная недостаточность, возможно, лежит в основе характерных для ДТЛ колебаний выраженности симптомов (флюктуаций), механизмом которых может быть преходящая церебральная ишемия [13, 19, 20].
Распространение атрофического процесса, согласно данным нейровизуализации, различно при ДТЛ и БА. Так, для ДТЛ характерно большее расширение задних рогов боковых желудочков при относительно неизмененных передних рогах в сочетании с атрофией затылочных отделов головного мозга. При БА наиболее выраженные атрофические изменения затрагивают теменные и височные доли. Атрофический процесс при ДТЛ сочетается с диффузными изменениями белого вещества головного мозга (лейкоареоз), вероятно, ишемического характера [13, 19, 20].
Заболевания с преимущественным поражением подкорковых базальных ганглиев. КН являются важной составной частью клинической картины БП и симптоматического паркинсонизма в рамках других нейродегенеративных заболеваний. По нашим данным, они отмечаются у всех пациентов с БП, однако выраженность их значительно варьирует (рис. 2) [4, 6, 7, 25].
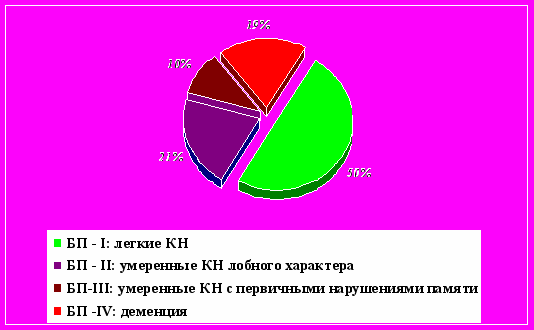
Рис. 2. КН при БП
КН при БП представлены снижением психической активности и замедленностью мышления, снижением интеллектуальной гибкости (трудности переключения с одного этапа деятельности на следующий), нарушением пространственного гнозиса и праксиса, недостаточностью воспроизведения информации из памяти. Нейропсихологический анализ качественных особенностей КН свидетельствует о том, что в их основе лежит вторичная лобная дисфункция в результате нарушения связи лобных долей с подкорковыми базальными ганглиями. Первичные нарушения памяти менее характерны и встречаются главным образом у пациентов пожилого возраста [4, 6, 7].
КН при БП носят прогрессирующий характер, однако темп прогрессирования относительно небольшой: по нашим данным, существенные изменения КФ заметны лишь при длительных сроках наблюдения (2–5 лет). Быстрее КН прогрессируют у пациентов более пожилого возраста, с поздним началом заболевания и при переходе на поздние стадии БП. Деменция развивается у наиболее пожилых пациентов с длительным стажем БП и значительной выраженностью двигательных расстройств [15].
Количественные и качественные характеристики КН играют важную роль в дифференциальной диагностике БП и симптоматического паркинсонизма в рамках других нейродегенеративных заболеваний. Как показали наши исследования, при одинаковой длительности заболевания наиболее выраженные КН отмечаются при прогрессирующем надъядерном параличе (ПНП). Они носят преимущественно лобный характер, в то время как первичные нарушения памяти нехарактерны. При множественной системной атрофии (МСА) КФ в целом более сохранны, чем при БП или ПНП, однако отдельные когнитивные симптомы могут достигать значительной выраженности. Так, по нашим данным, выраженность таких когнитивных симптомов, как повышенная истощаемость, снижение концентрации внимания, при МСА может превосходить таковую при БП [4, 6, 7].
Лечение КН. Оптимальное ведение больных с КН предусматривает:
• раннее выявление КН;
• определение характера и тяжести КН, установление нозологического диагноза;
• динамическое наблюдение за больным;
• раннее начало лечения с применением по возможности патогенетической терапии;
• длительность и непрерывность терапии;
• лечение сопутствующих неврологических, психических и соматических расстройств;
• психологическую поддержку и при необходимости – коррекцию поведения ближайших родственников пациента.
Выбор терапевтической тактики определяется причиной (нозологический диагноз) и выраженностью КН. При БА, сосудистых и смешанных КН, ДТЛ и БП с деменцией хорошо зарекомендовали себя ацетилхолинергические и глутаматергические препараты [3, 5, 26, 29].
В терапии деменции используются 4 препарата из группы ингибиторов ацетилхолинэстеразы: донепезил, ривастигмин, галантамин и ипидакарин. Их применение способствует уменьшению выраженности КН, нормализации поведения, повышения адаптации в повседневной жизни, что в конечном счете приводит к повышению качества жизни пациентов и их ближайшего окружения [3, 5, 26, 29].
Имеются некоторые различия механизмов действия между используемыми ингибиторами ацетилхолинэстеразы, поэтому при неэффективности или недостаточной эффективности одного препарата, его следует заменить на другой. К препаратам с двойным механизмом действия относится реминил (галантамин), который сочетает в себе свойства ингибитора ацетилхолинэстеразы и агониста пост-синаптических никотиновых рецепторов. Дополнительное влияние на никотиновые рецепторы способствует повышению концентрации внимания и оказывает нейропротективное действие. В отношении реминила накоплен обширный опыт использования как при нейродегенеративных, так и при сосудистых и смешанных (сосудисто-дегенеративных) когнитивных нарушениях. В серии масштабных рандомизированных исследованиях было показано, что применение реминила оказывает долговременный положительный эффект в отношении КФ, поведения и функциональной адаптации пациентов с хронической сосудистой мозговой недостаточностью, БА и смешанной деменцией. Двойным механизмом действия обладает также экселон (ривастигмин), который блокирует как ацетил- так и бутирилхолинэстеразу. Последнее обеспечивает продолжительный терапевтический эффект, который был продемонстрирован при БА, ДТЛ, БП с деменцией и других церебральных заболеваниях [3, 5, 26, 29].
Другой подход к патогенетической терапии деменции состоит в использовании мемантина – обратимого неконкурентного блокатора N-метил-D-аспартат рецепторов к глутамату. Он применяется при тех же заболеваниях, что и ингибиторы ацетилхолинэстеразы. В случае недостаточной эффективности монотерапии допустимо и целесообразно комбинированное применение ингибитора ацетилхолинэстеразы и мемантина [3, 5, 26, 29].
На стадии недементных (легких и умеренных) КН приоритетны препараты с нейропротекторным действием, так как они потенциально способны предотвратить или отсрочить развитие деменции. Однако на практике оценить профилактический эффект того или иного препарата очень трудно. Поэтому единого подхода к ведению больных с легкими или умеренными КН пока не выработано [5, 26].
В целом своевременная диагностика и адекватная терапия КН способствуют увеличению периода независимости и самостоятельности пациента, повышению его качества жизни и качества жизни его ближайших родственников.
Литература
Дамулин И. В., Яхно Н. Н. Сосудистая мозговая недостаточность у пациентов пожилого и старческого возраста (клинико-компьютерно-томографическое исследование) // Журн. невропатол. и психиатрии. – 1993; 93 (2): 10–13.
Дамулин И. В. Болезнь Альцгеймера и сосудистая деменция / Под ред. Н. Н. Яхно. – М., 2002. – С. 85.
Захаров В. В., Дамулин И. В., Яхно Н. Н. Медикаментозная терапия деменций // Клиническая фармакология и терапия. – 1994; 3 (4): 69–75.
Захаров В. В., Ярославцева Н. В., Яхно Н. Н. Когнитивные нарушения при болезни Паркинсона // Неврол. журн. – 2003; 8 (2): 11–16.
Захаров В. В., Яхно Н. Н. Нарушения памяти. – М.: ГеотарМед, – 2003. –С. 150.
Захаров В. В. Когнитивные нарушения у пациентов с болезнью Паркинсона // Журн. неврол. и психиатр. – 2005; 1: 13–19.
Захаров В. В. Деменция при болезни Паркинсона // Неврол. журн. –2006; 11 (приложение № 1): 13–18.
Захаров В. В. Всероссийская программа исследований эпидемиологии и терапии когнитивных расстройств в пожилом возрасте («Прометей») // Неврол. журн. – 2006; 11: 27–32.
Климов Л. В., Парфенов В. А. Когнитивные нарушения в остром периоде ишемического инсульта // Неврол. журн. – 2006; 11 (приложение 1): 53–56.
Левин О. С., Дамулин И. В. Диффузные изменения белого вещества (лейкоареоз) и проблема сосудистой деменции. В кн.: Достижения в нейрогериатрии. Под ред. Н. Н. Яхно, И. В. Дамулина. – Ч. 1. – С. 30–39.
Мхитарян Э. А., Преображенская И. С. Болезнь Альцгеймера и цереброваскулярные расстройства // Неврол. журн. – 2006; 11 (приложение 1): 31–36.
Парфенов В. А., Никитина Л. Ю. Доинсультные когнитивные нарушения. В кн.: IX Всероссийский съезд неврологов. Тезисы докладов. – С. 440.
Преображенская И. С. Когнитивные нарушения при деменции с тельцами Леви // Неврол. журн. – 2006. – Приложение 1. – С. 19–26.
Результаты Всероссийской переписи населения. //www.perepis.ru
Степкина Д. А., Захаров В. В. Прогрессирование когнитивных нарушений при болезни Паркинсона // Клин. геронтол. – 2007; 13 (8): 55–59.
Яхно Н. Н., Дамулин И. В., Бибиков Л. Г. Хроническая сосудистая мозговая недостаточность у пожилых: клинико-компьютерно-томографические сопоставления // Клин. геронтол. – 1995; 1: 32–36.
Яхно Н. Н., Левин О. С., Дамулин И. В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 1: двигательные нарушения // Неврол. журн. – 2001; 6 (2): 10–16.
Яхно Н. Н., Левин О. С., Дамулин И. В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения // Неврол. журн. – 2001; 6 (3): 10–19.
Яхно Н. Н., Преображенская И. С. Деменция с тельцами Леви // Неврол. журн. – 2003; 8 (6): 4–12.
Яхно Н. Н., Дамулин И. В., Мхитарян Э. А. Болезнь Альцгеймера и деменция с тельцами Леви: некоторые аспекты клиники, диагностики и лечения // Русск. мед. журн. – 2004; 11 (10): 567–570.
Яхно Н. Н., Локшина А. Б., Захаров В. В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии // Клин. геронтол. – 2005; 11 (9): 38–39.
Яхно Н. Н., Захаров В. В., Локшина А. Б. Синдром умеренных когнитивных нарушений при дисциркуляторной энцефалопатии // Журн. неврол. и психиатр. – 2005; 105 (2): 13–17.
Яхно Н. Н., Захаров В. В., Локшина А. Б. Нарушения памяти и внимания в пожилом возрасте // Журн. неврол. и психиатр. им. С. С. Корсакова. – 2006; 106 (2): 58–62.
Яхно Н. Н., Коберская Н. Н., Дамулин И. В. и соавт. Организация помощи пациентам с нарушениями памяти и других когнитивных функций // Неврол. журн. – 2006; 11 (приложение 1): 75–79.
Яхно Н. Н. Когнитивные расстройства в неврологической клинике // Неврол. журн. – 2006; 11 (приложение 1): 4–12.
Golomb J., Kluger A., Garrard P. et al. Clinician,s manual on mild cognitive impairment. – London: Science Press, 2001.
Iqbal K., Winblad B., Nishumura T. et al. Alzheimer's disease: biology, diagnosis and therapeutics // J. Willey and sons ltd, 1997.
Kosaka K., Yoshmura M., Ikeda K. et al. Diffuse type of Lewy bodies disease: Progressive dementia with abundant cortical Lewy bodies and senile changes of various degree 0- a new disease? // Clin. Neuropathol. – 1984; 3: 185–192.
Lovenstone S., Gauthier S. Management of dementia. –London: Martin Dunitz, 2001.
Pasquier F., Henon H., Leys D. Risk factors and mechanisms of post-stroke dementia // Rev Neurol. – 1999; 155 (9): 749–753.
Pasquier F., Leys D. Why are stroke patients prone to develop dementia? // J. Neurol. – 1997; 244 (3): 135–142.
Snowdon D.A., Greiner L.H., Mortimer J.A. et al. Brain infarction and the clinical expression of Alzheimer’s disease. The Nun Study // JAMA. – 1997; 277 (10): 813–817.
