Факторы риска и особенности течения рахита у детей раннего возраста в современных условиях 14. 01. 08 Педиатрия
| Вид материала | Автореферат |
- Психомоторное развитие недоношенных детей раннего возраста, родившихся в условиях йоддефицита, 317.2kb.
- Факторы риска, гомеостаз, распространенность и интенсивность кариеса у детей раннего, 234.91kb.
- Особенности терапевтической тактики при желчнокаменной болезни у детей раннего возраста, 450.78kb.
- Развитие речи детей раннего возраста в условиях группы кратковременного пребывания, 97.7kb.
- Клинико-морфологических особенности атрезии внепеченочных желчных протоков у детей, 334.57kb.
- Доклад на гмо воспитателей групп раннего возраста «Адаптация детей раннего возраста, 137.69kb.
- Тематический план лекций на V курсе лечебного факультета на 2011-2012 учебный год (осенний, 53.8kb.
- Тема : Периоды детского возраста. Этапы становления физического, моторного, нервно-психического, 249.01kb.
- Экологическое воспитание детей раннего и младшего дошкольного возраста через ознакомление, 97.13kb.
- Программа воспитания и обучения детей раннего возраста (от года до 3 лет), 1297.77kb.
На правах рукописи
ДМИТРИЕВА ЮЛИЯ АНДРЕЕВНА
ФАКТОРЫ РИСКА И ОСОБЕННОСТИ ТЕЧЕНИЯ РАХИТА У ДЕТЕЙ РАННЕГО ВОЗРАСТА В СОВРЕМЕННЫХ УСЛОВИЯХ
14.01.08 - Педиатрия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва - 2011
Работа выполнена в ГОУ ДПО Российская медицинская академия последипломного образования Росздрава
Научный руководитель: доктор медицинских наук
профессор Захарова Ирина Николаевна
Официальные оппоненты: доктор медицинских наук
профессор Мухина Юлия Григорьевна
доктор медицинских наук
профессор Яцык Галина Викторовна
Ведущая организация: ГОУ ВПО Московский государственный
медико-стоматологический университет
Защита состоится «___» __________ 2011 г. в ___часов на заседании диссертационного совета Д.208.071.01 при ГОУ ДПО Российская медицинская академия последипломного образования Росздрава по адресу: 123955, г.Москва, ул.Баррикадная, д.2/1
С диссертацией можно ознакомиться в фундаментальной библиотеке ГОУ ДПО РМАПО по адресу: 125445, г.Москва, ул.Беломорская, д.19
Автореферат разослан «____» ________ 2011 г.
Ученый секретарь
Диссертационного совета Зыков В.П.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ.
Актуальность проблемы. Рахит в России является одним из самых распространенных заболеваний среди детей первых лет жизни. По данным отечественных исследователей, заболеваемость рахитом к концу ХХ века составляла от 50 до 70% [Рывкин А.И.(1985), Коровина Н.А. с соавт.(1998), Запруднов А.М. с соавт. (1998)]. По данным Минздравсоцразвития РФ, в 2006 году распространенность рахита среди детей раннего возраста не превышала 51,05%.
Не вызывает сомнений, что младенческий рахит является не только педиатрической, но и медико-социальной проблемой. Перенесенный в раннем детстве рахит и связанное с ним нарушение накопления пиковой костной массы может предрасполагать к развитию остеопороза в последующем. Вследствие нарушения абсорбции кальция, фосфора, магния развивается мышечная гипотония, вегетативные дисфункции, нарушения моторики желудочно-кишечного тракта. Выявляемые при рахите иммунологические нарушения предрасполагают к частым инфекционным заболеваниям, нарушая социальную адаптацию ребенка [Коровина Н.А. с соавт. (2005), Струков В.И. (2004)].
В соответствии с существующими в России рекомендациями (1991), специфическая профилактика рахита проводится витамином D в дозе от 500 до 1000 МЕ, хотя отмечаются случаи использования и более высоких доз препарата. Высокая частота заболеваемости рахитом, несмотря на активную специфическую профилактику, требует уточнения его патогенеза в современных условиях и определения возможных причин неэффективности проводимых профилактических мероприятий.
К настоящему времени понимание рахита, как заболевания, обусловленного исключительно недостатком витамина D в организме, нельзя считать обоснованным. Ряд отечественных и зарубежных авторов указывают на то, что клинические проявления рахита у детей первого и второго года жизни недостаточно коррелируют с обеспеченностью организма витамином D [Мальцев С.В. с соавт. (1987), Демин В.Ф. (2003), DeLucia MC et al. (2003)]. Учитывая современные представления о метаболизме и физиологических функциях холекальциферола, значение его дефицита в патогенезе заболевания, очевидно, следует рассматривать не столько с позиции недостаточного поступления его в организм ребенка, сколько с учетом особенностей обмена витамина D под влиянием совокупности экзо- и эндогенных факторов, предрасполагающих к развитию рахитического процесса. Так, у младенцев, родившихся преждевременно, с задержкой внутриутробного развития ферментативная незрелость может проявляться нарушением фосфорно-кальциевого обмена, метаболизма витамина D и минерализации костной ткани, что определяет развитие клиники рахита даже на фоне проводимой специфической профилактики [Демин В.Ф. (2003), Мальцев С.В. (2010), Яцык Г.В. (2004)]. К развитию рахита могут приводить высокие темпы прибавки в массе и росте в первые месяцы жизни. Немаловажную роль в нарушении обмена холекальциферола D может сыграть наличие патологии со стороны желудочно-кишечного тракта (синдром мальабсорбции), печени, почек [Новиков П.В., (2006), Мухина Ю.Г., (2006)].
Основные факторы риска развития рахита впервые были определены А.И.Рывкиным в 1985 году. Однако в современных условиях исследований, направленных на уточнение структуры факторов риска рахита с учетом изменения социально-экономических условий жизни, состояния здоровья женщин репродуктивного возраста, особенностей физического развития и характера вскармливания младенцев, не проводилось. Открытым остается вопрос относительно того, при каком уровне 25(ОН)D3 (печеночного метаболита холекальциферола, отражающего обеспеченность организма ребенка витамином D), возможно развитие рахита и как коррелируют клинические проявления заболевания с биохимическими параметрами фосфорно-кальциевого обмена при сочетанном воздействии экзогенных и эндогенных факторов риска. Не вызывает сомнения, что недостаток данных, характеризующих особенности течения рахита в настоящее время, затрудняет разработку современных рекомендаций по диагностике, профилактике и лечению заболевания.
Цель работы - установить особенности клинических и лабораторных маркеров рахита у детей раннего возраста в современных условиях для оптимизации профилактики и лечения заболевания.
Задачи исследования:
- Определить факторы риска развития рахита на современном этапе.
- Установить взаимосвязь между клиническими проявлениями рахита и лабораторными показателями фосфорно-кальциевого обмена в зависимости от степени тяжести и активности патологического процесса.
- Определить содержание активных метаболитов витамина D в сыворотке крови у детей с рахитом для уточнения роли гиповитаминоза D в этиологии заболевания.
- Оценить эффективность профилактики рахита в зависимости от сочетания факторов риска развития заболевания.
Научная новизна.
Впервые установлены особенности метаболизма витамина D в зависимости от степени тяжести и активности рахитического процесса. Доказана достоверная прямая корреляционная связь (r=0,8, p<0,001) между печеночным [25(ОН)D3] и почечным [1,25(ОН)2D3] метаболитами холекальциферола при рахите у детей, наиболее выраженная в период начальных проявлений заболевания. Установлено, что вегетативные симптомы рахита сопровождаются снижением уровня 25(ОН)D3 у 62,5% младенцев.
Показано, что наибольшее значение в патогенезе рахита в современных условиях играют факторы риска эндогенного происхождения, наиболее значимыми из которых являются ускоренные темпы прибавки в массе и росте на первом году жизни, а также сопутствующие заболевания, обнаруженные более, чем у 50% обследованных. Сравнительный анализ факторов риска рахита, выявляемых в настоящее время и описанных Рывкиным А.И. 26 лет тому назад, свидетельствует об увеличении доли детей с рахитом, рожденных от патологически протекавшей беременности, имеющих высокие темпы физического развития и находящихся на грудном вскармливании. Анализ клинико-анамнестических сведений младенцев, имевших в анамнезе начальные проявления рахита, показал клиническую эффективность назначения 1000-2000 МЕ витамина D на данной стадии заболевания.
Практическая значимость.
Показано, что клинические проявления рахита у младенцев могут отмечаться и при нормальном уровне кальция, фосфора и витамина D, что свидетельствует о необходимости адекватного клинического обследования ребенка для выявления характерных симптомов рахита, включая начальные проявления заболевания.
Выявленные особенности фосфорно-кальциевого обмена и метаболизма витамина D у младенцев, имеющих только вегетативные симптомы рахита, определяют необходимость ранней диагностики и терапии заболевания в период его начальных проявлений.
Доказано, что при сочетанном влиянии неблагоприятных экзогенных и эндогенных факторов рахит у ребенка может развиваться даже при дополнительном назначении препаратов витамина D, что определяет важную роль неспецифической профилактики рахита в современных условиях с коррекцией сопутствующих факторов риска.
Установлено, что костные изменения могут прогрессировать после стихания активности рахитического процесса в условиях недостаточного обеспечения кальцием ребенка второго полугодия жизни. Это указывает на необходимость профилактики нарастания остеопении после перенесенного рахита путем коррекции рациона питания или дополнительного назначения препаратов кальция.
Связь с научными программами, планами, темами.
Диссертация выполнена в соответствии с отраслевой научно-исследовательской программой ГОУ ДПО РМАПО Росздрава, осуществляемой на кафедре педиатрии. Тема диссертации утверждена на заседании Совета педиатрического факультета ГОУ ДПО РМАПО Росздрава (протокол №4 от 14 апреля 2009 года).
Основные положения диссертации, выносимые на защиту:
- В структуре факторов риска развития рахита в современных условиях преобладают факторы эндогенного происхождения, обуславливающие особенности фосфорно-кальциевого обмена и метаболизма витамина D в организме ребенка.
- При сочетании определенных факторов риска рахит у детей раннего возраста развивается вне зависимости от характера вскармливания и проведения специфической профилактики препаратами витамина D.
- Клинические проявления легких форм рахита в современных условиях в большинстве случаев не сопровождаются типичными биохимическими изменениями в виде гипокальциемии и гипофосфатемии и возникают на фоне нормального содержания витамина D в организме ребенка.
- Особенности метаболизма витамина D на стадии начальных вегетативных проявлений рахита определяют эффективность проведения терапевтических мероприятий в раннем периоде заболевания.
Внедрение результатов исследования в практику. Результаты проведенного исследования включены в программу лекций, семинаров, практических занятий для специалистов, проходящих обучение на кафедрах педиатрии ГОУ ДПО РМАПО Росздрава. Основные положения работы были представлены на конференциях молодых ученых ГОУ ДПО РМАПО Росздрава и ГОУ ДПО Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию, XVIII Российском национальном конгрессе «Человек и лекарство» (2011), а также на международных конференциях 26th International pediatric association congress of pediatrics (2010) и 4th International Symposium on Trace Elements and Minerals in Medicine and Biology (2010).
Апробация работы. Апробация диссертации состоялась на совместной конференции сотрудников кафедры педиатрии ГОУ ДПО РМАПО Росздрава и врачей Тушинской детской городской больницы г. Москвы 9 марта 2011 года.
Личный вклад автора. Автор лично проводила подбор, клинико-анамнестическое обследование пациентов, забор анализов для лабораторного исследования, оценку полученных данных и их статистическую обработку.
Публикации. По теме диссертации опубликовано 10 печатных работ, в том числе 3 работы - в рецензируемых научных журналах, определённых Высшей аттестационной комиссией. Одна работа опубликована в международном издании.
Объем и структура диссертации. Диссертация изложена на 123 страницах машинописного текста, состоит из введения, обзора литературы, описания методов и объема исследований, результатов собственных исследований, обсуждения результатов, выводов, практических рекомендаций и списка литературы, включающего 40 отечественных и 72 зарубежных источника. Работа иллюстрирована 20 таблицами, 13 рисунками и 4 клиническими примерами.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования.
Работа выполнена на кафедре педиатрии ГОУ ДПО РМАПО Росздрава с участием лабораторной службы компании «ГЕМОТЕСТ» (Москва) в период с 2008 по 2011 год. Набор детей проводился на базе отделений Тушинской детской городской больницы г. Москвы. Поводом для госпитализации детей в стационар явились острые инфекционные заболевания (ОРВИ, отит, бронхит, пневмония), инфекция мочевой системы, функциональные нарушения желудочно-кишечного тракта, атопический дерматит. Осмотр пациентов и забор анализов для лабораторных исследований производились в течение первых 3 суток от момента госпитализации.
В настоящее исследование было включено 179 детей в возрасте от 2 до 30 месяцев. Критериями включения в исследование явилось наличие у пациентов в анамнезе или при клиническом обследовании симптомов рахита. Диагностика заболевания основывалась на выявлении при клиническом обследовании характерных для рахита вегетативных симптомов (потливость волосистой части головы, разлитой красный дермографизм), мышечной гипотонии и/или признаков остеомаляции и остеоидной гиперплазии со стороны костной системы. Указанные вегетативные симптомы нами относились к проявлениям рахита в том случае, если они отсутствовали у ребенка с рождения, появлялись к возрасту 2-4 месяцев на фоне активного роста и предшествовали или сочетались с характерными костными изменениями. Дополнительным критерием, позволившим относить симптомы вегетативной дисфункции к проявлениям рахита у младенцев, явилось уменьшение их выраженности или исчезновение при дополнительном назначении ребенку витамина D. Диагноз разгара рахита устанавливался в случае, если вегетативные и костные проявления заболевания сопровождались повышением уровня щелочной фосфатазы в сыворотке крови. Повышение щелочной фосфатазы является самым ранним лабораторным признаком разгара рахита, что позволяет его использовать в качестве маркера активности заболевания [Шабалов Н.П. (2003), Романюк Ф.П. с соавт. (2002)]. Остаточные явления рахита диагностировались в случае наличия у ребенка костных проявлений при нормальном уровне щелочной фосфатазы. В соответствии с данными клинического осмотра и результатами лабораторных исследований дети были распределены на 4 группы.
Первую группу (n=54) составили дети с рахитом в период разгара заболевания. В составе данной группы было выделено 2 подгруппы:
- подгруппу А (n=16) составили дети, у которых при осмотре были выявлены симптомы вегетативной дисфункции (потливость волосистой части головы, разлитой стойкий красный дермографизм), в ряде случаев - в сочетании с умеренной мышечной гипотонией, при отсутствии признаков остеоидной гиперплазии или остеомаляции;
- подгруппу В (n=38) составили младенцы, у которых клинические симптомы рахита включали в себя проявления как со стороны вегетативной, так и костно-мышечной системы. Среди пациентов данной подгруппы преобладали дети с рахитом легкой степени (73,7%). Доля детей с рахитом средней степени тяжести составила 26,3%, детей с тяжелыми формами рахита в ходе нашего исследования выявлено не было.
Во вторую группу (n=31) вошли дети с остаточными явлениями рахита.
Третью группу (n=32) составили дети, у которых на момент осмотра признаки рахита выявлены не были, однако в анамнезе у них отмечались вегетативные проявления начального периода заболевания, которые были купированы путем коррекции витамином D, что позволило предотвратить развитие костных проявлений.
Группу сравнения (n=62) составила младенцы, не имеющие симптомов рахита.
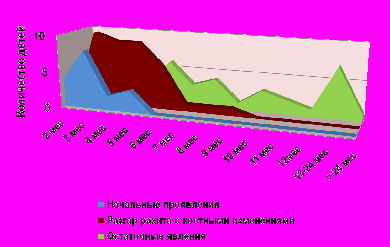
Рис 1. Распределение детей в зависимости от стадии рахита.
Среди детей с разгаром рахита преобладали младенцы первого полугодия жизни, средний их возраст на момент постановки диагноза составил 4,55±0,25 мес. В группе детей с остаточными симптомами заболевания преобладали дети второго полугодия жизни, средний возраст обследованных составил 10,7±1,1 мес. (рис. 1).
Общий объем проведенных исследований представлен в табл. 1.
Таблица 1.
Объём проводимых исследований.
| Исследования | Количество |
| Клинико-анамнестическое обследование | 179 |
| Оценка физического развития | 179 |
| Биохимический анализ крови | 117 |
| Определение метаболитов витамина D в сыворотке крови | 85 |
| Статистическая обработка данных | |
| ВСЕГО: | 560 |
Сбор анамнеза осуществлялся путём опроса родителей и анализа амбулаторных карт детей с занесением полученных данных в специально разработанные индивидуальные карты пациентов. На основании полученной информации проводилась оценка соматического и акушерско-гинекологического анамнеза матерей, условий жизни семьи, особенностей течения беременности, родов и раннего неонатального периода, характера вскармливания, сроков введения прикорма, состояния специфической профилактики рахита витамином D. Фиксировались динамика массо-ростовых показателей ребенка и перенесенные им заболевания. При сборе анамнеза особое внимание уделялось выявлению возможных факторов риска, предрасполагающих к развитию рахита, как со стороны матери, так и со стороны ребенка.
Осмотр детей проводился в отделениях Тушинской детской городской больницы и включал в себя оценку физического развития, общесоматического статуса ребенка с целью выявления у него симптомов рахита. Исследование физического развития детей проводилось с использованием методов антропометрии и анализа полученных результатов в соответствии с центильными таблицами. Помимо оценки физического развития изучалась динамика антропометрических показателей на основании эмпирических формул.
Лабораторные методы исследования включали проведение биохимического анализа крови обследуемых пациентов и определение содержания в сыворотке метаболитов витамина D [25(ОН)D3 и 1,25(ОН)2D3]. Биохимический анализ крови проводился в лаборатории Тушинской детской городской больницы (зав. лабораторией Гавеля Н.В.) и включал определение уровня общего и ионизированного кальция, фосфора и щелочной фосфатазы. Анализ крови проводился натощак. Изучение биохимических параметров младенцев производилось с использованием анализаторов SAPPHIRE 400, SUPER Z Analyzer и RAPID. Уровень общего кальция и фосфора изучался с помощью фотометрического метода. Для определения щелочной фосфатазы использовался кинетический фотометрический тест – оптимизированный стандартный метод в соответствии с рекомендациями DGKS (Германское Общество Клинической Химии). Концентрация ионизированного кальция в сыворотке крови измерялась с помощью ионселективных электродов. Определение метаболитов витамина D проводилось в лаборатории ГЕМОТЕСТ (Москва) методом высокоэффективной жидкостной хроматографии. В качестве основного маркера обеспеченности организма витамином D рассматривался уровень печеночного метаболита витамина D - 25-гидроксихолекальциферола. Содержание витамина D в организме признавалось достаточным при уровне 25(ОН)D3 выше 30 нг/мл. Снижение содержания метаболита ниже 30 нг/мл свидетельствовало о недостаточной обеспеченности организма ребенка холекальциферолом, при уровне 25(ОН)D3 менее 20 нг/мл констатировался дефицит витамина D.
Полученные результаты исследования обрабатывались статистически с помощью программ "Microsoft Excel 2007" , BIOSTAT. В ходе статистического анализа вычислялись следующие показатели: среднее арифметическое значение (M) и стандартная ошибка среднего (m), доли пациентов с тем или иным показателем и ошибка доли. Статистическая значимость различий изучалась с помощью параметрических критериев (t критерий Стьюдента). При этом статистически значимыми считались отличия при p<0,05. Связь между изучаемыми показателями оценивалась по результатам корреляционного анализа с вычислением коэффициента корреляции Пирсона (r).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ.
В ходе анализа анамнестических данных пациентов, включенных в настоящее исследование, установлено, что у всех исследуемых детей имелись факторы риска, предрасполагающие к развитию рахитического процесса.
Доказано, что ведущими факторами риска развития рахита на современном этапе являются ускоренные темпы прибавки в массе и росте на первом году жизни (67,5%) и сопутствующие заболевания со стороны органов, участвующих в метаболизме витамина D в организме ребенка (патология ЖКТ и почек) (53,8%). Указанные факторы риска среди детей с рахитом встречались достоверно чаще (р<0,05), нежели в группе здоровых детей. Установлена большая заболеваемость рахитом детей, родившихся от матерей с экстрагенитальной патологией (21,4%), имеющих вредные привычки (23,1%) или проживающих в неблагополучных социально-экономических условиях (25,6%). У 23% детей с рахитом в анамнезе чаще отмечались повторные ОРЗ.
Нами проведено сравнение факторов риска развития рахита в современных условиях с таковыми, выявленными в исследовании А.И.Рывкина в 1985 году. Установлено, что за прошедшие 26 лет отмечен достоверный (p<0,001) рост числа детей с рахитом, рожденных от женщин старше 25 лет (29,1±1,5% и 42,5±4,6% соответственно). При этом доля младенцев с рахитом, рожденных от молодых матерей, достоверно (p<0,001) уменьшилась (45,6±1,7% и 27,4±4,1%, соответственно). Обращало на себя внимание достоверное (p<0,05) увеличение частоты патологического течения беременности у женщин (42,8±1,7% и 55,5±4,6%). Среди детей с рахитом в настоящее время достоверно (p<0,01) увеличилась доля младенцев, имеющих ускоренные темпы прибавки в массе и росте (53,9±1,7% и 67,5±4,3%).
Анализ состояния специфической профилактики рахита в исследуемой группе продемонстрировал, что заболевание у детей раннего возраста развивалось даже в случае дополнительного приема витамина D. Специфическая профилактика рахита не проводилась у 45,3±4,6% обследованных, в то время как 54,7±4,6% младенцев регулярно получали препараты холекальциферола. Обращало на себя внимание, что в современных условиях достоверно увеличилась частота рахита среди младенцев, которым регулярно проводилась специфическая профилактика заболевания (31,3±1,6% и 54,7±4,6%, p<0,001). Полученные данные подтверждают положение о том, что в настоящее время ведущую роль в патогенезе рахита играет не столько экзогенный дефицит витамина D, сколько особенности его метаболизма под влиянием совокупности факторов риска эндогенного происхождения.
В ходе проведенного исследования установлено, что рахиту подвержены дети вне зависимости от характера вскармливания. В 51,3±4,6% случаев исследуемые младенцы в первые 6 месяцев жизни вскармливались исключительно или преимущественно грудью, 47,0±4,6% детей находились на раннем искусственном вскармливании адаптированными молочными смесями, 2 ребенка (1,7±1,2%) получали грудное молоко и молочную смесь в равных соотношениях. За прошедшие 26 лет отмечено достоверное снижение частоты рахита среди младенцев, находящихся на раннем искусственном вскармливании (60,1±1,7% и 47,0±4,6%, p<0,01), что, очевидно, связано усовершенствованием рецептуры детских смесей. Современной тенденцией производства молочных смесей является их адаптация по белковому, углеводному и жировому компонентам и обогащение комплексом витаминов и микроэлементов. Большинство современных формул в настоящее время содержат 400 МЕ/л холекальциферола, а также кальций и фосфор в оптимальном соотношении 1,8-2:1, обеспечивающим максимальное усвоение элементов в желудочно-кишечном тракте младенца.
Анализ зависимости тяжести рахита от характера вскармливания и состояния специфической профилактики в современных условиях продемонстрировал, что на фоне грудного вскармливания и дополнительного приема витамина D рахит имеет тенденцию к более легкому течению. Так, среди детей с начальными проявлениями заболевания половина младенцев (50,0±12,5%) получала дополнительно витамин D, в то время, как ни одному ребенку с рахитом средней степени тяжести специфическая профилактика рахита витамином D не проводилась. Среди пациентов с начальными проявлениями заболевания преобладали дети, вскармливаемые грудным молоком (75,0±10,5%). По мере нарастания тяжести рахитического процесса увеличивалась доля детей, находящихся на искусственном вскармливании.
Анализ заболеваемости рахитом в зависимости от календарной даты рождения ребенка продемонстрировал, что наибольшее количество больных рахитом детей родились в июле (18,8%), а наименьшее – в феврале месяце – 0,85%. Большинство (69,2±4,3%) обследованных нами детей с рахитом были рождены в период с июня по ноябрь месяц. Полученные данные согласуются с результатами исследования Рывкина А.И., указавшего на аналогичную зависимость заболеваемости рахитом от активности ультрафиолетового излучения.
В ходе клинического обследования достоверных различий в показателях физического развития в наблюдаемых группах детей нами не установлено. Обращало на себя внимание, что среди 3 группы пациентов, у которых начальные проявления рахита были купированы до развития костных изменений, отсутствовали дети с низким или ниже среднего физическим развитием, в то время как среди пациентов с остаточными явлениями рахита доля детей с данными вариантами физического развития составила 3,2% и 16,1% (соответственно).
В структуре клинических симптомов рахита в период разгара заболевания преобладали вегетативные проявления (96,3%), мышечная гипотония (72,2%) и изменения со стороны костей черепа (68,5%). В 31,5% случаев определялась развернутая нижняя апертура грудной клетки, у 12,9% пациентов - «четки» на ребрах. У одного ребенка 1 группы (1,9%) обнаружены «браслеты» на запястьях. В 40,7% случаев обращало на себя внимание медленные темпы закрытия большого родничка, а у 2 детей второго полугодия жизни (3,7%) отсутствовали зубы. При оценке навыков и умений детей обращало на себя внимание, что 29,6% младенцев отставали в моторном развитии. Клиническая картина рахита в период остаточных явлений характеризовалась преимущественно изменениями со стороны костей черепа в виде лобных и теменных бугров (77,4%) и уплощения затылка (25,8%), а также наличием деформации грудной клетки в виде развернутой нижней апертуры у большинства обследованных детей, которая во второй группе наблюдения встречалась достоверно чаще, чем в первой (87,1% и 31,5%, соответственно, р<0,001). Обращало на себя внимание, что кифосколиотическая деформация позвоночника (16,1%) и деформация нижних конечностей (12,9%) были выявлены нами только в период остаточных явлений заболевания у детей второго полугодия жизни (средний возраст 14,5±3,3 и 16±3,4 месяцев, соответственно). Нельзя исключить, что формирование данных костных изменений происходило уже после купирования активной фазы заболевания в период максимальной нагрузки на данные отделы костной системы к моменту вертикализации ребенка и начала ходьбы.
Анализ биохимических показателей фосфорно-кальциевого обмена был проведен с учетом активности рахитического процесса и степени тяжести заболевания. Обращало на себя внимание отсутствие у большинства обследованных нами пациентов ранее описанных в литературе типичных для рахита биохимических изменений в виде гипокальциемии и гипофосфатемии в период разгара заболевания. Уровень общего кальция в сыворотке крови у подавляющего большинства детей с рахитом оставался в пределах нормы. Более чувствительным маркером нарушений фосфорно-кальциевого обмена при рахите явился уровень ионизированного кальция, снижение которого было зафиксировано у 33,3% детей в период разгара заболевания. Уровень фосфора в сыворотке оставался в пределах нормальных значений у подавляющего большинства детей вне зависимости от активности рахитического процесса. Снижение содержания элемента было выявлено лишь у 5 пациентов (9,2%) 1 группы наблюдения, 3 из которых имели клинику начальных проявлений заболевания (рис.2).
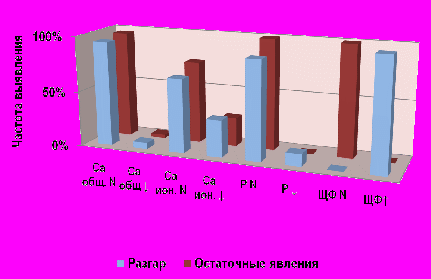
Рисунок 2. Частота нарушений фосфорно-кальциевого обмена в зависимости от стадии рахита.
Анализируя динамику показателей фосфорно-кальциевого обмена в зависимости от степени тяжести рахитического процесса, нами отмечена тенденция к снижению уровня ионизированного кальция и повышению активности щелочной фосфатазы по мере нарастания выраженности симптомов заболевания (табл.2).
Таблица 2.
Изменения фосфорно-кальциевого обмена в зависимости от степени тяжести рахита.
| Показатель | Группа 1 (n=54) | ||
| Подгруппа А | Подгруппа В | ||
| Начальные проявления рахита (n=16) | Рахит легкой степени (n=28) | Рахит средне-тяжелой степени (n=10) | |
| Са(общ), ммоль/л | 2,24±0,03 | 2,34±0,03 | 2,44±0,04 |
| Са (ион), ммоль/л | 1,2±0,03 | 1,19±0,04 | 1,09±0,05 |
| Р, ммоль/л | 1,95±0,16 | 1,79±0,08 | 1,89±0,15 |
| ЩФ, ед/л | 560,9±25,0 | 600,2±22,5 | 712,4±96,7 |
Исследование содержания метаболитов витамина D [25(ОН)D3 и 1,25(OH)2D3] было проведено у 85 детей с клиническими симптомами рахита на момент включения в исследование.
Установлено, что в период разгара рахита достоверно чаше (p<0,05) отмечалось снижение как печеночного, так и почечного метаболита витамина D (табл.3). Средний уровень исследуемых метаболитов в первой группе детей был достоверно (p<0,01) ниже аналогичного показателя у детей второй группы наблюдения и составил, соответственно, 29,3±1,6 нг/мл и 40,8±1,9 нг/мл для 25(ОН)D3 и 30,7±2,4 пг/мл и 43,2±2,5 пг/мл для 1,25(OH)2D3 (табл.3). Обращало на себя внимание, что среди детей с уровнем 25(ОН)D3 менее 30 нг/мл отмечалось снижение среднего уровня метаболита по мере нарастания тяжести рахитических изменений (22,0±1,3 нг/мл - при начальных проявлениях, 18,8±1,2 нг/мл - при легкой степени и 18,0±1,9 нг/мл - при средней тяжести).
Таблица 3.
Частота снижения уровня 25(ОН)D3 и 1,25(OH)2D3 в зависимости от степени тяжести и активности рахита.
| Уровень метаболитов | Группа 1 (n=54) | Группа 2 (n=31) | |||
| Подгруппа А (n=16) | Подгруппа В | Всего (n=54) | |||
| Рахит легкой степени (n=28) | Рахит средне-тяжелой степени (n=10) | ||||
| 25(ОН)D3 < 20 нг/мл | 4 | 5 | 3 | 12 22,2±5,7%** | 1 3,2±3,1%** |
| 25(ОН)D3 20-30 нг/мл | 6 | 6 | 1 | 13 24,1±5,8% | 4 12,9±6,0% |
| Всего 25(ОН)D3 < 30 нг/мл | 10 62,5±12,1%* | 11 39,3±7,9%* | 4 25±13,7%* | 25 46,3±6,8%** | 5 16,1±6,6%** |
| 1,25(OH)2D3 < 20 пг/мл | 5 31,2±11,6%* | 7 25,0±7,8%* | 3 30±14,5%* | 15 27,8±6,1%** | 2 6,4±4,4%** |
*примечание: частота снижения уровня 25(ОН)D3 указана по отношению к количеству детей в подгруппах
**достоверность различия между показателями p<0,05
С целью оценки влияния экзогенных и эндогенных факторов на метаболизм витамина D у младенцев с рахитом, нами была проанализирована структура этих факторов в зависимости от содержания 25-гидроксихолекальциферола в организме детей. Показано, что недостаточное содержание витамина D в организме чаще отмечалось у недоношенных, младенцев, рожденных с признаками внутриутробной гипотрофии, а также среди пациентов, имеющих интеркуррентные заболевания и ускоренные темпы роста (рис.3).
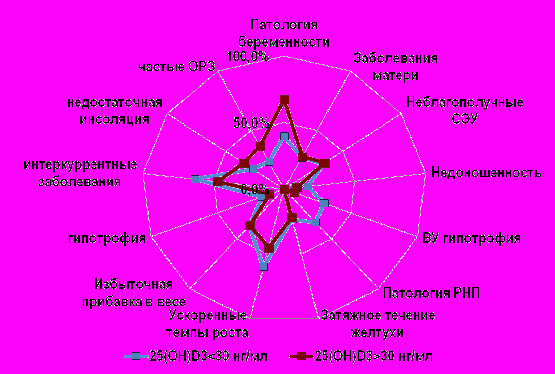
Рисунок 3. Влияние факторов риска на метаболизм витамина D у детей с рахитом.
Учитывая выявленную нами зависимость между тяжестью рахитического процесса и уровнем 25(ОН)D3 у младенцев со сниженным уровнем метаболита, можно полагать, что эта группа детей предрасположена к более тяжелому течению заболевания и особенно нуждаются в адекватно проводимой специфической профилактике рахита препаратами витамина D.
Анализ зависимости уровня 25-гидроксихолекальциферола от характера вскармливания и состояния специфической профилактики рахита витамином D продемонстрировал, что среди пациентов с низким содержанием 25(ОН)D3 доля детей, не получавших с целью профилактики витамин D, была выше, чем среди детей с достаточным уровнем метаболита (56,7±9,0% и 38,2±6,6% соответственно). Недостоверно чаще (p=0,1) снижение 25(ОН)D3 отмечалось среди младенцев, находившихся на грудном вскармливании (табл.4).
Таблица 4.
Влияние характера вскармливания и дополнительного приема витамина D на содержание 25(ОН)D3 в организме.
| Характер вскармливания | 25(ОН)D3 < 30 нг/мл (n=30) | 25(ОН)D3 > 30 нг/мл (n=55) | р | ||
| абс.ч. | % | абс.ч. | % | ||
| Грудное вскармливание | 7 | 23,3±7,7% | 5 | 9,1±3,9% | >0,05 |
| Искусственное вскармливание | 10 | 33,3±8,6% | 16 | 29,1±6,1% | >0,05 |
| Грудное вскармливание + витамин D | 11 | 36,7±8,8% | 18 | 32,7±6,3% | >0,05 |
| Искусственное вскармливание + витамин D | 2 | 6,7±4,6% | 16 | 29,1±6,1% | <0,05 |
Установлено, что как в разгар рахита, так и период остаточных явлений заболевания отмечается прямая достоверная корреляция (r=0,8, p<0,001) между уровнем 25(ОН)D3 и 1,25(OH)2D3 в организме ребенка. Наиболее сильная корреляция между уровнем 25(ОН)D3 и 1,25(OH)2D3 отмечалась на стадии начальных проявлений рахита, что указывает на активность метаболизма витамина D на ранних стадиях заболевания.
Нами были проанализированы клинико-анамнестические сведения детей 3 группы исследования, имевших в анамнезе характерные начальные проявления рахита, которые были купированы до развития костных изменений путем коррекции витамином D.
Распределение детей данной группы в зависимости от характера вскармливания и состояния специфической профилактики рахита представлено на рисунке 4.
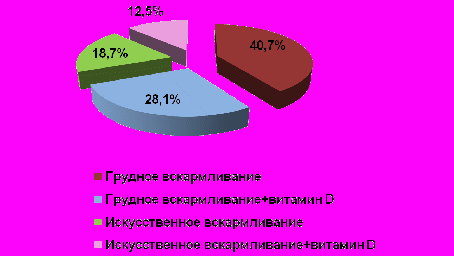
Рисунок 4. Характер вскармливания и состояние специфической профилактики рахита в 3 группе наблюдения.
Вегетативные нарушения в виде беспокойства, потливости волосистой части головы, отмечающиеся при плаче, кормлении или во время сна ребенка и сопровождающиеся облысением затылка, наблюдались у детей, в среднем, в возрасте 2,3±0,13 мес. Появление указанных симптомов послужило поводом к назначению витамина D или увеличению его дозы до 1000-2000 МЕ (табл.5).
Прием витамина D в указанной дозировке приводил к купированию вегетативных симптомов заболевания в течение 1-1,5 месяцев.
Таблица 5.
Частота назначения различных дозировок витамина D
при начальных проявлениях рахита в зависимости от характера вскармливания
| Дозы витамина D | Грудное вскармливание | Искусственное вскармливание | ||
| абс.ч. | % | абс.ч. | % | |
| 1000 МЕ | 7 | 21,9±7,3% | 7 | 21,9±7,3% |
| 1500 МЕ | 8 | 25±7,7% | 2 | 6,2±4,3% |
| 2000 МЕ | 4 | 12,5±5,8% | 4 | 12,5±5,8% |
Полученные данные в сочетании с результатами анализа особенностей фосфорно-кальциевого обмена и метаболизма витамина D указывают на целесообразность проведения терапевтических мероприятий на стадии вегетативных проявлений рахита и могут лежать в основе дальнейших исследований по отработке эффективных лечебных доз витамина D, показанных младенцам в начальный период заболевания.
Установлено, что в период остаточных явлений рахита у детей преобладают симптомы остеомаляции. Только в данной группе наблюдения нами были выявлены кифосколиотическая деформация позвоночника и деформация нижних конечностей. Средний возраст пациентов с данными симптомами составил 14,5±3,3 мес. и 16±3,4 мес. (соответственно). С целью уточнения возможных причин формирования костных изменений в период стихания рахитического процесса нами был проанализирован рацион питания детей второй группы наблюдения. Установлено, что 40,7±9,5% детей в возрасте старше 6 месяцев не употребляли творог или ели его нерегулярно. Обращало на себя внимание, что деформация позвоночника и нижних конечностей отмечались только среди этих пациентов. В отсутствие творога в рационе у детей чаще определялось снижение уровня ионизированного кальция в сыворотке крови, чем при регулярном употреблении продукта (36,4% и 25% соответственно). Среднее содержание ионизированного кальция при регулярном использовании продукта составил 1,2±0,03 ммоль/л, при отсутствии творога в рационе – 1,16±0,04 ммоль/л.
Таким образом, профилактика и лечение рахита могут быть эффективными только если проводятся с учетом существующих факторов риска и особенностей течения данного заболевания. Полученные нами данные определяют необходимость дальнейших исследований с целью разработки современных рекомендаций по ведению данной группы пациентов.
Выводы:
- В патогенезе рахита в современных условиях ведущую роль играет сочетание факторов риска эндогенного происхождения, определяющих особенности фосфорно-кальциевого обмена и метаболизма витамина D. Наиболее значимыми факторами риска развития рахита в настоящее время являются ускоренные темпы прибавки в массе и росте на первом году жизни и сопутствующие заболевания со стороны органов, участвующих в метаболизме витамина D в организме ребенка (патология ЖКТ и почек), отмечающиеся в 67,5% и 53,8% случаев.
- В современных условиях рахиту подвержены дети вне зависимости от характера вскармливания и проводимой специфической профилактики, при этом на фоне грудного вскармливания и дополнительного назначения витамина D заболевание протекает в более легкой форме.
- Рахит в современных условиях характеризуется преимущественно подострым течением (78,9%) с преобладанием в клинической картине легких форм заболевания (73,7%). Высокий удельный вес детей с преобладанием симптомов остеомаляции в период остаточных явлений рахита (38,7%) определяет необходимость их динамического наблюдения для обеспечения адекватного поступления в организм кальция с целью профилактики нарастания остеопении в последующем.
- При рахите у детей раннего возраста отмечается прямая достоверная корреляция (r=0,8, p<0,001) между содержанием печеночного [25(ОН)D3] и почечного [1,25(ОН)2D3] метаболитов холекальциферола, что подтверждает четкую зависимость гормонально активной формы витамина D от обеспеченности организма холекальциферолом.
- Выявленные особенности фосфорно-кальциевого обмена и метаболизма витамина D в период вегетативных проявлений рахита [повышение активности щелочной фосфатазы в 100% случаев, снижение уровня 25(ОН)D3 у 62,5% обследованных, сильная прямая корреляционная связь между 25(ОН)D3 и 1,25(ОН)2D3 (r=0,77, p<0,001)] и положительная динамика клинических симптомов на фоне дополнительного назначения витамина D указывают на эффективность и целесообразность проведения терапевтических мероприятий на стадии начальных симптомов заболевания.
практические рекомендации
- Специфическая профилактика рахита в современных условиях должна проводиться с учетом факторов риска, среди которых особое значение имеют сопутствующая патология ЖКТ и почек, ускоренные темпы прибавки в массе и росте на первом году жизни, а также недоношенность, внутриутробная гипотрофия и патология раннего неонатального периода.
- Детям второго полугодия жизни с клиническими проявлениями рахита целесообразно проведение профилактики дефицита кальция путем назначения творога. При невозможности введения продукта может потребоваться дополнительное назначение препаратов кальция.
- При наблюдении за ребенком первых месяцев жизни необходимо обращать внимание на начальные характерные вегетативные проявления рахита в виде потливости волосистой части головы, возникающей при беспокойстве, кормлении или во время сна ребенка, которые требуют своевременного назначения витамина D с целью предотвращения развития костных проявлений.
Список научных работ, опубликованных по теме диссертации
- Коровина Н.А., Захарова И.Н., Дмитриева Ю.А. Рахит: профилактика и лечение.// Consilium medicum.-2008.-№3.- с.77-82.
- Коровина Н.А., Захарова И.Н., Дмитриева Ю.А. Современные представления о физиологической роли витамина D у здоровых и больных детей.// Педиатрия.- 2008.-т.87.-№4.- с.124-129.
- Захарова И.Н., Коровина Н.А., Овсянникова Е.М., Дмитриева Ю.А., Суркова Е.Н. Профилактика дефицита кальция у детей первого года жизни.// Вопросы практической педиатрии.-2010.-т.5.-№1. - с.63-68.
- Захарова И.Н., Коровина Н.А., Дмитриева Ю.А. Роль метаболитов витамина D при рахите у детей.// Педиатрия.-2010.-т.89.-№3.- с.68-73
- Дмитриева Ю.А. Современные особенности рахита у детей раннего возраста.// Материалы конференции молодых ученых, посвященной 80-летию РМАПО - Москва, 2010 - с.17.
- Дмитриева Ю.А. Современный взгляд на рахит у детей раннего возраста.// Материалы юбилейной конференции молодых ученых «Актуальные вопросы клинической и экспериментальной медицины».- СПбМАПО.-2010.-с.316.
- Дмитриева Ю.А. Рахит и гиповитаминоз D.// Материалы XXXII итоговой конференции молодых ученых. ГОУ ВПО Государственный медико-стоматологический университет.-2010.-с.105-106.
- Захарова И.Н., Коровина Н.А., Боровик Т.Э., Дмитриева Ю.А. Рахит и гиповитаминоз D – новый взгляд на давно существующую проблему./Пособие для врачей. - Москва, 2011.-96 с.
- Zakharova I.N., Dmitrieva Y.A. Vitamin D metabolism in children with rickets.// Trace elements in medicine.-2010.-vol.11.-№2.- p.39.
- Zakharova I.N., Dmitrieva Y.A. Rickets as a multifactorial disease.// The 26th International pediatric association congress of pediatrics.- 2010.- A-235-0012-00509
СПИСОК СОКРАЩЕНИЙ
25(ОН)D3 – 25-гидроксихолекальциферол (печеночный метаболит витамина D)
1,25(ОН)2D3 – 1,25-дигидроксихолекальциферол (кальцитриол, почечный метаболит витамина D)
Ca общ. – общий кальций
Са ион. – ионизированный кальций
Р – фосфор
ЩФ – щелочная фосфатаза
ЖКТ – желудочно-кишечный тракт
