Ранняя диагностика и профилактика рака почки на основе клинико эпидемиологического исследования 14. 00. 40 «урология» 14. 00. 33 «общественное здоровье и здравоохранение»
| Вид материала | Автореферат диссертации |
- Академия Кафедра «Общественное здоровье и здравоохранение», 807.94kb.
- Программа по дисциплине «Общественное здоровье и здравоохранение», 120.06kb.
- Примерная программа дисциплины общественное здоровье и здравоохранение Для студентов, 386.71kb.
- Рабочая программа дисциплины общественное здоровье и здравоохранение I. Цели и задачи, 1223.51kb.
- Совместный курс последипломного образования для врачей и молодых специалистов «Заболевания, 17.1kb.
- Квалификационный тест по специальности «организация здравоохранение и общественное, 1347.84kb.
- План статистического исследования, его содержание, 81.37kb.
- План занятий по общественному здоровью и здравоохранению для студентов 5 курса в Xсеместре, 371.26kb.
- Эпидемиология рака желудка в регионе сибири и дальнего востока и иркутской области, 372.04kb.
- Вопрос ы к государственным экзаменам, 94.15kb.
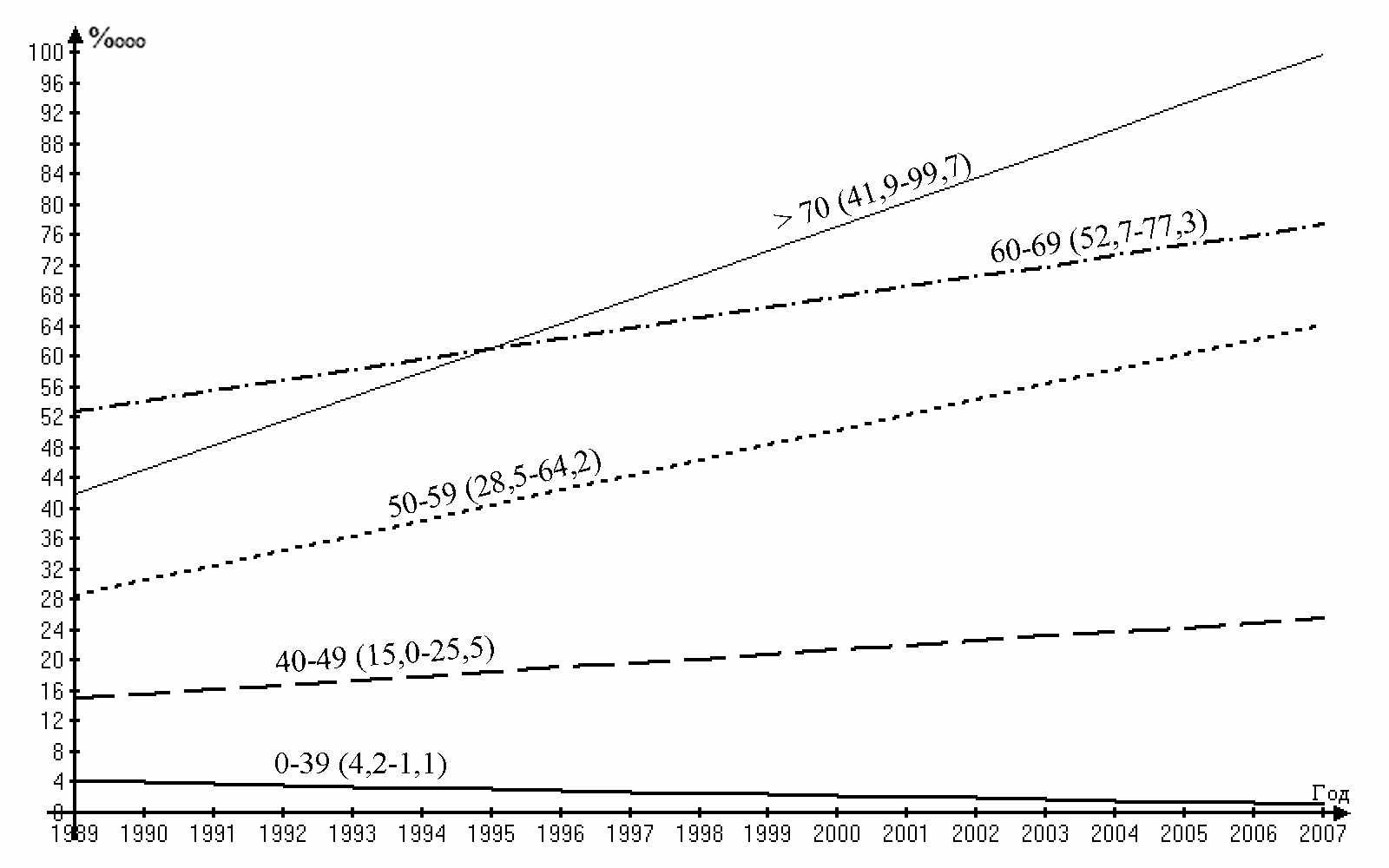
Рис. 1 Динамика повозрастных показателей заболеваемости раком почки мужчин Самарской области в 1989–2007 годах при аналитическом выравнивании по прямой.
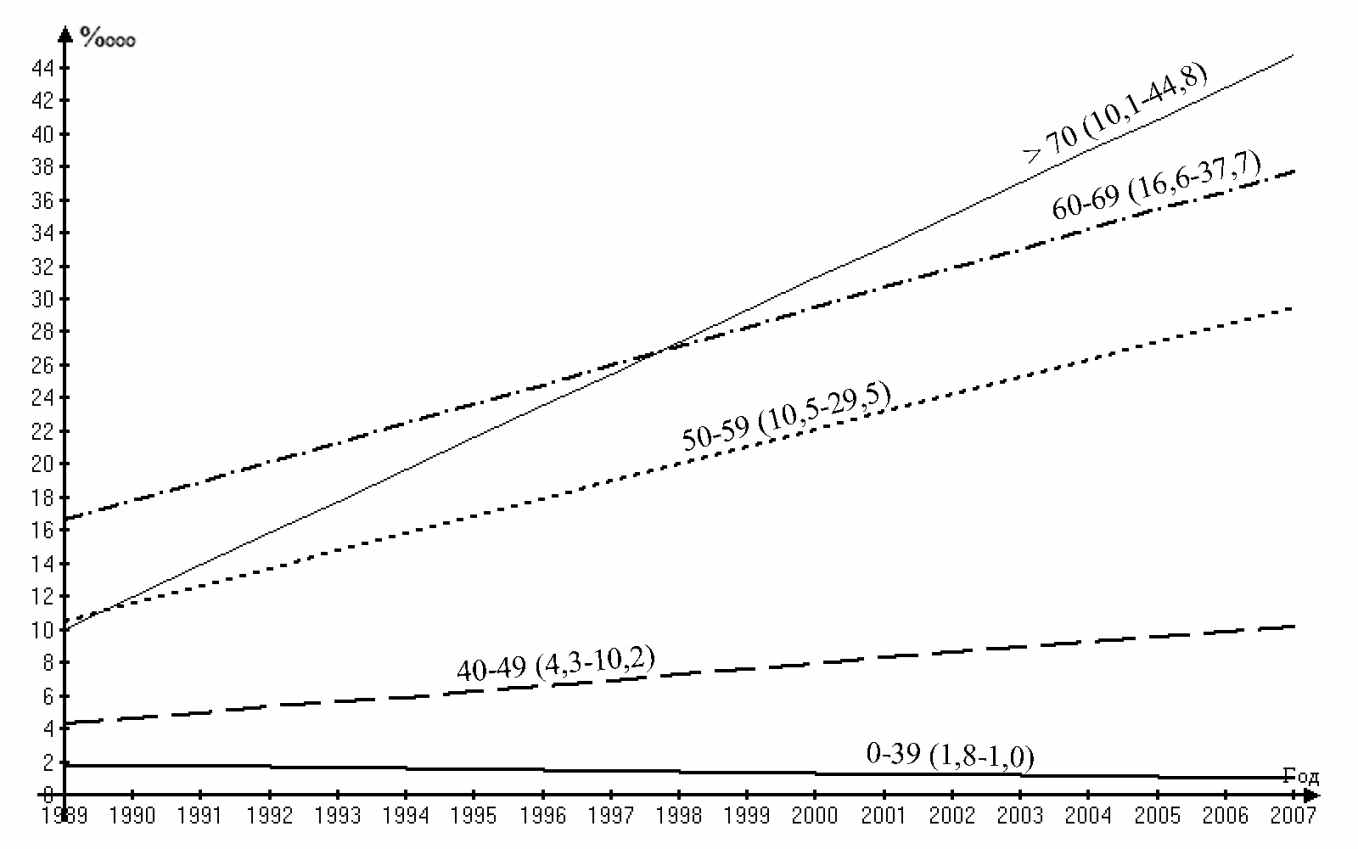
Рис. 2 Динамика повозрастных показателей заболеваемости раком почки женщин Самарской области в 1989–2007 годах при аналитическом выравнивании по прямой.
При сравнении полученных данных, с аналогичными за 1963 по 1987 годы следует отметить, что доля рака почки увеличилась в 2,5 раза (1,3%). Стандартизованный показатель заболеваемости в целом вырос в 8,5 раз, по сравнению с 2,00/0000. Показатели заболеваемости в 1963 – 1987 годах были значительно ниже как в целом, так и раздельно у мужчин и женщин – 1,00/0000 и 3,40/0000; (р < 0,01); 1,40/0000 – 3,8 (р < 0,002); 1,20/0000 – 2,6 (р < 0,002) соответственно.
Наибольший рост заболеваемости у мужчин в период с 1963 по 1987 годы наблюдался в возрастной группе 50 – 59 лет с 2,40/0000 до 14,40/0000 и 60–69 лет с 3,50/0000 до 20,30/0000 (Р < 0,001), прирост заболеваемости в этих возрастных группах составлял 500,0% и 480,0% соответственно. Выраженный прирост заболеваемости у женщин в этот период отмечен в возрастной группе 50–59 лет – 369,2% (с 1,30/0000 до 6,10/0000 ; Р < 0,002).
Установленный рост заболеваемости свидетельствует о необходимости прогнозирования ее, поскольку требует неотложных мероприятий по профилактике. Прогнозирование заболеваемости основано на выявлении действующих в настоящее время трендов заболеваемости и экстраполяции их на будущее.
Выполненное прогнозирование до 2015 года установило рост заболеваемости раком почки, в целом прогнозируемый показатель составил 24,6 ± 6,90/0000, у мужчин – 30,5 ± 8,60/0000; у женщин – 19,7 ± 5,70/0000 (Р = 0,95).
Относительно возрастных прогнозируемых показателей заболеваемости у мужчин и женщин (рис. 3, 4) следует сказать, что наибольшие показатели и максимальный ее рост в 1,2 раза отмечены в самой старшей возрастной группе 70 лет и старше с 102,9 ± 26,80/0000 в 2008 г. до 125,3 ± 42,00/0000 в 2015 г.; 46,7 ± 10,80/0000 до 60,2 ± 16,90/0000 соответственно (Р = 0,95).

Рис. 3 Динамика заболеваемости раком почки мужчин 70 лет и старше за 1989–2007 годы и прогноз на 2015 год (Р = 0,95)
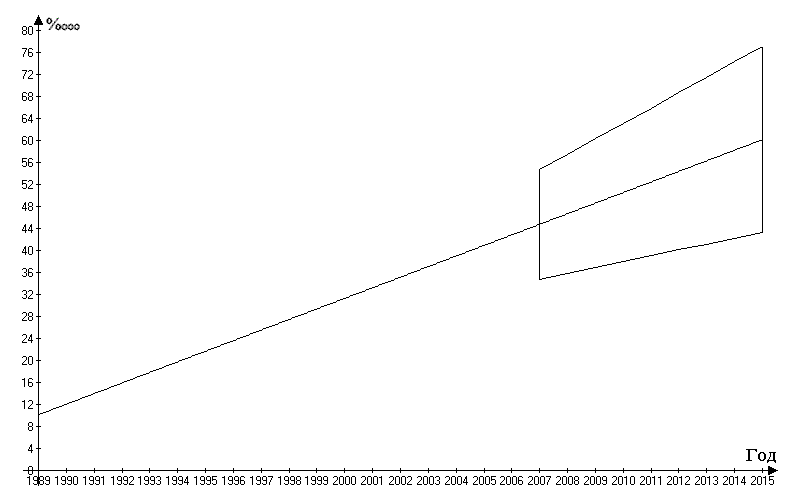
Рис. 4 Динамика заболеваемости раком почки женщин 70 лет и старше за 1989–2007 годы и прогноз на 2015 год (Р = 0,95)
Для выяснения причин роста заболеваемости и правильной оценки изменений ее динамики у мужчин и женщин применен компонентный анализ, позволяющий выяснить, в какой мере рост заболеваемости обусловлен соответствующими изменениями в возрастной структуре, а в какой – повышением риска заболеть в связи с появлением новых или интенсификации существующих факторов (В.В. Двойрин с соавт., 1987).
Установлено, что с 1989 по 2007 годы интенсивный показатель мужчин увеличился с 4,70/0000 до 19,40/0000, то есть на 312,77%. Прирост мужского населения составил 1,99%. При разложении прироста заболеваемости мужчин вычислены значения трех компонент: первой – структурной, определяемой изменением в половозрастной структуре населения и составившей 10,64%; второй – показательной, определяемой изменением уровней возрастных показателей и равной 274,47%; третьей – компоненты взаимодействия, представляющей совместное влияние изменений в половозрастной структуре населения и уровнях возрастных показателей и равной 27,66% (табл. 2).
Прирост женского населения за это время составил 0,9%, грубый показатель увеличился с 3,60/0000 до 15,40/0000, то есть на 327,77%. Составные части прироста в процентах к исходному уровню составили: 44,44% + 186,11% + 97,22% = 327,77% (табл. 3).
С помощью компонентного анализа установлено, что рост заболеваемости у мужчин и женщин вызван не изменением возрастной структуры населения, то есть «постарением» его, а повышением риска заболевания. В период с 1963 по 1987 гг. наблюдалась аналогичная картина.
Общая пятилетняя выживаемость больных раком почки невысока и составляет 60,0% (А.С. Переверзев, 1997; Д.А. Носов с соавт., 2005; P. Althausen et al., 1997; G. Citterio et.al., 1997). На выживаемость больных раком почки оказывает влияние комплекс факторов – клинических, морфологических особенностей опухоли, некоторые биохимические сдвиги, происходящие в организме.
Общая пятилетняя выживаемость 174 наших пациентов составила 75,3%.
Изучена выживаемость больных раком почки в зависимости от клинических факторов. Для этого больные разделены на две группы: 1-я группа – больные с клиническими проявлениями болезни (55,7%) и 2-я – больные без симптомов заболевания (44,3%).
Выживаемость в двух сравниваемых группах имела различия. В группе больных с клиническими проявлениями болезни она ниже – 63,6%, по сравнению с группой больных с «немыми» опухолями почки – 89,3% (Р = 0,95; α < 0,05).
У больных с бессимптомными опухолями доля стадии Т1N0M0 преобладала – 76,6%; в группе больных с проявлением симптоматики заболевания – 42,3%. Стадия Т2N0M0 в этих группах больных составила 23,7% и 19,5% соответственно.
Таблица 2
Компонентный анализ прироста заболеваемости раком почки мужчин Самарской области за 1989–2007 гг.
| Возраст (i) | Возрастная структура населения (Sij = Nij/Nj) | Прирост структурных показателей (Si2-Si1) (3)-(2) | Заболеваемость раком почки (Pij) | Прирост заболеваемости | |||||
| Общий (Pi2-Pi1) (6)-(5) | в связи с изменением в том числе | ||||||||
| 1989 г. (Si1) | 2007 г. (Si2) | 1989 г. (Pi1) | 2007 г. (Pi2) | возрастной структуры (4)х(5) | риска заболеть (2)х(7) | возрастной структуры + риска заболеть (4)х(7) | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 0-39 лет | 0,622 | 0,5748 | -0,0472 | 0,3 | 1,0 | 0,6 | -0,0152 | 0,393603758 | -0,0299 |
| 40-49 лет | 0,141 | 0,1575 | 0,0165 | 2,8 | 24,4 | 21,5 | 0,0467 | 3,037747147 | 0,3549 |
| 50-59 лет | 0,107 | 0,1378 | 0,0308 | 14,9 | 49,2 | 34,3 | 0,4607 | 3,669889864 | 1,0574 |
| 60-69 лет | 0,074 | 0,0756 | 0,0016 | 23,4 | 58,9 | 35,5 | 0,0374 | 2,629649979 | 0,0568 |
| больше 70 лет | 0,056 | 0,0543 | -0,0017 | 13,1 | 69,5 | 56,4 | -0,0224 | 3,156750972 | -0,0966 |
| Всего | ΣSi1 = 1 | ΣSi2 = 1 | | P1 = 4,7 | P2 = 19,4 | | 0,5073 | 12,88764172 | 1,3428 |
| | | | | P2-P1 = 14,7 | | (ΣΔB ≈ 0,5) | (ΣΔP ≈ 12,9) | (ΣΔBP ≈ 1,3) | |
Сумма 3-х компонент равна разности грубых показателей: ΣΔB + ΣΔP + ΣΔBP = 0,5 + 12,9 +1,3 = 14,7 = P2-P1
Составные части прироста в процентах к исходному уровню составили:
100х0,5/4,7 + 100х12,9/4,7 +100х1,3/4,7 = 10,64% + 274,47% + 27,66% = 312,77%
Таблица 3
Компонентный анализ прироста заболеваемости раком почки женщин Самарской области за 1989-2007 гг.
| Возраст (i) | Возрастная структура населения (Sij = Nij/Nj) | Прирост структурных показателей (Si2-Si1) (3)-(2) | Заболеваемость раком почки (Pij) | Прирост заболеваемости | |||||
| Общий (Pi2-Pi1) (6)-(5) | в связи с изменением в том числе | ||||||||
| 1989 г. (Si1) | 2007 г. (Si2) | 1989 г. (Pi1) | 2007 г. (Pi2) | возрастной структуры (4)х(5) | риска заболеть (2)х(7) | возрастной структуры + риска заболеть (4)х(7) | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 0-39 лет | 0,612 | 0,4786 | -0,1334 | 0,5 | 0,6 | 0,2 | -0,0609 | 0,09254699 | -0,0202 |
| 40-49 лет | 0,151 | 0,1512 | 0,0002 | 3,2 | 10,8 | 7,5 | 0,0007 | 1,139358985 | 0,0017 |
| 50-59 лет | 0,107 | 0,1530 | 0,0460 | 8,5 | 26,6 | 18,1 | 0,3906 | 1,937669955 | 0,8336 |
| 60-69 лет | 0,074 | 0,1037 | 0,0297 | 15,3 | 35,9 | 20,6 | 0,4552 | 1,520895071 | 0,6099 |
| больше 70 лет | 0,056 | 0,1135 | 0,0575 | 14,2 | 50,7 | 36,5 | 0,8158 | 2,045541367 | 2,1002 |
| Всего | ΣSi1 = 1 | ΣSi2 = 1 | | P1 = 3,6 | P2 = 15,4 | | 1,6015 | 6,736012368 | 3,5251 |
| | | | | P2-P1 = 11,8 | | (ΣΔB ≈ 1,6) | (ΣΔP ≈ 6,7) | (ΣΔBP ≈ 3,5) | |
Сумма 3-х компонент равна разности грубых показателей: ΣΔB + ΣΔP + ΣΔBP = 1,6 + 6,7 +3,5 = 11,8 = P2-P1
Составные части прироста в процентах к исходному уровню составили:
100х1,6/3,6 + 100х6,7/3,6 +100х3,5/3,6 = 44,44% + 186,11% + 97,22% = 327,77%
Количество опухолей, выявленных случайно, уменьшается с ростом стадии болезни, а количество опухолей с клиническими проявлениями симптоматики увеличивается. В 1-ой группе больных доля опухолей в стадии Т3N1M0 и Т4N1M1 (20,6% и 13,4% соответственно) преобладала над долей таковых во 2-ой группе (2,6% и 1,3%) нашего исследования (Р = 0,99; α = 0,01). Гистологическая верификация опухолей составила 98,1%.
Средний размер новообразований в 1-ой группе наших больных составил— 7,0 см (от 1,0 до 11,0 см), опухоли размером ≤ 7 см составили 52,6%, более 7см – 47,4%. Во 2-ой группе средний размер опухолей составил 6,3 см (от 1,8 до 15,7 см), новообразования ≤ 7 см составили 85,7%, более 7 см – 14,3%.
Выяснены различия и в гистологических типах опухолей у представителей этих двух групп. Для случайно диагностированных опухолей характерен светлоклеточный вариант почечно-клеточного рака, для опухолей с клиническими симптомами – светлоклеточный и смешанный варианты (Р = 0,95; α = 0,02).
При отсутствии симптоматики у больных опухолями почки, как правило, выявляется светлоклеточный вариант почечно-клеточного рака, ранняя стадия заболевания Т1N0M0, меньший размер опухоли и лучший прогноз (5 - летняя выживаемость).
На прогноз заболевания может оказывать влияние и морфологический тип опухоли. Изучение морфологических особенностей опухолей почки у 174 больных показало следующие их гистологические формы: светлоклеточный рак, смешанный вариант почечно-клеточного рака, зернистоклеточный, железистый, кистозный, лимфосаркома, доброкачественные опухоли, папиллярный рак почечной лоханки. Самой многочисленной группой оказались больные со светлоклеточным раком. Гистологическая верификация опухолей составила 98,1%.
Выживаемость больных в зависимости от морфологической верификации опухоли почки была следующей: при светлоклеточном раке - 83,3%, при зернисто-клеточном –71,4%, смешанно-клеточном – 60,1%.
На прогноз рака почки оказывает влияние стадия заболевания. В нашем исследовании 56,1% больных отнесено к T1N0M0 стадии, пятилетняя выживаемость у них составила 96,6%, к стадия Т2N0M0 – 21,5% пациентов, выживаемость – 64,6%, к Т3N1M0 –15,9%, выживаемость – 38,4%, к Т4N1M1 – 6,5%, выживаемость – 0%.
Влияние размера опухоли на выживаемость было следующим: при опухолях 7 см и менее выживаемость составила 94,8%, при размерах новообразований более 7 см – 46,6%.
Таким образом, установлено, что пятилетняя выживаемость больных опухолями почки лучше при светлоклеточном варианте почечно-клеточного рака, стадии заболевания T1N0M0, размерах опухоли равном 7 см и менее.
Биохимическое исследование активности ЛДГ мочи и крови 101 больного опухолями почки и 119 лиц контрольной группы показало отсутствие достоверной связи рака почки с повышением активности фермента в крови как в целом, так у мужчин и у женщин в отдельности. Однако полученные данные свидетельствуют о различиях ее активности у лиц группы наблюдения и контроля.
Высокий уровень ЛДГ в сыворотке крови выявлен у 47% мужчин, больных раком почки, и у 21,1% в контрольной группе (ОР (СI) = 3,3(0,6–17,8); Р = 0,94; α = 0,06). У женщин этот процент был несколько ниже и составил, соответственно, 40% и 27,9% (ОР (СI) = 1,7(0,2–13,4); Р = 0,87; α = 0,13).
Что касается активности лактатдегидрогеназы мочи, то установлен достоверный риск рака почки при повышении активности фермента (ОР(СI) = 12,7(1,0–190,5); Р = 0,98; α = 0,02) (табл. 4).
Таблица 4 Показатели ЛДГ мочи у больных раком почки мужчин и женщин,
лиц контрольной группы и относительный риск возникновения заболевания от активности фермента
| Обследуе- мые лица | Больные | Контроль | Р | α | ОР(СI) | ||
| n | Показатели ЛДГ мочи | n | Показатели ЛДГ мочи | ||||
| Мужчины | 66 | 51,14±51,14 | 76 | 23,90±16,10 | 0,95 | 0,05 | 20,2(1,7–238,4) |
| Женщины | 35 | 52,88±44,99 | 43 | 26,20±15,91 | 0,91 | 0,09 | 9,4(0,6–136,3) |
| Средние величины | 101 | 51,74±51,74 | 119 | 24,71±16,03 | 0,98 | 0,02 | 12,7(1,0–190,5) |
Высокая его активность выявлена у каждого четвертого больного и только у каждого сорокового обследуемого контрольной группы (табл. 5).
Таблица 5 Распределение больных опухолями почек и лиц контрольной группы
в зависимости от уровня ЛДГ мочи на 100 обследованных
| Активность ЛДГ в моче | Больные | Контроль | ||||||||||
| мужчины | женщины | мужчины | женщины | |||||||||
| Абс. чис-ла | % | Средний показатель ЛДГ | Абс. чис-ла | % | Средний показатель ЛДГ | Абс. чис-ла | % | Средний показатель ЛДГ | Абс. чис-ла | % | Средний показатель ЛДГ | |
| Повышенная | 14 | 21,2 | 122,4±93,4 | 11 | 31,4 | 106,8±40,9 | 1 | 1,3 | 69,0±0 | 2 | 4,7 | 70,5±3,5 |
| Нормальная | 52 | 78,8 | 32,2±18,2 | 24 | 68,6 | 28,2±15,4 | 75 | 98,7 | 23,5±15,4 | 41 | 95,3 | 24,1±12,8 |
| Всего | 66 | 100 | 51,1±51,1 | 35 | 100 | 52,9±45,0 | 76 | 100 | 23,9±16,1 | 43 | 100 | 26,2±15,9 |
Раздельное изучение активности ЛДГ мочи у мужчин и женщин выявило некоторые различия. Так, высокий уровень активности ЛДГ в моче выявлен у 21,2% больных мужчин, т.е. у каждого пятого; в контроле у 1,3%, т.е. у каждого 76-го обследуемого (ОР(СI) = 20,2(1,7–238,4); Р = 0,95; α = 0,05). Среди больных женщин высокая активность фермента выявлена у 31,4% (у каждой третей), в контроле у 4,7% (у каждой 20-ой) (ОР(СI) = 9,4(0,6–136,3); Р = 0,91; α = 0,09).
Определенные различия активности ЛДГ мочи наблюдаются в различных возрастных группах. Было установлено, что показатели ее активности у больных раком почки с возрастом увеличиваются и максимально они выражены у мужчин возрастных групп 60–69 лет и 70-лет и старше (Р = 0,94; a = 0,06), у женщин – группах 50–59 лет (Р = 0,94; a = 0,06) и 60–69 лет (Р = 0,92; a = 0,08). В контроле такой закономерности не прослеживается.
Среди различных форм рака почки наиболее высокие показатели активности фермента в моче отмечены при смешанной и светлоклеточной формах (57,7 ± 36,6 и 44,0 ± 37,7 соответственно); у лиц с папиллярным раком почечной лоханки они несколько выше (118,8 ± 157,3), чем при злокачественных опухолях паренхимы почки (48,7 ± 40,5) (Р = 0,66; a = 0,34).
При нормальной активности ЛДГ мочи у больных раком почки выживаемость составила 81,4%. Увеличение уровня активности лактатдегидрогеназы мочи коррелирует со снижением выживаемости – 71,4%.
Прогнозируемый рост заболеваемости у мужчин и женщин свидетельствует о необходимости пополнения сведений о факторах, способствующих возникновению рака почки, и использовании полученных данных в ранней диагностике заболевания.
Ретроспективное эпидемиологическое исследование выявило экзогенные факторы (вредные привычки, особенности питания, употребление некипяченой водопроводной воды, прием лекарственных препаратов, проживание вблизи промышленных предприятий, контакт с нефтепродуктами, влияние рентгенологического излучения), факторы эндогенного характера (изменение уровня ЛДГ в моче, наследственность, групповая принадлежность крови), а также заболевания, предшествующие раку почки в зависимости от половой принадлежности.
Несмотря на то, что среди больных раком почки было 65,6% рабочих, подвергавшихся действию нефтепродуктов, ядохимикатов, лаков, красок, солей тяжелых металлов, строительных материалов и прочих веществ, наше исследование не выявило зависимости развития заболевания от определенной профессии. Но обращает на себя внимание распространение контакта с нефтепродуктами среди больных раком почки как на производстве, так и в быту. Показатель зависимой пропорции равен 35,8% у мужчин
(ОР( СI) = 5,3(3,5–8,0), и 23,0% у женщин (ОР(СI) = 5,7(3,2–10,2).
На риск заболевания оказывает влияние проживание вблизи промышленных предприятий, выбросы вредных веществ которых загрязняют атмосферу (ОР(СI) = 1,6(1,1–2,4), ЗП = 5,2%).
Говоря о влиянии вредных привычек на возникновение рака почки, необходимо отметить, что курение достоверно повышает риск заболевания у мужчин – ОР(СI) = 12,3(7,5–20,0) и в популяции распространено широко – ЗП = 53,5%. Имеет значение раннее начало курения (до 15 лет), стаж курения (более 10 лет), интенсивность курения (10–20 штук сигарет или папирос в день).
У женщин не выявлено повышение риска заболевания от курения ОР(СI) = 0,4(0,2–1,0). Низкий показатель относительного риска у женщин может свидетельствовать только о том, что женщины сравнительно недавно пристрастились к этой привычке и поэтому пока еще не наступило время значительного изменения показателей заболеваемости у них.
То же можно сказать и об употреблении алкогольных напитков. Систематическое употреблении крепких алкогольных напитков (40° и более) у мужчин значимо увеличивает риск заболевания ОР(СI) = 18,9(11,7–30,4), ЗП = 69,8%.
При этом и относительно редкий, 1-2 раза в неделю, прием алкоголя достоверно повышал риск – ОР(СI) = 10,8(6,0–19,5), ЗП = 38,8%, низкая крепость употребляемого алкоголя также достоверно увеличивала риск – 4,6(2,9–7,4), ЗП = 29,0%; то же можно сказать и о небольших дозах его (менее 250,0 гр.), ОР(СI) = 10,6(6,1–18,4), ЗП = 40,4; и сроке употребления алкоголя менее 10 лет – ОР(СI) = 24,4(7,5–79,8), ЗП = 21,6.
Достоверного повышения риска заболевания у женщин при употреблении алкоголя не выявлено ОР(СI) = 0,3(0,13–0,7).
Из особенностей питания, значительно повышающих риск рака почки, следует указать на недостаточное количество молочно-растительных продуктов, частое употребление копченых и крепкой засолки со специями продуктов – ОР(СI) = 1,4(1,0–1,8), ЗП = 8,2%; мясной жирной пищи ОР(СI) = 3,2(2,4–4,4), ЗП = 26,6%, особенно это касается женщин ОР(СI) = 9,3(5,9–14,7), ЗП = 54,6%, и употребление искусственных сладостей и заменителей сахара ОР(СI) = 9,3(4,8–18,1).
Общим для мужчин и женщин фактором, значительно повышающим риск заболевания, является употребление сырой водопроводной воды для питья –ОР(СI) = 4,4(2,6–7,4), ПЗ = 22,4%; ОР(СI) = 4,5(2,6–7,8), ПЗ = 22,2% соответственно. Известно, что при хлорировании в воде появляются мутагенные и канцерогенные субстанции.
Длительный прием лекарственных препаратов до заболевания был более характерным для женщин. Риск заболевания у них значимо повышает прием гипотензивных препаратов, анальгетиков и диуретиков ОР(СI) = 9,7(5,9–15,9); 6,2(3,9–9,8); 5,8(3,7–9,2) соответственно. У мужчин причинная зависимость и статистическое подтверждение связи рака почки с лекарственными препаратами выявлена при приеме гипотензивных, противотуберкулезных и диуретических препаратов ОР(СI) = 2,3(1,3–3,9); 2,2(1,2–3,9); 1,6(1,0–2,7) соответственно.
Среди эндогенных факторов следует отметить перенесенные ранее заболевания. Повышенный риск рака почки характерен для лиц страдающих гипертонической болезнью – ОР(СI) = 4,6(3,3–6,6); ЗП = 26,3%, предшествующими воспалительными заболеваниями почек и МКБ = 2,9(1,3–6,8), ПЗ = 13,4%; туберкулезом – 1,8(1,1–2,7), ЗП = 5,8%.
Наследственность, отягощенная злокачественной опухолью, наблюдалась у 35,7% больных. Этот фактор значимо повышает риск рака почки как у мужчин, так и у женщин – ОР(СI) = 2,0(1,0–5,0), ЗП = 16,6% и 2,7(1,0–7,6), ЗП = 24,7%, соответственно.
Случаи первично-множественных опухолей также относятся к аспекту генетических особенностей рака почки, среди наших больных этот фактор встретился у двух женщин, ранее лечившихся от рака шейки матки.
Изучение зависимости рака почки от групповой принадлежности крови выявило риск развития заболевания у мужчин с группой крови 0(I) – ОР(СI) = 1,4(1,0–2,1), а у женщин с группой А(II) – ОР(СI) = 1,7(1,1–2,5), ЗП = 13,3% и 15,5% соответственно. У мужчин отмечена статистически значимая зависимость заболевания с Rh+ фактором крови ОР(СI) = 2,5(1,5–4,2); ЗП = 5. У женщин подобной зависимости не выявлено.
Ранняя диагностика заболевания должна быть связана с определением индивидуального риска у каждого обследуемого на данной территории. Для этого применена балльная оценка статистически значимых факторов риска при помощи статистической неоднородной последовательной процедуры распознавания, определен индивидуальный риск заболевания в зависимости от значимости каждого имеющегося у него фактора риска в отдельности и всего комплекса факторов в целом. В результате ретроспективного изучения эпидемиологии рака почки уточнены критерии формирования групп риска с помощью предложенной прогностической таблицы, в основу которой легли статистически значимые факторы риска, вычислен диагностический коэффициент и информативность каждого фактора и его подгрупп, что позволило определить индивидуальный риск заболевания при суммарном действии факторов. Установлены различия информативности указанных факторов у мужчин и женщин. Для мужчин высокоинформативным фактором риска является употребление алкоголя (J = 3,949). Хорошей информативностью обладают факторы – курение (J = 2,824) и контакт с нефтепродуктами (J = 1,466). Относительно низкую информативность имеют факторы: употребление некипяченой водопроводной воды (J = 0,614) и влияние радиации (J = 0,544); низкая информативность характерна для факторов – группа крови 0(I)Rh + (J = 0,441), особенности питания (J = 0,399), прием лекарственных препаратов (J = 0,347), ранее перенесенные заболевания (J = 0,283), проживание вблизи промышленных предприятий (J = 0,050) и отягощенная злокачественными новообразованиями наследственность (J = 0,023).
Для женщин высокой информативностью обладают факторы: прием лекарственных препаратов (J = 3,383) и особенности питания (J = 3,026). Относительно низкая информативность установлена для факторов: ранее перенесенные заболевания (J = 0,840), контакт с нефтепродуктами (J = 0,815) и употребления некипяченой водопроводной воды (J = 0,608). Низкую информативность имеют факторы: отягощенная злокачественными новообразованиями наследственность (J = 0,398), группа крови А(II) (J = 0,118), влияние радиации (J = 0,112) и проживание вблизи промышленных предприятий (J = 0,111).
На этой основе была разработана прогностическая таблица для отбора лиц в группу риска в зависимости от половой принадлежности (табл. 6). После определения комплекса факторов риска у обследуемого им приписывают соответствующие баллы, их суммируют и при сумме баллов, равной 6 или более, определяют наличие риска заболевания раком почки, а при сумме менее 6 – отсутствие риска заболевания.
Таблица 6 – ПРОГНОСТИЧЕСКАЯ ТАБЛИЦА ОЦЕНКИ РИСКА ЗАБОЛЕВАНИЯ РАКОМ ПОЧКИ МУЖЧИН И ЖЕНЩИН
Ф.И.О. ___________________________________________ Возраст ____
Пол _______ Место работы _____________________________________
Домашний адрес ______________________________________________
Дата заполнения «_____ » _______________________ 200 __ года
| № | Фактор (диапазоны фактора) | Диагностический коэффициент | |
| мужчины | женщины | ||
| 1 | 2 | 3 | 4 |
| 1. | Употребляет некипяченую водопроводную воду | +5 | +5 |
| 2. 2.1. 2.2. 2.3. 2.4. | Особенности питания Частое употребление мясной жирной пищи Недостаток овощей и фруктов Частое употребление заменителей сахара Употребление молочно-растительной пищи | +1 +1 +2 –4 | +6 +5 +8 –2 |
| 3. 3.1. | Курение Не курит | +8 –3 | - - |
| 4. 4.1. | Употребляет алкоголь Не употребляет | +8 –5 | - - |
| 5. 5.1 5.2 5.3 | Ранее перенесенные заболевания Заболевания почек Гипертония Туберкулез легких | +1 +2 +3 | +2 +3 +1 |
| 6. 6.1. 6.2. 6.3. 6.4. | Частый прием лекарственных препаратов Анальгетики Гипотензивные препараты Противотуберкулезные Диуретики | +1 +3 +3 +3 | +6 +7 +1 +5 |
| 7. | Контакт с нефтепродуктами Нет контакта | +5 –2 | +6 –3 |
| 8. | Влияние радиации | +8 | +5 |
| 9. | Проживание вблизи промышленных предприятий < 1 км | +2 | +2 |
| 10. 10.1. 10.2. | Наследственность В семье есть больной ЗО (кровный родственник) Нет больных ЗО | +1 - | +3 –3 |
| 11. 11.1. 11.2. | Принадлежность к группам крови и Rh фактору 0(I) А(II) | +7 - | +1 +2 |
Диагностический коэффициент______________
Группа учета________________________Диагноз_______________________
Для определения чувствительности прогностической таблицы выделена группа риска из больных и здоровых. Из 378 больных в группу риска вошло 269 человек (71,1%), из 538 лиц контроля – 104 человека (19,3%). Если учесть, что чувствительность выражается отношением числа больных, отнесенных к группе риска, к числу больных, отнесенных и не отнесенных к группе риска, то в данном случае она составила 71,1%.
Определение риска рака почки и диагностика его на ранних стадиях возможна с помощью эпидемиологических критериев. Немаловажное значение в ранней диагностике заболевания принадлежит УЗИ, которое позволяет выявлять не только опухоли почки, проявляющиеся клинической симптоматикой в 100,0% случаев, но и 43,7% бессимптомных небольших размеров новообразований.
Биохимические критерии ранней диагностики рака почки определены на основании установленного в результате исследования риска заболевания при повышении активности ЛДГ мочи в совокупности с действующими эпидемиологическими факторами риска. Индивидуальный риск заболевания при повышенной активности ЛДГ в моче составляет у мужчин ДК = +12 (J = 1,294), у женщин +8 (J = 1,205). Постоянный, нормальный уровень активности ЛДГ в моче снижает риск развития рака почки как у мужчин, так и у женщин (ДК = -1).
Целесообразно выполнять биохимический тест по определению активности ЛДГ мочи у лиц, отобранных в группы риска по эпидемиологическим критериям. Установлено, что показатели активности фермента лактатдегидрогеназы мочи у лиц группы риска ниже, чем у больных, но выше, чем у лиц контрольной группы, т.е. имеют промежуточное значение (табл. 7).
Выполнение указанного биохимического теста у наблюдаемого контингента дает возможность более точно определить круг лиц, требующих пристального наблюдения уролога.
Таблица 7 Активность ЛДГ мочи у больных раком почки,
лиц группы риска и контроля (МЕ/ л)
| Показатели активности ЛДГ | Больные | Группа риска | Контроль |
| Моча | 51,1±51,1 | 26,3±21 | 24,7±16,0 |
Формирование групп риска проводится во время профилактических осмотров. Сбор и обработка информации, разделение населения на здоровых лиц и группу риска является трудоемким процессом. Реальную помощь врачу в реализации диспансерного метода работы обеспечит разработанная автоматизированная система с определенным видом программы – «Программа отбора лиц в группу риска заболевания раком почки», разработанной на основе прогностической таблицы.
Программа обеспечивает удобство работы и сохранение ее результатов в удобном формате, предлагает оригинальную методику проведения отбора, содержащую встроенные алгоритмы расчетов, планирования, работы с данными и файлами. Программа имеет особенности: не требует самостоятельной настройки и доработки методики отбора; имеет дружественный интерфейс и интуитивно понятный алгоритм работы, позволяет легко и быстро обучиться работе в программе; содержит справку по используемым в программе данным; не требует установки; предоставляет специалистам возможность автономной работы на переносных компьютерах (типа - ноутбук) и сохранения результатов в той же директории, где находится программа, благодаря чему легко переносится.
Работа с программой разделена на 3 этапа: 1 этап – ввод паспортных данных (рис. 5).
2 этап – процедура отбора, внесение всех эпидемиологических данных, на основе которых будет делаться вывод о принадлежности обследуемого к группе риска (рис. 6).
