Рекомендації Асоціації кардіологів України Київ, 2009
| Вид материала | Документы |
- Льність спеціальних бібліотек україни важлива складова розвитку сучасного бібліотекознавства, 3175.95kb.
- Методичні рекомендації Київ 2009 міністерство охорони здоров`я україни, 343.33kb.
- Кабінету Міністрів України від 28. 11. 2007 n 1059-р "Про перенесення робочих днів, 13.79kb.
- Методичні рекомендації соціальний супровід І медична допомога для дискордантних пар, 1792.04kb.
- Методичні рекомендації київ – 2009 міністерство охорони здоров’я україни академія медичних, 735.15kb.
- Державна митна служба україни наказ київ, 1588.46kb.
- Методичні рекомендації Київ-Кременчук 2007 ббк 88. 8: 74. 56 Удк 159. 9: 616. 89-008., 1375.57kb.
- Інформація про виконання Порядку денного асоціації Україна – єс за 10 місяців 2011, 636.13kb.
- Методичні рекомендації щодо організації діяльності психологічної служби міста, 374.46kb.
- Типове положення про Регіональне відділення Всеукраїнської асоціації районних та обласних, 206.68kb.
Профілактика РСС у хворих з дилятаційною кардіоміопатією
та хронічним міокардитом
| |  | | |
| Стратифікація ризику | | | |
| Первинна профілактика | | | |
| Вторинна профілактика | | | |
* - можна рекомендувати хворому.
ПРОФІЛАКТИКА РСС ПРИ АРИТМОГЕННІЙ ДИСПЛАЗІЇ ПРАВОГО ШЛУНОЧКА
Аритмогенна дисплазія правого шлуночка (ПШ) чи правошлуночкова кардіоміопатія (ПШКМП), є хворобою міокарда, що характеризується регіональною або глобальною фіброзною заміною міокарда ПШ, з чи без захоплення ЛШ та із збереженням товщини міжшлуночкової перетинки. Поширенність цього захворювання досконало не відома, але як вважають, знаходиться між 1:1000-1:10000.
Для даної патології характерна графіка ЕКГ у вигляді перевернутих зубців Т та поширених QRS комплексів з епсіло-хвилями у правих грудних відведеннях. Хвороба виявляється у підлітків та молодих дорослих із шлуночковими аритміями, в той же час, як клінічні прояви у дітей виявляються рідко. Початковою ознакою захворювання може бути втрата свідомості ( у 29% хворих) чи зупинка серця (у 7-23% випадків).
Мономорфна ШТ з блокадою лівої ніжки пучка Гіса, найбільш часта (70-92%) аритмія, яка спостерігається при аритмогенній дисплазії правого шлуночка, проте прояви її можуть бути іншими: від безсимптомної шлуночкової екстрасистолії до важко переносимої поліморфної шлуночкової тахікардії.
Аритмогенна дисплазія є однією із головних причин РСС у віковій групі без захворювань коронарних артерій. Хоча прогностичні маркери РСС ще не були визначені у великих проспективних дослідженнях, РСС виникає частіше у пацієнтів з поширеними змінами у правому шлуночку з втягненням лівого шлуночка. Вважають, що пацієнти із стійкою мономорфною шлуночковою тахікардією мають більш сприятливе прогнозування.
Докази, які привели до даних рекомендацій, основані на невеликих дослідженнях чи на думку експертів. Вони наведені в таблиці 17.
Таблиця 17
Профілактика РСС у хворих з аритмогенною дисплазією правого шлуночка
| | 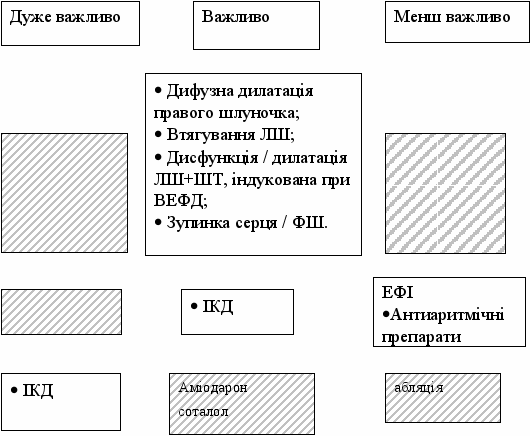 | | |
| Стратифікація ризику | | | |
| Первинна профілактика | | | |
| Вторинна профілактика | | | |
* - можна рекомендувати хворому
ПРОФІЛАКТИКА РСС ПРИ ПРОЛАПСІ МІТРАЛЬНОГО КЛАПАНУ
Пролапс мітрального клапану (ПМК) є досить поширена зміна стулок завдяки, в основному, нечітким Ехо-кардіографічним критеріям. Поширеність його помітно зменшилась після їх уточнень. Останні дані Фремінгемського дослідження продемонстрували, що у невідібранній групі амбулаторних пацієнтів поширеність ПМК складала 1-3% на 3491 суб’єктів. ПМК, в основному, не є невідкладним станом, хоча РСС і була відмічена у поєднанні з ПМК.
Вважається, що в основі РСС при ПМК лежать аритмії, а фібриляція шлуночків мабуть є безпосередньою причиною РСС у більшості випадків. Zuppiroli та співавтори, повідомили про результати проспективного дослідження, у якому спостерігались 316 хворих протягом, в середньому 102 місяці. На протязі спостереження тільки 6 пацієнтів померли від серцевих причин, з них 3 випадки РСС, один пацієнт пройшов корекцію мітрального клапану за 14 місяців до смерті. Однак, слід підкреслити, що через відносно високу поширенність ПМК в загальній популяції, навіть низький рівень ускладнень може супроводжуватись великою кількістю випадків.
Надлишкові та міксоматозні стулки найбільш важливі Ехо-кардіографічні знахідки, пов’язані з РСС. В дослідженні Nishimuri та співавт., усі 6 пацієнтів з ПМК, котрі померли раптово, мали надлишкові стулки. Взаємозв’язок між присутністю та важкістю регургітації на мітральному клапані та РСС невідомий. Boudoulas та співавтори і Kampbal та співавтори виявили, що зміни сегмента ST в задньобокових відділах були пов’язані із виникненням шлуночкової тахікардії чи фібриляції шлуночків. В інших дослідженнях було вирішено, що подовження інтервалу QT та збільшення дисперсії QT може бути корисним маркером аритмічної смертності. Часті чи комплексні шлуночкові екстрасистоли, як передбачалось, виявились фактором ризику РСС, але їх прогностична роль все ж не була доведена. ЕКГ високого дозвілу може бути корисна при ідентифікації пацієнтів з ПМК, не схильних до злоякісних аритмій. Виникнення шлуночкової тахікардії при ВЕФД, в той же час, не вважається корисною прогностичною ознакою. Найбільш важливими прогностичними маркерами РСС у цій групі пацієнтів є попередня зупинка серця, РСС у сімейному анамнезі у молодому віці, та надлишковість мітральної стулки.
Проспективні дослідження, які вивчали ефективність β-адренобетаблокаторів та інших антиаритміків у запобіганні РСС не проводились. Але β-адреноблокатори, мабуть, повинні бути основними препаратами вибору у пацієнтів із клінічними симптомами. Пацієнти із анамнезом зупинки серця підлягають імплантації ІКД. Ці висновки базуються тільки на даних невеликих оглядових досліджень та консенсусі експертів, наведені у вигляді рекомендацій в таблиці 18.
Таблиця 18
Рекомендації по профілактиці РСС у хворих з пролапсом мітрального клапана
| | 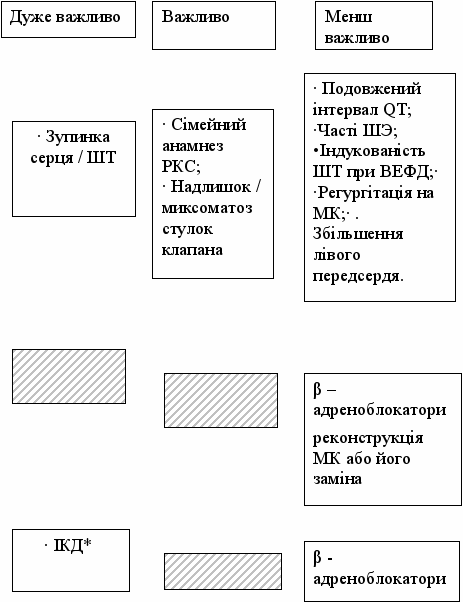 | | |
| Стратифікація ризику | | | |
| Первинна профілактика | | | |
| Вторинна профілактика | | | |
* - можна рекомендувати хворому
ПРОФІЛАКТИКА РСС ПРИ АОРТАЛЬНОМУ СТЕНОЗІ
Аортальний стеноз (АС) може бути вродженою патологією, а також придбаною після гострої ревматичної атаки чи внаслідок вікового дегенеративного процесу (сенільний АС). Звичайно анамнез захворювання АС характеризується довгим безсимптомним періодом, на протязі якого наростає ступінь стенозу. У 1968 році Ross і Braunwald показали, що ризик РСС у пацієнтів без клінічних проявів низький (3-5%). Пізніше проспективне дослідження продемонструвало, що РСС не відмічалось ні в одному із 123 випадків безсимптомного перебігу, які спостерігались на протязі 2-5 років. Клінічна маніфестація АС включає втрату пам’яті, стенокардію і/або диспное. Як тільки з’являється клінічна картина, прогноз хворих драматично погіршується і частота РСС коливається в межах від 8 до 34% в різних дослідженнях. Механізми РСС при АС добре не вивчені, хоч наявні дані приписують можливу роль неправильному рефлексу Бетцольда-Яроша, шлуночковим тахіаритміям або порушенням проведення крізь атріовентрикулярноме з’єднання. Аналіз Холтер-моніторінгу у семи пацієнтів, які вмерли раптово, показали наявність шлуночкової тахіаритмії у шістьох випадках, але тільки в одному випадку смерть була зв’язана з брадиаритмією. Втрата свідомості і РСС відмічалась у багатьох пацієнтів, але не ясно, чи є втрата свідомості предиктором РСС. АС також пов’язаний з порушеннями провідності в АВ вузлі і трьохпучковій системі, які є більш частими при кальцифікації клапана.
Важкість у тому, щоб передбачити наявність АС у хворого без клінічних проявів, коли ризик РСС ще низький. Ступінь стенозу (систолічний градієнт, площа відкриття клапана), рівень кальцифікації та важкість гіпертрофії лівого шлуночка може використовуватися для передбачення швидкості прогресування стенозу, який потребує хірургічного втручання. Однак, предиктори РСС, основані на виникненні частих і/або комплексних шлуночкових аритмій, пізніх потенціалів або зниженої варіабельності серцевого ритму все ще обговорюються, і ще нема достатньо точних прогностичних факторів щодо рекомендацій заміни аортального клапана.
Після заміни аортального клапана у пацієнтів залишається деякий ризик РСС, викликаної аритміями серця, блокадами ніжок пучка Гіса, повною блокадою серця, порушенням функції ЛШ, залишковою гіпертрофією ЛШ, фіброзом, супутньою ІХС або дисфункцією протезованого клапану. В цій групі пацієнтів, РСС виникала з частотою 2-4% на протязі 7 років. Більш висока частота зустрічаємості РСС була виявлена на протязі раннього періоду відновлення (3 тижні) після заміни клапану. Перехідна повна АВ блокада на протязі післяопераційного періоду не є предиктором повторних порушень провідності. Прогнозуючі фактори щодо АВ блокади, яка потребує імплантації постійного водія ритму, є наступні: існуюче раніше порушення провідності, низька фракція викиду та кальциноз субаортального відділу МШП.
Обмеження фізичної активності повинно бути рекомендоване пацієнтам з помірним і, особливо, з важким аортальним стенозом. Запобігання РСС – одна з цілей хірургічного лікування АС. Однак, якщо операція виконується для зменшення ризику РСС, ризик можливого ускладнення захворювання, в даному випадку, повинен бути співставлений із смертністю при хірургічному втручанні і відомими ускладненнями протезування клапанів. Більшість клініцистів відкладає хірургічне втручання до появи клінічних ознак. Пацієнти повинні бути інформовані про типові симптоми захворювання і необхідність раннього оперативного лікування до виникнення симптомів захворювання. Якщо пацієнту проводиться АКШ, рекомендується паралельно проводити заміну аортального клапану для попередження ранньої повторної операції. Пацієнти з триваючими шлуночковими тахікардіями або фібриляцією, спровокованою ВЕФД, повинні розглядатися, як претенденти для імплантації кардіовертера-дефібрилятора. Роль антиаритмічної терапії аміодароном поки що не ясна. Пацієнтам з триваючими шлуночковими тахіаритміями показано імплантація ІКД. Дані рекомендації були основані на невеликих дослідженнях та на думці експертів і вони наведені в таблиці 19. Таблиця 19
Профілактика РСС у хворих із стенозом аорти
| | | Дуже важливо | Важливо | Менш важливо |
| Стратифікація ризику | Перед заміною клапана | Сінкопе, Стенокардія | Значна шлуночкова аритмія; Дисфункція лівого шлуночка; Неадекватна реакція на навантаження | Ступінь стенозу |
| Після заміни клапана | | Значна шлуночкова аритмія | | |
| Первинна профілактика | | Хірургічне лікування (заміна аортального клапана) | Аміодарон | |
| Вторинна профілактика | | ІКД* | | Аміодарон |
* - можна рекомендувати хворому
ПРОФІЛАКТИКА РСС ПРИ ВПУ СИНДРОМІ
Поширеність синдрому Вольфа-Паркінсона-Уайта (ВПУ) складає 0,1-0,2%. ВПУ може приводити до раптової кардіальної смерті (РСС). Це трапляється, коли пароксизм фібриляції передсердь призводить до дуже швидкої активації шлуночків через додатковий АВ шлях з коротким антероградним періодом рефрактерності та провокує фібриляцію шлуночків. РСС при синдромі ВПУ – рідкий, але драматичний випадок у практично здорової людини. У пацієнтів з клінічними проявами, з виявленими третинними водіями ритму, поширеність РСС із вдалою реанімацією – 2-11%. Популяційні дослідження вказують на набагато нижчу частоту РСС (0,15% у рік).
Декілька досліджень хворих, які вижили після РСС, показали високу частоту наступних маркерів: анамнез симптоматичної тахікардії, короткі інтервали RR між передзбудженими скороченнями у період фібриляції передсердь; множинні додаткові шляхи; шляхи, які розташовані задньо-септально; сімейний характер захворювання та збільшена частота аномалії Ебштейна. Нестійкий характер преекзитації та різка втрата феномену преекзитації при навантажувальному тестуванні вказують на низький ризик РСС. Втрата преекзитації після внутрішньовенної інфузії медикаментів, наприклад, аймаліну або прокаінаміду, також є свідченням низького ризику РСС. Однак, додаткові впливи (навантаження, стрес, алкоголь) можуть скорочувати рефрактерний період додаткового шляху. Часте проведення через додатковий шлях при фібриляції передсердь розглядається, як чутливий маркер ризику, але його специфічність та прогностична цінність є низькими. Однак, передзбуджений інтервал RR<250 мсек має негативну прогностичну цінність РСС>95%.
Приблизно 50% хворих з ЕКГ-синдромом ВПУ не мають аритмій в анамнезі. Більшість таких хворих мають добрий прогноз. Втрата свідомості не має прогностичної цінності для РСС. Але ж у той самий час РСС може бути першим проявом хвороби. При ВЕФД біля 20% хворих без клініки мали прискорений шлуночковий ритм при індукованій фібриляції передсердь. Однак, специфічність та позитивна прогностична цінність цього інвазійного предиктора занадто низькі для скрінінгового застосування при безсимптомному ВПУ. Таким чином, застосування ВЕФД для стратифікації ризику повинно застосовуватись у визначених хворих з анамнезом РСС у родині або у людей, чий спосіб життя або професійні дії потребують оцінки ризику. Детальне ВЕФД доцільне, коли планується абляція додаткових шляхів у хворих з клінічними проявами.
Вдала реанімація хворого з документованою фібриляцією шлуночків або фібриляцією передсердь з клінічними проявами та швидкою відповіддю шлуночків через додатковий шлях – беззаперечне показання для абляції додаткового шляху проведення. З клінічно значимими аритміями лікувальна тактика залежить від їх особливостей. Пацієнтам з безсимптомним синдромом ВПУ можна рекомендувати катетерну абляцію тільки при особливих обставинах, таких як анамнез РСС у родині, високий професійний ризик (у пілотів, шахтарів, операторів важкого індустріального обладнання, тощо) та у спортсменів.
Показання для терапії засновані на консенсусі експертів та клінічному досвіді. Рекомендації наведені в таблиці 20.
Таблиця 20
Синдром Вольфа-Паркінсона-Уайта
| | Дуже важливо | Важливо | Менш важливо |
| Стратифікація ризику | | Короткий (< 250 мс) RR інтервал під час фібриляції передсердь; Короткий (< 270 мс) антероградний рефрактерний період додаткового шляху; Численні додаткові шляхи; • Два та більше суправентрикулярних порушення ритму; • Синкопе в анамнезі, пов’язане з порушенням ритму. | Втрата збудника під час аймалінового або прокаїнамідового тесту |
| Первинна профілактика | Катетерна абляція* у симптомних хворих, при наявності фібриляції передсердь та додаткових шляхів проведення | Катетерна абляція* у асимптомних хворих із сімейним анамнезом РКС, у хворих із професіями високого ризику, у спортсменів | Аміодарон; Анти аритмічні препарати IA та IС класів. |
| Вторинна профілактика | Катетерна абляція* | | |
* - можна рекомендувати хворому.
ПРОФІЛАКТИКА РСС ПРИ ПОРУШЕННЯХ
ПРОВІДНОЇ СИСТЕМИ СЕРЦЯ
РСС може бути результатом брадиаритмій у 15-20% випадків. Коли порушення провідності визване необоротною структурною аномалією, у пацієнтів з порушенням провідності, РСС може бути викликана шлуночковою тахіаритмією. Водій серцевого ритму, безумовно, покращує стан пацієнтів з брадіаритміями і може зменшувати смертність.
Рекомендації по стратифікації ризику та профілактиці РСС при порушеннях провідної системи серця наведені у таблиці 21.
Таблиця 21
Профілактика РСС у хворих з порушеннями провідної системи серця
| | Дуже важливо | Важливо | Менш важливо | |
| Стратифікація ризику | Набута АВ блокада у дорослих | | AV – блокада III cт. AV – блокада II cт. II типу; Супутня кардіальна патологія або СН; Синкопе. | |
| Вроджена АВ блокада III cт. | Синкопе; Подовжений інтервал QT; Вроджені вади серця. | | | |
| Хронічна біфасцикулярна та трифасцикулярна блокада | Супутні захворювання серця СХ або СН | Синкопе, HV(His-Ventricle) 100 мс або відтворення інфра - Гіс блокади під час електростимуляції; Індукуємість ШТ під час ВЕФД | | |
| Профілактика РСС | Імплантація кардіо - стимулятора | | | |
ПРОФІЛАКТИКА РСС ПРИ КАТЕХОЛАМІНЕРГІЧНІЙ ПОЛІМОРФНІЙ ШЛУНОЧКОВІЙ ТАХІКАРДІЇ
Катехоламінергічна поліморфна шлуночкова тахікардія (КПШТ) - як клінічний синдром вперше описана Кумелем в 1978 та більш докладніше Ліндхардтом у 1995р. Це захворювання характеризується адренергічновикликанною поліморфною шлуночковою тахікардією при структурно нормальному серці. Пацієнти зазвичай звертаються до кардіолога у зв’язку з виникненням синкопальних станів, сімейним анамнезом ( втрата свідомості та РСС), які спостерігаються приблизно у третьої частини пацієнтів. ЕКГ графіка при КПШТ характеризується поліморфною шлуночковою тахікардією, яка часто має двонаправлений вигляд QRS-комплексів. Аритмія може бути виявлена при проведенні навантажувального стрес-тесту чи інфузії ізопротеренолу до ЧСС більше ніж 120 ударів на хвилину. Відсутність структурних змін була представлена у дослідженні Ліндхардт та співавт. із середньою тривалістю спостереження 7 років. Такі ж дані отримані і в інших роботах за цією проблемою, передбачаючи, таким чином присутність первинної електричної нестабільності.
У ранніх дослідженнях генетичний аналіз при КПШТ не проводився, однак існують свідчення стосовно аутосомного успадкування, що передбачає генетичні успадкування в основі патогенезу цього захворювання. Пізніше ця концепція була підтримана Сваном та його колегами, які продемонстрували взаємозв’язок між фенотипом КПШТ та участком хромосоми Iq42-q43 у двох великих уражених захворюванням сімей. В останніх дослідженнях Пріорі і соавт. продемонстрували присутність мутацій hRyR2 у 4 сім’ях, які страждають КПШТ, демонструючи таким чином зв’язок між зміненим hRyR2 білком і КПШТ. Ці дані підтверджують концепцію, що КПШТ залежить від генетично закладеного надлишку внутрішньоклітинного кальцію, можливо через вислизання іонів кальцію із саркоплазматичного ретикулуму.
На сьогодні, через недолік контрольованих клінічних досліджень, 0інформація про стратифікацію ризику пацієнтів із КПШТ обмежено. Найбільш крупне дослідження представлено Ліндхартом та соавт. в 1995р. У ньому демонструються дані сімейного анамнезу РСС у 33% випадків та виникнення першого епізоду втрати свідомості у середньому на 7,8±4 році життя. При цьому спостерігалась чітка кореляція між строком першого синкопального епізоду та ступенем важкості захворювання (вважається, що більш ранній початок може розглядатись як предиктор несприятливого прогнозування). Оцінка ризику розвитку важкої клінічної маніфестації повинна бути базована на результатах клінічної оцінки, серйозності анамнезу захворювання та у присутності анамнезу раптової непояснимої серцевої смерті серед родичів. Більшість летальних випадків відбувається у межах другого десятиріччя життя у зовні здорових індивідумів. Однак, відносно висока смертність у пацієнтів з використанням бета-адреноблокаторів (10-5%) може передбачати покази для імплантації ШВР по меншій мірі тим пацієнтам, у яких має місце ранній початок захворювання та наявність в сімейному анамнезі РСС.
Досвід фармакологічного лікування хворих КПШТ обмежений. На сьогодні, єдина терапія, яка мабуть є ефективною - антиадренергічна терапія із використанням бета-адреноблокаторів. Ця концепція базована на ретроспективному аналізі опублікованих випадків, які показали частоту РСС у 4/38 (10,5%) та у 10/21 (48%) пацієнтів з та без терапії бета-блокатором відповідно.
Все ж великі проспективні дослідження не проводились, предсталені рекомендації базуються на думці експертів. Вони наведені в таблиці 22.
Таблиця 22
Профілактика РСС у хворих з катехоламінергічною поліморфною шлуночковою тахікардією
| | Дуже важливо | Важливо | Менш важливо |
| Стратифікація Ризику | Зупинка серця / стійка ШТ | Сімейний анамнез РКС; Нестійка ШТ при Холтерівському моніторингу; Синкопе в дитячому віці | Синкопе |
| Первинна профілактика | - адреноблокатори | ІКД* у пацієнтів з синкопе/ШТ+ - адреноблокатори ІКД у хворих без синкопе / ШТ, коли діагноз встановлений у дитинстві | b - адреноблокатори |
| Вторинна профілактика | ІКД* + - адреноблокатори | - адреноблокатори | |
- - можна рекомендувати хворому.
ПРОФІЛАКТИКА РСС ПРИ АНОМАЛЬНОМУ ВІДХОДЖЕННІ КОРОНАРНИХ АРТЕРІЙ.
Аномалії коронарних артерій рідкі. Поширеність цих аномалій в загальній популяції невідома. По різним даним вони зустрічаються у 0,3%-1,2% пацієнтів, що пройшли коронарографію. Найбільш часта коронарна аномалія – артерії циркумфлекса (як правило, судина відходить від правого коронарного синуса). В цій групі не відмічалось несприятливих подій. Однак, початок лівої коронарної артерії від правого або не- коронарного аортального синуса Вальсальви, вірогідно, пов’язано з збільшенням ризику РСС, особливо, коли артерія проходить між аортою та легеневою артерією. Аномальне відходження правої коронарної артерії від лівого синуса Вальсальви, відповідно отриманим даним пов’язано з РСС, але не має того ж рівня ризику, як аномальне відродження лівої коронарної артерії. РСС є також основною причиною смерті у хворих з аномальним відходженням лівої коронарної артерії від легеневої артерії, що дожили до зрілості.
РСС звичайно виникає у чоловіків при фізичній активності. На жаль, дані літератури показують, що діагностувати подібні аномалії прижиттєво можливо лише приблизно у 20% випадків. Наявність аномально розташованої коронарної артерії слід запідозрити у молодих пацієнтів, переважно чоловіків, що мають загрудинні болі при навантаженнях, синкопальні стани в поєднанні з непояснюватними змінами QRS і ST-T. Стрес-тести, допплерівське кольорове картування і трансезофагальна ехокардіографія є часто застосовуваними неінвазивними методами діагностики аномального відходження лівої коронарної артерії. Тим не менше, коронарна ангіографія повинна бути рекомендована навіть при негативному навантажувальному тесті всім молодим пацієнтам, що перенесли зупинку серця.
У пацієнтів з аномальним відходженням лівої коронарної артерії від легеневої артерії реімплантація судини в аорту зменшує смертність та тривалість захворювання. У пацієнтів з аберантним відходженням лівої або правої коронарної артерії, які благополучно перенесли епізод шлуночкової фібриляції, може бути рекомендовано хірургічне втручання (як правило, шунтування). У хворих з ознаками ішемії міокарду доцільним є хірургічне лікування.
Дані рекомендації базуються на невеликих оглядових дослідженнях і консенсусі експертів. Вони наведені в таблиці 23. Таблиця 23
Профілактика РСС при аномальному розвитку коронарних артерій
| | Дуже важливо | Важливо | Менш важливо |
| Стратифікація ризику | Зупинка серця | Молоді пацієнти із стенокардією; Позитивний тест під час стрес- ехокардіографії | |
| Первинна профілактика | Хірургічне лікування* | | |
| Вторинна профілактика | Хірургічне лікування* | | |
* - можна рекомендувати хворому.
ПРОФІЛАКТИКА РСС ПРИ МІОКАРДІАЛЬНИХ “МІСТОЧКАХ”
Міокардіальні “місточки” складаються з фіброзно-м’язових ніжок, які покривають епікардіальні коронарні артерії на різній довжині. Міокардіальні “місточки” по даним ангіографії зустрічаються в 0,5-4,5% випадків. Ліва передня нисхідна артерія уражується практично у всіх випадках. Типовим ангіографічним проявом є систолічне звуження судини із-за минучої міокардіальної компресії. Хоча багато міокардіальних “місточків” можуть бути нешкідливими, вони також можуть бути причиною ішемії міокарду, інфаркта міокарду, злоякісних шлуночкових аритмій, АВ блокад та РСС.
Верифікація та оцінка важкості міокардіального “місточка” є важливим клінічним завданням. Для оцінки гемодинамічної значимості міокардіальних “місточків” застосовуються навантажуючий ЕКГ тест, добутамінова стрес-ехокардіографія або міокардіальна перфузійна сцинтиграфія. В окремих випадках проводиться внутрішньокоронарне допплерівське дослідження швидкості потоків або коронарографія при добутаміновому стрес-дослідженні для оцінки стану всередині судини під впливом міокардіального “місточка”. Міокардіальні “місточки” спостерігаються у 30-50% пацієнтів з гіпертрофічною каордіоміопатією та розглядаються як можлива причина РСС у цих пацієнтів.
Пацієнти з наявністю міокардіальних “місточків” та клінічними проявами добре піддаються терапії бета-адреноблокаторами. Ефект бета-адреноблокаторів в даному випадку обумовлений негативною інотропною та хронотропною дією. Нітрати збільшують ЧСС і можуть призводити до погіршення стану пацієнтів. Пацієнтам, які рефрактерні до медикаментозної терапіі, проводиться оперативне лікування (міотомія або коронарне шунтування). Доцільними також можуть бути ангіопластика або стентування. Довготривалий прогноз ізольованих міокардіальних “місточків” представляється сприятливим, але в деяких випадках вони можуть викликати шлуночкові тахіаритмії та РСС.
Рекомендації щодо стратифікації ризику раптової серцевої смерті при міокардіальних “місточках” основані на обмеженій кількості невеликих обзорних спостережень і консенсусі експертів. Вони наведені в таблиці 24.
Таблиця 24
Профілактика РСС у хворих з міокардіальними “містками”
| | Дуже важливо | Важливо | Менш важливо |
| Стратифікація ризику | Зупинка серця; Гемодинамічно значима ШТ | Ішемія міокарда | |
| Первинна профілактика | Хірургічне лікування у пацієнтів ІХС* | -адреноблокатори | |
| Вторинна профілактика | Хірургічне лікування у пацієнтів ІХС* | | -адреноблокатори |
- - можна рекомендувати хворому.
ПРОФІЛАКТИКА РСС ПРИ “СПОРТИВНОМУ СЕРЦІ”
Аномалії серцево-судинної системи у багатьох спортсменів заключаються в збільшеній масі ЛШ, збільшенні порожнини, збільшеній товщині стінки, або їх поєднання. Серцево-судинні причини РСС у спортсменів суттєво змінюються в залежності від віку. У віці більше 35 років переважна причина смерті – ІХС. Навпаки, у спортсменів менше 35 років є близько 20 основних причин у вигляді вроджених захворювань, які є рідкими в загальній популяції. Кілька досліджень вказують на гіпертрофічну кардіоміопатію, як найбільш часту причину РСС у молодих тренованих атлетів, що складає приблизно третю частину фатальних подій. Другою по важливості та частоті є вродженні аномалії коронарних артерій, такі як неправильне відходження судини від синуса Вальсальви. Вивчення аутопсій кількох тіл молодих спортсменів, що померли внаслідок РСС, показує, що кардіоміопатія правого шлуночка зустрічається не часто. Скринінг у безсимптомних нормальних популяцій спортсменів дозволяє виявляти деякі порушення, особливо при поєднанні 12-канальної ЕКГ та Ехо-КГ. Усунення атлетів з серцево-судинними захворюваннями від змагань та тренувань до проведення повної оцінки патології серцево-судиної системи зменшує ризик.
Оцінку стану спортсменів, які поступають з порушеннями ритму серця, органічними захворюваннями серця або другими признаками і симптомами, які вказують на можливу наявність серцево-судиного захворювання, слід проводить так же, як і у любого другого пацієнта, але з урахуванням специфічності їх заняття спортом.
Дані рекомендації були зроблені на основі неконтрольованих, ретроспективних та логічно виведених спостережень.
Профілактика РСС у вагітних
Вагітним, у яких розвинулась гемодінамически нестабільна ШТ або ФШ, слід провести кардіоверсію або дефібриляцію. У хворих с наявністю подовженого інтервалу QT, у котрих раніше відмічалися симптоми захворювання, необхідно подовження терапії β-адреноблокаторами на протязі усього періоду вагітності і після родів, за винятком , коли мають місце противопоказання к такому лікуванню.
Профілактика РСС у людей похилого віку
Не слід використовувати ІКД у людей похилого віку, у яких прогнозуема тривалість життя у зв’язку з основнимі супутніми захворюваннями триває менш 1 року. Необхідно використовувати β-адреноблокатори у людей похилого віку більш активніше для зниження общей смертності.
Раптова смерть у дітей.
У літературі останніх років велика увага надається синдрому раптової смерті у дітей грудного віку, причому цей синдром виділений у самостійну педіатричну проблему. Даний синдром характеризується несподіваною смертю практично здорової дитини у віці від 7 днів до 1 року, при якій ретельно проведена аутопсія не дозволяє пояснити причину смерті. Існуючі в даний час дві основні гіпотези, – порушення дихання у виді апное і порушення серцевої діяльності, — не пояснюють всіх аспектів даної проблеми.
ПЕРВИННА ПРОФІЛАКТИКА РСС ПРИ “ІСТИННО ЕЛЕКТРИЧНИХ” ЗАХВОРЮВАННЯХ СЕРЦЯ
У пацiєнтiв з "iстинно електричними" феноменами, при яких збільшується ймовірність РСС, доцiльнiсть первинної профiлактики нерідко викликає значно менше сумнiвiв та дискусiй, ніж у пацієнтів з ІХС, ускладненою шлуночковими аритміями.
