Лекция № Дата: Раздел: «Молекулярная физика. Термодинамика»
| Вид материала | Лекция |
- Молекулярная физика и термодинамика статистический и термодинамический методы Молекулярная, 12.67kb.
- Программа по физике для 10-11 классов общеобразовательных, 75.87kb.
- Лекция № Дата: Раздел: «Молекулярная физика», 39.5kb.
- Учебно-методический комплекс дисциплина «физика» Кафедра общей и экспериментальной, 611.05kb.
- Методические разработки кафедры «Физика», 155.63kb.
- Молекулярная физика и термодинамика. Лекция №1 Молекулярно-кинетическая теория Основные, 10053.18kb.
- Курс 1 семестр 2 количество кредитов, 29.05kb.
- Учебно-методический комплекс по дисциплине Молекулярная физика для специальности 010701, 480.43kb.
- Пуск Все программы Программы «Физикона» Физика 7-11 Локальная версия Лаборатории, 30.83kb.
- Физика систем многих частиц (молекулярная физика), 324.5kb.
Физика 10 кл. МКТ и термодинамика.
| Лекция № 1. | Дата: |
| Раздел: «Молекулярная физика. Термодинамика». | |
| Тема: «Молекулярно- кинетическая теория». | |
| Преподаватель: Сычева Е.В. | |
| | Молекулярная физика | |
| Молекулярно- кинетическая теория. | Термодинамика- раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями (не рассматривает микропроцессы, лежащие в основе). | |
| | Тепловые двигатели. | Агрегатные состояния. Фазовые переходы. |
| Идеальный газ- это модель, которая удовлетворяет следующим условиям: | Объем всех молекул газа много меньше объема сосуда |
| Силы притяжения между молекулами малы | |
| Молекулы взаимодействуют при соударении только упруго | |
| Время столкновения много меньше времени между столкновениями | |
| Свойства идеального газа | При столкновении молекул со стенками сосуда они оказывают давление |
| Газ можно сжать до 0 | |
| При абсолютном 0 температур давление газа равно 0 | |
| Положения молекулярно- кинетической теории: | Все вещества состоят из мельчайших частиц: атомов, молекул. |
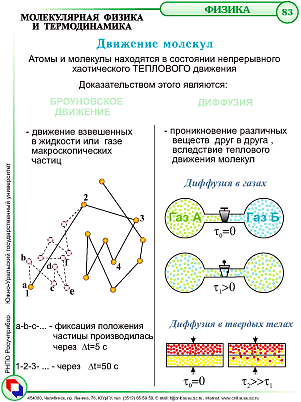
| Частицы находятся в беспрерывном хаотическом движении. | |
| Частицы взаимодействуют между собой. | |
| Броуновское движение | Хаотическое движение взвешенных в жидкости или газе частиц под действием ударов молекул жидкости или газа. |
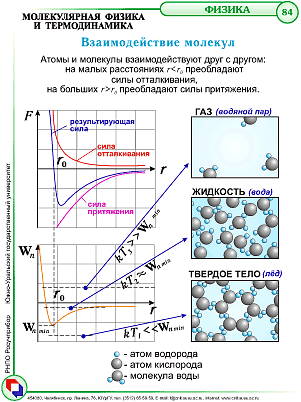
| Диффузия | Явление проникновения молекул одного вещества в межмолекулярные промежутки другого. |
| Температура | Скалярная физическая величина, характеризующая степень нагретости тела (мера средней кинетической энергии молекул). |
| | | Агрегатные состояния вещества | | | |||
| Внутренняя энергия вещества | | ||||||
| твердое | 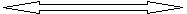 | | ж  идкое идкое | | | газо-образное | |
| Энергия взаимодействия частиц | Энергия движения частиц | | Энергия взаимодействия частиц | Энергия движения частиц | | Энергия взаимодействия частиц | Энергия движения частиц |
| | | | | | | | |
| | | | | | | | |
| Микропараметры системы | Макропараметры системы |
| Характеристики отдельно взятой частицы газа: | Характеристики всего газа как единого целого: |
| Масса, скорость, кинетическая энергия частицы. | Давление, объем, температура. |
| | |
| | Формула | Величина: название, обозначение, единицы измерения | Определение |
| | 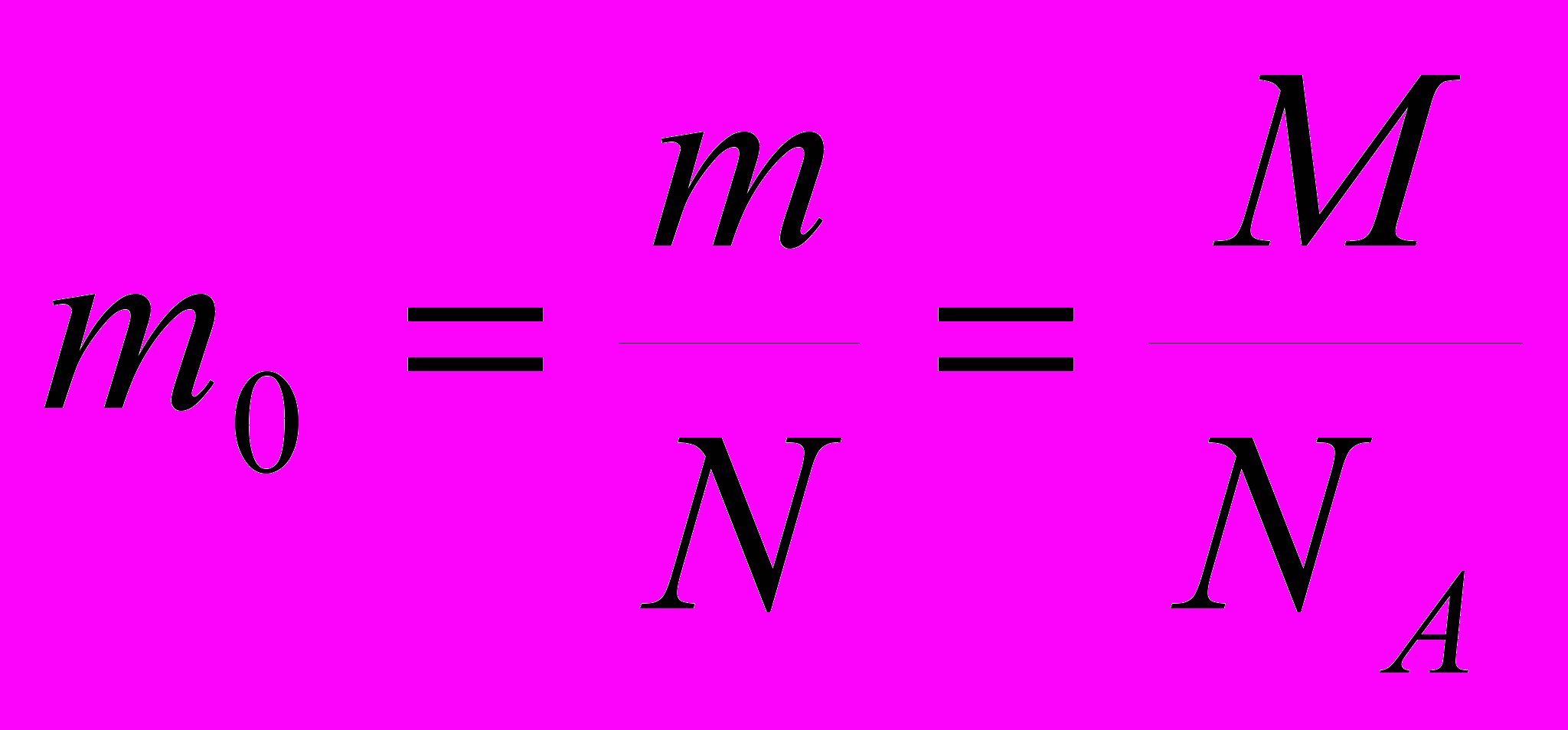 | масса одной частицы (кг), масса всего газа (кг), количество частиц, молярная масса газа (кг/моль), постоянная Авогадро (моль -1). | Скалярная физическая величина, численно равная отношению массы всего газа к количеству частиц, в нем содержащихся. |
| | 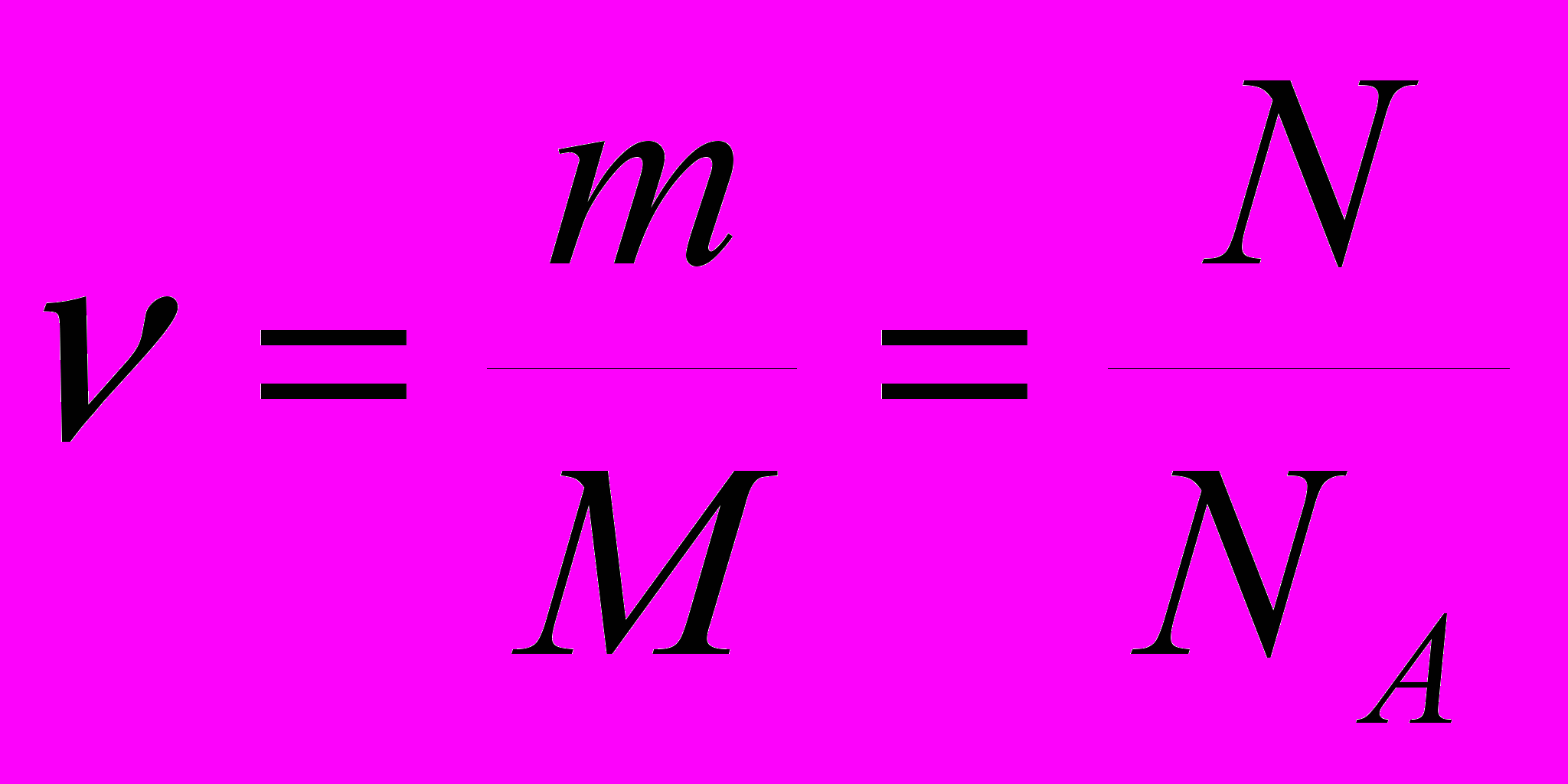 | количество вещества (моль), масса всего газа (кг), молярная масса газа (кг/моль), количество частиц, постоянная Авогадро (моль -1). | Скалярная физическая величина, численно равная отношению массы всего газа к его молярной массе. |
| | 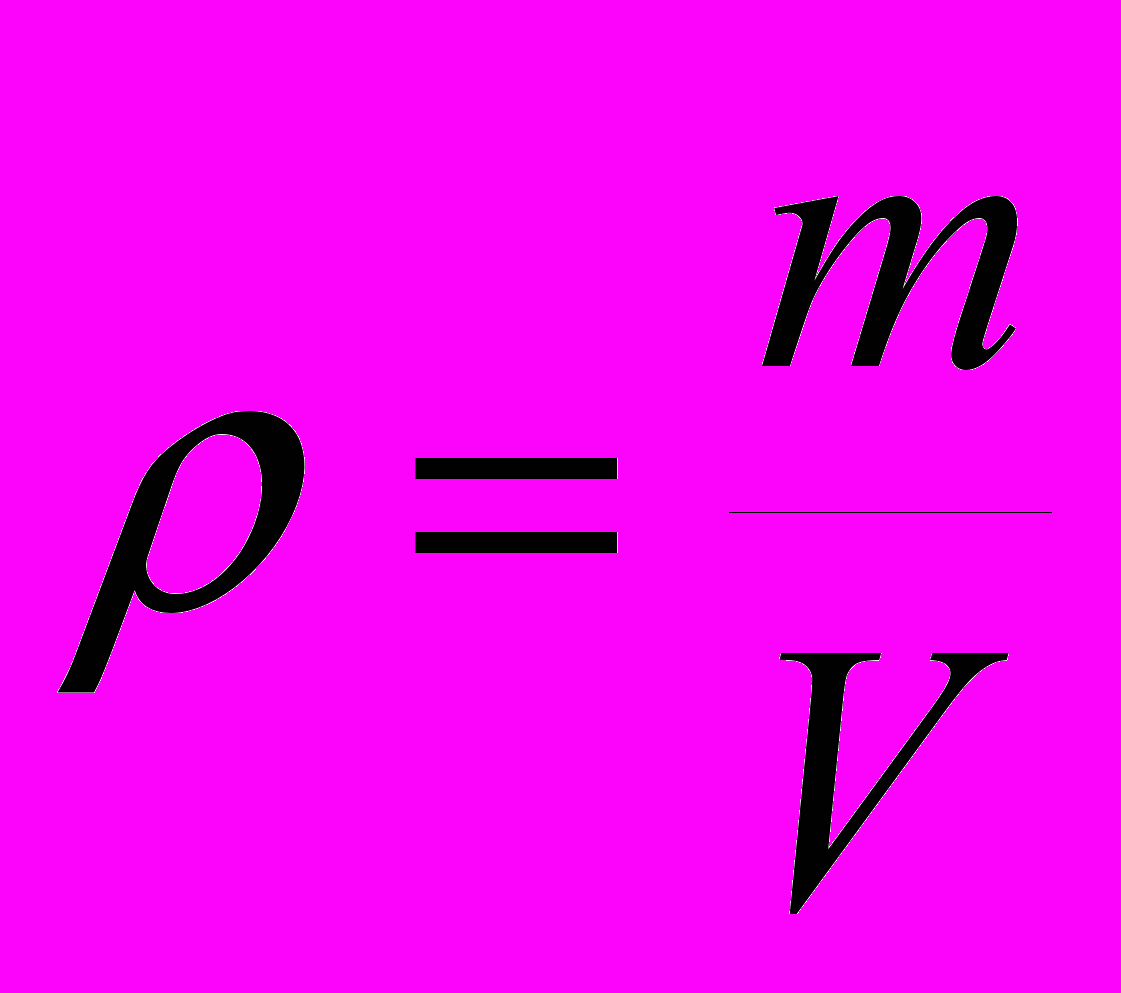 | плотность вещества (кг/ м3), масса вещества (кг), объем вещества (м3). | Скалярная физическая величина, численно равная отношению массы вещества к объему вещества. |
| | 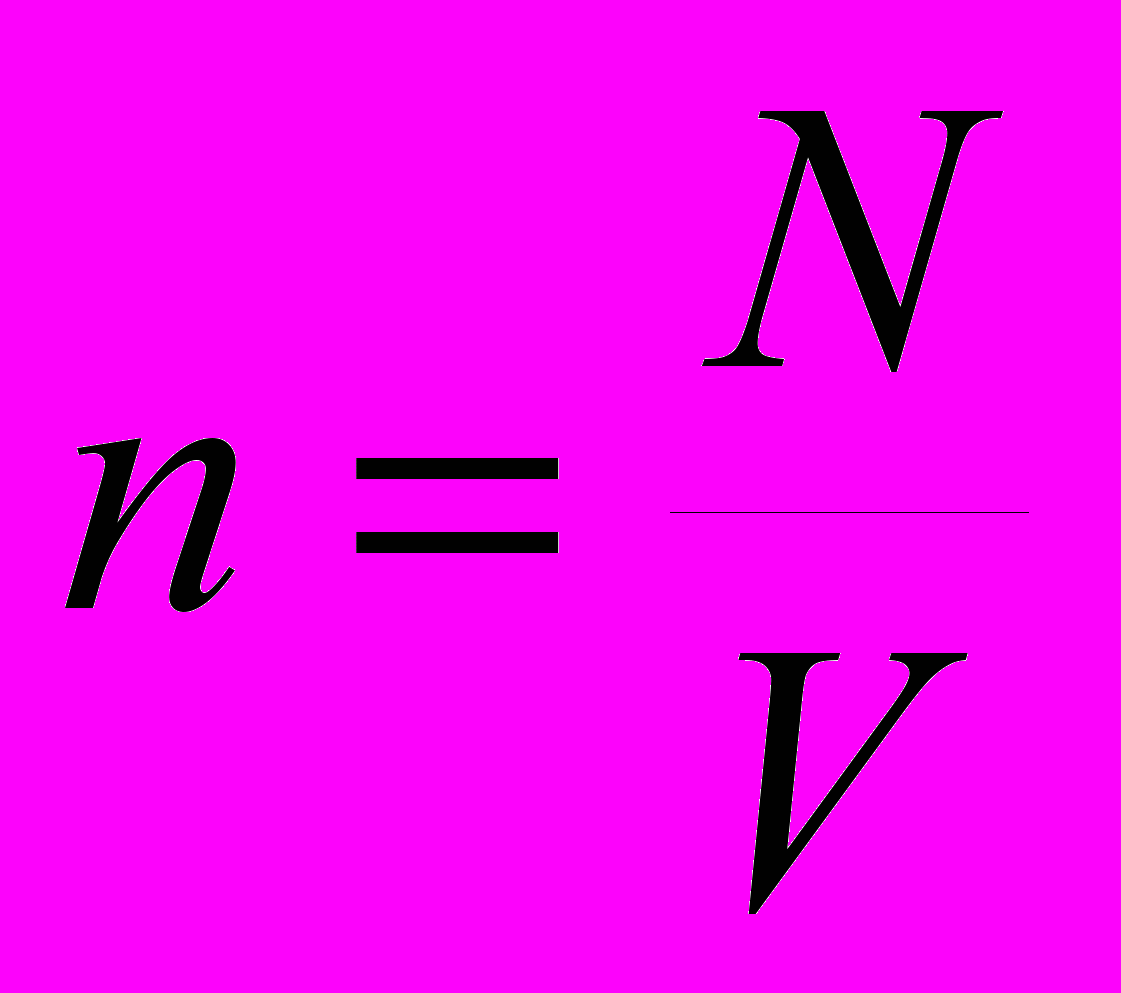 | концентрация частиц (м-3). количество частиц, объем вещества (м3). | Скалярная физическая величина, численно равная отношению количества частиц вещества к объему всего вещества. |
| | 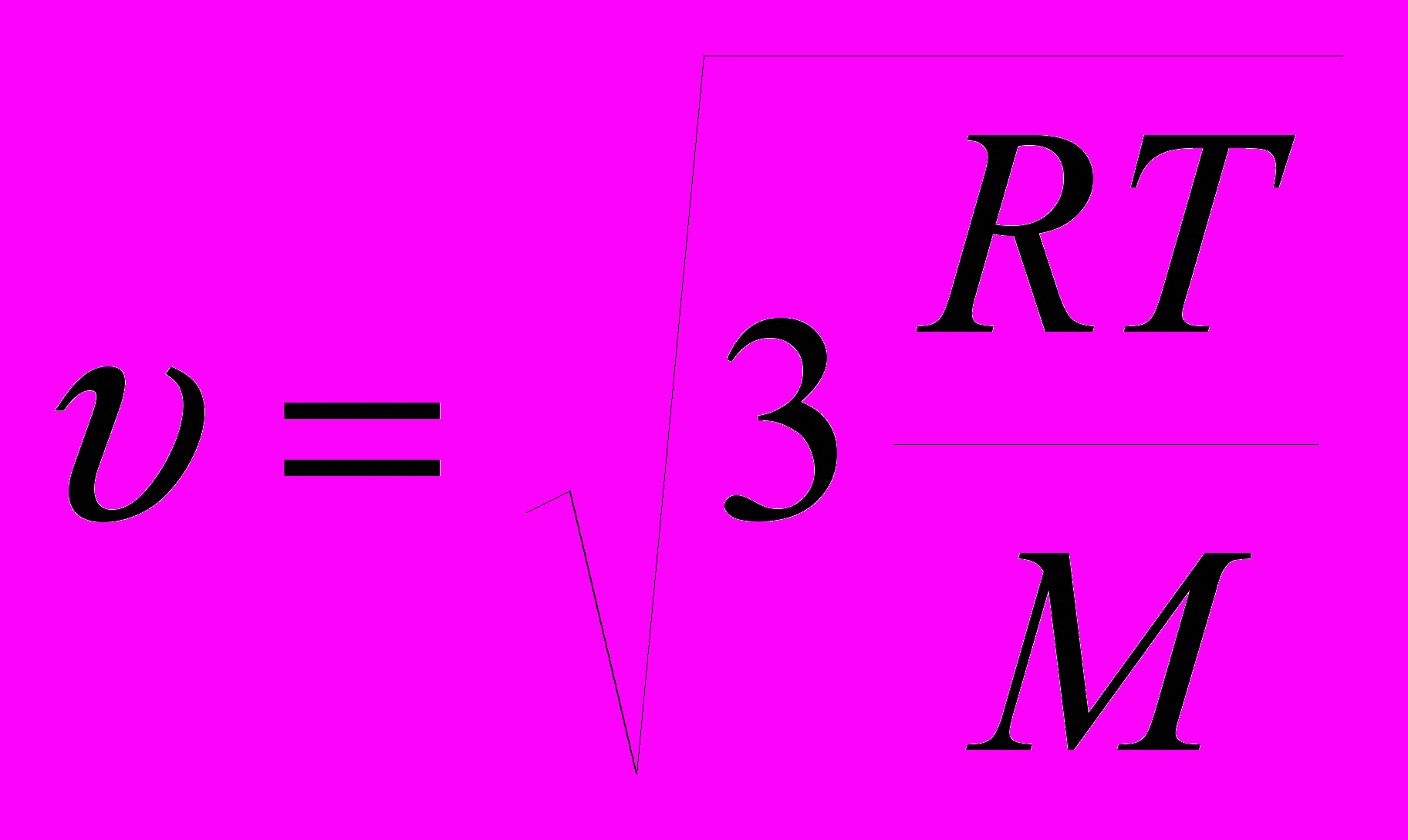 | скорость средняя квадратичная (м/c), универсальная газовая постоянная (Дж/ моль*К), абсолютная температура (К), молярная масса газа (кг/моль). | Скалярная физическая величина, численно равная корню квадратному из отношения произведения газовой постоянной на абсолютную температуру к молярной массе вещества. |
| | 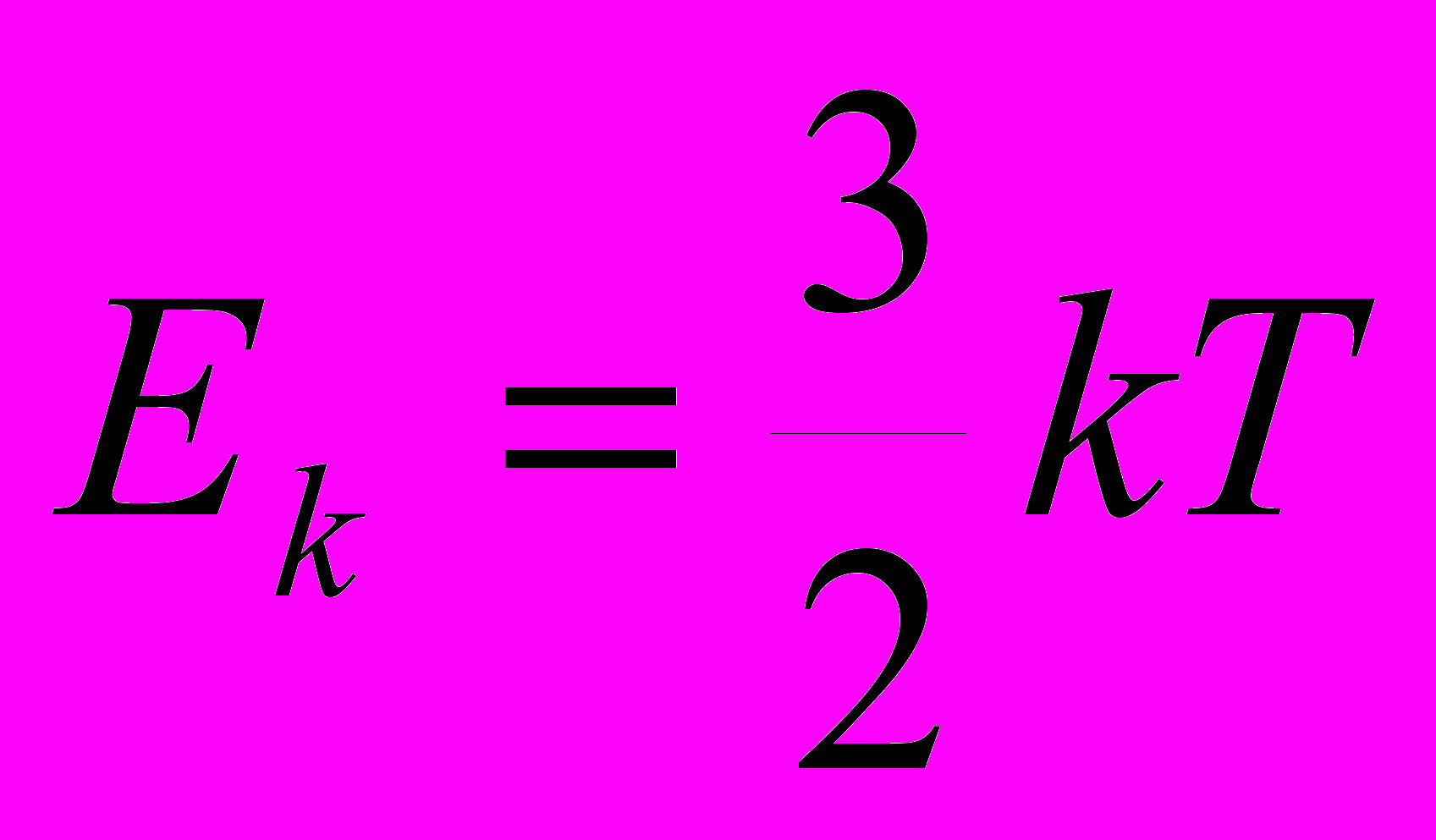 | кинетическая энергия (Дж), постоянная Больцмана (Дж/К), абсолютная температура (К). | Скалярная физическая величина, численно равная произведению постоянной Больцмана на абсолютную температуру. |
| | 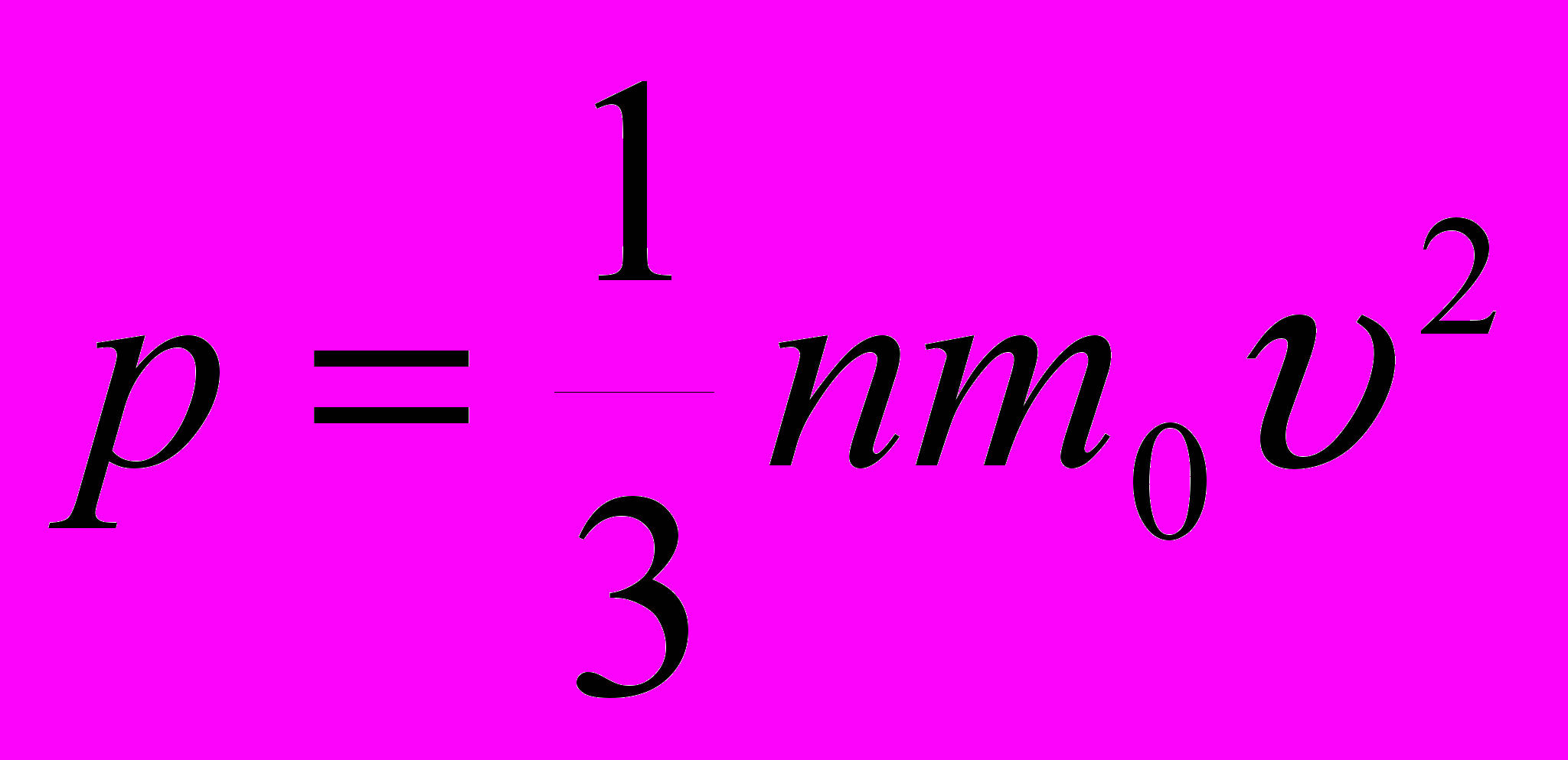 | давление газа (Па), концентрация частиц (м-3). масса одной частицы (кг), квадрат средней скорости (м2/с2). | Скалярная физическая величина, численно равная произведению концентрации частиц на массу одной частицы на квадрат средней скорости. |
| | 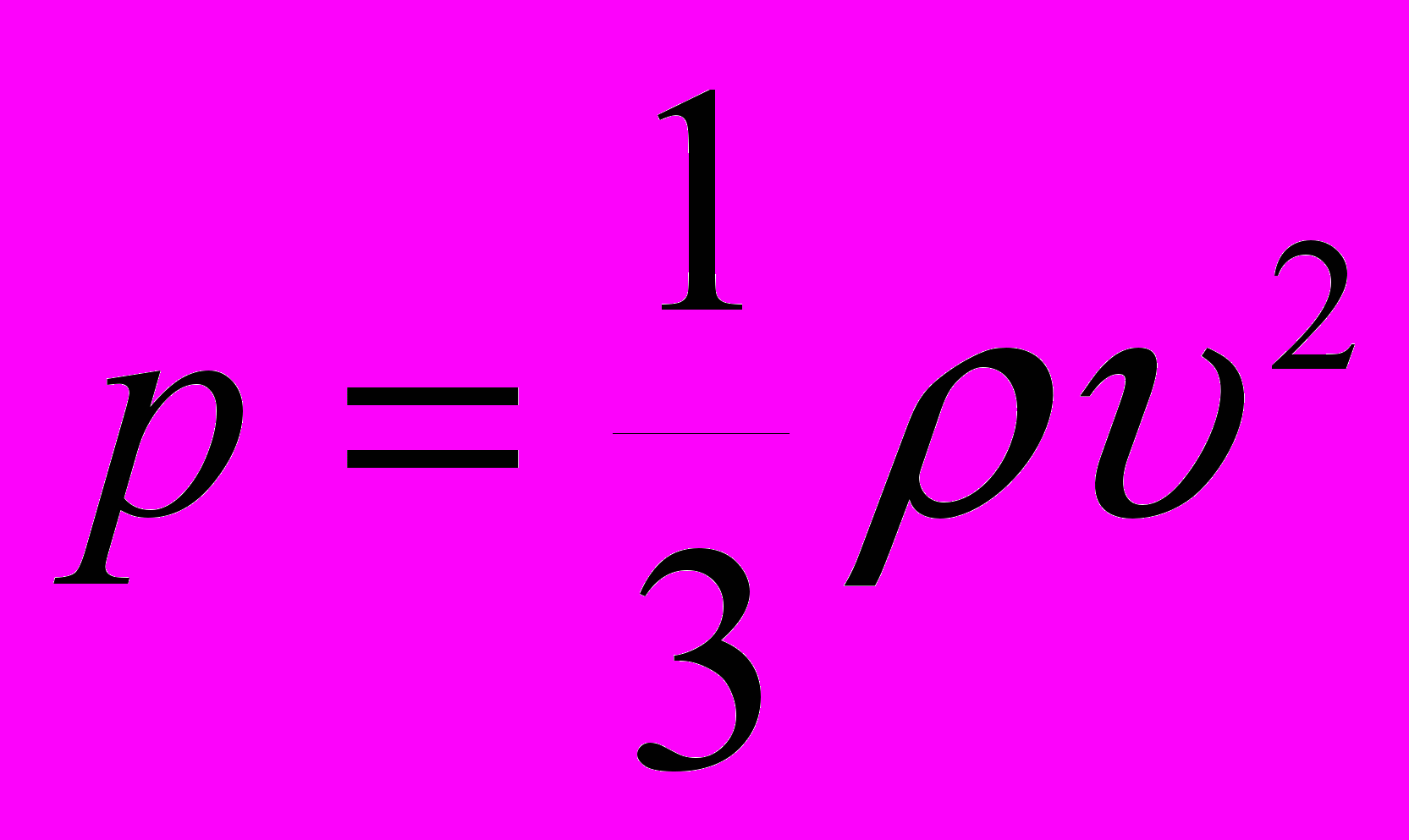 | давление газа (Па), плотность вещества (кг/ м3), квадрат средней скорости (м2/с2). | Скалярная физическая величина, численно равная произведению плотности вещества на квадрат средней скорости. |
| | 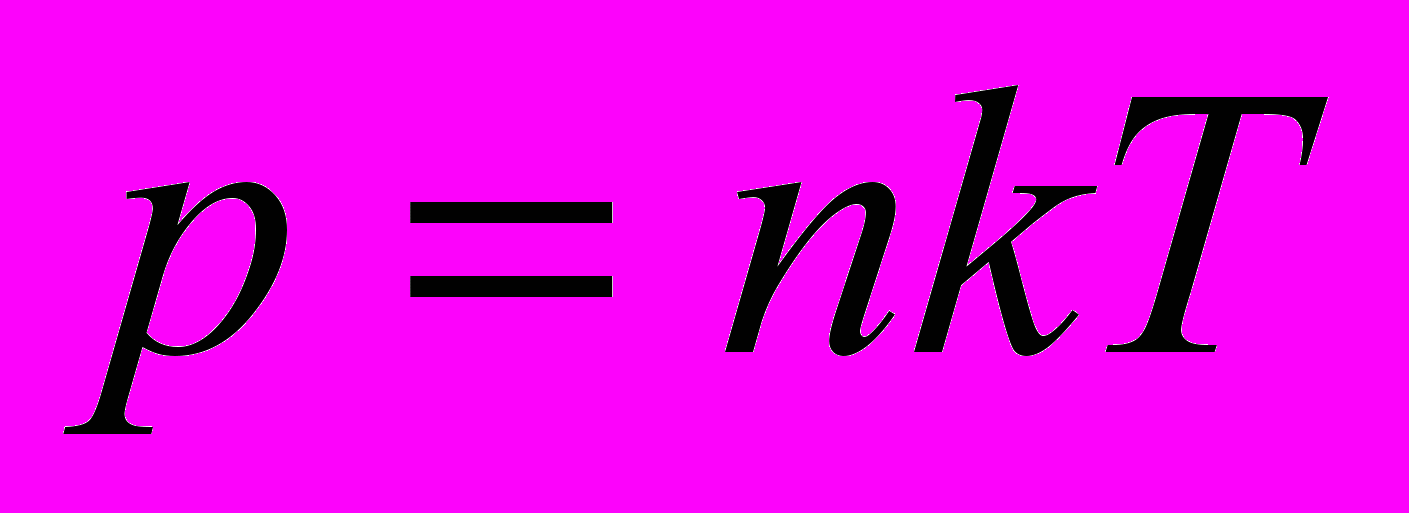 | давление газа (Па), концентрация частиц (м-3), постоянная Больцмана (Дж/К), абсолютная температура (К). | Скалярная физическая величина, численно равная произведению концентрации частиц на постоянную Больцмана на абсолютную температуру. |
| | 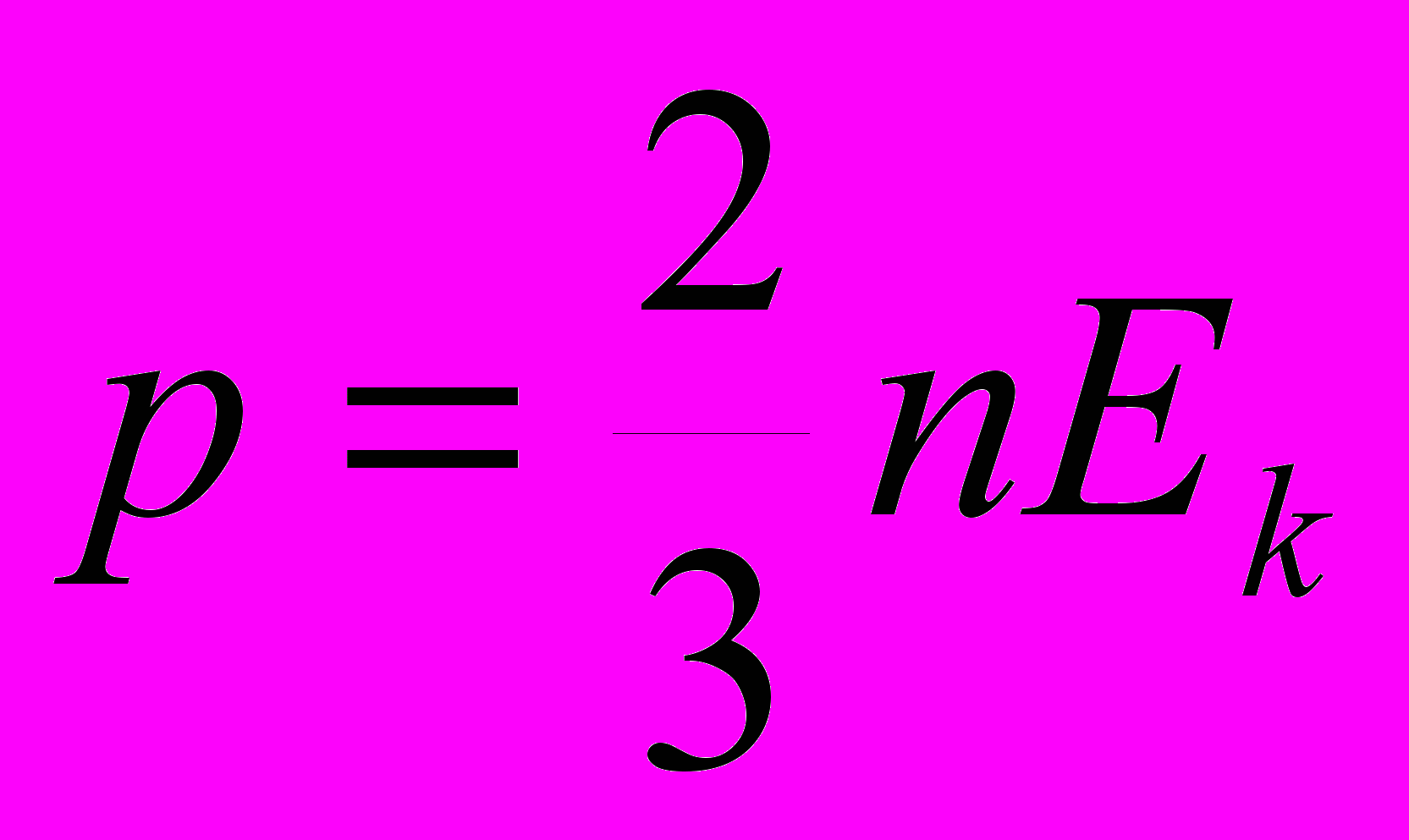 | давление газа (Па), концентрация частиц (м-3), кинетическая энергия (Дж). | Скалярная физическая величина, численно равная произведению концентрации частиц на среднюю кинетическую энергию частиц. |
| | 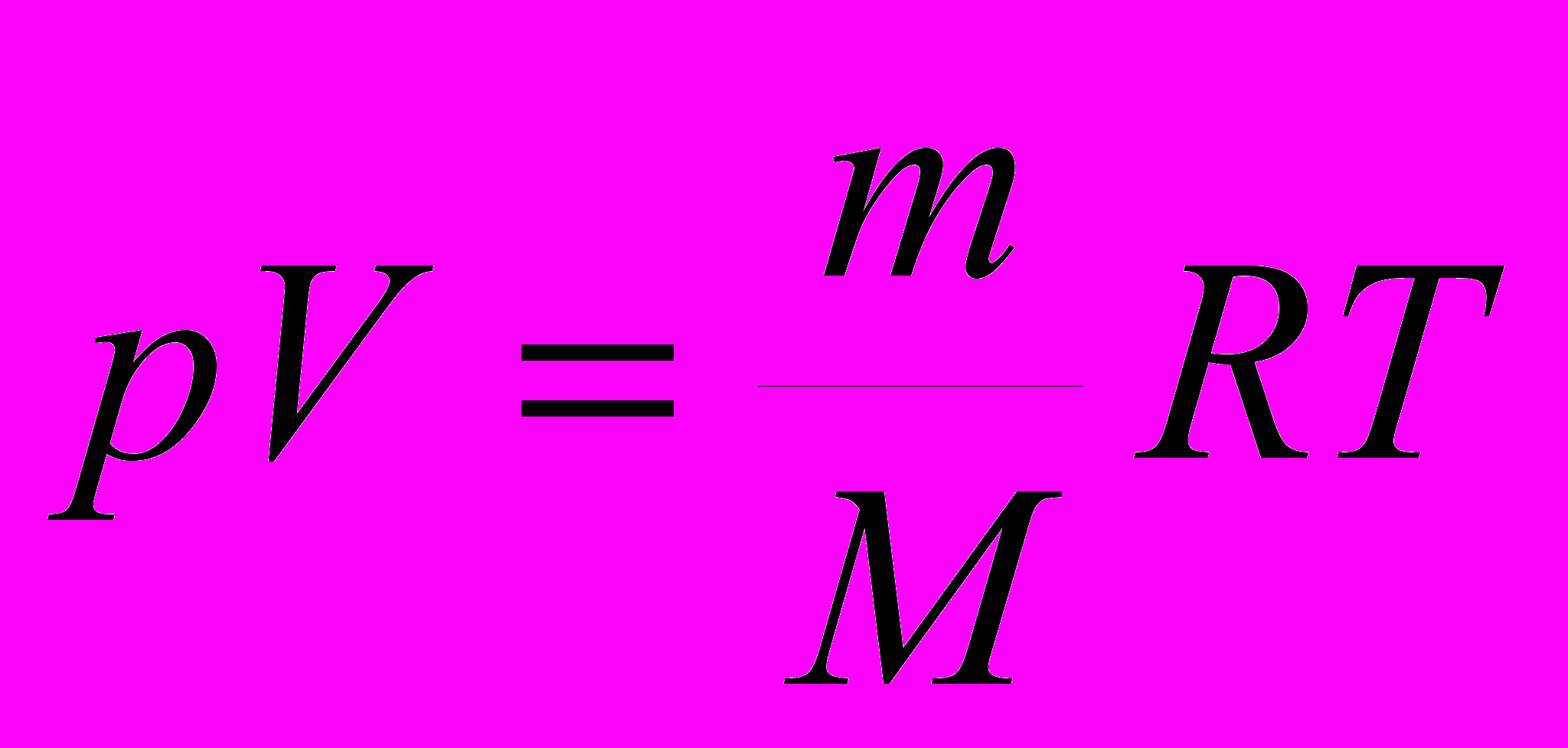 | давление газа (Па), объем вещества (м3), масса вещества (кг), универсальная газовая постоянная (Дж/ моль*К), абсолютная температура (К), молярная масса газа (кг/моль), | Уравнение Менделеева- Клапейрона (уравнение состояния идеального газа): произведение давления газа на его объем равно отношению произведения массы газа на газовую постоянную на абсолютную температуру к молярной массе газа. |
| | 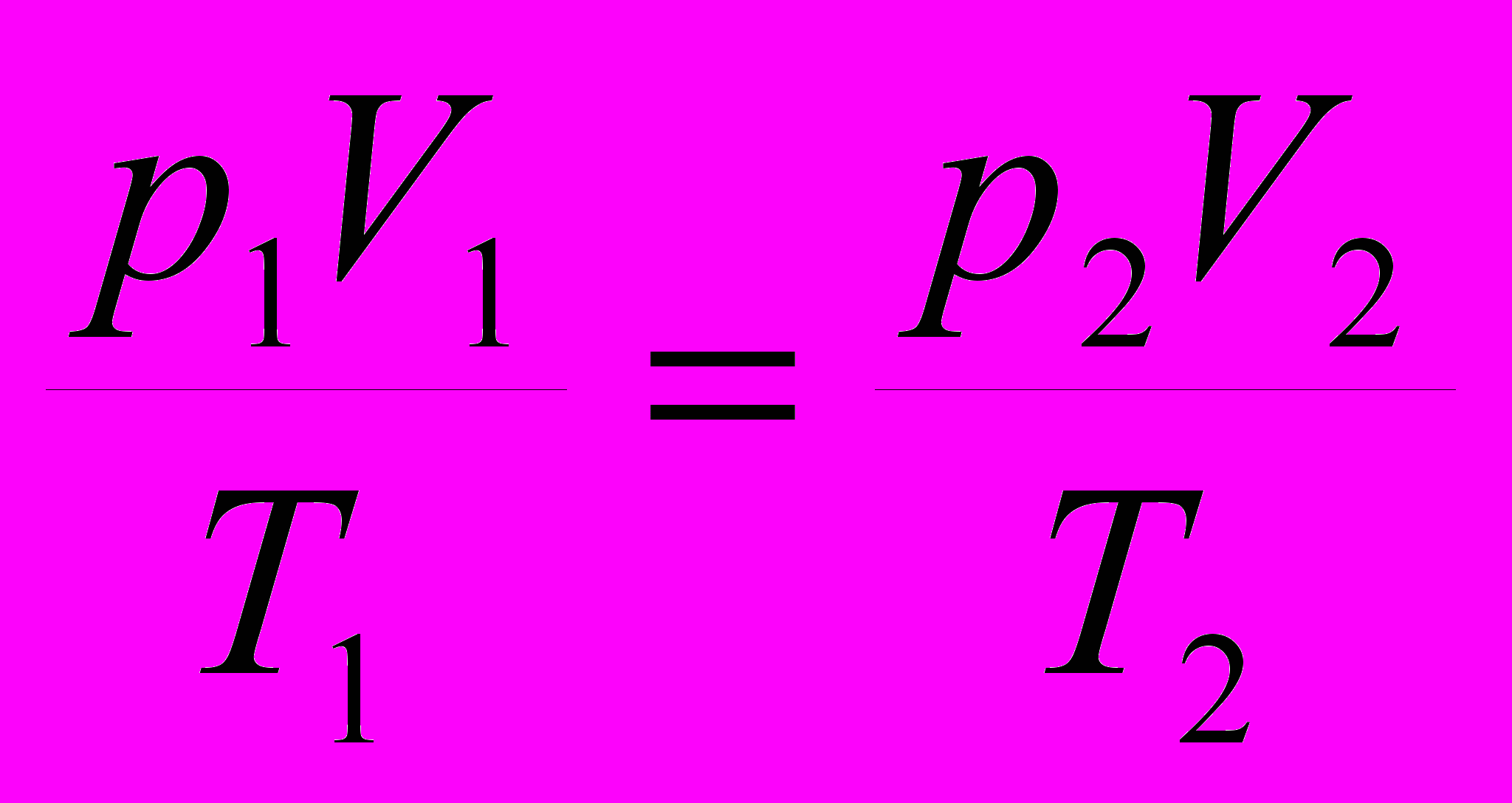 | давление газа (Па), объем вещества (м3), абсолютная температура (К). | Уравнение перехода газа из одного состояния в другое: при переходе газа из одного состояния в другое отношение произведения давления газа на объем к температуре есть величина постоянная. |
| Пример №1. | | |
| | ||
| Дано: | Система интернациональная | Решение. |
| | | |
| | | Ответ: |
| Лекция № 2. | Дата: |
| Раздел: «Молекулярная физика. Термодинамика». | |
| Тема: «Термодинамика». | |
| Преподаватель: Сычева Е.В. | |
| | Термодинамика | |
| Внутренняя энергия системы | Работа | Количество теплоты |
| Энергия хаотического (теплового) движения микрочастиц системы и энергия взаимодействия этих частиц. | Мера переданной энергии при трении, сжатии от одного тела к другому (при изменении объема). | Мера переданной энергии при процессе теплопередачи от одного тела к другому. |
| Термодинамическая система | Совокупность макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой, так и с другими телами. | |
| Термодинамическое равновесие | Равновесие макроскопической системы, если ее состояние с течением времени не меняется. | |
| Теплопередача | Процесс передачи тепла от более нагретого тела к менее нагретому без совершения работы. | |
| Первый закон термодинамики | Количество теплоты, переданное системе. Расходуется на увеличение ее внутренней энергии и совершение работы системой над внешними телами. | |
| Второй закон термодинамики | Невозможен процесс, единственным результатом которого была бы передача энергии от холодного тела к горячему. | |
| | Формула | Величина: название, обозначение, единицы измерения | Определение |
| | 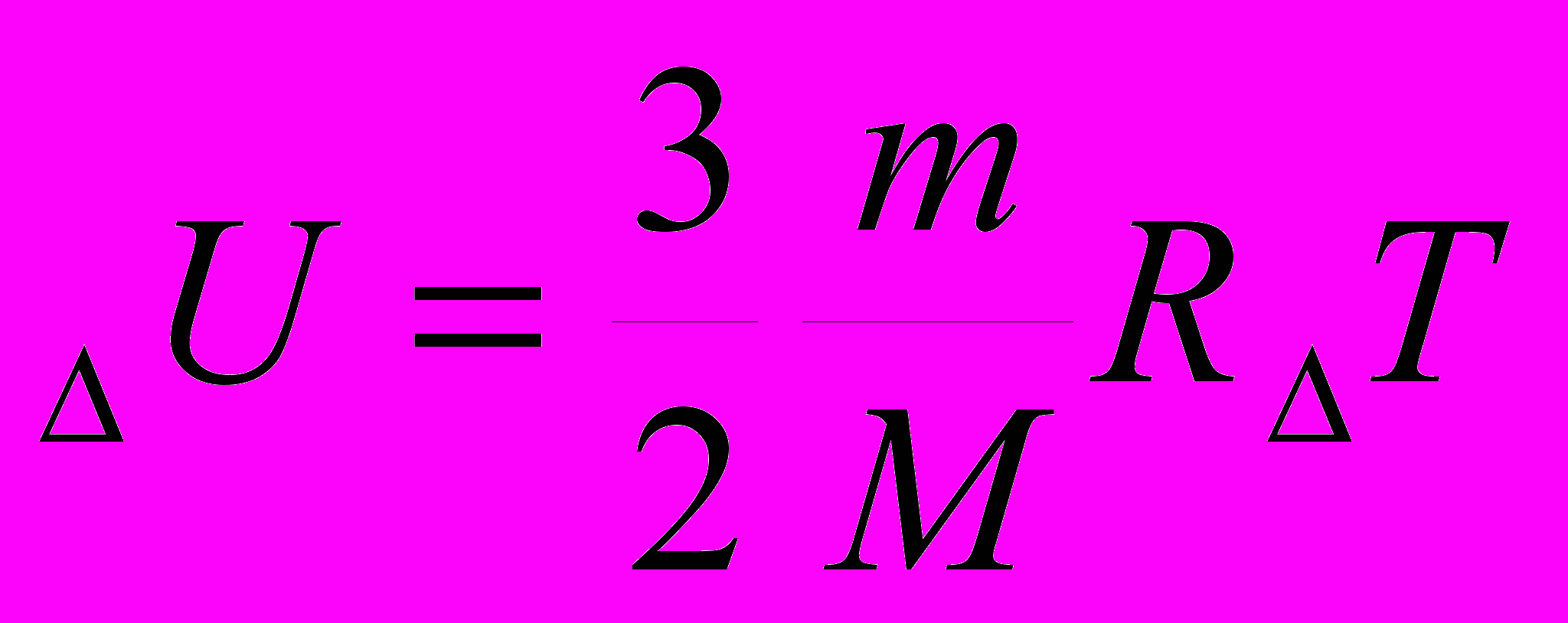 | изменение внутренней энергии (Дж), масса вещества (кг), универсальная газовая постоянная (Дж/ моль*К), изменение абсолютной температуры (К), молярная масса газа (кг/моль). | |
| | 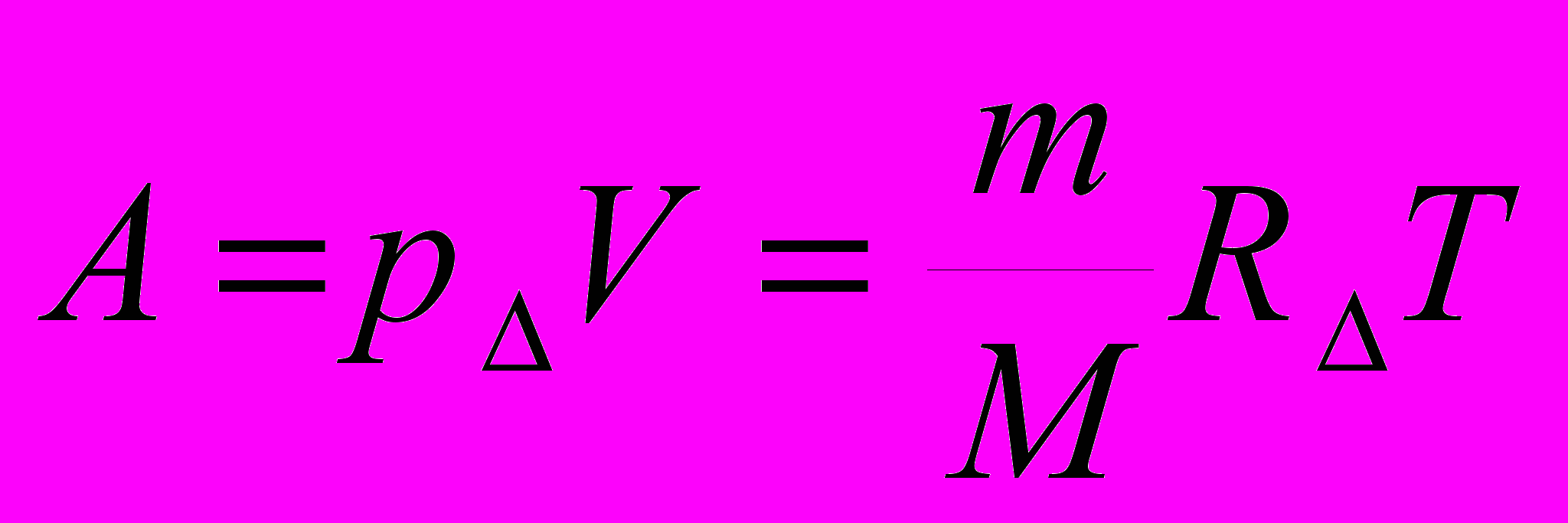 | работа газа (Дж), давление газа (Па), изменение объема (м3), масса вещества (кг), универсальная газовая постоянная (Дж/ моль*К), изменение абсолютной температуры (К), молярная масса газа (кг/моль). | |
| | 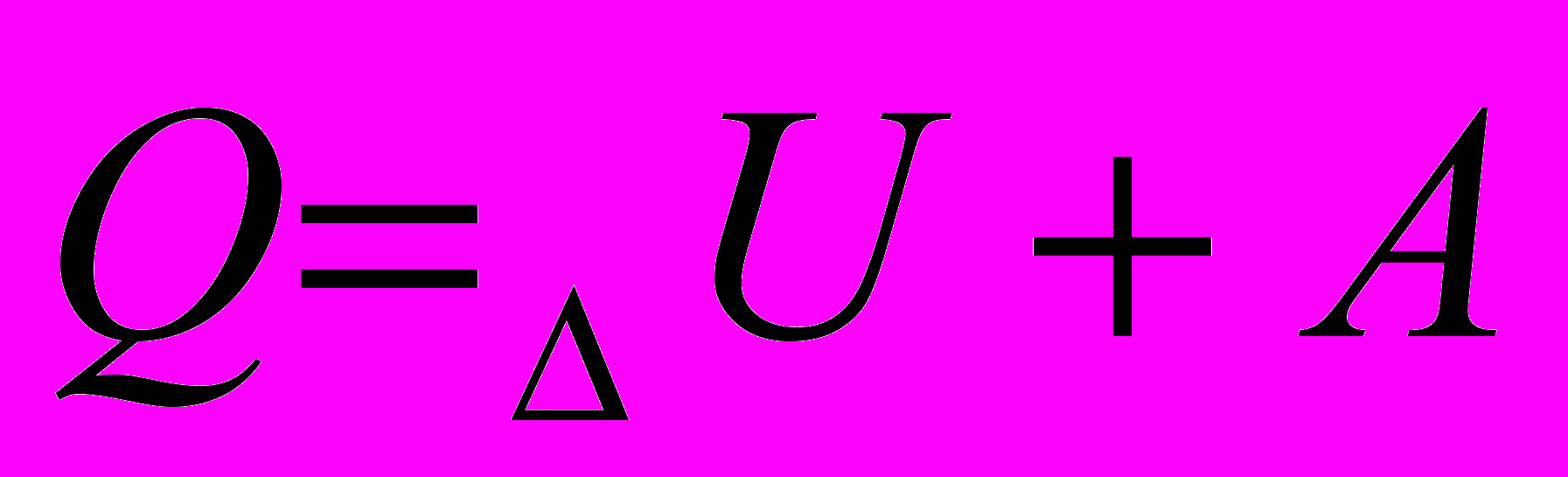 | количество теплоты (Дж), изменение внутренней энергии (Дж), работа газа (Дж). | |
| | 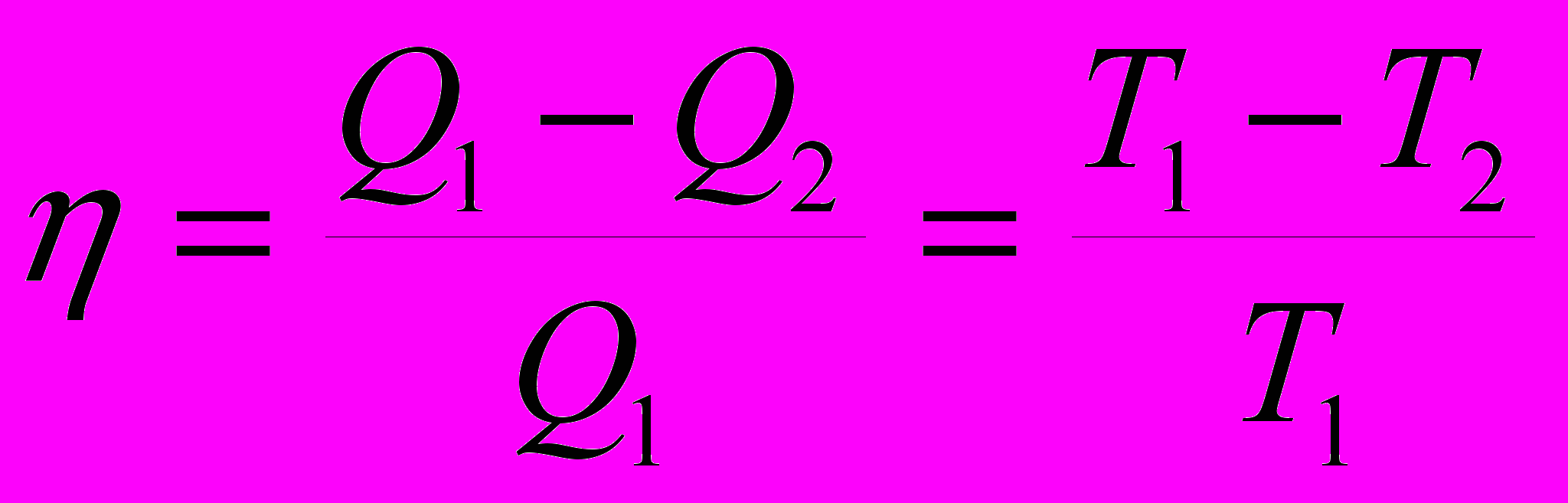 | коэффициент полезного действия, количество теплоты, переданное нагревателем (Дж), количество теплоты, отданное холодильником (Дж), количество теплоты, переданное нагревателем (Дж), абсолютная температура нагревателя (К), абсолютная температура холодильника (К), абсолютная температура нагревателя (К). | |
| | NA- постоянная Авогадро | 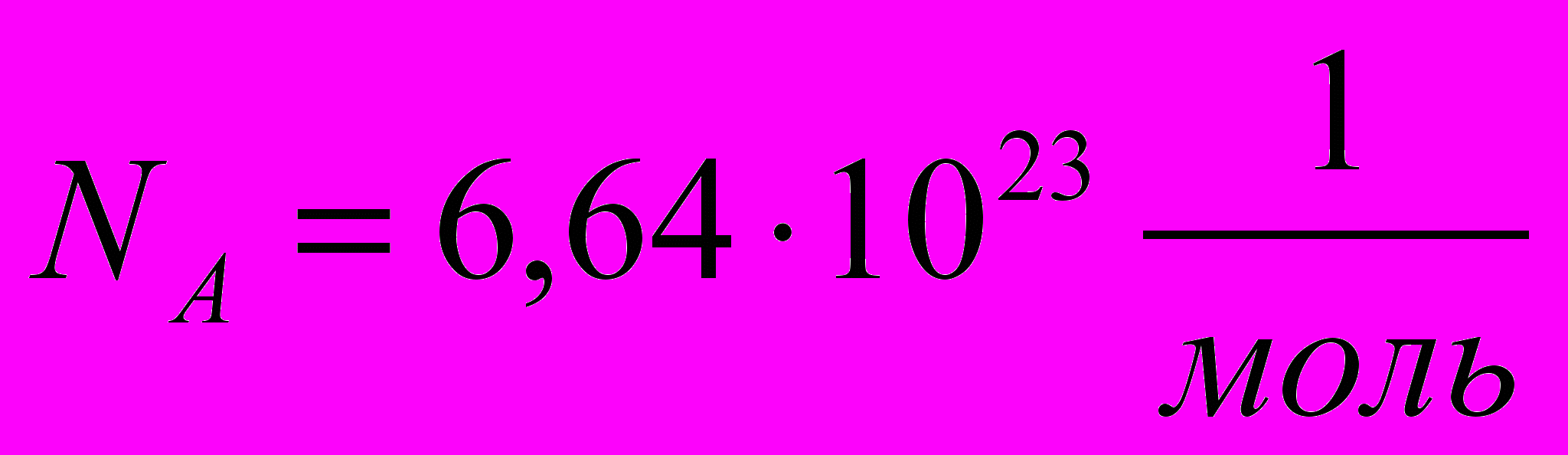 | |
| | k- постоянная Больцмана | 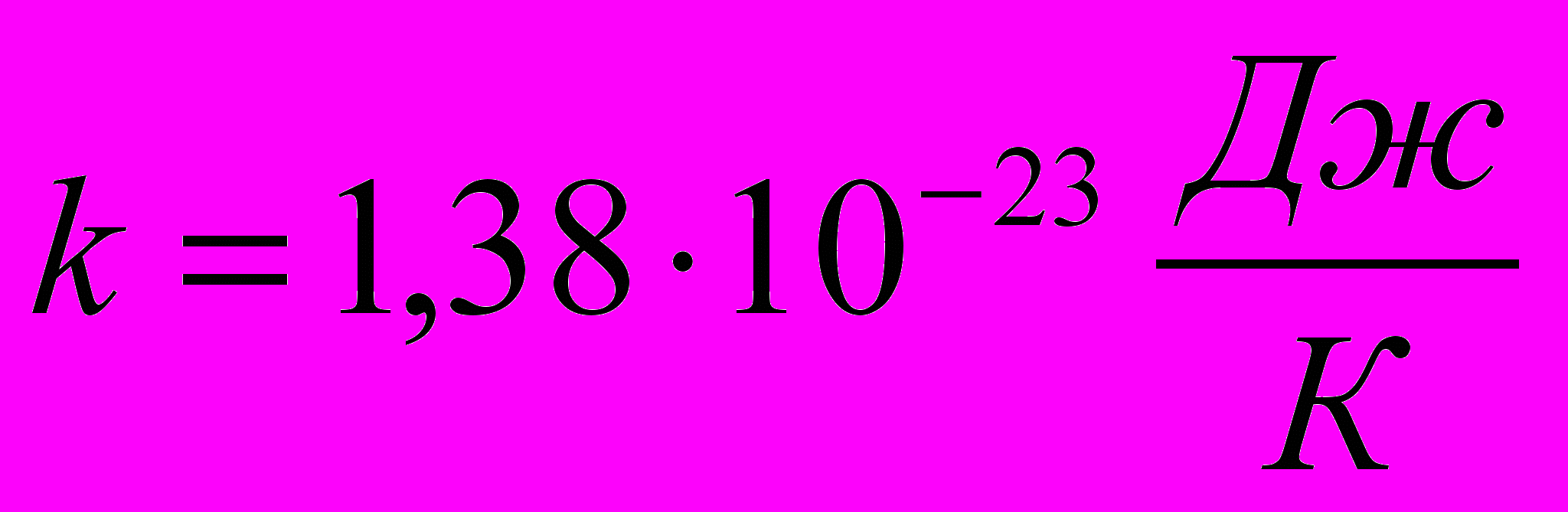 | |
| | R- универсальная газовая постоянная | 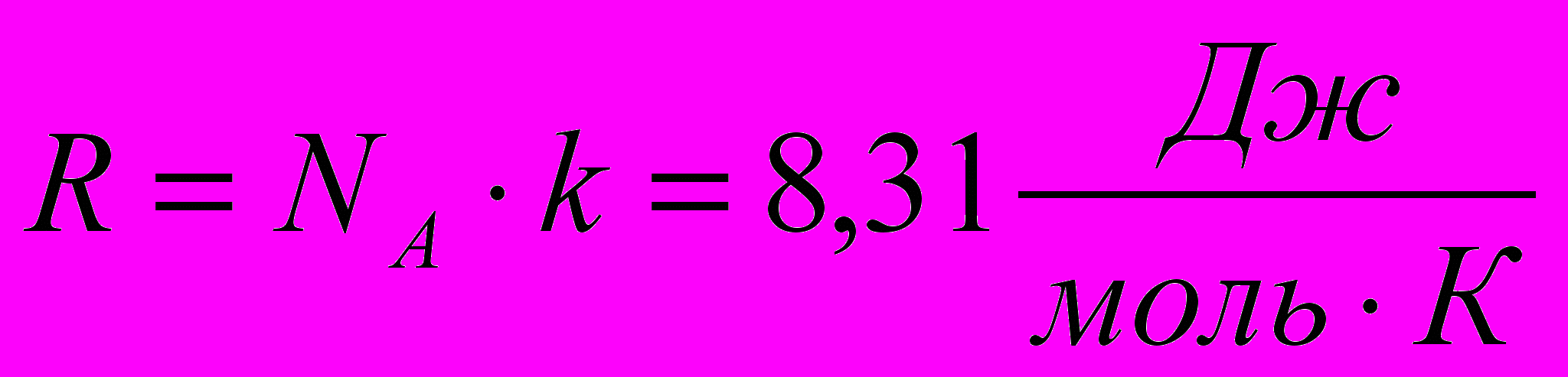 | |
| Пример №1. | | |
| | ||
| Дано: | Система интернациональная | Решение. |
| | | |
| | | Ответ: |
| Пример №2. | | |
| | ||
| Дано: | Система интернациональная | Решение. |
| | | |
| | | Ответ: |
| Лекция № 3. | Дата: |
| Раздел: «Молекулярная физика. Термодинамика». | |
| Тема: «Изопроцессы». | |
| Преподаватель: Сычева Е.В. | |
| Изопроцессы- процессы, которые происходят при постоянстве одного из макропараметров с данной массой газа. | Изобарный- - процесс, происходящий при постоянном давлении. | Изохорный - процесс, происходящий при постоянном объеме. | Изотермический- процесс, происходящий при постоянной температуре. | Адиабатный процесс- процесс, идущий без теплообмена с внешней средой. | |
| Определение закона | Закон Гей- Люссака: для газа данной массы при неизменном давлении отношениедавления газа к его температуре есть величина постоянная. | Закон Шарля: для газа данной массы при неизменном объеме отношение давления газа к его температуре есть величина постоянная. | Закон Бойля- Мариотта: для газа данной массы при неизменной температуре произведение давления газа на его объем есть величина постоянная. | | |
| Условия протекания | 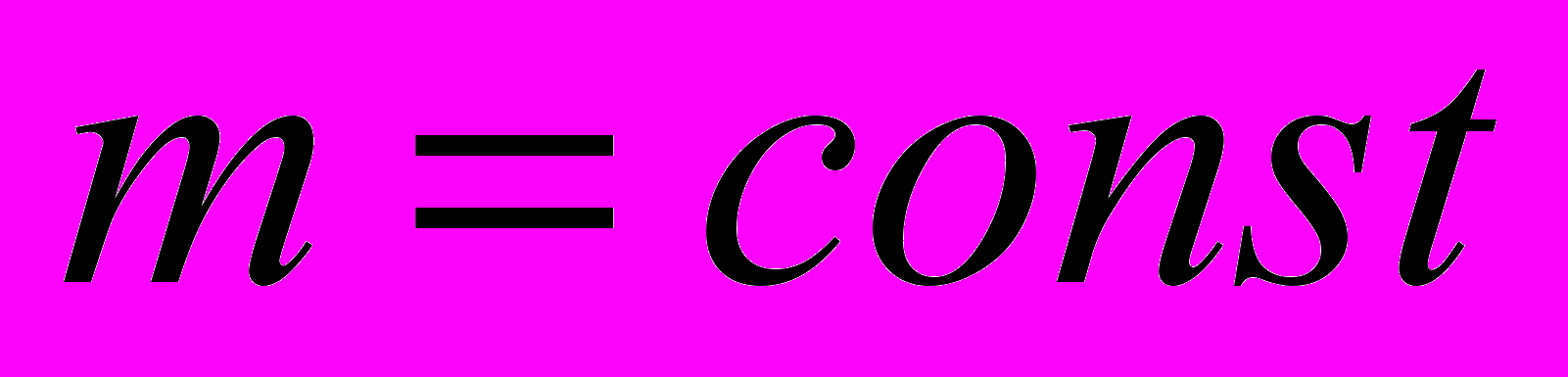 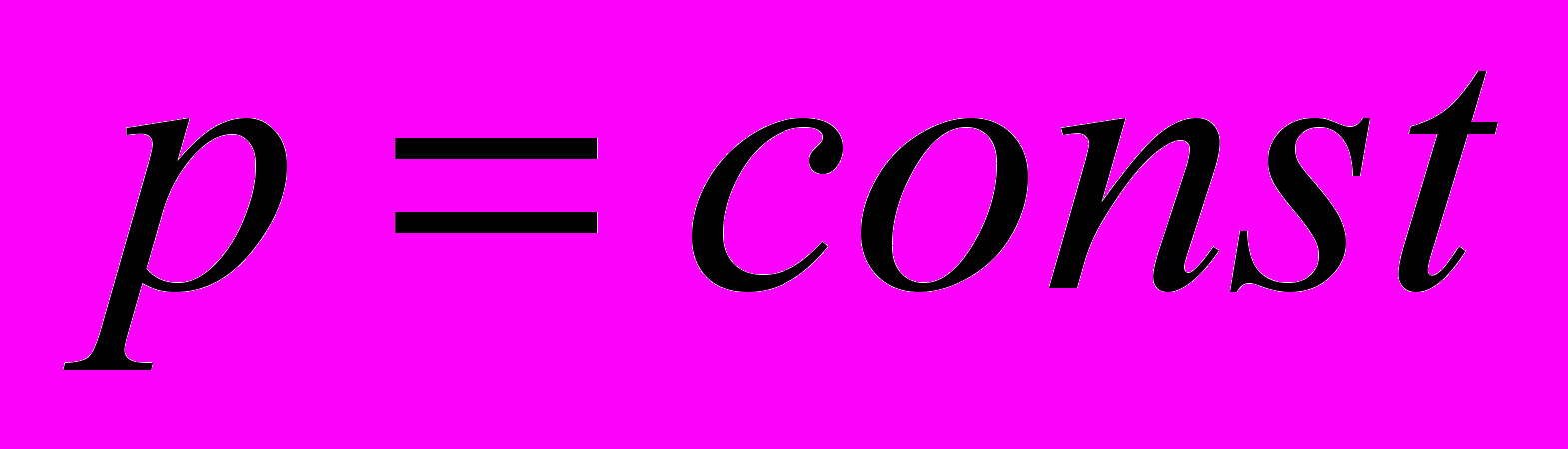 | 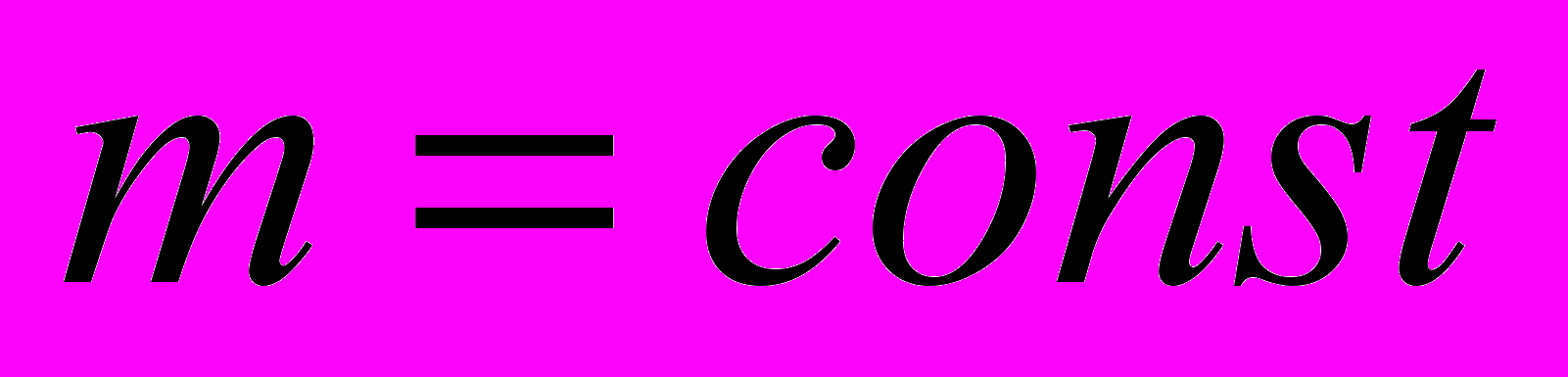 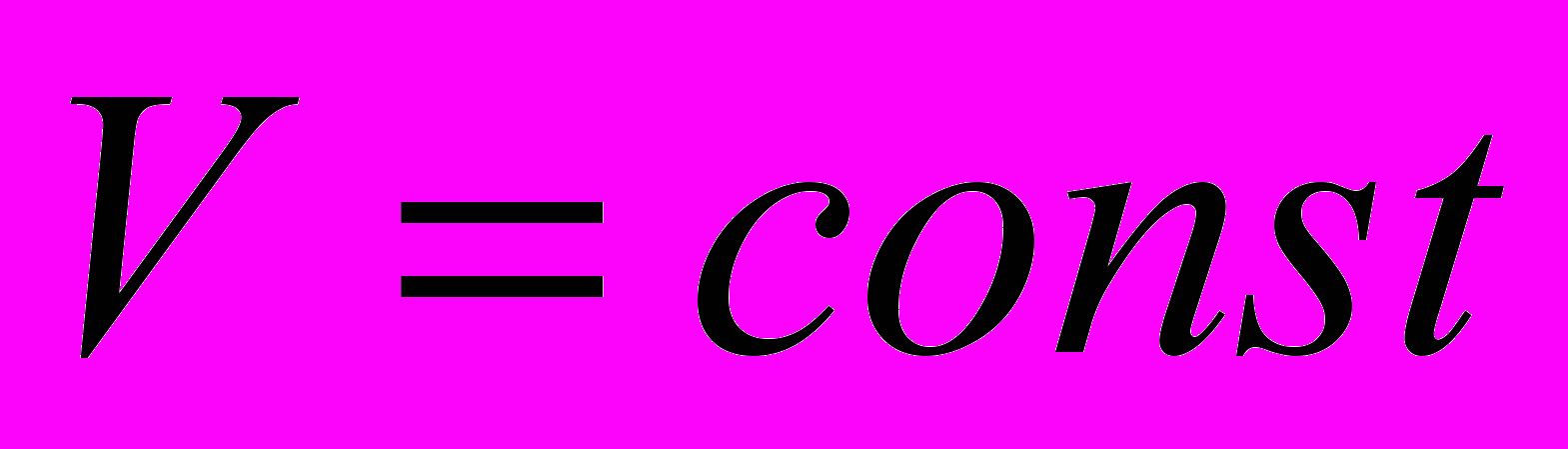 | 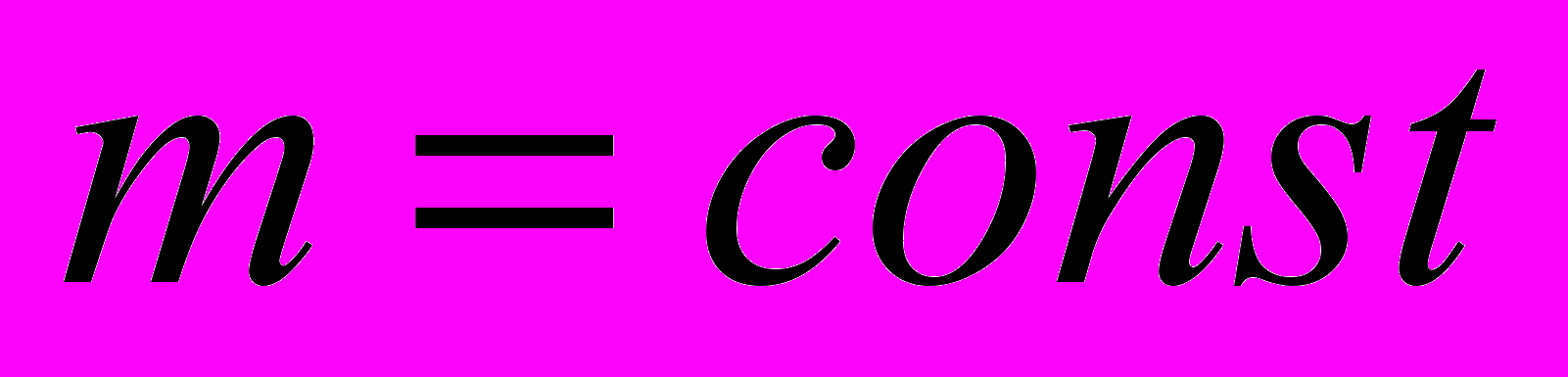 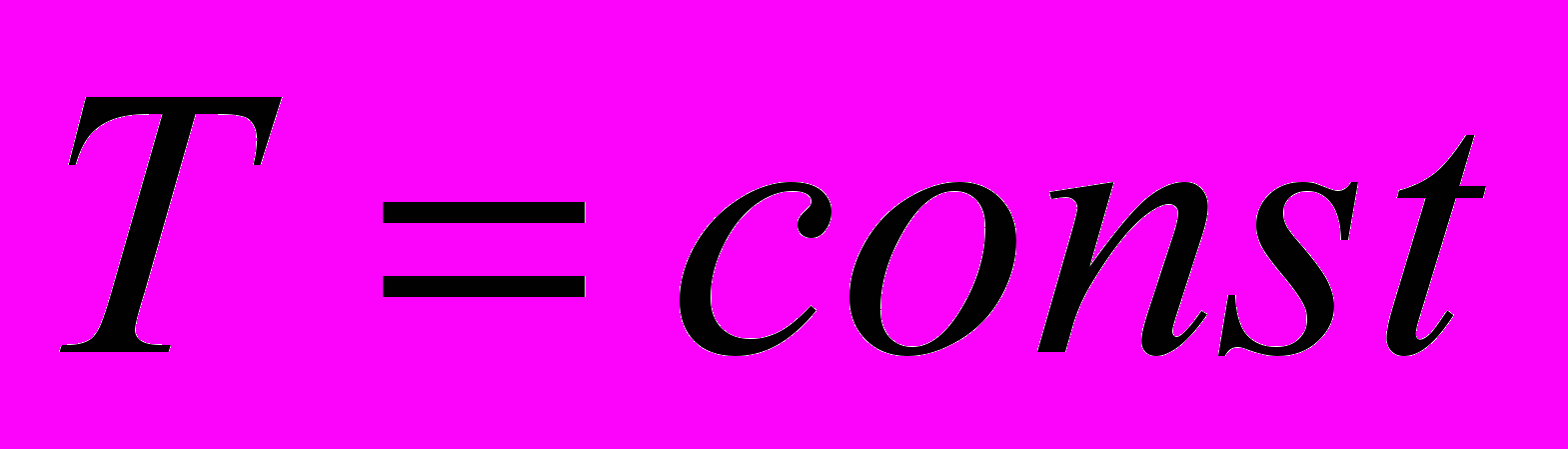 | | |
| Уравнение процесса | 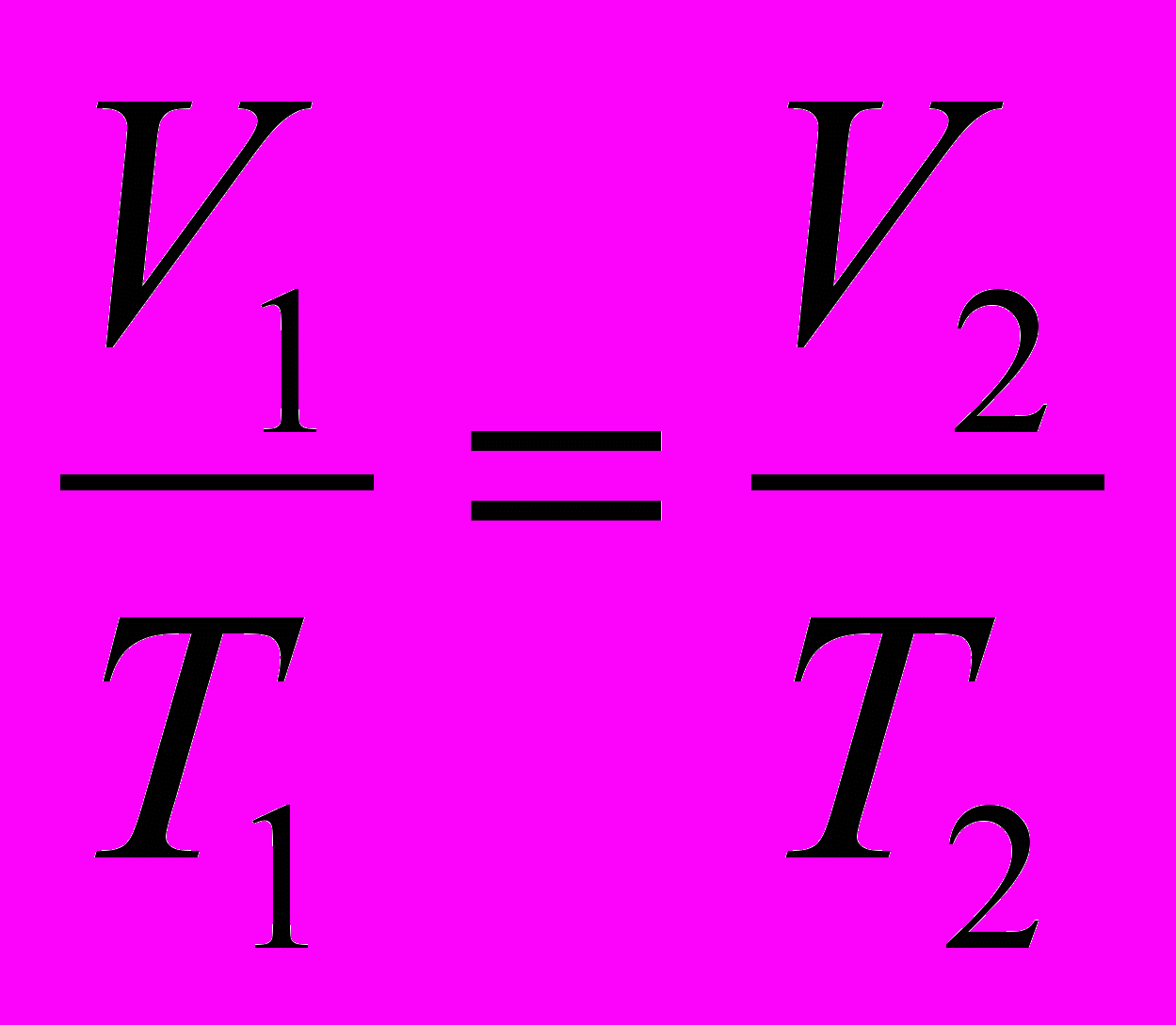 | 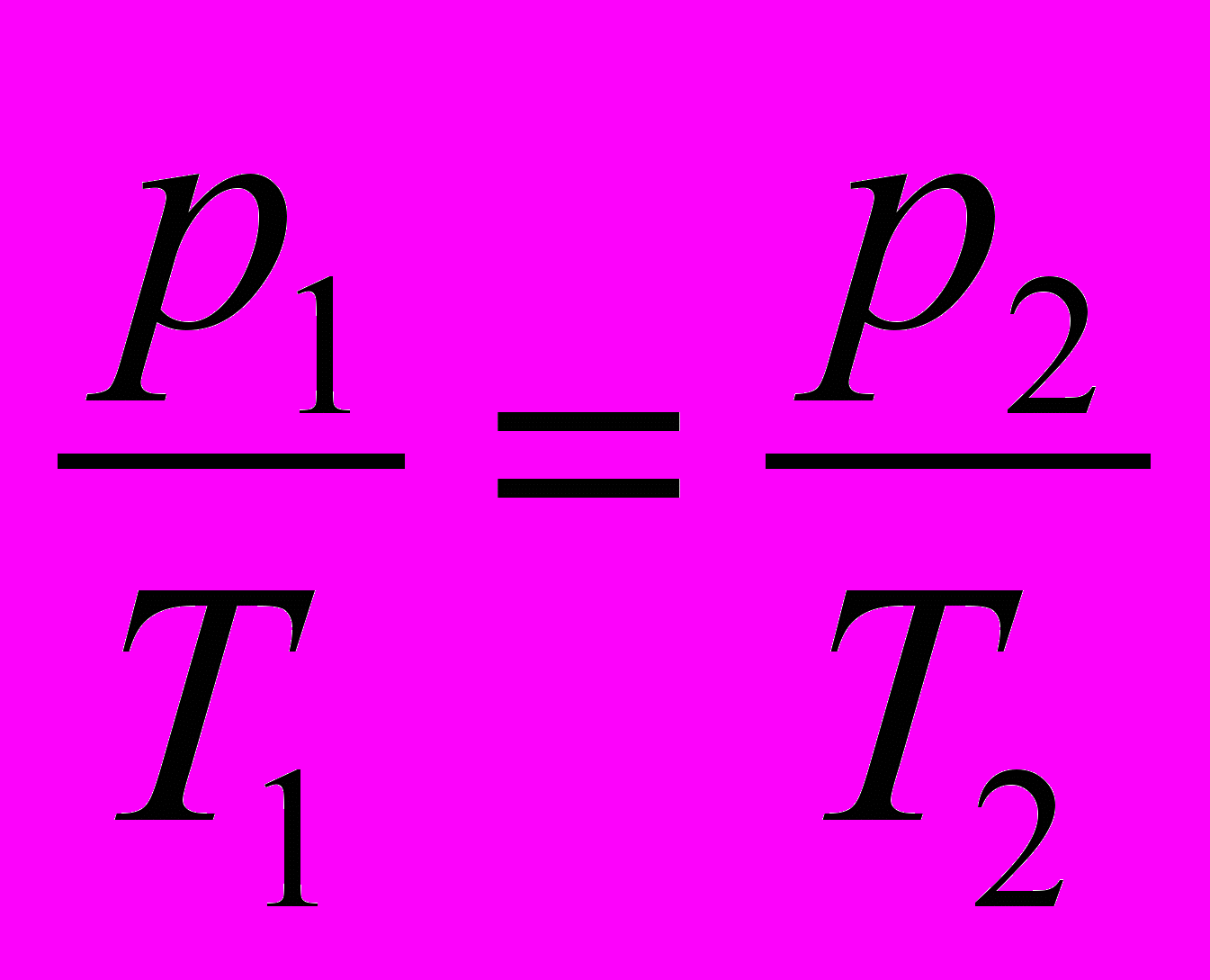 | 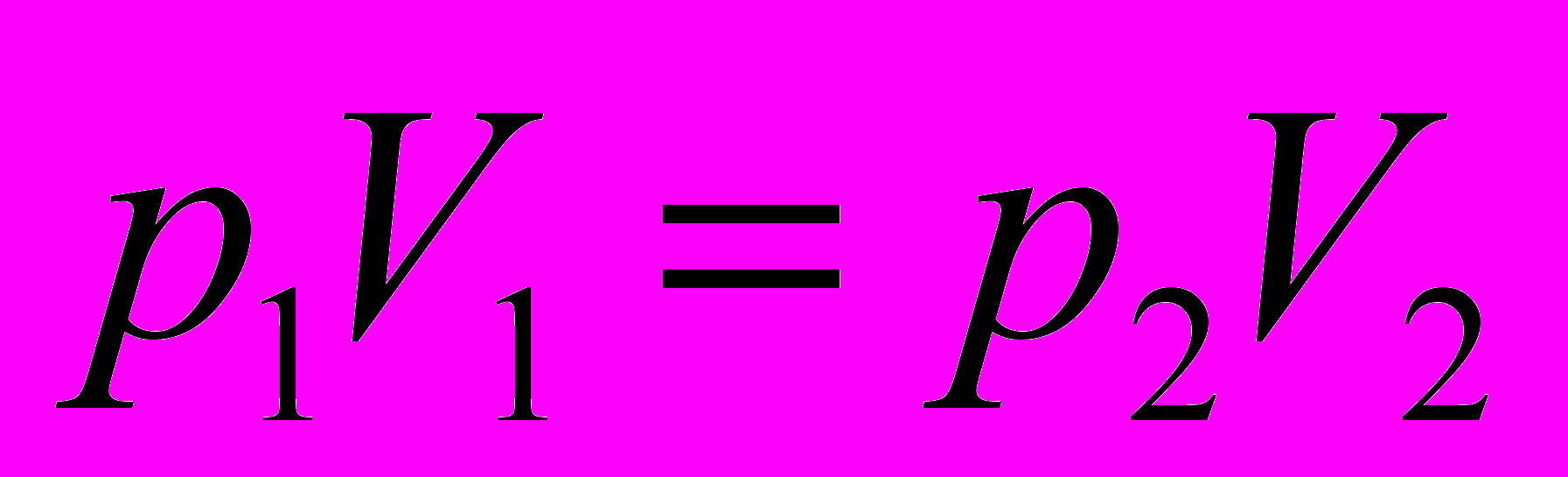 | | |
| Графики |  p  V  |   p V  | p V    |   p V  | |
| Г V рафики |  V  T  |   T T V  | 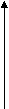 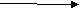 T  | 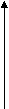 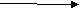 | |
| Г p рафики V | 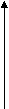 T p  T 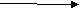 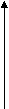 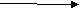  | 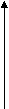 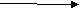 p  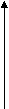 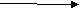 p |        |   | |
| | T    P3 P1 |  T p   V3 V1  | V  T3 T1  | | |
| | Давление растет | Объем растет | Температура растет | | |
| Лекция № 4. | Дата: | ||||
| Раздел: «Молекулярная физика. Термодинамика». | | ||||
| Тема: «Первый закон термодинамики в изопроцессах. Тепловой двигатель. КПД». | | ||||
| Преподаватель: Сычева Е.В. | | ||||
| Изопроцессы | Изобарный | Изохорный | Изотермический | Адиабатный процесс |
| Уравнение процесса | 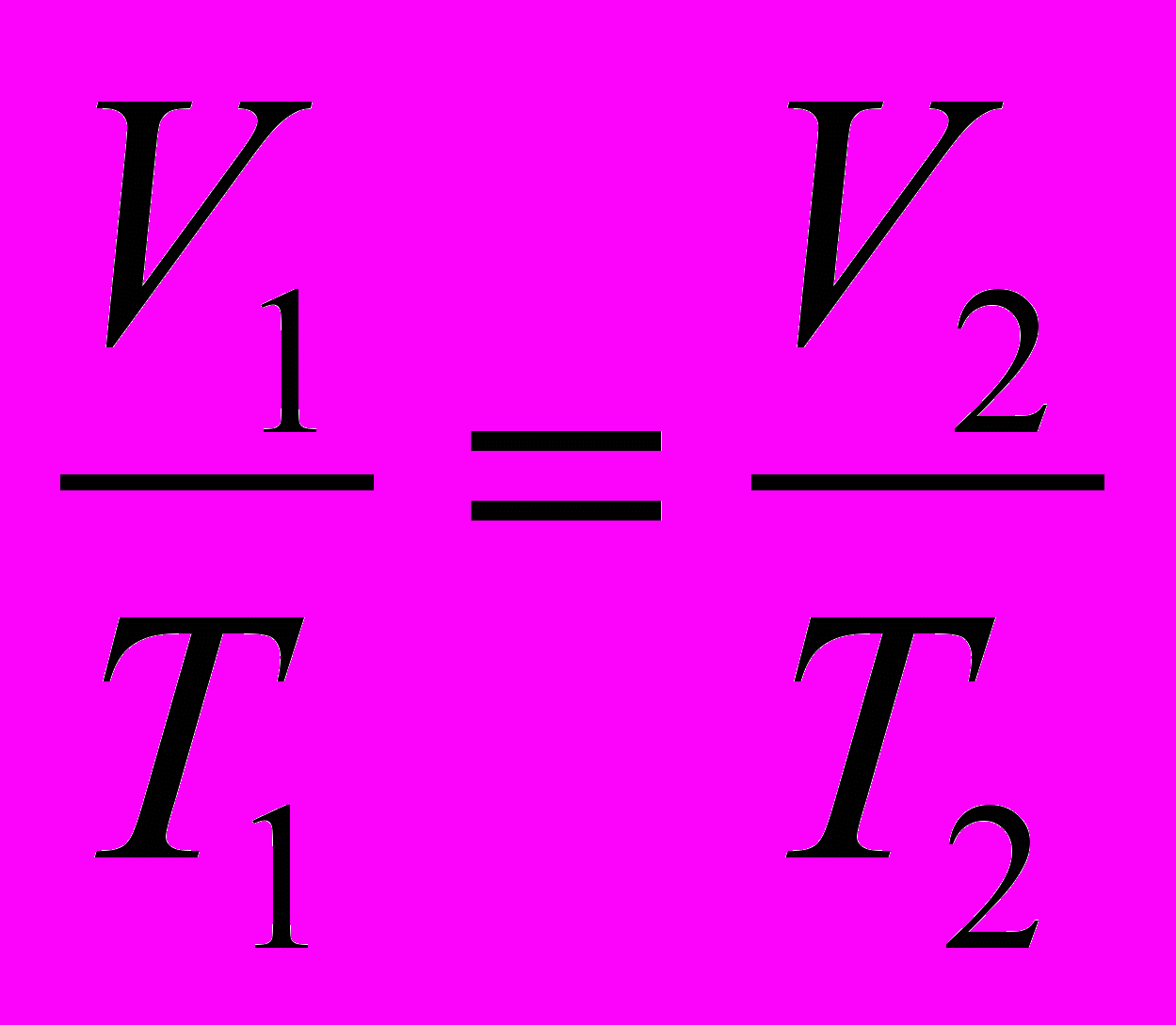 | 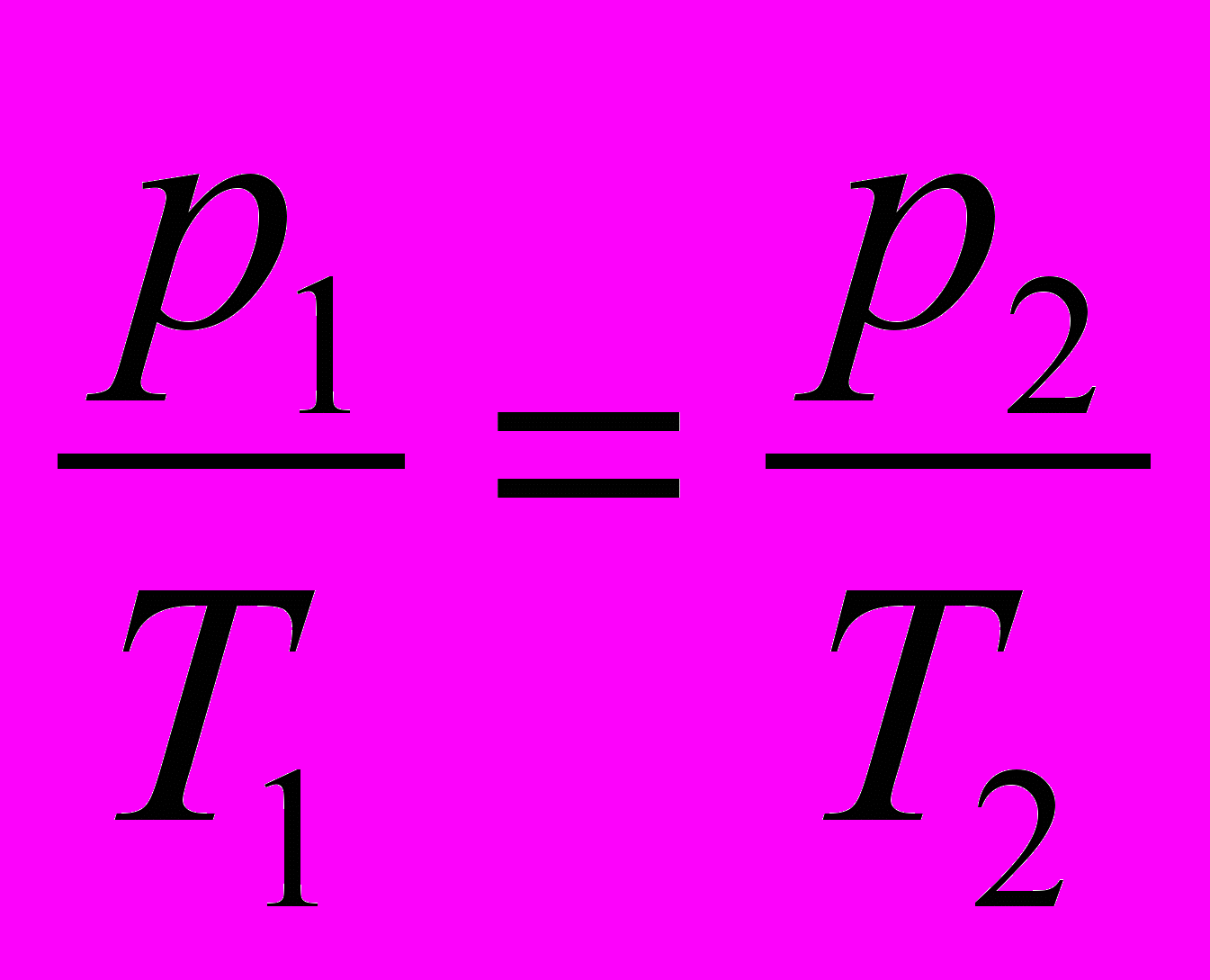 p | 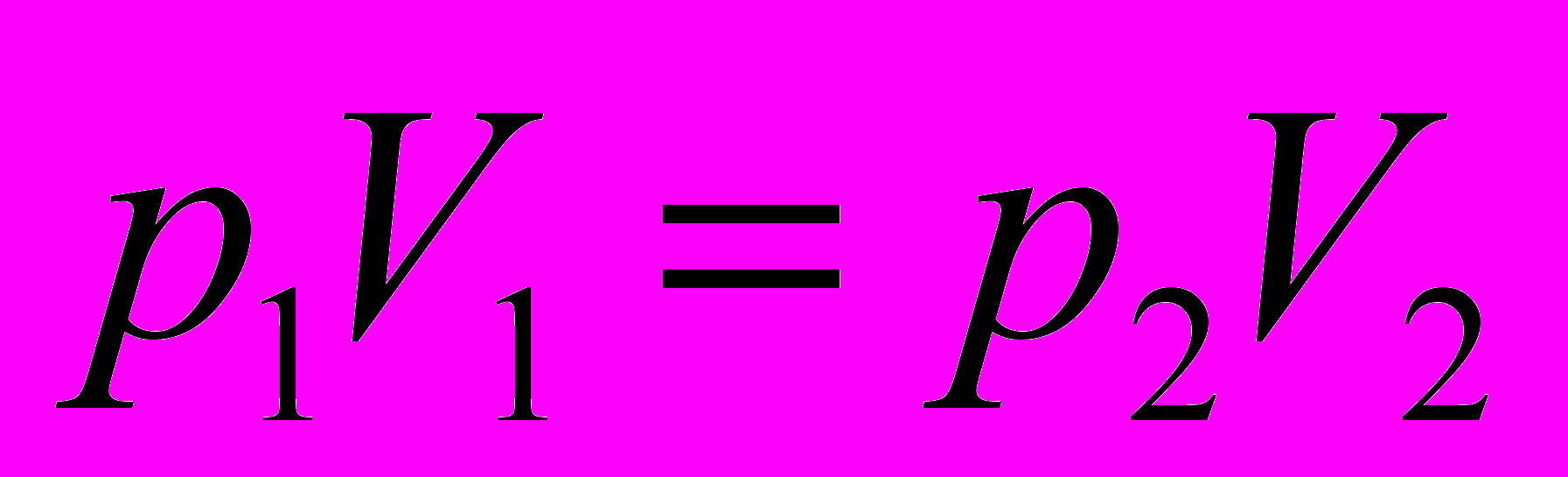 | |
| График |  V  T  |    T p | 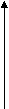 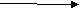 V p  | 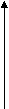 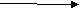  V |
| Первый закон термодинамики | 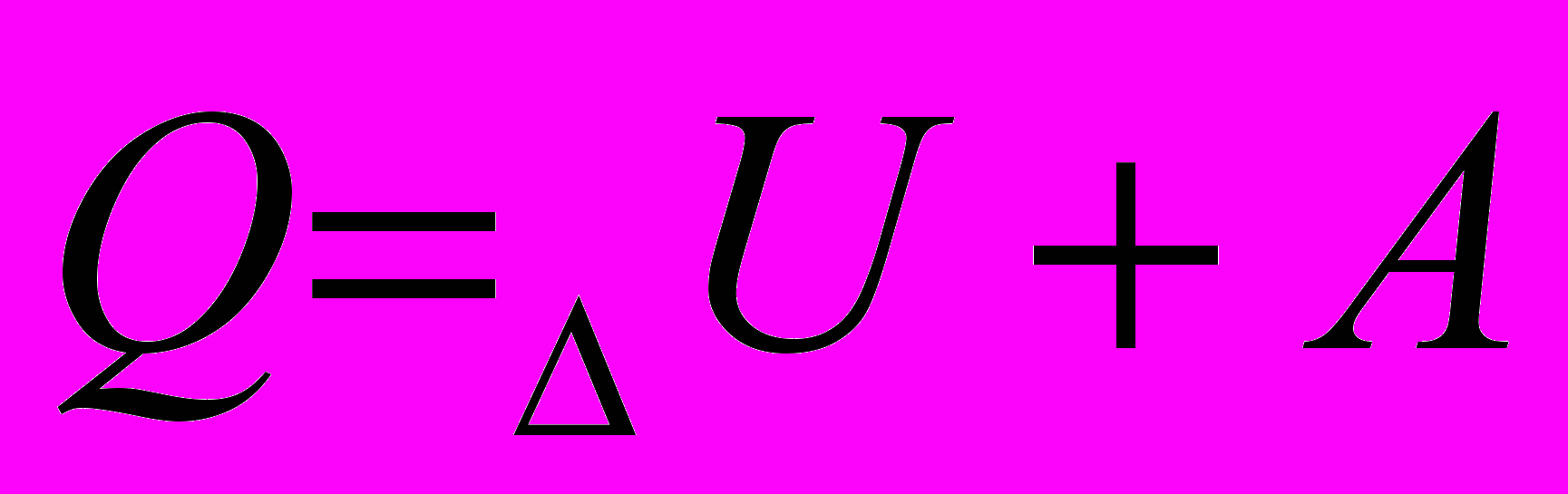 | 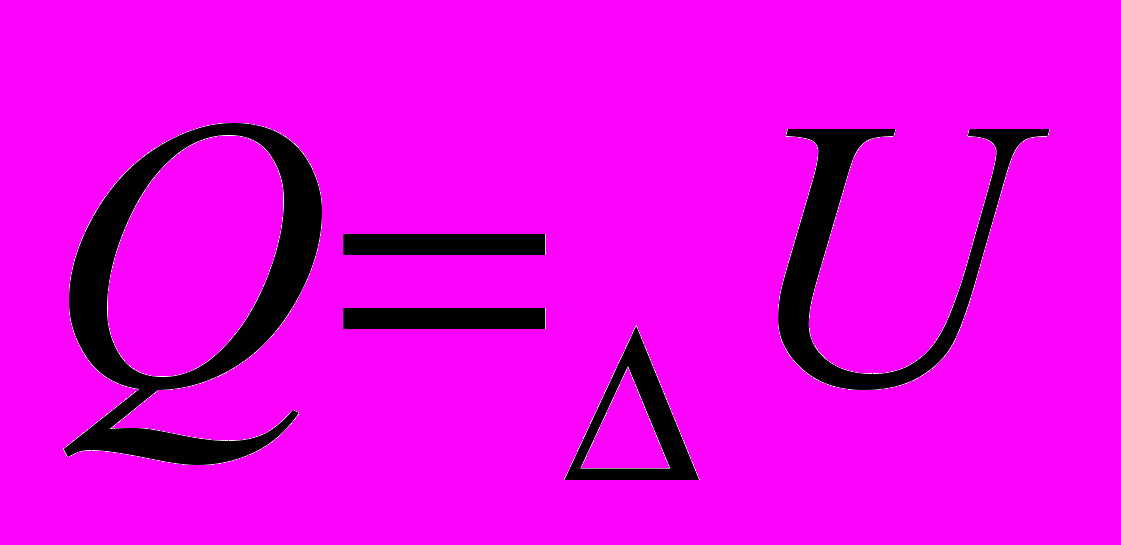 | 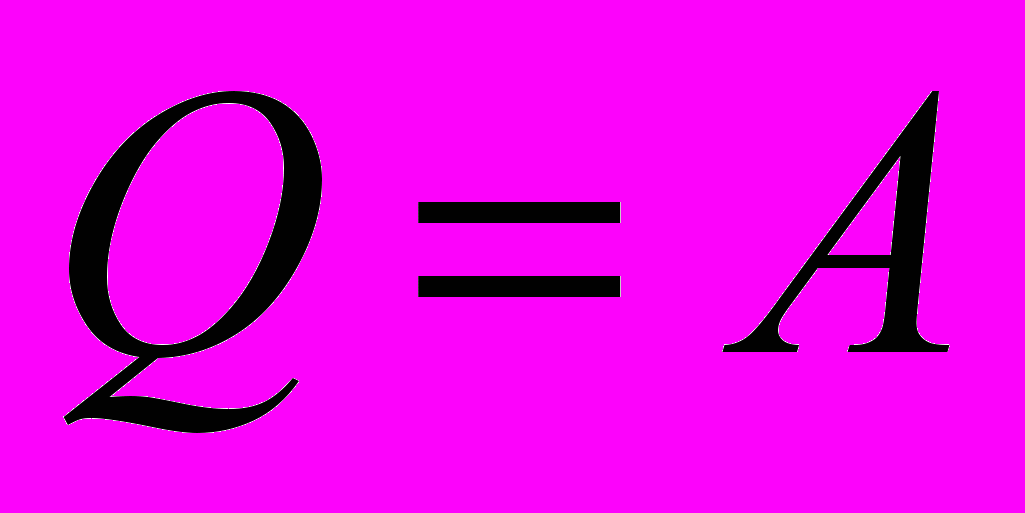 | 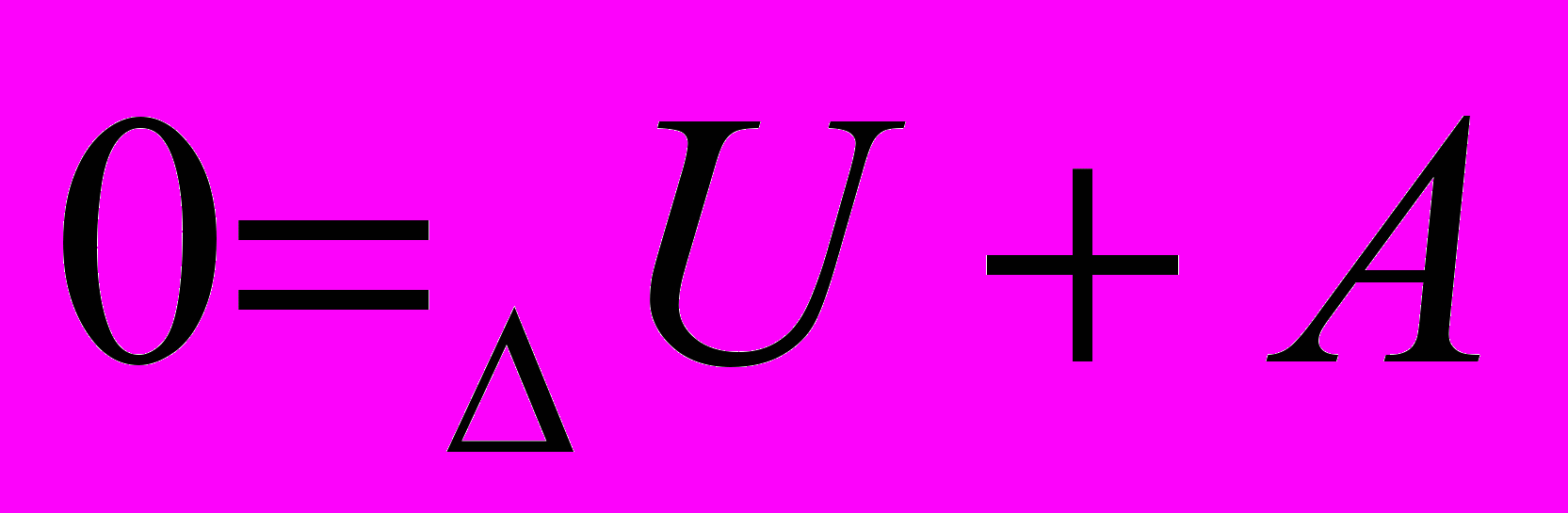 |
| Работа газа | 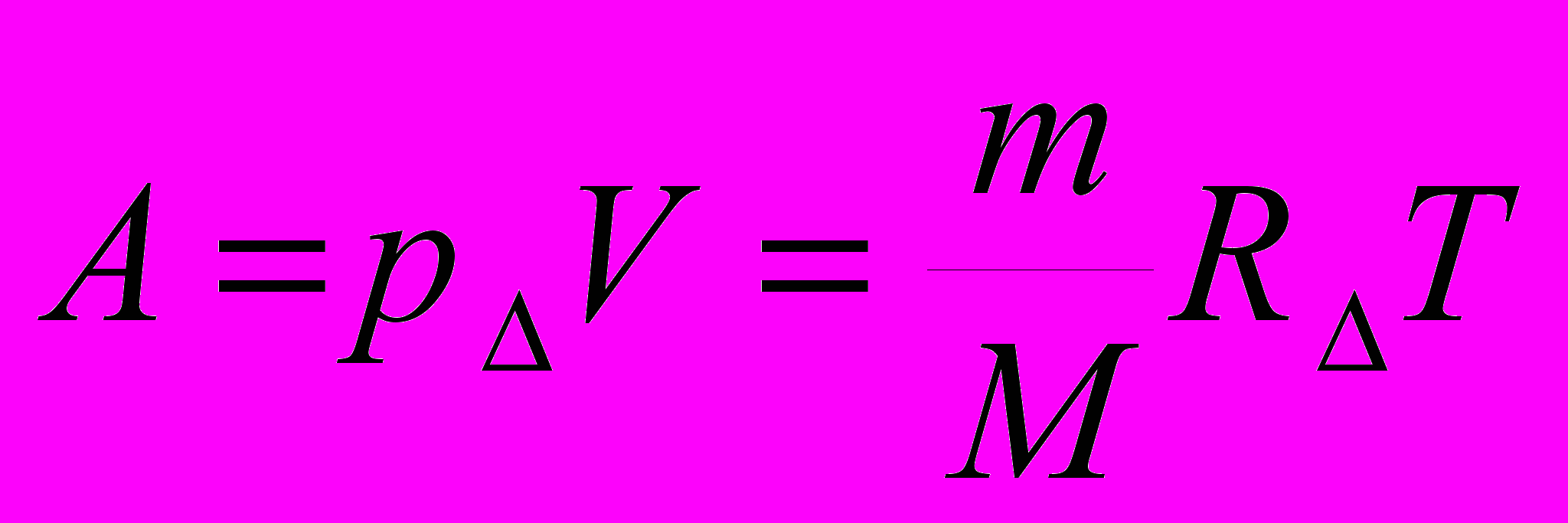 | 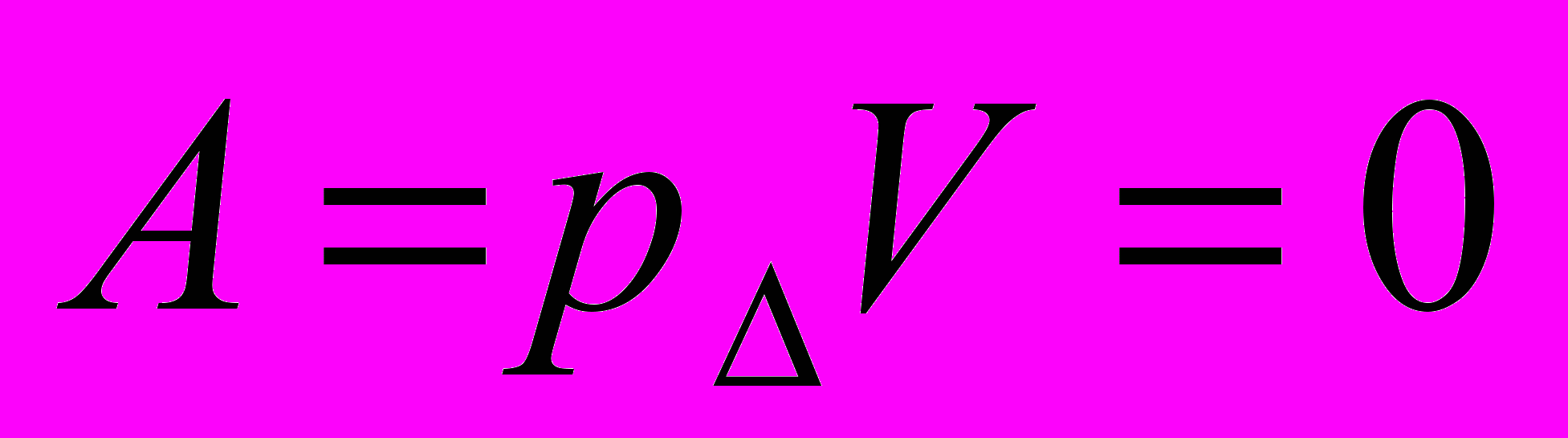 | 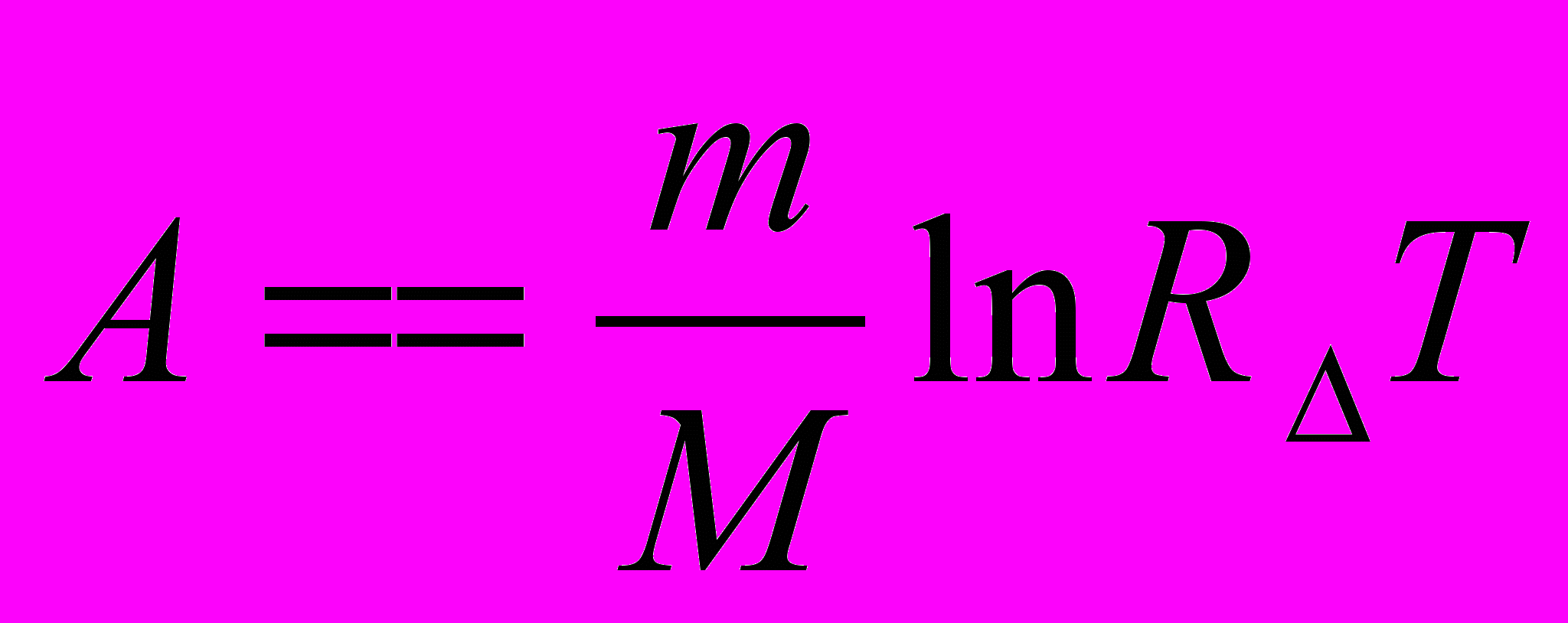 | 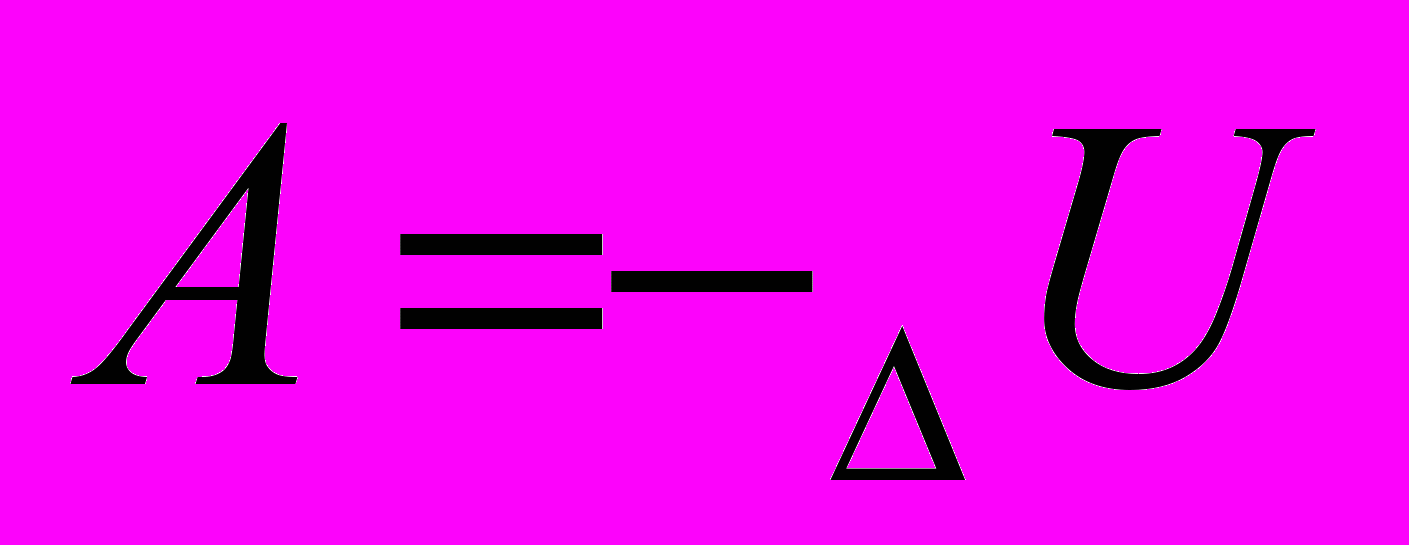 |
| Изменение внутренней энергии | 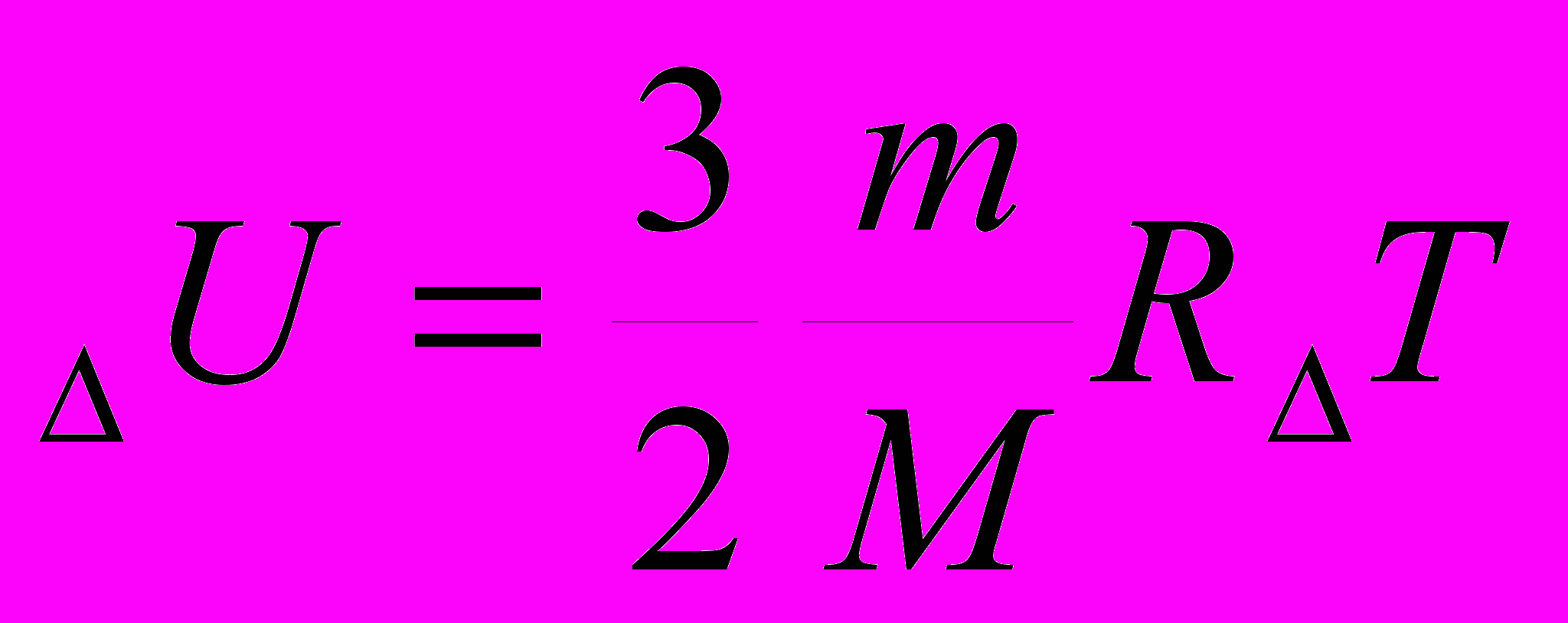 | 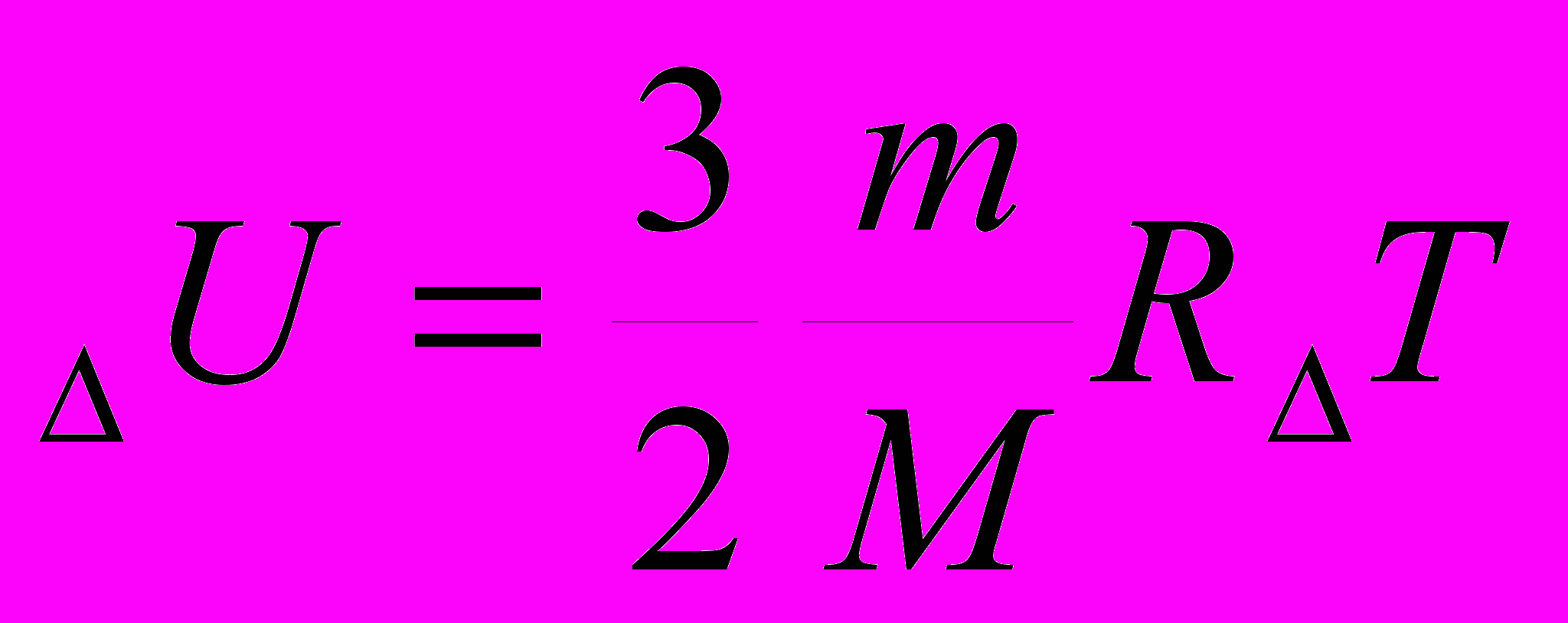 | 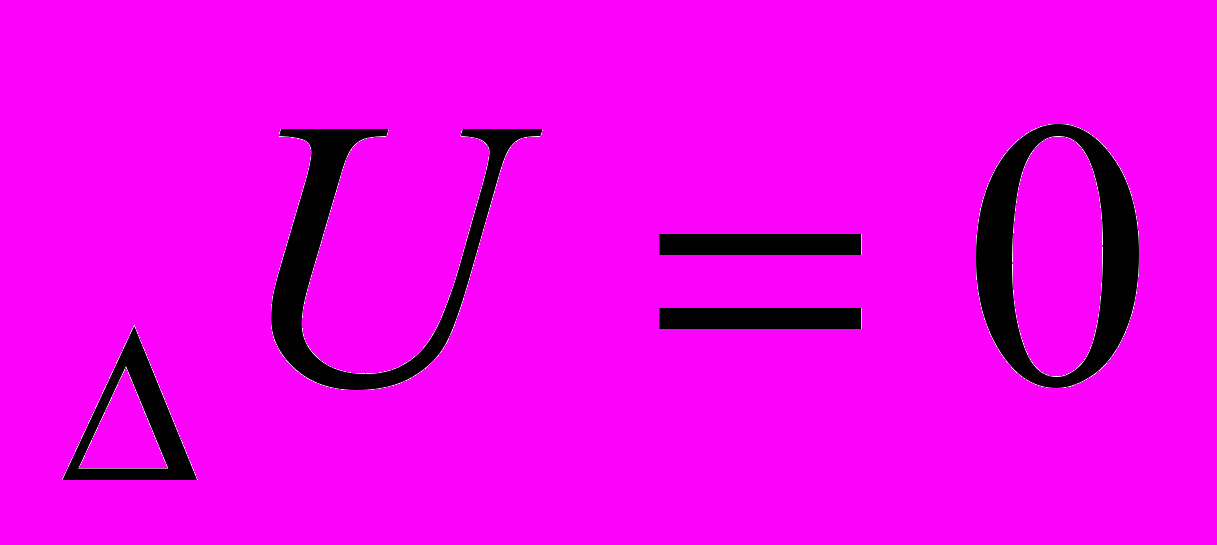 | 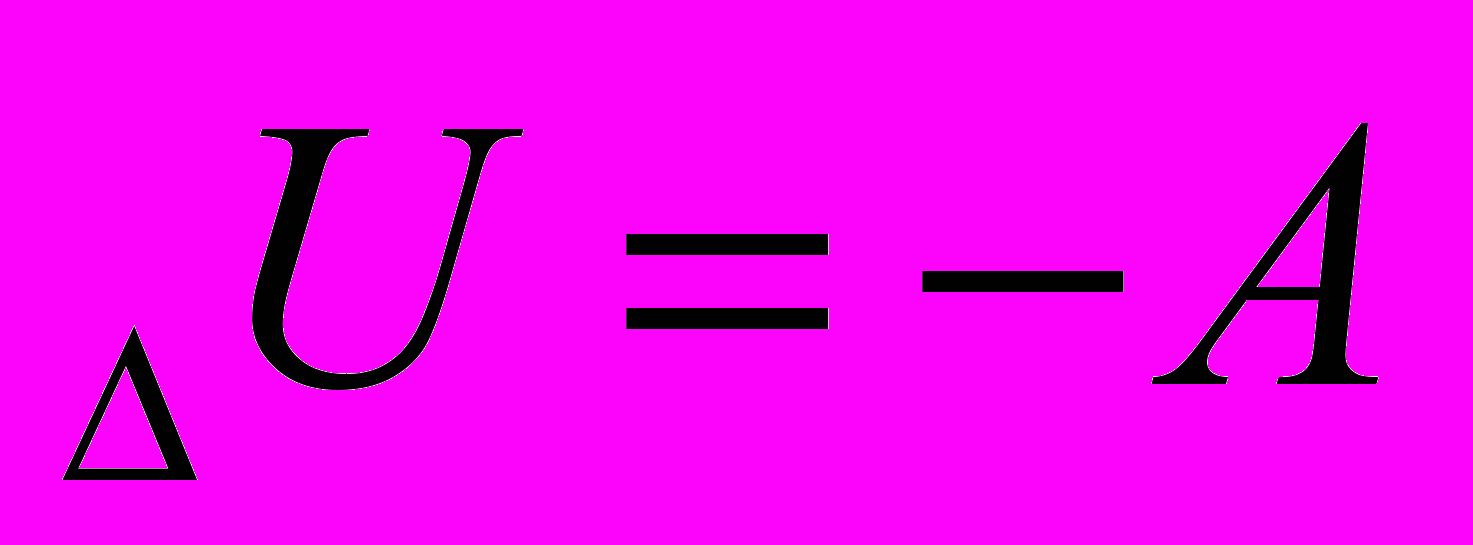 |
| Тепловой двигатель | | Цикл Карно |
 нагреватель  | Энергия, выделившаяся при сгорании топлива в нагревателе, передается рабочему телу- газу. Расширяясь, газ совершает механическую работу. Чтобы выполнялся цикл, газ нужно сжать после расширения. Для уменьшения работы над газом при его сжатии используют холодильник (окружающая среда). |  1   2   4 3  |
  рабочее тело   | | |
 холодильник | 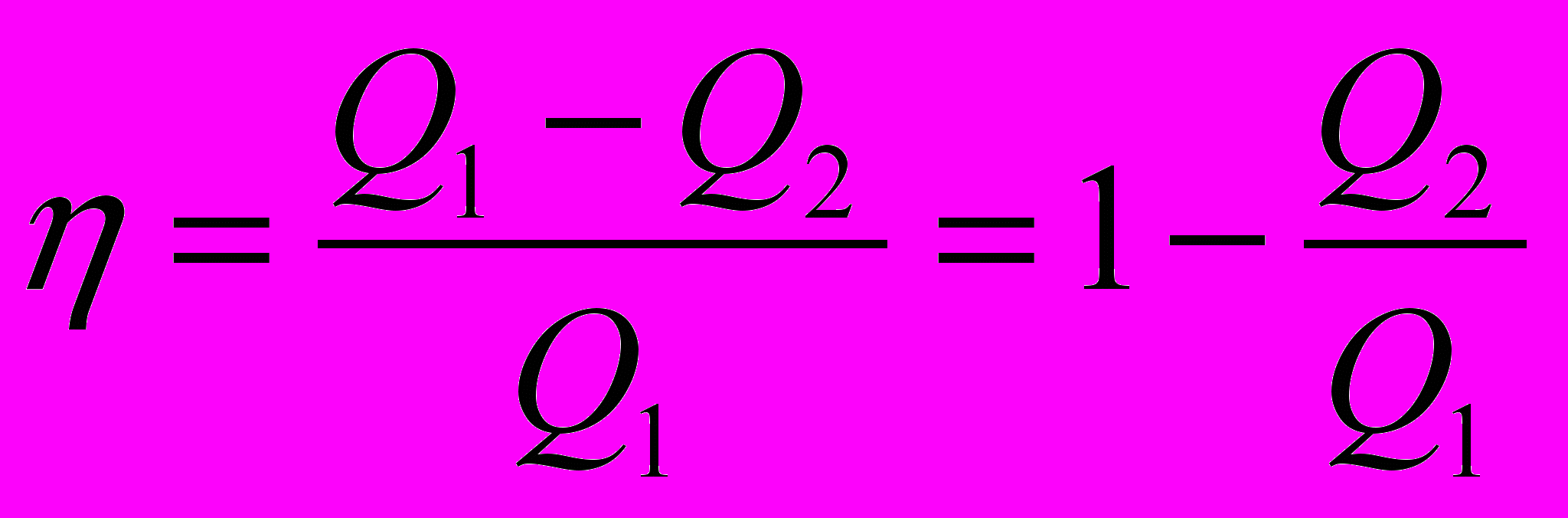 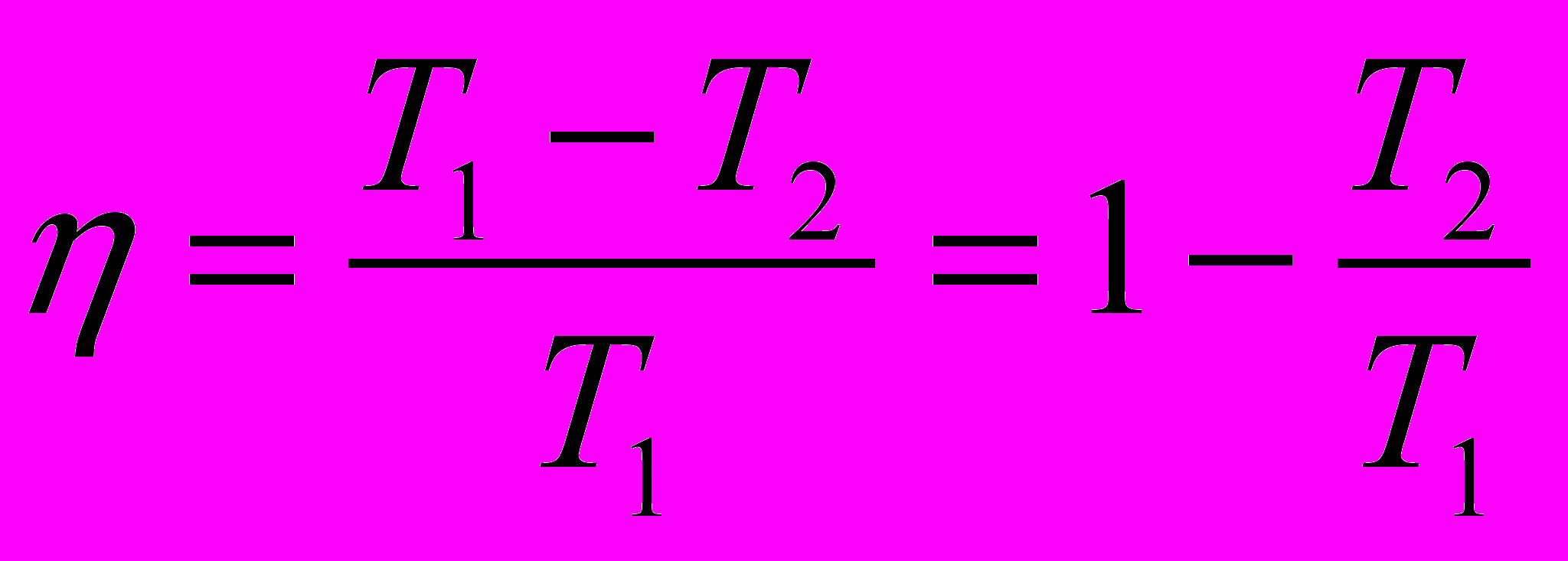 | Из всех циклических тепловых машин, имеющих одинаковые T1 ,T 2, наибольшим КПД обладают идеальные машины, цикл которых состоит из двух адиабат и двух изотерм (цикл Карно). |
| Лекция № 5. | Дата: |
| Раздел: «Молекулярная физика. Термодинамика». | |
| Тема: «Агрегатные состояния вещества. Фазовые переходы. Пар». | |
| Преподаватель: Сычева Е.В. | |
| | | Агрегатные состояния вещества | | | ||
| | плавление- процесс перехода вещества из твердого состояния в жидкое при неизменной температуре. | | | | кипение- процесс перехода вещества из жидкого состояния в газообразное при неизменной температуре. | |
| твердое |  | | жидкое |  | | газо-образное |
| | кристал-лизация -процесс перехода вещества из жидкого состояния в твердое при неизменной температуре | | | | конден-сация- процесс перехода вещества из газообразного состояния в жидкое при неизменной температуре. | |
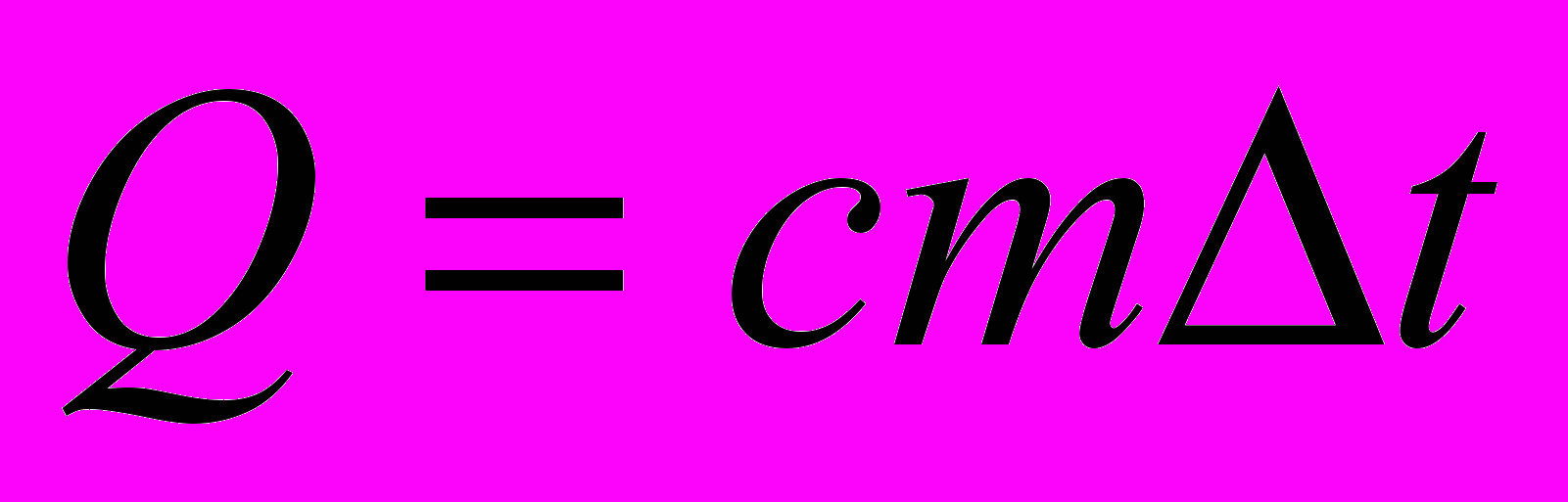 | 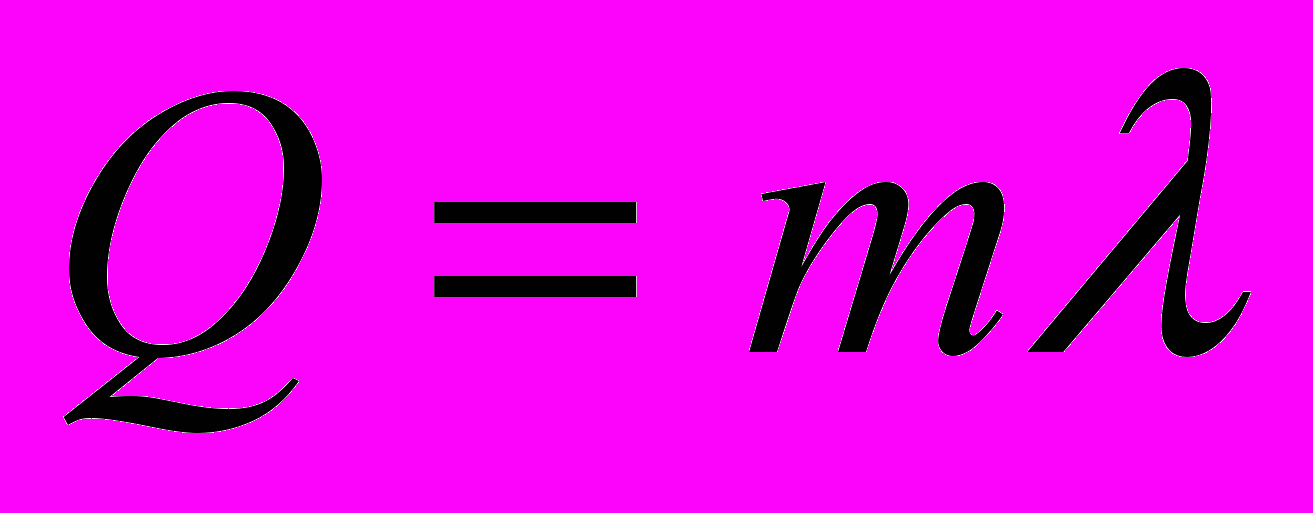 | 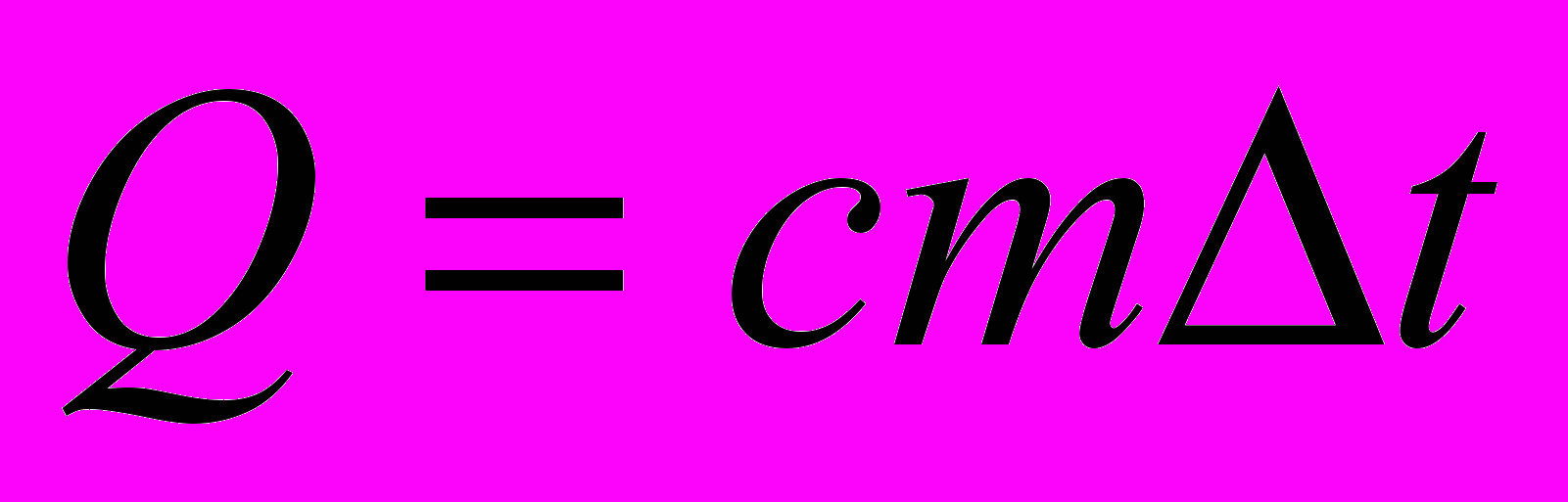 | 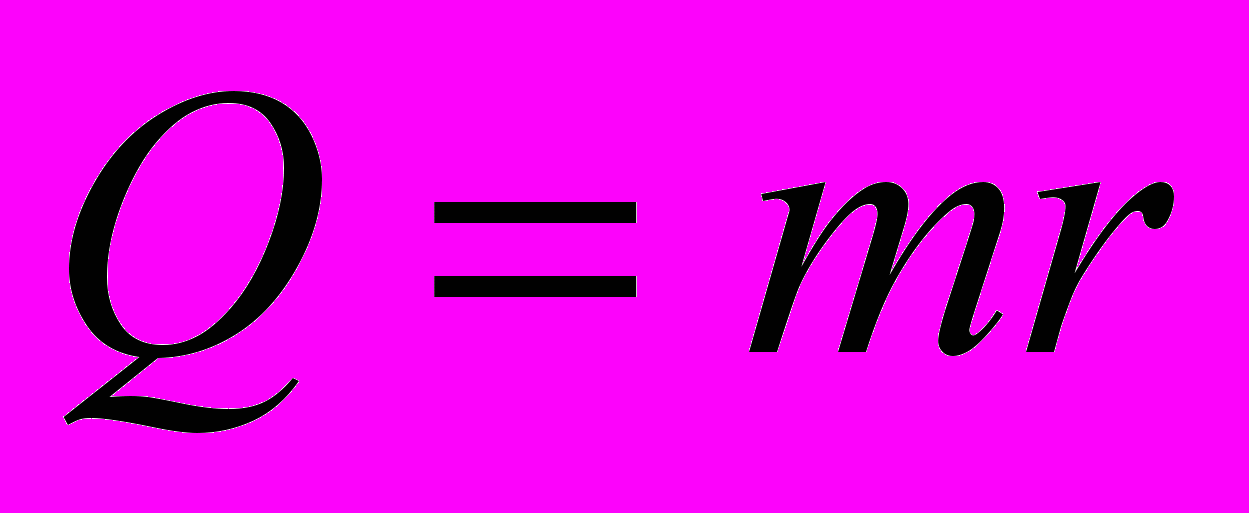 | 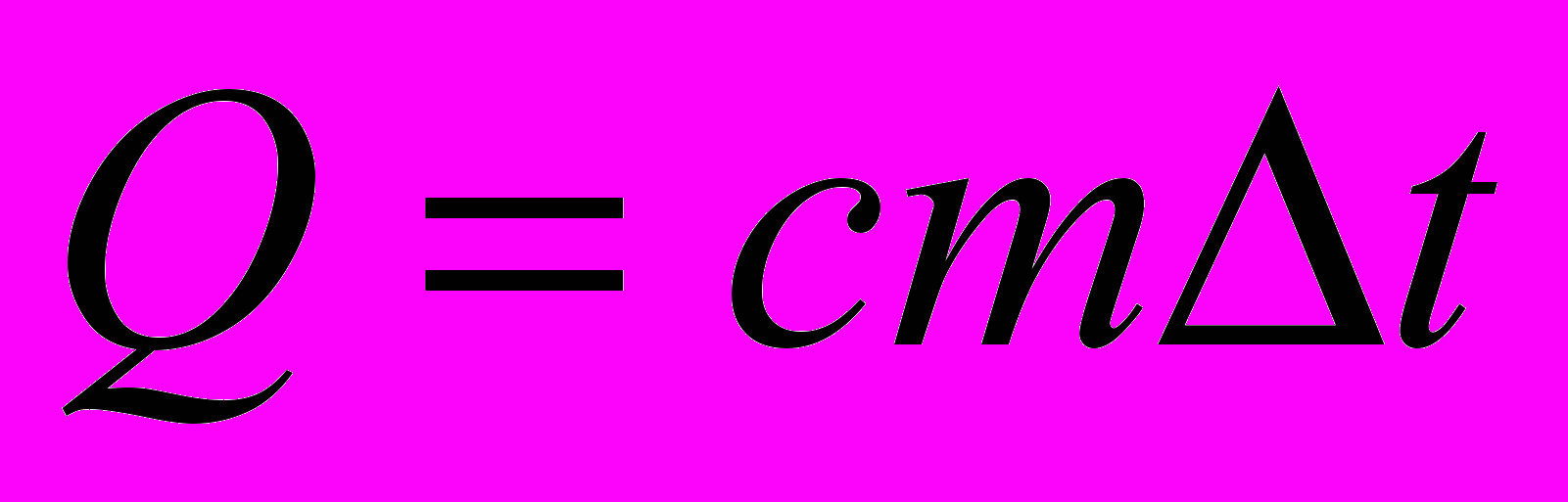 | 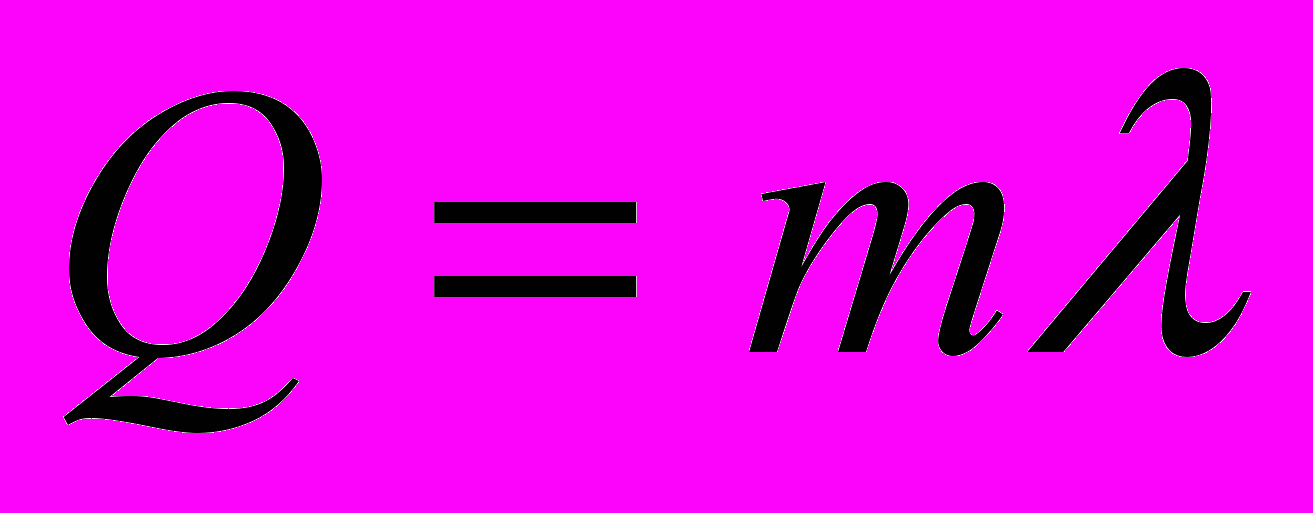 | 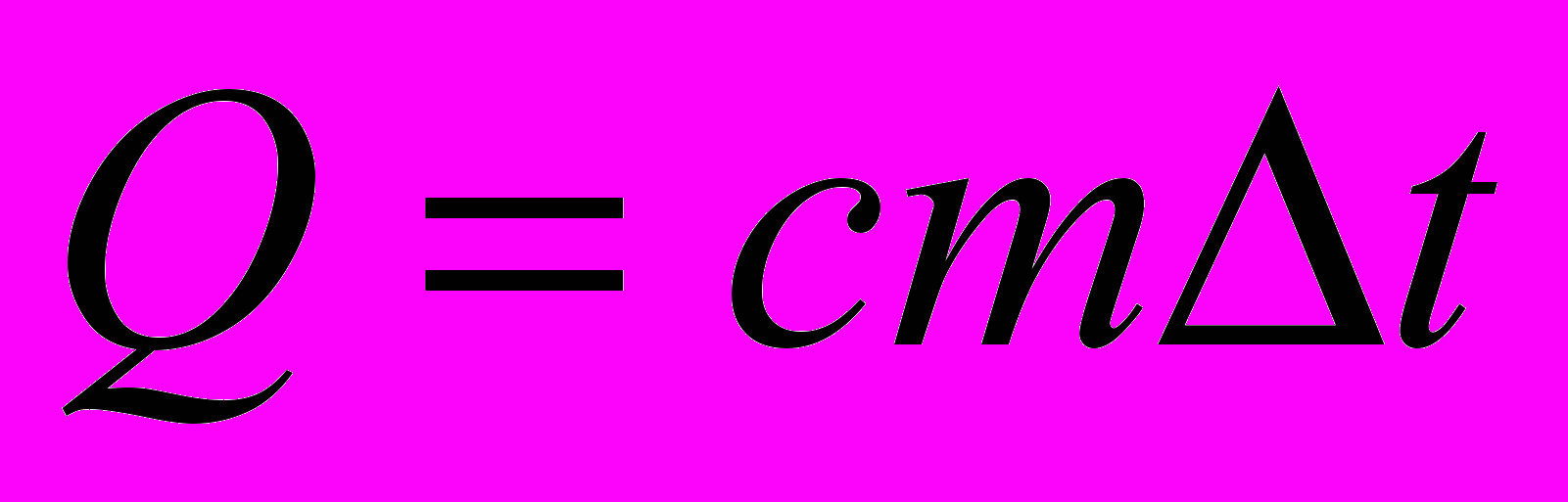 |
| энергия поглощается | энергия поглощается | энергия поглощается | энергия погл/выд | энергия выделяется | энергия выделяется | энергия выделяется |
   |  |   | |  |  |  |
| Механические свойства твердых тел. Д  еформация- изменение формы, объема тела. еформация- изменение формы, объема тела. | Поверхностное натяжение- физическая величина, численно равная силе поверхностного натяжения, действующей на единицу длины границы раздела жидкости: 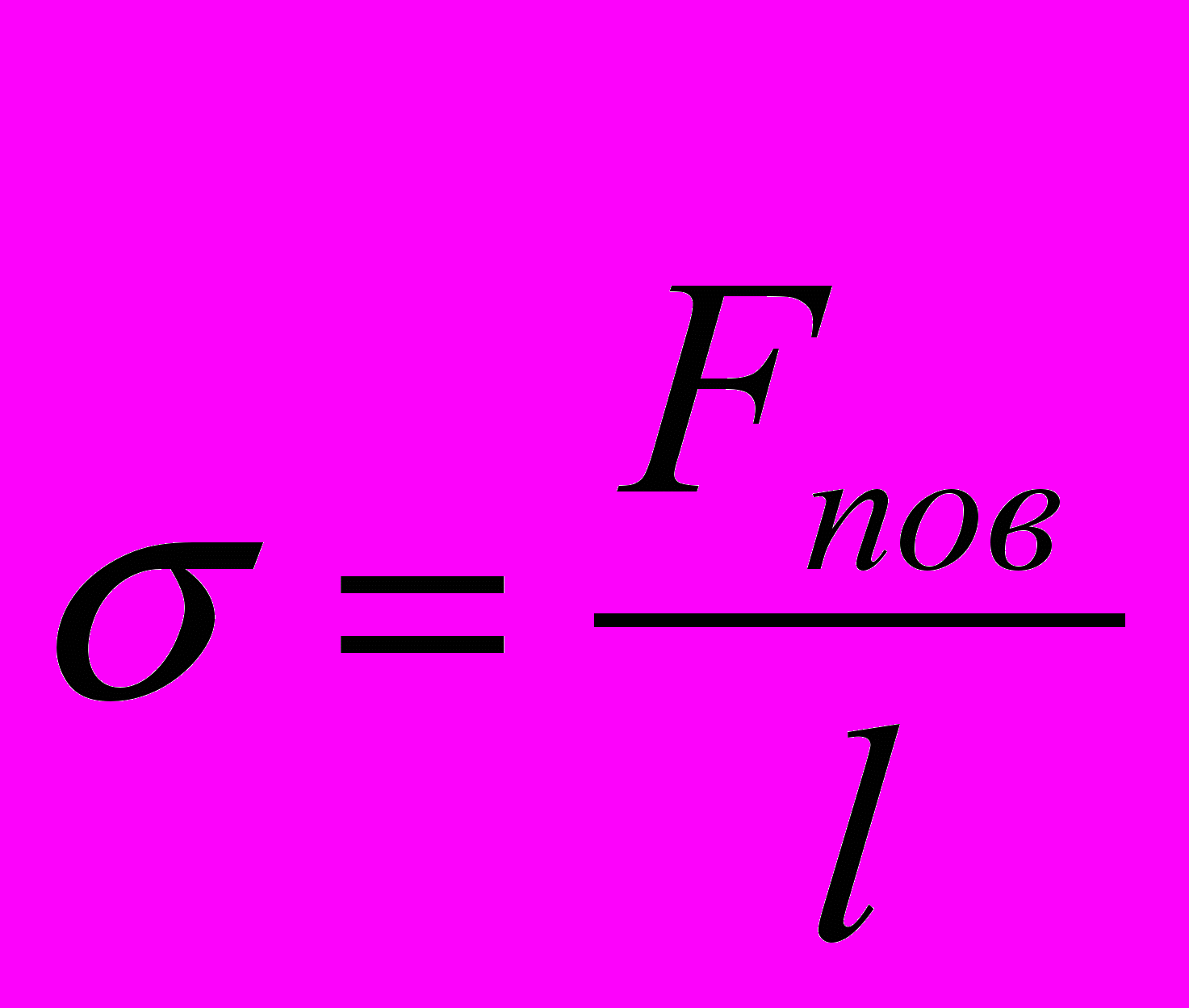 | Относительная влажность воздуха- физическая величина, которая показывает отношение давления водяного пара, содержащегося в воздухе при комнатной температуре, к давлению насыщенного водяного пара при той же температуре: 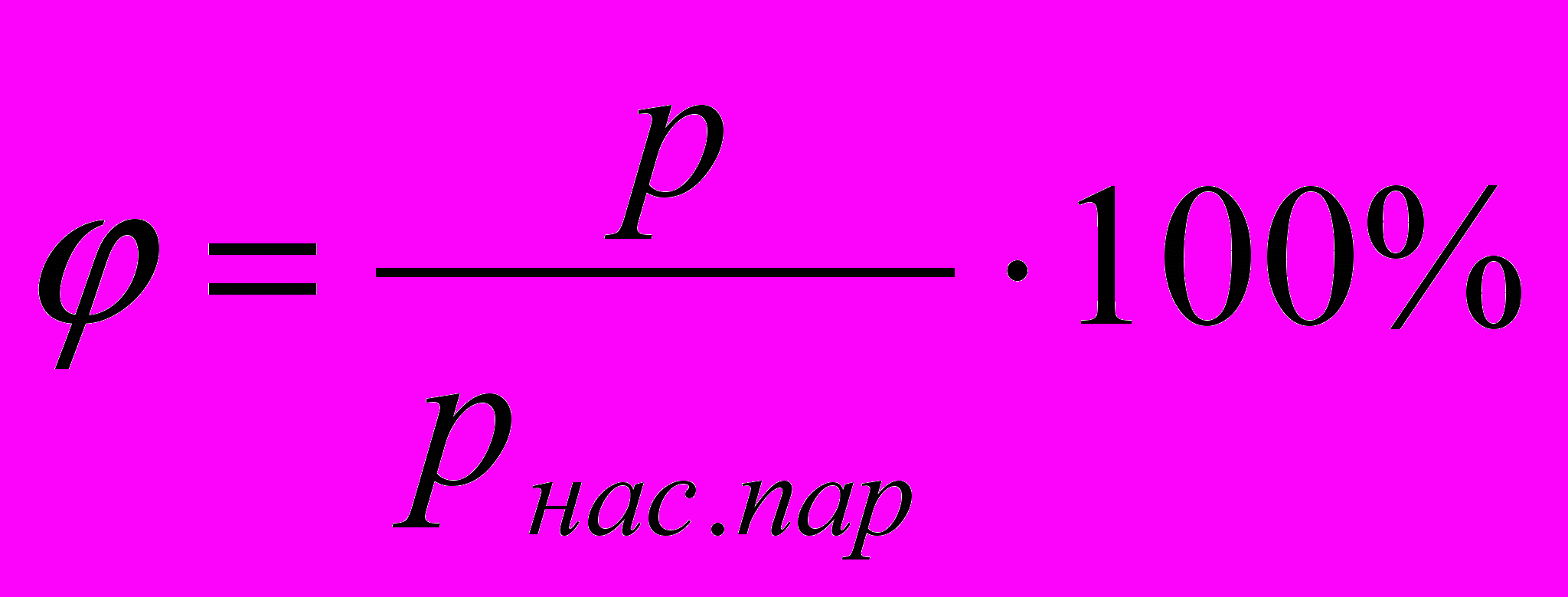 | |||
| Упругие- исчезают после прекращения действия внешних сил. | Пластические- не исчезают после прекращения действия внешних сил. | ||||
| Растяжение. | Сдвиг. | Смачивающая жидкость- силы притяжения жидкости к молекулам твердого тела больше, чем между молекулами жидкости.  вода | Несмачивающая жидкость- силы притяжения жидкости к молекулам твердого тела меньше, чем между молекулами жидкости.  ртуть | ||
| Изгиб. | Кручение. | ||||
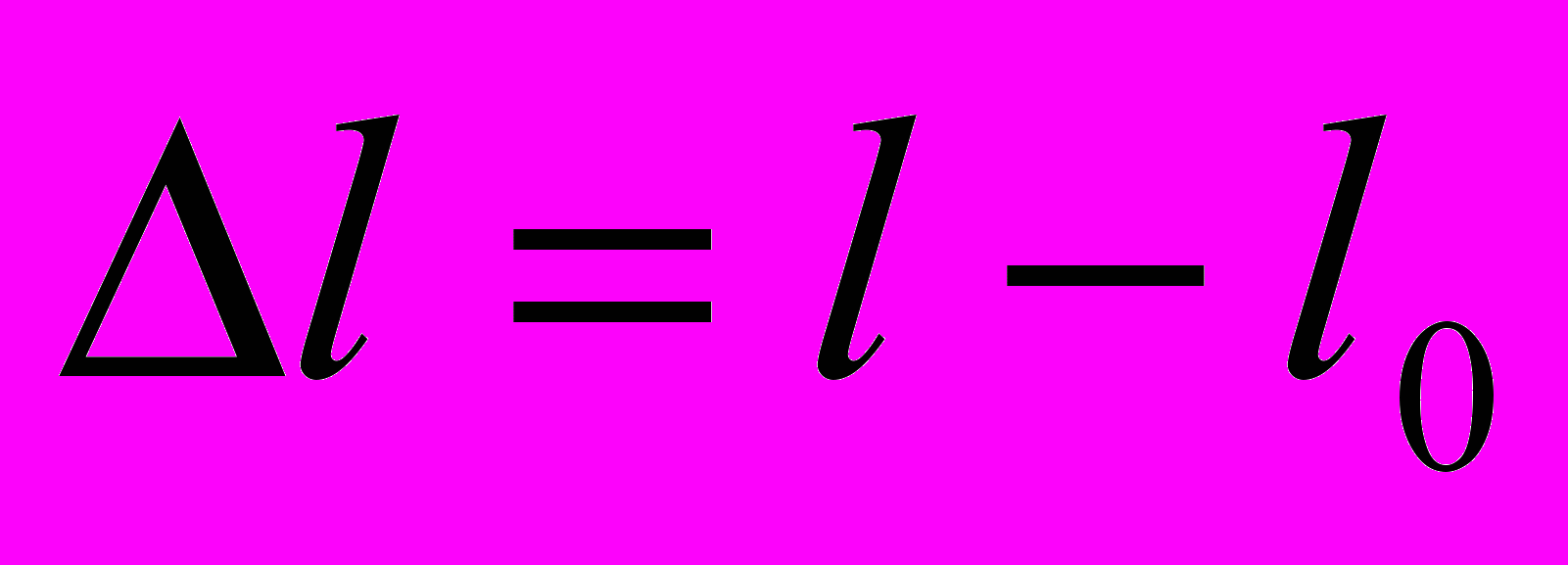 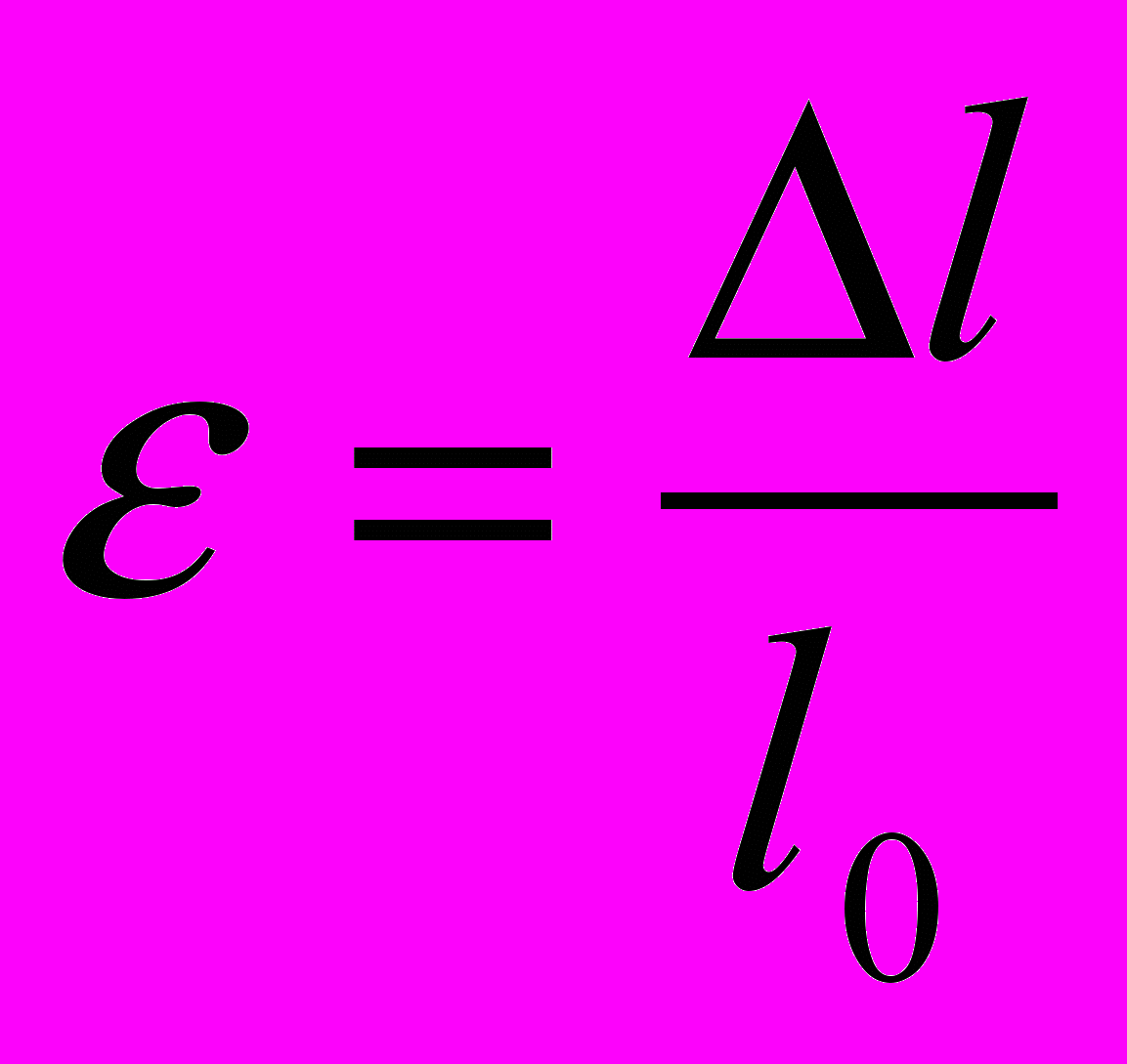 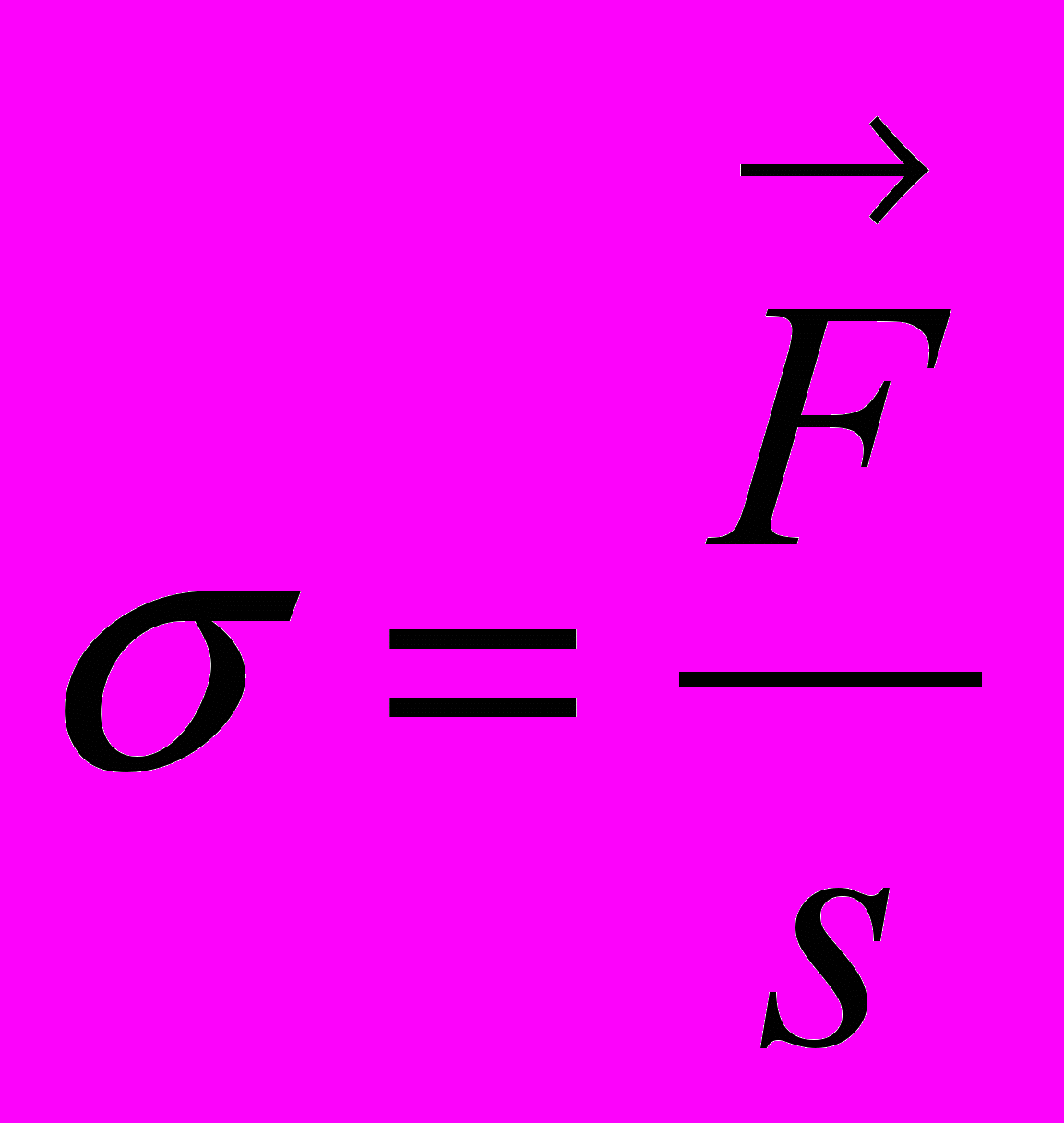 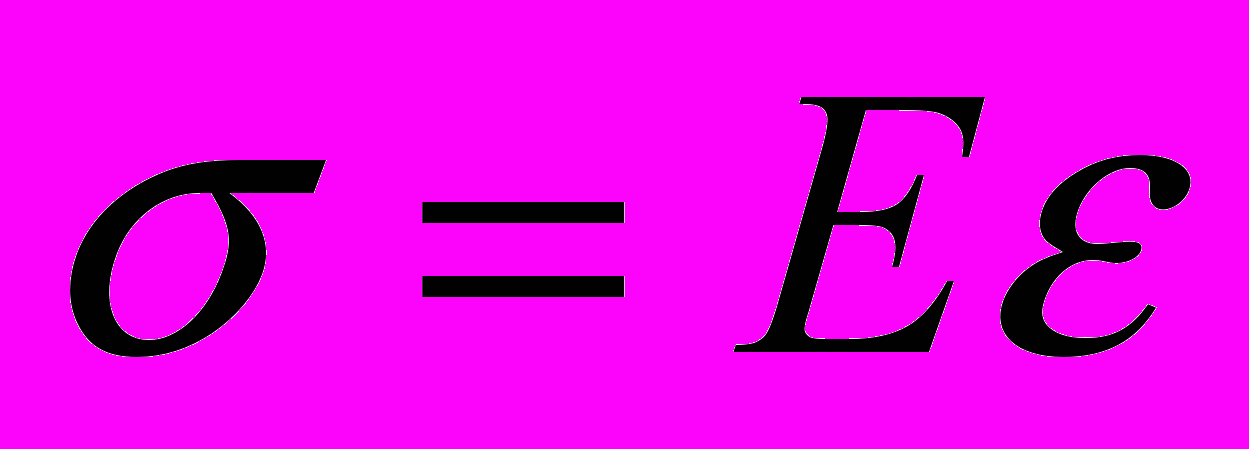 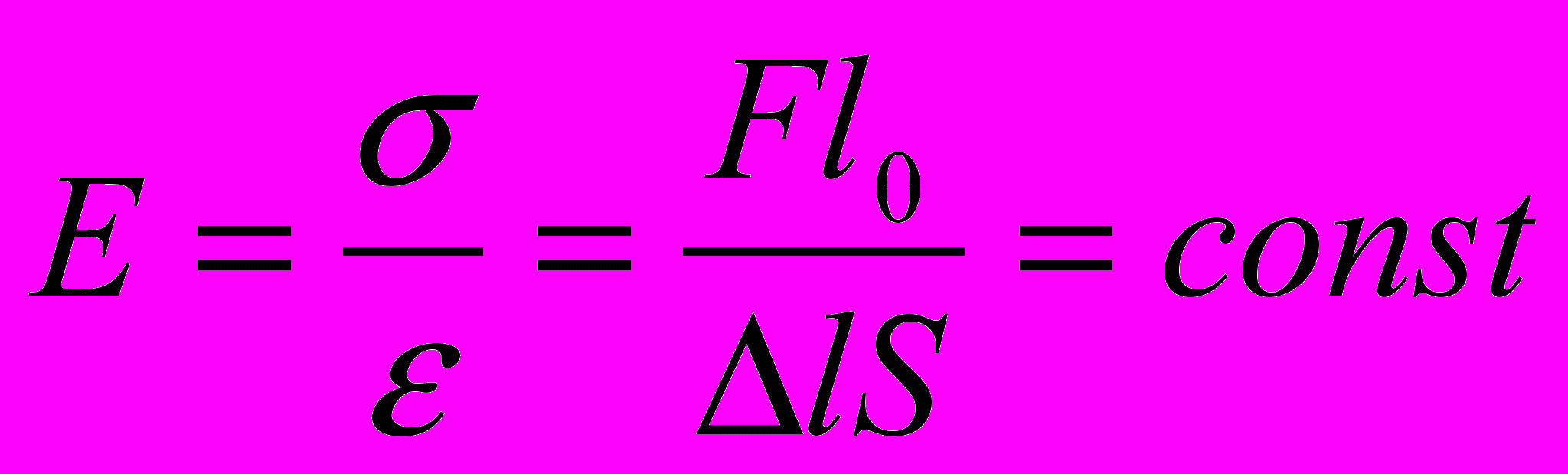 | 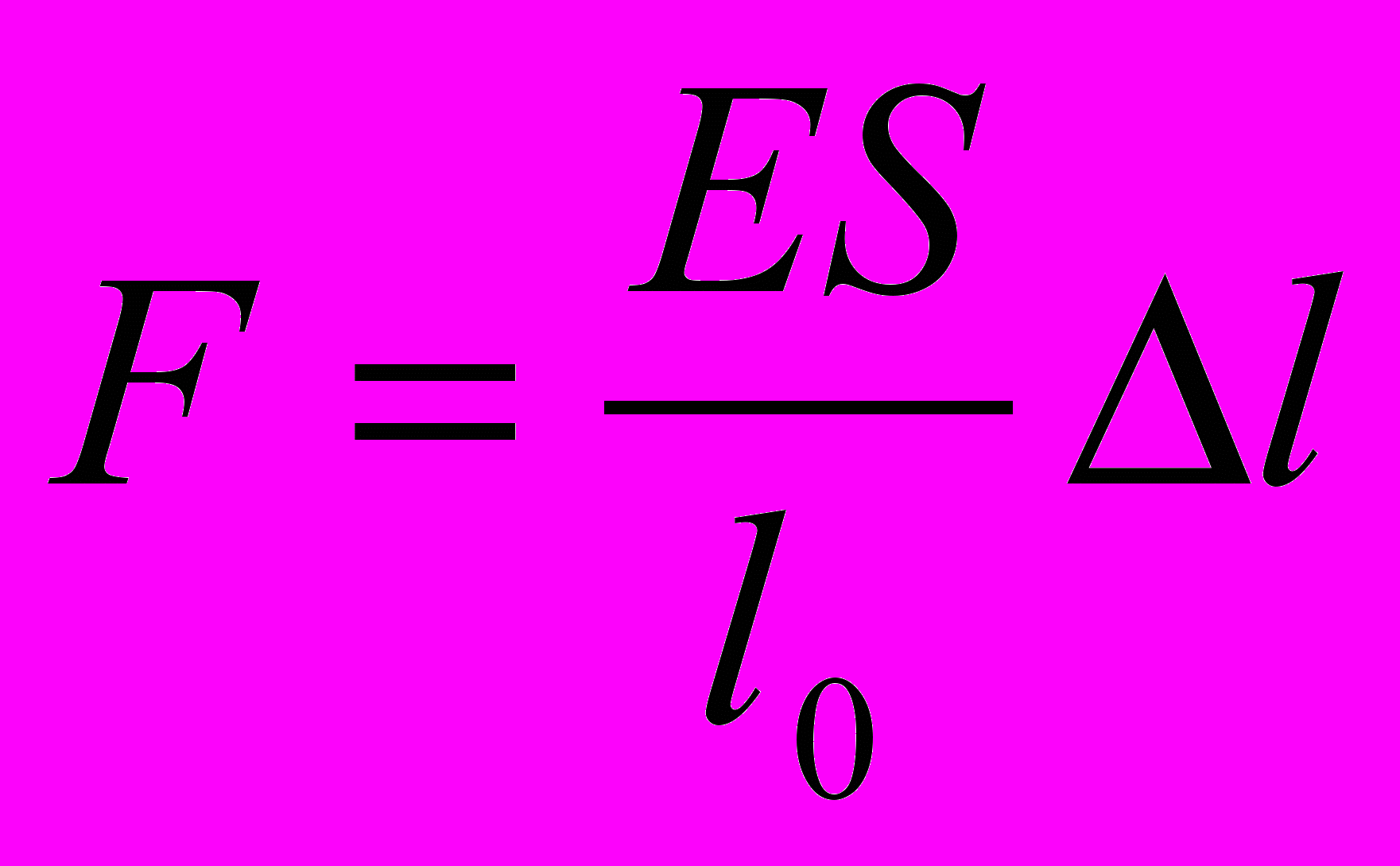 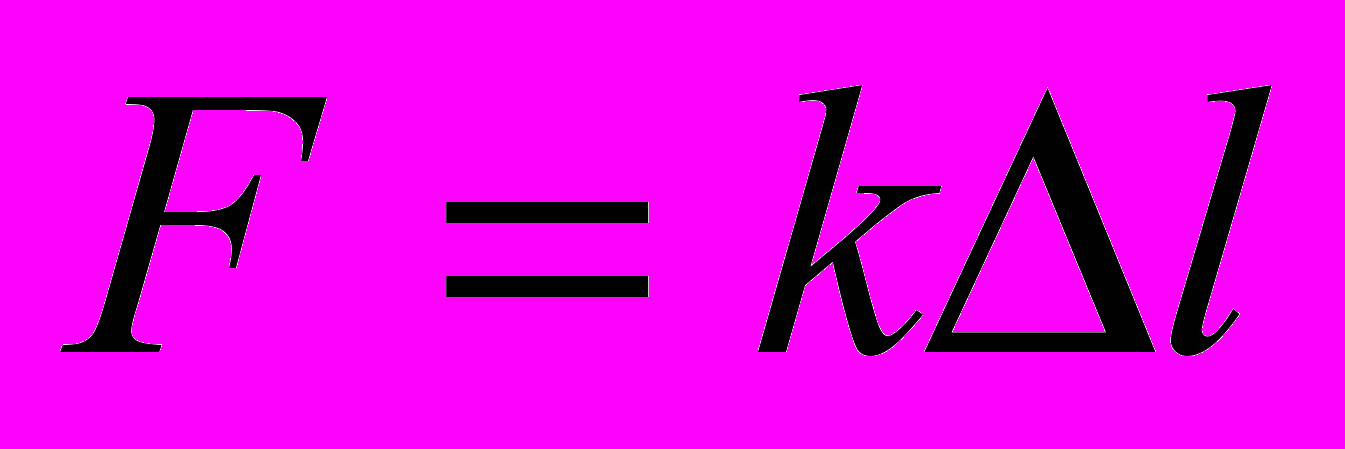 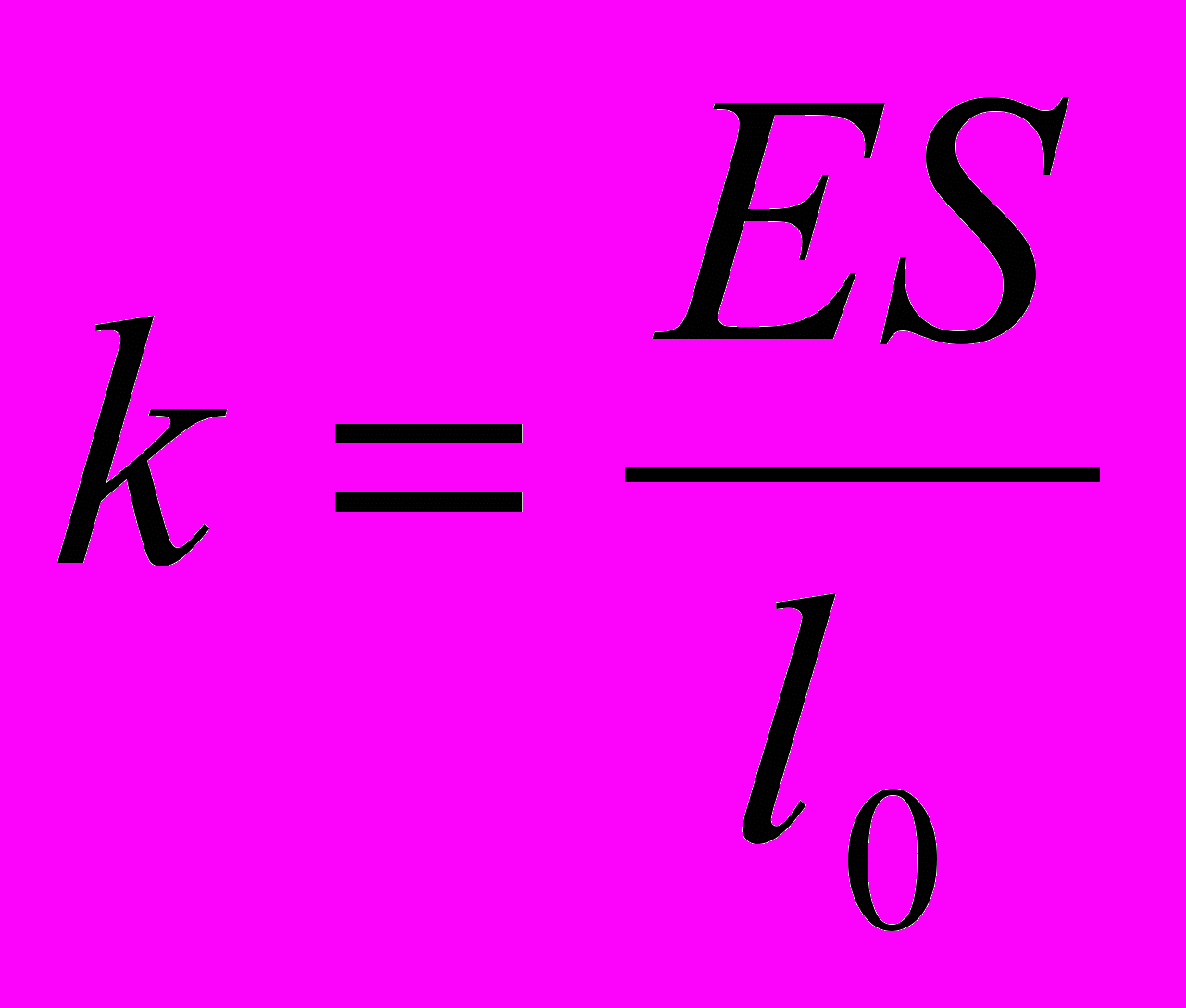 | 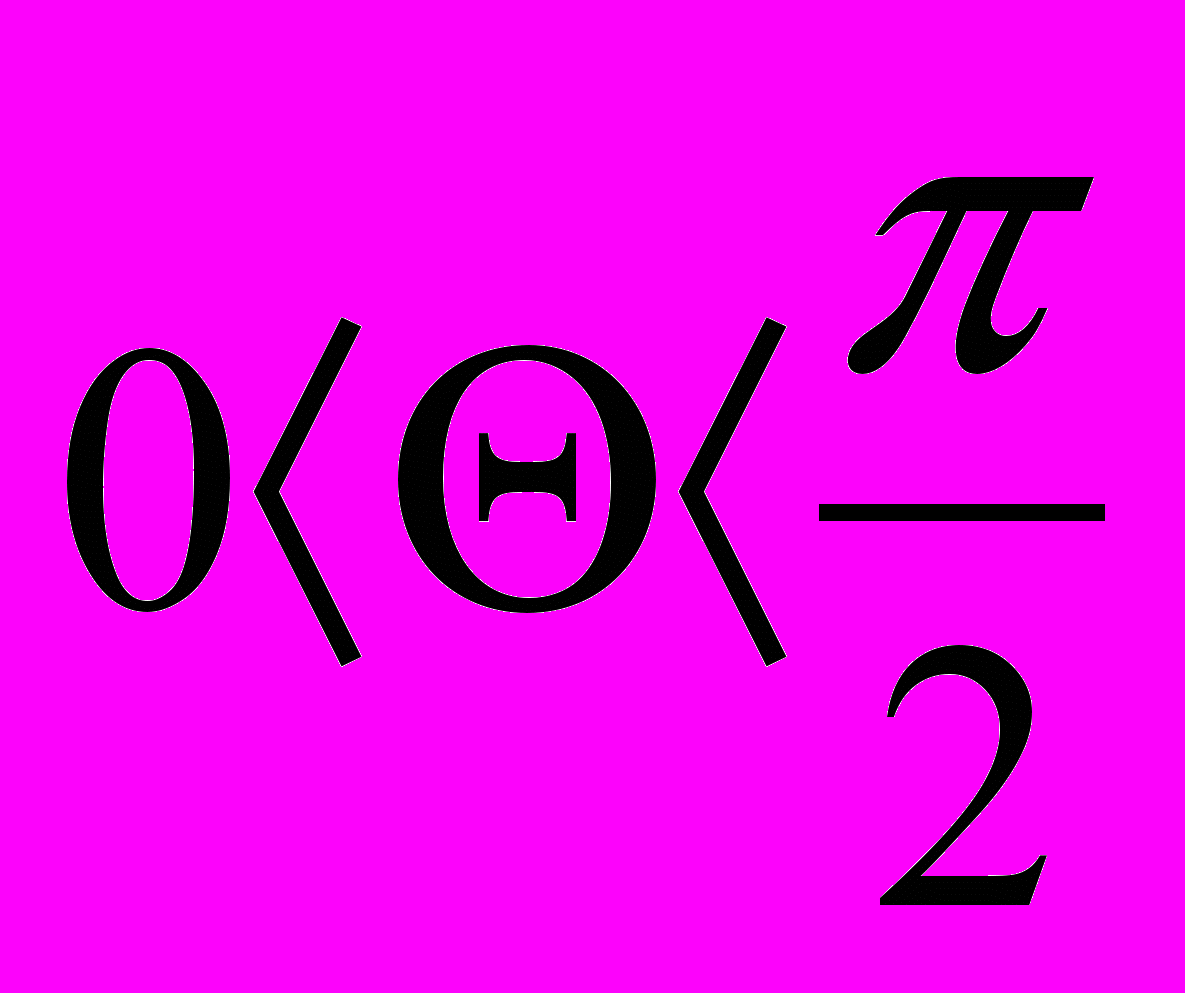 Краевой эффект |  Краевой эффект Краевой эффект | Динамическое равновесие в системе пар- жидкость: число молекул, испаряющихся с поверхности жидкости в единицу времени, равно числу возвращающихся молекул конденсируемого пара. | |
| К  ристаллические тела- твердые тела, в которых атомы и молекулы расположены упорядоченно и образуют периодически повторяющуюся внутреннюю структуру. ристаллические тела- твердые тела, в которых атомы и молекулы расположены упорядоченно и образуют периодически повторяющуюся внутреннюю структуру. | В капиллярах смачивающая жидкость поднимается. | В капиллярах несмачивающая жидкость опускается. | Пар насыщенный- пар, находящийся в динамическом равновесии со своей жидкостью. | ||
| Аморфные тела- имеют одинаковые физические свойства по всем направлениям. На расстояниях порядка межатомных наблюдается некоторая упорядоченность в расположении атомов. | Высота поднятия (опускания): 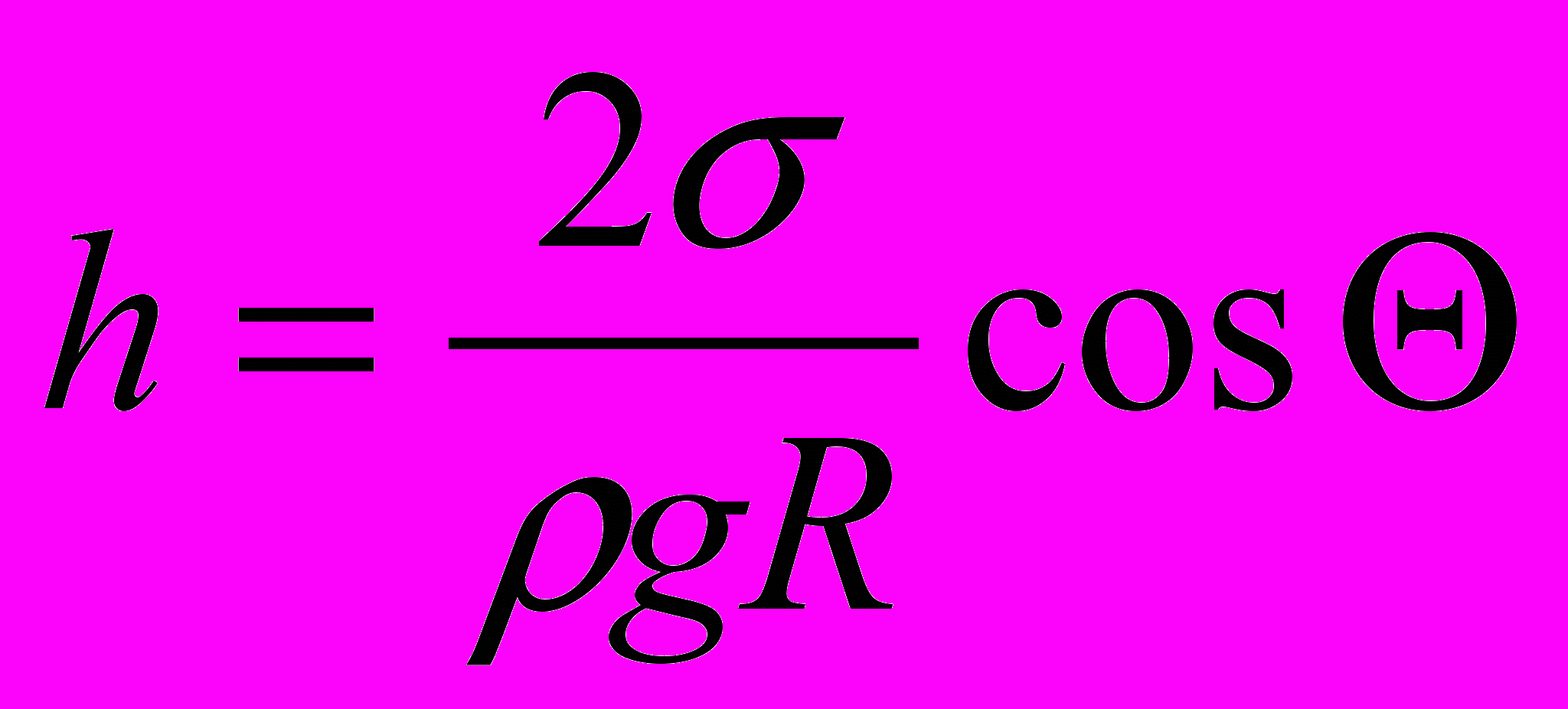 | Пар ненасыщенный- пар, находящийся при давлении ниже давления насыщенного пара. | |||
| Монокристаллы | Кристаллы, имеющие единую упорядоченную кристаллическую решетку. Особенность- анизотропность и постоянство углов между гранями. |
| Анизотропия | Зависимость физических свойств кристалла от направления. |
| Поликристаллы | Твердые тела, состоящие из маленьких кристаллов. Свойства по всем направлениям изотропны. |
| Изотропность | Одинаковость физических свойств кристалла от направления. |
