Автофоретическое формирование полимерных покрытий на поверхности алюминиевых и медных сплавов
| Вид материала | Автореферат диссертации |
Содержание3.3.Адсорбционные процессы и коррозионное поведение меди и её сплавов в растворах олигомера К Ч -0125 |
- Тема: сварка алюминия и его сплавов, 56.75kb.
- Флюсы и рециклинг алюминия, 130.43kb.
- Новые технологии и оборудование для формирования покрытий из полимерных экструдатов, 25.72kb.
- Протасов В. Н. Ргу нефти и газа им., 101.76kb.
- Реферат по научно-исследовательской работе г 08 Нано- и микроструктурная модификация, 64.1kb.
- Влияние импульсного электронного облучения на формирование ультрамелкозернистой структуры, 35.51kb.
- Развивающаяся область модификации поверхности это нанокомпозиты на основе сверхтонких, 41.9kb.
- Физические свойства вакуумно-плазменных покрытий для режущего инструмента, 338.06kb.
- Онно-твердеющих сплавов в основе своей связано с разработкой и исследованием высокопрочных, 98.83kb.
- Технологические и металлургические особенности лазерной сварки современных авиационных, 212.71kb.
3.3.Адсорбционные процессы и коррозионное поведение меди и её сплавов в растворах олигомера К Ч -0125
Так же как и в случае алюминия при погружении медных сплавов в растворы олигомера КЧ-0125 происходит образование адсорбционной пленки (рис.6).
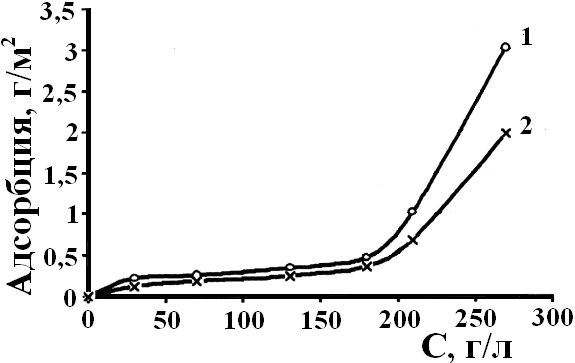 | Изотермы адсорбции можно разделить на три участка в исследуемой области концентраций растворов и описать первые и вторые участки уравнением Ленгмюра. На основании полученных данных по адсорбции олигомера КЧ-0125 на латуни рассчитаны толщины адсорбционных слоев (δ) и эффективные площадки, занимаемые одной усредненной молекулой (Sэф) (табл.3). |
| Рис.6. Изотермы адсорбции олигомера КЧ-0125 на медно-цинковых сплавах при различных значениях рН водного раствора: рН = 6,5 (1) и рН= 8,0 (2) |
Таблица 3
Характеристика адсорбционных слоев олигомера КЧ-0125 на поверхности латуни
| рН | А1∞, г/м2 | А2∞, г/м2 | ∆А∞, г/м2 | δ1 х 104, м | δ2 х 104, м | ∆δ х 104, м | Sэф х 1020, м2 |
| 6,5 | 0,16±0,01 | 0,65±0,02 | 0,52±0,02 | 1,043±0,01 | 6,58±0,02 | 5,537±0,02 | 0,62±0,02 |
| 8,0 | 0,11±0,03 | 0,35±0,01 | 0,24±0,03 | 0,717±0,03 | 2,28±0,01 | 1,563±0,03 | 0,90±0,01 |
Из таблицы следует, что толщина адсорбционных слоев уменьшается с увеличением щелочности раствора.
Проведенные исследования зависимостей потенциалов электродов от плотности тока в замкнутой модельной системе Zn – Cu (рис.7) свидетельствуют о том, что максимальная плотность тока коррозии достигается при установлении равновесия между анодным и катодным процессами. Изменение рН и состава электролита вызывают изменение стационарного потенциала и токового показателя коррозии.
При различных значениях рН фонового раствора (рис.7, кривые 1), стационарный потенциал и максимальный ток коррозии практически не изменяются. Контролирующим фактором коррозии в этих случаях является катодный процесс восстановления молекул кислорода (медный электрод). Анодный процесс окисления (цинковый электрод) протекает практически без поляризации и абсолютная величина коррозии соизмерима с величинами анодного растворения металла.
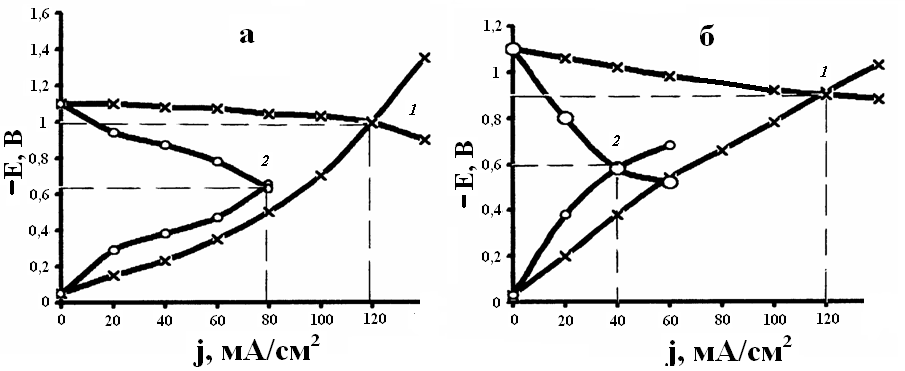 |
| Рис.7.Коррозионные диаграммы для модельного электрохимического элемента Zn – Cu при различных значениях рН водного раствора: а) – рН = 8; б) – рН = 6,5; 1 – фоновые растворы; 2 – растворы, содержащие 0,032% олигомера КЧ-0125. |
При переходе от фоновых растворов к олигомерным (рис.7, кривые 2) наблюдается смещение потенциала в сторону менее отрицательных значений, за счет торможения как анодного, так и катодного процесса. При этом величина тока коррозии снижается в 3 раза.
Об этом же свидетельствуют данные изменения потенциала на реальных образцах (рис.8.). На латунном электроде потенциал в течение времени процесса смещается в менее отрицательную сторону во всех исследуемых растворах. В фоновых растворах это возможно за счет образования оксалатов цинка, а в полимерном растворе – образования олигомерных пленок, наличие которых проверяли 25%-ным раствором аммиака. В фоновом растворе пробой пленок происходил через (20 – 30) с., а в олигомерном – через (30 – 40) мин.
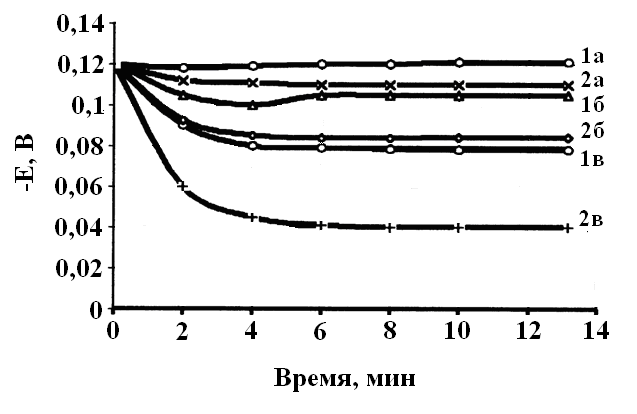 | Рис.8 Зависимость потенциала (по отношению к х.с.э.) от времени выдержки образца. 1 – фоновый раствор; 2 – полимерный раствор; а) – рН=8; б) – рН = 7; в) – рН = 6,5 |
Исходя из стационарного значения потенциала (рис.8) и диаграммы Пурбе, цинковые составляющие (рН = 6 – 7) находятся в области активного растворения, а медные – в области пассивации. Следовательно, возможна ионизация цинка на анодных составляющих, а на медном электроде – восстановление кислорода. Механизм образования Оп можно объяснить с учетом «солевой» и «кислой» форм.
Таким образом, механизм образования олигомерной пленки на медных сплавах, так же как и на алюминиевых можно описать тремя взаимосвязанными параллельно протекающими процессами:
1) образование адсорбционной пленки;
2) в результате чередования анодных и катодных участков на поверхности металла протекают следующие процессы:
А Zn + 2H2O → Zn(OH)2 + 2H+ + 2ē (6)
Zn(OH)2 ↔ Zn2+ + 2OH– (7)
К O2 + 4H+ +2ē ↔ 2H2O (8)
3) взаимодействие адсорбированных полиионов с ионами цинка и протонами с образованием Оп
в виде «солевой» формы:
R(COO–)α + α/2 Zn2+ ↔ [R(COO–)α Znα/2]↓ (9)
и в виде «кислой» формы:
R(COO–)α + α H+ → R(COOH)α↓ (10)
Образование Оп по «кислой» и «солевой» формам обосновано данными кислотных чисел и термогравиметрии.
Результаты определения кислотных чисел свидетельствуют о том, что процесс автоосаждения на 44% идет по механизму «солевой» формы и
56% – по механизму «кислой» формы, так как кислотное число снятых пленок составляет 58,2 мг КОН/г, а лака КЧ-0125 – 105 мг КОН/г.
Термогравиметрические исследования пленок выявили образование «солевой» формы на поверхности латуни в виде кристаллогидрата, что подтверждается выделением кристаллизационной воды при температуре (100 – 140)оС.
Как и в случае нанесения автофорезных Оп на алюминий использование в качестве растворителя смеси вода – ИПС (1:1) улучшает качество Оп на медных сплавах, что подтверждается изотермами адсорбции (рис.9).
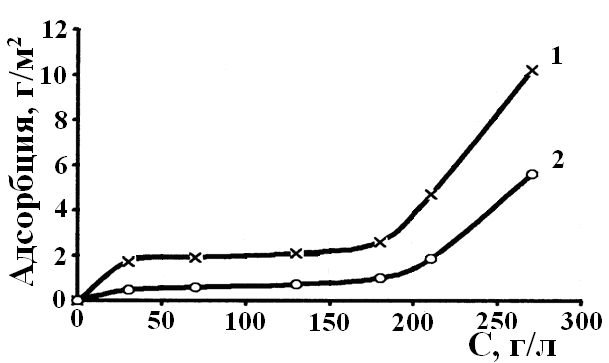
Рис.9. Изотермы адсорбции олигомера КЧ-0125 на поверхности латуни при разных значениях рН водно-спирто-вого раствора: рН = 6,5 (1), рН = 8 (2)
Кривые также имеют три участка в исследуемой области концентраций растворов, как и в водных растворах. Введение ИПС приводит к увеличению толщины адсорбционного слоя, по сравнению с водными растворами (рис.7). При увеличении рН раствора толщина адсорбционного слоя уменьшается в 1,7 раз.
Таким образом введение ИПС позволяет улучшить качество Оп, не меняя в целом механизма автоосаждения и данные, изложенные выше, являются решающими при создании Ок .
Глава 4. Разработка состава олигомерной композиции и технологии
автоосаждения
Разработку состава Ок и технологии процесса автоосаждения проводили с учетом установленных закономерностей, согласно которым сам факт осаждения Оп и значительное улучшение ее качества достигаются за счет двух основных факторов:
– увеличение количества генерируемых протонов на границе раздела металл//олигомерный раствор;
– введение ИПС в Ок.
