На дальнем востоке
| Вид материала | Автореферат диссертации |
- Козлов Л. Е. Точки пересечения внешней и региональной политики России на Дальнем Востоке, 155.08kb.
- Список трудов Раздел Революция и Гражданская война в Сибири и на Дальнем Востоке. История, 88.4kb.
- Е. Н. Принудительные миграции на советском Дальнем Востоке в 1920–1950-е, 75.33kb.
- Политика россии на дальнем востоке по закреплению тихоокеанского побережья (середина, 492.45kb.
- Научная книга в сибири и на дальнем востоке: издание, распространение, использование, 721.6kb.
- Мониторинг отраслевых новостей за 06. 10. 2009, 787.32kb.
- Статья напечатана в научном сборнике Из истории Гражданской войны на Дальнем Востоке, 495.73kb.
- Статья напечатана в сборнике научных статей Из истории Гражданской войны на Дальнем, 1656.39kb.
- Президента Российской Федерации в Дальневосточном федеральном округе Тема доклад, 58.49kb.
- Model United Nations of the Russian Far East отчет, 77.45kb.
Клиническая оценка состояния здоровья новорожденных включала оценку неонатальной адаптации, антропометрических показателей при рождении, анализ заболеваемости, данных лабораторного обследования с учетом данных стандартных учетных форм.
Оценка состояния здоровья женщин предусматривала анализ акушерско-гинекологического анамнеза, течения настоящей беременности и родов, данных лабораторного обследования, наличия профилактики микронутриентного дефицита в течение беременности и лактационного периода и проводилась на основе индивидуального интервьюирования по специально разработанной карте с использованием стандартных учетных форм.
Все новорожденные были распределены на 2 группы – доношенные с низким физическим развитием (ЗВУР) и недоношенные. Кроме этого, все недоношенные были разделены на группы по степени зрелости: 27-32 недели, 33-34 недели и 35-36 недель гестации. Новорожденные 35-36 недель гестации составили 2 подгруппы – недоношенные с нормальным физическим развитием (ФР), соответствующим ГВ (СГВ ФР) и низким физическим развитием (ЗВУР) для данного ГВ. Критериями отнесения в подгруппы с ЗВУР явилось изменение параметров ФР в соответствии с классификацией (Дементьева Г.М., 2003, Шабалов Н.П., 2004).
У всех новорожденных были определены и проанализированы следующие показатели: иммуноферментным методом определена концентрация ТГ: сТ4, ТТГ, Т4, Т3; иммунофлюоресцентным методом с использованием реактивов «DELFIA Neonatal hTSH" на оборудовании фирмы «Wallak» (Финляндия) проводился неонатальный скрининг на гипотиреоз. Ультрасонографическая морфометрия ЩЖ осуществлялась с применением УЗ аппарата «Siemens-Sienna Sonoline» в режиме реального времени. Определение содержания йода в моче и грудном молоке проводилось церий-арсенитовым способом по методике, рекомендованной МСКЙДЗ (ВОЗ, 1993), в модификации Dunn J.T. (1993). Анализ элементного состава волос выполняли с помощью масс-спектрометра с индуктивно связанной плазмой ICP-MS ELAN DRC II фирмы Perkin Elmer (США) методом количественного анализа. Флуорометрическим методом (Голубкина Н.А.,1995) установлена обеспеченность селеном здоровых жителей Дальнего Востока, определен уровень селена в волосах, сыворотке крови, моче, эритроцитах в основных и контрольной группах, а также в продуктах питания и биологических объектах. При помощи «перекисного теста» ((Kuklinski B.et al, 1990) проведено эпидемиологическое обследование селенового статуса у 864 человек в 32 возрастных, сопоставимых по основным показателям, группах населения г. Хабаровска.
Результаты сравнивались с клиническими и лабораторными данными 50 здоровых новорожденных и их матерей – контрольная группа. Проведено исследование в индикаторной группе (НБ) - у 22 молодых здоровых небеременных женщин, постоянно проживающих в г. Хабаровске, представителей однородной социальной группы, без индивидуальных особенностей в питании.
Полученные результаты были подвергнуты статистической обработке по общепринятым методикам: средний показатель (М), среднее квадратичное отклонение (δ), ошибка средней арифметической (m). Применяли также непараметрические методы: критерий знаков, Вилконсона, Манна-Уитни, корреляционный анализ (корреляция Пирсона), частотный анализ, метод множественной линейной регрессии. Достоверность различия определяли по формуле Фишера. Статистический анализ результатов исследования выполнен на ПК с использованием стандартных программ Microsoft Excel 7.0 и Statistic 6.0 с привлечением специалистов-математиков (проф. кафедры общественного здоровья и здравоохранения ДВГМУ, д.м.н., Киселев С.Н.). Различия между группами считали достоверными при значении показателя не менее чем p<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Оценка тяжести йодного дефицита на Дальнем Востоке России
Согласно рекомендациям международных организаций (ВОЗ, ЮНИСЕФ, МСКЙДЗ) для оценки тяжести йододефицита используют индикаторы (клинические - размеры и структура ЩЖ, случаи кретинизма и биохимические - содержание йода в моче, уровень ТТГ и ТГ), позволяющие определить как исходное состояние йододефицита, так и контролировать эффективность лечебных и профилактических мероприятий.
По результатам скрининга на врожденный гипотиреоз установлено, что в 83% случаях уровень ТТГ был в пределах нормы (менее 5 мкЕД\л), с колебаниями от 1 до 5 мкЕД\л - у 55% детей. У 28% новорожденных значения ТТГ находились в пределах меньше 1 мкЕД\л, в эту группу входили все недоношенные дети. У 17% обследованных значения ТТГ превышали границы нормы, что служило основанием заподозрить врожденный гипотиреоз. Первично положительные пробы ТТГ со значением более 20 мкЕД\л были отмечены в 0,59% от общего числа проведенных исследований, т.е. выявлены у 110 новорожденных детей с абсолютным показанием к повторным исследованиям, у 4 детей диагноз врожденного гипотиреоза был подтвержден. Таким образом, оценка результатов неонатального скрининга на врожденный гипотиреоз на территории ДФО свидетельствовала о легкой степени йододефицита, уровень ТТТ ≥ 5 мкЕД\л составил 17%.
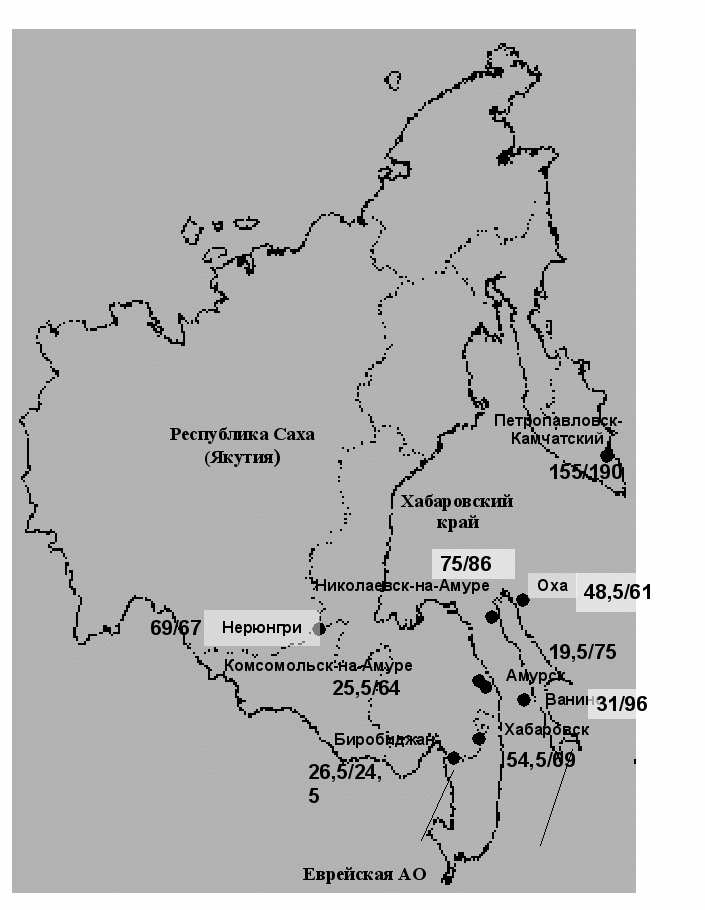
Однако, у беременных женщин и детей предполагаемая обеспеченность йодом может быть значительно ниже среднего уровня в популяции. Нами впервые изучен дефицит йода в перинатальном периоде на ДВ при нормальном течении гестации (рис.1). Для этого проводилось исследование йодурии в парах «мать-новорожденный» на 5-7 сутки после физиологических родов. Ввиду обширности территории и неравномерности размещения населения эпидемиологические исследования проводились в наиболее заселенных регионах ДВ. Всего нами было обследовано 232 женщины и 206 новорожденных из 9 населенных пунктов ДФО, в которых проживает более 2/3 общей численности населения, что обеспечивало репрезентативность эпидемиологических исследований.
Камчатский
край
Сахалинская
область
Рис. 1 Медиана йодурии (мкг/л) в парах «мать/ребенок» в ДФО
Жительницы только 1 из 9 регионов ДВ (г. Петропавловск-Камчатский, йодурия 155 мкг/л) имели оптимальную обеспеченность йодом, что объясняется, видимо, большой долей свежевыловленных морепродуктов в питании. При существенной вариабельности показателей обеспеченности между различными городами и населенными пунктами индивидуальные значения уровня йодурии в городах Амурск, Комсомольск-на-Амуре и Биробиджан достигали критических значений, когда резко возрастает риск возникновения патологии щитовидной железы у матери и плода. Несмотря на отсутствие выраженного йоддефицита, он отмечен у подавляющего большинства исследуемых почти на всей территории ДФО, что свидетельствует о необходимости коррекции дефицита йода у жителей ДВ в перинатальном периоде.
Таким образом, по результатам собственных исследований на ДВ установлена неадекватная обеспеченность йодом у практически здоровых женщин в раннем послеродовом периоде и у их новорожденных детей, что позволяет обосновать и разработать мероприятия по профилактике йодного дефицита у беременных и кормящих женщин, а именно проведение предгравидарной индивидуальной йодной профилактики.
Для выявления особенностей йодообеспечения при преждевременных родах у жительниц г. Хабаровска было обследовано 112 женщин (из них 25 -
индикаторной группы, 45 здоровых женщин в конце нормальной беременности и после родов, 42 родильницы, родившие недоношенных новорождённых при ГВ 33–36 недель). Без дополнительного приема медикаментозных препаратов йода у 100% обследованных уровень йодурии в конце нормальной беременности соответствовал йододефициту среднетяжелой степени (Ме - 46 мкг/л, с интервалом 21 - 74 мкг/л), прием препаратов йода у 90% женщин достоверно повышал до нормы обеспеченность йодом (Ме-162 мкг/л, границы колебаний 84 - 184 мкг/л).
В периоде новорожденности единственным продуктом питания для младенцев, находящихся на естественном вскармливании, является грудное молоко, и проблема адекватного потребления ребенком йода решается путем коррекции питания матери с регулярным приемом препаратов йода весь период лактации. Содержание йода в грудном молоке напрямую зависит от обеспеченности лактирующей женщины йодом и в условиях адекватного содержания должно составлять 150 мкг – 180 мкг (для недоношенных детей - 200 мкг) в литре зрелого женского молока или молочных смесях (ВОЗ, 2005, Герасимов Г.А., 2007, Трошина Е.А., 2008), что обеспечит синтез достаточного количества ТГ и формирование пула йода в ЩЖ новорожденного. При более низком содержании йода в молоке повышается риск развития гипотиреоза, особенно у недоношенных детей (Трошина Е.А., 2007, 2008).
При исследовании содержания йода в грудном молоке родильницы, родившие в срок и преждевременно, были разделены на группы - получавшие и нет индивидуальную профилактику йододефицита фармакологическими препаратами во время исследования. В качестве средства индивидуальной профилактики йододефицита применяли 200 мкг калия йодида (фармакологический препарат).
По нашим данным, медиана содержания йода в грудном молоке ниже оптимального уровня как при нормальных (Ме = 55 мкг/л с интервалом 7-70 мкг/л), так и при преждевременных родах (Ме =56 мкг/л, от 9 до 97 мкг/л), но прием физиологических доз медикаментозных препаратов йода при нормальном сроке гестации достоверно повышает содержание йода в грудном молоке (Ме =119 мкг/л, с интервалом 95 - 218 мкг/л) и создает уникальную возможность для пищевой профилактики йододефицита у детей 1 года жизни. При преждевременных родах даже удвоение уровня содержания йода в грудном молоке (119,5 мкг/л, интервал концентраций 87-157 мкг/л) на фоне индивидуальной профилактики йододефицита фармакологическими препаратами йода оказывается недостаточным, что, по нашему мнению, требует поиска путей решения этой проблемы, в частности увеличения дозы препаратов йода до 250-350 мкг/сутки.
Полученные нами данные подтвердили необходимость проведения индивидуальной йодной профилактики, т.к. большинство беременных женщин не получают адекватную йодную профилактику, их новорожденные уже в раннем неонатальном периоде испытывают йодный дефицит, который будет нарастать при отсутствии йодной профилактики лактирующим женщинам. При этом оптимальной дозой препарата йода для кормящей женщины следует считать ту, которая обеспечивает содержание йода в грудном молоке на уровне физиологических величин (130-180 мкг йода в литре), т.е. она должна быть разной для женщин с физиологическим и патологическим течением беременности, проживающих в условиях йодного дефицита и на территориях с нормальной концентрацией йода в окружающей среде.
Уровень йодного обеспечения недоношенного ребенка имеет значение для прогноза риска развития гипотиреоза, поэтому важно было определить обеспеченность йодом недоношенных новорожденных с разными сроками гестации. У обследованных нами 179 недоношенных детей йодурия имела значительный разброс значений (32–336 мкг/л), поэтому первоначально был проведен сравнительный анализ йодурии в группах, сформированных по значению йодной экскреции - ниже или выше медианы (Ме - 80,5 мкг/л). Среди недоношенных со значениями йодурии выше медианы (32 – 80,5мкг/л) преобладали дети с ГВ 33-34 недели (68%), у них был отмечен более напряженный период ранней адаптации. Более зрелые новорожденные с ГВ 35-36 недель чаще встречались в группе со значениями йодурии ниже медианы (80,5 – 336 мкг/л).
Предположив, что существует зависимость между ГВ и степенью удержания йода в организме, нами проведено исследование йодурии в возрасте 7-10 дней у недоношенных новорожденных в зависимости от ГВ (табл. 2).
Таблица 2
Динамика йодурии (Me) (мкг/л) у маловесных новорожденных
| Группа, ГВ | Mе | Интервал концентраций | % проб с йодурией ≥100 мкг/л | n |
| контрольная | 72,5 | 12 - 193 | 38,5 | 26 |
| 27-32 недель | 77 | 12 - 211 | 16,6 | 24 |
| 33-34 недель | 86 | 12 - 153 | 29,3 | 41 |
| 35-36 недель СГВ ФР | 91 | 10 - 204 | 41,2 | 51 |
| 35-36 недель ЗВУР | 76 | 9 - 186 | 18,9 | 37 |
| Доношенные ЗВУР | 55 | 5 - 198 | 24,1 | 29 |
При проведении корреляционного анализа установлена достоверная прямая связь средней силы (r = 0, 342) между уровнем йода в моче и МТ при рождении – с увеличением массы возрастает уровень йода в моче. Медиана концентрации йода в моче оказалась минимальной в группе доношенных новорожденных с ЗВУР и составила 55 мкг/л, в этой группе установлена высоко достоверная прямая корреляция средней силы (r = 0,369) между уровнем йодурии и длинной тела.
Проведенные нами исследования позволили установить, что выраженность йододефицита тем выше, чем менее зрелый ребенок, усугубляется при недоношенности с синдромом ЗВУР, максимальный йодный дефицит обнаруживается у доношенных новорожденных с синдромом ЗВУР. Также установлено, что чем ниже степень йодурии, тем значительнее диспропорции развития за счет снижения длины тела, но чем выше срок гестации, тем больше детей в подгруппах имели йодурию более 100 мкг/л.
Следовательно, клиническими проявлениями антенатального дефицита йода можно считать морфофункциональную незрелость, недоношенность, особенно в сочетании с синдромом ЗВУР, наличие синдрома ЗВУР при доношенной беременности, нарушение пропорциональности телосложения со сниженной длиной тела.
Однако содержание йода в моче является индикатором только уровня потребления йода с питанием и не дает прямой информации о функциональном состоянии ЩЖ.
На следующем этапе нами были изучены особенности содержания тиреоидных гормонов (ТГ) - Т3, Т4, сТ4 и ТТГ у маловесных новорожденных в конце раннего неонатального периода (табл. 3) и у недоношенных детей в возрасте 45 суток жизни. В качестве референтных значений ТГ приняты собственные данные, полученные в группе контроля.
При невынашивании беременности в ЩЖ достоверно уменьшается выработка и Т3 и Т4, но за счет компенсаторного усиления периферического превращения Т4 в Т3, уровень Т3 поддерживается на достаточно высоком уровне. К снижению функции щитовидной железы приводят и более низкие уровни ТТГ, который является главным стимулятором секреции Т3 и Т4, регулирует синтез и секрецию ТГ по принципу отрицательной обратной связи: высокий уровень Т3 и Т4 подавляет продукцию ТТГ, а низкий, наоборот, стимулирует, но такой механизм осуществляется только при нормальном течении гестации при условии адекватного обеспечения йодом.
Таблица 3
Гормональная функция ЩЖ недоношенных новорожденных (М+m)
| Группа | n | Т3 | Т4 | сТ4 | ТТГ мк/МЕ/мл | Т4/Т3 |
| нмоль/л | ||||||
| 27-32 нед. | 30 | 2,2 + 0,1 * | 126,7 + 7,6 * | 16,4 + 0,9 * | 3,3 + 0,7 | 57,5 |
| 33-34 нед. | 32 | 1,9 + 0,2 * | 166,4 + 13,1* | 19,3 + 0,9 * | 3,9 + 0,4 | 87,6 |
| 35-36 нед. СГВ ФР | 35 | 2,5 + 0,3 | 168,1 + 7,02* | 20,9 + 0,9 * | 3,1 + 0,5 | 67,2 |
| контроль | 30 | 2,8 + 0,3 | 181,4 + 8,3 | 24,5 + 1,1 | 4,1 + 0,7 | 66,7 |
* - достоверность различий (p < 0,05) в сравнении с контролем
В наших исследованиях у недоношенных новорожденных при низких уровнях Т3 и Т4 не происходит увеличения ТТГ, причем, как видно из данных таблицы 3, чем глубже незрелость, тем значительнее снижение как общего, так и свободного Т4.
Изучение уровней гормонов ЩЖ у недоношенных детей в возрасте 1,5 месяцев выявило нормализацию обнаруженных ранее изменений у большинства недоношенных новорожденных. Достоверные различия при сравнении с контролем обнаружены в содержании общего и свободного Т4 в группе недоношенных новорожденных с ГВ 27-32 недели в возрасте 45 суток, что свидетельствовало о сохраняющемся низком функциональном уровне и низких адаптационных возможностях ЩЖ в данной группе детей. У более зрелых недоношенных к 1,5 месячному возрасту уровень гормонов нормализовался и не отличался от данных контрольной группы в таком же возрасте.
При синдроме ЗВУР существующие достоверные различия в содержании гормонов ЩЖ, заключающиеся в снижении содержания Т3, и, в большей степени, Т4 и сТ4 при нормальном уровне ТТГ свидетельствуют о низкой гормональной функции ЩЖ. Преимущественное снижение фракции Т4, являющейся метаболически наиболее активной фракцией ТГ, обусловлено катаболической направленностью обмена у детей с ЗВУР, кроме того, в условиях дефицита йода повышается активность и выработка в плаценте фермента дейодиназы, вызывающего выраженную катаболическую направленность обменных процессов у развивающегося плода, при этом избыток дейодиназы является одним из этиологических факторов низковесности на фоне дефицита йода.
Транзиторная гипотироксинемия – наиболее частый вариант нарушения функции ЩЖ у маловесных новорожденных, т.к. реактивность гипоталамо-гипофизарно-тиреоидной системы недоношенных новорожденных ослаблена, и её включение отсрочено до различных по времени сроков постнатальной жизни. У всех недоношенных новорожденных уровень Т4, как общего, так и свободного был достоверно ниже, чем в контрольной группе, что указывало на снижение гормональной функции ЩЖ. Степень выявленных изменений находилась в прямой зависимости от срока гестации - чем меньше ГВ, тем ниже уровень как общего, так и свободного Т4.
Учитывая, что ЩЖ обеспечивает только 30-40% необходимого организму количества гормона Т3, а в основном он образуется за счет ферментативной конверсии Т4 в Т3, которая происходит в мозге, печени и почках, можно предположить, что у недоношенных новорожденных, в силу морфофункциональной незрелости, этот процесс снижен. Снижение фракции Т4, установленное нами у маловесных новорожденных, приводит к дефициту Т3 - гормона с внутриклеточной точкой приложения, что также является одним из этиологических факторов низковесности.
У недоношенных новорожденных при проведении корреляционного анализа установлена прямая связь средней силы (r = 0,370) между уровнем йодурии и Т3, прямая сильная высоко достоверная связь (r = 0,789) между уровнем йодурии и значением Т4. Полученные результаты расценены нами как проявление повышенной конверсии Т3 в Т4 на периферии и как проявление своеобразной автономии щитовидной железы маловесных новорожденных. У недоношенных новорожденных снижение Т4 при нормальных значениях ТТГ, возможно, свидетельствует не о нарушении функции ЩЖ, а обусловлено повышением тироксинсвязывающей способности плазмы крови на фоне острой адаптации за счет патологически протекающих процессов метаболизма у недоношенных новорожденных при выраженной незрелости, что требует в первую очередь не гормональной коррекции, а нормализации обмена веществ. Результаты исследования гормонов ЩЖ у недоношенных новорожденных в возрасте 1,5 месяцев, когда основные процессы адаптации завершены или стабильны, подтверждают выдвинутую нами гипотезу. Следует также отметить, что нарушение конверсии Т4 может быть вызвано недостатком селена за счет его влияния на селенпротективную дейодиназу и поддерживаться дефицитом йода.
Основными предикторами маловесности, по нашим данным, являются снижение Т4 при нормальных значениях ТТГ, антенатальный дефицит йода, вызывающий выраженную катаболическую направленность обменных процессов у развивающегося плода и преобладание катаболических процессов над анаболическими во время беременности. Клиническим индикатором преобладания катаболических процессов является синдром ЗВУР.
В настоящее время общепризнано, что
