Возможности уз-диагностики в диагностике рака предстательной железы
| Вид материала | Документы |
- Рак предстательной железы, 186.21kb.
- Брахитерапия, 18.32kb.
- Локальная, системная и сочетанная лучевая терапия костных метастазов, 150.74kb.
- Российско-американской конференции «Актуальные вопросы онкоурологии» с мастер-классом:, 116.71kb.
- Нимает в структуре онкологической заболеваемости мужского населения Санкт-Петербурга, 172.34kb.
- Иммунодиагностика и иммунотерапия рака молочной железы, 241.98kb.
- Иммунодиагностика и иммунотерапия рака молочной железы, 212.29kb.
- И. С. Собенников диагностика рака предстательной железы методические рекомендации, 388.71kb.
- Рак пищевода представляет собой наименее исследованную и наиболее агрессивную по течению, 162.36kb.
- Гормонотерапия генерализованного рака предстательной железы, 145.42kb.
Возможности УЗ-диагностики в диагностике рака предстательной железы
Рак предстательной железы (РПЖ) – одно из наиболее часто встречающихся новообразований у мужчин среднего и пожилого возраста. В настоящее время наблюдается тенденция к выходу этого заболевания на лидирующее место в структуре онкологической и онкоурологической заболеваемости у мужского населения России и стран СНГ. В некоторых странах мира (США, Швеции, Германии) РПЖ прочно занимает второе место в структуре онкологической заболеваемости у мужчин.
Клинически неопределяемые очаги злокачественного перерождения предстательной железы выявляются у 15-30% мужчин старше 50 и у 80% мужчин старше 80 лет. По данным американских исследователей, РПЖ составляет 23,4% от всех онкологических заболеваний и 67,9% от онкологических заболеваний мочеполовых органов. В России РПЖ составляет 2,9% всех онкологических и 36% онкоурологических заболеваний. Эти цифры свидетельствуют о том, что, к сожалению, в России мужчины не доживают до РПЖ, так как их средняя продолжительность жизни составляет всего лишь 64,8 лет, по сравнению с 82 годами на Западе.
До последнего времени считалось, что "малый" рак предстательной железы (объем опухоли не превышает 1 см3) является клинически малозначимым, так как редко обладает инфильтрирующим (проникающим в другие органы и ткани) ростом и не проявляется симптомами раковой интоксикации. Новые данные, полученные в результате обследования больных раком предстательной железы, показывают, что течение заболевания при небольших по размерам опухолях практически непредсказуемо и зависит, в основном, от их биологической активности. Из-за отсутствия ранних симптомов злокачественные опухоли простаты распознаются, как правило, на поздней стадии распространенности процесса. От 60 до 80% пациентов с раком предстательной железы при первичном обращении уже имеют отдаленные метастазы. Диагностика рака предстательной железы в доклинической стадии приобрела особую актуальность в последние годы благодаря появлению реальных шансов на радикальное хирургическое лечение. Однако до настоящего времени, несмотря на бурное развитие новейших лучевых технологий, включающих спиральную компьютерную томографию (СКТ), магнитно-резонансную томографию (МРТ) и позитронно-эмиссионную томографию (ПЭТ), обладающих высокой чувствительностью и специфичностью, диагностика "малого" рака предстательной железы представляет определенные трудности.
В
 норме предстательная железа располагается в малом тазу, под мочевым пузырем. По форме напоминает плод каштана. В железе различают основание, прилежащее к мочевому пузырю, верхушку, примыкающую к тазовой диафрагме, заднюю поверхность выпуклой формы, прилежащую к передней стенке прямой кишки и переднюю поверхность выпуклой формы, обращенную к лону. На задней поверхности есть борозда, условно разделяющая предстательную железу на доли. Предстательная железа плотно охватывает часть мочеиспускательного канала.
норме предстательная железа располагается в малом тазу, под мочевым пузырем. По форме напоминает плод каштана. В железе различают основание, прилежащее к мочевому пузырю, верхушку, примыкающую к тазовой диафрагме, заднюю поверхность выпуклой формы, прилежащую к передней стенке прямой кишки и переднюю поверхность выпуклой формы, обращенную к лону. На задней поверхности есть борозда, условно разделяющая предстательную железу на доли. Предстательная железа плотно охватывает часть мочеиспускательного канала.Выделяют четыре зоны: центральную, периферическую, переходную, располагающуюся с боков проксимальной уретры, переднюю фибромускулярную, покрывающую переднюю часть предстательной железы. Предстательная железа состоит из 30-50 желез, выводные протоки которых сливаясь открываются в уретру. В предстательной железе имеются периуретральные железы – вокруг простатического отдела уретры. Помимо желез, предстательная железа содержит большое количеств гладкомышечных волокон и прослоек соединительной ткани, переходящих в капсулу.
Диагностический комплекс должен включать в себя обязательное пальцевое ректальное исследование, определение уровня простатспецифического антигена (ПСА) в сыворотке крови и трансректальное ультразвуковое исследование (ТРУЗИ) с последующей биопсией и морфологической верификацией.
Опухоли предстательной железы проявляются локальным уплотнением. Однако метод пальпации достаточно субъективен и зависит от опыта врача. Кроме того, опухоли небольшого размера, расположенные у передней поверхности и в срединной части предстательной железы, недоступны для исследования. C трудом определяется опухолевый узел размером менее 1,5-2 см3.
На сегодняшний день ПСА является одним из самых чувствительных биологических маркеров для ранней диагностики РПЖ. В норме уровень ПСА не превышает 2,5-4,0 нг/мл. Повышение уровня ПСА выше этих значений требует дополнительных диагностических манипуляций. Однако следует отметить, что уровень ПСА может повышаться и при неопухолевых заболеваниях простаты, таких как простатит и доброкачественная гиперплазия (увеличение) и при урологических манипуляции, травмирующих железу, но значения его не превышают 10-16 нг/мл. Повышение уровня ПСА даже при отрицательном результате пальцевого и ультразвукового ректального исследования требует биопсии простаты под ультразвуковым наведением.
Определенные успехи в области раннего распознавания, дифференциальной диагностике и оценке местного распространения рака предстательной железы достигнуты в последние годы. Это связано с новыми достижениями в технике получения изображения на современных ультразвуковых аппаратах, позволяющих с высокой точностью распознавать ткани предстательной железы; и принципиально новым направлением – цветовой ультразвуковой ангиографией (исследование сосудов), включающей цветовое и энергетическое допплеровское к
 артирование, трехмерную (3D) реконструкцию сосудов.
артирование, трехмерную (3D) реконструкцию сосудов.И
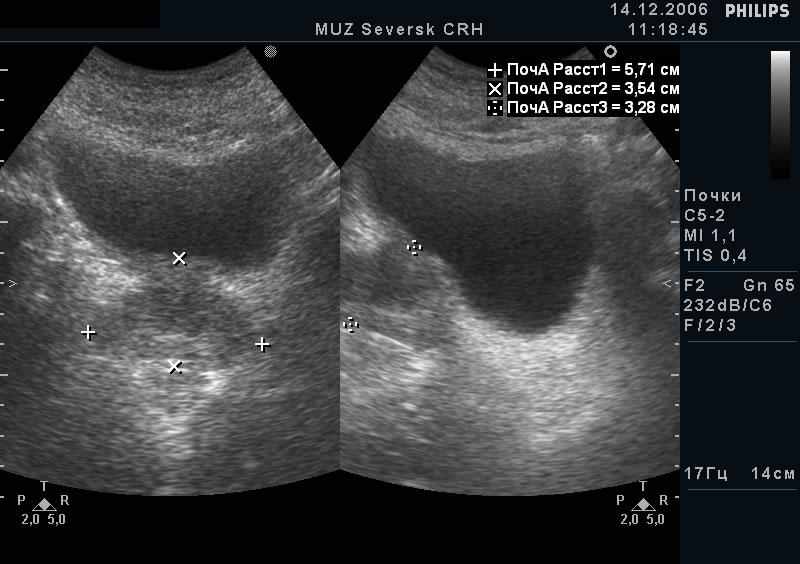 звестно, что наиболее ранними ультразвуковыми признаками злокачественного перерождения предстательной железы являются очаговые изменения ее эхоструктуры. В большинстве случаев локализованного рака предстательной железы наблюдается появление одного или нескольких узлов неправильной формы и пониженной проводимости, расположенных преимущественно в периферических зонах предстательной железы. Периферическая зона занимает 75% объема простаты и в этой части железы рак возникает в 80% случаев. Большей частью опухоль располагается на глубине 3-4 мм от пограничного слоя. В ряде случаев они имеют признаки инфильтративного роста, с распространением на внутреннюю поверхность капсулы предстательной железы или ее прорастанием. Важными являются локальное утолщение капсулы и нечеткость наружного контура, патологические изменения семенных пузырьков. К характерным особенностям рака простаты относится бугристый контур железы с признаками прорастания в пограничный слой. Выявление данных ультразвуковых признаков позволяет правильно установить степень локального распространения опухолевого процесса, особенно при инфильтрации переднебоковой поверхности железы, которая не определяется при пальцевом исследовании. Центральная зона занимает около 20% объема железы. В этой части простаты развивается только 5% злокачественных новообразований. Вокруг простатического отдела уретры располагается тонкий участок железистой ткани - так называемая переходная зона. В норме она практически не дифференцируется от центральной зоны и занимает всего 5% объема простаты. В переходной зоне рак развивается в 20% случаев. Однако опухоли данной локализации являются наиболее сложными для диагностики.
звестно, что наиболее ранними ультразвуковыми признаками злокачественного перерождения предстательной железы являются очаговые изменения ее эхоструктуры. В большинстве случаев локализованного рака предстательной железы наблюдается появление одного или нескольких узлов неправильной формы и пониженной проводимости, расположенных преимущественно в периферических зонах предстательной железы. Периферическая зона занимает 75% объема простаты и в этой части железы рак возникает в 80% случаев. Большей частью опухоль располагается на глубине 3-4 мм от пограничного слоя. В ряде случаев они имеют признаки инфильтративного роста, с распространением на внутреннюю поверхность капсулы предстательной железы или ее прорастанием. Важными являются локальное утолщение капсулы и нечеткость наружного контура, патологические изменения семенных пузырьков. К характерным особенностям рака простаты относится бугристый контур железы с признаками прорастания в пограничный слой. Выявление данных ультразвуковых признаков позволяет правильно установить степень локального распространения опухолевого процесса, особенно при инфильтрации переднебоковой поверхности железы, которая не определяется при пальцевом исследовании. Центральная зона занимает около 20% объема железы. В этой части простаты развивается только 5% злокачественных новообразований. Вокруг простатического отдела уретры располагается тонкий участок железистой ткани - так называемая переходная зона. В норме она практически не дифференцируется от центральной зоны и занимает всего 5% объема простаты. В переходной зоне рак развивается в 20% случаев. Однако опухоли данной локализации являются наиболее сложными для диагностики.При прорастании опухолью пограничного слоя опухолевый инфильтрат распространяется по парапростатической клетчатке к стенкам таза, инфильтрирует семенные пузырьки и дно мочевого пузыря. Патологические процессы приводят к изменению формы, размеров, структуры семенных пузырьков и симметричности относительно срединной линии. При этом нарушается сократимость семенного пузырька с понижением его эхогенности, иногда в сочетании с кистозными изменениями.
Однако существует группа опухолей предстательной железы, составляющих, по мнению ряда авторов, до 30%, обладающих изоэхогенными (одинаковой проводимости с тканью железы) свойствами или имеющих картину чередования гипоэхогенных и изоэхогенных участков различных размеров. С другой стороны, аналогичные по характеру участки могут наблюдаться и при остром простатите, и при некоторых формах доброкачественной гиперплазии. В таких случаях поможет ультразвуковая ангиография. Различия в кровоснабжении при простатите и раке позволяют проводить диагностику между отдельными патологическими участками в железе. Для опухолевых сосудов характерно патологическое ветвление, различный их калибр, извитой ход и слепые карманы вместо концевых артериол. Наиболее перспективным методом в оценке сосудистого рисунка предстательной железы стала 3D-ангиография.
Заключение:
- Использование ТРУЗИ в сочетании с УЗ-ангиографией и 3D объемной
реконструкцией предстательной железы позволяет диагностировать рак предстательной железы на разных стадиях заболевания и обеспечивает получение объективной информации о пространственном расположении новобразования и прорастании стенки мочевого пузыря.
- При заболеваниях предстательной железы исследование ее кровоснаб
жения имеет определяющее значение и повышает положительную предсказательную ценность ТРУЗИ в выявлении инфильтрирующих опухолей и опухолей с нечеткими контурами.
- Использование ТРУЗИ с 3D-реконструкцией значительно расширяет
возможности ранней диагностики рака предстательной железы и позволяет судить о распространении опухоли за пределы капсулы или поражении семенных пузырьков, что имеет важное значение для точного установления стадии заболевания, определяющего тактику лечения.
Андрей Алексеевич Ивлюков
врач ультразвуковой диагностики
отделения ультразвуковой диагностики
ОКД «ЦД и ССХ»
