 Авторефераты по всем темам >>
Авторефераты по ветеринарии
Авторефераты по всем темам >>
Авторефераты по ветеринарии
Методологические основы определения солей тяжелых металлов в кормах и биологических жидкостях организма и профилактика их токсического влияния на животных
Автореферат докторской диссертации по ветеринарии
|
Страницы: | 1 | 2 | 3 | |
МИРОНОВ
Николай Андреевич
МЕТОДОЛОГИЧЕСКИЕ ОСНОВЫ
определениЯ солей тяжелых металлов
в кормах и биологических жидкостях
организма и профилактика их
токсического влияния на животных
06.02.01 - Диагностика болезней и терапия животных,
патология, онкология и морфология животных
Автореферат
диссертации на соискание ученой степени
доктора ветеринарных наук
Москва 2011
Работа выполнена во ВГНИКИ стандартизации и сертификации ветпрепаратов лаборатории химиотерапии и на кафедре внутренних незаразных болезней животных ФГОУ ВПО Московская государственная академия ветеринарной медицины и биотехнологии имени К.И. Скрябина.
Научный консультант: заслуженный деятель науки РФ
а доктор ветеринарных наук, профессор
Коробов Александр Васильевич.
Официальные оппоненты: доктор ветеринарных наук, профессор
Паршин Павел Андреевч;
аазаслуженный деятель науки РФ,
доктор ветеринарных наук, профессор
Папуниди Константин Христофорович;
а азаслуженный деятель науки РФ,
доктор ветеринарных наук, профессор
Бессарабов Борис Филиппович
Ведущая организация: а Государственное научное учреждение
Всероссийский научно-исследовательскийаа
Институт ветеринарной санитарии, гигиеныа
и экологии Российской академии
сельскохозяйственных наук
Защита состоится л_7____ _______декабря_ 2011 г.
в 10___ час. на заседании диссертационного совета Д 220.042.02 при ФГОУ ВПО Московская государственная академия ветеринарной
медицины и биотехнологии имени К.И. Скрябина по адресу: 109472, г. Москва, ул. Академика Скрябина, д.23; т. 377-93-83.
С диссертацией можно ознакомиться в библиотеке ФГОУ ВПО
Московская государственная академия ветеринарной медицины и
биотехнологии имени К.И. Скрябина.
Автореферат разослан л______ ___________________ 2011 г.
Ученый секретарь
диссертационного совета Сотникова Л.Ф.
1. общая характеристика работы
Актуальность темы. Животноводство России, как и все живое, испытывает в настоящее время экологический стресс. С чем же он связан и какое пагубное влияние имеет? В этом случае хочется отметить следующее.
Загрязнение внешней среды, в том числе и почвы, выбросами в атмосферу солей тяжелых металлов заводами, фабриками, предприятиями по переработке и добыче горнорудной промышленности ядовитых токсических веществ или солей тяжелых металлов, содержащиха Cd, Hg, Pb, F, As (кадмий, ртуть, свинец, фтор, мышьяк, никель, марганец и т.д.), которые накапливаются в почве, затем в растениях, попадают в организм животных и человека, что пагубно отражается на здоровье как животных, так и человека. Кроме того, перечисленные токсические вещества входят в состав лекарств, например сулема (ртуть), каломель (мышьяк), пропитывают древесину от гниения кремнефтористым натрием.
Соли тяжелых металлов в природной среде встречаются повсеместно, так например Pb (свинец) входит как противодетонизирующее вещество в нефтеперерабатывающей промышленности, в частности в бензин. Сгорая, он оставляет на обочинах дорог свинец. Животные, поедая траву вдоль дорог, накапливают его в своем организме (в мышцах, в печени, мозгу и других органах). Свинец с молоком, мясом попадает в пищу людям и снова идет его накопление, что приводит порой к тяжелым отравлениям, к онкологическим заболеваниям и к гибели как животных, так и смертельных случаев у людей.
As (мышьяк). Препараты мышьяка широко используют в борьбе с полевыми, огородными и садовыми вредителями, для протравливания семян, в приманках для грызунов. В ветеринарии они применяются как акарициды и антигельминтики. Неумелое использование их, передозировка при лечении могут привести к отравлениям животных, от животных попадают в организм человека, из которого с трудом выводятся.
Hg (ртуть) - это единственный жидкий тяжелый металл серебристого цвета, в виде сернистой ртути (киноварь). Этот металл был известен с глубокой древности. В природе встречается в соединении с другими элементами (ртутные воды). Современное промышленное и техническое использование ртути и ее соединений исключительно велико (ртутные выпрямители, лампы дневного света и др. приборы).
С давних времен ртутные препараты используются в медицине и ветеринарии. За последние десятилетия некоторые органические соединения стали применяться в сельском хозяйстве для протравливания семян (гранозон и др.), для консервирования древесины и т.д.
F (фтор). Из фтористых препаратов наиболее частые отравления животных вызывают фторид и кремнефторид натрия, уралит и суперфосфат.
Фторид натрия в ветеринарии применяется как антигельминтик и репеллент (средство для отпугивания насекомых), в полеводстве используется для борьбы с вредителями полей и огородов, а так же как родентицид.
Кремнефтористый натрий в ветеринарии применяется как антигельминтик и для опыления растений.
.
Поступление солей в поверхностные водоемы может происходить не только при спуске сточных вод, но и при выпадении из атмосферы на акваторию и площадь водосбора, а также в результате смыва дождевыми и паводковыми водами с поверхности земли соединений никеля, входящих в состав производственных выбросов и промышленных отходов.
В атмосферный воздух соединения солей тяжелых металлов поступают с выбросами предприятий по его производству и переработке. Загрязнение атмосферного воздуха соединениями происходит также при сжигании твердого и жидкого топлива. Установлено, что содержание солей в каменном угле колеблется в пределах от 4 до 24 мг/кг, а в нефти различных месторождений от 0,000003 до 0,00295%. Соли поступают в воздух также с выхлопными газами автотранспорта в количествах, зависящих от вида используемого топлива, а также при стирании автомобильных шин и деталей автомобилей.
Определение тяжелых металлов в пробах, отобранных по трем направлениям на расстоянии до 60 км от города, в котором нет предприятий промышленности, показало, что снеговой покров в окрестностях города содержит в 6 раз больше солей тяжелых металлов, чем на периферии. Зона наибольшего обогащения была смещена в соответствии с розой ветров.
Целью настоящей работы являлось получение количественных и качественных химических методик с высоким процентом точности при исследовании солей тяжелых металлов и таких ядовитых элементов как ртуть, свинец, кадмий, фтор, мышьяк в кормах, в органах и тканях животных, в природных материалах (почва, вода, продукты питания и т.д.), а также установить профилактический барьер для попадания их в животный организм через корма микробиологического синтеза, которые готовятся из отходов нефтеперегонной промышленности. Таким барьером мы выбрали клиноптилолиты или цеолиты, которые скармливали лабораторным животным, мышам, крысам, курам, а также проводили исследования на куриных эмбрионах, что позволило дать практические рекомендации по скармливанию кормов микробиологического синтеза, паприна в корма животным.
В задачи исследования входило:
1. Проверить все существующие химические методики на процент точности определения содержания солей тяжелых металлов.
2. Модифицировать данные методики и ввести новые химические реактивы, химические растворы, элементы, позволяющие улучшить количественное определение солей тяжелых металлов в кормах, тканях и жидкостях организма, в природных материалах, что нами и было сделано, доведя методики исследования до 95% точности.
3. Профилактировать вредное влияние кормов микробиологического синтеза, которые входят, как добавки, во все комбикорма для всех видов животных и рыб.
4. Изучить новую кормовую добавку, состоящую из паприна и клиноптилолитов, т.к. цеолиты, обладая целым комплексом положительных качеств, уникальными сорбционными и каталитическими свойствами, с большим эффектом используются в различных областях промышленности, охране окружающей среды и сельском хозяйстве.
Результаты исследования позволили:
1. Изучить острую и подострую токсичность белково-минеральной добавки на основе паприна и клиноптилолитов на лабораторных животных цыплятах-бройлерах.
2. Выяснить субхроническую и хроническую токсичность белково-минеральной добавки на основе паприна и клиноптилолитов на лабораторных животных и цыплятах.
3. Изучить аллергизирующее действие БМД на морских свинках.
4. Изучить эмбриотоксическое и тератогенное действие БМД на куриных эмбрионах.
Научная новизна. Сравнены химические методы для определенияа солей тяжелых металлов и в сравнительном аспекте показана их точность. Модифицированы существующие методы и повышенаа точность количественного определения солей тяжелых металлов в кормах, тканях и жидкостях организма - методы утверждены Департаментом Ветеринарии. Методика по определению кадмия, свинца, фтора колометрическим методом (разработанная Мироновым Н. А., ВГНКИ ветеринарных препаратов) утверждена заместителем начальником Главного управления ветеринарии Л. П. Маланиныма от 28. 08. 1989 года. Апробация проведена в центральной ветеринарной лаборатории совместно с автором на кормах микробиологического синтеза Паприн и на органах и тканях животных. Установлена воспроизводимость методик (среднее значения определения кадмия, свинца, ртути, фтора составило 90 %). Предложенные модифицированные методики могут использоваться в ветеринарных лабораториях для количественного определения кадмия, свинца, ртути, фтора в кормах, органах и тканях животных. Утверждено центральной ветеринарной лабораторией Главного управления ветеринарии Б. И. Антоновым от 25. о8. 1989 года за № 287.аа Впервые определена эмбрионотоксичность белково - минеральной добавки на основе паприна и клиноптилолита; ее острая и подострая, хроническая и субхроническая токсичность; аллергизирующиеа свойства. Определена антитоксическая функция печени, а критериями ее контроляа при лечении являются альбумины. глобулины в сыворотке крови, пролин, глютаминовая кислота, аргинин и другие показатели крови. Предложенные методы определения солей и тяжелых металлов позволяют проводить экологический мониторинг при контроле триады: почва - растение - животноеа (человек). Подверждается отчетом: л Исследование безвредности опытной партии белково-минеральной добавки (БМД) на основе паприна и клиноптилолита, утвержденным Генеральным директором МП Донское Ростовской области, Новочеркасского района А. И. Кочикьянцома от 09. 12. 1991 года и директором ВГНКИ ветпрепаратова А. П. Паниным от 27. 11. 1991 года.
Практическая значимость работы заключается в модификации существующих методов исследования Cd, F, Hg, Pbа путем подбора новых инградиентов, что позволило повысить их точность. Предложена токсилогическая методика для определения аLD50 и LD100 и ряда других нормативных токсилогических показателей. Предложены адсорбенты - цеолиты, клиноптилолиты, способствующие удалению токсических элементов из кормов и организма. Усовершенствовано определениеа альбуминов, глобулинов, креатинина, бромсульфаминовая проба, определение глютамина, пролина, аргинина, аминокислот.а Это позволяет повысить эффективностьа проведенияа терапевтических мероприятий, нейтрализовать содержащиеся в рационе и соли и тяжелые металлыа и таким образом повысить качество продукции животноводства, сохранить здоровье животных и человека
Апробацию работ проводили на Всесоюзных конференциях по усовершенствованию государственного контроля и сертификации ветеринарных препаратов в ВГНИКИ 1979, 1984, 1989, 1994, 1998, 2003 годах; на Всесоюзных конференциях по кормам микробиологического синтеза, апробация методов и методик в центральной ветеринарной лаборатории Департамента Ветеринарии МСХ России и их утверждение Департаментом Ветеринарии.
Основные положения, выносимые на защиту:
- Разработаны и усовершенствованыа методы определения мышьяка, свинца, кадмия, ртути, фтора.
- Предложены биохимические методы контроля влияния солей и тяжелых металлов на организм животных
- Показаноа влияние БВК при профилактике отравления солями тяжелых металлов
- Испытаны цеолиты на основе клиноптилолитов на продуктивные качества животных.
- Разработанные методы утверждены Департаментом ветеринарии РФ и внедрены в производство.
Публикации. По теме диссертации опубликовано 29 работ, из них в ведущих рекомендуемых ВАК научных журналах и изданиях 14 работ.
Структура и объем диссертационной работы. Диссертация изложена на 175 с., состоит из введения, обзора литературы, материала и методики собственных исследований, результатов и анализа исследований, исследования биоматериала животного для выявления резистентности организма, исследования белково-минеральной добавки на основе паприна и клиноптилолита для профилактики токсического влияния солей тяжелых металлов на животных, выводов, практических предложений, списка литературы. Содержит 22 таблицы и 6 рисунков.
2. материалы и методы исследований
Методика определения токсичности
премикс-кормов на белых мышах
1. Премикс-корма - комплексный препарат. Представляет собой мелкий порошок светло-серого цвета, расфасованный в пакеты массой 1 кг, упакованный в бумажные мешки или фанерные барабаны. В его состав входят витамины, аминокислоты и минеральные соли цинка, меди, марганца и других химических элементов, а также наполнитель (отруби, вторичный фосфат, кормовые дрожжи). Выпускается фирмой по рекомендации автора.
2. Препарат применяют с комбикормом для лечения и профилактики болезней животных с нарушением обмена веществ.
3. Для анализа образцы премиксов-кормов в количестве 200Ц500 г от каждой серии поступают на проверку ВО Союзглавзооветснабпром. Препарат контролируют на токсичность. Испытанию подлежит каждая поступающая серия.
4. Определение токсичности.
4.1. Оборудование, материалы и реактивы:
Ц весы лабораторные второго класса точности с пределом взвешивания 1 кг, ГОСТ 2404-80;
Ц баня водяная;
Ц аппарат для встряхивания жидкости в сосудах (шуттель-аппарат);
Ц колбы вместимостью 150 см3 с притертой пробкой;
Ц стаканы химические мерные вместимостью 100 см3;
Ц шприц вместимостью 1Ц2 см3 с тупыми иглами (длина иглы 3 и более см, диаметр внутреннего отверстия не менее 1,5 мм);
Ц фильтры бумажные (белая лента);
Ц мыши белые беспроводные массой 18Ц20 г.
4.2. Приготовление суспензии.
Навеску препарата в количестве 10 г, взятую после тщательного перемешивания, измельчают в фарфоровой ступке до пылевидного состояния, помещают в колбу, предварительно взвешенную на лабораторных весах, и приливают 90 г дистиллированной воды, подогретой до 70C. Встряхивают на шуттель-аппарате 30 минут.
4.3. Проведение испытания.
Партию мышей, взятую из питомника, предварительно выдерживают под наблюдением в течение 5 дней. Для проверки каждой серии берута 6 мышей, взвешенных с точностью до 0,1 г. Препарат вводят орально при помощи шприца и металлического зонда (игла с направленной оливой) из расчета 5 г на 1 кг живой массы в виде 10%-ной водной суспензии.
Препарат вводят утром на голодный желудок в течение 3 дней подряд. Не допускается гибели ни одной мыши в течение 7 дней после последнего введения премикс-корма. Если присланный образец выдерживает испытание, то данная серия считается нетоксичной и может быть использована в ветеринарной практике. Образцы, не выдержавшие проверки, подвергаются повторному испытанию на удвоенном количестве мышей массой 200,5 г.
Образцы препарата, не прошедшие повторной проверки на мышах, проверяют на том виде животных, которому рекомендован препарат, в тройной терапевтической дозе. В случае гибели одного или нескольких животных препарат бракуется. Опыт проводят на трех животных в течение 7 дней.
Методика определения мышьяка
в кормах микробиологического синтеза
Методика распространяется на белково-витаминный концентрат (БВК), гидролизные дрожжи и другие корма микробиологического синтеза.
Метод основан на измерении интенсивности окраски раствора молибденовой сини, образующейся при восстановлении мышьяковомолибденовой сини под действием молибденовокислого аммония на мышьяк и выделении в виде мышьяковистого водорода.
Отбор проб
Отбор проб проводится в соответствии с техническими условиями на дрожжи кормовые - БВК (паприн) по ГОСТ 13496.0-80.
Метрологическая характеристика
Диапазон определяемых концентраций мышьяка - 0,5 мг/кг. Предел обнаружения мышьяка - 5 мкг в пробе или 0,5 мг/кг. Размах варьирования при определении мышьяка в параллельных пробах составляет 12,3Ц15,3%.
Среднее значение определения мышьяка - 92,9%.
Аппаратура, материалы, реактивы
Прибор для отгонки и поглощения мышьяка (рис. 1).
Спектрометр-26, 46 и др.
Весы аналитические с погрешностью взвешивания не более 0,0002 г по ГОСТ 24104-80.
Весы технические 1-го класса.
Шкаф сушильный с терморегулятором СЭШ-1 или СЭШ-3М, или другой аналогичной марки, обеспечивающий поддержание температуры 1306C.
Эксикатор по ГОСТ 25336-82 (СТ СЭВ 2945-81).
Колбонагреватели или электроплитка с регулятором температуры, или печь желобковая по ГОСТ 13496.4-74.
Колба Къельдаля вместимостью 250 см3 по ГОСТ 25336-82аа (СТ СЭВ 2945-81).
Каплеуловители по ГОСТ 25336-82 (СТ СЭВ 2945-81).
Холодильники (прямые или шариковые) стеклянные лабораторные по ГОСТ 25336-82 (СТ СЭВ 2945-81) с удлиненным нижним концом трубки до 16Ц17 см.
Воронка Брюхера ГОСТ 9147-80.
Воронка стеклянная диаметром 6 см по ГОСТ 25336-82. Палочки стеклянные ГОСТ 21400-75.
Колбы мерные 50, 100 и 1000 см3 по ГОСТ 1770-74.
Стаканы химические вместимостью 100 см3 по ГОСТ 25336-82.
Пипетки 1-1-1; 1-1-2; 1-1-5; 1-1-10 по ГОСТ 25336-82.
Цилиндры мерные вместимостью 10, 25, 100 и 1000 см3 по ГОСТ 1770-74.
Спирт этиловый ректификат ГОСТ 5962-67.
Калий бромистый ГОСТ 4160-65, х.ч.
Гидразин сернокислый ГОСТ 5841-65, ч.д.а.
Аммоний молибденовокислый ГОСТ 3765-6, х.ч.
Фенолфталеин ГОСТ 5850-72 ч.д.а.
Кислота соляная ГОСТ 3118-77, х.ч.
Кислота серная ГОСТ 4204-77, х.ч.
Кислота азотная ГОСТ 4461-77, х.ч.
Кислота хлорная по ТУ 6-09-2887-73 ч.
Натрия гидроокись ГОСТ 4328-77, ч.д.а.
Калий йодистый ГОСТ 4432-74, х.ч.
Перекись водорода (пергидроль) ГОСТ 10926-76, х.ч.
Ангидрид мышьяковистый ГОСТ 1973-77, х.ч.
Натрий мышьяковистый двузамещенный, 7-водный или стандарт-титр.
Допускается применять импортное оборудование, посуду и реактивы с техническими характеристиками не ниже отечественных аналогов.
Подготовка к испытанию
4.1. Минерализация
Способ основан на полном разрушении органических веществ (гидролизных дрожжей, БВК) при нагревании с серной и азотной (концентрированными) кислотами с добавлением хлорной кислоты.
4.2. Подготовка к минерализации
4.2.1. Стеклянную посуду после обычной мойки дополнительно промывают раствором азотной кислоты, ополаскивают водопроводной, а затем дистиллированной водой.
4.2.2. Навеску гидролизных дрожжей, БВК взвешивают в стакане и переносят в колбу Къельдаля, стараясь не попасть на стенки колбы.
4.2.3. В колбу Къельдаля с навеской пробы, подготовленной по пп. 4.2.1., 4.2.2., вносят по 10 мл серной и азотной кислоты и выдерживают в течение 12 часов (лучше оставить на ночь).
4.2.4. Колбу Къельдаля медленно нагревают на электроплитке в течение 2-х часов, избегая бурной реакции.
После прекращения выделения бурых паров азотной кислоты колбу вынимают, ставят на 20Ц30 минут для охлаждения и затем добавляют 10 мл азотной кислоты с последующим постепенным нагреванием. Как только жидкость начнет кипеть, температуру накала электроплитки увеличивают до максимума и продолжают озолять до исчезновения бурых паров азотной кислоты. Затем колбу вынимают, дают остыть содержимому и после этого приливают еще 10 мл азотной кислоты и продолжают постепенно нагревать.
После исчезновения бурых паров азотной кислоты колбу вынимают, дают остыть и в центр жидкости приливают 1 мл хлорной кислоты с последующим нагреванием. Озоление проводят до полного обесцвечивания жидкости. Хлорную кислоту добавляют по мере необходимости. Всего за период озоления пробы расходуется до 5 мл хлорной кислоты.
4.2.5. После обесцвечивания содержимого колбу вынимают, охлаждают, добавляют 5 мл насыщенного раствора щавелевокислого аммония и нагревают до испарения раствора и выделения белых паров серной кислоты, затем охлаждают. После охлаждения стенки колбы обмывают дистиллированной водой и нагревают до удаления ее паров. Готовый раствор в колбе должен быть бесцветным или соломенно-желтого цвета.
4.2.6. Контрольную пробу готовят, используя те же реактивы, в тех же количествах и последовательности, как и при минерализации пробы, но вместо пробы приливают адекватное количество дистиллированной воды.
4.3. Подготовка прибора для отгонки и поглощения мышьяка
Прибор собирают в соответствии с рисунком. Прибор состоит из реакционной (отгонной) колбы вместимостью 150 мл, соединительной трубки со шлифом 24/29 и капилляром на одном конце, доходящим до дна отгонной колбы, а на другом конце имеется каплеуловитель и воронка с притертым краном. Каплеуловитель соединяется с холодильником. Колба-приемник и колба-ловушка соединяются между собой и холодильником. Перед использованием прибор следует промыть азотной кислотой (1:1), затем тщательно промыть водой.
4.4. Приготовление молибденовокислого аммония
4.4.1. Для перекристаллизации молибденовокислого аммония берут 200 г последнего и тщательно взбалтывают с 300 мл бидистиллированной воды, нагретой до 70Ц80C. Нерастворившийся осадок отфильтровывают и отбрасывают. К фильтрату добавляют 1/3 по объему абсолютного этилового спирта. Выпавший мелкокристаллический осадок отфильтровывают на воронке Бюхнера, промывая 5Ц6 раз по 80Ц100 мл абсолютного этилового спирта, и высушивают в эксикаторе.
4.4.2. Растворяют 1 г перекристаллизованного молибдата аммония, не содержащего фосфора, в 45 мл теплой 6 н. серной кислоты. После охлаждения раствора объём доводят до 100 мл 6 н. серной кислотой. Раствор хранят в плотно закрытой посуде (устойчив в течение месяца).
4.5. Приготовление основного раствора мышьяка
Основной раствор мышьяка готовят одним из способов:
а) используют стандарт-титр или берут навеску 0,264 г мышьяковистого ангидрида (As2O3) растворяют в 10 мл 10%-ного раствора едкого натра с последующей нейтрализацией серной кислоты (1:1) и после этого раствор количественно переносят в мерную колбу на 1000 мл, куда добавляют 10 мл концентрированной серной кислоты и доводят объем до метки дистиллированной водой; в 1 мл основного раствора содержится 20 мкг мышьяка;
б) используют стандарт-титр или берут навеску 0,8320 г двузамещенного мышьяковистого натрия (Na2HAsO4), вносят в мерную колбу вместимостью 1000 мл и доводят дистиллированной водой до метки; полученный раствор содержит 200 мкг мышьяка в 1 мл.
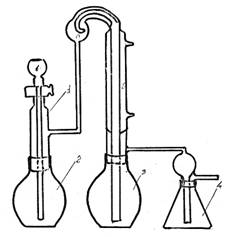
Рис. 1. Прибор для отгонки и поглощения мышьяка
1 - капельная воронка с каплеуловителем (а) и холодильником (б);
2 - отгонная колба; 3 - колба-приемник; 4 - колба-ловушка
4.6. Приготовление рабочего раствора мышьяка
Непосредственно перед определением мышьяка берут 2,5 мл основного раствора мышьяка, помещают в мерную колбу на 250 мл и доводят до метки дистиллированной водой. Полученный таким образом раствор содержит в 1 мл 2 мкг мышьяка.
4.7. Приготовление калибровочного раствора мышьяка
4.7.1. В термостойкие стаканчики вместимостью 100 мл из мерной колбы рабочего раствора мышьяка вносят: 0,0; 12,5; 25,0; 37,5 и 50,0 мл и доводят дистиллированной водой до 50 мл. В каждый стаканчик приливают по 10 мл концентрированной азотной кислоты и ставят под тягу в сушильный шкаф при 130C.
4.7.2. После выпаривания в стаканчики приливают по 25 мл дистиллированной воды, нейтрализуют по фенолфталеину 5 н. раствором едкого натра, приливают 1Ц4 капли 0,1 н. раствора йодистого калия, 5 мл 1%-ного раствора молибдата аммония и 2 мл свежеприготовленного 0,15%-ного раствора сульфата гидразина. Стаканчики ставят в сушильный шкаф при 130C на 30 минут или кипятят в течение 3 минут.
4.7.3. После охлаждения раствора содержимое количественно переносят в мерную колбу на 50 мл и доводят до метки дистиллированной водой. В 1 мл содержится соответственно: 0,0 (контроль); 0,5; 1,0; 1,5 и 2,0 мкг мышьяка.
4.7.4. Оптическую плотность раствора измеряют по отношению к контролю на ФЭК при красном светофильтре (690 нм) в кювете с расстояниями между рабочими гранями 10 мм.
4.7.5. Строят градуировочный график, откладывая на оси абсцисс массу мышьяка (в мкг), а на оси ординат - соответствующие значения оптической плотности раствора.
5. Проведение испытания
5.1. В отгонную (реакционную) колбу количественно переносят минерализат из колбы Къельдаля. В колбу-приемник и колбу-ловушку наливают 15 и 10 мл соответственно дистиллированной воды, по 3Ц4 капли перекиси водорода и соединяют с прибором и между собой. Затем присоединяют отгонную колбу к холодильнику и через капельную воронку приливают 5 мл концентрированной соляной кислоты, 5 мл насыщенного раствора сульфата гидразина и закрывают кран капельной воронки, в которую приливают 5 мл 30%-ного раствора бромистого калия.
5.2. Отгонную колбу ставят на нагретую электроплитку с большим накалом и, как только начинается бурное кипение жидкости в отгонной колбе, в последнюю из капельной воронки продувают бромистый калий, затем промывают воронку дистиллированной водой. Отгоняют 2/3 объема жидкости в отгонной колбе.
5.3. Снимают колбу-приемник, колбу-ловушку, затем отгонную колбу снимают с электроплитки. Дистилляты в колбе-приемнике и колбе-ловушке объединяют, приливают 10 мл азотной кислоты и ставят стаканчики на выпаривание, как сказано в пп. 4.7.1 и 4.7.2. Далее испытание проводят согласно пп. 4.7.3. и 4.7.4.
5.4. По полученному значению оптической плотности опытних проб с помощью градуировочного графика находят количество мышьяка.
6. Обработка результатов
6.1. Массовую долю мышьяка (X) в мкг/кг вычисляют по формуле:
![]()
где а - количество мкг мышьяка в пробе, найденное по калибровочному графику; б - количество пробы (в г), взятой для мокрого озоления; 50 - количество раствора в мерной колбе после выпаривания дистиллята (из колбы-приемника и колбы-ловушки); 1000 - перевод мкг в мг и перерасчет на 1 кг пробы дрожжей.
6.2. Вычисления проводят до второго десятичного знака.
6.3. За окончательный вариант принимают среднее арифметическое значение результатов двух параллельных определений. Допустимое расхождение двух параллельных определений при P=0,95 не должно превышать 12,5Ц15,8% по отношению к среднему арифметическому значению (табл. 1Ц2).
Таблица 1
Содержание ртути и кадмия в кормах микробиологического
синтеза БВК и гидролизных групп
№ пп. |
№ партии дрожжей |
Ртуть |
Кадмий |
||||
Корма, мг/кг |
Содержание, мг/кг |
% |
Корма мг/кг |
Содержание, мг/кг |
% |
||
Дрожжи гидролизных и БВК с Кировского БХЗ |
|||||||
1. |
347 (гидр) |
0,1 |
0,190 |
190 |
3 |
16,5 |
550 |
2. |
018 (гидр) |
- |
0,177 |
170 |
- |
22,3 |
743 |
3. |
017 (гидр) |
- |
0,192 |
192 |
- |
23,1 |
770 |
4. |
24,01 (гидр) |
- |
0,165 |
165 |
- |
17,1 |
570 |
5. |
22,01 (гидр) |
- |
0,137 |
137 |
- |
14,9 |
496 |
6. |
020 (БВК) |
- |
0,0233 |
23,3 |
- |
15,7 |
523 |
7. |
021 (БВК) |
- |
0,0275 |
27,5 |
- |
14,9 |
496 |
8. |
212 Дрожжи БВК |
0,015 |
15 |
- |
10,4 |
346 |
|
Дрожжи БВК с Кировского БХЗ |
|||||||
9. |
166 (БВК) |
0,1 |
0,0249 |
24,9 |
3 |
11,7 |
390 |
10. |
166 (БВК) |
- |
0,0247 |
24,7 |
- |
10,9 |
363 |
11. |
167 (БВК) |
- |
0,0241 |
24,1 |
- |
12,8 |
426 |
12. |
167 (БВК) |
- |
0,0239 |
23,9 |
- |
12,7 |
423 |
13. |
122 (БВК) |
- |
0,0211 |
21,1 |
- |
14,9 |
496 |
14. |
122 (БВК) |
- |
0,0225 |
22,5 |
- |
15,6 |
520 |
15. |
165 (БВК) |
- |
0,0194 |
19,4 |
- |
17,4 |
580 |
16. |
165 (БВК) |
- |
0,0189 |
18,9 |
- |
17,0 |
566 |
17. |
93 (БВК) |
- |
0,0257 |
25,7 |
- |
16,9 |
563 |
18. |
93 (БВК) |
- |
0,0239 |
23,9 |
- |
15,7 |
523 |
|
Страницы: | 1 | 2 | 3 | |
 Авторефераты по всем темам >>
Авторефераты по ветеринарии
Авторефераты по всем темам >>
Авторефераты по ветеринарии

 СКАЧАТЬ ОРИГИНАЛ ДОКУМЕНТА
СКАЧАТЬ ОРИГИНАЛ ДОКУМЕНТА