Книга вторая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского
| Вид материала | Книга |
- Книга первая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского, 10010.77kb.
- А. Конан-Дойль новоеоткровени е перевод с английского Йога Рàманантáты, 2314.23kb.
- Copyright Сергей Александровский, перевод с английского Email: navegante[a]rambler, 619.61kb.
- "книга непрестанности осириса " 177, 7373.41kb.
- Н. М. Макарова Перевод с английского и редакция, 4147.65kb.
- Трудового Красного Знамени гупп детская книга, 2911.61kb.
- Трудового Красного Знамени гупп детская книга, 2911.77kb.
- Уайнхолд Б., Уайнхолд Дж. У 67 Освобождение от созависимости / Перевод с английского, 11462.2kb.
- Малиновской Софьи Борисовны Специальность: журналистика Специализация: художественный, 969.08kb.
- Духовные истины в психических явлениях перевод с английского 3-е издание Москва «Философская, 1557.75kb.
Наиболее распространенной причиной интраопе-рационного снижения диуреза являются гемодинамические расстройства — в большинстве случаев это уменьшение ОЦК (гиповолемия), сердечного выброса или среднего АД. Определенную роль играет также перераспределение почечного кровото-ка от коркового вещества к мозговому.
ОЦК быстро снижается в случае, когда объем инфузионной терапии не компенсирует величину
интраоперационнои кровопотери, скрытые потери и секвестрацию жидкости в "третьем пространстве". При олигурии необходимо как можно точнее оценить О ЦК, чтобы своевременно распознать наличие гиповолемии (гл. 29). Увеличение диуреза при объемной нагрузке (т. е. быстрой инфузии 250 мл раствора) служит доказательством гиповолемии. Напротив, олигурия при сопутствующей сердечной недостаточности — показание к применению инотропных средств, вазодилататоров и ди-уретиков. Мониторинг ЦВД или ДЛА показан при сопутствующих заболеваниях сердца и почек, тяжелом поражении печени, а также при массивной кровопотере (гл. 6).
При падении среднего АД ниже границы ауто-регуляции почечного кровотока (80 мм рт. ст.) диурез становится зависимым от величины АД. Этот эффект особенно характерен для больных с сопутствующей артериальной гипертензией, у которых ауторегуляция почечного кровотока настроена на более высокие цифры среднего АД, В таких случаях уменьшение глубины анестезии, быстрая инфузия жидкостей, назначение вазопрессоров позволяют увеличить АД и диурез.
Иногда снижение диуреза наблюдается несмотря на нормальный ОЦК, сердечный выброс и среднее АД. В этих случаях небольшие дозы петлевых диуретиков (фуросемид, 5-10 мг) позволяют нормализовать диурез.
^ Как хирургические манипуляции способны повлиять на диурез?
Помимо пейроэндокринной реакции организма на хирургическую травму, диурез может изменяться под влиянием механических факторов, характерных для некоторых типов операций. Это особенно справедливо для операций на тазовых органах, которые могут осложняться сдавлением мочевого пузыря ранорасширителями, непреднамеренной цистотомией и перевязкой или пересечением одного или обоих мочеточников. Сдавление мочевого
пузыря ранорасширителями в сочетании с положе-х нием Тренделенбурга (опущенный головной конец операционного стола) препятствует опорожнению мочевого пузыря. Чрезмерное сдавление мочевого пузыря часто сопровождается гематури-ей. Если мочевой катетер и система для сбора мочи установлены правильно, а гемодинамические параметры нормальны, то необходимо исключить хирургическое повреждение как причину сниженного диуреза. Попросите хирурга проверить положение ранорасширителей, идентифицировать мочеточники в операционной ране и убедиться в их целостности. Для выявления участка повреждения мочевого пузыря или места пересечения мочеточника в/в вводят метиленовый синий или инди-гокармин — оба красителя выделяются с мочой. Следует отметить, что появление красителя в резервуаре для сбора мочи не исключает перевязки одного из мочеточников. Метиленовый синий и, в гораздо меньшей степени, индигокармин, находясь в крови, могут временно занижать результаты пульсоксиметрии (гл. 6).
Заключение
После проверки мочевого катетера и системы сбора мочи в/в ввели 2 л раствора Рингера с лактатом, 250 мл 5 % раствора альбумина и 10 мг фуросеми-да, но диурез не увеличился. После в/в введения индигокармина был обнаружен проксимальный конец пересеченного левого мочеточника. В операционную пригласили уролога, который восстановил целостность мочеточника.
Избранная литература
Cogan M. G. Fluid and Electrolytes: Physiology and Pathophysiology. Appleton & Lange, 1991.
Rose B. D. Clinical Physiology of Acid-Base and Electrolyte Disorders, 4th ed. McGraw-Hill, 1994.
Schrier R. W. (ed.). Renal and Electrolyte Disorders, 4th ed. Little, Brown, 1992.
32
Анестезия при сопутствующих заболеваниях почек
При заболеваниях почек на основании клинических и лабораторных данных выделяют ряд синдромов: нефротический синдром, острая почечная недостаточность, хроническая почечная недостаточность, нефрит, мочекаменная болезнь, обструкция и инфекция мочевыводяших путей. Планирование анестезии облегчается, если больных группировать не по перечисленным синдромам, а в зависимости от состояния предоперационной функции почек. В настоящей главе обоснованы принципы такого подхода. Физиология почек и влияние анестезии на их функцию рассмотрены в гл. 31.
^ Оценка функции почек
Точная оценка функции почек основана на данных лабораторных исследований (табл. 32-1). Повреждение почек может быть обусловлено дисфункцией клубочков и/или канальцев, а также обструкцией мочевыводящих путей. Поскольку дисфункция клубочков имеет наиболее тяжелые последствия и ее относительно просто выявить, широкое распространение получили лабораторные тесты, позволяющие определить скорость клубочковой фильтрации (СКФ; гл.31).
^ ТАБЛИЦА 32-1. Соотношение между тяжестью дисфункции почек и СКФ
| Клиренс креатинина (мл/мин) |
| Норма 100-120 Снижение почечного резерва 60-100 Легкая дисфункция почек 40-60 Среднетяжелая дисфункция почек 25-40 Почечная недостаточность < 25 Терминальная почечная недостаточность1 < 10 |
| 1 Этот термин используют только у больных с хронической почечной недостаточностью. |
^ Азот мочевины крови
Основным источником мочевины в организме является печень. В ходе катаболизма белков при де-заминировании аминокислот образуется аммиак, накопление которого приводит к интоксикации. Превращение аммиака в мочевину предотвращает этот неблагоприятный эффект:
2NH3 + CO2 - H2N-CO-NH2 + H2O
Концентрация азота мочевины крови (AMK) прямо пропорциональна катаболизму белков и обратно пропорциональна СКФ. Из этого следует, что AMK является достоверным показателем СКФ только при условии, что катаболизм белков в организме нормален и его скорость постоянна. Более того, 40-50 % фильтруемой в клубочках мочевины в норме подвергается пассивной реабсорбции в почечных канальцах; фракция реабсорбируемой мочевины возрастает при гиповолемии. Транспорт мочевины в почках обсуждается в гл, 31.
В норме концентрация AMK составляет 10-20 мг/100 мл (3,6-7,1 ммоль/л; коэффициент пересчета — 0,357). Снижение концентрации AMK наблюдается при голодании и заболеваниях печени, увеличение — при уменьшении СКФ и усилении катаболизма белков. Последнее характерно для гиперкатаболических состояний (травма, сепсис), распада крови в организме (желудочно-кишечное кровотечение, большая гематома), а также при потреблении пищи с высоким содержанием белков. Концентрация AMK > 50 мг/100 мл обычно указывает на нарушение функции почек.
^ Креатинин сыворотки
Креатин — продукт метаболизма мышечной ткани — неферментативным путем превращается в креатинин. Скорость образования креатинина у большинства людей относительно постоянна и зависит от мышечной массы, в среднем составляя
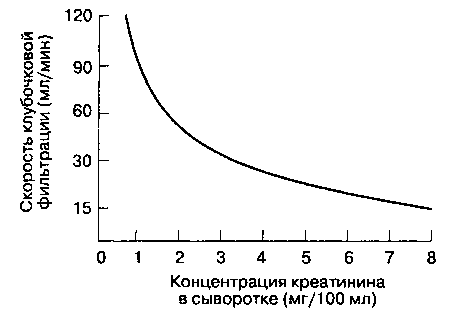
Рис. 32-1. Зависимость между концентрацией креатини-на в сыворотке и скоростью клубочковой фильтрации
20-25 мг/кг/сут у мужчин и 15-20 мг/кг/сут у женщин. В почках креатинин фильтруется (и в незначительной степени секретируется), но не реабсорбируется (гл. 31). Следовательно, концентрация креатинина в сыворотке прямо пропорциональна мышечной массе и обратно пропорциональна СКФ (рис. 32-1), Поскольку мышечная масса постоянна, концентрация креатинина в сыворотке является достоверным показателем СКФ. В норме концентрация креатинина сыворотки равна 0,8-1,3 мг/100 мл у мужчин и 0,6-1,0 мг/100 мл у женщин (соответственно 71-115 мкмоль/л и 53-88 мкмоль/л; коэффициент пересчета — 88,4). Каждое удвоение концентрации креатинина сыворотки соответствует снижению СКФ на 50 % (рис. 32-1). Потребление большого количества мяса, лечение циметидином и повышение уровня ацето-ацетата (например, при кетоацидозе) увеличивают концентрацию креатинина сыворотки в отсутствие изменений СКФ. При потреблении мяса концентрация креатинина сыворотки возрастает. Большинство стандартных лабораторных методик в условиях высокой концентрации ацетоацетата дает завышенные концентрации креатинина. Цимети-дин угнетает секрецию креатинина в почечных канальцах.
СКФ снижается на 5 % каждое десятилетие после достижения человеком 20-летнего возраста, но поскольку мышечная масса тоже уменьшается, концентрация креатинина в сыворотке изменяется незначительно; образование креатинина может уменьшаться до 10 мг/кг. Следовательно, у пожилых больных даже небольшое повышение концентрации креатинина сыворотки свидетельствует о значительном снижении СКФ. Зная возраст и безжировой вес (в кг), СКФ для мужчин рассчитывают по следующей формуле:
Клиренс креатинина =
[(14O- возраст) х безжировой вес]
(72 х креатинин плазмы) ' -
У женщин мышечная масса меньше, поэтому полученную величину необходимо умножить на 0,85.
Концентрация креатинина сыворотки стабилизируется на новом уровне только через 48-72 ч после резкого изменения СКФ.
^ Соотношение АМК/креатинин
Низкая скорость тока канальцевой жидкости в почках способствует реабсорбции мочевины, но не влияет на транспорт креатинина. В результате соотношение АМК/креатинин сыворотки превышает 10:1 (оба параметра выражены в мг/100 мл). Уменьшение скорости тока канальцевой жидкости может быть обусловлено снижением почечной перфузии или обструкцией мочевыводящих путей. Увеличение соотношения АМК/креатинин сыворотки крови свыше 15:1 наблюдается при гиповолемии, отеках, сопровождающихся снижением скорости тока канальцевой жидкости (например, при сердечной недостаточности, циррозе печени, нефротическом синдроме), а также при обструктивных уропатиях. Повышение катаболизма белков также сопровождается увеличением этого соотношения.
^ Клиренс креатинина
Как уже обсуждалось в гл. 31, измерение клиренса креатинина является наиболее достоверным методом клинической оценки почечной функции (точнее — СКФ). Обычно измерения проводят на протяжении 24 ч, однако определение клиренса креатинина в течение 2-х часов является достаточно точным и более удобным для практики. Клиренс креатинина, равный 40-60 мл/мин, соответствует легкой дисфункции почек. Клиренс креатинина от 25 до 40 мл/мин наблюдается при среднетяжелой почечной недостаточности и практически всегда сопровождается появлением у пациента жалоб. Клиренс креатинина меньше 25 мл/мин свидетельствует о явной почечной недостаточности.
При прогрессирующем заболевании почек секреция креатинина в проксимальных канальцах повышается. Следовательно, по мере ухудшения функции почек клиренс креатинина становится все выше и выше, чем истинная СКФ. Более того, на ранней стадии прогрессирующего заболевания почек отмечается относительная сохранность
СКФ, обусловленная компенсаторной гиперфильтрацией в оставшихся интактных нефронах и повышением фильтрационного давления в клубочках. Поэтому необходимо выявлять не только снижение СКФ, но и другие симптомы нарушения почечной функции: артериальную гипертен-зию, протеинурию, а также иные патологические изменения осадка мочи.
^ Анализ мочи
Анализ мочи остается наиболее распространенным тестом, рутинно используемым для оценки почечной функции. Хотя пригодность его для этой цели справедливо оспаривается, анализ мочи может быть полезным для выявления некоторых нарушений функции почечных канальцев, а также ряда внепочечных заболеваний. Стандартный анализ мочи включает измерение рН, удельного веса, присутствия и количественного содержания глюкозы, белка, билирубина, а также микроскопическое исследование осадка. рН мочи имеет значение только при сопоставлении с рН артериальной крови. рН мочи > 7,0 при ацидозе в артериальной крови указывает на почечный канальцевый ацидоз (гл. 30). Удельный вес мочи зависит от ее ос-моляльности; удельный вес 1010 соответствует осмоляльносги 290 мОсм/кг H2O. Удельный вес взятой натощак утренней мочи > 1018 указывает на нормальную концентрационную способность почек. Низкий удельный вес мочи при гиперосмо-ляльности плазмы характерен для несахарного диабета.
Глюкозурия свидетельствует либо о снижении канальцевого порога для глюкозы (в норме 180 мг/100 мл), либо о гипергликемии. Если при обычном анализе мочи выявляется протеинурия, то необходимо определить содержание белка в пробе мочи, собранной за сутки. Клинически значимой считают почечную экскрецию белка > 150 мг/сут. Концентрация билирубина в моче повышается при холестазе.
Микроскопическое исследование осадка мочи позволяет выявить эритроциты, лейкоциты, бактерии, цилиндры и кристаллы. Наличие эритроцитов — признак кровотечения вследствие опухоли, камней, инфекции, коагулопатии или травмы. Присутствие лейкоциюв и бактерий свидетельствует об инфекции. Патологические процессы на уровне нефрона вызывают образование цилиндров (которые представляют собой "слепки" канальцев). Кристаллы в осадке мочи наблюдаются при нарушении обмена щавелевой и мочевой кислот или цистина.
^ Влияние анестезии на организм при нарушении функции почек
Элиминация большинства лекарственных препаратов, применяемых во время анестезии, полностью или частично зависит от почечной экскреции. Нарушение функции почек требует корректировки дозы во избежание накопления (кумуляции) препарата или его активных метаболитов. Кроме того, азотемия потенцирует действие многих лекарственных препаратов. Этот эффект азотемии может быть обусловлен сниженным связыванием препаратов с белками плазмы, повышенной проницаемостью гематоэнце-фалического барьера, а также синергизмом токсинов, накапливающихся при почечной недостаточности.
^ Неингаляционные анестетики и вспомогательные препараты
Барбитураты
Почечная недостаточность не влияет на фармакоки-нетический профиль барбитуратов, но сопутствующая гипоальбуминемия приводит к увеличению свободной фракции препарата, не связанной с белками, этим объясняется повышенная чувствительность пациентов к индукции анестезии барбитуратами при почечной недостаточности. При ацидозе облегчается проникновение барбитуратов в мозг за счет увеличения его неионизированной фракции (гл. 25).
Кетамин
Заболевания почек незначительно влияют на фар-макокинетику кетамина. Некоторые активные продукты печеночного метаболизма кетамина выделяются почками и способны накапливаться при почечной недостаточности. Повышение АД, обусловленное применением кетамина, может быть нежелательным при заболеваниях почек, сопровождающихся артериальной гипертензией.
^ Пропофол и этомидат
Нарушение функции почек не влияет существенно на фармакокинетику пропофола и этомидата. Сниженное связывание этомидата белками плазмы при гипоальбуминемии усиливает его фармакологическое действие.
Бензодиазепины
Прежде чем выделиться с мочой, бензодиазепины подвергаются метаболизму и конъюгации в печени. Большинство бензодиазепинов в значительной
степени связывается с оелками, поэтому при гипо-альбуминемии чувствительность к ним повышается При почечной недостаточности диазепам необходимо применять с осторожностью в связи с риском накопления его активных метаболитов.
Опиоиды
Большинство опиоидов, применяемых в настоящее время в анестезиологической практике (морфин, меперидин, фентанил, суфентанил и альфентанил), инактивируются в печени; после чего некоторые их метаболиты выделяются с мочой. За исключением морфина и меперидина, клинически значимого накопления активных метаболитов при почечной недостаточности не наступает. Накопление метаболитов морфина и меперидина пролонгирует депрессию дыхания у некоторых больных с почечной недостаточностью. Повышенная концентрация нормеперидина (метаболита меперидина) сопряжена с риском возникновения судорог. Фармакоки-нетика наиболее распространенных агонистов-ан-тагонистов опиатных рецепторов (буторфанол, налбуфин, бупренорфин) при почечной недостаточности не изменяется.
Холиноблокаторы
При почечной недостаточности премедикация стандартными дозами атропина или гликопирро-лата считается безопасной. С другой стороны, до 50 % этих препаратов и их активных метаболитов в норме выделяются с мочой, поэтому при повторном введении возникает риск развития кумуляции. Элиминация скополамина в меньшей степени зависит от почечной экскреции, но азотемия может усиливаться его действие на ЦНС.
^ Фенотиазины и блокаторы Н2-рецепторов
Большинство фенотиазинов (например, промета-зин) метаболизируются в печени. Почечная недостаточность слабо влияет на фармакокинетику фенотиазинов, но азотемия может усиливать pix центральный депрессивный эффект. Противо-рвотное действие фенотиазинов особенно полезно для устранения тошноты в предоперационном периоде. Элиминация дроперидола в некоторой степени зависит от почечной экскреции, При использовании дроперидола в больших дозах на фоне почечной недостаточности он может накапливаться, но применение малых доз (< 2,5 мг) представ-чяется вполне безопасным. Элиминация всех антагонистов Н2-рецепторов в значительной степени зависит от почечной экскреции. Метоклоп-рамид частично выделяется с мочой в неизменен-
ной форме и накапливается при почечной недостаточности.
^ Ингаляционные анестетики
Ингаляционные анестетики не выделяются через почки, не имеют заметного прямого влияния на почечный кровоток, а также позволяют легко управлять АД. По этим причинам они считаются идеальными препаратами для использования при дисфункции почек (гл. 31). Легкая и среднетяже-лая дисфункция почек не влияет на поглощение и распределение анестетика, но при глубокой анемии (Hb < 50 г/л) у больных с ХПН может ускоряться индукция анестезии и пробуждение, что объясняют изменением коэффициента распределения кровь/газ, а также снижением МАК (гл. 7). Метоксифлюран — единственный ингаляционный анестетик, применение которого противопоказано из-за образования нефротоксичного метаболита — фторида (гл. 7 и 31). При длительных операциях у больных с сопутствующими заболеваниями почек не рекомендуется использовать также энфлюран и севофлюран, потому что при продолжительном применении концентрация их метаболитов-фторидов может возрасти до нефро-токсичной.
^ Закись азота
При сочетании почечной недостаточности и анемии, многие врачи не используют закись азота или ограничивают ее содержание в дыхательной смеси 50 %, что по их мнению позволяет повысить содержание кислорода в артериальной крови. Этот подход оправдан лишь при глубокой анемии (Hb < 70 г/л), когда даже небольшое увеличение содержания растворенного в крови кислорода оказывает существенное влияние на артериовенозную разницу по кислороду (гл. 22).
Миорелаксанты
Сукцинилхолин
^ Использование сукцинилхолина при почечной недостаточности безопасно, если к моменту индукции анестезии концентрация калия сыворотки не превышает 5 мэкв/л. Если концентрация калия сыво-ротки выше 5Мэкв/л или точно неизвестна, то вместо сукцинилхолина рекомендуется использовать подходящий недеполяризующий миорелаксант. Сообщалось о снижении активности псевдохолин-эстеразы у нескольких больных с уремией после диализа, но клинически значимое увеличение про-
должительности нервно-мышечного блока возникает редко.
^ Атракурий и мивакурий
Продолжительность действия мивакурия практически не зависит от почечной экскреции. Незначительное увеличение продолжительности действия препарата наблюдается при снижении активности псевдохолинэстеразы плазмы. Инактивация атра-курия осуществляется путем ферментативного гидролиза и неферментативной элиминации Хоффмана. Мивакурий и атракурий — это миоре-лаксанты выбора (короткой а средней продолжительного действия соответственно) при почечной недостаточности.
^ Векуроний и рокуроний
Элиминация векурония осуществляется преимущественно печенью, но до 20 % препарата выделяется с мочой. При почечной недостаточности векуроний в больших дозах (> 0,1 мг/кг) умеренно удлиняет продолжительность нервно-мышечной блокады. Рокуроний элиминируется преимущественно печенью, но сообщалось об увеличении длительности его действия при тяжелых заболеваниях почек.
Тубокурарин
Тубокурарин элиминируется как с мочой (40-60 %), так и с желчью. У больных с выраженной дисфункцией почек при многократном введении препарата значительно увеличивается продолжительность его действия. Поэтому при почечной недостаточности необходимо применять меньшие дозы препарата и увеличивать интервалы между введением.
^ Панкуроний, пипекуроний,алкуроний и доксакурий
Элиминация этих препаратов осуществляется преимущественно почками (60-90 %). В ходе печеночного метаболизма панкурония образуются менее активные метаболиты, но период полувыведения препарата зависит в основном от почечной экскреции (на 60-80 %). При назначении этих препаратов больным с нарушенной функцией почек, показан постоянный мониторинг нервно-мышечной проводимости.
^ Метокурин, галламин и декаметоний
Выделяются практически только через почки, поэтому при почечной дисфункции они противопоказаны.
