Крыжановской Инне Илларионовне посвящается Актовая речь на торжественном заседании Ученого Совета Днепропетровской государственной медицинской академии 13 сентября 2001 г. Главная задача
| Вид материала | Задача |
- А. И. На расширенном заседании ученого совета ижевской гсха 22 сентября 2009 года, 587.55kb.
- А. И. Любимова на расширенном заседании ученого совета ижевской гсха 21 сентября 2010, 601.66kb.
- А. А. Минаев на латыни произнес ответ-клятву. После этого ректором В. Рубичком ему, 120.11kb.
- Правовое регулирование отношений между Россией и европейским союзом 12. 00. 10 Международное, 603.25kb.
- Правовое регулирование отношений между Россией и европейским союзом 12. 00. 10 Международное, 605.66kb.
- Брачно-семейные отношения как объект международного частного права российской федерации, 601.92kb.
- В. В. Горбунцов Кафедра дерматовенерологии Днепропетровской государственной медицинской, 68.24kb.
- Автореферат диссертации на соискание ученой степени, 602.44kb.
- Судебные акты в гражданском и арбитражном процессе: теоретические и прикладные проблемы, 783.24kb.
- Повышение готовности персонала миротворческих организаций к регулированию региональных, 629.49kb.
Министерство здравоохранения Украины
Днепропетровская государственная медицинская академия
Член-корреспондент НАН и АМН Украины,
Заслуженный деятель науки,
лауреат Государственной премии Украины,
лауреат премии Правительства Российской Федерации,
профессор Новицкая-Усенко Л.В.
АКТОВАЯ РЕЧЬ
«СТРАТЕГИЯ ВОССТАНОВЛЕНИЯ ЛИЧНОСТИ БОЛЬНЫХ
ПОСЛЕ ПЕРЕНЕСЕННЫХ КРИТИЧЕСКИХ СОСТОЯНИЙ»
Днепропетровск, 2001
85-летию родной Alma Mater –
Днепропетровской государственной медицинской академии
и моему Учителю –
Заслуженному деятелю науки,
Заслуженному работнику высшей школы,
профессору Крыжановской Инне Илларионовне
посвящается
Актовая речь
на торжественном заседании Ученого Совета
Днепропетровской государственной медицинской академии
13 сентября 2001 г.
«Главная задача науки и техники – не рискованное расширение до бесконечности человеческих возможностей и способностей, а тщательная забота о сохранении жизни»
Карел Чапек
Глубокоуважаемый Георгий Викторович!
Глубокоуважаемые члены Ученого Совета, присутствующие!
Позвольте выразить искреннюю благодарность за оказанную мне высокую честь в третий раз выступить с актовой речью в столь знаменательный год – 85-летия со дня основания родной академии и 10-летия независимости Украины и посвятить её родной Alma Mater – Днепропетровской государственной медицинской академии и моему Учителю – Заслуженному деятелю науки, Заслуженному работнику высшей школы, профессору Крыжановской Инне Илларионовне.
Коллектив кафедры анестезиологии и интенсивной терапии рассматривает оказанную честь как высокую оценку его многогранной работы в плане подготовки медицинских и научно-педагогических кадров, научно-исследовательской работы.
За прошедшие годы на кафедре подготовлено 4 доктора и 44 кандидата медицинских наук.
Научно-исследовательская работа была посвящена проблеме изучения патогенеза различных критических состояний и разработке оптимальных вариантов анестезиологического пособия больным всех возрастных групп при различных хирургических вмешательствах и наиболее эффективных программ интенсивной терапии при отдельных экстремальных состояниях.
Кафедра является базой клинических испытаний Государственного фармакологического центра Украины. Научные исследования проводятся в творческом содружестве с учеными нашей академии, прежде всего кафедры анестезиологии, гипербарической и интенсивной терапии ФУВ, лаборатории психофизиологических исследований, ЦНИЛ, а также с российскими учеными. К научной работе привлекаются практические врачи базовых лечебных учреждений – областной клинической больницы им. И.И.Мечникова и областной детской клинической больницы.
По результатам научных исследований кафедры опубликовано 20 монографий. Работа коллектива отмечена премией Правительства Российской Федерации в области науки и техники за создание перфторуглеродных сред для управления жизнедеятельностью клеток, органов и организма (1998 г.) и Государственной премией Украины в области науки и техники за научную разработку и внедрение медицинской системы жизнеобеспечения пострадавших во время техногенных аварий и катастроф (2000 г.), медалями и дипломами ВДНХ СССР и УССР, результаты научных исследований многократно докладывались на Национальных, Европейских и Международных конгрессах, симпозиумах, конференциях, были обобщены и поэтапно изложены в двух актовых речах на торжественных заседаниях Совета академии:
1984 г. – «Механизмы адаптации гомеостаза при различных экстремальных состояниях в условиях анестезиологического обеспечения и интенсивной терапии»;
1994 г. – «Перфторан в медицине» с демонстрацией документального кинофильма «Другая кровь».
Последовательно развивая избранное научное направление, мы наряду с изучением отдельных звеньев патогенеза и поиском адекватных методов интенсивной терапии в остром периоде, поставили задачу выяснить влияние применяемых программ интенсивной терапии на качество жизни больных в отдаленном периоде и разработать систему наиболее полного восстановления личности больных для обеспечения их способности вести активную жизнь в обществе.
Это обусловлено большой актуальностью данной проблемы, имеющей важное не только медицинское, но и социально-экономическое значение.
В последние десятилетия в мире наблюдается неуклонный рост стихийных бедствий, техногенных катастроф, транспортных аварий, военных конфликтов, сопровождающихся массовыми травматическими повреждениями, особенно головного мозга, чаще у лиц трудоспособного возраста.
Нельзя не отметить и возрастающий уровень сердечно-сосудистых заболеваний, а нарушения мозгового кровообращения, острая сердечно-сосудистая недостаточность, всегда ведут к гипоксическому повреждению головного мозга.
Как травматические, так и нетравматические повреждения головного мозга характеризуются высокой летальностью, длительной нетрудоспособностью, инвалидизацией, приводят к утрате жизненного потенциала страны и приносят наибольшие убытки продуктивным силам общества (Україна в цифрах у 1999 р.).
Эта проблема, как отмечено в «Концепции развития здравоохранения Украины», утвержденной Указом Президента Украины 7 декабря 2000 г., и в докладе Министра здравоохранения Украины на итоговой коллегии МЗОУ 12.02.2001 г., имеет особо важное значение для нашего государства в виду сложившейся критической демографической ситуации, неудовлетворительного состояния здоровья населения, высокого уровня первичной инвалидизации взрослого населения (абсолютное число инвалидов в Украине 2,5 млн. человек), что требует новых подходов к лечению, в т.ч. и критических состояний, направленных как на снижение летальности, так и на профилактику инвалидизации и обеспечение более полного восстановления здоровья больных и пострадавших с возможностью возвращения их к активному труду.
На протяжении более 20 лет мы ведем поиск наиболее эффективных методов интенсивной терапии в остром периоде травматических и нетравматических повреждений головного мозга, направленных, прежде всего, на его защиту от гипоксии и профилактику постгипоксической энцефалопатии.
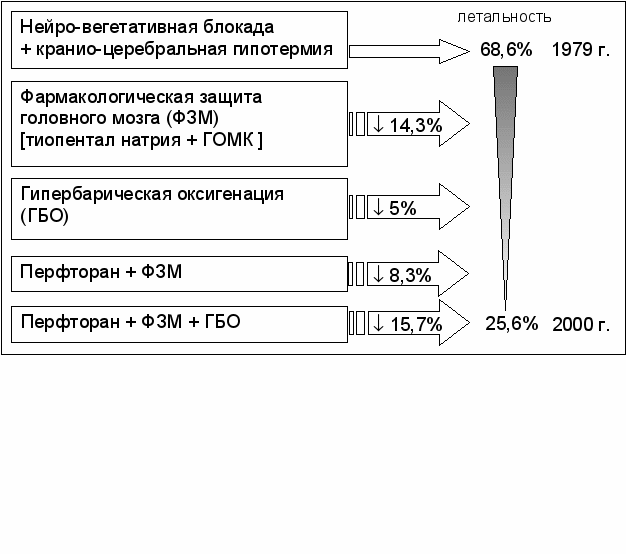
Динамика этих поисков у одной из наиболее тяжелых групп критических больных – с нейротравмой, представлена на рисунке 1.
Как видно, к началу наших исследований, на фоне применения нейровегетативной блокады и краниоцеребральной гипотермии летальность у этой группы больных составляла 68,6%.
Глубокие экспериментальные и клинические исследования, проведенных на кафедре, позволили нам раскрыть новые звенья патогенеза посттравматической и постреанимационной болезни и на этой основе в середине 80-х годов разработать методику ФЗМ, благодаря которой удалось снизить летальность на 14,3%.
Нами была также изучена целесообразность использования в комплексе интенсивной терапии ГБО, разработана технология и определены сроки её применения, что обусловило снижение летальности еще на 5%.
В дальнейшем наше внимание привлек уникальный полифункциональный препарат – кровезаменитель с газотранспортными свойствами – перфторан. Включение его в комплекс интенсивной терапии в остром периоде привело к снижению общей летальности на 8,3%. Внедрение в клиническую практику всего комплекса разработанных нами методик привело к снижению летальности в 2000 г. до 25,6%.
Данные литературы и наши собственные исследования доказали высокую эффективность перфторана в остром периоде критических состояний, сопровождающихся ишемией или гипоксией.
Медицинские препараты на основе перфторорганических соединений (ПФОС) стали активно создаваться к концу ХХ века, когда возникли серьезные проблемы с заготовкой и хранением донорской крови, значительно увеличилась о
пасность её переливания.
^ Рис. 1. Этапы разработки и результаты внедрения
в клиническую практику различных методов защиты
головного мозга от гипоксии.
В США, Японии, Китае, Франции, России и других странах было создано более 10 различных искусственных кровезаменителей с функцией переноса кислорода, среди которых лучшим для использования в клинике оказался перфторан, созданный группой российских ученых под руководством проф. Ф.Ф.Белоярцева в Институте биологической физики АН СССР (дир., чл.-корр. РАН Г.Р.Иваницкий). Именно этот препарат, в отличие от зарубежных, стал изучаться и находить всё большее клиническое применение не только как искусственный кровезаменитель в качестве компонента инфузионно-трансфузионной терапии, но и в комплексе интенсивной терапии различных критических состояний, благодаря своим уникальным многофункциональным свойствам.
Напомню краткие сведения об этом препарате. Он представляет собой 10% субмикронную эмульсию на основе ПФОС с функцией переноса кислорода и углекислоты и оказывает в организме следующее действие:
- улучшает кислородно-транспортную функцию крови;
- увеличивает газообмен и метаболизм на уровне тканей;
- улучшает реологические свойства крови и микроциркуляцию;
- обладает мембраностабилизирующим эффектом, нейро- и кардио-протекторным действием;
- имеет сорбционные и диуретические свойства;
- проявляет противоотечное действие;
- оказывает дозозависимое иммуннопротекторное действие;
- является блокатором медленно входящих кальциевых токов;
- оказывает антиаритмическое действие за счет активации энергетического обмена (В.В.Мороз, Н.И.Афонин, А.Н.Афонин, 2001).
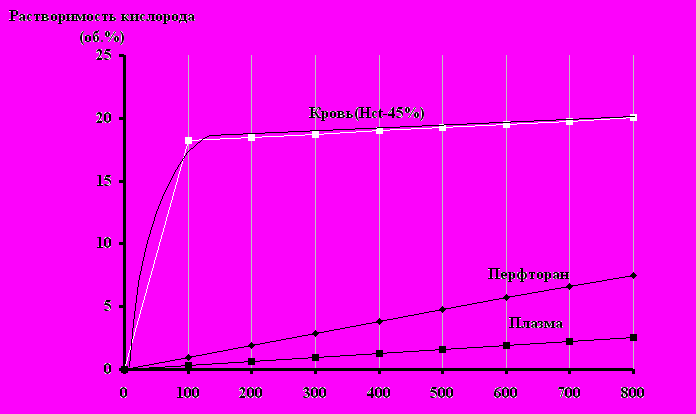
Растворимость кислорода в эмульсии перфторана значительно выше, чем в плазме (рис.2).
 ^ Напряжение кислорода (мм рт.ст.)
^ Напряжение кислорода (мм рт.ст.)Рис.2. Растворимость кислорода в различных средах.
И хотя растворимость кислорода в перфторане меньше, чем в цельной крови, газообмен в тканях существенно возрастает, что обусловлено несколькими механизмами (рис.3).
Главным является захват, транспорт и высвобождение О2 и СО2 частицами эмульсии перфторана, восстановление кислородно-транспортной функции собственных эритроцитов больного, более полное извлечение О2 из эритроцитов, увеличение вымывания СО2 из тканей.
С

убмикронный размер частиц эмульсии перфторана способствует их проникновению даже в те участки сосудистой системы, куда не может проникнуть эритроцит, как за счет своего размера, который в 50-70 раз больше, чем частица эмульсии, так и за счет значительного снижения пластичности вследствие гипоксии самого эритроцита. То есть, при применении перфторана увеличивается полезная площадь капиллярного массообмена, достигается снабжение кислородом тканей с плохим кровообращением.
^ Рис.3. Основные механизмы улучшения газообмена в тканях
при применении перфторана.
Кафедра располагает уникальным клиническим опытом применения перфторана в комплексе интенсивной терапии больных с различными критическими состояниями, который охватывает 258 больных (табл.1).
| ^ Характер патологии | Количество больных |
| Тяжёлая черепно-мозговая травма | 58 |
| Острое нарушение мозгового кровообращения | 6 |
| Постреанимационная болезнь | 37 |
| Политравма | 19 |
| Термические ожоги тела | 48 |
| Желудочно-кишечные кровотечения | 25 |
| Острый инфаркт миокарда | 21 |
| Сепсис | 30 |
| Острое поражение легких различной этиологии | 14 |
| Всего | 258 |
^ Таблица 1. Распределение больных, получавших перфторан
в комплексе интенсивной терапии (1984-1985, 1990-2000 гг.)
К числу критических состояний, вызывающих острую локальную ишемию относятся ишемический или геморрагический инсульты, тяжелая черепно-мозговая травма (ЧМТ). В последнем случае может наблюдаться и генерализация ишемии головного мозга вследствие его отека-набухания. Наиболее выраженная общемозговая ишемия наблюдается при клинической смерти. Менее выраженной, но часто достаточно существенной, является общемозговая ишемия вследствие циркуляторной недостаточности при острой патологии сердечно-сосудистой системы, например, при остром инфаркте миокарда (ОИМ). Нарушение системной гемодинамики в этом случае сопровождается нарушением кровоснабжения головного мозга в связи с сердечной недостаточностью вследствие уменьшения сердечного выброса.
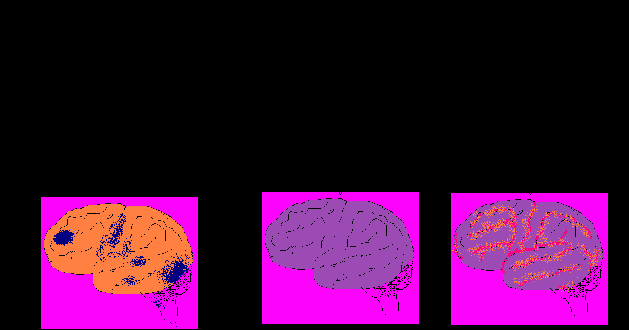
В настоящей актовой речи я хочу раскрыть один из фрагментов нашей многолетней работы, касающийся наиболее тяжёлой группы критических больных с локальной или общей ишемией головного мозга (рис.4).
Всем группам больных перфторан вводился согласно разработанной нами технологии: внутривенно капельно в первые 6-8 часов критического состояния со скоростью 30-60 капель/мин в дозе 3-6 мл/кг массы тела.
Нами впервые в мировой практике перфторан был применен у больных с нейротравмой.
Следует сказать, что в общей структуре травматизма повреждения ЦНС составляют 30-50%. В Украине ежегодно только от дорожно-транспортных происшествий (а они составляют 20-30% от общего числа всех травм) страдает более 50 тыс. человек и 10 тыс. из них умирают.
Н
ами в эксперименте на животных установлено противоотечное действие перфторана на головной мозг благодаря уменьшению отека глиальных клеток, уменьшению проницаемости гематоэнцефалического барьера, восстановлению мозговой гемо- и ликвородинамики; выявлен антистрессорный эффект за счет нормализации адрено-кортикальной функции гипофиза при одновременном снижении уровня кортизола, а также уравновешивания соотношения неспецифической сресс-реализующей гистаминореактивной и стресс-лимитирующей серотонинэргической систем, что отражено на диаграмме (рис.5).
Рис.4. Варианты ишемии головного мозга.
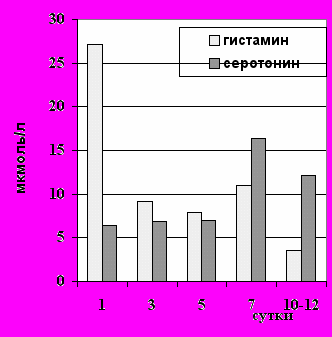
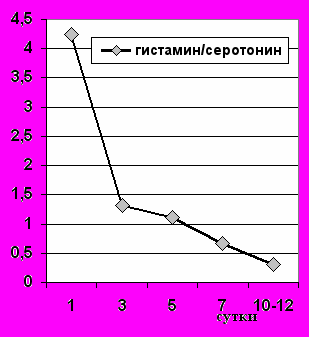
Рис.5. Показатели гистамина, серотонина и их соотношение
у больных с ЧМТ при использовании перфторана.
Преобладание физиологических эффектов серотонина на фоне улучшения газового состава крови, нормализации КЩС, центральной и периферической гемодинамики обеспечивало ускоренное восстановление утраченных в ходе травмы функций головного мозга, что обусловило улучшение параметров ЭЭГ. Так, уже к 3-м суткам после введения перфторана уменьшалось количество медленных σ-волн с 40,4% до 34,1% и увеличивалось число α-волн с 12,7% до21,7%. Под его влиянием формировался специфический характер восстановления сознания. Мы выделили 3 его варианта:
стремительный – отличается быстрым восстановлением сознания (за 20-30 мин) после введения перфторана. Для этих больных характерна ретроградная амнезия на фоне полного и качественного восстановления процессов мышления;
плавный – восстановление сознания происходит в течение 3-5 суток после введения перфторана при достаточно качественном восстановлении процессов мышления;
замедленный, когда коматозное состояние продолжается 10-14 суток с момента введения препарата, что имеет место в тех случаях, когда перфторан вводился больным через 3-4 суток после травмы. Психические функции при этом восстанавливаются с необратимыми неврологическими дефицитами.
Кроме того, нами выявлены стабилизация тромбоцитарного гемостаза, улучшение реологических свойств крови на фоне адекватного кислородного статуса, приведшие к получению следующего клинического эффекта:
- уменьшение глубины коматозного состояния у 61,2% больных,
- сокращение продолжительности комы на 2 суток,
- снижение летальности на 8,3%.
Одной из актуальных проблем современной медицины остается профилактика и лечение постгипоксической энцефалопатии после перенесенной клинической смерти.
Мне приятно отметить, что к этой проблеме внимание ученых нашей академии было приковано еще на заре развития реаниматологии, как науки.
В 1954 г. проф. Д.А.Василенко – заведующий кафедрой общей хирургии нашего медицинского института произнес актовую речь на тему: «Клиническая смерть – как обратимый процесс», в которой отметил актуальность этой темы, обобщил достижения отечественных ученых к тому времени, подчеркнул активную роль проф. В.А.Неговского в разработке комплексных мероприятий по борьбе с клинической смертью и подчеркнул перспективы развития этого направления медицины.
Ежегодно в мире регистрируется более 200 тыс. больных, которым проводилась сердечно-легочная реанимация. При этом выживает около 70 тыс. (30%), но только 10% из выживших способны возвратиться к прежнему образу жизни (В.В.Спас, 1987; А.Н.Коргин, И.Б.Холодов, 1988) в связи с наличием у них после выписки из стационара психо-неврологических нарушений различной степени выраженности. Проф. Алексеева Г.В. (1998) из НИИОР РАМН (дир., чл.-корр. РАМН В.В.Мороз) через 1 год у 70% выживших после клинической смерти отмечала серьезные неврологические расстройства и 50% из этих больных были инвалидами.
Поэтому, как указывал известный американский ученый П.Сафар (1997), - «Главной целью наших совместных усилий должно быть восстановление функций не только сердечно-сосудистой системы и дыхания, но и человеческого мышления. Вернувшиеся с берегов Леты должны иметь возможность вновь влиться в общество».
В настоящее время в эксперименте и в клинике обоснованно положительное влияние на течение постгипоксической энцефалопатии различных фармакологических препаратов, но нет единой терапевтической тактики, которая могла бы максимально устранить последствия глобальной ишемии мозга.
О
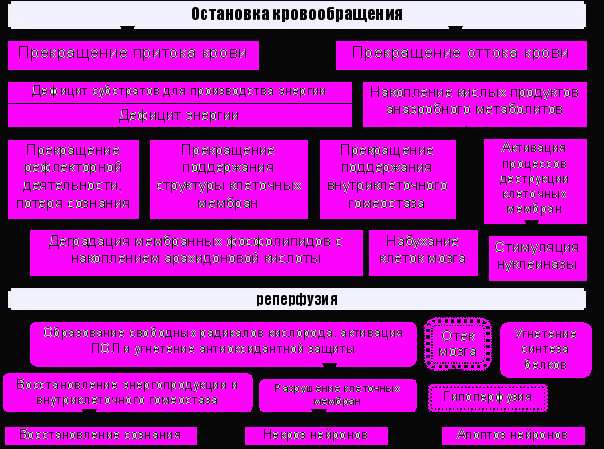
снованием для включения перфторана в комплекс интенсивной терапии этой группы больных послужил анализ патогенеза постреанимационной энцефалопатии, ключевую роль в котором играют ишемически-реперфузионные повреждения головного мозга (рис.6).
^ Рис. 6. Схема патогенеза постгипоксической энцефалопатии.
Как видно, на этапе ишемии тканей нарушаются все энергозависимые процессы – от выполнения специфических функций клетки в организме до поддержания структуры клеточных мембран и внутриклеточного гомеостаза. В то же время в клетках накапливаются продукты анаэробного метаболизма и деградации мембранных фосфолипидов. В период реперфузии происходит активация перекисного окисления липидов, что вызывает развитие реперфузионного синдрома со вторичной гипоперфузией тканей.
ПФОС способны блокировать одновременно несколько патогенетических звеньев, прямо или косвенно предупреждая как раннюю, так и отсроченную гибель нейронов (рис.7).
Всем больным перфторан вводился на фоне проведения стандартных реанимационных мероприятий.
Р
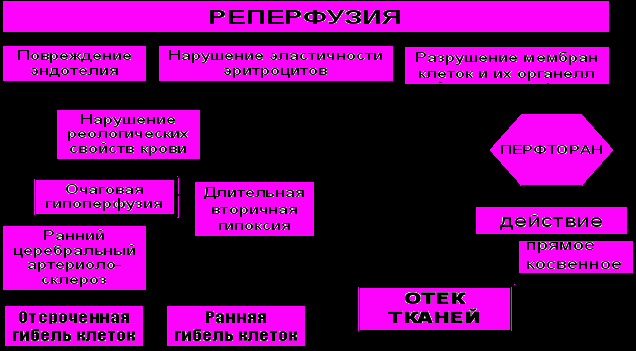
ис.7. Защита нейронов перфтораном при реперфузии.
Нами установлено уже при оценке динамики клинического индекса тяжести статуса (КИТС), что состояние больных, получавших перфторан, имело более выраженную тенденцию к нормализации, чем в контрольной группе и на 5-7 сутки этот показатель указывал на отсутствие энергодефицитных, а тем более структурнодефицитных нарушений, что мы расценили, как следствие многостороннего действия перфторана на различные органы и системы (рис.8).
Показательной была разница и в уровне трансаминаз в основной и контрольной группах (табл.2).
Ряд авторов (А.Т.Бурбелло с соавт., 1988; И.А.Иванова, Ю.Г.Бобков, 1988) увеличение их содержания в крови после клинической смерти связывают с разрушением мембран клеток головного мозга и считают, что это косвенно свидетельствует о глубине ишемического поражения нейронов, как клеток наиболее уязвимых в условиях ишемии.
У больных, получавших перфторан, наблюдалось плавное от этапа к этапу снижение уровня АлТ в отличие от контрольной группы.
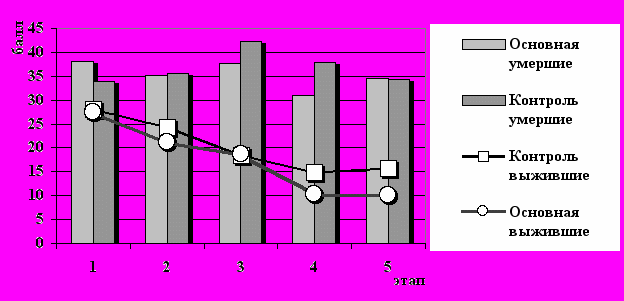
^ Рис.8. Динамика КИТС в раннем постреанимационном периоде
в основной и контрольной группах.
| Подгруппа | Этап | |||||
| 1 | 2 | 3 | 4 | 5 | ||
| Выжившие | Основная | 0,84±0,19 | 0,87±0,19 | 0,99±0,31 | 0,83±0,27 | 0,46±0,07 |
| Контрольная | 0,84±0,25 | 1,02±0,20 | 1,10±0,17 | 1,07±0,31 | 1,09±0,20 | |
| Разница между группами | ±0 | -0,33** | -0,11** | -0,24 | -0,63** | |
| Умершие | Основная | 0,88±0,28 | 0,90±0,02 | 0,78±0,14 | 0,61±0,14 | 0,50±0,21 |
| Контрольная | 0,90±0,24 | 1,31±0,21 | 1,38±0,43 | 1,02±0,23 | 0,78±0,11 | |
| Разница между группами | -0,02 | -0,41* | -0,60* | -0,41* | -0,28 | |
Примечание: * - достоверность разности p<0,05
** - достоверность разности p<0,01 по критерию Уайта
^ Таблица 2. Динамика уровня АлТ в крови у больных
на этапах исследования.
Еще более убедительной оказалась разница в динамике восстановления сознания у обследованных больных, которая носила более линейный характер в основной группе. Ко 2-3 дню постреанимационного периода, то есть тогда, когда обычно отмечается нарастание отека головного мозга, уменьшалась глубина комы. На фоне применения перфторана повышалась граница выживаемости больных (рис.9).
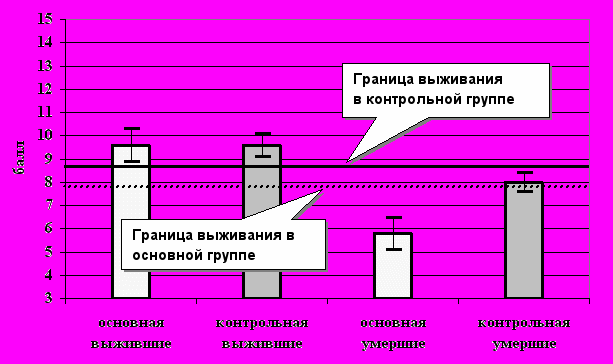
^ Рис.9. Исходные уровни нарушения сознания
в группах исследования и границы выживаемости.
Все выше сказанное дало возможность получить следующие результаты:
уменьшение глубины комы ко 2-3 суткам после введения перфторана;
- сокращение длительности коматозного состояния на 2 суток;
- ускорение регресса неврологической симптоматики;
- снижение летальности на 6,9%.
Ухудшение демографической ситуации в Украине в значительной степени обусловлено высокой смертностью от сердечно-сосудистых заболеваний, которая составляет 60,7% в структуре общей смертности (А.Ф.Возианов, 1996; В.Н.Коваленко, 2000). Ежегодно в Украине выявляется 1,5 млн. таких больных, из них 430-450 тыс. умирает. Этот показатель во многом определяется смертностью от ИБС и острого инфаркта миокарда (ОИМ), как одного из наиболее грозных её проявлений, Европейской статистикой отмечено, что именно в нашей стране смертность от ОИМ гораздо выше, чем в других странах Европы (S.Sans, H.Kromhout, 1997) и составляет 19,3 на 100 тыс. населения.
Б

азовую терапию ОИМ мы дополнили введением перфторана, исходя из механизмов его возможного действия (рис.10).
^ Рис.10. Механизмы возможного действия перфторана
при остром инфаркте миокарда.
Нами установлено, что уже в 1-е сутки после его введения нормализуются показатели газового состава крови и КЩС при одновременном увеличении экстракции кислорода и индекса его сосудисто-тканевого транспорта (рис.11).
Это обеспечивало баланс между потреблением кислорода и его доставкой, что приводило к уменьшению ишемии в периинфарктрой зоне, сохранению большего количества кардиомиоцитов, способных к активному сокращению. Этим можно объяснить почему клиническое течение ОИМ при использовании перфторана сопровождается уменьшением количества рецидивов и интенсивности болевого синдрома, начиная со 2-х суток (рис.12).
Уменьшались и проявления недостаточности кровообращения. Отмечено более раннее (на 2-е сутки) формирование ЭКГ-признаков подострой стадии инфаркта, увеличение объема сохраненного миокарда по сравнению с контрольной группой, что способствует более полному восстановлению функции миокарда левого желудочка (табл.3).
Р
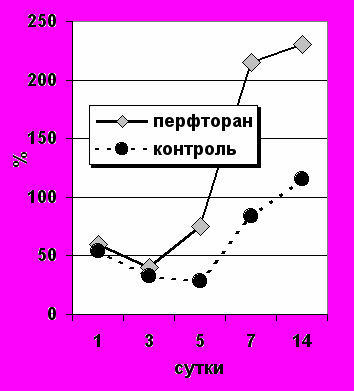
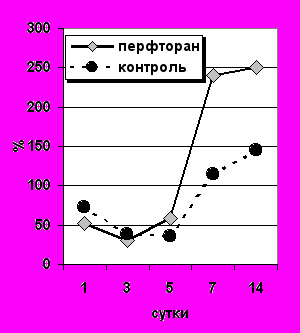
ис.11. Динамика показателей экстракции кислорода (слева) и индекса сосудисто-тканевого транспорта у больных острым инфарктом миокарда.
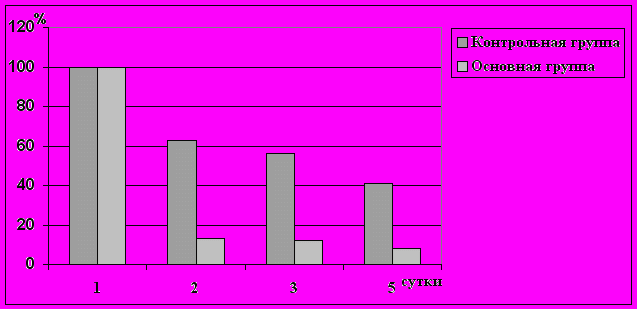
^ Рис.12. Частота рецидивов болевого синдрома (%) у больных с ОИМ
при различных вариантах интенсивной терапии.
| ^ Группы больных | Объем первичного повреждения миокарда (1-е сутки), % | Объем фактического некроза миокарда (10-е сутки), % | Объем сохраненного миокарда, % от первичного повреждения |
| Контрольная | 20,19±2,88 | 18,86±3,39 | 6,60±2,31 |
| Основная | 24,10±3,12 | 12,07±3,09 | 15,06±5,40 |
^ Таблица 3. Влияние перфторана на величину зоны некроза миокарда
у больных острым инфарктом миокарда.
Восстановление до физиологического уровня показателей симпатоадреналовой системы в первые сутки после применения перфторана и более благоприятное соотношение между её звеньями в последующем сопровождалось более быстрой нормализацией состояния гистаминореактивной и серотонинэргической систем с улучшением микроциркуляции и уменьшением тканевой гипоксии, чем и предупреждается расширение зоны некроза.
На фоне лечения перфтораном отмечено поэтапное уменьшение повреждающего действия процессов перекисного окисления липидов (ПОЛ) и компенсаторное повышение активности антиоксидантной системы, достигающей нормы к 5-м суткам заболевания.
Исследования функционального состояния левого желудочка выявили уменьшение глубины нарушений его систолической и диастолической функций, вследствие более полного сохранения миокарда в случаях применения перфторана, что способствует большей сохранности функций и ЦНС.
Таким образом, наши исследования убедительно доказали, что включение перфторана в комплекс интенсивной терапии в остром периоде позволяет значительно улучшить результаты лечения и исходы у данной категории критических больных.
Вместе с тем, как было отмечено выше, острые травматические и нетравматические повреждения головного мозга, вызывающие его локальную или общую ишемию, в посткритическом периоде характеризуются серьезными психо-неврологическими нарушениями.
Так, например, социальный портрет пострадавших, перенесших тяжелую ЧМТ, показывает, что:
- не участвуют в общественно-полезном труде – 18-38,8%
- вынуждены менять профессию или переходить на другую работу – 30-50%
- имеют стойкие нервно-психические последствия – 60-90%,
- что наносит высокий экономический ущерб и сопровождается низким качеством жизни больных (В.В.Лебедев, Л.Д.Быковников, 1987).
Это побудило нас к изучению влияния различных видов интенсивной терапии в остром периоде на качество жизни больных в отдаленном периоде.
При этом под качеством жизни понимают способность индивидуума функционировать в обществе соответственно своему положению и получать удовлетворение от жизни.
Наряду с оценкой физических функций по клинико-лабораторным показателям, оно включает в себя анализ активности в повседневной жизни, работоспособность, способность выполнять социальную роль и интеллектуальные функции, эмоциональную удовлетворенность, а также восприятие общего состояния здоровья, уровня благополучия и удовлетворения жизнью после перенесенного заболевания.
Для этого мы обследовали 77 больных в сроки от 1 до 4 лет и более после перенесенного критического состояния (табл.4).
Оценка степени психоневрологического восстановления производилась на основании опросника Ч.Д.Спилбергера, методики УНП (уровень невротизации-психопатизации), разработанной институтом им. В.М.Бехтерева и шкалы САН (самочувствие, активность, настроение).
| Заболевание | Группа | Всего | |
| контрольная | основная | ||
| Тяжелая ЧМТ | 10 | 7 | 17 |
| Постреанимационная болезнь | 15 | 10 | 25 |
| Острый инфаркт миокарда | 17 | 18 | 35 |
| Всего | 42 | 35 | 77 |
^ Таблица 4. Распределение больных по группам
Для оценки качества реадаптации к условиям труда и быта после перенесенного критического состояния мы разработали шкалу физиологической интеллектуальной и социальной реадаптации (ФИСР), выделив несколько её степеней: полная 11-13 баллов, частичная – 4-10 баллов, дезадаптация – 0-3 балла. (табл.5).
| ^ ФИЗИОЛОГИЧЕСКАЯ РЕАДАПТАЦИЯ | |
| Нормальное функционирование всех физиологических систем организма | 3 |
| Временная дисфункция одной из систем с редкими обострениями | 2 |
| Хроническая дисфункция нескольких систем (или частые обострения) | 1 |
| Стойкая дисфункция нескольких систем | 0 |
| ^ ИНТЕЛЛЕКТУАЛЬНАЯ РЕАДАПТАЦИЯ | |
| Интеллектуальные способности не ниже уровня перед травмы | 4 |
| Незначительное снижение интеллектуальных способностей, не нарушеющее способности общения с окружающими и адаптации к условиям жизни | 3 |
| Снижение интеллекта, затрудняющее общение с окружающими, нарушающее воспроизведение имевшихся навыков и выработку новых | 2 |
| Глубокое снижение интеллекта (деменция) | 1 |
| Отсутствие контакта с окружающим миром (апаллический синдром) | 0 |
| ^ СОЦИАЛЬНАЯ РЕАДАПТАЦИЯ | |
| Полное восстановление прежней профессиональной и общественной жизни | 6 |
| Возможность прежней профессиональной деятельности с незначительными ограничениями (нефизического характера) | 5 |
| Возможность работы не по специальности (если прежняя невозможна) | 4 |
| Полное самообслуживание в быту без возможности какой-либо профессиональной деятельности | 3 |
| Частичное самообслуживание в быту | 2 |
| Нуждается в постоянном уходе окружающих | 1 |
| Нуждается в постоянной медицинской помощи в условиях стационара | 0 |
^ Таблица 5. Шкала ФИСР
Физиологическая реадаптация оценивалась по клинико-лабораторным показателям, характеризующим основные жизненно важные системы организма. У больных, перенесших ОИМ, производилось исследование сердечно-сосудистой системы с точки зрения эффективности церебрального кровоснабжения.
Оценка интеллектуальной реадаптации проводилась на основании наличия и качества контакта с больным, выявления факторов, затрудняющих общение с ним (нарушение речи, зрения, слуха).
При оценке социальной реадаптации выяснялась возможность самообслуживания, выполнения прежней или более легкой профессиональной деятельности.
Обследовав больных в отдаленном периоде после лечения традициоными методами интенсивной терапии, мы выявили серьезные нарушения интегративной деятельности головного мозга, значительно ухудшающие качество жизни больных и их социальную активность (табл.6).
| Показатели | Характер изменения |
| Кратковременная память | Снижение на 35-40% |
| Скорость ориентировочно-поисковых движений | Замедление на 45% |
| Внимание | Снижение на 7% |
| Работоспособность | Снижение в 2 раза |
^ Таблица 6. Показатели интегративной деятельности головного мозга
у больных в отдаленном периоде после перенесенной тяжелой ЧМТ.
У этих больных спустя 1-4 года сохраняется выраженная невротизация, достигающая у перенесших клиническую смерть по шкале невротизации-психопатизации –27,15±2,73 балла при уровне невроза, равном –26,05±5,8 балла по данным института им.В.М.Бехтерева.
В то же время во всех трех основных группах больных наблюдался низкий уровень невротизации (+13,50±9,13 балла), соответствующий эмоциональной устойчивости и положительному фону основных переживаний.
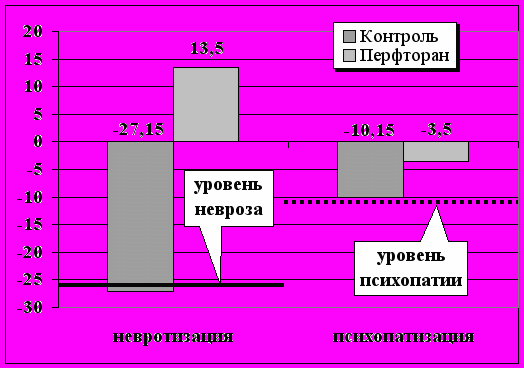
Перенесенная ишемия или гипоксия головного мозга отражалась и на психологическом статусе (рис.13). Как видно на рисунке, в отдаленном периоде даже у самой тяжелой группы больных (ПРБ), получавших в ранние сроки острого периода перфторан, уровень психопатизации был минимальным
(-3,50±1,70 балла) в отличие от контрольной группы (–10,15±1,23 балла), где он приближался к уровню психопатии (–11,2±2,3 балла по данным института им.В.М.Бехтерева).
Аналогичные результаты получены при анализе уровня тревожности по опроснику Ч.Д.Спилбергера. В контрольной группе отмечен высокий уровень тревожности (60,77±0,98 балла), в то время, как в основной он был умеренным (44,88±3,13 балла).
О
ценка качества жизни по шкале САН подтверждает бо́льшую стабильность психоневрологического статуса в группах больных, получавших перфторан (рис.14). Как видим, у них лучше самочувствие, выше активность, стабильнее настроение.
^ Рис.13. Качество жизни в отдаленном периоде после перенесенной клинической смерти при применении перфторана.
Сокращение у этих больных продолжительности и уменьшение глубины комы в остром периоде заметно улучшало состояние больных в отдаленном периоде. В то время, как 30% больных, перенесших ЧМТ и получивших традиционную терапию в первые 2-3 года после травмы отмечали нарушение жизненного стереотипа и невозможность работать, среди больных, получавших перфторан, частичная трудовая адаптация отмечена только у 2-х больных.
У кардиологических больных, кроме психоневрологических отклонений, связанных с острым периодом мозговой гипоксии во время циркуляторной недостаточности, на качество жизни в отдаленном периоде существенное влияние оказывает и состояние сердечно-сосудистой системы. Повторяющиеся периоды сердечно-сосудистой недостаточности ухудшают условия мозгового метаболизма, а сами приступы коронарной недостаточности сопровождаются выраженным чувством страха и беспокойства, что способствует дополнительной невротизации больных.
Р
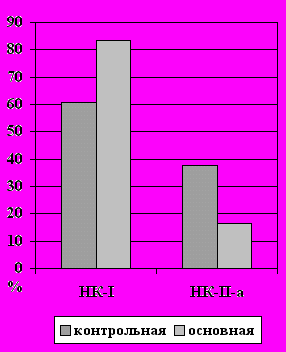
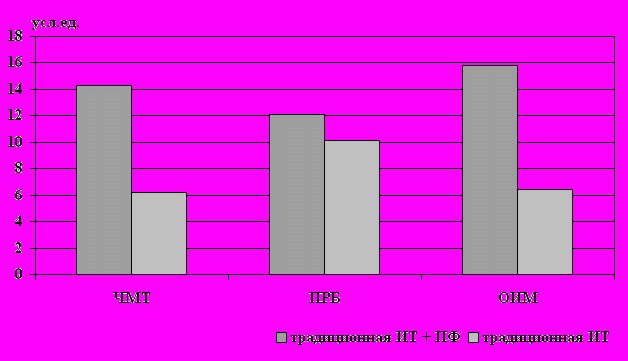
ис.14. Оценка качества жизни у обследованных больных
по шкале САН.
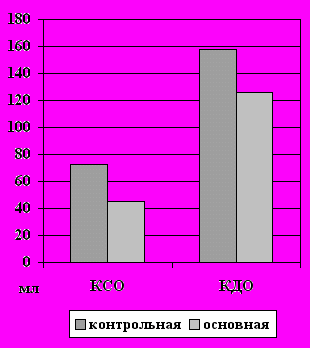
Рис.15. Выраженность сердечной недостаточности в отдаленном периоде инфаркта миокарда у больных основной и контрольной групп.
Инфузия перфторана улучшает не только мозговой метаболизм, но и миоардиальный, что в ближайшем периоде, как было отмечено выше, приводит к увеличению объема сохраненного миокарда, а в отдаленном проявляется уменьшением выраженности сердечной недостаточности вследствие энергетически более выгодной компенсации работы левого желудочка за счет гипертрофии интактного миокарда с уменьшением конечного систолического (КСО) и диастолического (КДО) объемов (рис.15).
Разница выраженности клинических признаков недостаточности кровообращения в обеих группах представлена в таблице 7.
| Признаки | Группы | |
| Контрольная | Основная | |
| Одышка при физической нагрузке | 100 | 94,4 |
| Одышка в покое | 17,8 | 5,6 |
| Приступы удушья в ночное время | 2,2 | – |
| Влажные хрипы в легких | 17,8 | 11,1 |
| ЧСС > 100 ударов в мин | 6,7 | – |
| Набухание шейных вен | 4,4 | – |
| Увеличение печени | 17,8 | 11,1 |
^ Таблица 7. Выраженность клинических признаков недостаточности кровообращения в отдаленном периоде после перенесенного ОИМ (в %).
Этим обусловлено возвращение к трудовой деятельности 16 из 18 больных основной группы и только 10 из 17 больных контрольной.
Совместно с сотрудниками психофизиологической лаборатории мы в отдаленные сроки провели психофизиологическое и психологическое исследование 22 больных, перенесших травматические или ишемические поражения головного мозга, и попытались составить обобщенный психологический портрет.
Больные, получавшие перфторан, не воспринимают прошлое как трагическое, настоящая жизнь им кажется управляемой и интересной, происходящие события и жизненные ситуации они воспринимают оптимистично, а себя как сильных людей, способных свободно принимать решения и их реализовывать. Выражена направленность на будущее, процесс жизни они оценивают как наполненный и результативный. Психологический возраст этих больных моложе биологического.
Больные контрольной группы характеризуются эмоциональной нестабильностью с пессимистическим настроением, прошлую жизнь воспринимают как неудавшуюся, настоящая жизнь им кажется неинтересной и неуправляемой, они не верят в собственные силы, с тревогой относятся к будущему, их цели не определены. Психологический возраст этих больных старше биологического.
Таким образом, при всех видах ишемического поражения головного мозга в большей или меньшей степени в отдаленном периоде обнаруживаются нарушения социально-психологического статуса, функций первично пораженных органов (например, сердца), в свою очередь ухудшающих условия функционирования ЦНС, что сказывается на качестве личной и социальной жизни больных.
Выбор варианта интенсивной терапии в остром периоде оказывает достоверное влияние на качество жизни даже спустя несколько лет после перенесенного критического состояния.
Применение перфторана в ближайшем посткритическом периоде оказывает положительное влияние на выраженность и скорость психоневрологического и интеллектуального восстановления, повышает адаптационные способности к социально-бытовым условиям жизни.
Стремление к более быстрому и полноценному восстановлению функций головного мозга в раннем и отдаленном периодах при ишемических поражениях головного мозга привели сотрудников кафедры к идее использования методов санаторно-курортного лечения. С этой целью нами обследовано 70 больных в возрасте от 17 до 65 лет, которые поступали на курортное лечение в сроки от 1 месяца до 1,5-2 лет после перенесенного эпизода критического состояния.
В санатории местной климатической зоны «Соленый Лиман» больным проводилась бальнео- и пелоидотерапия, в ряде случаев на фоне реабилитационной медикаментозной терапии. Основным лечебным фактором у всех больных явилось грязелечение (табл. 8).
Оптимальным методом грязевого лечения у больных с патологией ЦНС являются грязевые аппликации на воротниковую зону.
Одной из перспективных методик оказалась методика аппликации грязи на переносицу у больных с постгипоксической энцефалопатией уже в ранние сроки лечения, что приводило к более быстрому исчезновению асимметрии мозгового кровотока, улучшению венозного оттока по сравнению с контрольной группой.
| ^ Методы терапии | Количесво больных |
| Грязевая аппликация на воротниковую зону | 29 |
| Гальваногрязь на воротниковую зону | 13 |
| Грязевая аппликация на конечности | 8 |
| Гальваногрязь на конечности | 6 |
| Грязевая аппликация на область переносицы | 14 |
| Массаж | 18 |
| ЛФК | 18 |
| Ванны хвойно-солевые | 9 |
| Ванны йодо-бромистые | 9 |
| Парафиновые аппликации | 4 |
| Электрофорез с NaBr, KJ, лидазой | 5 |
^ Таблица 8. Виды бальнео- и пелоидотерапии,
применявшиеся в обследованных больных.
| ^ Клинические показатели | Больные с посттравматической энцефалопатией (n=54) | Больные с постишемической энцефалопатией (n=16) |
| Улучшение соматического статуса | 53 | 14 |
| Прекращение или уменьшение головной боли, мышечных болей | 27 | 8 |
| Улучшение памяти | 10 | |
| Увеличение объема движений конечностей | 21 | |
| Увеличение мышечной силы в конечностях | 25 | 12 |
| Улучшение походки, уменьшение чувства скованности при ходьбе | 11 | 7 |
| Уменьшение утомляемости при ходьбе | 9 | |
^ Таблица 9. Отдельные клинические показатели после санаторно-курортного лечения больных с постгипоксической энцефалопатией (в %).
При поступлении на санаторно-курортное лечение у 60% больных нами выявлен астено-невротический синдром, проявляющийся вегето-сосудистой дистонией, повышенной утомляемостью, неустойчивостью настроения, головной болью, метеозависимостью.
После проведенного курса лечения с использованием грязи Соленого Лимана улучшалось общее состояние организма (табл. 9).
Н
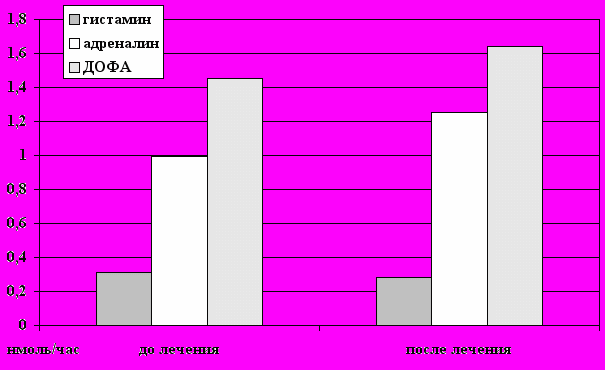
ормализовались основные жизненно важные функции с формированием положительных механизмов адаптации за счет рациональных ответов симпатико-адреналовой, серотонинэргической и гистаминореактивной систем (рис.16).
^ Рис.16. Показатели симпатико-адреналовой и гистаминореактивной систем после санаторно-курортного лечения.
Как видно на диаграмме, снижался уровень гистамина, повышалось содержание экскреторного адреналина, ДОФА, дофамина, что свидетельствовало об увеличении резервов симпато-адреналовой системы. Эти изменения на фоне доминирования серотонинэргической системы над гистаминореактивной приводили к формированию благоприятных адаптационных механизмов и сопровождалось увеличением (до 200%) кровенаполнения сосудов головного мозга в первую очередь за счет уменьшения спазма мозговых сосудов.
Наши исследования дают основание считать, что санаторно-курортное лечение должно быть обязательным компонентом восстановительной терапии больных с постгипоксической энцефалопатией.
Оптимальным является санаторно-курортное лечение в местной климатической зоне через 6 мес.–1,5 года после острого периода при отсутствии противопоказаний.
В современных условиях совершенно недостаточное внимание у этих больных уделяется восстановлению интеллекта. Вместе с тем, в работах отдельных зарубежных авторов указывается на целесообразность уже в раннем реабилитационном периоде использовать индивидуальные психотерапевтические воздействия на эмоции и самочувствие перенесших критические состояния.
Это позволяет уменьшить тревожность, восстановить механизмы волевой регуляции, улучшить эмоциональный фон, повысить коммуникабельность в общении, быстрее восстановить навыки по самообслуживанию, облегчить реадаптацию к бытовым, производственным и социальным условиям жизни. Мы в этом направлении делаем первые, но обнадеживающие шаги.
Проведенные нами многосторонние исследования позволили разработать стратегию восстановления личности больных в посткритическом периоде, включающую 3 основных составляющих программы профилактики и лечения постгипоксической энцефалопатии (рис.17).
Её основу составляют медикаментозные и немедикаментозные методы защиты головного мозга от ишемии, гипоксии и реперфузионного синдрома. Мы считаем, что защита его должна начинаться еще на месте происшествия и активно проводиться в остром периоде заболевания. С первых часов посткритического периода необходимо начинать восстановление функциональной активности нейронов с помощью интеллектуального и психологического тренинга на фоне продолжающейся медикаментозной защиты головного мозга. В случае коматозного состояния больного это может выглядеть как обращенная к больному речь. По мере восстановления психических функций тренинг расширяется, а с подострого периода должны активно включаться лечебная физкультура, эрго- и кинетикотерапия. Дополнение восстановительной терапии санаторно-курортными факторами позволяет еще ближе подойти к более полному восстановлению личности больных, перенесших критическое состояние.
Итогом научной работы нашего коллектива по изложенной в данной актовой речи проблеме явились следующие выводы:
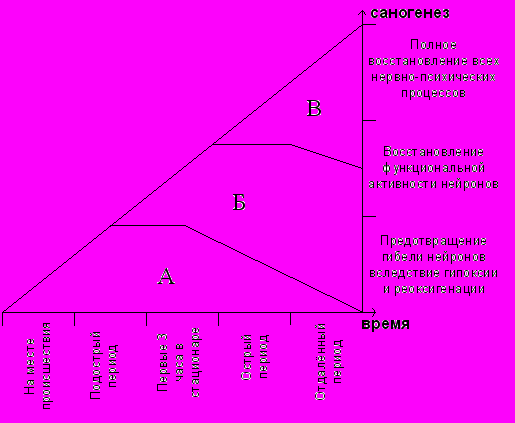
А – медикаментозная и немедикаментозная защита мозга от гипоксии, ишемии и реперфузионного синдрома.
Б – интеллектуальный и психологический тренинг.
В – ЛФК, эрго- и кинетикотерапия, санаторно-курортное лечение
^ Рис.17. Диаграмма стратегии лечения больных
с постгипоксической энцефалопатией.
Острая локальная и общемозговая церебральная ишемия оказывают существенное влияние не только на уровень сознания в остром периоде критического состояния, но и на восстановление трудоспособности и социального статуса в отдаленном периоде.
Выбор варианта интенсивной терапии в первые часы посткритического состояния любой этиологии заметно влияет на скорость и полноту реадаптации больных к социально-бытовым и производственным условиям в отдаленном периоде.
Инфузия перфторана в первые 6-8 часов критического состояния, сопровождающегося ишемией или гипоксией головного мозга, ускоряет выход из комы, повышает выживаемость больных с исходно более тяжелым состоянием.
Включение перфторана в комплекс интенсивной терапии острого периода церебральной ишемии при травматическом или нетравматическом повреждении головного мозга, а также вследствие острой сердечно-сосудистой недостаточности соответствует I классу лечебных мероприятий, которые ведут как к снижению летальности, так и к повышению качества жизни.
Стратегия трехкомпонентного лечения больных с травматическими и ишемическими поражениями головного мозга, включающая последовательное и согласованное применение медикаментозных средств, психотерапевтических методов, интеллектуального тренинга, факторов санаторно-курортного воздействия, ускоряет регресс неврологической симптоматики уже в остром периоде, увеличивает гибкость в формировании адаптационных механизмов с бо́льшей сохранностью структур ЦНС, что способствует снижению инвалидизации, более полному восстановлению личности больных с возвращением их в сферу трудовых ресурсов, к активной жизни в семье и обществе.
В получении максимального результата лечения этой категории больных особую важность приобретает понимание разработанной нами стратегии как непрерывной цепочки взаимодействия многих специальностей, начиная с врачей бригад СМП, врачей анестезиологов-реаниматологов стационара, других специалистов, прежде всего невропатологов, нейрохирургов, кардиологов, физиотерапевтов. В этой цепочке взаимодействия возрастает роль психологов, семейных врачей и социальных работников.
Как отметил проф. Ф.Углов,– «Здоровье – самое большое и неоценимое богатство человека. Оно – источник радости и счастья. Без него не может человек наслаждаться жизнью, не может быть полностью счастливым, все радости тускнеют, жизнь теряет не только свою прелесть, но нередко и смысл».
Вернуть людям радость и смысл жизни, а государству – активных трудоспособных граждан и есть благородная задача нашей врачебной деятельности.
ДЛЯ ЗАМЕТОК:
Патент Российской Федерации, полученный Л.В.Усенко, Е.Н.Клигуненко, Ф.Ф.Белоярцевым и др., 1995.
