Конспект лекций для студентов всех специальностей дневной и заочной формы обучения Челябинск
| Вид материала | Конспект |
- Конспект лекций по курсу Начертательная геометрия (для студентов заочной формы обучения, 1032.28kb.
- Краткий конспект лекций Кемерово 2002 удк: 744 (075), 1231.26kb.
- Конспект лекций по курсу "Начертательная геометрия и инженерная графика" Кемерово 2002, 786.75kb.
- Методические указания по подготовке к семинарским занятиям для студентов дневной формы, 1587.03kb.
- Тематический план, рабочая программа и методические рекомендации к семинарским занятиям, 755.58kb.
- Планы семинарских занятий по дисциплине «Экономическая теория» для студентов технических, 527.66kb.
- Конспект лекций для студентов заочной формы обучения по дисциплине " Организация производства", 16.36kb.
- Методические указания для студентов всех специальностей дневной формы обучения Новосибирск, 320.91kb.
- Тематический план, рабочая программа и методические рекомендации к семинарским занятиям, 755.41kb.
- Методические указания к выполнению задания по черчению для студентов всех специальностей, 589.35kb.
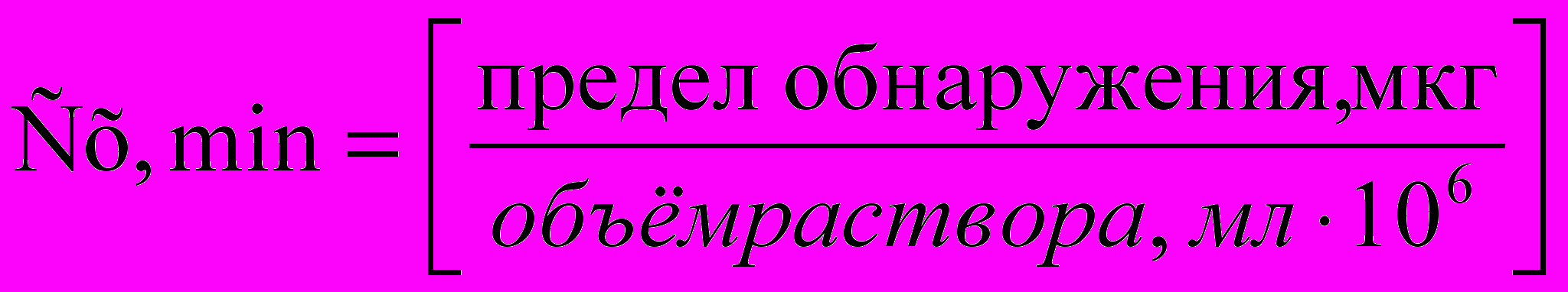
В качественном анализе используют только те реакции, пределы обнаружения которых меньше 50 мкг.
Иногда то или иное вещество можно обнаружить в присутствии других веществ с использованием специфических реакций. Чаще всего мешающие идентификации вещества переводят в осадок, слабодиссоциирующее или комплексное соединение, то есть используют маскирующие или отделяющие реакции.
Количественный анализ
Определение содержания (концентрации, массы и т.п.) компонентов в анализируемом веществе называется количественным анализом. С его помощью выявляют массовые соотношения компонентов в анализируемом образце, концентрацию вещества в растворе или газе. При количественном анализе измеряют те или иные химические, физико-химические и физические параметры анализируемого образца, которые зависят от его состава или содержания того или иного компонента. Результаты анализа обычно выражают в массовых долях, %.
Количественный анализ проводят в определенной последовательности, в которую входят отбор и подготовка проб, проведение анализа, обработка и расчёт результатов анализа. Как и в качественном анализе, различают макро-, полумикро-, микро- и ультрамикрометоды. Количественный анализ широко используют для изучения состава руд, металлов, неорганических и органических соединений. Особое внимание обращается на определение содержания токсичных веществ в воздухе, водоёмах, почвах, продуктах питания, различных товарах.
Аналитический сигнал
Практически все методы анализа основаны на зависимости каких-либо доступных измерению свойств вещества от их состава. Как правило, находят и используют уравнение связи между свойством и составом, разрабатывают способы регистрации количественных характеристик свойства, которые называют аналитическим сигналом. Величину аналитического сигнала переводят в единицы, характеризующие количество или концентрацию компонента. Измеряемыми величинами могут быть масса, объём, светопоглощение, электрический ток и т.д.
Ниже приведены названия методов и измеряемые величины.
| Измеряемая величина (свойство) | Название метода |
| Масса | Гравиметрический Масс-спектрометрический |
| Объём | Титриметрический Газоволюметрический |
| Плотность | Денсиметрический |
| Поглощение или испускание инфракрасных лучей | Инфракрасная спектроскопия |
| Колебания молекул | Комбинационное рассеяние |
| Поглощение или испускание видимых, ультрафиолетовых и рентгеновских лучей. Колебания атомов. Рассеяние света | Спектральный и рентгеноспектральный Фотометрический (колориметрия, спектрофотометрия идр.) Атомно-адсорбционная спектроскопия Люминесцентный анализ |
| Диффузионный ток на электроде | Полярография и вольтамперометрия |
| Электродный потенциал | Потенциометрический |
| Количество электричества | Кулонометрический |
| Электрическая проводимость | Кондуктометрический |
| Радиоактивность | Радиоактивных индикаторов |
| Скорость реакции | Кинетический Каталитический |
| Тепловой эффект реакции | Термометрия и калориметрия |
| Вязкость | Вискозиметрия |
| Поверхностное натяжение | Тензометрия |
| Понижение температуры замерзания | Криоскопия |
| Повышение температуры кипения | Эбуллиоскопия |
| Различная сорбция-десорбция | Хроматографический |
Химический анализ
Все методы количественного анализа делят на химические, физико-химические и физические. Это деление условно. К химическому анализу относятся гравиметрический, титриметрический, комплексонометрическое и окислительно-восстановительное титрование.
Гравиметрический метод. Сущность метода заключается в получении труднорастворимого соединения, в которое входит определяемый компонент. Затем, после отфильтровывания осадка, его высушивают, прокаливают и взвешивают. По массе вещества определяют массу нужного компонента, и проводят расчёт его массовой доли в анализируемой навеске. Имеются разновидности гравиметрического метода. Например, анализируемый компонент выделяют в виде газа, который взаимодействует с реактивом. По изменению массы реактива судят о содержании определяемого компонента в навеске. Например, СО32- + 2Н+ = Н2СО3 = Н2О + СО2, количество выделившегося углекислого газа можно определить по изменению массы вещества, например, СаО, с которым реагирует СО2. Гравиметрический метод трудоёмок и длителен.
Титриметрический анализ. Метод заключается в измерении объёма раствора, израсходованного на реакцию с анализируемым компонентом. Для этих целей используют титрованные растворы, то есть растворы с известной концентрацией – титром раствора. Определение проводят способом титрования, то есть постепенного приливания титрованного раствора к раствору анализируемого вещества, объём которого точно измерен. Титруют до достижения точки эквивалентности. Существует несколько разновидностей анализа: кислотно-основное, осадительное, комплексонометрическое, окислительно-восстановительное титрование.
Инструментальные методы анализа
Инструментальные методы анализа имеют массу достоинств: быстроту, высокую чувствительность, возможность одновременного определения нескольких компонентов, сочетание нескольких методов, автоматизация и использование компьютеров для обработки результатов анализа. Как правило, в инструментальных методах применяют сенсоры (датчики). Инструментальных методов очень много, мы рассмотрим только некоторые из них.
Электрохимические методы: потенциометрический, полярографический, кондуктометрический и др.
Потенциометрический метод основан на измерении электродных потенциалов, которые зависят от активности ионов, а в разбавленных растворах – от их концентрации. В основе лежит уравнение Нернста:
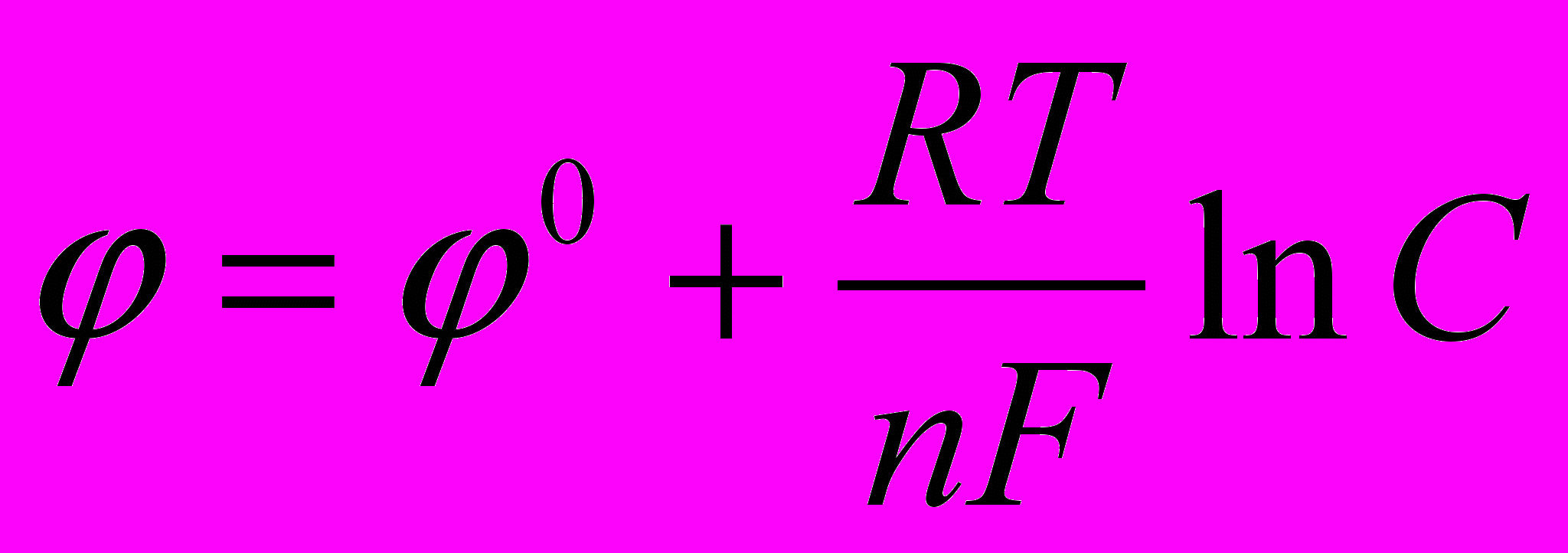 . Измерительная ячейка состоит из измерительного (индикаторного) электрода и электрода сравнения, который не чувствителен к определяемому веществу. Наиболее часто используют ионоселективные электроды, на границах раздела фаз которых протекают ионообменные реакции. Например, для измерения рН ионоселективным является стеклянный электрод. Существуют также ионоселективные электроды для определения концентрации ионов натрия, калия, аммония, хлора, кальция, магния, нитрат-анионов и т.д.
. Измерительная ячейка состоит из измерительного (индикаторного) электрода и электрода сравнения, который не чувствителен к определяемому веществу. Наиболее часто используют ионоселективные электроды, на границах раздела фаз которых протекают ионообменные реакции. Например, для измерения рН ионоселективным является стеклянный электрод. Существуют также ионоселективные электроды для определения концентрации ионов натрия, калия, аммония, хлора, кальция, магния, нитрат-анионов и т.д.Кондуктометрический метод основан на измерении электрической проводимости разбавленных растворов, которая пропорциональна концентрации электролитов. Этим методам, например, определяют общее содержание примесей в воде высокой чистоты.
Хроматографический анализ позволяет разделять двух- и многокомпонентные смеси газов, жидкостей и растворенных веществ методом сорбции в динамических условиях. Основной прибор – хроматограф. Разработано несколько методов, которые классифицируют по механизму процесса и природе частиц – молекулярная, ионообменная, осадительная, распределительная хроматография; и по формам применения – колоночная, капиллярная, тонкослойная и бумажная. Молекулярная хроматография основана на различной адсорбируемости молекул на сорбентах (адсорбентах), ионообменная – на различной способности к обмену ионов раствора. В осадительной хроматографии используют различную растворимость осадков, а в распределительной – различное распределение веществ между двумя несмешивающимися жидкостями. К достоинствам метода следует отнести быстроту и надёжность, возможность определения нескольких компонентов смеси из раствора.
Оптические методы анализа основаны на измерении оптических свойств веществ и излучений, взаимодействии электромагнитного излучения с атомами или молекулами анализируемого вещества, вызывающего излучение, поглощение или отражение лучей. Они включают в себя эмиссионные, люминесцентные и абсорбционные спектральные методы.
Методы, основанные на изучении спектров излучения, называют эмиссионными спектральными методами. В эмиссионной спектроскопии проба вещества нагревается до очень высоких температур (2000-15000 оС). Вещество, испаряясь, диссоциирует на атомы или ионы, которые дают излучение. В спектрографе излучение разлагается на спектр цветных линий. Сравнение этого спектра со справочными данными позволяет определить вид элемента, а интенсивность спектральных линий – его количество. Преимущества этого метода: быстрота выполнения анализа, возможность определения нескольких компонентов из одной навески.
Разновидность эмиссионного анализа – эмиссионная пламенная фотометрия, в которой исследуемый раствор вводят в бесцветное пламя горелки. По изменению цвета пламени определяют вид вещества, а по интенсивности окраски – о его концентрации. Метод выполняют с помощью пламенного фотометра и используют для анализа щелочных, щелочноземельных металлов и магния.
Методы, основанные на свечении анализируемого вещества ультрафиолетовых (фотолюминесценция), рентгеновских (рентгенолюминесценция) и радиоактивных (радиолюминесценция) лучей называют люминесцентными. Люминесцентные методы обладают очень высокой чувствительностью (до 10-10-10-13 г люминесцирующих примесей).
Методы, основанные на изучении спектров поглощения лучей анализируемыми веществами, называют абсорбционно-спектральными. При прохождении света через раствор свет или его компоненты поглощаются или отражаются. По величине поглощения или отражения лучей судят о природе и концентрации вещества. Определение ведут с помощью спектрофотометров или фотоколориметров. Если измеряют поглощение лучей атомами определяемого компонента, которые получают распылением раствора анализируемого вещества в пламени горелки, то метод называют атомно-абсорбционным. Оптический метод, основанный на отражении света твёрдыми частицами, взвешенными в растворе, называется нефелометрией, а прибор, используемый в нём – нефелометром.
Таким образом, использование законов электрохимии, сорбции, эмиссии, поглощения или отражения излучения и взаимодействия частиц с магнитными полями позволило создать большое число инструментальных методов анализа, характеризуемых высокой точностью, чувствительностью, быстротой и надёжностью определения, возможностью анализа многокомпонентных систем.
Заключение
Вопросы, рассмотренные в курсе лекций, позволяют получить современное научное представление о материи, формах ее движения, веществе как одном из видов материи, механизме превращения химических соединений, свойствах технических материалов и применении химических процессов в современной технике. Понимание химических законов помогает инженеру в решении технических проблем. Знание химии необходимо для последующего успешного изучения общенаучных и специальных дисциплин, таких, как сопротивление материалов, материаловедение, основы теплопередачи, электротехника, электроника, энергетика, а также ряда дисциплин, связанных с железнодорожным транспортом.
Знание химии полезно будущему инженеру, так как он будет постоянно сталкиваться с различными веществами и процессами. Научно-технический прогресс вызывает к жизни все новые материалы, новые машины, аппараты и приборы, в которых широко используются достижения химии.
Конспект курса лекций будет полезен при изучении, а также повторении материала в период подготовки к экзамену.
Литература
- Коровин Н.В. Общая химия. – М.: Высшая шк., 2000.
- Зубрев Н.И. Инженерная химия на ж/д транспорте. – М.: 1999
- Жук Н.П. Курс теории коррозии и защиты металлов. – М.:2002
- Глинка Н.Л. Задачи и упражнения по общей химии. – М.:1998
- Глинка Н.Л. Общая химия. – М.: Интеграл-пресс, 2003.
