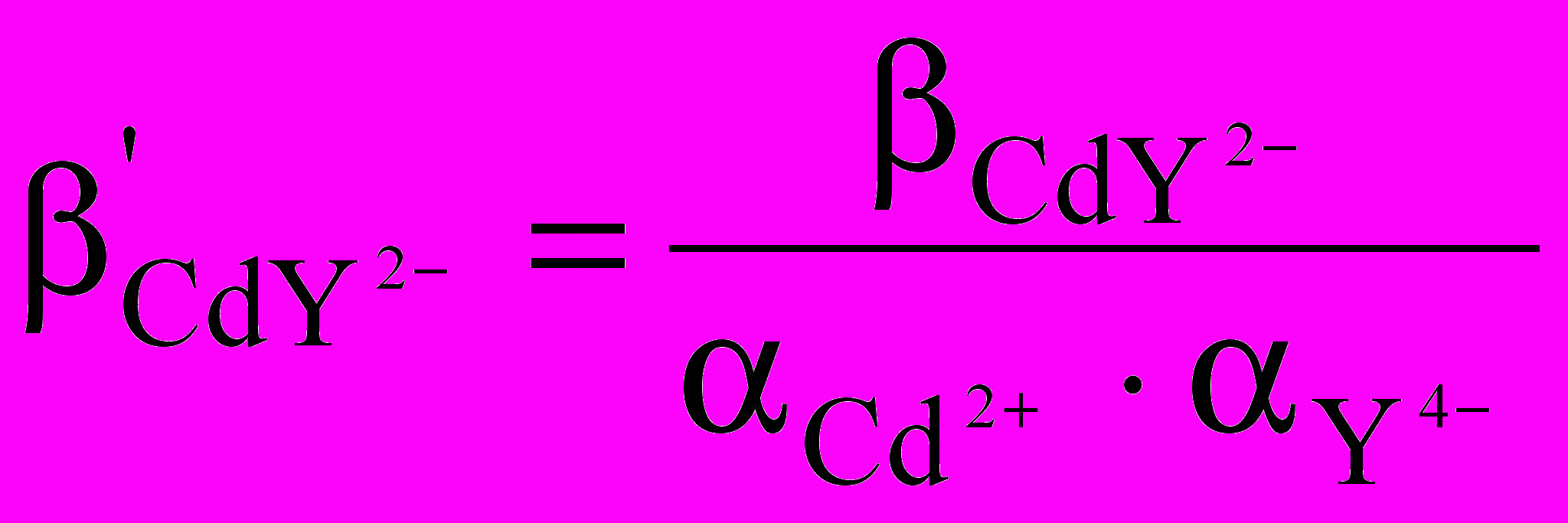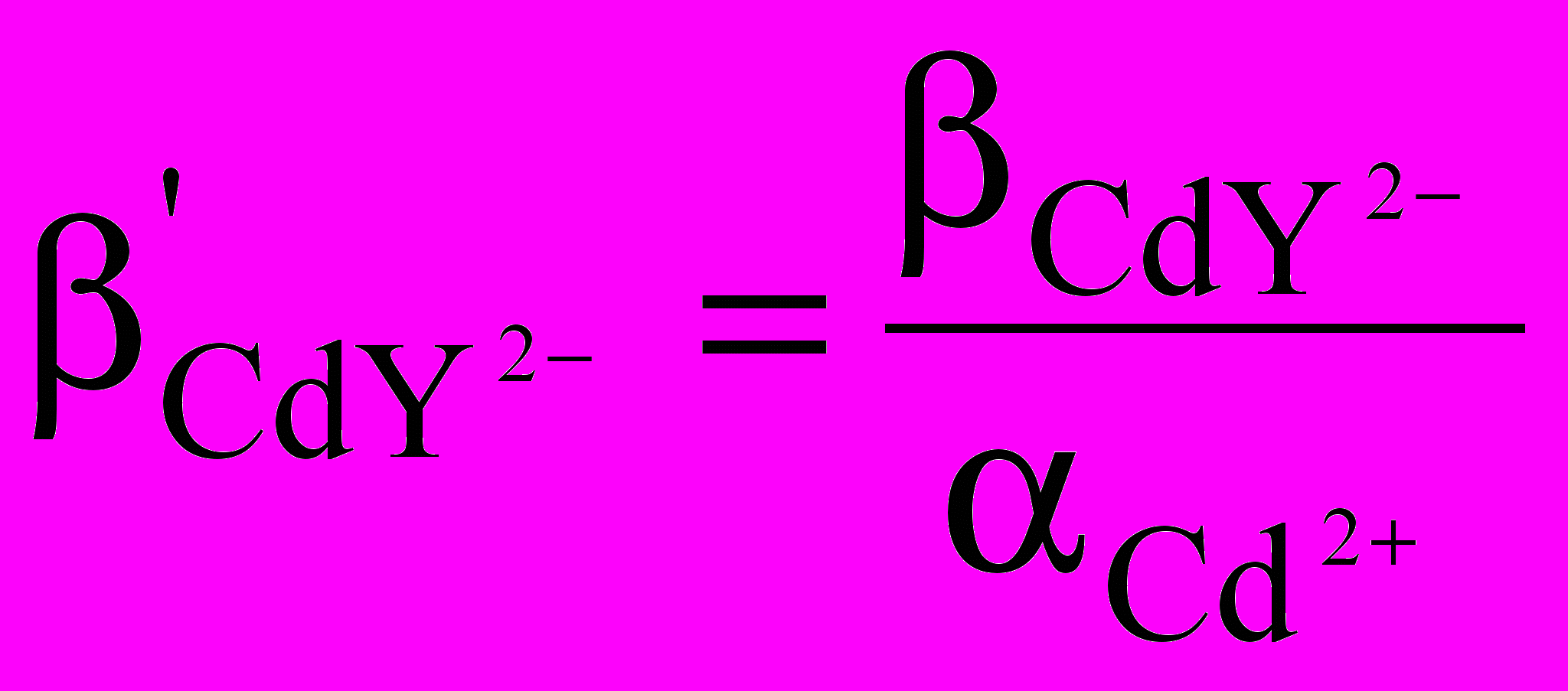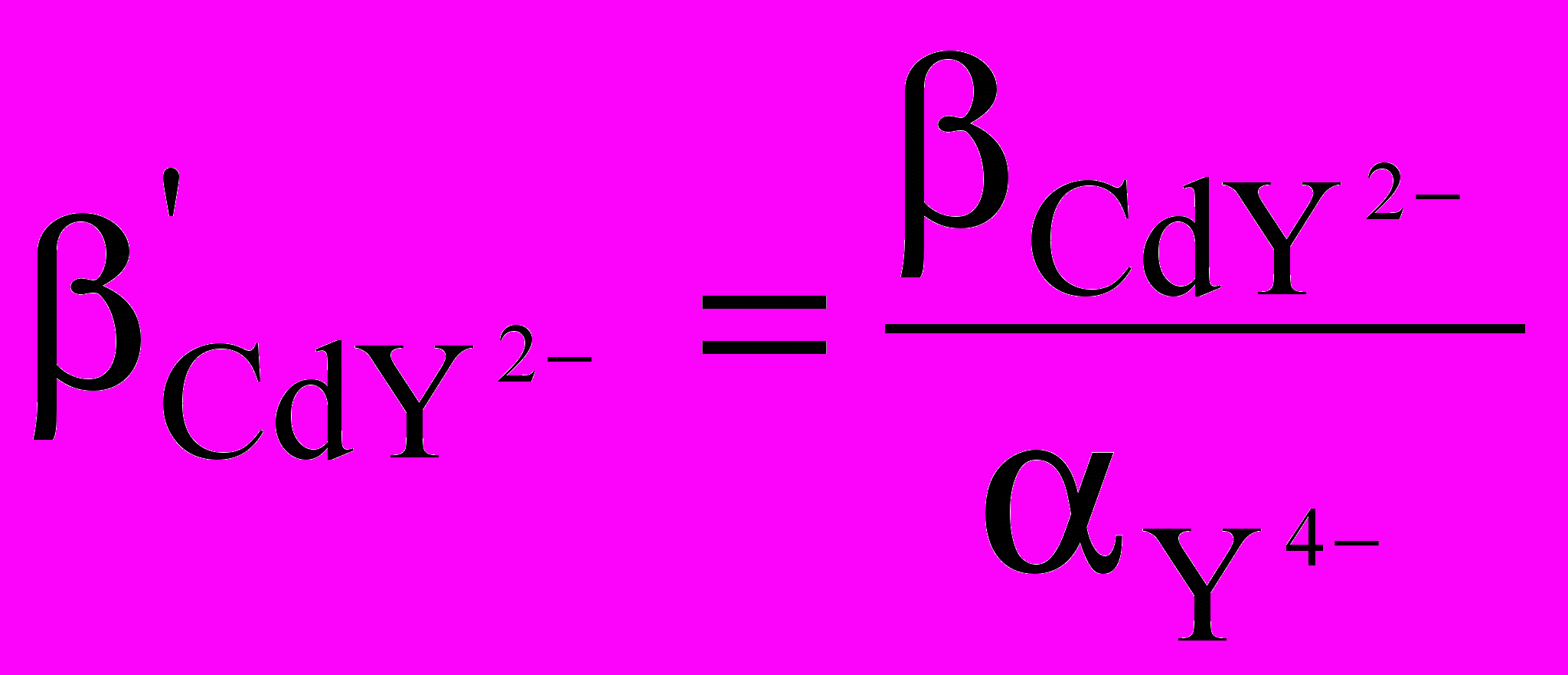Рабочая программа по дисциплине Аналитическая химия и физико-химические методы анализа Рекомендуется для направлений подготовки
| Вид материала | Рабочая программа |
СодержаниеПримерный тест для контроля текущей успеваемости по модулю 3 Примерный тест для итогового контроля знаний студентов по разделу «ФХМА». |
- Программа учебной дисциплины "Аналитическая химия и физико-химические методы анализа", 239.87kb.
- Рабочая программа по дисциплине ен. Ф. 07 «Аналитическая химия и физико-химические, 223.14kb.
- Рабочая программа по дисциплине «Аналитическая химия и физико-химические методы анализа», 326.88kb.
- Учебно-методический комплекс по дисциплине Аналитическая химия и физико-химические, 314.54kb.
- Рабочая программа по дисциплине енф. 04. 03 «Аналитическая химия и физико-химические, 231.96kb.
- Программа вступительного экзамена в аспирантуру по специальности 02. 00. 02 Аналитическая, 51.98kb.
- Самостоятельная работа студентов методические рекомендации по дисциплинам «Аналитическая, 645.42kb.
- Рабочая программа по дисциплине «Спектральные методы анализа» для специальности 020101, 175.88kb.
- Рабочая программа дисциплины «Аналитическая химия» модуль «Физико-химические методы, 245.32kb.
- Образовательная программа 240100 Химическая технология и биотехнология Дисциплина Химия, 54.66kb.
1 2
Примерный тест для контроля текущей успеваемости по модулю 3
1. Для определения цинка методом осадительного титрования используется рабочий раствор:
1) AgNO3
2) K4Fe(CN)6
3) Hg2(NO3)2
2. В аргентометрии для фиксирования точки эквивалентности адсорбционные индикаторы применяются :
- в методе Мора

- в методе Фольгарда
- в методе Фаянса
3. Для расчета равновесий в растворе при титровании иона Cd2+ Трилоном Б в среде аммонийного буфера следует использовать константу устойчивости:
4. Для стандартизации рабочего раствора в меркуриметрии в качестве установочного вещества используется:
1) NaNO3
2) NaCl
3) Na2CO3
5. Комплексонометрическое определение ионов Fe(III) проводят по методике:
- прямое титрование в кислой среде
- прямое титрование в среде аммонийного буфера
- титрование по замещению в кислой среде
Пример билета для сдачи коллоквиума по модулю 2
- Какие требования предъявляются к реакциям, используемым в титриметрическом анализе?
- В каком случае из двух сравниваемых величина скачка титрования будет больше: 0,1 M C6H5NH2 + 0,1 M HCl
0,1 М C2H5NH2 + 0,1 M HCl?
3. Какую индикаторную ошибку следует учитывать при титровании NаOH+HCl с метиловым оранжевым и какую при титровании с тимолфталеином?
4. Назвать способы установления нормальной концентрации рабочих растворов (титрантов) и привести примеры.
5. Какими способами определяется содержание Р2О5 в удобрениях?
Пример билета для сдачи коллоквиума по модулю 5
- Какое свойство измеряют в потенциометрических методах анализа? Какие функции выполняют индикаторные электроды и какие – электроды сравнения? Какие требования к ним предъявляются? Приведите примеры индикаторных электродов и электродов сравнения.
- Приведите принципиальную схему полярографической установки с ртутным капающим электродом. Что такое «постоянная капилляра» и какое значение она имеет для практики?
- Можно ли в растворе, содержащем NaOH и NH4OH, определить содержание обоих компонентов методом кондуктометрического титрования раствором HCl? Какой вид имеет кривая титрования этой смеси?
- Что такое потенциал разложения и перенапряжения? Назовите основные причины перенапряжения. Чему равна действительная величина ЭДС, при которой происходит электролиз?
Примерный тест для итогового контроля знаний студентов по разделу «ФХМА».
- В спектрофотометрических методах анализа используется свойство:
а) излучение света атомами вещества;
б) поглощение света атомами вещества;
в) поглощение света молекулами или ионами;
г) рассеяние света частицами вещества.
- В далекой ультрафиолетовой области ( < 200 нм) поглощает свет вещество:
а) С2Н6;
б) HCl;
в) MnCl2;
г) С6Н6.
- Закону Бугера–Ламберта–Бера соответствует формула:
а) I = I0 кc;
б) I = асb;
в) I = I0 10-lc;
г) I = I0 к(1 – 10-lc).
- При определении оптической плотности не взаимодействующих друг с другом веществ с концентрацией с1 и с2 получены значения А = 0,3 и А = 0,2. Оптическая плотность раствора, содержащего одновременно оба этих вещества в тех же концентрациях (l = const, = const) равна:
а) А = 0,1;
б) А = 0,2;
в) А = 0,5;
г) А = 0,3.
- В основу метода прямой кондуктометрии положена зависимость:
а) зависимость электрической проводимости от концентрации определяемого вещества;
б) зависимость подвижности определяемого иона от его концентрации;
в) зависимость силы тока от электрического сопротивления раствора;
г) зависимость электрической проводимости от величины заряда ионов определяемого вещества.
- В методе прямой потенциометрии линейный градуировочный график следует строить координатах:
а) Е – с(х);
б) Е – lgc(x);
в) lg E – lgc(x);
г) lg E – c.
- Потенциометрическое титрование HCl раствором NaOH характеризует кривая:
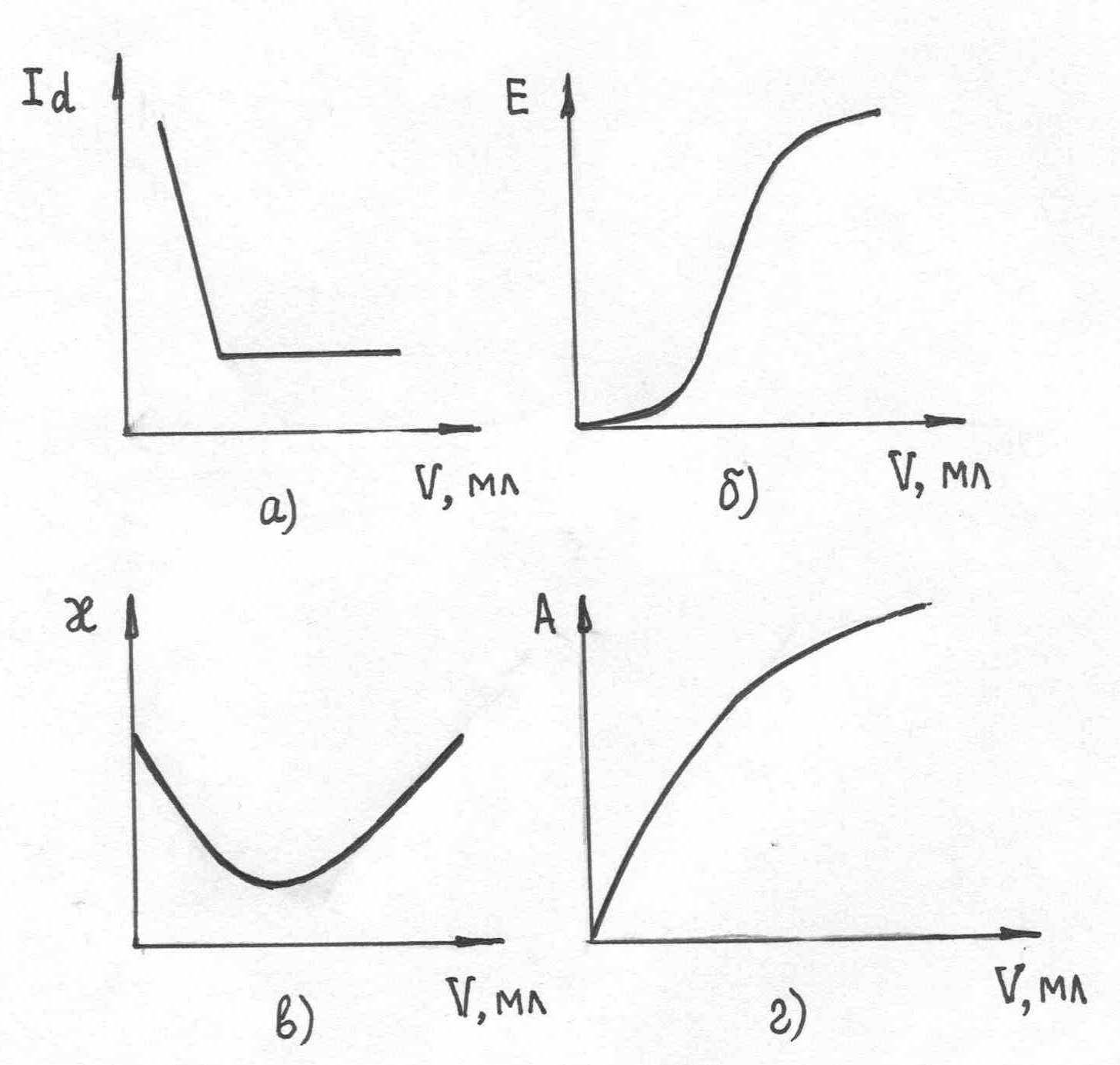
- Схематическая запись Pt(H2)/2H+ соответствует электроду:
а) стеклянному;
б) водородному;
в) хингидронному;
г) каломельному.
- В основе эмиссионного спектрального анализа лежит физический процесс:
а) энергетический переход внутренних электронов в молекуле;
б) энергетический переход внешних электронов в молекуле;
в) переход внешних электронов в атоме возбужденного уровня на более низкий;
г) переход внешних электронов в атоме с основного уровня на возбужденный.
- Наиболее точные результаты дает метод количественного эмиссионного анализа:
а) метод постоянного графика;
б) метод трех эталонов;
в) метод переводного коэффициента;
г) метод одного эталона.
- Выполнен анализ методом эмиссионной спектроскопии. Градуировочные графики имеют следующий вид:
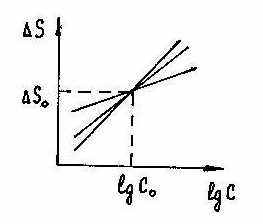
Они относятся к методу:
а) методу трех эталонов;
б) методу постоянного графика;
в) методу одного эталона;
г) методу добавок.
- В газовой хроматографии катарометр относится к типу детекторов:
а) к детекторам по теплопроводности (ДТП);
б) к детекторам ионизации в пламени (ДИП);
в) к детекторам электронного захвата;
г) к термохимическим детекторам.
_____________________________________________________________________________
Разработчики:
__ИГХТУ____________ ______зав. каф.____________ М.И._Базанов__________
(место работы) (занимаемая должность) (инициалы, фамилия)
___ИГХТУ________________ ___доцент___ А.В. Катровцева_______
(место работы) (занимаемая должность) (инициалы, фамилия)
___ИГХТУ________________ ___доцент___ Н.В. Чернявская_______
(место работы) (занимаемая должность) (инициалы, фамилия)
___ИГХТУ________________ ___профессор___ Л.А.Кочергина_______
(место работы) (занимаемая должность) (инициалы, фамилия)
___ИГХТУ________________ ___профессор___ А.И.Лыткин_______
(место работы) (занимаемая должность) (инициалы, фамилия)
Эксперты:
____ИвГУ________ _зав. кафедрой аналитической химии _ Е.В. Козловский
(место работы) (занимаемая должность) (инициалы, фамилия)