Методические указания для самостоятельной работы студентов 6 курса по специальности «Педиатрия»
| Вид материала | Методические указания |
- Методические указания для самостоятельной работы студентов 6 курса по специальности, 392.61kb.
- Методические указания для самостоятельной работы студентов 6 курса по специальности, 430.12kb.
- Методические указания для самостоятельной работы студентов 6 курса по специальности, 195.47kb.
- Методические указания по выполнению контрольной работы для самостоятельной работы студентов, 164.27kb.
- Методические указания по выполнению контрольной работы для самостоятельной работы студентов, 371.12kb.
- Методические указания по выполнению контрольной работы с использованием компьютерных, 1010.76kb.
- Методические указания по выполнению контрольных работ для самостоятельной работы студентов, 868.03kb.
- Методические указания по выполнению контрольной работы для самостоятельной работы студентов, 189.26kb.
- Методические указания для самостоятельной работы студентов 6 курса по специальности, 478.64kb.
- Методические указания к курсовому проекту по дисциплине "Газоснабжение" для студентов, 1460.12kb.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ УКРАИНЫ
ХАРЬКОВСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
ХРОНИЧЕСКИЕ ЗАБОЛЕВАНИЯ ОРГАНОВ ДЫХАНИЯ, ВОЗНИКАЮЩИЕ В ПЕРИНАТАЛЬНОМ ПЕРИОДЕ
Методические указания для самостоятельной работы
студентов 6 курса
по специальности «Педиатрия»
(составитель: асcистент Чайченко Т.В.)
Утверждено на методическом заседании кафедры
протокол №2 от 30 августа 2007
Харьков ХГМУ 2007
Заболевания бронхолегочной системы на протяжении многих лет сохраняют ведущие позиции в структуре педиатрической патологии. Несмотря на успехи современной медицинской науки и практики патология органов дыхания у новорожденных детей, а, особенно, недоношенных продолжает оставаться краеугольным камнем и лежит в основе формирования хронических заболеваний легких у детей.
Хронические заболевания легких (ХЗЛ) диагностируются тогда, когда у ребенка без первичной кардиальной или сосудистой патологии в возрасте старше 28 дней имеются признаки участия дополнительной мускулатуры в акте дыхания и патологические изменения в легких, выявляемые на рентгенограмме или с использованием других методов исследования.
Исходя из этого выделяют такие варинты ХЗЛ: бронхолегочная дисплазия, синдром Вильсона-Микити, хроническая легочная недостаточность недоношенных, пороки развития легких.
Эта патология представлена в МКБ 10 пересмотра таким образом:
P27 Хронические болезни органов дыхания, развившиеся в перинатальном периоде
P27.0 Синдром Вильсона-Микити
P27.1 Бронхолегочная дисплазия, возникшая в перинатальном периоде
P27.8 Другие хронические болезни органов дыхания, возникшие в перинатальном периоде
P27.9 Неуточненные хронические болезни органов дыхания, возникшие в перинатальном периоде
БРОНХОЛЕГОЧНАЯ ДИСПЛАЗИЯ
Первоначально БЛД рассматривалась как результат повреждающего действия кислорода и ИВЛ на легкие новорожденного, что нашло отражение в классической формуле A. Philip (1975): "кислород+давление+время+незрелое легкое". В настоящее время БЛД рассматривается как полиэтиологическое заболевание. Факторами, способствующими развитию БЛД, являются следующие:
- Незрелость легкого недоношенного ребенка
- Токсическое действие кислорода
- Баротравма легких
- Респираторные расстройства
- Инфекция
- Отек легких
- Легочная гипертензия
- Наследственная предрасположенность
- Гиповитаминозы А и Е
1) Незрелость легкого недоношенного ребенка.
Частота БЛД зависит от массы тела при рождении и гестационного возраста. Незрелость у недоношенного ребенка анатомических структур легкого, системы сурфактанта и созревающей одновременно с ней, в третьем триместре беременности, антиоксидантной системы легких, включающей супероксиддисмутазу, глютатион пероксидазу и каталазу, играет роль в избыточном растяжении дыхательных путей и предрасполагает к баротравме и повреждению кислородом [Fitzerald D. et al., 1994]. Недавние исследования, проведенные у недоношенных детей, показали перспективность интратрахеального применения рекомбинантной супероксиддисмутазы для профилактики БЛД [Carlo W. A., et al., 1997]. Вместе с тем, факт преждевременных родов не всегда обязателен для развития БЛД. Доношенные дети, потребовавшие ИВЛ с длительной экспозицией высоких концентраций кислорода в дыхательной смеси для лечения легочной гипертензии, синдрома аспирации мекония, врожденных пороков сердца или пневмонии тоже нередко развивают БЛД. Возможно развитие БЛД и у переношенных детей.
2) Токсическое действие кислорода.
Экспериментально показано, что кислород может участвовать в патогенезе поражений, наблюдаемых на разных стадиях БЛД. Гипероксидное повреждение легких приводит к некрозу эпителия дыхательных путей, эндотелия легочных капилляров, трансформации альвеолоцитов II типа в альвеолоциты I типа [Evans M. J., 1994]. Следствием "окислительной атаки" является нарушение мукоцилиарного клиренса, развитие ателектазов и легочной гипертензии.
3) Баротравма легких.
Этиологическое значение механической ИВЛ и токсического действия кислорода в развитии БЛД было подтверждено при моделировании заболевания у обезьян, свиней, кроликов. Имеется синергизм действия этих факторов. Токсическое действие высоких концентраций кислорода во вдыхаемой смеси приводит к повреждению эпителиального и эндотелиального клеточных барьеров и развитию протеинсодержащего отека легочной ткани, что сопровождается снижением растяжимости альвеол, уже нарушенной вследствие дефицита сурфактанта. Снижение комплайнса легких и нарастающие нарушения вентиляционно-перфузионных отношений обуславливают необходимость использования более высоких параметров ИВЛ, что замыкает порочный круг, усиливая повреждение легких [Davis J. M., Rosenlfeld W. N., 1994]. Частые колебания температуры и влажности в ходе ИВЛ нарушают мукоцилиарный клиренс. Применение ИВЛ с постоянным положительным давлением способствует возникновению разрывов альвеол с образованием интерстициальной эмфиземы и пневмоторакса.
4) Респираторные расстройства, по поводу которых проводится ИВЛ.
Они могут быть как первичными (синдром дыхательных расстройств, болезнь гиалиновых мембран, ателектаз, болезни утечки воздуха) так и вторичными, например апноэ. БЛД развивается у 1-8% детей с болезнью гиалиновых мембран и у 5-21% детей с данным заболеванием, находившихся на ИВЛ [Ю В.В. Х., 1989]. Вместе с тем, БЛД встречается у новорожденных, которым требовалось проведение ИВЛ по другим причинам, таким как персистирующее фетальное кровообращение и другие формы врожденных болезней сердечно-сосудистой системы, в частности врожденных пороков сердца, особенно с обогащением малого круга кровообращения [Эммануилидис Г. К., Байлен Б. Г., 1994].
5) Инфекция.
Многочисленными исследованиями показано, что колонизация дыхательных путей недоношенных новорожденных такими микроорганизмами, как Chlamydia trachomatis, Ureaplasma urealyticum, Mycoplasma hominis, цитомегаловирус, Pneumocysta carinii ассоциируется с высоким риском развития БЛД по сравнению с неинфицированными. Указанные возбудители могут вызывать хорионамнионит, преждевременные роды, а также легочные поражения (воспаление, сопровождающееся гиперреактивностью бронхов, инактивацию сурфактанта).
6) Отек легких.
Причинами отека легких могут быть избыточный объем инфузионной терапии, нарушения выведения жидкости, открытый артериальный проток.
7) Легочная гипертензия.
Повышение давления в системе легочной артерии при БЛД объясняется следующим образом. При БЛД диаметр артерий, по которым кровь поступает к тканям, подвергшимся рубцеванию, уменьшается, их мышечная стенка утолщается. Фиброзные изменения части артерий приводят к снижению суммарного поперечного сечения артериального русла легких. Повышенная проницаемость капилляров, низкое онкотическое давление крови, повышенный вследствие ИВЛ синтез вазопрессина и альдостерона и ухудшение лимфатического дренажа на фоне фиброзных изменений лимфатических сосудов способствуют развитию интерстициального отека легких. Это пролонгирует течение тканевой воспалительной реакции и ведет к развитию структурных аномалий сосудов, усугубляющих легочную гипертензию. К развитию легочной гипертензии предрасполагают внутриутробные герпетическая, цитомегаловирусная, микоплазменная инфекции, приводящие к внутриутробной перестройке сосудов легких и гиперактивному воспалительному ответу на повреждение вследствие хронической гипоксии, пневмонии или внутриутробной активации синтеза цитокинов [D. Fitzerald et al., 1994, Пулин А. М., 1997].
8) Наследственная предрасположенность.
Имеются эпидемиологические данные о большой частоте бронхиальной астмы среди родственников больных БЛД. Делается вывод, что генетически обусловленная гиперреактивность дыхательных путей увеличивает риск развития БЛД [Bertrand J. M. et al., 1985] . К факторам риска относят также мужской пол, принадлежность к кавказским национальностям [Гомелла Т. Л., Каннигам М. Д., 1995].
9) Гиповитаминозы А и Е.
У недоношенных новорожденных с СДР, развивших БЛД, имеет место снижение уровня ретинола и ретинол-связывающего белка в сыворотке крови, что приводит к нарушению мукоцилиарного клиренса, перемещения воды через трахеобронхиальный эпителий и к повышению резистентности дыхательных путей. Дети, которые имеют дефицит витамина Е, селена, серосодержащих аминокислот, могут иметь повышенный риск БЛД, но этот дефицит маловероятен у детей, не находящихся на парентеральном питании.
Патологическая анатомия и физиология
Согласно результатам патологоанатомических исследований, выделяюют 4 стадии развития БЛД, совпвдающие с ренгенологическими находками [Northway W. Н., 1967].
1 стадия (в первые три дня жизни) - типичный респираторный дистресс-синдром.
2 стадия (в течение последующих дней первой недели жизни) - деструкция клеток альвеолярного эпителия и эндотелия капилляров, развивается отек интерстициального и периваскулярного просранств, наблюдается некроз бронхиол, сквамозная метаплазия, гипертрофия гладкой мускулатуры, исчезновение клеток мерцательного эпителия.
3 стадия (на II-III неделе) - увеличивается число макрофагов, плазмоцитов и фибробластов. Повреждаются бронхиолы различного порядка, что в тяжелых случаях приводит к облитеририрующему бронхиолиту
4 стадия (в последующую неделю) - выявляются зоны ателектазов с интерстициальным и перибронхиальным фиброзом в сочетании с очагами эмфиземы. В стенках альвеол увеличивается число ретикулярных, коллагеновых, эластических волокон, структура которых нарушена.
Закономерно развивается эмфизема легких, обусловленная тремя механизмами: 1) рубцами, появляющимися вследствие перерастяжения нефиброзированного легкого; 2) нарушением процесса мультипликации альвеол в отдельных участках (гипопластическая форма эмфиземы); 3) деструкцией в результате воспаления и разрушения стенки альвеол и капиллярного русла.
Клиническая картина
Специфических клинических проявлений БЛД нет. Клиническая картина БЛД представлена симптоматикой хронической дыхательной недостаточности (тахипноэ до 80-100 в минуту, цианоз, эмфизема, ретракция ребер, стойкие физикальные изменения в виде удлиненного выдоха, сухих свистящих, влажных мелкопузырчатых хрипов, возможен стридор) у недоношенных новорожденных детей, зависимых от высоких концентраций кислорода во вдыхаемом воздухе и ИВЛ в течение более или менее продолжительного времени. Стойкая дыхательная недостаточность развивается после первичного улучшения состояния на фоне ИВЛ. Эта зависимость от кислорода и ИВЛ может проявляться по-разному. Диагноз БЛД объединяет широкий ряд клинических проявлений и изменений на рентгенограмме. В легких случаях можно наблюдать лишь невозможность снижения концентрации кислорода и смягчения параметров ИВЛ в течение 1-2 недель, удлинение периода выздоровления после дыхательной недостаточности; в тяжелых - на фоне ИВЛ сохраняется гипоксемия, гиперкапния, "снять" ребенка с ИВЛ не удается в течение нескольких месяцев, характерны реинтубации. Как правило, основания для подозрения на БЛД возникают, когда ребенку требуется ИВЛ, особенно с положительным давлением в конце выдоха, в течение более 1 недели. Кашель, стойкие признаки бронхообструктивного синдрома сохраняются у больных на фоне уже самостоятельного дыхания.
Дальнейшее, после неонатального периода, течение БЛД волнообразное, зависит от выраженности морфологических и функциональных нарушений. У большинства больных отмечается медленное, но четкое улучшение и нормализация состояния через 6-12 месяцев, но у части больных нарушения сохраняются длительно. По наблюдениям Г. М. Дементьевой с соавт. (1997) у 16-20% детей, выписанных из отделений для недоношенных, сохраняются патологические изменения со стороны легких и в старшем возрасте - на 1-4 годах жизни, а у 4% больных БЛД в дальнейшем ведет к инвалидности. Выздоровление у детей с БЛД может быть обусловлено тем, что наряду с фиброзно-пролиферативными процессами в легких у недоношенных происходят регенеративные процессы и продолжается рост и развитие легких [Bankalary E., Sosenko J., 1990].
Ренгенографическая картина
W. Northway (1967) описал 4 рентгенологические стадии развития БЛД
В первой стадии (1-3 день), соответстствующей картине СДР, выявляется нежная нодозно-ретикулярная сеть, положительная воздушная бронхограмма;
Вторая стадия (4-10 день) отражает нарастание легочного отека, что проявляется уменьшением прозрачности легкого, нечеткостью контуров сердечной тени, но главные бронхи еще воздушны.
В третьей стадии (10-20 день) образуются мелкокистозные просветления ("губка", "пузыри"), контур сердца визуализируется, эта стадия отражает начинающийся фиброз легочной стромы.
Если данные изменения сохраняются более 1 месяца, говорят о развитии IV стадии - хронической БЛД, при которой выявляются кардиомегалия, линейные и лентообразные уплотнения (участки фиброза), чередующиеся с зонами просветления за счет эмфиземы.
Таким образом, типичные рентгенологические изменения появляются только на третьей недели.
Лабораторные данные
Лабораторные данные отражают хроническую природу заболевания [Гомелла Т. Л., Каннигам М. Д., 1995, Шабалов Н. П., 1995].
Показатели газов артериальной крови свидетельствуют о гиперкапнии, однако вследствие длительного течения заболевания рН обычно нормальная, гипоксемия развивается, если не проводится дополнительная оксигенация. При изучении функционального состояния легких выявляют: повышение частоты дыхания, уменьшение дыхательного объема (при относительно нормальной легочной вентиляции), повышение артерио-альвеолярной разницы РaСО2, повышение остаточного объема, признаки повышения резистентности в бронхиолах, низкий динамический легочный комплайнс. Электролитные нарушения включают повышение концентрации бикарбоната, а также осложнения терапии диуретиками (гипонатриемия, гипокалиемия, гипохлоремия) или из-за ограничения введения жидкости (повышение азота мочевины, креатинина).
Классификация
Выделяют три степени тяжести болезни (Богданова А. В. с соавт., 2002):
- Легкая степень тяжести - отсутствие тахипноэ в покое, появление симптомов бронхообструкции на фоне респираторной инфекции, рентгенологически выявляется умеренная эмфизема.
- Средняя степень тяжести - отмечается тахипноэ при физической нагрузке (плач, беспокойство, кормление), сухие хрипы на выдохе, влажные мелкопузырчатые хрипы в период клинического благополучия. При присоединении респираторной инфекции обструктивные нарушения дыхания усиливаются. При рентгенографии грудной клетки выявляются эмфизема, участки локального пневмосклероза.
- Тяжелая степень БЛД - тахипноэ в покое и выраженными симптомами бронхообструкции, сочетающимися с ослаблением дыхания при аускультации легких, отставанием в физическом развитии, формированием легочного сердца, стойкими рентгенографическими изменениями в виде эмфиземы, обеднении легочного рисунка, множественных участков пневмосклероза, ателектазов, дистелектазов, перибронхиальных изменений, кардиомегалии
Осложнения
- ателектазы
- пневмоторакс
- правожелудочковая сердечная недостаточность
- хроническое легочное сердце
- хроническая дыхательная недостаточность
- легочные инфекции
- трахеобронхомаляция
- рецидивирующий обструктивный бронхит и бронхиальная астма
- эпизоды гипоксии
- артериальная гипертензия
- задержка роста и отставание физического развития
- задержка нервно-психического развития
- перинатальное поражение нервной системы
Летальность при БЛД на первом году жизни составляет 23-36% [Ю В.В. Х., 1989].
Алгоритм диагностики БЛД (Богданова А.В., 2002):
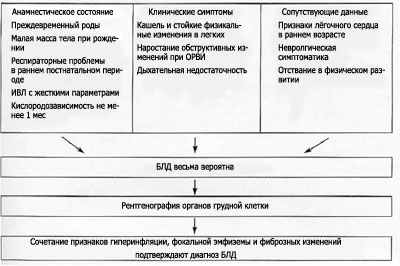
Критерии диагностики БЛД
В первые 3 недели БЛД тяжело отличить от затянувшейся стадии выздоровления при СДР, пневмонии, легочного кровоизлияния. Позднее приходится дифференцировать с синдромом Вильсона-Микити, интерстициальной эмфиземой, лобарной эмфиземой, врожденными аномалиями сосудов легких, муковисцидозом, бронхиальной астмой.
Лечение
Лечение БЛД симптоматическое (Богданова А.В., 2002)
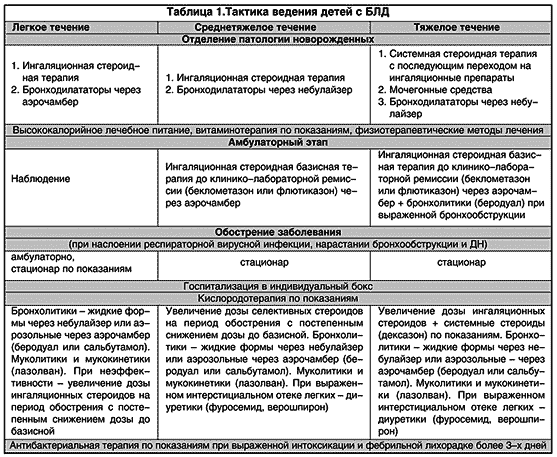
Необходимо обеспечить максимально возможный покой и оптимальный температурный режим, поддерживая температуру кожи на уровне 36,5оС.
Хотя ИВЛ является одним из основных этиологических факторов БЛД, лечение этого заболевания может потребовать дополнительного проведения ИВЛ и/или обеспечения кислородом в течение недель или месяцев. Давление в аппарате ИВЛ и концентрацию кислорода в подаваемом воздухе необходимо максимально уменьшить, при этом чрезвычайно важно не допустить развития гипоксемии, поскольку низкое раО2 способствует спазму сосудов легких и может привести к легочной гипертензии, развитию легочного сердца и правожелудочковой недостаточности. Возможно поддержание РаСО2 на уровне 45-60 мм рт. ст., при рН более 7,25, сатурации кислородa - 90-95%, РО2 - 55-70 мм рт. ст. При торпидной гипоксемии, требующей высокого давления на выдохе, применяются курсы высокочастотной осцилляторной ИВЛ, что позволяет уменьшить длительность вентиляции, баротравму и частоту БЛД. На стадии клинических испытаний находится жидкостная вентиляция легких. Обязательным является контроль за оксигенацией крови и концентрацией кислорода во вдыхаемой смеси. Предпочтение отдается непрерывному транскутанному мониторингу РО2 или показателям насыщения крови кислородом. После прекращения ИВЛ осуществляют дотацию кислорода в концентрации, позволяющей поддерживать РО2 на уровне 55 мм рт. ст. Когда эти параметры стабильны у ребенка, находящегося в кислородной палатке с содержанием кислорода менее 30%, можно переходить на подачу кислорода через носовой катетер. Срок госпитализации может быть сокращен путем внедрения программы кислородотерапии на дому [Дементьева Г. М., 1999].
В связи с повышенными метаболическими потребностями при дыхательной недостаточности принципиальное значение имеет обеспечение адекватной калорийности питания, равной 120-140 ккал/кг/сут. В зависимости от состояния новорожденного питание может осуществляться парентерально (с введением аминокислот из расчета белка 2-3 г/кг/сут и жировых эмульсий из расчета 0,5-3 г/кг/сут) или с помощью назогастрального зонда. Раннее введение коллоидных растворов в парентеральное питание (до 5-6 дня жизни) увеличивает риск развития БЛД. Суточное количество жидкости ограничивают минимальными потребностями - 100-120 мл/кг/сут из-за опасности развития отека легких, особенно при персистирующем артериальном протоке.
Направленность фармакологических воздействий при БЛД обусловлена наличием у этих больных персистирующего отека легких, бронхиальной гиперреактивности, воспалительного процесса в дыхательных путях, постоянным действием повреждающих факторов и течением процессов репарации [Rush M. G., Hasinski T. A. 1992].
Для улучшения дренажной функции бронхов проводится вибрационый и перкуссионный массаж грудной клетки, важно своевременное удаление мокроты из интубационной трубки, применяются муколитические препараты: ацетилцистеин, амброксол энтерально или в ингаляциях через небулайзер [Дементьева Г. М., 1999].
Диуретики применяют у детей с БЛД для улучшения легочной эластичности и уменьшения резистентности дыхательных путей за счет выведения излишков натрия и воды, при этом уменьшается потребность в дополнительном проведении кислородотерапии, хотя ее продолжительность может не уменьшаться. Фуросемид (1 мг/кг в/в или в/м или 2 мг/кг внутрь) от 1 до 3 раз в день применяется короткое время (до 1 недели), длительное его использование вызывает гиперкальциурию и как следствие - остеопороз, переломы, нефрокальциноз. Современная тактика применения этого препарата при БЛД предусматривает введение через небулайзер 1 мг/кг внутривенного препарата, растворенного в 2 мл 0,9% раствора натрия хлорида каждые 6 ч, это приводит к улучшению растяжимости легких и дыхательного объема без влияния на функции почек.
В течение всего периода лечения диуретиками производят мониторинг водно-электролитного состояния, ультразвуковое исследование почек с коррекцией выявленных нарушений [Шабалов Н. П., 2000, Kao L. C., 1994].
Дексаметазон прочно вошел в практику лечения новорожденных с БЛД с 1980-х годов. Проведенный T. Bhuta, A. Ohlsson (1998) мета-анализ профилактического применения дексаметазона в 10 опубликованных в середине 1990-х годов работах привел авторов к заключению, что назначение через рот профилактического курса дексаметазона в суточной дозе 500 мкг/кг, разделенной на два приема или введенного внутривенно, на 2-й недели жизни, приводит к достоверному снижению смертности, длительности ИВЛ и частоты БЛД и других хронических заболеваний легких в группе детей с массой тела менее 2 кг.
Существует несколько объяснений эффектов стероидов, ведущих к улучшению функции легких: поддержание бета-адренергической активности, стимуляция продукции антиоксидантов, стабилизация клеточных и лизосомальных мембран, торможение аггрегации гранулоцитов и улучшение легочной микроциркуляции, угнетение синтеза простагландинов и лейкотриенов, выведение из легких избытка жидкости, супрессия цитокиновой индукции воспалительной реакции в легочной ткани. Побочные эффекты при назначении стероидов многочисленны и включают сепсис, системную артериальную гипертензию, обратимую гипертрофию желудочков сердца, нередко протекающую с клапанной дисфункцией, интолерантность к глюкозе, гипервозбудимость, перфорацию кишечника, супрессию функции надпочечников, персистирующую 2-4 недели при курсе дексаметазона более 10 дней [Шабалов Н. П., 2000, Ng P. C., 1993, Rush M. G., Hasinski T. A., 1992]. Имеются данные о том, что раннее введение дексаметазона у недоношенных детей с СДР с целью профилактики БЛД коррелирует с развитием перивентрикулярной лейкомаляции [Pladis P. et al., 2002]. Показано достоверное увеличение частоты неврологических нарушений у детей, получавших раннюю постнатальную терапию дексаметазоном в первые три дня жизни, пролеченые дексаметазоном дети имели более высокую частоту церебрального паралича и задержки развития (Shinwella E. S. et al., 2000). Поэтому в ряде клиник дексаметазон в лечении БЛД используется в более поздние сроки (после 2-й недели жизни) [Цыбулькин Э. К. и др., 2002].
Альтернативой системного применения дексаметазона при БЛД являются будесонид (пульмикорт) и другие ингаляционные стероиды (флутиказон, беклометазон). Суточная доза ингаляционных стероидов составляет примерно 400 мкг/кг, дается в два приема через спейсер (аэрочамбер) или небулайзер.
Учитывая важную патогенетическую роль инфекционного воспаления в развитии БЛД, при наличии внутриутробной инфекции, трахеобронхита, пневмонии назначается антибактериальная терапия. Выбор антибиотика производится с учетом предполагаемого возбудителя: цефалоспорины III поколения, имипенемы, аминогликозиды назначаются при частом внутрибольничном инфицировании аэробными грамотрицательными бактериями; макролиды - при атипичной этиологии инфекции [Дементьева Г. М., 1999, Заболотских Т. В. и др., 1999] , кларитромицина у детей раннего возраста с БЛД, связанной с колонизацией дыхательных путей U. Urealyticum, при подтвержденной респираторно-синцитиальной инфекции нижних дыхательных путей у детей с БЛД в США используют рибавирин [Шабалов Н. П., 2000]. Кроме того, в лечении таких детей доказана важная роль активного воздействия на процессы воспаления путем назначения иммуноглобулинов, препаратов, воздействующих на протеазы, уровень которых значительно увеличен при БЛД.
В 1980-1990-х годах в ряде исследований для снижения частоты БЛД использовали внутримышечное или внутривенное введение фармакологических доз витамина Е сразу после рождения. В настоящее время все парентеральные препараты витамина Е исключены из общей практики из-за неудачных результатов применения, вероятно в связи с мембраностабилизирующим действием, а введение витамина Е внутрь ассоциируется с повышением частоты некротизирующего язвенного колита, что может быть связано с высокой осмолярностью препарата.
Родители больного ребенка нуждаются в эмоциональной поддержке, поскольку течение БЛД непредсказуемо, а выздоровление может быть очень медленным. Рождение недоношенного ребенка - тяжелый психологический стресс для обоих родителей. Это приводит к нарушению поведения и трудностям социальной адаптации. Вот почему чрезвычайно важна ранняя психологическая помощь родителям для формирования нормального взаимодействия "мать-ребенок".
Диспансерное наблюдение
После выписки из стационара детей с клинико-рентгенологическими или только рентгенологическими признаками БЛД диспансерное наблюдение этих больных проводится по следующему плану [Гомелла Т. Л., Каннигам М. Д., 1995, Кузьмина Т. Б., 1996].
- Рекомендуется гипоаллергенный режим в связи с риском развития бронхиальной астмы, минимизация контактов с инфекционными больными, строгое соблюдение режима дня, адекватная диета с повышенным содержанием белка.
- Больные БЛД нуждаются в повторном рентгенологическом обследовании в возрасте 6-12 мес. и контроле за состоянием функции дыхания и показателями газов крови, наблюдении пульмонолога. Это особенно важно в связи с тем, что нередко встречается гиподиагностика БЛД и заболевание диагностируется во втором полугодии жизни.
- Рекомендуется периодически выполнять биохимические исследования с целью диагностики рахита, эхокардиографические - для выявления гипертрофии правого желудочка.
- Осмотр ребенка специалистами - невропатологом, физиотерапевтом, окулистом, иммунологом - помогает оптимизировать лечение с учетом сопутствующей патологии.
- Должна быть полностью проведена иммунизация.
- Важное значение имеет обучение родителей подсчету частоты дыхания и пульса, диагностике дыхательной недостаточности по наличию свистящего дыхания, комплексу пассивных дыхательных упражнений и массажа с рекомендациями регулярных занятий, все родители обязаны получить инструкции по проведению сердечно-легочной реанимации.
- При развитии интеркуррентной инфекции с нарастанием обструктивных нарушений используются ингаляционные бронхолитические препараты (сальбутамол, беродуал) на 5-7 дней, как для купирования приступа бронхиальной астмы, при нарастании дыхательной недостаточности необходима госпитализация.
- При развитии тяжелого рецидивирующего обструктивного бронхита или истинной бронхиальной астмы у больных с БЛД, при отсутствии контроля над воспалительным процессом в дыхательных путях назначается базисная противовоспалительная терапия ингаляционными кортикостероидами (бекотид - 100-200 мкг или фликсотид - 50-100 мкг) до клинического и рентгенологического улучшения курсом от 3 месяцев до 3 лет в зависимости от тяжести болезни [Богданова А. В. и др., 2002]. В связи с возможной этиологической ролью атипичных возбудителей (C. trachomatis , U. urealyticum, M. hominis) в развитии БЛД и способностью этих микроорганизмов персистировать и вызывать рецидивирующие инфекции дыхательных путей у детей с БЛД при необходимости назначения антибиотиков по поводу респираторных инфекций предпочтительно использование макролидов (азитромицин, мидекамицин) [Заболотских Т. В. и др., 1999, Delollis R. D. et al., 1996].
Профилактика
Профилактика БЛД включает мероприятия, направленные на профилактику преждевременных родов (токолитики), СДР (назначение глюкокортикоидных гормонов беременной при угрозе преждевременных родов, заместительная терапия препаратами сурфактанта - достоверно снижали частоту развития БЛД [Konishi M. et al., 1988, Morales W. et al., 1989]), собственно БЛД (сокращение до минимума длительности ИВЛ, щадящие режимы ИВЛ, использование высокочастотной осцилляторной вентиляции, ограничение объема жидкости, раннее медикаментозное с помощью индометацина или оперативное закрытие гемодинамически активного артериального протока, назначение дексаметазона).
СИНДРОМ ВИЛЬСОНА-МИКИТИ
Преимущественно развивается у детей с гестационным возрастом менее 32 недель и массой тела менее 1500 грамм.
Этиология этого заболевания сложна и до конца не выяснена.
В отличие от БЛД дыхательных расстройств в первые 1-2 недели жизни не отмечают, но на 15-35 день жизни появляются и далее нарастают одышка, цианоз, приступы апноэ, западение грудины, увеличивается переднезадний размер грудной клетки. Признаки интоксикации отсутствуют. Типичны кашель, кислородозависимость цианоза.
Морфологически изменения в легких представлены вздутием, утолщением или истончением межальвеолярных перегородок, фиброзными изменениями в межуточной ткани.
В начале заболевания на рентгенограмме грудной клетки выявляется нежный рисунок интерстиция, который лучше виден в верхнемедиальных отделах легких с обеих сторон. Постепенно происходит огрубление интерстиция, который становится похожим на кружево. Далее изменения на рентгенограмме не дифференцируются от проявлений бронхолегочной дисплазии, визуализируются как грубые ленточные уплотнения, «пузыри», и кисты (фиброзно-сетчатая деформация сосудисто-интерстициального рисунка легких на фоне участков эмфизематозного вздутия легких). В этой фазе могут наблюдаться изменения со стороны сердца в виде расширения его границ вправо. Изменения могут сохраняться в течение 3-12 мес.
Лечение то же, что и при БЛД.
Прогноз неблагоприятный: летальность достигает 70%.
Хроническая легочная недостаточность недоношенных
Термин введен А.Краусом в 1957 году. Также как и при БЛД дыхательные расстройства появляются в конце перврй-начале второй недели жизни.
Клиника подобна той, что бывает при Синдроме Вильсона – Микити, но на рентгенограмме не выявляют кистозных изменений и ленточных уплотнений, хотя имеются признаки отёка, задержки жидкости в легких.
Течение более благоприятное, нежели при БЛД или синдроме Вильсона-Микити, хотя периодически могут возникать эпизоды апноэ.
На 3-4 неделе жизни начинается улучшение состояния и через 2 месяца – выздоровление.
Лечение то же, что и при БЛД – положение на животе большую часть суток, диуретики, ограничение жидкости, короткий курс глюкокортикоидных гормонов.
Прогноз при отсутствии наслоения вторичной инфекции и тяжелой сопутствующей патологии благоприятный.
КОНТРОЛЬНЫЕ ВОПРОСЫ
- Какие хронические заболевания органов дыхания развиваются у новорожденных?
- Синдром Вильсона-Микити
- Бронхиальная астма
- Бронхолегочная дисплазия
- Пороки развития
- Эозинофильный инфильтрат
- Хроническая легочная недостаточность новорожденных
- Туберкулез легких
Ответ: A, C, D, F
2. Какие факторы ведут к формированию бронхолегочной дисплазии у новорожденных?
- Незрелость легкого
- Инфекции
- токсическое действие кислорода
- легочная гипертензия
- Все перечисленное
- Ничего из перечисленного
Ответ: E
3. Каковы специфические клинические проявления бронхолегочной дисплазии?
- Сухие свистящие хрипы в нижних долях легких
- Влажные хрипы в верхних долях легких
- Влажные хрипы в нижних долях легких
- Мозаичная картина перкуторного звука
- Специфических проявлений нет
Ответ: E
4. Сколько рентгенологических стадий формирования БЛД было предложено Northway (1967) ?
- 3
- 4
- 5
- 6
Ответ: B
5. Перечислите основные принципы терапии новорожденных с БЛД.
- Кислородотерапия, ИВЛ
- Вибрационый и перкуссионный массаж грудной клетки
- Ограничение суточного количества жидкости
- Введение диуретиков
- Глюкокортикоидная
- Антибактериальная терапия
Ответ: A, B, C, D, E, F
6.Выберите основные побочные эффекты стероидов.
- Артериальная гипертензия
- Интолерантность к глюкозе
- Отеки верхней половины туловища
- Супрессия функции надпочечников
- Неврологические нарушения
- Инфаркт миокарда
Ответ: A, B, D, E
- С каким осложением ассоциируется введение витамина Е в больших дозах энтерально?
- Лейкомаляция
- Деструктивная пневмония
- Некротизирующий язвенный колит
- Цирроз печени
Ответ: С
- В каком возрасте обычно диагностируют синдром Вильсона-Микити?
- На 3 часу жизни
- На 3 день жизни
- На 3 неделе жизни
- На 3 месяце жизни
- На 3 году жизни
Ответ: С
- Задача
Ребенок от 4 беременности, протекавшей с гестозом и угрозой её прерывания, родился в сроке гестации 40 недель. Роды с наложением выходных акушерских щипцов. Состояние на момент рождения тяжелое: оценка по шкале Апгар на 1 минуте 2 бала, на 5 минуте – 5 балов. Выраженная мышечная гипотония, гипорефлексия, крик стонущий, фиксация взора. Оценка по шкале Сильвермана 6 балов, в динамике – 9 балов. Для обеспечения адекватной респираторной поддержки использовался метод ИВЛ с концентрацией кислорода во вдыхаемой смеси 80% в течение 5 суток, затем – 60% в течение 7 суток.
После первичного клинического улучшения в состояние вновь ухудшилось: ЧДД до 100 в минуту, кислородзависимый цианоз, эмфизема, ретракция ребер, удлиненный выдох, разнокалиберные сухие и влажные хрипы, стридор. Неоднократно проводились реинтубации. Обратила на себя внимание зависимость от ИВЛ с положительным давлением в конце выдоха, в течение более 1 недели. На рентгенограмме ОГП на 14 сутки: прозрачность легочных полей снижена, мелкокистозные просветления типа "губки", контур сердца визуализируется.
Вопросы:
- Что послужило причиной развития дыхательных расстройств у ребенка?
- Какое состояние требует проведения ИВЛ на 14 сутки жизни?
- Какова причина его возникновения?
- Назначьте план терапии ребенка.
Ответы:
- Родовая травма ЦНС.
- Формирование бронхолегочной дисплазии.
- Длительная ИВЛ с высокими концентрациями кислорода во вдыхаемой кислородо-воздушной смеси.
- Необходимые терапевтические мероприятия включают в себя следующее:
- Максимально возможный покой и оптимальный температурный режим с температурой кожи на уровне 36,5оС.
- Адекватная калорийность питания, равная 120-140 ккал/кг/сут.
- Кислородотерапия, ИВЛ
- Для улучшения дренажной функции бронхов проводится вибрационый и перкуссионный массаж грудной клетки, своевременное удаление мокроты из интубационной трубки, муколитические препараты
- Ограничение суточного количества жидкости до минимальных - 100-120 мл/кг/сут из-за опасности развития отека легких
- Введение диуретиков для улучшения легочной эластичности и уменьшения резистентности дыхательных путей за счет выведения излишков натрия и воды
- Глюкокортикоидная терапия (дексаметазон, будесонид, флутиказон, беклометазон)
- Антибактериальная терапия
- Иммуноглобулины
- Антипротеазы
- Психологическая поддержка
ЛИТЕРАТУРА
- Н.П. Шабалов. Неонатология. Учебник для студентов, интернов и резидентов медицинских институтов. Издание второе, исправленное и дополненное. Т.1. – СПб: «Специальная литература», 1997. – 496 с.: ил.
- Неонатология / под ред. Т.Л.Гомеллы, М.Д. Каннигам. Москва: Медицина, 1995 г..
- Педиатрия: Учебник для студентов высших мед. Учеб. Заведений III – IV уровней аккредитации. – 3-е изд. / В.Г.Майданник. – Харьков: Фолио, 2006. – 1125 с.
- Рациональная фармакотерапия детских заболеваний: Рук. Для практикующих врачей / под.ред.А.А.Баранова, Н.Н.Володина, Г.А.Самсыгиной. – М.: Литтерра, 2007. – В 2 книгах (Рациональная фармакотерапия: Сер.рук. для практикующих врачей; Т.15).
