Малова елена Сергеевна
| Вид материала | Автореферат |
- Мама, мама, тебя не слышно! Елена Сергеевна, скорчившись на диване, кричала в трубку, 40.18kb.
- Зуева Елена Сергеевна Учебных часов: лекций 6 семинар, 278.17kb.
- Россия, ты у нас одна, 87.44kb.
- А. М. Горького Программы повышения квалификации и профессиональной переподготовки Экономика, 402.4kb.
- «Лизинговая компания уралсиб», 169.91kb.
- Кузнецова Елена Сергеевна г. Сергиев Посад 2009 г. Содержание Введение глава I. Теоретическое, 602.57kb.
- Заварина Елена Сергеевна Статистика Труда лекции, 659.42kb.
- Жвакина Елена Сергеевна мау дод «дши им. Алябьева» г. Тобольска Тема доклад, 65.21kb.
- Крюкова Елена Сергеевна старший преподаватель гражданского и предпринимательского права, 21.9kb.
- Г. К. Борескова со ран, конференц-зал 12 апреля, начало 30. Регламент, 189.27kb.
На правах рукописи
МАЛОВА
Елена Сергеевна
ХРОНИЧЕСКИЕ ГЕПАТИТЫ В И С: ИММУНОПАТОГЕНЕЗ
И ИММУНОДИАГНОСТИКА ФИБРОЗНЫХ ИЗМЕНЕНИЙ
В ПЕЧЕНИ
14.03.09 – клиническая иммунология, аллергология
14.01.19 – инфекционные болезни
А в т о р е ф е р а т
диссертации на соискание учёной степени
доктора медицинских наук
Москва - 2011
Работа выполнена в ГОУ ВПО «Московский государственный медико-стоматологический университет» Федерального агентства по здравоохранению и социальному развитию
Научные консультанты:
доктор медицинских наук ЕРЕМИНА
Ольга Федоровна
академик РАМН, ЮЩУК
доктор медицинских наук, профессор Николай Дмитриевич
Официальные оппоненты:
доктор медицинских наук, профессор БОРИСОВА
Алла Михайловна
доктор медицинских наук, профессор ЯРИЛИН
Александр Александрович
доктор медицинских наук, профессор ТОКМАЛАЕВ
Анатолий Карпович
Ведущая организация: ГОУ ВПО «Российский государственный медицинский университет» Росздрава
Защита диссертации состоится «16» февраля 2011 г. в «17» часов на заседании диссертационного совета Д 212.203.26 в ГОУ ВПО Российский университет дружбы народов (117198, г. Москва, ул. Миклухо-Маклая, д.6).
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО Российский университет дружбы народов.
Автореферат разослан « »___________________ 2011 года
Ученый секретарь диссертационного совета,
доктор медицинских наук, профессор Т.А.Славянская
ОБЩАЯ ХАРАКТЕРИСТИКА ДИССЕРТАЦИИ
Актуальность проблемы
По данным Всемирной Организации Здравоохранения (ВОЗ) по меньшей мере 400 миллионов жителей планеты страдают хроническим гепатитом В (ХГВ) и около 2 миллиардов имеют серологические маркеры перенесенной или текущей инфекции вирусом гепатита В (ВГВ) [You J. et al., 2008; Das A. et al., 2008]. Среди инфицированных ВГВ у 10-40% взрослых и 90% новорожденных происходит хронизация инфекции [ссылка скрыта., 2006; Meuleman P. et al., 2006; You J. et al., 2008], в 10-30% случаев связанная с повышенным риском развития прогрессирующей болезни печени, включая фиброз, цирроз печени и гепатоцеллюлярную карциному [ссылка скрыта., ссылка скрыта., 2007; ссылка скрыта. et al., 2004; ссылка скрыта., ссылка скрыта., 2004; ссылка скрыта., 2006]. Ежегодно в мире около миллиона инфицированных ВГВ погибает от неблагоприятных исходов заболевания [ссылка скрыта. et al., 2007; ссылка скрыта., ссылка скрыта., 2000; Das A. et al., 2008]. Тем не менее в последние годы отмечается падение частоты встречаемости прогрессирующего течения ХГВ в мире вообще и в России, в частности [Г.Г. Онищенко, А.Б. Жебрун, 2009; ссылка скрыта., ссылка скрыта., 2008], и у 70-80% инфицированных на протяжении многих лет сохраняются нормальные показатели функции печени, что, однако, не предотвращает в полной мере вероятность формирования у них декомпенсации печеночной функции и развития гепатоцеллюлярной карциномы [ссылка скрыта., 2010; Shi Y.-H., Shi C.-H., 2009].
Вирусом гепатита С (ВГС), по последним данным ВОЗ, в мире инфицировано около 500 миллионов человек, причем не менее 170 миллионов из них имеют клинические проявления заболевания [Козлов В.К., Стельмах В.В., Радченко В.Г., 2009; ссылка скрыта. et al., 2006; ссылка скрыта., ссылка скрыта., 2008; ссылка скрыта. et al., 2005]. Хроническим гепатитом С (ХГС) инфицировано до 2% популяции развитых стран, в России число инфицированных ВГС составляет не менее 2 миллионов человек [Козлов В.К., Стельмах В.В., Радченко В.Г., 2009; ссылка скрыта., ссылка скрыта., 2008]. Острая ВГС-инфекция в 75-85% случаев завершается формированием хронической формы заболевания с частотой неблагоприятных исходов в пределах 20-50% для цирроза печени и 20-30% для гепатоцеллюлярной карциномы [Murakami H. et al., 2004; Nahon P. et al., 2008].
Известно, что в основе патогенеза воспалительных и фиброзных изменений в печени при хронических гепатитах В и С, приводящих к неблагоприятным исходам данных инфекций, лежат сложные взаимодействия между вирусом и иммунной системой хозяина, и любое повреждение ткани печени при данных инфекциях является иммуноопосредованным [ссылка скрыта., ссылка скрыта., 2008; ссылка скрыта., ссылка скрыта., ссылка скрыта., 2007; ссылка скрыта., ссылка скрыта., 2006; Meuleman P. et al., 2006]. Тем не менее, большинство современных исследователей делает акцент на изучении специфических механизмов иммунного реагирования, что закономерно проявляется недостаточной изученностью роли факторов врожденного иммунитета, в частности, CD56+ клеток, в иммунопатогенезе хронических вирусных поражений печени и составляет актуальный аспект решения проблемы в целом.
При хронических гепатитах В и С прогноз заболевания и тактика ведения больных в большой степени зависят от выраженности фиброзного процесса в печени, который оказывает влияние на сроки проведения противовирусной терапии и дозы препаратов, служит критерием эффективности лекарственной терапии, определяет риск развития неблагоприятных исходов [Глушенков Д.В. и др., 2008; Павлов и др., 2006; ссылка скрыта. et al., 2008]. Процедура биопсии печени, являющаяся на современном этапе «золотым стандартом» диагностики фиброза печени у больных хроническими гепатитами В и С, несет в себе определенный риск для здоровья пациентов, а современный уровень гистологической оценки образцов имеет ряд недостатков, снижающих ее диагностическую точность [ссылка скрыта, ссылка скрыта., 2007; Павлов и др., 2008]. Кроме того, все существующие неинвазивные способы диагностики фиброза при хронических вирусных гепатитах не систематизированы, имеют ряд ограничений в применении и проявляют определенное несовершенство в сравнении с результатами биопсии печени [Poynard T., 2010; Gebo K.A., 2002; Rosenberg W.M. et al., 2004; ссылка скрыта. et al., 2008]. Перечисленные аргументы подчеркивают актуальность поиска альтернативных путей диагностики фиброза печени у больных хроническими гепатитами В и С и объясняют причину повышенного интереса современных исследователей к неинвазивным методам прогнозирования стадий фиброза.
Таким образом, решение задач по совершенствованию методов неинвазивной диагностики фиброза и цирроза печени у больных хроническими гепатитами В и С на базе иммунологических концепций относится к числу актуальных проблем современного российского и мирового здравоохранения.
Цель исследования
Разработка методического подхода к способам неинвазивной иммунодиагностики стадий фиброза печени при хронических гепатитах В и С на основе оценки патогенетического значения CD56+ лимфоцитов, подтверждение диагностической и прогностической эффективности новых Иммунотестов.
Задачи исследования
- Сформировать новый методический подход к разработке способа неинвазивной иммунодиагностики стадий фиброза печени у больных хроническими вирусными гепатитами и апробировать его при исследовании крови больных хроническим гепатитом В.
- Апробировать методический подход к разработке способа неинвазивной иммунодиагностики стадий фиброза печени при исследовании крови больных хроническим гепатитом С.
- Разработать способ неинвазивной иммунодиагностики (Иммунотест) стадий фиброза печени у больных хроническим гепатитом В и дать оценку его диагностической точности, чувствительности и специфичности.
- Разработать способ неинвазивной иммунодиагностики (Иммунотест) стадий фиброза печени у больных хроническим гепатитом С и дать оценку его диагностической точности, чувствительности и специфичности.
- Установить влияние эпигенетических факторов (пола, возраста, уровня вирусной нагрузки, генотипического варианта ВГС) на оценку способов неинвазивной иммунодиагностики стадий фиброза печени при хронических гепатитах В и С.
- Обосновать показания для применения предложенных способов неинвазивной иммунодиагностики стадий фиброза печени у больных хроническими гепатитами В и С в форме разработки диагностического алгоритма.
- Сопоставить диагностическую и прогностическую значимость разработанных способов неинвазивной иммунодиагностики стадий фиброза печени у больных хроническими гепатитами В и С с другими апробированными методами с использованием мета-анализа.
Научная новизна работы
При выполнении диссертационных исследований впервые:
Предложен новый методический подход к оценке иммунологических данных как критериальных признаков отдельных стадий фиброза печени у больных хроническими гепатитами В и С.
Уточнен иммунопатогенез хронических гепатитов В и С, а также фиброзных изменений в печени при данной патологии с участием CD56+ клеток.
Разработан оригинальный способ неинвазивной иммунодиагностики стадии F1 (начальной) фиброзных изменений в печени при хроническом гепатите В – Иммунотест ХГВ/F1.
Разработан оригинальный способ неинвазивной иммунодиагностики 3-й стадии (предцирротической) фиброзных изменений в печени при хроническом гепатите С – Иммунотест ХГС/F3.
Показаны диагностическая точность, чувствительность и специфичность разработанных Иммунотестов при неинвазивной диагностике соответствующих стадий фиброза печени у больных хроническими гепатитами В и С.
Выявлена зависимость оценки Иммунотеста ХГВ/F1 от пола больных и отсутствие зависимости Иммунотеста ХГС/F3 от половозрастных характеристик больных, вирусной нагрузки, генотипа вируса гепатита С.
Установлены основные направления диагностического применения Иммунотестов и алгоритм их использования при неинвазивной диагностике соответствующих стадий фиброза печени у больных хроническими гепатитами В и С.
Проведен мета-анализ неинвазивных методов диагностики фиброза печени при хронических гепатитах В и С в строгом соответствии со стадиями фиброза печени и показана высокая эффективность и конкурентоспособность разработанных Иммунотестов.
Теоретическая и практическая значимость
В процессе проведения исследований были получены новые научные данные о патогенетической роли CD56+ клеток в развитии реакций врожденного иммунитета и фиброза печени при хронических гепатитах В и С, что позволило создать уточненные схемы иммунопатогенеза названных заболеваний. Разработан и апробирован новый подход к оценке критериального значения отдельных показателей иммунного статуса при неинвазивной иммунодиагностике отдельных стадий фиброза печени у больных хроническими гепатитами В и С. Показана уникальность иммунологических сдвигов со стороны CD56+ лимфоцитов на стадии дебюта фиброзного процесса в печени при хроническом гепатите В и на стадии предцирротических изменений при хроническом гепатите С.
Разработаны Иммунотест ХГВ/F1 и Иммунотест ХГВ/F3 для использования в клинической практике в качестве методов неинвазивной иммунодиагностики хронических гепатитов В и С. Показана перспективность использования Иммунотестов в процессе диспансерного мониторинга больных данной инфекционной патологией. Показана конкурентоспособность Иммунотестов по диагностической точности, чувствительности и специфичности с другими неинвазивными методами диагностики фиброза печени при хронических гепатитах В и С. Проведен системный обзор (мета-анализ) современных данных о состоянии неинвазивной диагностики фиброза печени у больных хроническими гепатитами В и С.
Внедрение результатов работы в практику и учебный процесс
Новые сведения о роли CD56+ лимфоцитов в развитии реакций врожденного иммунитета и фиброза печени при хронических гепатитах В и С и уточненные схемы иммунопатогенеза названных заболеваний используются в учебном процессе на кафедрах инфекционных болезней Московского государственного медико-стоматологического университета (МГМСУ) и Российского университета дружбы народов (РУДН), а также на кафедре аллергологии и иммунологии ФПК медработников РУДН.
Разработанные Иммунотесты для неинвазивной диагностики фиброза печени у больных хроническим гепатитом В и прогноза цирроза печени у больных хроническим гепатитом С используются в научно-практической деятельности лаборатории патогенеза и методов лечения инфекционных заболеваний НИМСИ МГМСУ, а также медицинской компании «Гепатолог» (г. Самара).
На способ прогнозирования цирроза печени при хроническом гепатите С подана заявка на патент РФ (№ 2009144106 от 30.11.2009 г.) «Способ оценки фиброза печени у больных хроническим вирусным гепатитом С».
На способы прогнозирования цирроза печени при хроническом гепатите С и диагностики начала фиброзных изменений в печени при хроническом гепатите В получены разрешения Федеральной службы по надзору в сфере здравоохранения на применение медицинских технологий (ФС № 2009/392 от 08.12.2009 г. «Способ иммунопрогнозирования цирроза печени при хроническом вирусном гепатите С», ФС № 2010/029 от 24.02.2010 г. «Способ иммунопрогнозирования фиброза печени у больных хроническим вирусным гепатитом В»).
Положения, выносимые на защиту
- CD56+ лимфоциты играют значительную роль в иммунопатогенезе хронизации процесса и фиброзных изменений в печени при хронических гепатитах В и С, специфично проявляющуюся на стадии F1 фиброза печени у больных хроническим гепатитом В и на стадии F3 у больных хроническим гепатитом С и позволяющую сформулировать новый методический подход к оценке фиброзных изменений.
- Характерные изменения иммунологических показателей на стадии F1 фиброза печени у больных хроническим гепатитом В и на стадии F3 у больных хроническим гепатитом С могут служить критериальными признаками данных патологических состояний.
- Иммунотесты ХГВ/F1 и ХГС/F3, основанные на критериальных признаках фиброзного процесса в печени у больных хроническими гепатитами В и С, показаны при проведении неинвазивной диагностики указанных заболеваний, обладают высокой диагностической точностью, чувствительностью и специфичностью.
- Проведение мета-анализа неинвазивной диагностики фиброза печени при хронических гепатитах В и С подтверждило обоснованность включения в существующий арсенал методов Иммунотестов ХГВ/F1 и ХГС/F3 и установило их конкурентоспособность.
Апробация диссертации
Апробация диссертационной работы проведена на совместном научном заседании лаборатории патогенеза и методов лечения инфекционных заболеваний НИМСИ и кафедры инфекционных болезней и эпидемиологии Московского государственного медико-стоматологического университета. Материалы диссертации доложены и обсуждены в рамках International Congress «Advances in Immunology and Allergology at the Threshold of the XXI Century», 2000 (Eilat, Israel); VII Международного конгресса по иммунореабилитации «Аллергия, иммунология и глобальная сеть: взгляд в новое тысячелетие», 2001 (Нью-Йорк, США); IV съезда иммунологов и аллергологов СНГ, 2001 (Москва); I Съезда физиологов СНГ, 2005 (Сочи); International Symposium «Interaction of Neural and Immune Systems in Health and Disease», 2007 (Sankt-Petersburg); Национальной конференции «Аллергология и клиническая иммунология – практическому здравоохранению», 2010 (Москва); XVII Российского национального конгресса «Человек и лекарство», 2010 (Москва); ХV Международного конгресса по реабилитации в медицине и иммунореабилитации, 2010 (Дубай, ОАЭ); ХХI съезда физиологического общества им. И.П.Павлова, 2010 (Москва-Калуга); XV Российской конференции «Гепатология сегодня», 2010 (Москва); II Ежегодного Всероссийского Конгресса по инфекционным болезням, 2010 (Москва); 14th International Congress of Immunology, 2010 (Kobe, Japan); Межрегионального форума «Актуальные вопросы аллергологии и иммунологии – междисциплинарные проблемы, 2010 (Санкт-Петербург).
Публикации
По материалам диссертации опубликовано 26 научных работ, из них 10 в реферируемых журналах, в том числе в 2 зарубежных.
Объем и структура диссертации
Диссертация изложена на 217 страницах и состоит из введения, обзора литературы, главы по материалам и методам исследования, 4 глав собственных исследований, заключения и обсуждения, выводов и практических рекомендаций. Работа иллюстрирована 31 таблицами и 59 рисунками. Список литературы содержит 496 источников, из которых 52 отечественных и 444 зарубежных авторов.
СОДЕРЖАНИЕ ДИССЕРТАЦИИ
Объем, характер и методы проведенных исследований
Для решения поставленных задач проведено обследование: в составе основных групп исследования 37 больных с верифицированным диагнозом хронического гепатита В (ХГВ) и 127 больных с верифицированным диагнозом хронического гепатита С (ХГС), в составе групп сравнения 10 пациентов с алкогольным циррозом печени и 6 больных первичным билиарным циррозом печени, в составе контрольной группы 32 доноров и добровольцев – клинически здоровых лиц. Пациенты наблюдались в инфекционных клинических больницах № 1 и № 2 г. Москвы, клинике пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х.Василенко ММА им. И.М.Сеченова, Медицинской Компании «Гепатолог» г.Самары. Включение в группы производилось в строгом соответствии с критериями включения и исключения и предполагало обязательное информированное согласие пациента на обследование.
Критериями включения в основные группы служили: верифицированный диагноз хронического гепатита В или С; отсутствие этиотропной терапии в течение последних 6 месяцев перед обследованием; наличие полученных в течение последнего месяца данных биопсии печени; наличие в течение 2-х недель положительных результатов на наличие в крови вируса гепатита В или С по данным ПЦР, а также позитивных результатов серологических исследований; возраст от 18 до 65 лет; информированное согласие на обследование. Критериями отбора в группы сопоставления являлись: наличие верифицированного диагноза заболевания; отсутствие по результатам обследования вирусных гепатитов В и С; наличие полученных в течение последних 2-х недель данных гематологических, биохимических исследований крови, ультрасонографического обследования брюшной полости; возраст от 18 до 65 лет; информированное согласие на обследование. Критериями отбора в контрольную группу являлись: отсутствие каких-либо жалоб и клинико-лабораторных признаков острых и хронических заболеваний на момент обследования; отсутствие в анамнезе сведений, позволяющих причислить обследуемых к категории часто и длительно болеющих лиц, лиц с хроническими заболеваниями, с признаками инфекционно-воспалительных, аллергических, аутоиммунных, иммунодефицитных состояний; отсутствие по данным анамнеза, результатам ПЦР, серологических и биохимических исследований вирусного гепатита В или С и других заболеваний печени; возраст от 18 до 65 лет; информированное согласие на обследование. Критерии исключения пациентов из исследования были следующие: наличие тяжелых соматических заболеваний, сопутствующих аутоиммунных заболеваний и заболеваний соединительной ткани, тяжелых заболеваний эндокринной системы, онкологических заболеваний, ВИЧ-инфекции, органических заболеваний центральной нервной системы; сочетание хронического гепатита В и С; возраст до 18 лет или старше 65 лет; отсутствие информированного согласия на обследование; нарушение больным протокола исследования.
Всем пациентам проводилось единое обследование, включавшее:
- Клиническое исследование периферической крови (гемометрия) на гематологическом анализаторе фирмы «BECMAN-COULTER» с определением стандартного набора показателей в составе: абсолютное число лейкоцитов, эритроцитов, тромбоцитов, абсолютное содержание гемоглобина, относительный показатель гематокрита, абсолютное и относительное число гранулоцитов, лимфоцитов, моноцитов.
- Биохимическое исследование крови с определением общего билирубина, холестерина, мочевины, креатинина, глюкозы, общего белка, альбуминов, протромбинового индекса, а также активности аспаратаминотрансферазы (АсАТ), аланинаминотрансферазы (АлАТ), гаммаглутамилтранспептидазы (γГТП) и щелочной фосфатазы на биохимических анализаторах Hitachi Roche (Япония), 902 Automatic analyzer, Erba XL-600 и A-25 Bio Systems (Испания).
- Определение в сыворотке крови маркеров вирусных гепатитов методом иммуноферментного анализа (ИФА) при помощи диагностических тест-систем ЗАО «Вектор-Бест», Sanofi Diagnostics Pasteur, НПО «Диагностические системы», «Lа Roche» (Швейцария), др.
- Качественное и количественное определение ДНК HBV и РНК HCV в крови и определение генотипа HCV методом полимеразной цепной реакции (ПЦР) с преимущественным использованием диагностических наборов ДНК-сорб, АмплиСенс-200, ЭФ-200 и РИБО-сорб, РЕВЕРТА, АмплиСенс-200, ЭФ-200.
- Ультрасонографическое исследование органов брюшной полости по месту наблюдения пациентов на аппаратах Esaote Megas, SonoFine, GE Logiq, др.
Хронический гепатит В диагностировали в случае длительности заболевания более 6 месяцев, наличия HBs антигена, анти-HBcorIgG и ДНК HВV в крови. Хронический гепатит С диагностировали в случае длительности заболевания более 6 месяцев, наличия анти-HCV и РНК HCV в крови. Диагноз цирроза печени устанавливался на основании данных анамнеза и комплексной оценки клинико-лабораторных и инструментальные показателей: снижение общего количества тромбоцитов, протромбинового индекса, альбумина в крови, признаков портальной гипертензии при ультразвуковом исследовании брюшной полости, данных эзофагогастродуоденоскопии с оценкой состояния вен пищевода и кардиального отдела желудка.
- Все пациенты основных групп были подвергнуты в стационарных условиях чрезкожной пункционной биопсии печени иглами «Hepafix» (типа Menghini) диаметром 1,2-1,6 мм по методу Менгини под местной анестезией с последующим гистологическим исследованием биоптатов, проведенным в лабораториях стационарных баз по месту наблюдения пациентов. Оценка степени (стадии) фиброза печени в биоптатах при хронических гепатитах В и С проводилась полуколичественным методом с использованием критериев шкалы METAVIR.
- Изучение клеточного состава крови обследуемых выполнялось посредством иммунологического лабораторного исследования венозной крови в лаборатории патогенеза и методов лечения инфекционных заболеваний отдела клинической медицины НИМСИ МГМСУ с использованием проточного цитофлуориметра BD FACSCanto II (Becton Dickinson, США) после автоматизированной пробоподготовки цельной крови с помощью моноклональных антител (МКАТ) и включало определение: (1) типовой иммунограммы, (2) субпопуляционного состава и (3) функциональной активности CD56+ клеток в крови.
При определении типовой иммунограммы проводилось изучение абсолютного и относительного числа СD45+/CD3+ клеток (общего числа Т-лимфоцитов), СD3+/CD4+ (Т-хелперов), СD3+/CD8+ (цитотоксических Т- клеток), CD3+/CD56+ (ЕКТ), CD19+ (В-лимфоцитов), CD3-/СD16+/CD56+ (естественных киллеров) при использовании стандартизированного комплекта моноклональных антител (МКАТ) BD Multitest 6-Color TBNK Reagent (BD Biosciences).
Определение относительного содержания субпопуляций CD56bright и CD56dim естественных киллеров (ЕК) в крови проводился методом проточной цитофлуориметрии на основе проб с меченными РЕ-Су5 anti-CD56 МКАТ (IOTest, Beckman Coulter). Относительное число субпопуляций CD4+, CD8+ и CD8-/CD4- (DN) ЕКТ лимфоцитов выявлялось с использованием комплекта МКАТ BD Multitest 6-Color TBNK Reagent (BD Biosciences).
Для анализа функциональной активности СD56+ клеток регистрировались уровни экспрессии на их мембране следующих маркеров: 1) киллингингибирующие рецепторы (KIR) из суперсемейства иммуноглобулинов (CD158a,h), 2) ингибирующие рецепторы суперсемейства лектинов С-типа (CD94), 3) активирующие рецепторы суперсемейства лектинов С-типа (NKG2D), 4) гликопротеиды, ассоциированные с мембраной лизосом и отражающие состояние гранулярного аппарата клетки (CD107a), 5) рецепторы естественной цитотоксичности (NKp46), 6) CD16 рецепторы, опосредующие механизм антителозависимой клеточной цитотоксичности (АЗКЦТ). Определение относительного количества CD56+ клеток, экспрессирующих все перечисленные маркеры, за исключением CD107a, проводилось в раздельной пробе крови и использованием в каждом случае комплекта из двух моноклональных антител: меченных РЕ-Су5 anti-CD56 МКАТ (IOTest, Beckman Coulter) и меченных РЕ специфических МКАТ (IOTest, Beckman Coulter). Для регистрации CD56+ клеток, несущих маркер CD107a, производилось внутриклеточное определение данного рецептора с использованием пермабилизирующих компонентов фирмы Beckman Coulter и комплекта из двух моноклональных антител: меченных FITC anti-CD107a МКАТ (BD Biosciences) и меченных РerCP-Cy5-5 anti-CD56 МКАТ (BD Biosciences).
Тестирование уровней всех классов иммуноглобулинов (IgA, IgM, IgG, IgE), уровней интерферона γ (ИФНγ), интерлейкинов 10 и 13 (ИЛ10, ИЛ13) в сыворотке крови, а также трансформирующего фактора роста β (ТФРβ) в плазме крови осуществлялось методом ИФА с использованием комплекта аппаратуры (планшетный фотометр «OPSYS MR» (ридер) фирмы «THERMOLABSYSTEMS», планшетный вошер ПП2-428 фирмы «ИММЕДТЕХ», принтер «EPSON») для раздельного определения в соответствии с инструкцией по применению аппаратуры и комплекта МКАТ.
- Для статистической обработки данных применялись методы дискриптивной статистики, сравнение величин осуществлялось приемами непараметрической статистики с использованием критериев Манна-Уитни и Колмогорова-Смирнова и критерия 2 в соответствии с распределением данных. Для подтверждения информативности и диагностической значимости проведенных исследований проводился дискриминантый анализ с определением стандартизированного канонического коэффициента дискриминантной функции (СККДФ). Определение влияния отдельных факторов на гетерогенность данных для разработанных критериальных значений на основе критерия Фишера (F) проводилось методом дисперсионного анализа. Проверка гипотезы по соответствию полученных данных разработанным критериям осуществлялась на основе определения относительного риска несоответствия, а чувствительность и специфичность разработанных способов иммунодиагностики стадий фиброза печени характеризовались методом линейной регрессии с построением ROC-кривой и расчетом площади под кривой – AUROC. Математическая обработка данных проводилась на основе пакета статистических программ SPSS 17.0 (допустимая ошибка Е=5%). Мета-анализ способов неинвазивного определения стадий фиброза печени у больных хроническим гепатитом В и С осуществлялся с использованием программы Comprehensive Meta-Analyse Version 2.
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ
Для реализации поставленной цели был сформирован новый методический подход к разработке способов неинвазивной иммунодиагностики стадий фиброза печени (Иммунотестов) у больных хроническими гепатитами В и С, основанный на предположении о том, что характер иммунного процесса при качественном изменении состояния фиброза вследствие перехода от одной стадии к другой в значительной степени отличается друг от друга. При этом каждой стадии соответствует свой уровень вовлечения отдельных компонентов иммунной системы в формирование фиброзных изменений.
Новый методический подход к разработке способа неинвазивной иммунодиагностики стадий фиброза печени у больных ХГВ. Группу обследования составили 37 больных ХГВ в возрасте от 18 до 65 лет, среди которых по данным пункционной биопсии печени отсутствие фиброза (F0) диагностировано у 4-х больных (10,8%), начальная стадия фиброзных изменений в печени (F1) у 16 больных (43,2%), умеренный фиброз (F2) у 5 пациентов (13,6%), выраженный (F3) – у 3 (8,1%), цирроз печени (F4) – у 9 (24,3%). Результаты исследований сопоставлялись с таковыми в контрольной группе из 32 здоровых людей, при этом, в связи с малочисленностью группы на стадии F3, значительно снижающей возможность статистической обработки данных, группы больных ХГВ на стадиях F2 и F3 были объединены в единую группу F2-F3 в составе 8 человек.
Типовое иммунологическое обследование больных ХГВ оказалось малоинформативным для выявления критериев перехода одной стадии фиброза в другую, однако отчасти подтвердило возможное участие CD56+ клеток в фиброгенезе в целом, а ЕК (CD16+/CD56+) в развитии цирроза печени, в частности. Последующее углубленное исследование CD56+ лимфоцитов у больных хроническими гепатитами В и С проводилось одновременно на нескольких уровнях: путем определения субпопуляционного состава этих клеток, регистрации их функционального состояния, а также путем выявления уровня секреции регуляторных цитокинов этих клеток – ИФНγ, ТФРβ, ИЛ10 и ИЛ13. Результаты иммунологического исследования по стадиям фиброза печени у больных ХГВ представлены на астрограмме рисунка 1.
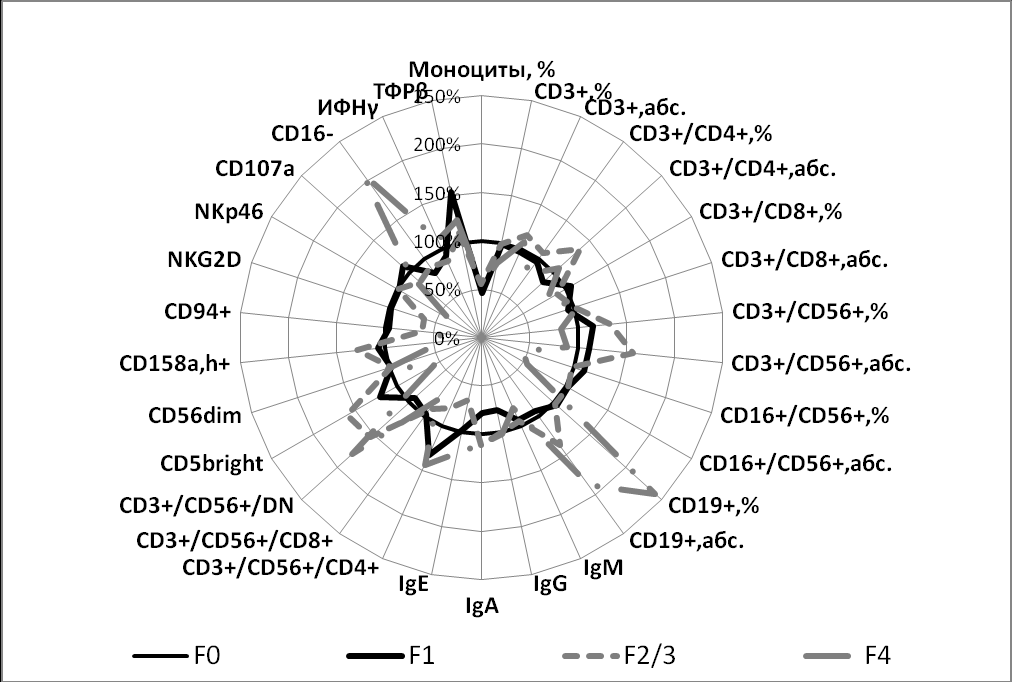
Рис.1 Астрограмма соответствия иммунологических данных стадиям
фиброза печени у больных хроническим гепатитом В
Анализ показателей экспрессии рецепторов функционального состояния CD56+ лимфоцитов в крови больных ХГВ продемонстрировал динамическое изменение способности данных клеток к проявлению цитотоксических свойств на разных стадиях фиброза печени. Кроме того, в процессе проведения углубленных иммунологических исследований у больных ХГВ удалось подтвердить предположение о четком соответствии характера иммунологических сдвигов отдельным стадиям фиброзного процесса. При этом наиболее характерные изменения со стороны CD56+ клеток наблюдались на стадии фиброза F1, а 5 из набора тестированных параметров могли иметь критериальное значение в идентификации данной стадии в определенном диапазоне величин. К их числу принадлежали относительное число CD3+/CD8+ клеток (Тцтл); СD4+ и CD8+ субпопуляций ЕКТ (СD3+.СD6+); CD56+ клеток, экспрессирующих рецепторы естественной цитотоксичности – NKp46+, уровень ТФРβ в крови больных ХГВ. Стойкое повышение уровня последнего в крови больных ХГВ относительно контроля сопровождало развитие фиброзных изменений в печени на всех стадиях, что согласовывалось с профиброзным действием данного цитокина по данным литературы [Галимова С.Ф. и др., 2001; Пинцани М., 2002].
Интересно, что информативность 4 из 5 показателей как критериальных значений была установлена с использованием дискриминантного анализа и не выявлялась при общепринятом статистическом подходе. Оказалось, что практически все эти показатели, кроме уровня ТФРβ, на стадии F1 давали два варианта отклонения: в сторону повышения и в сторону снижения, что не улавливалось при анализе средних величин (рисунок 2).
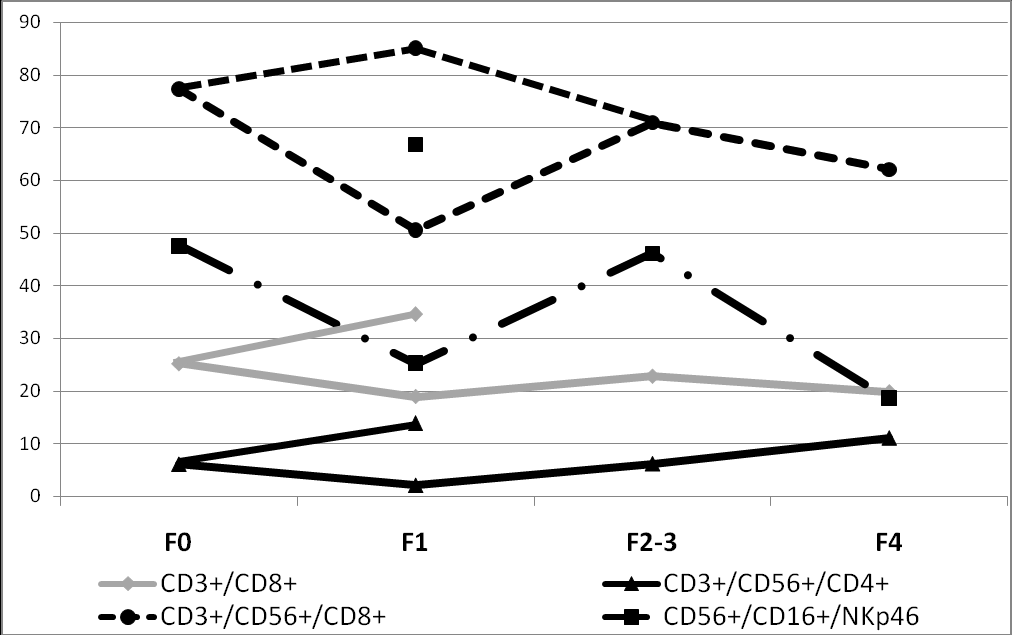


Рис. 2. Разнонаправленные сдвиги величин критериальных параметров
стадии фиброза печени 1 у больных хроническим гепатитом В
На следующем этапе исследования выяснялось, могут ли критериальные показатели из числа иммунологических параметров при ХГВ быть дополнены данными, полученными в результате общеклинических исследований крови – гематологических и биохимических. Комплексный анализ гематологических сдвигов у больных ХГВ, включавший определение стандартизированного канонического коэффициента дискриминантной функции (СККДФ), дополнил перечень информативных параметров относительным содержанием моноцитов в крови. Данный показатель демонстрировал достоверные различия между группами больных ХГВ при их распределении в соответствии со стадиями фиброза печени и, таким образом, претендовал на роль прогностического критерия прогрессирования фиброза с переходом от одной стадии к другой. Биохимические показатели, несмотря на многочисленные отклонения от контроля, не показывали достоверных различий между группами обследованных, что определило их низкую информативность для диагностики стадий фиброза печени у больных ХГВ.
Анализ частоты встречаемости диапазонов каждого из информативных показателей на различных стадиях фиброза печени у пациентов ХГВ позволил подтвердить особую диагностическую значимость шести отобранных параметров только для начальной стадии фиброза печени (F1), поскольку каждый из отмеченных критериальных признаков регистрировался не менее чем у 81,2% больных.
Таким образом, углубленное изучение субпопуляционного состава и функциональной активности CD56+ клеток (ЕК и ЕКТ) крови показало возможность формирования набора критериальных признаков для иммунодиагностики, в первую очередь, начальных фиброзных изменений в печени (F1) при ХГВ. Было установлено 6 критериальных признаков для регистрации F1 стадии фиброза печени у больных ХГВ в виде диапазона значений показателей с частотой встречаемости выше 70%, не регистрируемых на других стадиях. Итоговая шкала критериев иммунодиагностики стадии F1 фиброза печени у больных ХГВ представлена на таблице 1.
Таблица 1. Шкала критериев иммунодиагностики стадии 1
фиброза печени у больных хроническим гепатитом В
| Критериальные параметры | Диапазон критериальных значений | Частота регистрации | |
| ниже: | выше: | ||
| Моноциты, % | 3,6% | - | 81,2% |
| CD3+/CD8+, % | 19,6% | 30,8% | 100% |
| CD3+/СD56+/CD4+, % | 2,9% | 9% | 87,5% |
| CD3+/CD56+/CD8+, % | 71,8% | 82,4% | 81,2% |
| CD56+/NKp46+, % | 35% | 62% | 100% |
| ТФРβ, пг/л | - | 10,3 пг/л | 93,8% |
