Ю. А. Александров Основы радиационной экологии Учебное пособие
| Вид материала | Учебное пособие |
Содержание3.4. Молекулярные повреждения, возникающие в клетках |
- Учебное пособие Житомир 2001 удк 33: 007. Основы экономической кибернетики. Учебное, 3745.06kb.
- Учебно-методическое пособие для студентов естественных специальностей Павлодар, 1215.72kb.
- Методические указания по выполнению лабораторной работы по дисциплине «Основы радиационной, 237.73kb.
- Учебное пособие Минск, 338.57kb.
- Ответы к экзамену по радиационной медицине и экологии., 7050.62kb.
- «физиотерапия позвоночника», 197.9kb.
- Н. Г. Сычев Основы энергосбережения Учебное пособие, 2821.1kb.
- В. И. Александров Учебное пособие. Российская медицинская академия последиплом, 207.44kb.
- Е. Г. Степанов Основы курортологии Учебное пособие, 3763.22kb.
- Н. Ю. Каменская основы финансового менеджмента учебное пособие, 1952.65kb.
3.4. Молекулярные повреждения, возникающие в клетках
В результате процессов, происходящих на первичных стадиях действия излучений, изменения могут возникнуть в любых молекулярных структурах, входящих в состав живой клетки.
К наиболее биологически значимым повреждениям должны быть отнесены в первую очередь нарушения структуры ДНК. Прежде всего, это повреждения оснований, выщепление отдельных оснований из цепи, разрушение фосфоэфирных связей, лежащее в основе одиночных и двойных разрывов цепочек ДНК, распад дезоксирибозы, повреждения ДНК-мембранного комплекса, разрушение водородных связей, нарушение связей ДНК-белок, повышающее атакуемость ДНК вторичными радикалами и ферментами, сшивки ДНК-ДНК и ДНК-белок.
Аналогичные радиационно-химические изменения наблюдаются и в облученной РНК. Разница состоит лишь в том, что в РНК, в связи с ее однонитчатой структурой, не может быть двунитевых разрывов.
Не менее значимыми для жизнедеятельности клетки являются и вызванные прямым или непрямым действием радиации повреждения белка. В белковых молекулах участками, в которых чаще всего реализуется поглощенная энергия, являются тиоловые и дисульфидные группировки, а также аминокислоты, содержащие спаренные циклы (триптофан, фенилаланин, тирозин). В результате, хотя все аминокислоты поглощают энергию облучения с равной вероятностью, в конце физико-химической стадии некоторые из них оказываются избирательно пораженными.
При смертельных уровнях облучения (6-10 Гр) инактивация белков и ферментов незначительна и не обнаруживается сразу после облучения. Образующиеся в присутствии кислорода и воды свободные радикалы могут приводить к разрыву пептидной связи, образованию амида, кетокислоты и гидропе-рекисного радикала. Все это приводит к нарушению структуры белка: разрыву дисульфидных мостиков, водородных связей, пептидной цепи, образованию сшивок между пептидными цепями, отщеплению аммиака, сероводорода, окислению сульфгидрильных групп и ароматических аминокислот, к конформационным изменениям вторичной и третичной структуры белка.
В частности, возникают реакции окисления белковых SH-групп, которые нередко протекают по цепному механизму с образованием дисульфидов:
R–SH + НО* R–S* + Н2О;
R–SH +
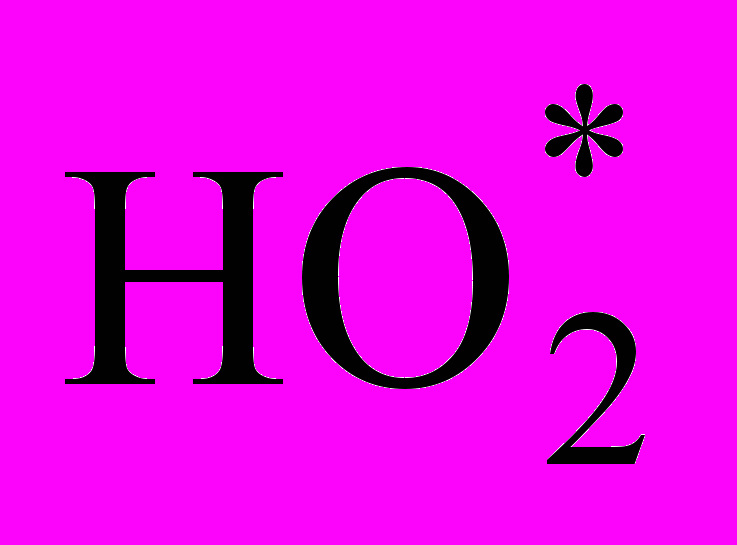 R–S* + Н2О2;
R–S* + Н2О2; R–S* + R–SH R–S–S–R + Н*.
Кроме того, дисульфиды могут образовываться путем рекомбинации появляющихся при облучении радикалов R–S*:
2R–S* R–S–S–R
или в результате взаимодействия тиолов с Н2О2:
2R–SH + Н2О2 R–S–S–R + H2O.
Радиационно-химические повреждения структуры белка могут возникать и в результате реакций дезаминирования:
H3N+ – СН2 – СОО– + НО* НО – СН2 – COO– + N+H2.
Радиационно-химические изменения белков, прежде всего изменения их вторичной и третичной структуры, могут привести к изменению биологических свойств, в том числе ферментативной активности.
В липидной фракции первичные изменения при воздействии ионизирующих излучений состоят в образовании свободных радикалов, которые, взаимодействуя с кислородом, являются источником возникновения перекисных соединений. Последние в свою очередь могут вступать в реакцию с жирами, в результате чего образуются гидроперекиси:
LH L* + Н*;
L* + О2
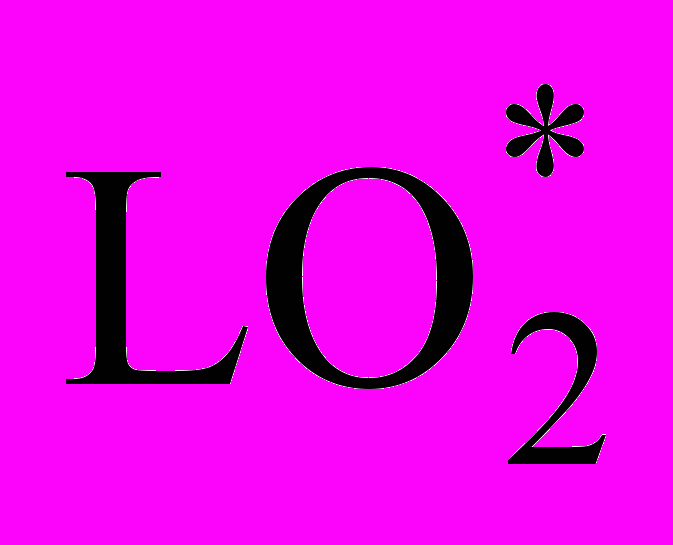 + LH LOOH + L*;
+ LH LOOH + L*;L* +
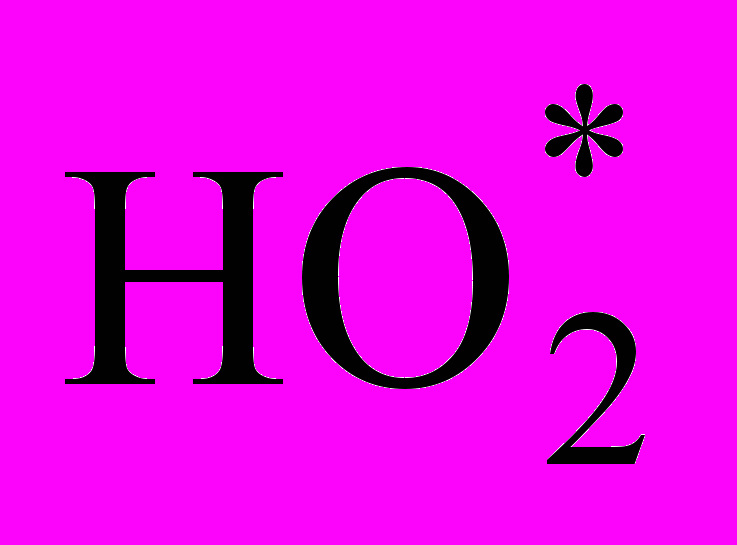 LOOH,
LOOH,где L* – радикал липида.
Гидроперекиси очень нестойки и при наличии ионов металлов с переменной валентностью легко распадаются с образованием ряда высокоактивных радикалов:
LOOH L*+ НО2; LOOH LO* + НО–; LOOH
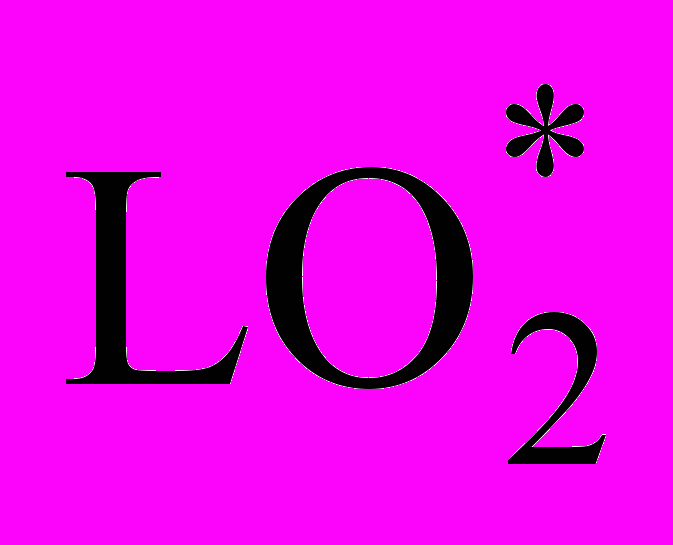 + Н*.
+ Н*.Образовавшиеся радикалы могут дать толчок к развитию цепных реакций окисления, в том числе перекисного окисления липидов.
Перекисные соединения разрушаются в дальнейшем с образованием оксикислот, альдегидов и других продуктов окисления жиров. При облучении большими дозами радиации происходит декарбоксилирование жирных кислот и даже их распад.
Важные последствия лучевых повреждений структуры липидов проявляются в нарушении строения клеточных мембран. Вовлечение липидов мембран в процессы перекисного окисления может вызывать деструкцию липопротеидных комплексов, что служит причиной изменения проницаемости мембран, смещения ионных градиентов в клетке, нарушения процессов адсорбции и активного транспорта ряда веществ. Нарушаются также процессы окислительного фосфорилирования, нормальное течение которых обеспечивается упорядоченной локализацией ферментов на мембранах. Повреждение мембран лизосом приводит к выходу и активации гидролитических ферментов.
Продукты перекисного окисления ненасыщенных жирных кислот вследствие обнаруженных у них радиомиметических свойств (способность вызывать разрывы цепей ДНК, возникновение хромосомных аберраций, подавление репарации повреждений ДНК) получили наименование первичных или липидных радиотоксинов, и им отводится существенная роль в дальнейшем развитии лучевого поражения клетки. К первичным радиотоксинам относят также обнаруживаемые в облучаемых клетках хиноны и семихиноны – продукты окисления фенолов (по Ю.Б. Кудряшову, 2001).
Изменения структуры углеводов наблюдаются преимущественно при воздействии высоких доз ионизирующих излучений. Они сводятся к деполимеризации и окислению полисахаридов, что приводит к распаду углеводородной цепи и образованию кислоты формальдегида. Среди продуктов распада углеводов могут обнаруживаться глиоксаль и гиалуроновые кислоты. Довольно существенное значение для развития изменений в соединительнотканных структурах имеет распад мукополисахаридов, в частности, гиалуроновой кислоты.
По степени проявления морфологических изменений клетки и ткани млекопитающих, т.е. по степени возрастания радиочувствительности можно расположить в следующем порядке: нервная ткань, хрящевая и костная ткань, мышечная ткань, соединительная ткань, щитовидная железа, пищеварительные железы, легкие, кожа, слизистые оболочки, половые железы, лимфоидная ткань и костный мозг.
Таблица 34 – Радиочувствительность клеток по Д0 , Гр
| Виды тканей | Д0 |
| Лимфоидные клетки | 0,5 |
| Клетки костного мозга (кроветворные) | 0,9-1,0 |
| Клетки эпителии кишечника | 1,3 |
| Клетки спермиогонного эпителия | 1,7 |
| Эпителии почечных канальцев | 1,5-1,6 |
| Эпителии альвеол молочной железы | 1,3 |
| Фолликулы щитовидной железы | 2,0 |
Примечание. Д0 – доза, при которой доля живых клеток уменьшается в сравнении с исходной в е раз (е – основание натуральных логарифмов = 2,72).
Исходы поражения зародышевых и соматических клеток при воздействии ионизирующей радиации различны. Когда поражаются зародышевые клетки, возникающие мутации (генные и хромосомные) с той или иной скоростью, зависящей от степени доминантности и от степени снижения жизнеспособности, элиминируются (выводятся) из популяции. Но многие мутации, в особенности рецесивные, благодаря генетическому дрейфу и эффекту родоначальника, могут размножаться в популяции и приводить к увеличению числа случаев врожденных уродств, аномалий обмена веществ и т.д.
Мутационные изменения в соматических клетках могут выражаться в гибели клеток или в приобретении клеткой новых наследственных свойств, которые проявляются процессами малигнизации, преждевременного старения клеток и тканей, развитием новообразований.
Резюмируя вышесказанное, можно сказать, что критической мишенью радиационного поражения клеток является ДНК, облучение на клеточном уровне приводит к замедлению прохождения цикла деления клетки, образованию хроматидных и хромосомных аберраций, возникновению микроядер, гибели клеток по апоптотическому и некротическому пути в интерфазе деления и после вступления в митоз.
Мутагенное воздействие ИИ впервые установили отечественные ученые Г.А. Надсон и Г.С. Филиппов в 1925 г. в опытах на дрожжах. В 1927 году это открытие было подтверждено Г. Меллером на классическом генетическом объекте – дрозофиле. ИИ способны вызывать все виды наследственных изменений – генные, хромосомные, геномные. Эти изменения носят дозозависимый характер и современными представлениями считается, что любая дополнительная выше природного радиационного фона (ПРФ) доза ИИ, независимо от величины и мощности приводит к опасности кумулятивного генетического эффекта и способна вызвать генетические изменения, поскольку биологическая репарация мутации невозможна (Коглл Дж., 1986).
Таким образом, прямое и косвенное действие ионизирующего излучения на биологические молекулы приводит к тому, что в живом организме отмечается много разных биологических эффектов, наблюдаемых после облучения, которые представлены в таблице 35.
Таблица 35 – Типы радиологических повреждений
| Тип биологической организации | Важнейшие радиационные эффекты |
| Молекулярный | Повреждение макромолекул – ферментов, РНК, ДНК, воздействие на обменные процессы |
| Субклеточный | Повреждение клеточных мембран, ядер, хромосом митохондрий и лизосом, высвобождение их ферментов |
| Клеточный | Нарушения деления клеток, их гибель и трансформация, в т.ч. злокачественная |
| Ткани, органы | Нарушения в красном костном мозге, желудочно-кишечном тракте, центральной нервной системе могут привести к радиационным повреждениям и гибели, отдаленным последствиям |
| Организм | Различные виды радиационных последствий, вплоть до летального исхода |
| Популяции | Изменение генетических характеристик вследствие генных, хромосомных мутаций у индивидуумов |
