Министерства Обороны Российской Федерации автореферат
| Вид материала | Автореферат |
СодержаниеПрактические рекомендации Список опубликованных работ по теме диссертации |
- А. Э. на расширенном заседании коллегии Министерства обороны Российской Федерации, 148.35kb.
- Председатель Федерального Оргкомитета конкурс, 107.46kb.
- Приказ Министра обороны Российской Федерации «Об утверждении Регламента Министерства, 956.27kb.
- Устюхина ирина Анатольевна, 341.54kb.
- Правительства Российской Федерации от 31. 12. 1999 года №1441 «Об утверждении Положения, 126.44kb.
- Маршал Российской Федерации И. Сергеев приложение к Приказу Министра обороны Российской, 812.52kb.
- Маршал Российской Федерации И. Сергеев Приложение к приказу Министра обороны Российской, 618.94kb.
- Приказ Министра обороны Российской Федерации «О службе медицины катастроф Министерства, 139.54kb.
- Министерства Российской Федерации по делам гражданской обороны, чрезвычайным ситуациям, 167.77kb.
- Вооруженных Силах Российской Федерации материальных и финансовых ресурсов свидетельствует,, 59.79kb.
**р≤0,05, в сравнении с нативной МРТ
Как следует из таблицы 5, по сравнению с информативностью нативного МР-сканирования чувствительность при использовании методики МРТ с ДКУ значимо повышалась до 94,1%, а специфичность – до 91,7%. При этом уровни прогностичности положительного и отрицательного результатов возросли до 97,0% и 84,6%, соответственно.
Поэтому использование методики МРТ с ДКУ в комплексном МР-исследовании позволяет повысить диагностическую информативность метода в выявлении локализованных форм рака предстательной железы. И, более того, по сравнению с долей повышения диагностических показателей других методик МРТ (ДВИ, МР-спектроскипии) ДКУ показала наивысший их прирост.
Таким образом, при анализе диагностической эффективности методик МРТ в выявлении опухолей предстательной железы определено, что дополнительное применение методик ДВИ, МР-спектроскопии и МРТ с ДКУ позволяет достоверно повысить эффективность первичного выявления рака предстательной железы. При этом, наибольший прирост показателей диагностической информативности показала методика МРТ с ДКУ.
Сопоставление данных комплексного МР-исследования согласно TNM-классификации (UICC, 2002; Wittekind C. et al., 2007) позволило дать оценку отдельным методикам МРТ в определении неинвазивных стадий опухолей (Т2а, Т2b, T2c), местнораспространенных (Т3а, Т3b), регионарных (N1, Т4) и метастатических стадий (М1а, М1b, М1с).
Сложности методики гистологической оценки объема поражения предстательной железы не позволили выполнить точное сопоставление геометрических размеров истинной опухоли (по гистологическим данным) и выявленной опухоли (по данным МРТ). Поэтому оценку возможностей методик МРТ в диагностике неинвазивных опухолей проводили на основе разработанного способа сопоставления данных пункционной биопсии и результатов МРТ. Произведен расчет показателей диагностической информативности основных методик МРТ в определении локализованных стадий рака предстательной железы (табл. 6). Из таблицы 6 следует, что использование дополнительных методик (ДВИ, МР-спектроскопия, МРТ с ДКУ) существенно не увеличивает диагностическую информативность МРТ в определении степени внутриорганного поражения при раке предстательной железы. Более того, использование МР-спектроскопии и МРТ с ДКУ приводило к большему количеству ложно положительных заключений. Это объясняется описанным выше эффектом МР-спектроскопического «тумана» в зоне уретры и семявыбрасывающих протоков, секрет которых имел измененные уровни метаболитов, что имитировало опухолевое поражение. При использовании методики ДКУ ложные результаты были связаны с интенсивным накоплением контрастного препарата парауретральным сплетением в зоне интереса, что в некоторых случаях расценивалось как распространение опухоли.
Таблица 6
Диагностическая информативность методик МРТ в определении Т2с стадии рака предстательной железы (n=86)
| | Нативная МРТ (р<0,001) | ДВИ (р=0,016) | МР-спектроскопия (р=0,003) | МРТ с ДКУ (р=0,002) |
| Se, % (95 ДИ) | 71,4 (53,5-84,8) | 72,2 (58,5-79,8) | 82,6 (70,8-90,8) | 85,7 (76,7-91,7) |
| Sp, % (95 ДИ) | 80,0 (74,2-84,3) | 80,0 (55,4-93,7) | 69,2* (48,3-83,7) | 70,0* (44,8-86,9) |
| Ac, % (95 ДИ) | 77,9 (69,2-84,4) | 75,0 (57,4-84,8) | 77,8 (62,7-88,2) | 81,6 (68,3-90,5) |
| PPV, % (95 ДИ) | 53,6* (40,1-63,6) | 86,7 (70,3-95,8) | 82,6 (70,8-90,8) | 88,9 (79,6-95,1) |
| NPV, % (95ДИ) | 89,7* (83,2-94,5) | 61,5 (42,6-72,1) | 69,2 (48,3-83,7) | 63,6 (40,7-79,0) |
*р<0,05, по сравнению с другими методиками МРТ
В отношении диагностики распространенности опухолевого процесса за пределы железы важно определить состояние ее капсулы. Проведен анализ МР-симптоматики, указывающей на капсулярную инвазию (табл.7).
Таблица 7
Диагностические показатели нативной МРТ
в определения экстракапсулярной экстензии рака предстательной железы
| | Se, % (95 ДИ) | Sp, % (95 ДИ) | Ac, % (95 ДИ) | PPV, % (95 ДИ) | NPV, % (95 ДИ) |
| Изменения капсулы железы (0,000) | 89,5 (74,0-96,8) | 76,9 (65,6-82,3) | 82,2 (69,1-88,4) | 73,9 (61,1-80,0) | 90,9 (77,5-97,3) |
| Изменения контура железы (0,001) | 84,2 (67,9-93,9) | 69,2 (57,3-76,3) | 75,6 (61,8-83,7) | 66,7 (53,7-74,3) | 85,7 (70,9-94,5) |
| Изменения клетчаточных пространств (0,000) | 73,7 (57,6-84,3) | 84,6 (72,8-92,4) | 80,0 (66,4-89,0) | 77,8 (60,8-89,0) | 81,5 (70,1-89,0) |
Из таблицы 7 следует, что в диагностике экстракапсулярной экстензии аденокарциномы высоко информативными следует считать МР-симптомы изменения капсулы железы (чувствительность – 89,5%; специфичность – 76,9%, точность – 82,2%) и симптомы изменения контура железы (чувствительность – 84,2%; точность – 75,6%). МР-симптомы изменения клетчаточных пространств обладают наибольшей специфичностью (84,6%) и прогностичностью положительного результата (77,8%). Однако при сравнении указанных показателей статистически значимых различий не получено.Поэтому можно сделать вывод, что отсутствие МР-признаков изменения структуры капсулы железы и ее четкая визуализация, а также отсутствие деформации контура железы практически позволяли исключить инвазию опухоли в парапростатическую клетчатку. И с другой стороны, наличие МР-признаков облитерации клетчаточных пространств или выявление экстраорганного тканевого компонента опухоли в пределах парапростатической клетчатки указывали на экстракапсулярную экстензию опухоли.
В процессе работы был проведен анализ диагностической эффективности нативной МРТ и методики ДВИ в определении стадии местного распространения рака предстательной железы (табл. 8).
Таблица 8
Диагностическая информативность методики нативной МРТ и ДВИ в определении Т3а и Т3b стадий рака предстательной железы (n=40)
-
Экстракапсулярная
экстензия (Т3а)
Инвазия семенных
пузырьков (Т3b)
Нативная МРТ
(р<0,001)
ДВИ
(р=0,001)
Нативная МРТ
(р=0,009)
ДВИ
(р=0,004)
Se, % (95 ДИ)
87,5
(60,0-97,5)
75,0
(46,3-91,4)
60,0
(26,1-83,7)
62,5
(34,8-82,0)
Sp, % (95 ДИ)
93,8
(86,9-96,3)
90,6
(83,5-94,7)
94,3
(89,4-97,7)
90,6
(83,7-95,5)
Ac, % (95 ДИ)
92,5
(81,5-96,5)
87,5
(76,0-94,1)
90,0
(81,5-95,9)
85,0
(73,9-92,8)
NPV, % (95ДИ)
96,8
(89,7-99,4)
93,5
(86,1-97,8)
94,3
(89,4-97,7)
90,6
(83,7-95,5)
PPV, % (95 ДИ)
77,8
(53,4-86,7)
66,7
(41,2-81,3)
60,0
(26,1-83,7)
62,5
(34,8-82,0)
Как следует из таблицы 8, использование методики ДВИ в диагностике экстракапсулярной экстензии опухоли не приводило к значимому повышению диагностической информативности МР-исследования. Однако при выявлении признаков поражения семенных пузырьков использование методики ДВИ приводило к незначительному повышению чувствительности комплексной МРТ. Поэтому, выявление экстракапсулярной экстензии или инвазии опухоли в семенные пузырьки с применением методики ДВИ существенного изменения показателей диагностической информативности не демонстрировало, а, напротив, в случае поражения капсулы железы имело тенденцию к занижению степени распространения опухоли.Такие же расчеты произведены для анализа возможностей методики ДКУ (табл. 9).
Таблица 9
Диагностическая информативность нативной МРТ и МРТ с ДКУ в определении Т3а и Т3b стадий рака предстательной железы (n=87)
| | Экстракапсулярная экстензия (Т3а) | Инвазия семенных пузырьков (Т3b) | ||
| Нативная МРТ* | МРТ с ДКУ* | Нативная МРТ* | МРТ с ДКУ* | |
| Se, % (95 ДИ) | 73,3 (54,7-82,4) | 86,7 (67,5-95,8) | 70,0 (44,7-85,8)* | 90,0 (66,4-98,0)* |
| Sp, % (95 ДИ) | 97,2 (93,3-99,1) | 94,4 (90,5-96,3) | 96,1 (92,8-98,2) | 97,4 (94,3-98,4) |
| Ac, % (95 ДИ) | 93,1 (86,7-96,2) | 93,1 (86,5-96,3) | 93,1 (87,3-96,7) | 96,6 (91,1-98,4) |
| NPV, % (95ДИ) | 94,6 (90,8-96,4) | 97,1 (93,0-99,1) | 96,1 (92,8-98,2) | 98,7 (95,6-99,7) |
| PPV, % (95 ДИ) | 84,6 (63,1-95,1) | 76,5 (59,6-84,5) | 70,0 (44,7-85,8) | 81,8 (60,4-89,1)* |
* р<0,001
Из таблицы 9 следует, что использование методики МРТ с ДКУ позволило повысить чувствительность и прогностичность отрицательного результата при определении признаков экстраорганного местного распространения опухоли предстательной железы. При определении признаков инвазии опухоли в семенные пузырьки получено повышение эффективности при использовании методики МРТ с ДКУ. При этом, достоверное повышение наблюдали в показателях чувствительности. В связи с этим, можно утверждать, что наличие гиперваскулярной ткани в просвете семенного пузырька указывает на опухолевую инвазию. Однако, при определении признаков экстракапсулярной экстензии опухоли использование методики ДКУ приводило к парадоксальному снижению показателя специфичности и прогностичности положительного результата. Данное обстоятельство вероятно связано с ошибочной интерпретацией гиперваскулярной зоны параканкрозной реактивной гиперемии, как экстрапростатической опухоли. Поэтому, методика МРТ с ДКУ снижала информативность комплексной МРТ в определении экстрапростатической экстензии опухоли.
Для оценки диагностической информативности МРТ в выявлении метастатического поражения скелета проведен анализ данных МРТ 38 пациентов, у которых клинически подозревалось наличие метастатического поражения костей (уровень ПСА сыворотки крови более 20 нг/мл; боли в костях) (табл.10). В качестве референтных данных использовали результаты полипозиционной статической сцинтиграфии скелета с фосфатными соединениями, мечеными 99mТс (технеций).
Таблица 10
Диагностические показатели нативной МРТ в определении
костных метастазов при раке предстательной железы (М-критерий)
| | Se, % (95 ДИ) | Sp, % (95 ДИ) | Ac, % (95 ДИ) | PPV, % (95 ДИ) | NPV, % (95 ДИ) |
| Очаговое снижение интенсивности МР-сигнала на Т1-ВИ и Т2-ВИ (р=0,012) | 87,5 (81,2-91,7) | 66,7 (33,3-89,1) | 84,2 (73,7-91,3) | 93,3 (86,7-97,8) | 50,0 (24,9-66,8) |
| Локальное снижение интенсивности МР-сигнала на Т1-ВИ с зоной отека вокруг очага на Т2-ВИ с жироподавлением (р=0,005) | 81,3 (74,5-83,8) | 83,3 (47,5-96,9) | 81,6 (70,3-85,9) | 96,3 (88,3-99,3) | 45,5 (25,9-52,9) |
Из таблицы 10 следует, что при включении в симптомокомплекс метастатического поражения костной ткани МР-симптома отека костного мозга диагностические показатели существенно не изменялись, за исключением специфичности, которая повышалась в среднем на 16,6%. Однако, данное повышение не имело статистической значимости (р=0,183). Поэтому применение функции жироподавления может использоваться в дифференциальной диагностике ранее выявленных очагов изменения МР-структуры костей.
Таким образом, использование методик ДВИ, МР-спектроскопии и ДКУ, как дополнение к нативному МР-сканированию, не увеличивает диагностическую информативность МРТ в определении степени внутриорганного распространения опухоли. В определении экстракапсулярной экстензии опухоли основной методикой также является нативная МРТ (Т2-ВИ). При определении признаков инвазии опухоли в семенные пузырьки получено повышение эффективности МР-исследования при использовании методики ДКУ, с другой стороны, данная методика снижала информативность комплексной МРТ в определении экстракапсулярной экстензии опухоли. Применение функции жироподавления для поиска метастатического поражения скелета несколько облегчает дифференциальную диагностику ранее выявленных очагов.
На основании принципа первоочередного использования диагностических тестов с наибольшей чувствительностью и прогностичностью положительного результата, а затем методик с наибольшей специфичностью и прогностичности отрицательного результата, нами разработаны алгоритмы использования основных методик МР-исследования в диагностике опухолей внутренних половых органов у мужчин в различные периоды лечебно-диагностического процесса.
При первичном обследовании пациентов с подозрением на рак предстательной железы проводится не только выявление МР-симптомов, указывавших на рак предстательной железы, но и осуществляется комплексная оценка особенностей макроскопического строения внутренних половых органов (нативная МРТ) и особенностей функционирования на гистологическом (ДВИ, МРТ с ДКУ) и клеточном (МР-спектроскопия) уровнях. Полученные данные в совокупности дают всестороннюю характеристику внутренних половых органов и формируют условный «МР-паспорт» внутренних половых органов. Данные «МР-паспорта» используются для объективизации в процессе динамического наблюдения (контроль «МР-паспорта»).
МР-исследование пациентов после отрицательной биопсии имело несколько особенностей. Как было изложено выше, МР-исследование в период до 60 дней после проведенной биопсии мало эффективно в оценке внутриорганных изменений предстательной железы. Поэтому исследования в этот период могут проводиться с целью диагностики осложнений после биопсии. Проведение исследования в сроки более 60 дней после биопсии позволяло с большей эффективностью оценить изменения внутренних половых органах в постбиопсийный период (обновление «МР-паспорта»). Если же обновленные данные «МР-паспорта» подтверждают клинико-лабораторную картину рака предстательной железы, то такие пациенты могут подвергаться прицельной биопсии.
МР-исследование пациентов после положительной пункционной биопсии проводится с целью получения дополнительной информацию о внутриорганном и экстрапростатическом распространении опухоли, не дожидаясь срока регрессии постбиопсийных изменений (до 60 дней после биопсии). Реактивные изменения в ранний постбиопсийный период характеризуются умеренным отеком и геморрагическим пропитыванием паренхимы и капсулы железы, а иногда и парапростатической клетчатки, несмотря на это при нативной МРТ возможно визуализировать распространение опухоли за пределы капсулы железы. Также при нативной МРТ в ранний постбиопсийный период возможно заподозрить наличие тканевого компонента опухоли в просвете семенного пузырька. Кроме того, нативная МРТ позволяет визуализировать увеличенные лимфатические узлы, очаговое изменение структуры костей таза и позвоночника, указывающие на регионарное или отдаленное метастазирование опухоли. При этом, наличие выраженного геморрагического компонента в ткани предстательной железы не позволяет эффективно использовать методики ДВИ и МР-спектроскопии.
Контрастное усиление используется при обнаружении внутрипузырькового тканевого содержимого для проведения дифференциальной диагностики геморрагического постбиопсийного сгустка и опухоли, которая в отличие от сгустка демонстрирует накопление контрастного препарата.
Поэтому в ранний постбиопсийный период, если необходимо провести МР-исследование с целью характеристики внутренних половых органов, то объем исследования целесообразно сократить до применения нативного МР-сканирования с возможным контрастированием.
В поздний постбиопсийный период подобные проблемы возникают значительно реже, поэтому объем МР-исследования расширяется до максимального (нативная МРТ, ДВИ, МР-спектроскопия, МРТ с ДКУ). Целью такого МР-исследования является регистрация или обновление т.н. «МР-паспорта» внутренних половых органов и определение степени распространенности аденокарциномы.
Алгоритмы МР-исследования при контроле эффективности лечения рака предстательной железы зависят от вида проводимого лечения (консервативная антиандрогенная терапия или простатэктомия) и их сроков (рис.1).
МР-исследование пациентов при консервативной терапии проводится при клинических и лабораторных данных, указывающих на вероятность прогрессии рака предстательной железы или на недостаточность ее метаболической супрессии. Для полноценной характеристики внутренних половых органов проводится полный спектр МР-исследования, включенных в т.н. «МР-паспорт». Задачи использования методик МР-исследования зависят от периода проводимой терапии (до 6 недель; от 6 до 34 недель; более 34 недель).
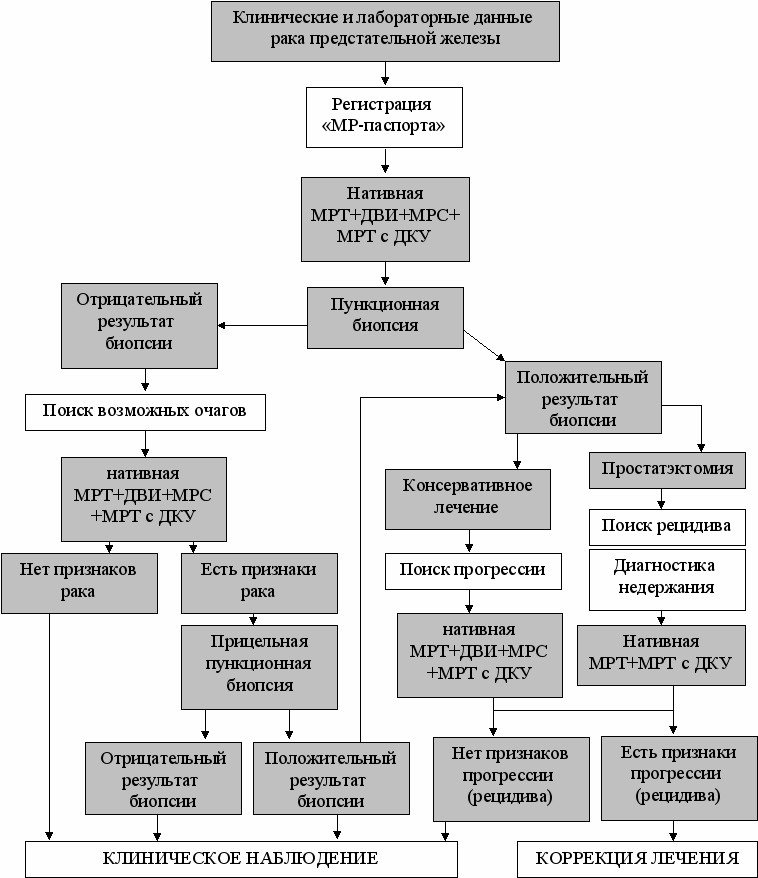
Рис. 1. Схема алгоритма МР-исследования пациентов в диагностике рака предстательной железы (объяснение в тексте).
При нативной МРТ определяются особенности макроскопического строения внутренних половых органов и выявляются признаки местного, регионарного отдаленного метастазирования опухоли.
Методика ДВИ служит дополнительной для дифференцирования опухолевой ткани на фоне выраженного атрофического процесса в железе.
МР-спектроскопия позволяет оценить полноценность проводимой антиандрогенной блокады, а также выявить участки гиперметаболизма, которые соответствуют продолженному росту аденокарциномы.
Методика МРТ с ДКУ наиболее эффективна в выявлении прогрессирования рака при условии первоначальной гиперваскулярности очага аденокарциномы.
МР-исследование пациентов после простатэктомии может проводиться в ранний (в течение 7 дней после операции), поздний и в отсроченный (в сроки более 6 месяцев) послеоперационные периоды. Целью исследований в ранний послеоперационный период является визуализация изменений после проведенной операции и поиск морфологического субстрата при клинических симптомах осложнений (кровотечение, несостоятельность анастомоза, воспаление).
Тяжелое состояние пациента и отсутствие железистой ткани обуславливают сокращение объема применяемых методик до использования одной нативной МРТ.
МР-исследование в поздний период не является высоко эффективным в поиске рецидива опухоли при использовании методик нативного МР-сканирования, ДВИ и МР-спектроскопии, а имеющаяся гранулематозная ткань может имитировать при проведении методики МРТ с ДКУ гиперваскулярность, характерную также для рецидива опухоли.
Целью МР-исследования в поздний послеоперационный период наиболее часто является поиск осложнений, не связанных напрямую с проведенной операцией.
МР-исследование в отсроченный период после проведенной операции также может быть сокращено до использования нативного МР-сканирования и методики МРТ с ДКУ, которая позволяет визуализировать рецидив опухоли по участку гиперваскулярности в зоне операции, т.к. гранулематозная ткань к этому сроку уже инволюционирует и представляет собой гиповаскулярные фиброзные рубцы.
ВЫВОДЫ
- Разработанная концепция и методика комплексного МР-исследования с использованием эндоректальной катушки обеспечивает получение полной и объективной характеристики нормального строения и патологических изменений внутренних половых органов у мужчин.
- МР-симптомы сохранности эластичности предстательной железы и семенных пузырьков являются дополнительными дифференциально-диагностическими критериями их нормальной МР-анатомии. По особенностям строения семенные пузырьки делятся на три типа: мезоморфный, долихоморфный или асимметрический. Межпротоковая зона характеризуется метаболической неоднородностью, что потенциально затрудняет диагностику патологических изменений при МР-спектроскопии.
- МР-семиотика патологических изменений внутренних половых органов характеризуется четырьмя основными комплексными характеристиками: симптомы изменения положения и подвижности; симптомы изменения общего вида и эластичности; симптомы структурной, в том числе метаболической и перфузионной трансформации; а также симптомы изменения других внутритазовых структур.
- Для аномалий внутренних половых органов гипопластического типа свойственно уменьшение их размеров и фиброзно-дегенеративная трансформация предстательной железы, что проявляется отсутствием зональной дифференцировки, снижением интенсивности МР-сигнала, снижением ИКД и уровня Ci. Кистозно-диспластические аномалии характеризуются выявлением при МР-исследовании разнокалиберных кист.
- Хроническое воспаление внутренних половых органов характеризуется утратой зональной дифференцировки, мозаичностью метаболических нарушений при МР-спектроскопии, неоднородностью васкуляризации предстательной железы при МРТ с ДКУ, а также рубцово-атрофической трансформацией семенных пузырьков. Дегенеративно-гиперпластические изменения внутренних половых органов характеризуется увеличением объема предстательной железы по округлому или вытянутому типам, деформацией и образованием псевдокапсулы. Периферическая зона истончена и имеет реактивные атрофические изменения, которым не свойственно специфическое отображение на ДВИ и МР-спектроскопии. Семенные пузырьки трансформируются по обструктивному или атрофическому типам.
- Комплексное МР-исследование является высокоэффективным в выявлении рака предстательной железы. Использование комплекса МР-методик позволяет повысить чувствительность, специфичность, точность диагностики рака предстательной железы по сравнению с нативным МР-сканированием на 14,9%, 13,0% и 14,2% до 97,3%, 92,5% и 95,2%, соответственно. Диагностика рака предстательной железы основана на сочетании данных нативного МР-сканирования в виде снижения ее эластичности, локального снижения интенсивности МР-сигнала, локального снижения ИКД на ДВИ, снижения Ci и отношения ((Сho+Cr)/Ci) при МР-спектроскопии, а также быстрым накоплением контрастного препарата при ДКУ. Выраженность снижения Ci и подъема отношения ((Сho+Cr)/Ci) соответствуют степени злокачественности опухоли.
- Комплексное МР-исследование является объективным методом контроля эффективности проводимой консервативной терапии и оперативного лечения рака предстательной железы, а также позволяет выявить послеоперационные осложнения, признаки рецидива и прогрессирования опухоли. Наиболее эффективными критериями оценки метаболической супрессии при антигормональной терапии рака являются потеря объема железы при нативном МР-сканировании и прогрессирующее снижение Ci при МР-спектроскопии. О прогрессировании рака предстательной железы при консервативной терапии достоверно свидетельствует локальное повышение уровня Ci. Выявление послеоперационных осложнений (кровотечение, несостоятельность анастомозов, недержание мочи) базируется на данных нативного МР-сканирования. Признаком рецидива рака предстательной железы является обнаружение зоне операции через 6 месяцев гиперваскулярной ткани.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- При проведении МРТ пациентам с клинической симптоматикой рака предстательной железы следует использовать эндоректальную катушку.
- При первичном МР-исследовании внутренних половых органов у мужчин целесообразно выполнять следующие методики комплексного МР-исследования, составляющие «МР-паспорт»: нативное МР-сканирование, методику ДВИ, МР-спектроскопию, МРТ с ДКУ. При повторном проведении МР-исследования оценка изменений должна осуществляться на основе сопоставления данных «МР-паспорта».
- Допускается сокращение методик комплексного МР-исследования с использованием абдоминальной катушки при патологии прямой кишки и тяжелом общем состоянии пациента.
- Для сокращения общего времени исследования рекомендуется в базовом наборе протоколов использовать только один протокол Т1-ВИ, при этом зону сканирования целесообразно расширять до границ таза.
- При проведении методики ДВИ следует ограничиваться тремя факторами диффузии (b): 0 или 50; 600-800 и 1100-1200. При этом, сокращается время сканирования и повышается наглядность визуализации опухолевой ткани.
- Для снижения количества артефактов при выполнении МР-спектроскопии (3D-csi) рекомендуется использовать TE=120 мс и не менее 8 сатураторов с ближайшим расположением к капсуле железы. Позиционирование блока спектроскопии должно строго соответствовать плоскостям полученных ранее Т2-ВИ.
- Для повышения наглядности накопления контрастного препарата при МРТ с ДКУ рекомендуется использовать прием субтракции первой (доконтрастной) серии и последующих серий изображений. Сокращение времени исследования и повышение качества графика интенсивность-время достигается увеличением толщины среза до 3,0 мм и сокращением одной серии до 6 секунд. При этом длительность сканирования при МРТ с ДКУ целесообразно ограничивать 180-200 секундами.
- В качестве референтных зон при построении графиков интенсивность-время целесообразно использовать следующие участки: просвет подвздошной артерии (эталон гиперваскулярности и времени доставки контрастного препарата); участок внутренней запирательной мышцы (эталон гиповаскулярности); контралатеральный зоне поражения участок железы (эталон фоновых изменений).
- При подозрении на острый простатит или абсцесс внутренних половых органов, а также при диагностике ранних послеоперационных осложнений МРТ необходимо ограничивать нативным МР-сканированием с использованием поверхностной катушки.
- Для повышения эффективности диагностики опухолевого поражения семенных пузырьков рекомендуется использовать методику ДКУ и функцию субтракции до- и постконтрастных изображений.
- В период до 2 месяцев после пункционной биопсии МР-исследование в оценке внутриорганных изменений при раке предстательной железы проводить нецелесообразно.
- Для выявления признаков рецидива рака следует использовать методику МРТ с ДКУ, но не ранее, чем через 6 месяцев после простатэктомии.
- Комплексное МР-исследование пациентов с клинической симптоматикой рака предстательной железы при динамическом контроле рекомендуется проводить раз в 1-2 месяца. Сокращение этого срока нежелательно из-за неопределенности изменений и повышения риска ложноположительных и ложноотрицательных результатов.
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ ПО ТЕМЕ ДИССЕРТАЦИИ
- Ратников, В.А. Методика и возможности визуализации органов малого таза на магнитном томографе Magnetom Symphony 1.5 / В.А. Ратников, Г.Е. Труфанов, В.В. Рязанов, Н.В. Марченко, А.В. Мищенко, А.Г. Атаев, А.В. Одинцов, А.Н. Кириллов // Научно-практическая конференция «Актуальные вопросы лучевой диагностики заболеваний и повреждений у военнослужащих» и вторая конференция «Спиральная компьютерная томография –XXI век»: Сборник статей научной сессии, СПб., Нордмед-Издат. – 2001. – 260 с. – С. 143-146.
- Ратников, В.А. Опыт использования магнитно-резонансной томографии в диагностике опухолей мочевыделительной системы / В.А. Ратников, В.М. Черемисин, В.В. Рязанов, А.В. Мищенко, Е.Л. Перегудова, Н.В. Марченко, А.Н. Кириллов // V Всероссийская научно-практическая конференция «Актуальные вопросы диагностики и лечения в многопрофильном лечебном учреждении»: Тезисы докладов. – СПб., 2001. – С. 252.
- Mishchenko, A.V. MR-urography in the diagnosis of urinary tract pathology / A.V. Mishchenko, N.V. Martchenko, V.A. Ratnikov, V.V. Ryazanov, I.V. Pyanov, V.A. Fokin // Eur. Radiol. – 2002. – Vol. 12, № 2, Suppl.1. – P.402.
- Mishchenko, A.V. Hematuria: possibilities MRI in definition of its causes / A.V. Mishchenko, V.M. Cheremisin, V.V. Riazanov, S.B. Petrov // Eur. Radiol. – 2003. – Vol.13, № 2, Suppl.1. – P. 402.
- Петров, С.Б Сравнительная характеристика простат-специфического антигена, пальцевого ректального, трансректального ультразвукововго исследований и магнитно-резонансной томографии эндоректальной катушкой в диагностике рака предстательной железы / С.Б. Петров, А.В. Мищенко, А.В. Куренков, Д.В. Фадеев, К.Х. Чибиров // Юбилейная конференция «Современная лучевая диагностика в многопрофильном лечебном учреждении»: Материалы. – СПб., 2004. – С. 205-206.
- Шпиленя, Е.С. Магнитно-резонансная томография эндоректальной катушкой в диагностике интраэпителиальной неоплазии и ранних форм рака предстательной железы / Е.С. Шпиленя, С.Б. Петров, В.В. Протощак, А.В. Мищенко, И.Г. Рагимов, Н.Д. Кубин // Юбилейная конференция «Современная лучевая диагностика в многопрофильном лечебном учреждении»: Материалы. – СПб., 2004. – С. 318-319.
- Фокин, В.А. Основы и клиническое применение магнитно-резонансной томографии (пособие) / В.А Фокин, А.В.Мищенко, Г.Е. Труфанов // Сборник учебных пособий по актуальным вопросам лучевой диагностики и лучевой терапии / Под ред. проф. Г.Е. Труфанова. – СПб.: «ЭЛБИ-СПб», 2004. – С. 5-44.
- Петров, С.Б. Сравнительная характеристика простатспецифического антигена, пальцевого ректального, трансректального ультразвукового исследований и магнитно-резонансной томографии эндоректальной катушкой в диагностике рака предстательной железы / С.Б. Петров, Е.С. Шпиленя, А.В. Мищенко // Онкологическая урология: от научных исследований к кинической практике (современные возможности диагностики и лечения опухолей предстательной железы, мочевого пузыря и почки): Материалы конференции. – М., 2004. – С. 79.
- Труфанов, Г.Е. Роль магнитно-резонансной томографии с использованием эндоректальной катушки в выявлении интраэпителиальной неоплазии и ранних стадий рака предстательной железы / Г.Е. Труфанов, С.Б. Петров, В.В. Протощак, А.В. Мищенко, И.Г. Рагимов // Невский радиологический форум «Наука - клинике»: Материалы конгресса. – СПб.. – 2005. – С. 43-44.
