Лекція Склад І будова комплексних сполук. Природа хімічного зв’язку в комплексних сполуках Вже у першій половині XIX ст вчені помітили, що деякі сполуки, в яких атоми начебто вичерпали свої валентні можливості, здатні до подальшого сполучення між собою.
| Вид материала | Лекція |
| Проста речовина Лабораторні методи добування кисню Фізичні властивості. Хімічні властивості. |
- Методи синтезу, властивості та систематика координаційних сполук, 265.45kb.
- А Виникнення термодинаміки, 229.77kb.
- Реферат роботи Михальської В. М. на тему: "Вплив комплексних сполук міді на клінічний, 88.3kb.
- Зміст Частина перша, 194.3kb.
- Реферат з хімії, 99.66kb.
- План комплексних заходів з екологічної освіти І виховання та формування екологічної, 99.84kb.
- На основі взаємозвязку між термодинамічними, 509.6kb.
- В. І. Вернадський ще в першій половині XX століття передбачав, що біосфера розвинеться, 50.35kb.
- Мозок. Різновиди та будова. Будова та функції спинного мозку, 99.22kb.
- Тема. Становище українських земель у складі Російської імперії наприкінці X viii - першій, 22.34kb.
Проста речовина
Добування. Основним промисловим методом добування кисню є виділення його з повітря за допомогою скраплення останнього та фракційної дистиляції. Оскільки кисень є газом, щоб його перевести у рідкий стан газ необхідно спочатку охолодити до температури, нижчої за критичну, яка досить низька (-118 °С), а потім піддати дії високого тиску.
Кисень має вищу температуру кипіння (-183 °С) порівняно з азотом (-196 °С), тому під час дистиляції азот випаровується і збирається для використання, а кисень залишається в рідкому стані в нижній частині ректифікаційної колони. Такий кисень містить незначні домішки азоту, вуглекислого газу ти близько 3 % аргону, який має близьку до кисню температуру кипіння (-186 °С).
Кисень високого ступеня чистоти добувають електролізом води. Цей метод використовують переважно для добування водню (катодний процес), але одночасно на аноді одержують другий корисний продукт - кисень.
Кисень зберігають і транспортують під тиском 15 МПа у стальних балонах, пофарбованих у блакитний колір з чорним написом «Кисень». Великі кількості кисню зберігають у скрапленому стані. Для цього використовують спеціальні ємкості (так звані танки), які мають ефективну теплоізоляцію.
Лабораторні методи добування кисню ґрунтуються на розкладі багатих на нього, але відносно нестійких хімічних сполук. Наприклад, кисень можна одержати під час термічного розкладу перманганату калію КМnО4, хлорату калію КСlO3 (за наявності каталізатора, наприклад МnO2, Fe2О3, Сr2О3), нітратів, оксидів металів тощо:
2KC1O3 2KC1 + 3O2;
2KMnO4 K2MnO4 + MnO2 + O2;
2KNO3 2KNO2 + O2;
2HgO 2Hg + O2.
Зручним способом лабораторного добування кисню є розклад гідроген пероксиду за наявності каталізатора МnО2:
2Н2О2 = 2Н2О + О2.
Фізичні властивості. Вільний кисень складається з двохатомних молекул O2. Внаслідок ковалентної природи зв' язку кисень є типовим газом з низькими температурами кипіння (-183 °С) та плавлення (-218,7 °С). Газоподібний кисень безбарвний, не має запаху і смаку, у рідкому та твердому станах має блідо-синє забарвлення.
У 100 об’ємах води за температури 0°С розчиняється близько 5 об’ємів кисню, за 20 °С - близько 3 об’ємів (або 0,004 % (мас.)).
Води гідросфери вміщують 1,5 -1013 т розчиненого кисню. Він легко розчиняється в органічних розчинниках, тому простого переливання таких рідин на повітрі достатньо для насичення їх киснем. Кисень здатний також розчинятися у деяких розплавлених металах (сріблі, платині, золоті, паладії). Так, один об’єм срібла вбирає близько 10 об’ємів кисню.
Низькі температури кипіння і плавлення кисню пояснюють тим, що молекула О2 неполярна і має малу здатність до поляризації. Це зумовлює існування в конденсованих станах речовини лише слабких сил дисперсійної міжмолекулярної взаємодії, які легко долаються вже за відносно низьких температур. Саме тому неполярні і малополяризовані молекули кисню мають низьку розчинність у поляризованій воді.
Довжина хімічного зв'язку в молекулі О2 становить 120,7 пм, що істотно менше за довжину одинарного ковалентного зв' язку О—О. Наприклад, у молекулі Н—О—О—Н вона становить 149 пм. Згідно з цим енергія зв' язку в молекулі O2 велика і становить 494 кДж/моль, що значно перевищує енергію одинарного зв’язку О—О (в молекулі Н—О—О—Н вона становить 210 кДж/моль.)- Цим пояснюють той факт, що гемолітична дисоціація молекул кисню на атоми розпочинається лише за температури понад 1500 °С. Вона може відбуватися також у разі вбирання ультрафіолетового випромінювання (фотоліз). Тому біля земної поверхні кисень в атмосфері перебуває у молекулярному стані О2, а вище за 100 км основною формою існування кисню стає атомарний. Молекули О2 розщеплюються тут на атоми під впливом ультрафіолетового випромінювання Сонця.
Молекула кисню парамагнітна, наявність парамагнетизму відповідає розміщенню на молекулярній орбіталі двох неспарених електронів. Внаслідок парамагнетизму рідкий і твердий кисень притягається магнітним полем.
Утворення хімічних зв' язків у молекулі О2 та деякі її властивості пояснює метод молекулярних орбіталей. Так, мала-довжина зв' язку між атомами О-О та висока його енергія зумовлені тим, що кратність зв' язку в молекулі кисню О2 дорівнює 2.
Парамагнітні властивості молекули О2 спричинені наявністю двох неспарених електронів, які, за правилом Хунда, займають дві окремі вироджені розпушувальні молекулярні орбіталі. Атом кисню порівняно з молекулою має більшу енергію іонізації (відповідно 1313 і 1165 кДж/моль), оскільки у разі іонізації молекули О2 електрон відщеплюється з енергетично вищої (ніж атомні) розпушувальної молекулярної орбіталі. Утворення молекулярних іонів О2+, О2- та О22- можливе тому, що число зв' язувальних електронів перевищує число розпушувальних (кратність зв’язку більша за нуль).
На Землі виявлено три стабільні нукліди кисню:
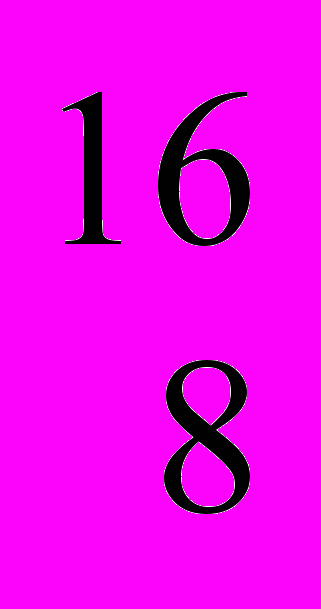 О (99,759 % (мас.)),
О (99,759 % (мас.)), 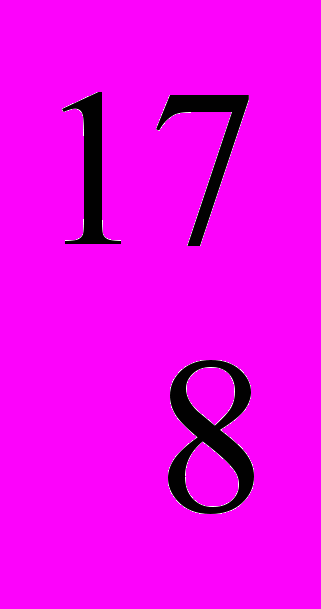 О (0,037 % (мас.)) та
О (0,037 % (мас.)) та 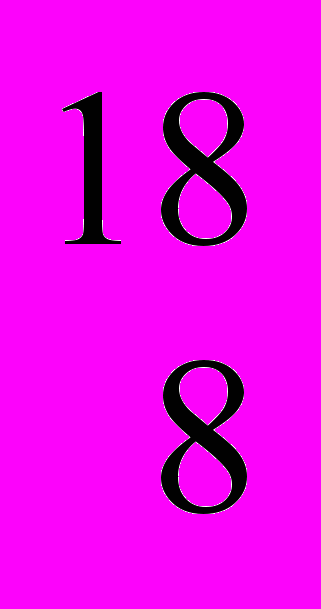 О (0,204 % (мас.)). Штучно одержано три радіоактивні нукліди кисню, період піврозпаду яких не перевищує десятків секунд.
О (0,204 % (мас.)). Штучно одержано три радіоактивні нукліди кисню, період піврозпаду яких не перевищує десятків секунд.Кисень має алотропну модифікацію — озон О3.
Хімічні властивості. Кисень характеризується високою хімічною активністю і належить до типових окисників. Він реагує з більшістю простих речовин, найчастіше утворюючи оксиди, в яких має ступінь окиснення -2. Такі реакції зазвичай відбуваються з досить великою швидкістю лише за підвищених температур, оскільки потребують активації молекул О2:
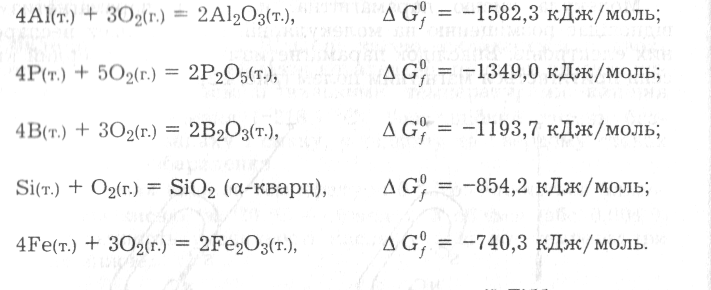
Великі від’ємні значення стандартної енергії Гіббса утворення багатьох оксидів свідчать про значну спорідненість цих елементів до кисню.
Кисень безпосередньо не окиснює лише благородні гази, деякі метали (золото, платину) та галогени. Для таких систем зміна енергії Гіббса має додатне значення, наприклад G°(Au2О3(т)) = 79 кДж/моль, G°(ClO2(г.))=122 кДж/моль.
Проте оксиди цих елементів, за винятком гелію, неону та аргону, можна одержати непрямим шляхом, наприклад:
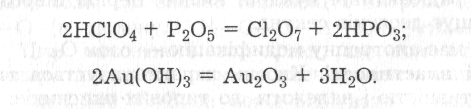
Оксиди можуть утворюватися не лише під час окиснення киснем простих речовин. Багато складних речовин за певних умов також взаємодіє з киснем. При цьому утворюються оксиди елементів, а іноді й оксиди, і прості речовини, наприклад:
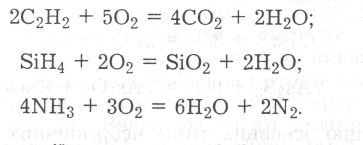
Здебільшого реакції окиснення відбуваються з достатньою швидкістю лише за підвищеної температури, оскільки потрібна деяка енергія для активації молекул O2.
Якщо окиснення речовин відбувається енергійно, з виділенням великої кількості теплоти і світла, то такі процеси називають горінням. Вони відбуваються, як правило, за умови надлишку повітря або чистого кисню і завершуються утворенням кінцевих продуктів окиснення (СО2, Н2О, SО2, Р2О5, N2 тощо). Наприклад, під час горіння ацетилену в середовищі кисню температура полум'я досягає 3200 °С.
Відносно повільні реакції окиснення залежно від характеру речовини називають іржавінням (окиснення металів), тлінням (окиснення органічних решток), а найчастіше просто окисненням.
Майже 90 % кисню, що потрапляє в організм людини, використовується під час дихання як акцептор електронів. Енергію, що виділяється в разі окиснення різних субстратів молекулярним киснем, організм використовує для синтезу життєво необхідного аденозинтрифосфату (АТФ). М’яке окиснення молекулярним киснем різних субстратів у живих організмах є основним джерелом енергії для забезпечення перебігу процесів життєдіяльності.
Про значну окиснювальну здатність кисню у водних розчинах свідчить високе значення стандартного електродного потенціалу його відновлення до води:
О2 + 4Н+ + 4е- = 2Н2О, Е° = 1,23 В (при рН = 0).
Для пірометалургійних способів добування металів та деяких неметалів широко використовують процес окиснювального випалювання природних сульфідних мінералів з метою їх переведення у відповідні оксиди (далі оксиди відновлюють до простих речовин), наприклад:
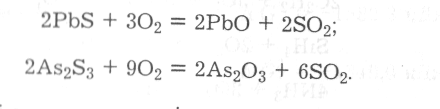
Класифікацію основних типів неорганічних сполук кисню за ступенями його окиснення подано наведеною нижче схемою:
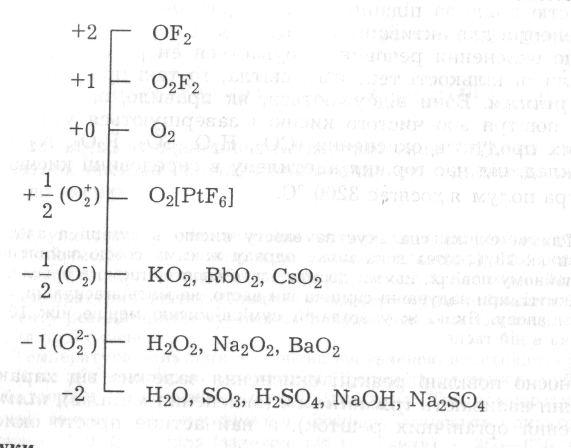
Оксиди. Загальні методи добування оксидів вам відомі із курсу хімії середньої школи.
Взагалі утворення одноатомних багатозарядних аніонів типу Еn- енергетичне невигідне. З цієї причини не існує сполук, до складу яких входять вільні іони О2-. Навіть у кристалічних оксидах найактивніших металів (Na2О, СаО тощо) ефективний негативний заряд атома кисню істотно менший за -2.
В оксидах неметалів різниця між електронегативностями атомів кисню і неметалу невелика, тому хімічний зв' язок у них ковалентний полярний. Більшість таких сполук за звичайних умов — гази, леткі рідини або легкоплавкі тверді речовини. Це пояснюється тим, що вони в твердому стані утворюють, як правило, молекулярні кристалічні ґратки зі слабкими силами міжмолекулярної взаємодії. Навпаки, оксиди з полімерними структурами значно міцніші і більш тугоплавкі. До таких речовин належить, наприклад, SiO2. Він має полімерну структуру, в якій кожен атом силіцію сполучений з чотирма атомами кисню (відбувається sр3-гібридизація валентних орбіталей атомів силіцію) й утворює тетраедр, а кожен атом оксигену, у свою чергу, сполучений з двома атомами силіцію. Внаслідок цього полімерний SіО2 на відміну від мономерного СО2 за звичайних умов хімічно неактивний і має високу температуру плавлення (1700 °С). В оксидах неметалів валентні орбіталі атомів кисню найчастіше перебувають у стані sр3-гібридизації.
Оксиди неметалів за хімічною природою кислотні. Більшість із них розчиняється у воді з утворенням відповідних кислот, тому їх називають ангідридами кислот:
СO2 + Н2O Н2СO3;
SО3 + Н2О Н2SО4.
Оксиди найактивніших металів мають переважно іонний зв'язок і за хімічною природою основні. До найтиповіших з них належать оксиди лужних і лужноземельних металів, їм відповідають гідроксиди, які є сильними основами.
У міру зростання ступеня окиснення металу збільшується частка ковалентності в його хімічному зв'язку з киснем. Такі оксиди з іонно-ковалентним зв'язком амфотерні, їм відповідають амфотерні гідроксиди, здатні дисоціювати за типом слабких основ за місцем зв' язку Ме—ОН і за типом слабких кислот — за місцем зв' язку МеО—Н. До таких оксидів належать переважно оксиди металів, які мають відносно невелику електронегативність, наприклад А12О3, Сr2О3, РbО, ZпО, Fе2О3 тощо. Залежно від умов вони виявляють властивості основних або кислотних оксидів. Амфотерні оксиди з водою не взаємодіють (не розчиняються), але можуть реагувати як з кислотами, так і з лугами, а під час нагрівання — з основними та кислотними оксидами з утворенням солей.
Оксиди металів (d-елементів) з високими ступенями окиснення мають ковалентний характер зв' язків між атомами в молекулах (СrО3, Мn2О7, Rе2О7, ОsО4 тощо). Частина з них розчиняється у воді з утворенням гідратів, які дисоціюють за типом кислот за місцем найбільш полярного зв' язку Н—О:
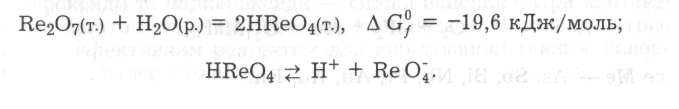
Перелічені оксиди мають кислотну природу і також належать до ангідридів кислот.
Перехідні елементи здатні утворювати нестехіометричні оксиди, їхні кристалічні ґратки складаються зі щільно упакованих іонів оксиду, а частина пустот такої структури заповнена іонами металу, наприклад FеО1-x (х=0,05-0,10). Існують також неcтехіометричні оксиди, у кристалічних ґратках яких пустоти наповнені надлишковим, тобто надстехіометричним киснем, наприклад U2+Х (х = 0,00—0,30).
На початкових стадіях реакцій металів з киснем можуть утворюватися субоксиди — сполуки з металічним зв' язком. Вони є продуктом вкорінення атомів оксигену в кристалічні ґратки металів, наприклад Ті6О, Ті3О.
Хімічні властивості води. Відносно нагрівання вода є досить, стійкою сполукою. Вона практично не розкладається під час нагрівання до температури 1200 °С, і тільки за вищих температур термічне дисоціює на атом Н і групу -ОН. За температури 5000 °С вода розкладається з вибухом.
Відносно різноманітних хімічних сполук вода поводить себе як досить активний реагент. Вона може реагувати з речовинами як неорганічного, так і органічного походження. Під час взаємодії з ними вона може руйнуватися або залишатися незмінною.
Найхарактернішими для води є хімічні реакції, наведені нижче.
1.Приєднання основних та кислотних оксидів з утворенням основ і кислот:
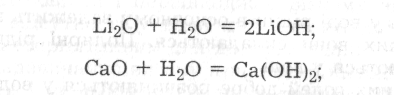
2. Приєднання до основ, кислот і солей з утворенням кристалогідратів, наприклад: КОНН2О, Н2SО42Н2О, Nа2SО410Н2О.
3.Окиснення за рахунок водню в ступені окиснення +1 сильних відновників за звичайних умов або за високої температури
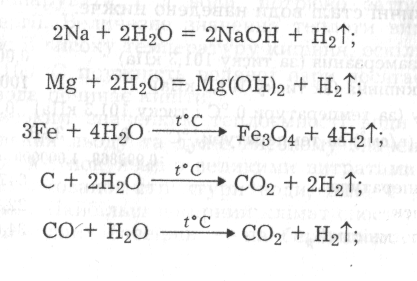
4.Відновлення за рахунок кисню в ступені окиснення -2. Наприклад, водяна пара горить у середовищі фтору:
F2 + Н2О = 2НF + О.
5.Участь у донорно-акцепторних взаємодіях. За рахунок донорних властивостей атома оксигену, який має дві неподілені пари електронів, вода часто відіграє роль ліганда в реакціях комплексоутворення. Вона може бути і донором протона, тому в кислотно-основних перетвореннях відіграє роль амфоліту:
Н+ + Н2О Н3О+.
Згідно з протонною теорією кислот і основ Й. Н. Бренстеда (1879-1947) в цій реакції вода є основою. Відносно електролітів, здатних приєднувати протон, вода поводить себе як кислота, наприклад:
NН3 + Н2О NH4+ + ОН-.
Вона утворює велику кількість аквакомплексів:
Сu2++4Н2О=[Сu(Н2О)4]2+;
Сr3+ + 6Н2О = [Сr(Н2О)6]3+.
Вода може не лише створювати середовище, а й бути безпосереднім учасником окисно-відновних реакцій:
С12 + Н2О НС1 + НОСl;
2КМnО4 + 3К2SО3 + Н2О = 2МnО2 + 3К2SО4 + 2КОН.
Чиста вода є дуже слабким електролітом і майже не проводить електричний струм. Іонний добуток води за температури 22 °С відповідає стану рівноваги:
Н2О Н+ + ОН-,
і дорівнює Кв = [Н+][ОН-] = 10-14.
У водних розчинах зазначену рівновагу дисоціації можна змінювати у той чи інший бік не лише розчиненням у воді кислот і лугів, а й солей слабких кислот або основ (гідроліз солей):
Fе3+ + Н2О FеОН2+ + H+;
РО43- + Н2О HРО42-+ ОН-.
Внаслідок цих реакцій змінюється концентрація протонів або гідроксил-іонів.
Відомо багато сполук, які повністю розкладаються водою, наприклад:
Аl2S3 + 6Н2О = 2А1(ОН)3 + 3Н2S;
РС13 + 3Н2О = Н3РО3 + 3НС1.
Важка вода. Сполуку D2О (оксид дейтерію) називають важкою водою. Вперше її одержали у 1933 р. американські хіміки Г. Н. Льюїс (1875-1946) та Ф. Г. Спеддінг (1902-1989) електролізом лужного розчину. Вміст її у морській воді становить близько 0,018 %, тому для добування 1 кг важкої води необхідно розкласти 170 т звичайної води. Одержують D2О електролізом звичайної води (іони дейтерію розряджаються повільніше, ніж іони протію), фракційною дистиляцією рідкого водню та іншими методами. Температура її плавлення становить 3,8 °С, густина — 1,104 г/см3, температура кипіння 101,43 °С, іонний добуток — 0,2-10"14. Біологічні процеси у важкій воді відбуваються дещо повільніше, ніж у звичайній.
Виробляють важку воду у великих кількостях, її широко використовують в атомній енергетиці. В ядерних реакторах її застосовують для уповільнення нейтронів.
Гідроген пероксид. Пероксид водню є однією з найважливіших сполук кисню. У промисловості його добувають електрохімічними та хімічними способами. Для електрохімічного добування Н2О2 використовують розчини сірчаної кислоти або її солей (зокрема, (NН4)2SО4). У цьому разі електролізу піддають 50 %-й розчин Н2SО4 за високої густини струму та охолодження. За таких умов на платиновому аноді окиснюються гідросульфат-іони до пероксодисірчаної кислоти Н2S2О8:
2НSО4- = Н2S2О8 + 2е.
Слабке нагрівання розчину Н2S2О8 сприяє перебігу процесу гідролізу, внаслідок чого утворюється Н2О2:
Н2S2О8 + 2Н2О = Н2О2 + 2Н2SО4.
Хімічні методи добування Н2О2 ґрунтуються на окисненні киснем органічних сполук, наприклад таких, як алкільні похідні антрагідрохінону та ізопропіловий спирт.
Пероксид водню легко утворюється з пероксиду барію під дією на нього розбавленого розчину сірчаної кислоти:
ВаО2 + Н2SО4 = Н2О2 + ВаSО4.
Осад нерозчинного у воді ВаSО4 повністю відокремлюється від розчину Н2О2 звичайним фільтруванням.
У промисловості добувають пероксид водню концентрацією, яка не перевищує 60 %, оскільки більш концентровані його розчини вибухонебезпечні при транспортуванні. 30%-й стабілізований розчин Н2О2 називають пергідролем. Для медичних цілей застосовують 3%-й розчин Н2О2. Щорічне світове виробництво пероксиду водню становить 0,5 млн тонн.
Пероксид водню високого ступеня чистоти та його розчини за звичайних умов досить стійкі й можуть зберігатися протягом тривалого часу, але під час нагрівання, в разі ультрафіолетового опромінення, а також за наявності іонів перехідних металів Н2О2 інтенсивно розкладається з виділенням кисню. Чистий Н2О2 та його концентровані розчини розкладаються бурхливо, часом з вибухом.
Для запобігання розщепленню Н2О2 до його розчину додають стабілізатори (звичайно фосфати натрію), які зв’язують шкідливі іони металів і тим самим гальмують небажаний процес, їх зберігають у прохолодному місці у темних посудинах. При цьому слід мати на увазі, що луги, навіть у кількостях, що вилуговуються зі звичайного скла, істотно прискорюють розщеплення молекули Н2О2.
Молекула Н2О2 нелінійна, два зв’язки О-Н розміщені у двох площинах під кутом 120°:
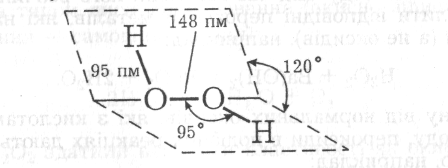
Внаслідок несимметричного розміщення зв’язків О-Н молекула Н2О2 дуже полярна.
Наявність неподілених електронних пар у атомів оксигену створює можливість донорно-акцепторної взаємодії. Так, подібно до води, пероксид водню може входити до складу кристалічних речовин, наприклад Ка2СО31,5Н2О2Н2О.
Рідкий і твердий пероксиди водню, а також його розчини у воді характеризуються наявністю стійких водневих зв'язків, які спричиняють асоціацію молекул. Тому за звичайних умов чистий пероксид водню — сиропоподібна в'язка блідо-блакитна рідина без запаху, яка майже в 1,5 раза важча за воду. Тиск пари Н2О2 нижчий за тиск пари води (за однакової температури), тому температура кипіння пероксиду водню вища і становить 150,2 °С. На цій властивості ґрунтується відокремлення Н2О2 від води шляхом фракційної перегонки. Слід також зазначити, що температуру кипіння Н2О2 за атмосферного тиску безпосередньо визначити неможливо, оскільки вже за температури 90 °С він починає розкладатися. Твердий Н2О2 має температуру плавлення -0,43 °С, його густина становить 1,71 г/см3.
Пероксид водню змішується з водою у будь-яких співвідношеннях завдяки виникненню нових водневих зв' язків. Він розчиняється також в ефірі, яким його можна екстрагувати із суміші з водою. З водних розчинів пероксид водню виділяється у вигляді нестійкого кристалогідрату Н2О22Н2О, температура плавлення якого становить -52 °С.
Діелектрична проникність чистого Н2О2 за температури 25 °С становить 93, а його 65 %-го водного розчину — 120, тому чистий Н2О2 та його водні розчини є чудовими іонізуючими розчинниками, які подібно до води добре розчиняють речовини з полярними та іонними зв' язками. Однак використання таких розчинників обмежене недостатньою стійкістю Н2О2.
У водних розчинах пероксид водню є слабкою кислотою:
Н2О2 Н+ + НО-, К = 2,2410-12,
але сильнішою за воду. Під час взаємодії його розчинів з лугами можна виділити відповідні пероксиди металів, які належать до класу солей (а не оксидів), наприклад:
Н2О2 + Ва(ОН)2 = ВаО2 + 2Н2О.
На відміну від нормальних оксидів, які з кислотами утворюють сіль і воду, пероксиди в подібних реакціях дають сіль і пероксид водню, наприклад:
ВаО + Н2SО4 = ВаSО4 + Н2О;
ВаО2 + Н2SО4 = ВаSО4 + Н2О2.
Пероксиди металів як солі слабкої кислоти у водному розчині нестійкі. Це зумовлено їх сильним гідролізом та розкладом Н2О2 у лужному середовищі:
Na2O2 + 2H2O = 2NaOH + H2O2;
2H2O2
 2H2O + O2.
2H2O + O2.Відомі численні неорганічні та органічні сполуки, які містять пероксидні групи.
Зв' язок між атомами кисню НО—ОН слабкий, що може бути пояснено взаємним електростатичним відштовхуванням неподілених пар електронів двох сполучених між собою атомів кисню. Він майже втричі слабкіший за зв'язок О—Н, тому для пероксиду водню особливо властиві реакції, які супроводжуються руйнуванням зв язку НО—ОН з утворенням сполук кисню з характерним для нього ступенем окиснення -2 або 0. Тобто для Н2О2 найхарактерніші окисно-відновні реакції. Пероксиди в окисно-відновних реакціях можуть перетворюватись згідно з такою схемою:
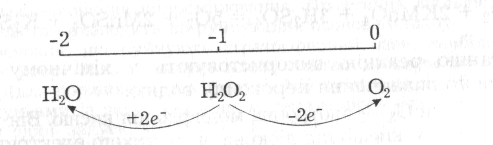
Прикладом може бути характерна для пероксиду водню реакція розкладу за типом диспропорціювання (окисно-відновна реакція самоокиснення — самовідновлення):
2Н2О2 = 2Н2О + О2.
Отже, Н2О2 здатний виявляти властивості як окисника, так і відновника, що властиво сполукам з проміжними ступенями окиснення елементів. Окисна та відновна активності Н2О2 характеризуються такими значеннями електродних потенціалів відповідних перетворень:
Н2О2 + 2Н+ + 2е- = 2Н2О, Е° = 1,78 В;
О2 + 2Н+ + 2е- = Н2О2, Е° = 0,68 В.
Порівняння цих електродних потенціалів свідчить про те, що окиснювальна здатність Н2О2 (Е° = 1,78 В) виражена значно сильніше, ніж відновна (Е° = 0,68 В). Справді, пероксиди — сильні окисники. Вони легко окиснюють йодиди до вільного йоду, нітрити — до нітратів, сполуки хрому(ПІ) — до хрому(VІ) тощо, наприклад:
2КІ + Н2О2 + Н2SО4 = І2 + 2Н2О + К2SО4;
2К3[Сr(ОН)6] + 3Н2О2 = 2К2СrО4 + 8Н2О + 2КОН.
Лише під час взаємодії із сильними окисниками Н2О2 виявляє відновні властивості, продуктом його окиснення є кисень, наприклад:
Н2О2 + С12 = О2 + 2НС1;
Н2О2 + О3 = 2О2 + Н2О;
3Н2О2 + 2КМnО4 = 3О2 + 2МnО2 + 2КОН + 2Н2О;
.5Н2О2 + 2КМnО4 + 3Н2SО4 = 5О2 + 2МnSО4 + К2SО4 + 8Н2О.
Останню реакцію використовують у хімічному аналізі для кількісного визначення пероксиду водню.
Озон. Озон О3 — алотропна модифікація кисню. Він утворюється з газоподібного кисню під дією на нього тихого електричного розряду або ультрафіолетового випромінювання. Для штучного добування О3 використовують озонатори. Тихий розряд проходить у просторі між стінками
внутрішньої та зовнішньої скляних посудин. Кисень, який виходить з озонато-ра, містить кілька відсотків озону (до 10 %).
Озон також утворюється під час обробки молекулярного кисню потоком електронів, протонів, короткохвильового випромінювання, тобто за рахунок радіо- та фотохімічних реакцій.
У приземній атмосфері концентрація озону дуже мала і становить 10-7-10-6 %. У стратосфері на висоті 18-50 км земна куля оточена тонким шаром озону, максимальна його кількість скупчена на висоті 20-30 км. Загальна площа атмосферного озонового шару становить 500 млн км2.
У земній атмосфері озон утворюється під час грозових розрядів, а у верхніх її шарах - під дією ультрафіолетового випромінювання. Географія озону дуже динамічна, на неї впливають повітряні течії — вітри атмосфери. Антициклони зменшують, а циклони збільшують кількість О3 у стратосфері.
Вільний стратосферний озон відіграє дуже важливу роль у природі. Озоновий шар затримує небезпечне для живих істот жорстке короткохвильове сонячне випромінювання. Практична діяльність людини дуже часто призводить до руйнування озонового шару.
Серед речовин, які руйнують стратосферний озон, найбільш небезпечним є хлор. Одна молекула хлору здатна знищити до 100 тис. молекул О3 (для порівняння: 1 молекула NО руйнує лише 10 молекул О3). Розрахунками із застосуванням математичного моделювання доведено, що один запуск космічного корабля багаторазового використання «Шаттл» (США) спричинює руйнування 0,3 % загальної кількості озону земної атмосфери.
Озон - отруйний газ синього кольору з різким характерним запахом (tкип = -110 °С, tпл = -192,7 °С). Рідкий озон має темно-синє забарвлення, твердий - чорне.
Молекула О3 діамагнітна, має кутову будову, що зумовлює її полярність. Крім того, порівняно з киснем вона має більшу поляризованість внаслідок більшого розміру молекули. Енергія міжмолекулярної взаємодії О3 у конденсованих станах перевищує цю величину для молекул О3, тому температури кипіння і плавлення озону вищі, ніж кисню. Цими чинниками пояснюють також вищу розчинність озону в полярній воді (за звичайних умов 45 об’ємів О3 розчиняється у 100 об’ємах води).
Довжина зв'язку між атомами кисню (128 пм) проміжна порівняно з одинарним (149 пм) та подвійним (121 пм) зв'язками, тому вважають, що порядок зв' язків у молекулі О3 дорівнює 1,5. Величина валентного кута (116,5°) вказує на sр2-гібридизацію валентних орбіталей центрального атома кисню. Наведені дані свідчать про наявність у молекулі О3 делокалізованого трицен-трового -зв' язку:
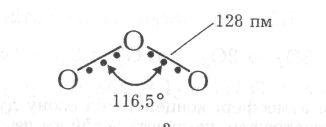
При цьому центральний sр2-гібридизований атом оксигену утворює два -зв'язки з крайніми атомами, а його негібридизована 2рz-орбіталь, яка розміщена під прямим кутом до площини трьох атомів, та аналогічно спрямовані 2рz-орбіталі крайніх атомів оксигену утворюють трицентровий нелокалізований -зв' язок.
Озон — ендотермічна сполука (Н= 142,3 кДж/моль, G°298 = 162,7 кДж/моль). Він легко розкладається з утворенням вільних атомів оксигену, що зумовлює його високу окиснювальну здатність:
О3 = О2 + О.
Про значно більшу хімічну активність О3 порівняно з О2 свідчать стандартні електродні потенціали озону у водних розчинах:
нейтральне середовище: О3 + Н2О + 2е- = О2 + 2ОН-, Е° = 1,24 В;
О2 + 2Н2О + 4е- = 4ОН-, Е° = 0,401 В;
кисле середовище: О3 + 2Н+ + 2е- = О2 + Н2О, Е° = 2,07 В;
О2 + 4Н+ + 4е- = 2Н2О, Е° = 1,23 В.
Озон легко окиснює різноманітні сполуки з утворенням іона О2- та молекули О2:
2Аg + O3 = Аg2O + O2;
РbS + 4O3 = РbSO4 + 4O2;
2КІ + О3 + Н2О = І2 + О2 + 2КОН.
Останню реакцію використовують для виявлення та кількісного визначення озону.
Іноді продуктами реакцій за участю озону є озоніди (спорідненість О3 до електрона становить 180 кДж/моль), наприклад:
К + О3 = КО3;
4КОН + 4О3 = 4КО3 + О2 + 2Н2О.
Такі сполуки вміщують молекулярний іон О3-. На відміну від озону Оз іон О3- має неспарений електрон, який зумовлює його парамагнетизм. Озоніди лужних металів мають червоне забарвлення, вони дуже сильні окисники.
