Исследование роли парамагнитных интермедиатов в биологически важных процессах методами спиновой химии и химической радиоспектроскопии 01. 04. 17 химическая физика, в том числе физика горения и взрыва
| Вид материала | Исследование |
- Развитие метода кинетической радиофлуорометрии для исследований ион-радикалов, 783.92kb.
- Механизмы образования и взаимодействий углеродных нанокластеров 01. 04. 17 химическая, 933.55kb.
- Программа-минимум кандидатского экзамена по специальности, 79.71kb.
- Программа аттестационных испытаний Факультет Физики и информационных технологий Бакалавриат, 45.71kb.
- Н. Г. Чернышевского кафедра теоретической и математической физики рабочая программа, 152.3kb.
- Программа по физике для 10-11 классов общеобразовательных, 75.87kb.
- Горение гранулированной железоалюминиевой термитной смеси при получении железа и его, 356.74kb.
- Физика биологических систем, 39.45kb.
- Омус-2012 Ключевые слова: , 13.52kb.
- Химическая и радиационная физика мемориал О. И. Лейпунского, 152.71kb.
На правах рукописи
Поляков Николай Эдуардович
ИССЛЕДОВАНИЕ РОЛИ ПАРАМАГНИТНЫХ ИНТЕРМЕДИАТОВ В БИОЛОГИЧЕСКИ ВАЖНЫХ ПРОЦЕССАХ МЕТОДАМИ СПИНОВОЙ ХИМИИ И ХИМИЧЕСКОЙ РАДИОСПЕКТРОСКОПИИ
01.04.17 – химическая физика, в том числе физика горения и взрыва
Автореферат диссертации
на соискание учёной степени
доктора химических наук
Новосибирск – 2009
Работа выполнена в Институте химической кинетики и горения Сибирского отделения Российской академии наук
Официальные оппоненты: доктор физико-математических наук,
профессор, Бердинский Виталий Львович
доктор химических наук,
Володин Александр Михайлович,
доктор химических наук,
Анисимов Олег Александрович
Ведущая организация: Институт «Международный томографический центр» СО РАН
Защита состоится “21” октября 2009 года в 15 часов на заседании Диссертационного совета Д 003.014.01 при Институте химической кинетики и горения СО РАН по адресу: 630090, г. Новосибирск, ул. Институтская, 3.
С диссертацией можно ознакомиться в библиотеке ИХКГ СО РАН.

Автореферат разослан “ 17 ” июля 2009 г.
Ученый секретарь диссертационного совета
Д.х.н. А. А. Онищук
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Диссертационная работа посвящена исследованию современными физическими методами короткоживущих парамагнитных интермедиатов, образующихся в процессах с участием биологически важных молекул в растворах и организованных средах.
Актуальность работы связана как с объектами исследования, поскольку парамагнитные частицы в биологических системах находятся в зоне пристального внимания, так и с полученными результатами, дающими ответы на ряд вопросов важных сегодня для физической органической химии, биохимии, фармакологии и медицины. В работе на примерах модельных фотоиндуцированных реакций исследованы детальные механизмы окислительно-восстановительных превращений биологически важных соединений, или их аналогов. Прежде всего, это - процессы с участием синтетических аналогов NADH – 1,4-дигидропиридинов, и природных полиенов, включая каротиноиды, в растворах и организованных средах. На основании проведенных методом химической поляризации ядер (ХПЯ) исследований можно считать установленной роль одноэлектронного переноса в трансформации дигидропиридинового цикла в пиридиновый, а также в процессах цис-транс фотоизомеризации природных полиенов. В частности, изучение свойств ион-радикалов природных полиенов в настоящее время приобретает особую актуальность, поскольку они входят в состав многих биологических систем, для цис–транс изомеризации которых предполагаются процессы с переносом заряда. Так, например, в диссертации обнаружены ион-радикальные стадии цис–транс изомеризации ретиналя, входящего в состав зрительного пигмента родопсина. Считается, что именно цис-транс изомеризация инициирует процесс зрительного восприятия в глазу человека и других млекопитающих.
Значительный интерес представляют и радикальные процессы с участием каротиноидов - широко распространенного класса природных пигментов. Они синтезируются растениями и микроорганизмами и присутствуют во многих пищевых продуктах, включая овощи, фрукты и рыбу. В большинстве природных процессов, включая фотосинтез, их роль чаще всего связывают с реакциями переноса энергии и электрона. В медицине интерес к каротиноидам связан, прежде всего, с их антиоксидантными свойствами. Сегодня антиоксиданты, и в частности каротиноиды, используются на практике в комплексном лечении таких серьезных заболеваний как рак, болезни сердца, нервной системы, а также возрастные дегенеративные изменения мышечных тканей. В связи с упомянутым интересом к антиоксидантным свойствам каротиноидов можно утверждать, что химические и физико-химические исследования реакционной способности каротиноидов в окислительно-восстановительных процессах в настоящий момент являются приоритетными. Имеющаяся в литературе информация о короткоживущих парамагнитных и диамагнитных интермедиатах, образующихся в реакциях каротиноидов со свободными радикалами, весьма ограничена, а структура интермедиатов, как правило, только предполагается. Поэтому именно исследованиям, связанным с реакционной способности каротиноидов, а также их короткоживущих парамагнитных интермедиатов принадлежит значительное место в настоящей диссертации.
Понимание механизмов терапевтического действия лекарственных препаратов на молекулярном уровне является одной из важнейших задач биохимии и фармакологии. Успешное решение этой проблемы имеет принципиальное значение не только для фундаментальной науки. Знание тонких механизмов процессов определяющих связывание и диссоциацию лиганд-рецепторных комплексов позволит понять причину терапевтического действия лекарства, разработать методы для контроля действия лекарства в организме, и минимизировать возможные побочные эффекты. До настоящего времени, однако, физико-химические аспекты связывания мало изучены. В частности, отсутствуют представления о физико-химических взаимодействиях, заставляющих лекарство связываться с рецептором, а также о химических трансформациях лекарства в активном центре рецептора, облегчающих дальнейшую диссоциацию комплекса лекарство-рецептор. Предпринятые в настоящей работе попытки обосновать возможность метаболизма лекарственных препаратов при взаимодействии с рецептором, и, в результате исследования модельных систем, установить факторы, ответственные за образование и диссоциацию комплекса «лекарство–рецептор», в этом смысле являются пионерскими.
Самостоятельный практический интерес представляют исследования фотопревращений лекарственных препаратов, выполненные в диссертации на примерах нифедипина и лаппаконитина, т.к. в литературе имеются сведения о фототоксичности этих препаратов.
Исследование методами спиновой химии и химической радиоспектроскопии окислительно-восстановительных процессов в организованных средах, предпринятое во второй части диссертации, представляется актуальным с нескольких точек зрения. Кроме необходимости понимания механизмов межмолекулярных взаимодействий в системах с ограниченной подвижностью, к которым можно отнести практически все биологические системы, самостоятельный интерес представляет исследование воздействия магнитного поля на течение этих процессов. Напомним, что проведение реакций во внешнем магнитном поле является одним из способов управления физико-химическими свойствами биологически активных соединений. Обнаружение в настоящей работе значительных магнитных эффектов (сотни процентов) на выход свободных радикалов в фотоинициированных процессах с участием ряда карбонильных соединений является наглядной демонстрацией возможностей методик спиновой химии. Эти эффекты легли в основу разработанного в настоящей работе кинетического метода, позволяющего изучать динамику радикальных пар в организованных средах.
Во второй части диссертации представлен также цикл работ, посвященных исследованию структуры и реакционной способности комплексов включения нифедипина и лаппаконитина с глицирризиновой кислотой. Актуальность данного исследования связана с известными из литературы и собственных исследований автора фактами воздействия комплексообразования на лечебные свойства препаратов. В частности, в настоящей работе было обнаружено значительное (в десятки и сотни раз) усиление терапевтической активности препаратов нифедипина и лаппаконитина в присутствие глицирризиновой кислоты. Создание эффективных лекарственных препаратов на основе комплексов включения с природными соединениями сегодня является бурно развивающейся областью медицинской химии. Использование комплексов включения позволяет направленно регулировать (усиливать или ослаблять) те или иные свойства лекарственных соединений. Полученные в настоящей работе результаты могут иметь практическое значение для регулирования свойств и других лекарственных препаратов, в частности, увеличения их фотостабильности и биодоступности, а также снижения токсичности (включая фото-токсичность).
Цель работы.
Целью настоящей диссертационной работы являются исследования роли короткоживущих парамагнитных интермедиатов, в процессах с участием дигидропиридинов - синтетических аналогов NADH, природных полиенов, включая ретиналь и каротиноиды, а также биологически активных карбонильных соединений и некоторых лекарственных препаратов. Исследования проводятся в растворах и организованных средах с целью установления основных факторов, определяющих воздействие среды на процессы. Кроме традиционных методик спиновой химии и химической радиоспектроскопии в диссертации используется специально развитый кинетический метод, основанный на импульсной микроволновой накачке электронных переходов в радикальной паре.
Научная новизна и практическая значимость.
Для процесса фотоокисления ряда 1,4-дигидропиридинов – синтетических аналогов NADH, удалось проследить все постулируемые в литературе стадии: перенос электрона, протона, атома водорода. При этом получены практически важные данные о свойствах ион-радикалов и нейтральных радикалов дигидропиридинов. Эти данные, в частности, использованы в настоящей работе при обсуждении возможного метаболизма лекарств на рецепторах.
Систематически изучен процесс фотоиндуцированной цис-транс изомеризации полиненасыщенных соединений в присутствии акцепторов электрона в растворах и организованных средах. Показано, что геометрическая изомеризация, протекающая по механизму переноса электрона, который ранее был известен для замещенных этиленов, в случае полиенов может осуществляться по нескольким различным каналам. Продемонстрировано, что различные изомеры могут иметь общее триплетное состояние, и возможна одновременная цис-транс изомеризация вокруг двух двойных связей. Показано, что метод ХПЯ дает информацию об относительных квантовых выходах образования различных изомеров и их предшественниках, недоступную другими методами.
Измерены константы скорости реакции различных каротиноидов с перекисными радикалами, и обнаружена корреляция констант скоростей с окислительными потенциалами каротиноидов. Кроме того обнаружена зависимость окислительно-восстановительных свойств каротиноидов от среды (раствор или супрамолекулярное окружение), а также определены условия, при которых каротиноиды могут проявлять как антиоксидантную, так и про-оксидантную активность. Эти результаты не только ставят точку в споре о том, чем определяются антиоксидантные свойства каротиноидов, но и могут использоваться на практике при подборе каротиноидов, обладающих антиоксидантными или про-оксидантными свойствами для решения конкретных задач.
Работы по исследованию природы и свойств супрамолекулярных комплексов глицирризиновой кислоты с каротиноидами и лекарственными препаратами нифедипином и лаппаконитином можно считать пионерскими. Впервые детально изучены практически важные процессы фотодеградации лаппаконитина, а также воздействие глицирризиновой кислоты на фотостабильность лаппаконитина и нифедипина.
Учитывая, что в настоящее время создание супрамолекулярных комплексов лекарственных препаратов с различными природными соединениями является одним из самых многообещающих направлений в области медицинской химии, полученные в работе результаты, безусловно, имеют и самостоятельную значимость в плане использования глицирризиновой кислоты для повышения биодоступности и фотостабильности других биологически активных соединений.
Выдвинута гипотеза о возможной роли процессов переноса электрона в механизме связывания ряда лекарственных препаратов с клеточными рецепторами. Гипотеза проиллюстрирована на модельной реакции двух лекарств (нифедипина и лаппаконитина) с аминокислотами, входящими в состав центров связывания соответствующих рецепторов. Продемонстрировано, что образующиеся анион-радикалы указанных соединений нестабильны и в акте обратного переноса электрона в лиганд-рецепторном комплексе получаются уже другие соединения. Это может служить причиной распада лиганд-рецепторного комплекса.
Создан время-разрешенный импульсный вариант метода product-yield-detected-ESR, PYESR. Применение данной методики позволяет детектировать спектр ЭПР промежуточной радикальной пары по изменениям в выходе продукта реакции – долгоживущего спинового аддукта, а также предоставляет уникальные возможности для получения кинетической информации о динамике радикальных пар в растворах. В работе были измерены кинетические параметры радикальных пар образующихся при фотолизе ряда карбонильных соединений, включая биологически активные ацетиленовые кетоны, в мицеллах SDS.
Апробация и публикации.
Основное содержание диссертации опубликовано в 32 статьях. Результаты работы были также представлены автором на ряде международных и российских конференций, в том числе на XI Международной конференции “Магнитный резонанс в химии и биологии”, Москва, 2001; VII Международном симпозиуме “Magnetic Field and Spin Effects in Chemistry and Related Phenomena”, Tokyo, Japan, 2001; VI конференции памяти Воеводского “Физика и химия элементарных химических процессов, Новосибирск, 2002; X APAM topical seminar and Conference “Nanoscience and Technology”, Novosibirsk, 2003; IX International Seminar on Inclusion Compounds, Novosibirsk, 2003; Международной конференции «Происхождение и эволюция биосферы», 2005, Новосибирск; International Symposium “Advances in Science for Drug Discovery”, Moscow, 2005; IV International Conference on Nitroxide Radicals: Synthesis, Properties and Implications of Nitroxides (SPIN-2005), Novosibirsk, 2005; IV International Symposium "Design and Synthesis of Supramolecular Architectures", Kazan, 2006; XVII Симпозиум «Современная химическая физика», Туапсе, 2006; 36-th and 37-th Southeast Magnetic Research Conferences, USA, 2007 and 2008; International Conference on Molecular/Nano-Photochemistry, Photocatalysis and Solar Energy (Solar‘08). Cairo, Egypt, 2008.
Структура и объём работы.
Диссертация состоит из введения, семи глав, списка основных результатов и выводов, а также списка цитированной литературы (363 ссылки). Работа изложена на 280 страницах, содержит 114 рисунков и 32 таблицы.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Первая глава диссертации посвящена подробному описанию используемых в работе методических подходов и экспериментальных установок. Важнейшее место в исследованиях процессов с участием радикальных частиц в настоящее время занимают методики спиновой химии. В основе этих методик лежат эффекты химической поляризации ядер (ХПЯ) и электронов (ХПЭ), а также влияние внешних и внутренних магнитных полей на радикальные химические процессы. К преимуществам этих методов относится их более высокая чувствительность по сравнению с традиционными методами ЯМР и ЭПР, а также высокая информативность. Так, метод ХПЯ позволяет одновременно получать информацию о парамагнитных интермедиатах, конечных продуктах реакции, и кинетике отдельных стадий.
Говоря о преимуществах тех или иных методов исследования, нельзя не отметить, что каждый метод имеет и свои ограничения, и по области применения, и по чувствительности, и по временному разрешению. Поэтому каждый метод в отдельности, как правило, не дает всей необходимой информации о процессе, особенно для таких сложных объектов, какими являются биологические системы. Для более глубокого изучения механизмов сложных процессов необходимо применение комбинации различных методов, а также создание новых методик и экспериментальных установок, наилучшим образом подходящих для решения конкретной задачи. В представленной работе значительное внимание уделяется разработке и применению комплексного использования современных физико-химических методов для исследования биологически важных процессов. Особое внимание уделено время-разрешенным методам спиновой химии в сочетании с оптической спектроскопией, ЭПР и ЯМР в стационарном и импульсном вариантах. Основная часть работ выполнена в лаборатории Магнитных явлений Института химической кинетики и горения СО РАН на ЯМР спектрометрах фирм Varian, Bruker и Jeol с различной напряженностью магнитного поля, снабженных стационарными и импульсными источниками света для проведения фотохимических экспериментов и регистрации эффектов ХПЯ. Кроме того, часть работ выполнена автором диссертации в рамках международного сотрудничества с коллегами из Латвии, США и Японии. Мы благодарны коллегам из Латвии за синтез широкого набора замещенных 1,4-дигидропиридинов – аналогов природного кофермента NADH. В содружестве с Университетом штата Алабама, США (Проф. Л.Д. Кисперт), выполнен цикл работ, посвященный исследованию окислительно-восстановительных процессов с участием каротиноидов и их супрамолекулярных комплексов. Совместно с группой Д-ра Оказаки (National Industrial Research Institute of Nagoya, Japan) создан время-разрешенный вариант метода PYESR (product-yield-detected-ESR) для исследования динамики радикальных пар и магнитных эффектов в организованных средах.
Главы 2-7 настоящей диссертации содержат описание конкретных исследований, при этом работа поделена на две части: исследования парамагнитных интермедиатов для процессов в растворах (главы 2-5) и в организованных средах (комплексы типа «хозяин–гость» и мицеллы, главы 6-7).
Вторая глава диссертации посвящена процессам фотоиницированного окисления 1,4-дигидропиридинов (ДГП) – синтетических аналогов природного кофермента NADH в присутствии акцепторов электрона. Дискуссия о реализации гетеролитического или гомолитического механизмов превращения NAD+ в NADH в живых системах не утихает последние несколько десятилетий. В настоящей работе исследования проводились с использованием различных методов спиновой химии: стационарная ХПЯ в сильных и слабых магнитных полях, ХПЯ с временным разрешением, а также СПЯ (стимулированная поляризация ядер). Исследование модельных процессов фотоиницированного окисления ряда замещенных 1,4-дигидропиридинов в присутствии различных акцепторов электрона позволило установить роль радикальных частиц и проследить за всеми стадиями процесса превращения ДГП в пиридин. Показано, что во всех случаях первым актом реакции является перенос электрона с ДГП на акцептор – хинон. Дальнейшая судьба катион-радикала ДГП существенно зависит от структуры заместителей в пиридиновом кольце. Наибольшее влияние при этом оказывает наличие и природа заместителя при атоме азота. Для N-незамещенных ДГП наиболее вероятным является перенос протона в ион-радикальной паре с атома азота на анион-радикал хинона с образованием последовательной нейтральной радикальной пары. Третьим шагом реакции является отрыв атома водорода из 4-го положения пиридинового кольца в нейтральном радикале с образованием соответствующего пиридина (Схема 1).
Схема 1.
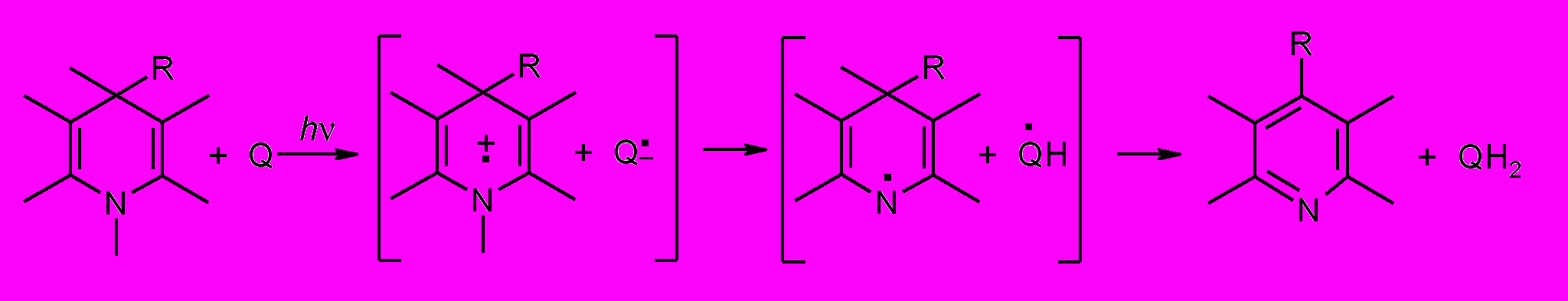
Показано, что катион-радикалы ДГП являются нестабильными частицами независимо от наличия заместителя при атоме азота. Поскольку образование N-центрированного нейтрального радикала ДГП для N-замещенных ДГП, как правило, невозможно, дальнейшие превращения их катион-радикалов происходят уже в растворе, а не в геминальной РП. Вторым актом реакции для таких ДГП является отрыв атома водорода из 4-го положения в катион-радикале с образованием соответствующего катиона пиридиния. Для ДГП с метильным заместителем при атоме азота катионы пиридиния стабильны и могут быть зарегистрированы в ЯМР спектре. С другой стороны, ацильный заместитель при атоме азота дестабилизирует катион пиридиния, что приводит к его распаду в микросекундном временном диапазоне с образованием соответствующего пиридина (Схема 2).
Схема 2.
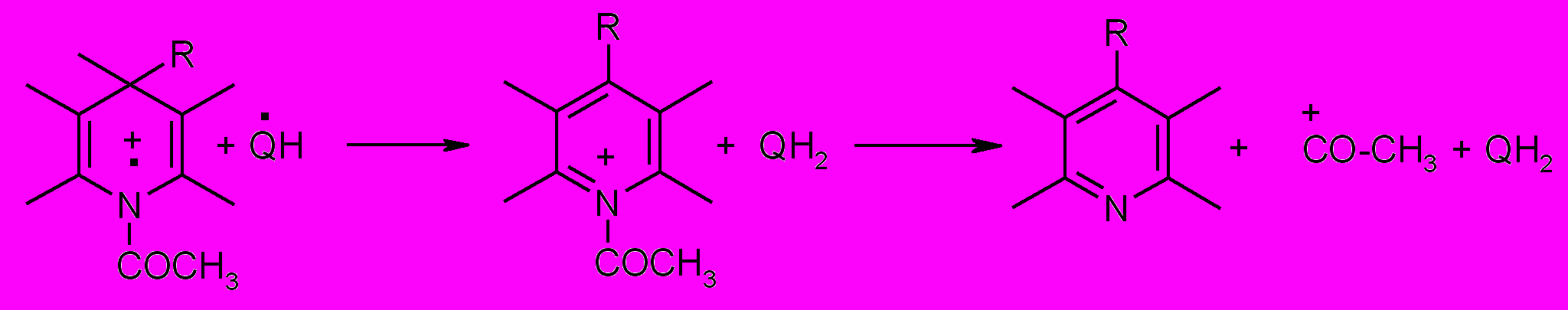
Отметим, что разнообразие путей фотопревращения дигидропиридинов позволило нам в данной серии работ продемонстрировать широкие возможности методов спиновой химии для исследования механизмов сложных радикальных превращений синтетических аналогов NADH, и для идентификации парамагнитных интермедиатов. Но самый главный вывод касается того, что установленные для фотоинициированных реакций ДГП с акцепторами электронов последовательности радикальных стадий, скорее всего, будут таковыми и для реакций смешения, в которых ХПЯ не проявляется, но образуются те же продукты. Подтверждением этого заключения являются недавние работы М.С. Афанасьевой (J. Phys. Chem. B, 2006, 110, 21232-21237; J. Am. Chem. Soc., 2006, 128, 8651-8658), в которых были зарегистрированы спиновые эффекты в процессах ферментативного окисления NADH и нифедипина (диметиловый эфир 1,4-дигидро-2,6-диметил-4-(2’-нитрофенил)-3,5-дикарбокси пиридина) пероксидазой хрена в растворах. На основании анализа полевых зависимостей магнитного эффекта были предложены схемы процессов, включающие в качестве первой стадии перенос электрона от NADH и ДГП на активный центр фермента.
Третья глава диссертации посвящена исследованию механизмов цис-транс изомеризации полиненасыщенных соединений. В этой главе описаны механизмы фотоинициированной цис-транс изомеризации полиенов, в присутствии акцепторов электрона, включающие стадию переноса электрона. В отличие от оптических методов исследования, методы ЯМР и ХПЯ позволяют раздельно наблюдать сигналы от разных изомерных форм, что позволило нам впервые применить эти методы для исследования механизмов изомеризации сложных молекул, содержащих несколько сопряженных двойных связей. В качестве примера на рисунке 1 приведены спектры ХПЯ зарегистрированные при фотолизе ненасыщенного кетона в присутствие донора электрона трифениламина (ТФА).
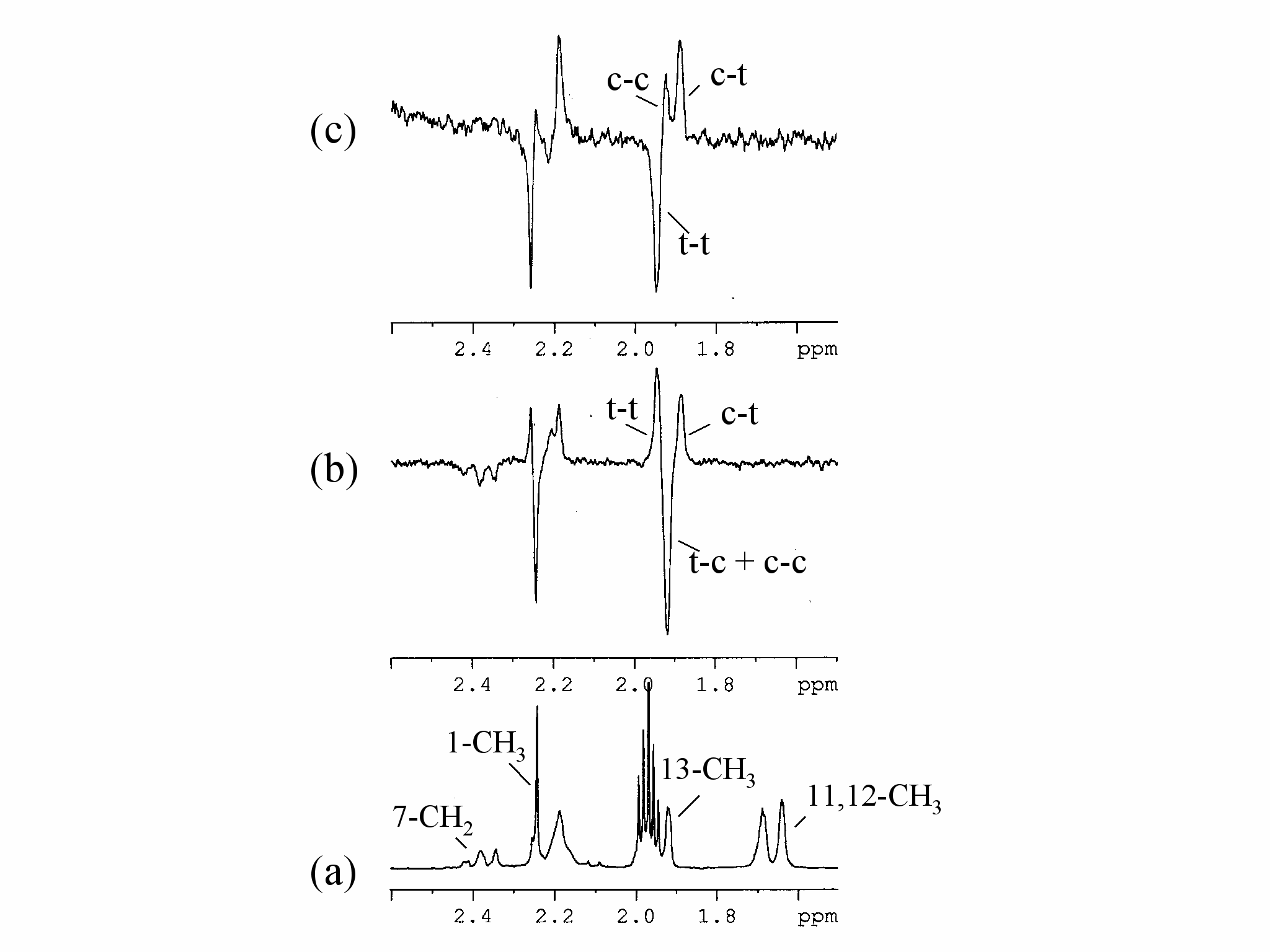
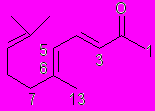
Рисунок 1. (a) Фрагмент 1H ЯМР спектра (алифатическая часть, транс-цис изомер, (т-ц)) в CD3CN; (b) и (c) спектры ХПЯ зарегистрированные при фотолизе изображенного кетона в присутствие ТФА в CD3CN. Исходный изомер т-ц (b) и т-т (c).
Следует отметить, что доказательство участия одноэлектронного переноса в процессе цис-транс фотоизомеризации замещенных этиленов в присутствие доноров и акцепторов электрона впервые было получено именно методами спиновой химии и это считается одним из важных её достижений. В представленном цикле работ получены экспериментальные доказательства участия следующих промежуточных короткоживущих частиц в реакциях цис-транс изомеризации полиенов: триплетные возбужденные состояния, образующиеся при рекомбинации триплетной ион-радикальной пары; катион-радикалы и дикатионы; а также вторичные интермедиаты образующиеся из ион-радикалов: нейтральные радикалы и бирадикалы (Схема 3).
Схема 3. Механизмы изомеризации полиненасыщенных соединений, включающие стадию переноса электрона.
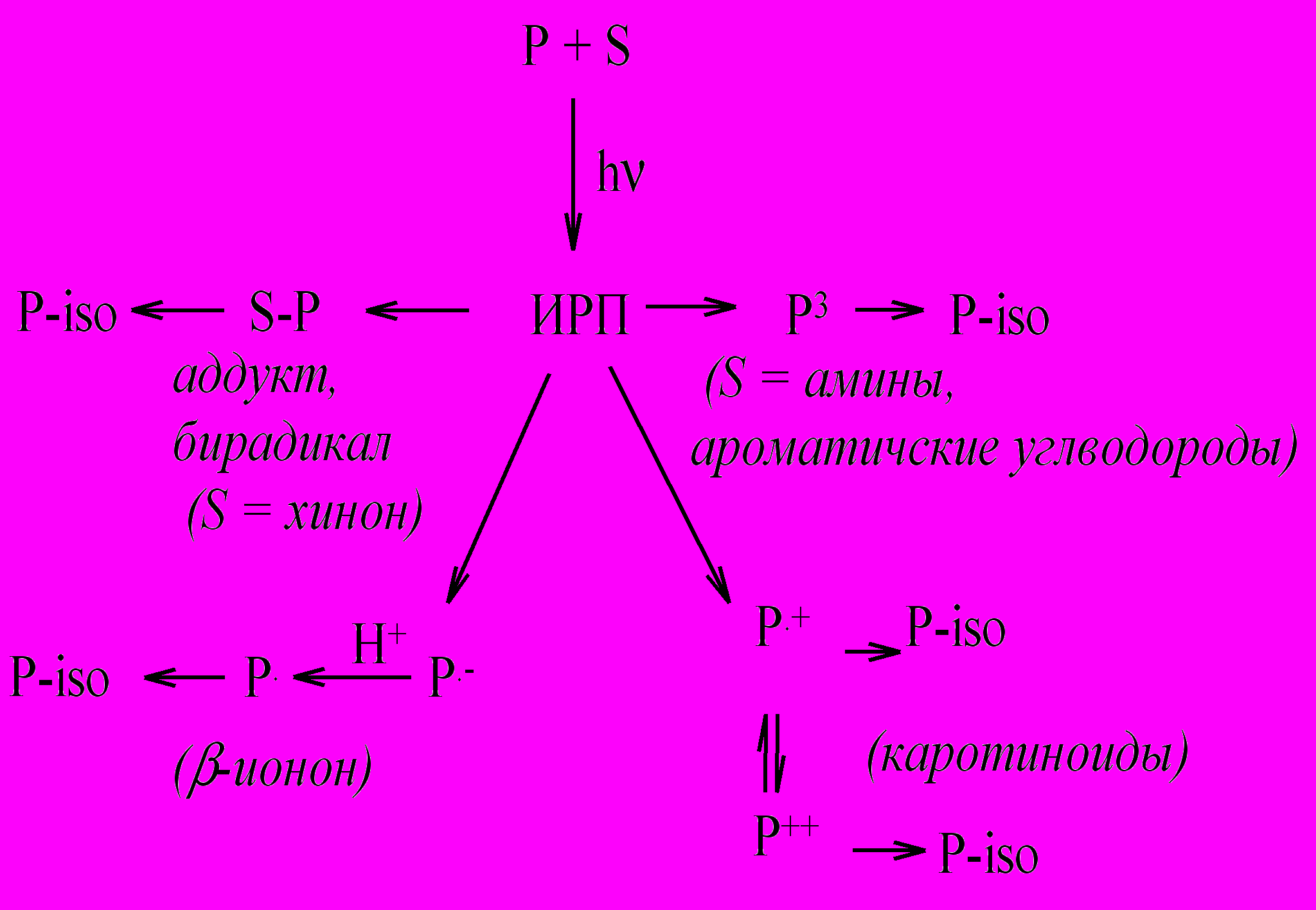
На схеме Р – это полиен, а S – партнеры (амины, хиноны, ароматические углеводороды), которые могут играть роль донора либо акцептора электрона. Для каждого из описанных вариантов установлен детальный механизм изомеризации.
Примером комплексного подхода к изучению биологически важных процессов является исследование окислительно-восстановительных реакций каротиноидов, описанное в четвертой главе. В представленном цикле работ, выполненных с использованием различных физико-химических методов (ЯМР, ЭПР (включая импульсные методики), ХПЯ, ВЭЖХ, электрохимия, оптическая спектроскопия и флюоресценция) изучен ряд окислительно-восстановительных процессов с участием природных и синтетических каротиноидов. В работе исследованы реакции каротиноидов с хинонами, ионами металлов, а также со свободными кислород-центрированными и углерод-центрированными радикалами в растворах. Структуры некоторых изученных каротиноидов представлены на рисунке 2.
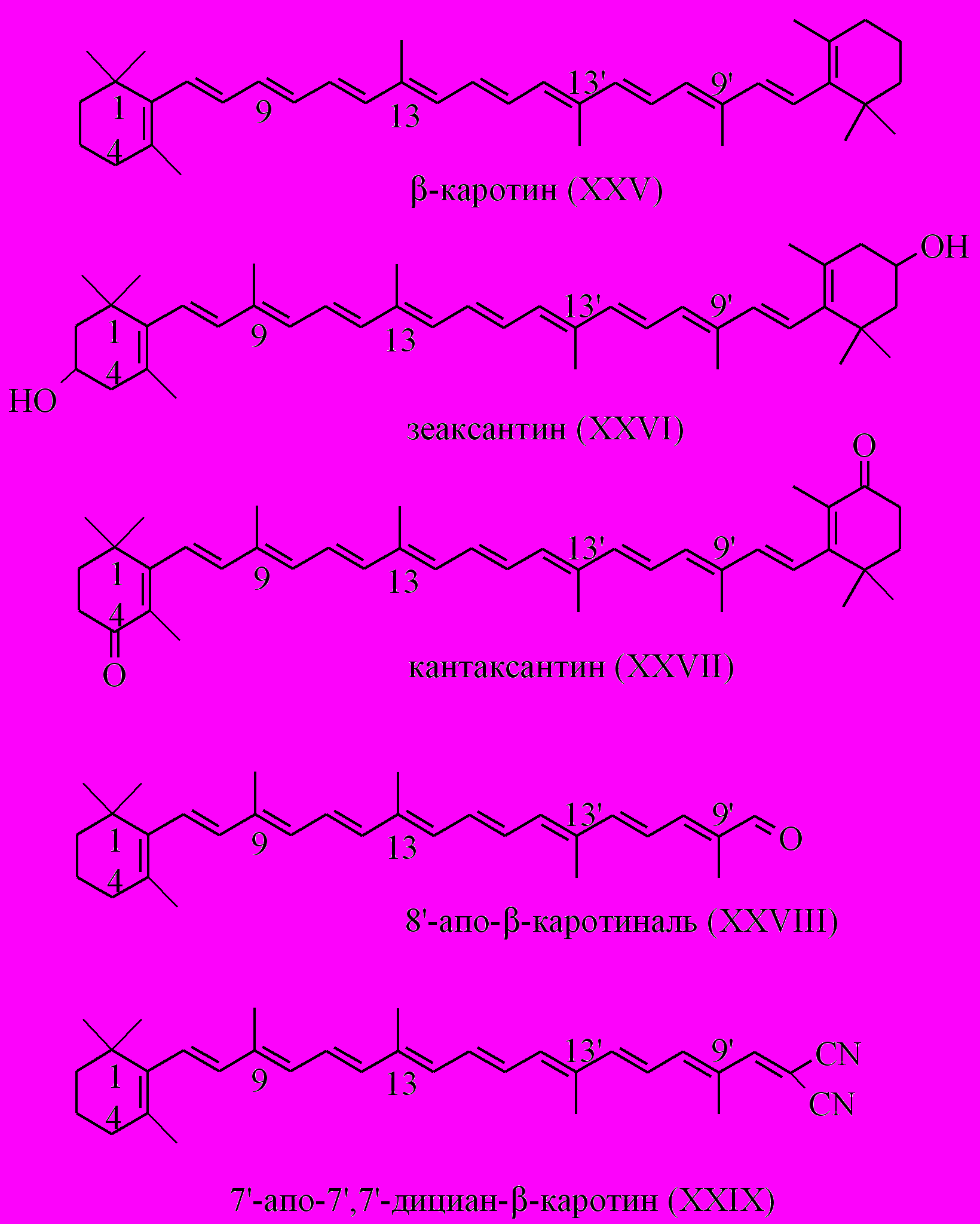
Рисунок 2. Структурные формулы некоторых каротиноидов.
Методом ЭПР со спиновыми ловушками были измерены относительные скорости реакции каротиноидов со свободными радикалами (kCar/kST). kST – константа скорости реакции радикала с ловушкой. Одним из важных достижений настоящей работы явилось обнаружение корреляции kCar/kST с потенциалами окисления каротиноидов (Рис. 3).
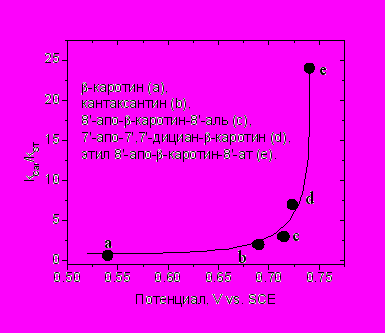
Рисунок 3. Диаграмма зависимости относительных констант скорости захвата перекисных радикалов каротиноидами от потенциала окисления каротиноидов.
При этом наименьшая скорость реакции наблюдалась для -каротина, а наибольшая для апо-каротиноидов с полярными заместителями (структура некоторых из этих каротиноидов показана на рисунке 2). Этот результат позволил нам сделать выбор между обсуждаемыми в литературе возможными направлениями реакции свободных радикалов с каротиноидами (радикальное присоединение, отрыв атома водорода, и окисление) в пользу последнего. Показано, что в присутствие ионов железа каротиноиды могут проявлять как антиоксидантные, так и про-оксидантные свойства, и предложено объяснение данному явлению.
Проведенное в настоящей главе рассмотрение позволяет сделать несколько важных заключений. Прежде всего, перенос электрона характерен для каротиноидов не только при их превращениях в фотосинтетических центрах, но и при взаимодействии со свободными радикалами, а также при цис–транс изомеризации. Можно констатировать, что именно склонность к одноэлектронному переносу объединяет наиболее важные биологические процессы с участием каротиноидов. Среди них фотосинтез и фотоизомеризации ретиналя, являющегося частью зрительного пигмента родопсина, а также реакции со свободными радикалами (антиоксидантная способность).
В пятой главе диссертации описан развитый в рамках настоящей работы оригинальный подход к изучению механизмов лиганд-рецепторных взаимодействий на молекулярном уровне. Представленный экспериментальный подход основан на моделировании отдельных стадий процесса взаимодействия лекарства с аминокислотами, расположенными в активных центрах клеточных рецепторов. Основой для построения модели послужили приведенные в литературе расчеты (K.-J. Schleifer, e.a., J. Med. Chem., 1999, 42, 2204-2211), указывающие на образование донорно-акцепторного комплекса между молекулой гипотензивного препарата нифедипина и аминокислотой тирозином, располагающимся в активном сайте кальциевого рецептора. В работе было предположено, что в таком комплексе может происходить одноэлектронный перенос. Данная гипотеза проиллюстрирована на примере двух лекарственных препаратов: гипотензивного лекарства нифедипина – блокатора кальциевых рецепторов, и антиаритмика лапаконитина – блокатора натриевых каналов.
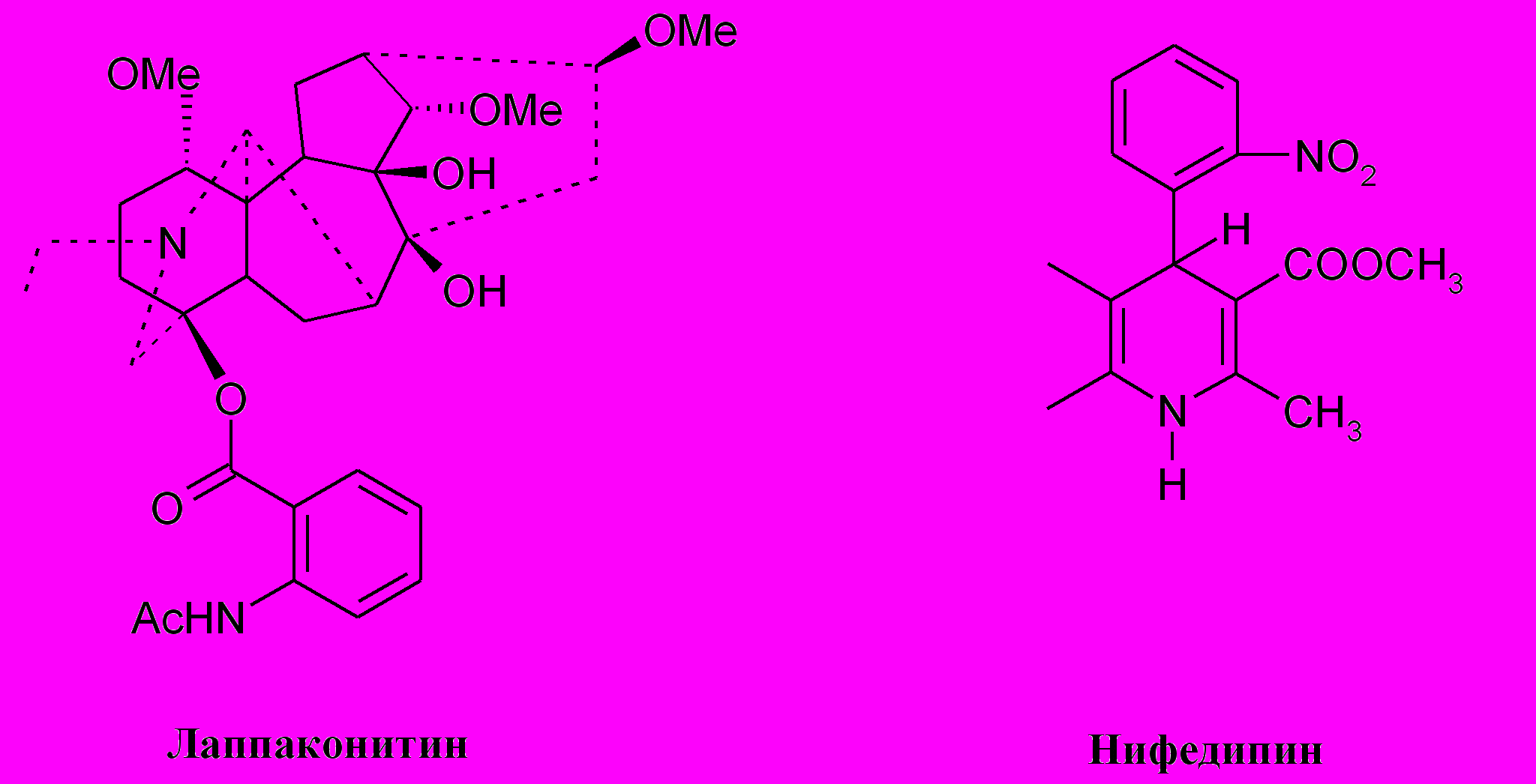
Механизм взаимодействия между молекулами лекарств и аминокислотами тирозином и триптофаном, входящими в состав активных центров соответствующих рецепторов, изучен методом химической поляризации ядер, включая время разрешенный вариант. Установлено, что первичной стадией процесса в обеих системах действительно является перенос электрона. Показано, что анион-радикалы этих лекарственных соединений нестабильны и быстро (в микросекундном временном диапазоне) превращаются в продукты, не способные к связыванию с рецептором (Схемы 4, 5). Этот факт важен, поскольку проливает свет на практически не изученную природу диссоциации комплекса лекарства с рецептором.
Отдельная часть работы посвящена исследованию возможных механизмов фототоксичности нифедипина и лаппаконитина. Показано, что оба этих соединения фоточувствительны в УФ диапазоне и при фото возбуждении вступают в реакции переноса электрона с как рядом аминокислот, так и с другими органическими молекулами. Установлено, что результатом реакции является образование набора короткоживущих N-, O-, и С-центрированных свободных радикалов и ион-радикалов нифедипина, лаппаконитина и партнеров.
Кроме того, в триплетном возбужденном состоянии лаппаконитин сам подвергается внутримолекулярному переносу электрона с последующим образованием пары свободных радикалов. Детально описаны механизмы всех исследованных процессов. Логично предположить, что короткоживущие парамагнитные интермедиаты могут быть причиной высокой токсичности лаппаконитина.
Схема 4. Механизм фотоиндуцированного взаимодействия нифедипина с N-ацетил-тирозином.
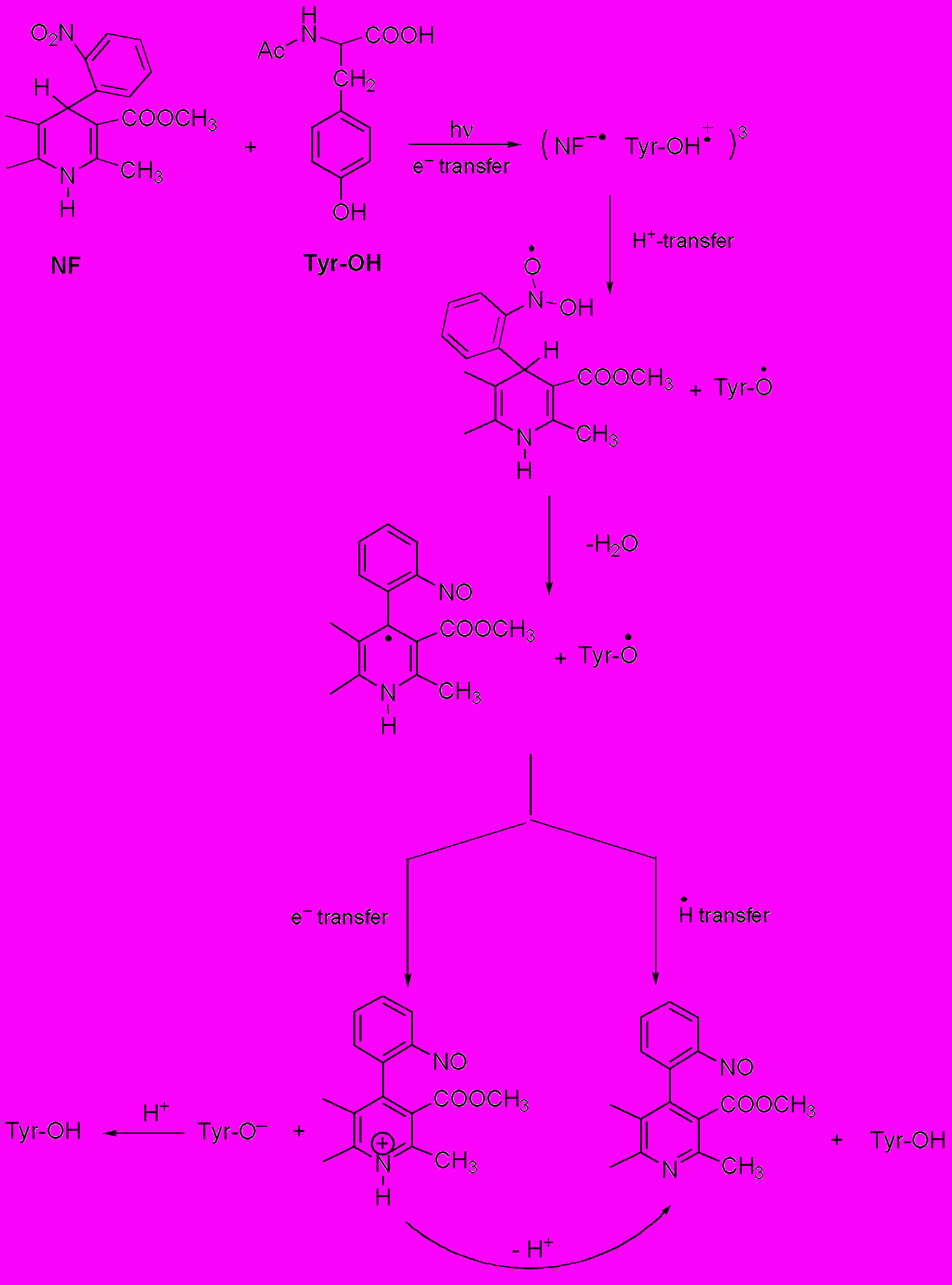
Схема 5. Механизм фототрансформации лаппаконитина (Lap) в присутствии аминокислот (А-Н).
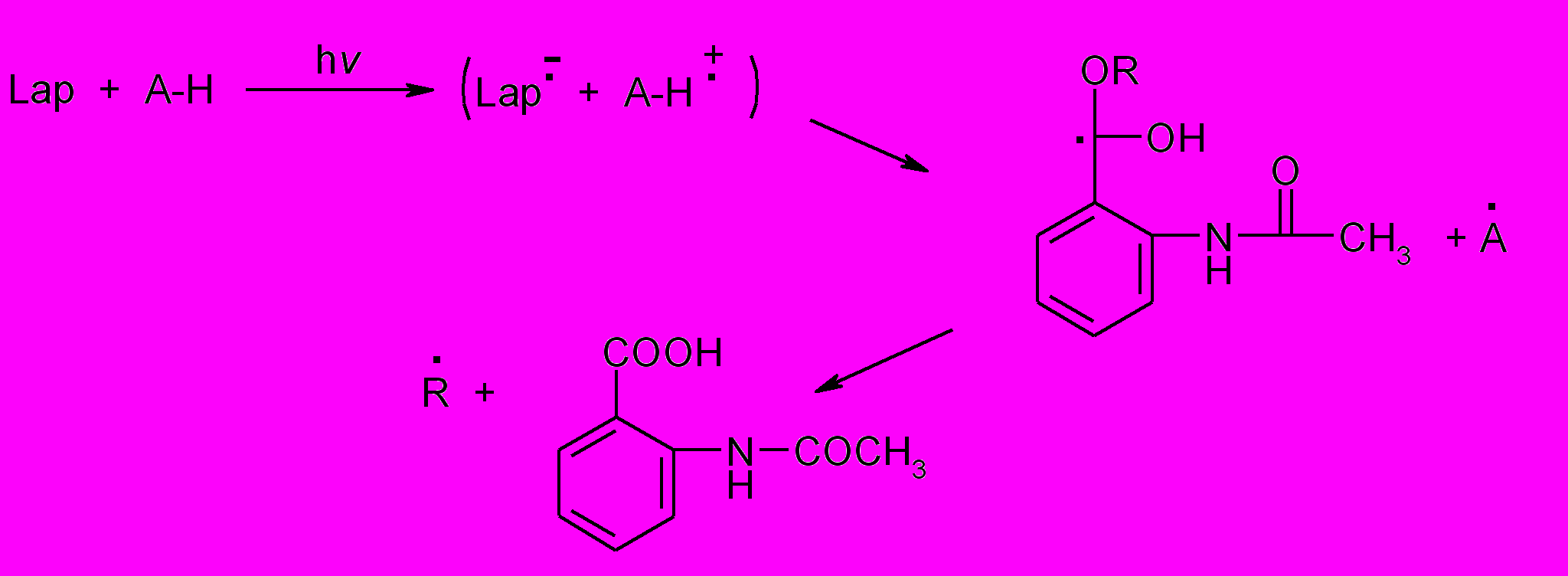
Во второй части диссертации (главы 6-7) описываются окислительно-восстановительные процессы с участием биологически активных соединений в организованных средах (супрамолекулярные комплексы включения и мицеллы).
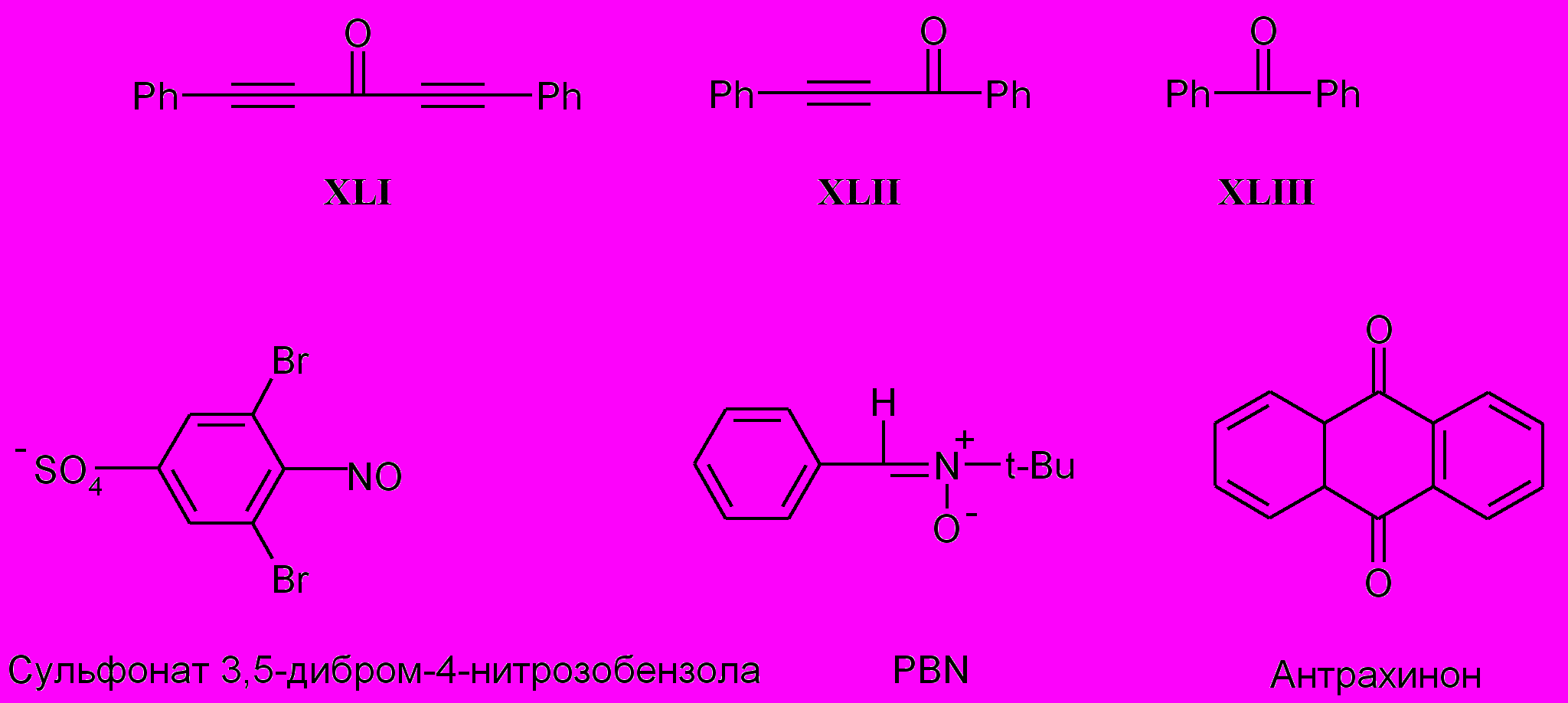
Шестая глава посвящена изучению динамики радикальных пар в мицеллярных растворах. В представленном цикле работ реализована идея об использовании импульсной микроволновой накачки электронных переходов в РП для получения кинетической информации о скоростях образования и гибели радикальных пар в мицеллах. За основу была взята стационарная методика PYESR (product-yield-detected-ESR), с использованием спиновых ловушек для захвата и последующей регистрации короткоживущих радикалов с помощью стационарного ЭПР. Применение данной методики позволяет детектировать спектр ЭПР промежуточной радикальной пары по изменениям в выходе продукта реакции – долгоживущего спинового аддукта. Созданный в результате данной работы время-разрешенный импульсный вариант метода PYESR обладает целым рядом преимуществ перед существовавшими на тот момент методиками, использующими аналогичный принцип микроволновой накачки электронных переходов в РП, поскольку в рамках этого подхода нет ограничений ни в выборе системы (не требуется присутствие флуоресцирующего реагента как в методе ОД ЭПР), ни в скорости регистрации (как в методе СПЯ). С помощью развитого подхода были измерены кинетические параметры радикальных пар, образующихся при фотолизе ряда биологически-активных карбонильных соединений, таких как антрахиноны и ацетиленовые кетоны (Схема 6). Известно, что многие природные и синтетические антрахиноны и их производные обладают противоопухолевой активностью, а ацетилен-содержащие кетоны используются как антигрибковые препараты.
Схема 6. Структурные формулы антрахинона, ацетиленовых кетонов и спиновых ловушек, используемых в работе.
В первую очередь отметим, что для всех кетонов и хинонов зарегистрированы значительные магнитные эффекты на выхода продуктов в реакциях фотовосстановления (сотни процентов). В качестве примера на рисунке 4 приведена зависимость выхода спинового аддукта от внешнего магнитного поля при фотолизе ацетиленового кетона в мицелле SDS. Точка 334 мТл демонстрирует масштаб эффекта наложения микроволнового поля.
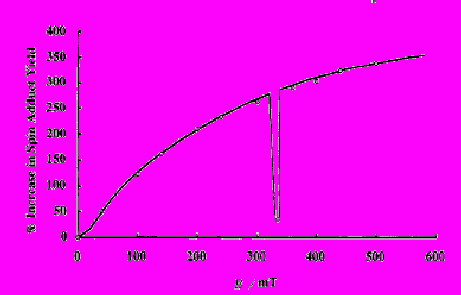
Рисунок 4. Влияние магнитного поля на выход спинового аддукта при фотолизе кетона XLII в 0.2 M растворе мицеллы SDS. Эффект ЭПР переходов кетильного радикала индуцированных микроволновым полем проявляется при резонансном значении поля 334 мТл. Сплошная линия представляет расчетную кривую.
Полевая зависимость магнитного эффекта при приложенном микроволновом поле представляет собой ЭПР спектр промежуточной радикальной пары (Рисунок 5).
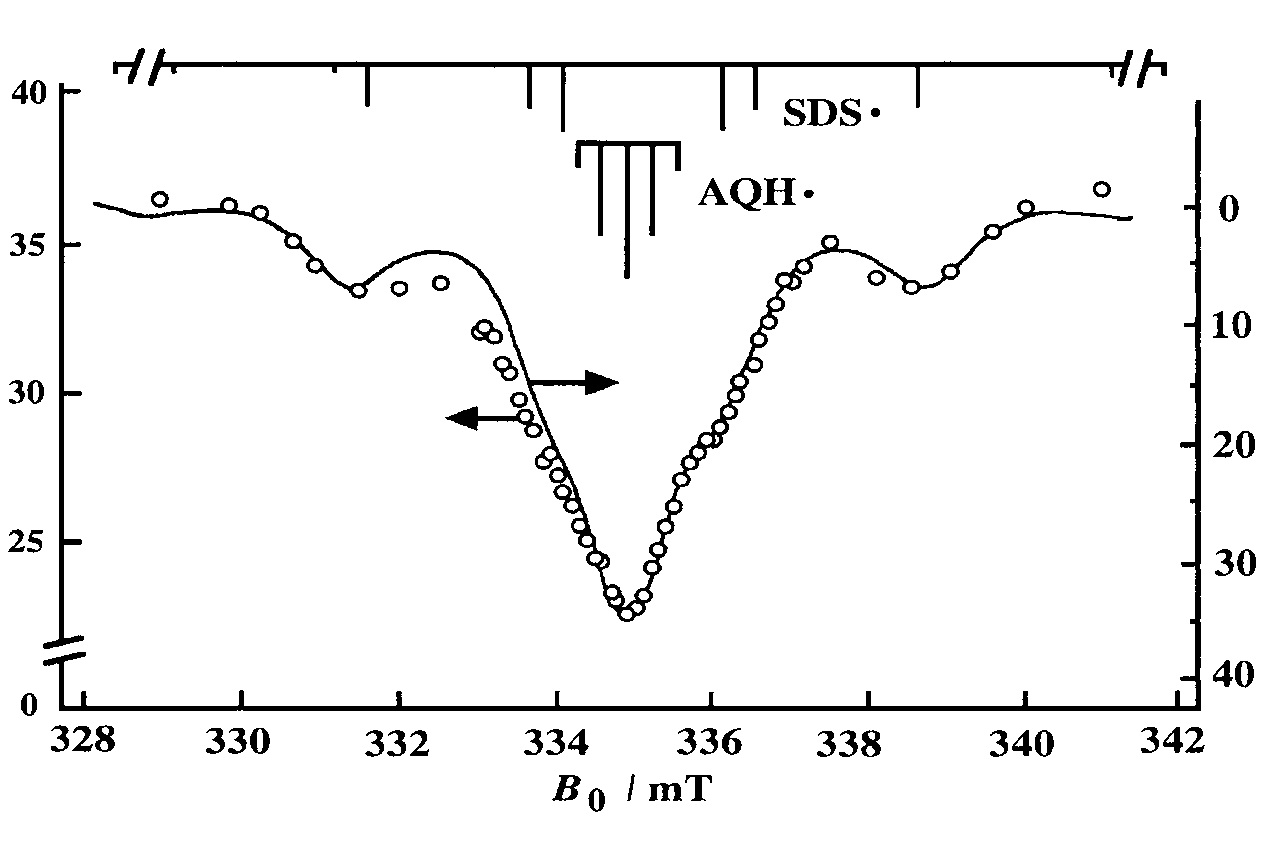
Рисунок 5. ЭПР спектр радикальной пары, зарегистрированный при фотолизе антрахинона в мицеллярном растворе SDS. Микроволновое поле мощностью 4 W прикладывалось в течение 5 мкс сразу после импульса лазера ( = 308 нм, 124 mJ). Правая ось: выход спинового аддукта в микромолях/литр, левая ось: уменьшение выхода аддукта (в %).
Применение импульсной микроволновой накачки электронных переходов позволяет проследить за временной эволюцией радикальных пар и рассчитать следующие кинетические параметры: kH – скорость образования РП в результате отрыва атома водорода от соответствующего донора; kISC – скорость синглет-триплетной конверсии в РП; kP – скорость рекомбинации РП и kesc – скорость выхода радикалов из мицеллы.
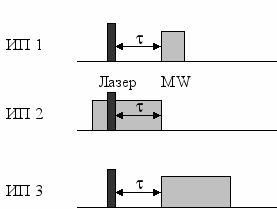
Рисунок 6. Три импульсных последовательности с изменяемой длительностью микроволнового импульса и варьируемой задержкой между микроволновым и лазерным импульсом.
На рисунке 6 изображены три реализованных в работе варианта импульсных последовательностей. В первом методе (отмеченном как ИП 1) короткий микроволновой импульс (обычно это 50 нс) прикладывается к системе через варьируемое время после лазерного импульса. При этом величина отклика системы (уменьшение выхода спинового аддукта) будет пропорциональна мгновенной концентрации РП в данный момент времени. Во втором методе (ИП 2) микроволновой импульс стартует до подачи импульса лазера и заканчивается через варьируемое время после лазерного импульса. В этом случае воздействию микроволнового поля подвергнутся все РП, образовавшиеся за время после лазерного импульса.
В результате, варьируя время , мы получим зависимость концентрации РП от времени отражающую только кинетику образования радикальных пар. Импульсная последовательность 3 позволяет детектировать только те РП, время жизни которых превышает время . В результате получается спадающая кинетическая кривая с характерным временем спада отражающем время жизни РП и релаксационные процессы (Рис. 7). Кинетические параметры РП, полученные в данной работе суммированы в Таблице 1.
| | kp | kESC | kH |
| AQ/SDS | 11.8 | 0.2 | 6.0 |
| AQSO3-/SDS | 45.0 | 3.0 | 6.0 |
| XLI | 10 | 0.2 | 10 |
| XLII | 6.5 | 0.2 | 1.0 |
| XLIII | 7.0 | 0.2 | 3.7 |
Таблица 1. Кинетические параметры радикальных пар. Константы скорости даны в единицах 106 с-1.
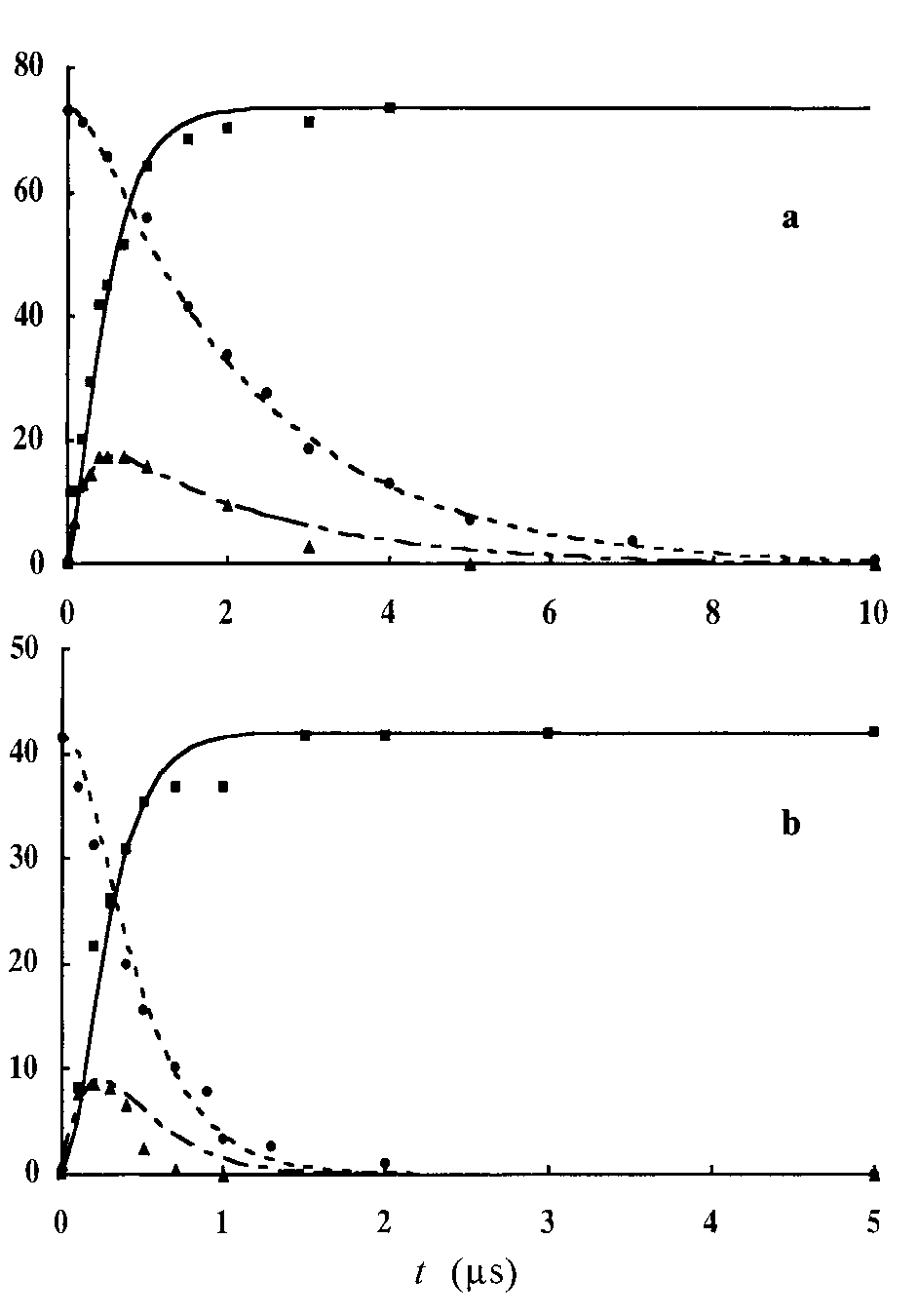
Рисунок 7. Зависимости сигнала PYESR от времени для трех импульсных последовательностей (см. Рис. 5.), зарегистрированные при фотовосстановлении антрахинона (а) и антрахинон-2-сульфоната (b) в мицелле SDS (0.2 M). Концентрация спиновой ловушки 1 мМ. Лазерное облучение проводилось в течение 20 с. на длине волны 335 нм. Расчетные кривые представлены прерывистой линией (ИП-1), сплошной линией (ИП-2) и пунктиром (ИП-3).
Эксперименты по лазерному импульсному фотолизу ацетиленовых кетонов позволили измерить времена жизни триплетных состояний кетонов и соответствующих кетильных радикалов, а также зарегистрировать значительный магнитный эффект на времена жизни кетильных радикалов (Рис.8 и Таблица 2).
Отметим, что магнитный эффект не наблюдается на времена жизни триплетных состояний кетонов, поскольку их образование не включает магнито-чувствительных стадий.
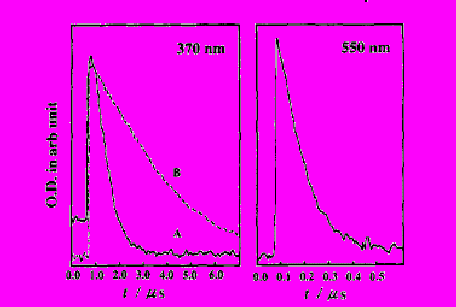
Рисунок 8. Кинетика спада промежуточного поглощения при фотолизе кетона XVI в мицеллярном растворе. Слева – кетильного радикала (λ = 370 нм) в отсутствие (a) и в присутствие (b) магнитного поля (150 мТл), справа – триплетного состояния (λ = 550 нм) (зависимость от магнитного поля отсутствует).
Таблица 2. Времена жизни возбужденного триплетного состояния и кетильного радикала кетонов XLI-XLII в мицеллярных растворах SDS и Brij 35 измеренные по спектрам промежуточного поглощения на длинах волн 550 и 370 нм. Времена жизни приведены в наносекундах. (*) не измерялась из-за перекрывания сигналов продуктов.
| кетон | XLI | XLII | ||||
| мицелла | τT | τК (H=0) | τК (H=150 мТл) | τT | τК (H=0) | τК (H=150 мТл) |
| SDS | 91 | 440 | 2800 | 1460 | * | 2420 |
| Brij 35 | <5 | 950 | 3800 | 56 | 1130 | 3100 |
Приведенные в данной главе примеры использования метода PYESR с временным разрешением демонстрируют уникальные возможности данного метода для получения кинетической информации о динамике радикальных пар в растворах. Полученные данные о структуре радикальных пар и о кинетике процесса фотовосстановления ряда карбонильных соединений хорошо согласуются с данными полученными другими методами, в частности, методами ХПЯ и лазерного импульсного фотолиза. Отметим, что использование в исследовании комбинации различных кинетических методов существенно повышает объем и достоверность полученной информации. В последующие годы этот метод успешно применялся нашими японскими коллегами для исследования бирадикалов, а также радикальных пар в других средах с ограниченной подвижностью, в частности, в нанопорах (M. Okazaki, et al., Phys. Chem. Chem. Phys., 2002, 4, 1201-1205).
В контексте исследования природы влияния организованной среды на реакционную способность химических соединений, наиболее важными являются следующие наблюдения. Это существенные изменения времен жизни РП и вероятностей клеточной рекомбинации свободных радикалов в мицеллах по сравнению с гомогенным раствором, а также зависимость динамики партнеров РП от параметров самой мицеллы. Эти наблюдения содержат указания на возможные причины изменений в механизмах и направлении реакций для многостадийных радикальных процессов в организованных средах. Исследованию таких процессов с участием биологически важных соединений методом ХПЯ, а также другими физическими методами посвящена следующая глава диссертации.
В Главе 7 представлены два цикла работ посвященных исследованию комплексов включения ряда лекарственных препаратов и каротиноидов. В первой части рассматривается важная проблема, имеющая отношение к практическому применению каротиноидов в качестве антиоксидантов. Это - комплексообразование каротиноидов и влияние организованной среды на их реакционную способность в окислительно–восстановительных процессах. Известно, что такие свойства каротиноидов, как гидрофобность, высокая фоточувствительность и химическая активность, существенно затрудняют их применение на практике. Одним из путей решения подобных проблем в фармакологии является использование комплексов включения типа «гость-хозяин». Молекулы «гостя» в комплексе могут менять свои физические, и химические свойства, а также биодоступность и стабильность. На первом этапе методами ЯМР, ЭПР и оптической спектроскопии были исследованы комплексы включения каротиноидов и их структурного аналога -ионона с циклодекстринами. Показано, что комплексы каротиноидов с циклодекстринами образуют агрегаты в водных растворах, обладают повышенной фотостабильностью, однако теряют способность захватывать свободные радикалы. Интересной находкой в этом плане явилось использование в качестве молекулы «хозяина» -глицирризиновой кислоты (ГК) - природного соединения принадлежащего к тритерпеновым гликозидам. Впервые показано, что ГК образует комплексы с каротиноидами не только в водных растворах, но и в ряде органических растворителей (ДМСО, ацетонитрил, спирты). В частности, по изменению интенсивности флюоресценции кантаксантина в ДМСО была оценена константа стабильности комплекса между молекулой кантаксантина и димером ГК (Рис. 9).
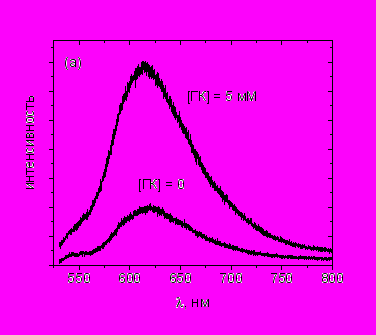
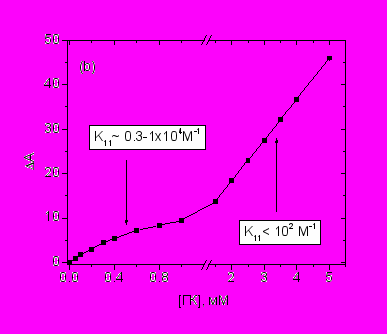
Рисунок 9. (а) Спектр флюоресценции раствора кантаксантина, 0.02 мМ в отсутствие и в присутствие глицирризиновой кислоты (ГК) в ДМСО содержащем 5% воды. Длина волны возбуждения 470 нм, регистрации – 620 нм. (b) Зависимость изменения интенсивности флюоресценции каротиноида от концентрации ГК в растворе.
Из рисунка видно, что ход кривой отличается для диапазона концентраций 0.01 – 1 мМ и > 1 мМ. На момент выполнения настоящей работы, кроме вышеописанных комплексов состава 2:1 были описаны мицеллы глицирризиновой кислоты, образующиеся в растворах с концентрацией более 1 мМ.
В работе показано, что комплексообразование с глицирризиновой кислотой оказывает заметное воздействие на реакционную способность каротиноидов. Было зарегистрировано уменьшение скоростей переноса электрона в реакции с акцепторами, а также удлинение времени жизни катион-радикалов каротиноидов в комплексах, приводящее к изменению соотношения продуктов реакции. На Рис. 10 приведен пример изменения кинетики спада сигнала поглощения катион-радикала -каротина в реакции с дихлор-дициан-бензохиноном (ДДХ) в присутствие ГК.
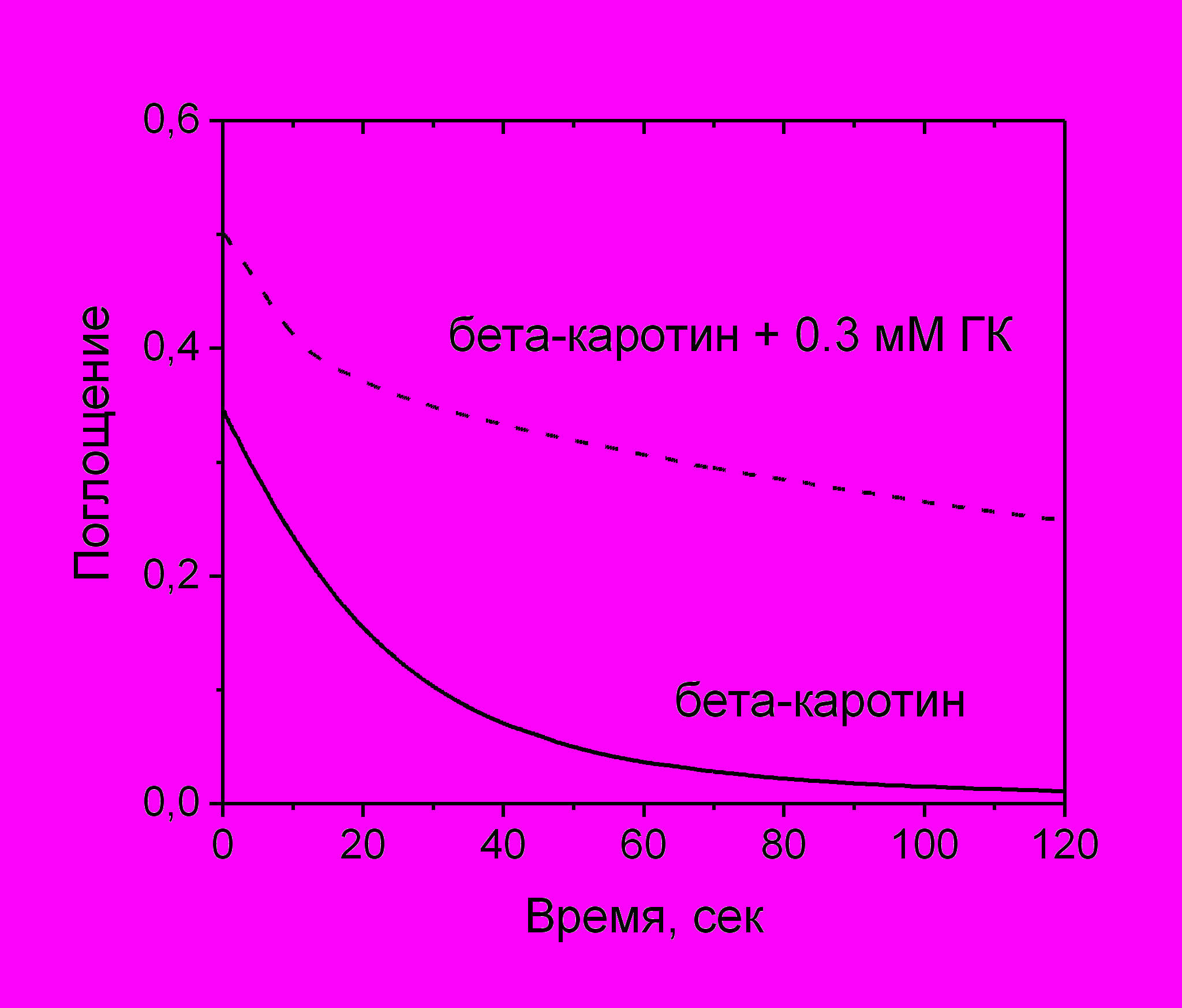
Рисунок 10. Кинетики спада сигнала поглощения катион-радикала -каротина на 935 нм в отсутствие и в присутствие ГК. Концентрации -каротина и ДДХ равны 4 М.
В отличие от комплексов с циклодекстринами, экспериментально обнаружено многократное (в десятки раз) увеличение скорости захвата перекисных радикалов (антиоксидантная активность) каротиноидами в комплексе с ГК (Рис. 11), и установлено, что причина этого явления кроется во влиянии комплексообразования на окислительные потенциалы каротиноидов.
Следует отметить, что, несмотря на большой интерес к использованию комплексов включения с целью направленного изменения свойств включенных соединений, до сих пор остается открытым вопрос о природе влияния комплексообразования на их реакционную способность. Представленные в настоящей главе результаты исследований процессов одноэлектронного переноса с участием комплексов каротиноидов являются практически единственной попыткой приблизиться к решению этого вопроса.
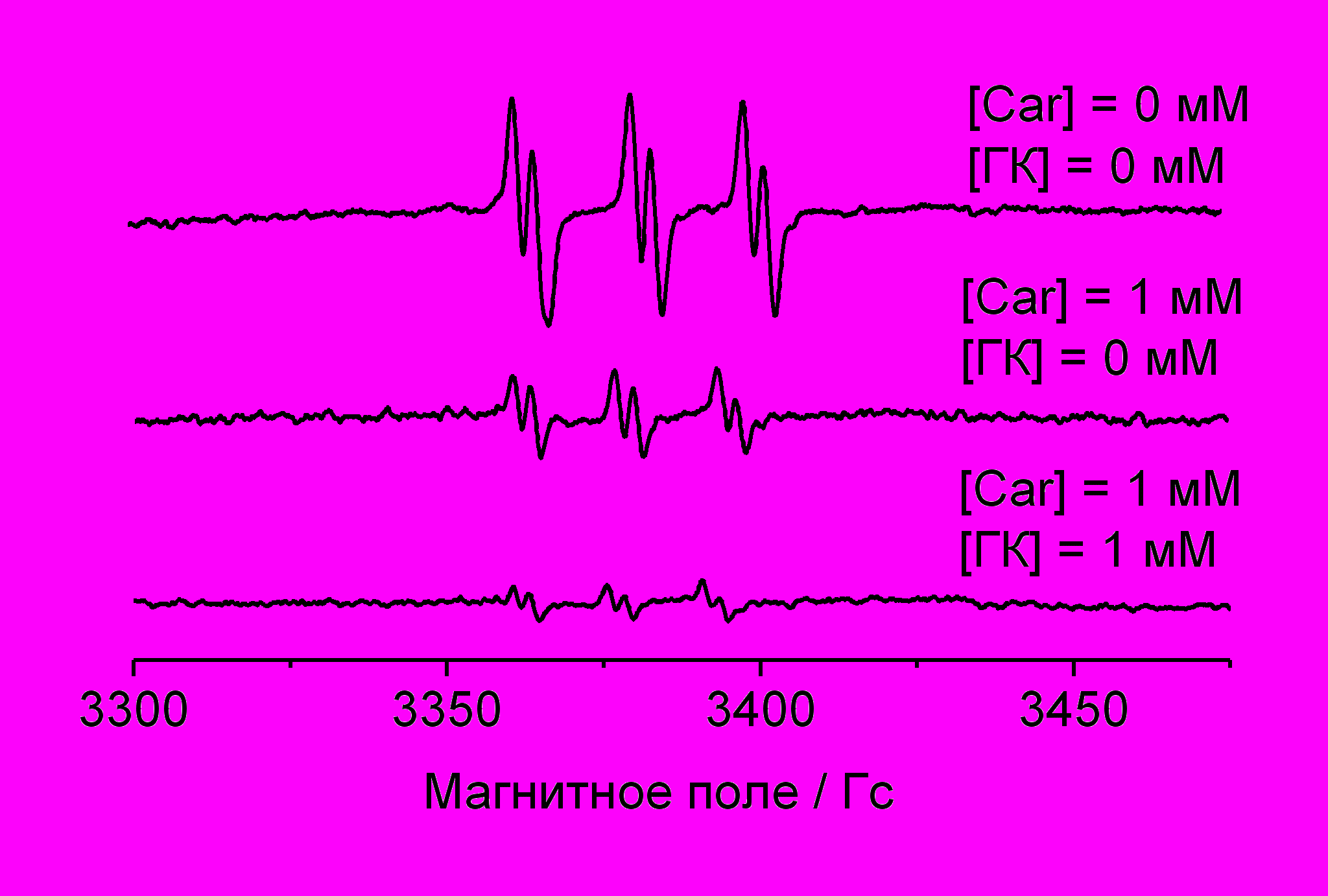
Рисунок 11. Спектры ЭПР аддукта PBN-OOH в отсутствие (вверху) и в присутствие кантаксантина и его комплекса с ГК в ДМСО. [PBN] = 5 мМ, [FeCl2] = 1 мМ, [H2O2] = 0.5 M.
В Главе 7 представлен также цикл работ, посвященных исследованию комплексов включения нифедипина и лаппаконитина с глицирризиновой кислотой, в частности, влияния комплексообразования на реакционную способность этих соединений. Используя оптическую и ЯМР спектроскопию (включая релаксационные методы) нам удалось показать, что глицирризиновая кислота образует очень стабильные комплексы как с нифедипином, так и с лаппаконитином (константа стабильности порядка 105 М-1, что на два порядка превышает типичное значение для комплексов циклодекстринов). В частности для нифедипина образование комплекса было доказано по изменению его растворимости в присутствие ГК (Рис. 12), а также по изменению времени фазовой релаксации Т2 (Рис. 13). Следует отметить, что в экспериментах на животных с участием автора диссертации было обнаружено значительное (в сотни раз) усиление терапевтической активности нифедипина в присутствие ГК.
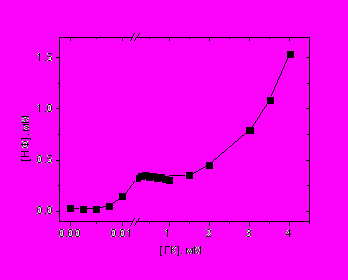
Рисунок 12. Диаграмма растворимости нифедипина как функция концентрации ГК в 5% метанольном растворе в воде.
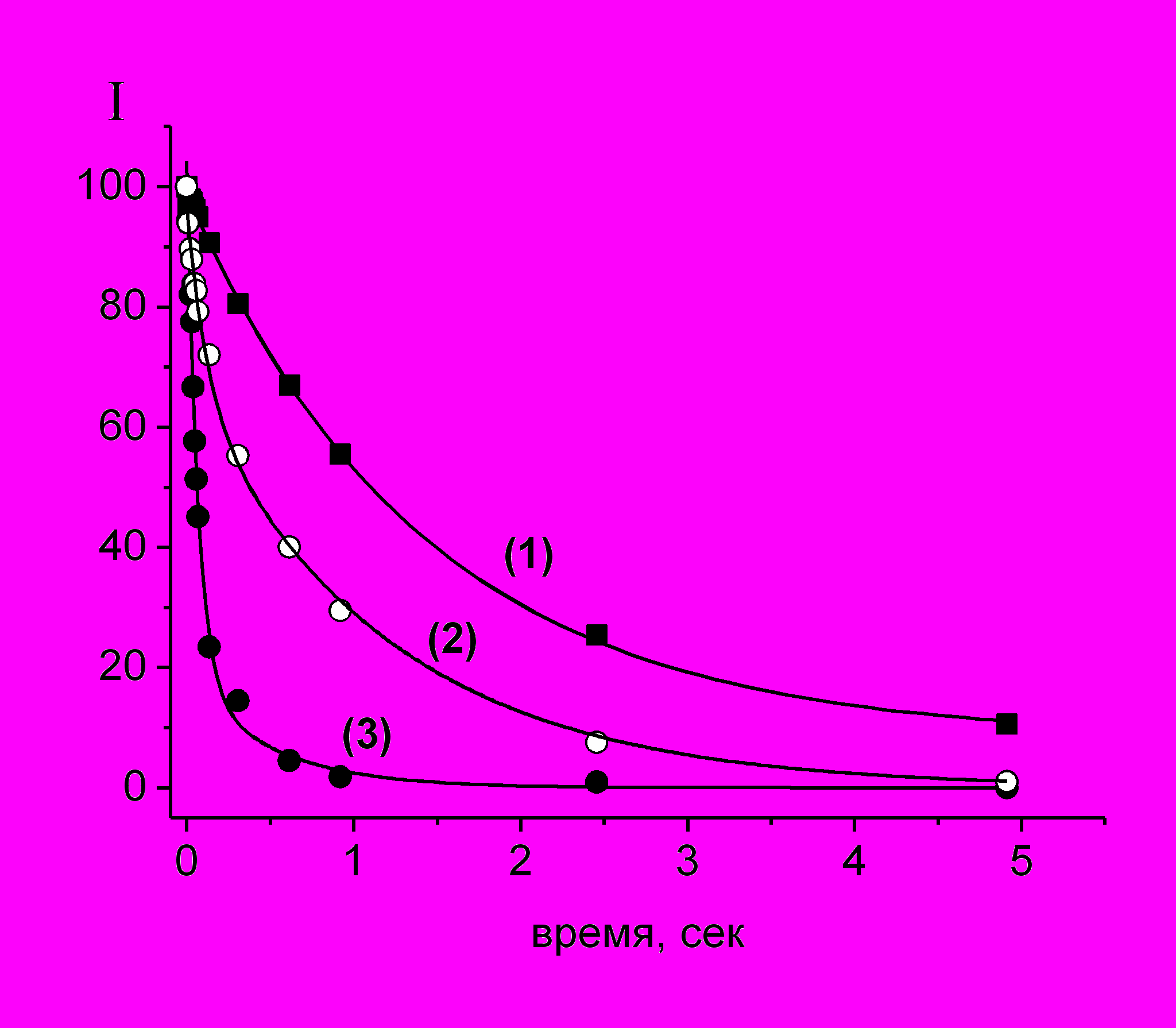
Рисунок 13. Кинетики спада сигнала эха метильных протонов НФ в чистом метаноле (1), в метаноле в присутствие 0.7 мМ ГК (2), и в 30% метанольном растворе в присутствие 0.7 мМ ГК (3).
В работе также продемонстрировано, что комплексообразование с ГК существенно снижает скорость фотодеградации нифедипина и лаппаконитина, приводящей к образованию активных свободных радикалов. Данный результат может иметь практическое значение при использовании комплексообразования для увеличения фотостабильности этих, а также других лекарственных препаратов, для увеличения их биодоступности и снижения токсичности (включая фото-токсичность).
ОСНОВНЫЕ РЕЗУЛЬТАТЫ И ВЫВОДЫ
I. В первой части работы, в результате исследования строения и свойств радикальных интермедиатов в растворах, установлены детальные механизмы ряда биологически значимых процессов:
- Продемонстрировано, что фотоинициированное окисление акцепторами электрона синтетических аналогов NADH - 1,4-дигидропиридинов (ДГП) проходит по радикальному пути с образованием тех же продуктов, которые получаются и в реакциях смешения: соответствующих пиридинов или катионов пиридиния.
- На примере широкого набора полиненасыщенных соединений получены экспериментальные доказательства участия короткоживущих парамагнитных частиц в реакциях фотоинициированной цис-транс изомеризации.
- Продемонстрировано, что скорости реакций перекисных радикалов с каротиноидами с коррелируют с их окислительными потенциалами. Это прямо указывает на связь антиоксидантной активности каротиноидов с процессом переноса электрона. Установлено, что каротиноиды могут проявлять как антиоксидантные, так и про-оксидантные свойства, и определена роль ионов металлов в этих процессах.
- Показано, что при фотолизе лекарственных препаратов нифедипина и лаппаконитина в растворах образуются активные короткоживущие парамагнитные интермедиаты: бирадикалы, ион-радикалы и нейтральные радикалы, могущие быть причиной фототоксических побочных эффектов, возникающих при медицинском применении этих препаратов.
II. Во второй части исследованы процессы в организованных средах:
- Создан время разрешенный импульсный вариант метода PYESR, позволяющего регистрировать спектры ЭПР короткоживущих радикальных пар. Измерены кинетические параметры радикальных пар образующихся при фотолизе ряда биологически активных карбонильных соединений в мицеллах SDS, а также зарегистрированы значительные магнитные эффекты на выхода и времена жизни свободных радикалов.
- Показано, что комплексообразование с глицирризиновой кислотой оказывает заметное воздействие на реакционную способность каротиноидов в окислительно-восстановительных реакциях. Обнаружено, что комплексообразование повышает растворимость препаратов в воде, и существенно увеличивает фотостабильность нифедипина и лаппаконитина. Последний результат может быть использован в медицинской практике, т.к. исследованные лекарства являются фототоксичными.
Основное содержание диссертации опубликовано в следующих статьях:
- The Mechanisms of the Oxidation of NADH Analogs. 1 .Photochemical Oxidation of N-Unsubstituted 1,4-Dihydropyridines by Various Acceptors /М.В. Taraban, A.I. Kruppa, N.E. Polyakov, et al. //J. Photochem. Photobiol. A Chem.- 1993.- V.73.- P.151-156.
- The Mechanisms of the Oxidation of NADH Analogs 2. N-Methyl Substituted 1,4-Dihydropyndines /A.I. Kruppa, М.В. Taraban, N.E. Polyakov, et al. //J. Photochem. Photobiol. A Chem.- 1993.- v.73.- P.159-163.
- The Mechanisms of the Oxidation of NADH Analogs. 3. Stimulated Nuclear Polarization (SNP) and CIDNP in Low Magnetic Fields in Photooxidation Reactions of 1,4-Dihydropyridines by Quinones /N.E. Polyakov, A.I. Kruppa, М.В. Taraban, et al. //J. Photochem. Photobiol. A Chem.- 1993.- V.74.- P.75-79.
- The mechanisms of the oxidation of NADH analogues. 4. Photooxidation of N-acetyl-substituted 1,4-dihydropyridine in the presence of quinones /N.E. Polyakov, A.I. Kruppa, T.V. Leshina et al. //J. Photochem. Photobiol. A: Chem.- 1997.- V.111.- P.61-64.
- EPR Spin trapping detection of carbon-centered carotenoid and β-ionone radicals /T.A. Konovalova, N.E. Polyakov, L.D. Kispert et al. //Free Rad. Biol. Med.- 2000.- V.28.- P.1030-1038.
- One-electron transfer product of quinone addition to carotenoids: EPR and optical absorption studies /N.E. Polyakov, V.V. Konovalov, T.V. Leshina, et al. //J. Photochem. Photobiol A: Chem.- 2001.- V.141.- P.117-126.
- The Carotenoids as Antioxidants. Spin-Trapping ESR and Optical Study /N.E. Polyakov, A.I. Kruppa, T.V. Leshina, et al. //Free Rad. Biol. Med.- 2001.- V.31.- P.43-52.
- Carotenoids as scavengers of free radicals in a Fenton reaction: antioxidants or pro-oxidants? /N.E. Polyakov, T.V. Leshina, T.A. Konovalova et al. //Free Rad. Biol. Med.- 2001.- V.31.- P.398-404.
- Electron transfer mediated geometrical cis-trans isomerization of polyenes /N. E. Polyakov, T. V. Leshina, L. D. Kispert //RIKEN Review- 2002.- V.44.- P.140-148.
- The influence of electron donors and acceptors on isomers distribution under the photolysis of β-ionone /N. E. Polyakov, T.V. Leshina //Mol. Phys.- 2002.- V.100.- P.1297-1302.
- Photoinitiated electron transfer interaction of all-trans retinal with electron donors and acceptors /N. E. Polyakov, V. S. Bashurova, P. S. Schastnev, et al. //J. Photochem. Photobiol., A: Chem.- 1997.- V.107.- P.55-62.
- Single electron transfer in the phototransformations of β-ionone in the presence of electron acceptors /N. E. Polyakov, A. I. Kruppa, V. S. Bashurova, et al. //J. Photochem. Photobiol. A: Chem.- 1999.- V.128.- P.65-74.
- The role of radicals in the phototransformations of β-ionone in the presence of electron donors in solution /N. E. Polyakov, A. I. Kruppa, V. S. Bashurova, et al. //J. Photochem. Photobiol. A: Chem.- 2002.- V.153.- P.113-119.
- Electron transfer mediated geometrical photoisomerization of ,-unsaturated ketones in the presence of electron donors in solution /N. E. Polyakov, V. S. Bashurova, T. V. Leshina, et al. //J. Photochem. Photobiol. A: Chem.- 2002.- V.153.- P.77-82.
- Изучение комплексов включения некоторых терпеноидов с -циклодекстрином методом ЯМР (Обзор) /О.А. Лузина, Н.Ф.Салахутдинов, Н.Э. Поляков, и др. /Химия и компьютерное моделирование. Бутлеровские сообщения- 2002.- №7.- С.21-25.
- Radical pair dynamics observed with pulse-mode PYESR /N.E. Polyakov, M. Okazaki, Y. Konishi et al. //Applied Mag. Res.- 1994.- V.7.- P.149-166.
- Dynamic properties of SDS micelle as detected by «Radical-pair-probe» with using pulse PYESR technique /M. Okazaki, N.E. Polyakov, K. Toriyama //J.Phys.Chem.- 1995.- V.99.- P.6452-6456.
- Radical pair dynamics in the photoreduction of anthraquinone in SDS micellar solution detected by pulse-mode PYESR: temperature and salt dependences /N.E. Polyakov, M. Okazaki, Y. Konishi et al. //J.Phys.Chem.- 1995.- V.99.- P.15108-15113.
- A pulse-mode PYESR study on the dynamics of radical pair produced in photoreaction of anthraquinone in SDS micellar solution /N.E. Polyakov, M. Okazaki, Y. Konishi et al. //J. Phys. Chem.- 1998.- V.98.- P.10558-10562.
- PYESR study on the dynamic behaviour of RP generated in photoreaction of acetylenic ketones in SDS micellar solution /N.E. Polyakov, T.V. Leshina, M. Okazaki et al. //J. Phys. Chem.- 1994.- V.98.- P.10563-10567.
- Photochemistry of acetylenic ketones in SDS micellar solution as studied by PYESR and transient absorption techniques /N.E. Polyakov, M. Okazaki, H. Fukaya et al. //Photochem. Photobiol.- 1995.- V.61.- P.545-551.
- Photo-CIDNP Study of the Interaction of Tyrosine with Nifedipine. An Attempt to Model the Binding Between Calcium Receptor and Calcium Antagonist Nifedipine /N.E. Polyakov, M.B. Taraban, T.V. Leshina //Photochem. Photobiol.- 2004.- V.80.- P.565-571.
- Mechanisms of photoinduced electron transfer reactions of lappaconitine with aromatic amino acids. Time-resolved CIDNP study /N. E. Polyakov, V. K. Khan, M. B. Taraban, et al. //Org. Biomol. Chem.- 2005.- V.3.- P.881-885.
- Некоторые аспекты реакционной способности каротиноидов. Окислительно-восстановительные процессы и комплексообразование /Н. Э. Поляков и Т. В. Лёшина //Успехи химии- 2006.- Т.75.- №12.- С.1175-1192.
- β-Ionone cyclodextrins inclusion complexes: 1H NMR study and photolysis /N.E. Polyakov, T.V. Leshina, A. Petrenko, et al. //J. Photochem. Photobiol. A: Chem.- 2003.- V.161.- P.261-267.
- Inclusion Complexes of Carotenoids with Cyclodextrins. 1H NMR, EPR and Optical Studies /N.E. Polyakov, T.V. Leshina, T.A. Konovalova et al. //Free Rad. Biol. Med.- 2004.- V.36.- P.872-880.
- Complexation of lappaconitine with glycyrrhizinic acid. Structure, stability and reactivity studies /N. E. Polyakov, V. K. Khan, M. B. Taraban //J. Phys. Chem. B.- 2005.- V.109.- P.24526-24530.
- Host-Guest Complexes of Carotenoids with β-Glycyrrhizic Acid /N. E. Polyakov, T. V. Leshina, N. F. Salakhutdinov et al. //J. Phys. Chem. B.- 2006.- V.110.- P.6991-6998.
- Antioxidant and Redox Properties of Supramolecular Complexes of Carotenoids with β-Glycyrrhizic Acid /N.E. Polyakov, T.V. Leshina, N. F. Salakhutdinov, et al. //Free Rad. Biol. Med.- 2006.- V.40.- 1804-1809.
- Окислительно-восстановительные реакции природного алкалоида лаппаконитина /Н. Э. Поляков и Т. В. Лёшина //Известия РАН, сер. Химическая- 2007.- №4.- С.608—619.
- Phototransformation products of alkaloid lappaconitine: multinuclear NMR study /N. E. Polyakov, T. V. Leshina, A. V. Tkachev, et al. //J. Photochem. Photobiol., A: Chem.- 2008.- V.197.- P.290–294.
- Complex of Calcium Receptor Blocker Nifedipine with Glycyrrhizic Acid /N. E. Polyakov, V. K. Khan, M. B. Taraban, et al. //J. Phys. Chem. B.- 2008.- V.112.- P.4435-4440.
