Эпидуральная анестезия Леон Виссер, Медицинский Центр Мичиганского Университета, Энн Арбор, Мичиган, США
| Вид материала | Документы |
- Children Making Tomorrow, Мичиган, США. Вконкурс, 16.36kb.
- Эта глава посвящена как особенностям многоплодных родов, так и возможным осложнениям, 239.34kb.
- Ингаляционная анестезия с использованием низких потоков свежего газа у детей, 315.4kb.
- Медицинский центр Университета Аахен, 43.39kb.
- Рекомендации Американской ассоциации по изучению заболеваний, 1707.88kb.
- Абелес леон игнатьевич, 11950.78kb.
- Конкурс на проведение исследований по программе «Студенческие малые гранты», 77.91kb.
- «Учебно-научный медицинский центр», 922.54kb.
- Генри Форд и его автомобиль, 405.04kb.
- Научно-технический, исторический центр «космодром байконур», 50.5kb.
Эпидуральная анестезия
Леон Виссер,
Медицинский Центр Мичиганского Университета, Энн Арбор, Мичиган, США
Введение
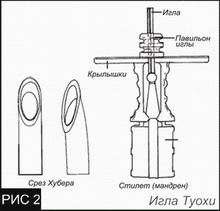
Эпидуральная анестезия является одним из наиболее часто используемых методов регионарного обезболивания. Анатомическое строение эпидурального пространства было описано в 1901 г. Корнигом, а уже в 1921 г. Фидель Пейдж впервые провел эпидуральную анестезию. В 1945 г. Туохи ввел в обращение иглу, которая и в настоящее время используется для выполнения пункции эпидурального пространства. Простота исполнения, усовершенствования в методике, появление новых препаратов вывели эпидуральную анестезию в число наиболее популярных и универсальных методов обезболивания и контроля над болью в хирургии и акушерстве. При выполнении эпидуральной анестезии может быть использована как техника однократного введения препарата, так и техника катетеризации эпидурального пространства. Применяются как местные анестетики, так и различные адъюванты, улучшающие качество анестезии. Эпидуральную анестезию включают в схемы общей анестезии, она используется для контроля над болью после торакальных вмешательств, операций на органах малого таза, брюшной полости и нижних конечностях.
Показания
Общие
В условиях эпидуральной анестезии могут быть выполнены оперативные вмешательства на нижних конечностях, органах брюшной полости и малого таза. Также возможно проведение и торакальных вмешательств, однако необходим высокий уровень блока, при котором не избежать возникновения побочных эффектов, выраженного дискомфорта и риска для пациента. Преимущества эпидуральной анестезии перед спинальной заключается прежде всего в возможности проведения продленной анестезии через катетер, устанавливаемый при операциях большой продолжительности. Эта особенность также дает возможность использовать данный метод для послеоперационной анальгезии, применяя местные анестетики или их комбинации с различными адъювантами.
Особые показания
- Ортопедия. Открытая фиксация переломов бедра, выполненная в условиях эпидуральной или спинальной анестезии, сопровождается значительно меньшей кровопотерей. У пациентов, перенесших артропластику или протезирование сустава под эпидуральной анестезией, меньше частота возникновения тромбоза глубоких вен.
- Сосудистая хирургия. Эпидуральная анестезия улучшает периферический кровоток у пациентов, подвергшихся реконструктивным сосудистым операциям на нижних конечностях.
- Ампутации. Пациенты, перенесшие ампутацию нижних конечностей и получавшие в течение 48-72 часов после операции эпидуральную анальгезию, имели низкую частоту развития фантомных болей, хотя это и не было доказано статистически достоверно.
- Акушерство. Эпидуральная анальгезия показана при родах с высоким риском, например, при заднем предлежании, беременности двойней, преэклампсии и затяжных родах. Кроме того, кесарево сечение, выполненное в условиях эпидуральной или спинальной анестезии, благодаря анестетическому фактору, ассоциируется с низкой материнской смертностью, чем проведенное под наркозом.
- Местные анестетики, опиоиды или их комбинации высоко эффективны в лечении послеоперационной боли. Эпидуральная анальгезия, как было доказано, сводит до минимума отрицательное влияние операции на сердечно-сосудистую и дыхательную системы, в частности, улучшает функцию внешнего дыхания и способность к откашливанию у пациентов со скомпрометированной дыхательной системой, таких как пожилые, тучные и страдающие обструктивными болезнями легких. Эпидуральная анальгезия способствует ранней активизации, снижает риск возникновения тромбоза глубоких вен и в сочетании с физиотерапией предупреждает развитие пневмоний.
- Травма грудной клетки с переломами ребер или грудины. Адекватная анальгезия в комбинации с физиотерапией улучшает показатели внешнего дыхания у пациентов с травмой грудной клетки.
Противопоказания
Абсолютные
- Отказ пациента
- Коагулопатия. Пункция и проведение катетера могут стать причиной травматического кровотечения в эпидуральном пространстве с образованием большой гематомы и сдавлением спинного мозга.
- Антикоагулянтная терапия. См. выше.
- Инфекции кожи в области пункции. При пункции в области инфицированной кожи возможно занесение патогенных микроорганизмов в эпидуральное пространство с последующим развитием таких серьезных осложнений, как менингит или эпидуральный абсцесс.
- Внутричерепная гипертензия. Случайный прокол твердой мозговой оболочки у пациента с высоким внутричерепным давлением может привести к вклинению головного мозга.
- Гиповолемия. Симпатическая блокада, вызываемая вводимыми эпидурально местными анестетиками, на фоне некоррегированной гиповолемии может стать причиной тяжелого циркуляторного коллапса.
Относительные
- Неконтактные пациенты могут представлять определенные трудности в их позиционировании и безопасном выполнении эпидуральной пункции.
- Неврологические заболевания, такие как, например, рассеянный склероз, могут быть противопоказанием, поскольку появление новых симптомов может быть ложно приписано эпидуральной блокаде.
- Фиксированный сердечный выброс. Скорее относительное противопоказание, чем абсолютное. Формируется при аортальном стенозе, гипертрофической обструктивной кардиомиопатии, митральном стенозе и полной сердечной блокаде. Пациенты, имеющие фиксированный сердечный выброс, не способны изменять его в ответ на периферическую вазодилятацию, вызываемую эпидуральной блокадой, а циркуляторный коллапс, который у них может возникнуть, с трудом поддается лечению.
- Анатомические аномалии позвоночника могут вызвать определенные трудности при выполнении эпидуральной блокады.
- Профилактическое назначение низких доз гепарина (см. обсуждение ниже).
Эпидуральная анестезия и антикоагулянты
- Применение стандартных доз гепарина или варфарина является абсолютным противопоказанием к эпидуральной блокаде.
- Использование низкомолекулярных гепаринов или небольших доз варфарина (INR<1.5) считается относительным противопоказанием.
- Введение небольших доз гепарина (по 5000 ед. одномоментно) не связано с риском развития эпидуральной гематомы. Выждите 4 часа после введения гепарина перед выполнением эпидуральной пункции. Не следует также назначать гепарин в течение ближайшего часа после выполнения блокады. Используйте данные рекомендации и при удалении катетера.
- Низкомолекулярные гепарины (<40mg эноксапарина и дальтепарина): выждите 12 часов после введения НМГ перед эпидуральной блокадой, а также и перед удалением катетера.
- НПВС (включая аспирин) не повышают риска развития эпидуральной гематомы.
- Интраоперационное болюсное введение 5000 Ед гепарина в вену после выполненной эпидуральной или спинальной пункции кажется безопасным, однако тщательное послеоперационное наблюдение за пациентом все-таки требуется. Появление крови в катетере может служить индикатором развития кровотечения. В связи с этим некоторые хирурги предпочитают оперировать через 12 часов после установки эпидурального катетера, другие же (если предоперационные показатели коагулограммы нормальные) вводят гепарин не ранее, чем через 1 час после установки катетера.
- Фибринолитики и тромболитики: избегайте пункции эпидурального пространства в течение 24 часов. Перед процедурой проконтролируйте состояние свертывающей системы.
- Тромбоцитопения. Количество тромбоцитов менее 100 000 является относительным противопоказанием для выполнения эпидуральной блокады.
- Эпидуральную гематому следует заподозрить у пациентов, которые предъявляют жалобы на сильные боли в спине в течение нескольких часов или дней после блокады или при наличии длительного неврологического дефицита (#включающего потерю чувствительности, парестезии, мышечную слабость и потерю контроля за естественными сфинктерами). При подозрении на гематому направьте больного к ортопеду или нейрохирургу для проведения ранней хирургической декомпрессии. Несмотря на своевременную диагностику, заболеваемость по-прежнему остается высокой.
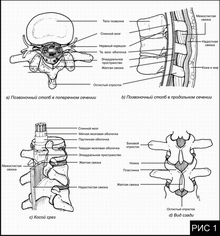
Анатомия эпидурального пространства (рис.1)
Техника выполнения эпидуральной анестезии
Подготовка
Катетеризация эпидурального пространства должна выполняться только при наличии оборудования для проведения СЛР. Обеспечьте мониторинг АД и ЧСС. Также как и при выполнении других инвазивных вмешательств, необходимо получить информированное согласие пациента на выполнение эпидуральной пункции. Пациент должен быть информирован о потенциальном риске и возможном осложнениях. Традиционный осмотр анестезиолога должен быть не менее тщательным, чем перед проведением общей анестезии. Специальные исследования должны включать обследование сердечно-сосудистой системы с исключением поражения клапанного аппарата или других состояний, при которых невозможно увеличение сердечного выброса в ответ на вазодилятацию, вызываемую симпатической блокадой. Обследуйте спину пациента на наличие различных патологических изменений. Весьма важно лабораторное исследование системы гемостаза пациентов, подозрительных на наличие коагулопатии или получающих антикоагулянты. ПТВ, АЧТВ и количество тромбоцитов должны быть в пределах нормальных границ. В сомнительных случаях исследуйте функциональное состояние тромбоцитов и проконсультируйтесь с гематологом.
Прежде чем выполнять блокаду, проверьте все оборудование. Обеспечьте венозный доступ, желательно канюлей большого диаметра. Кожа обрабатывается спиртом или йод-содержащим препаратом. Спина накрывается стерильным операционным бельем, а анестезиолог принимает все меры предосторожности против инфекции, включая стерильную одежду, маску и перчатки.
Оборудование
В настоящее время широко доступны асептически упакованные одноразовые эпидуральные наборы. Все оборудование и используемые препараты должны быть стерильны и не содержать консервантов.
Методы идентификации эпидурального пространства
Пройдя желтую связку, срез иглы попадает в эпидуральное пространство. Само по себе эпидуральное пространство очень узкое и иногда его называют потенциальным пространством, т.к. нередко желтая связка тесно примыкает к твердой мозговой оболочке. Будьте внимательны при выполнении эпидуральной пункции, как только игла прошла желтую связку, остановитесь, так как при дальнейшем бесконтрольном продвижении иглы легко перфорировать твердую мозговую оболочку. За эти годы было разработано несколько способов идентификации эпидурального пространства, но большинство анестезиологов в настоящее время используют методику «утраты сопротивления» с физиологическим раствором или воздухом.
Данные способы практически схожи, но разница в ощущениях при давлении на поршень во время продвижения иглы и попадании ее в эпидуральное пространство очевидна. Такие методики, как «метод висячей капли» использовались раньше. В соответствии с ней, на павильон продвигаемой без шприца иглы подвешивалась капля физиологического раствора. Эпидуральное пространство идентифицировали по втяжению капли внутрь иглы за счет отрицательного давления в первом. Сегодня данная методика используется крайне редко.
При выполнении блокады пациент может лежать на боку или сидеть. Ему нужно помочь правильно согнуть спину, что «приоткроет» промежутки между остистыми отростками и облегчит идентификацию межпозвонковых пространств. После выбора места проведения пункции спина обрабатывается антисептиком и накрывается стерильным бельем (см. выше).
- Удалите стилет и к павильону иглы подсоедините шприц. Для использования теста потери сопротивления жидкости, заполните шприц 5-10 мл физиологического раствора. Держите шприц в правой руке, установив большой палец на поршень. Большим и указательным пальцами левой руки удерживайте иглу за крылышки, упираясь тылом ладони в спину пациента. Левой рукой поддерживаете иглу в стабильно срединном положении и одновременно препятствуете ее случайному глубокому введению. Осуществляя постоянное давление большим пальцем на поршень шприца, продвигайте иглу сквозь межостистую связку. В тот момент, как срез иглы пройдет ее, появится некоторое чувство потери сопротивления, поскольку подлежащая ткань имеет меньшую по сравнению со связкой плотность. Но незначительное сопротивление давлению на поршень все же имеется. Иногда эта ложная потеря сопротивления может вызвать определенные сложности в идентификации эпидурального пространства. При дальнейшем продвижении игла входит в желтую связку и появляется значительное сопротивление давлению на поршень, поскольку желтая связка по плотности близка к коже. Оказывая постоянное давление на поршень, медленно продвигайте иглу, пока ее срез не пройдет сквозь желтую связку. Остановитесь, как только солевой раствор свободно посылается в ткани.
- Отсоединив шприц, аккуратно введите катетер через иглу. Катетер имеет маркировку, показывающую расстояние от дистального конца. Он должен быть продвинут до появления у павильона иглы 15-18 см отметки, что гарантирует нахождение достаточной его длины в эпидуральном пространстве. Аккуратно, чтобы не удалить катетер, извлеките иглу. Маркировка на игле поможет узнать глубину расположения эпидурального пространства. Данный показатель можно использовать также и для определения необходимой глубины введения катетера. Например, если эпидуральное пространство располагается на глубине 5 см, катетер необходимо подтянуть до появления на коже 10 см отметки. Оставшиеся примерно 5 см в эпидуральном пространстве считаются оптимальными.
- Методика с использованием потери сопротивления воздуху несколько отличается от вышеописанной. Присоединяют шприц с 5-10 мл воздуха, как только игла входит в межостистую связку. Иглу за крылья удерживают большими и указательными пальцами обеих рук. Нажав на поршень шприца и ощутив упругое сопротивление, аккуратно продвигают иглу дальше, обеспечивая упором обеими руками в спину пациента ее стабильность. Через 2-3 мм вновь аккуратно давят на поршень и продолжают введение иглы. При вхождении иглы в желтую связку ощущается значительное сопротивление. Далее продвигайте иглу по 2 мм. При попадании иглы в эпидуральное пространство обычно ощущается характерный «щелчок». Далее воздух может быть инъецирован в эпидуральное пространство без сопротивления. Отсоедините шприц и введите катетер как описано выше.
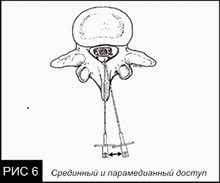
Парамедианный доступ
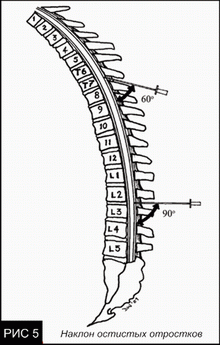
Эпидуральную блокаду на грудном уровне выполнить намного сложнее, чем на поясничном. Она должна выполняться только подготовленными и уверенными в себе специалистами.
Трудности, возникающие в процессе выполнения эпидуральной блокады
- Постоянно встречаемое костное сопротивление – попробуйте придать пациенту более согнутую позицию или изменить его положение. Если и это не помогло, используйте парамедианный доступ (если выполняли срединным).
- Затруднения при введении катетера – слегка повращайте иглу, чтобы изменить направление среза. Большинство наборов содержит направитель, устанавливаемый в павильон иглы и позволяющий значительно легче осуществить подачу катетера. Если данные способы не привели к успеху, значит игла, скорее всего, находится не в эпидуральном пространстве. Извлекайте катетер вместе с иглой, чтобы избежать его срезывания.
- Истечение жидкости из иглы – если использовался физиологический раствор, выждите несколько секунд для контроля. При продолжающемся истечении вероятен прокол твердой мозговой оболочки. Используйте другой уровень для блокады. Если же истечение жидкости прекратилось, установите катетер, но вводите уменьшенные дозы местных анестетиков, постепенно их увеличивая и внимательно наблюдая за признаками возможного спинального блока.
- Поступление жидкости из катетера – см. выше.
- Боль при катетеризации эпидурального пространства – ощущения «прострела» при введении катетера иногда встречаются, но если подобные болевые ощущения сохраняются, значит игла или катетер соприкасаются с корешком и должны быть извлечены, а пункция и катетеризация повторены.
- Кровь в катетере. Это свидетельствует о попадании катетера в эпидуральную вену. Подтяните его на 1-2 см и промойте физиологическим раствором. Проведите аспирационную пробу. Если крови в катетере нет, его можно использовать, но с осторожностью, выполняя следующие условия: 1) проводя аспирационную пробу перед каждым введением местного анестетика, 2) дозы наращивайте постепенно, небольшими объемами, 3) необходимо следить за появлением ранних симптомов проявления токсичности местного анестетика.
Факторы, влияющие на проведение эпидуральной анестезии
Место пункции
- При поясничном введении раствор анестетика распространяется как каудально, так, и, причем в большей степени, краниально, задерживаясь на уровне L5 и S1 сегментов из-за больших размеров соответствующих корешков.
- После введения на грудном уровне анестетик распространяется равномерно от места инъекции. Верхние грудные и нижние шейные корешки из-за своего большого диаметра устойчивы к действию анестетика. В грудном отделе объем эпидурального пространства невелик и для осуществления блокады требуется значительно меньшее количество местного анестетика по сравнению с поясничной зоной.
Дозировка
Доза, необходимая для анальгезии или анестезии определяется, но в целом для блокады 1 сегмента требуется от 1 до 2 мл местного анестетика. Вследствие большой вариабельности размеров эпидурального пространства трудно предугадать распространение раствора местного анестетика в нем, когда еще часть препарата просачивается в паравертебральную область.
Физиологический эффект при эпидуральной блокаде не зависит от дозы препарата, выраженной в миллиграммах. Большую роль здесь играют не только концентрация препарата, но и его объем. Больший объем местного анестетика низкой концентрации приведет к блокаде большего количества сегментов, но с легкой степенью сенсорной и моторной блокады. Важно помнить, что симпатические нервные волокна имеют самый малый диаметр и легко блокируются даже при использовании низких концентраций анестетиков. Не забывайте также, что степень или выраженность симпатического блока прямо зависит от количества блокированных сегментов. При наличии эпидурального катетера не вводите сразу большое количество анестетика, чтобы не вызвать высокого блока с гипотонией.
Необходимость в повторении или повышении дозы местного анестетика прямо зависит от продолжительности действия препарата. Повторные дозы вводят еще до того момента, как пациент начнет испытывать боль. Целесообразно руководствоваться так называемым «временем двухсегментарной регрессии». Это время, которое проходит от введения первой дозы препарата до момента снижения уровня сенсорной блокады на два сегмента. Повторная доза как правило составляет 1/2 первоначальной. Например, время двухсегментарной регрессии для лидокаина составляет 90-150мин, а для бупивакаина 200-260мин.
Возраст, рост и вес
С возрастом уменьшается объем местного анестетика, необходимого для формирования достаточного уровня блокады, возможно, вследствие уменьшения размеров и снижения податливости эпидурального пространства. Рост пациента в некоторой степени коррелирует с необходимым для блокады объемом анестетика. Так, например, пациенту ростом 150 см необходимо около 1 мл на сегмент, в то время как для высоких пациентов могут потребоваться дозы до 2 мл на сегмент. Наиболее безопасный подход в таких ситуациях заключается в постепенном болюсном введении и тщательном контроле за уровнем возникающего блока. Между весом пациента и необходимым объемом анестетика имеется небольшая взаимосвязь. Например, у тучных пациентов эпидуральное пространство уменьшено за счет эффектов, вызываемых повышенным внутрибрюшным давлением, поэтому им требуются меньшие объемы препаратов. Кроме того, полнокровие эпидуральных венозных сплетений, вызываемое затруднением оттока в системе непарной вены, уменьшает объем эпидурального пространства и увеличивает риск прокола эпидуральных вен. Данное положение относится и к пациентам с асцитом, с внутрибрюшными опухолями больших размеров и беременным на поздних сроках.
Положение пациента
Влияние силы тяжести на распространение анестетика весьма спорно. Однако, в положении пациента сидя интенсивнее блокируются нижние поясничные и сакральные корешки, а в положении на боку – корешки на зависимой стороне. И хотя имеется крайне мало научных доказательств на этот счет, опыт практикующих врачей свидетельствует об определенном влиянии силы тяжести на распространение анестетика.
Вазоконстрикторы
Известно, что добавление сосудосуживающих препаратов к местным анестетикам увеличивает продолжительность действия проводниковой или инфильтрационной анестезии, однако их влияние на длительность эпидуральной блокады не однозначно. Назначение адреналина (1:200 000) с бупивакаином не удлиняет время блокады, в то время как добавление его к лидокаину увеличивает продолжительность блока. Но тем не менее, вазоконстрикторы уменьшают системную всасываемость анестетика и снижают риск проявления токсичности.
pH местных анестетиков
Доступные растворы местных анестетиков имеют pH 3.5-5.5, обеспечивающее химическую стабильность и бактериостатичность. Большинство местных анестетиков являются слабыми основаниями и все они гидрофильны. Возможность блокады нерва зависит от проницаемости липидных мембран. Наиболее легко этого добиваются неионизированные (липофильные) формы препарата. Из этого следует, что увеличивая рН препарата, можно увеличить его проникающую способность и ускорить наступление блокады. Добавление 8.4% соды (0.5мл на 10мл местного анестетика) стало, например, весьма популярным решением в достижении более быстрого начала действия препарата при кесаревом сечении.
Физиологические эффекты эпидуральной блокады
Сегментарные нервы в грудном и поясничном отделах содержат чувствительные, двигательные и симпатические волокна. Чувствительные и симпатические волокна имеют меньший диаметр и легче блокируются, чем толстые, но быстрее проводящие импульсы двигательные волокна. Симпатическая блокада обычно распространяется на 1-2 сегмента выше сенсорной.
Влияние на системы и органы
- Сердечно-сосудистая система. Возникающая дилятация емкостных сосудов и сосудов сопротивления становится причиной развития относительной гиповолемии и как следствие тахикардии с гипотензией. Это поддерживается и симпатической блокадой надпочечников, которая препятствует выбросу катехоламинов. Если блок распространяется до Th2, развивается и симпатическая блокада сердца (Тh2-Тh5) и, как результат, возникает брадикардия. Благодаря всему выше описанному может возникнуть гипоперфузия во всех жизненно важных органах и потребоваться мероприятия, направленные на повышение АД и сердечного выброса, заключающиеся во введении жидкости и назначении вазопрессоров. При блокаде ниже уровня L2, что требуется, например, в хирургии нижних конечностей, не наблюдается столь выраженных нарушений гемодинамики, как при операциях, для которых необходим уровень блока выше пупка.
- Дыхательная система. Блокада грудных корешков с межреберными нервами, иннервирующими дыхательную мускулатуру, приводит к диафрагмальному дыханию с появлением выраженного дискомфорта у пациентов.
- Желудочно-кишечный тракт. Блокада симпатических сплетений на уровне Тh5-L1 приводит к преобладанию парасимпатического влияния блуждающего нерва и крестцового сплетения. Расслабляются естественные сфинктеры, усиливается перистальтика, уменьшается дилятация кишечника.
- Эндокринная система. Симпатическая блокада надпочечников ведет к снижению выработки катехоламинов.
- Мочевыводящая система. Обычно возникает задержка мочи. При значительной вазодилятации, способной вызвать гипотонию, уменьшается и скорость клубочковой фильтрации.
Влияние на сердечно-сосудистую систему при беременности. Увеличенная матка, в положении женщины на спине, сдавливая нижнюю полую вену, вызывает ухудшение венозного возврата и снижение сердечного выброса. Вазодилятация, возникающая при эпидуральной блокаде, усиливает эти эффекты. Сдавление аорты приводит к редукции маточного кровотока. Сочетание эпидуральной блокады и аорто-кавальной компрессии может значительно ухудшить маточно-плацентарный кровоток. При проведении эпидуральной анестезии и анальгезии у женщин необходимо избегать положения на спине. Предпочтение следует отдавать левому боковому или слегка наклонному положению. При возникновении гипотонии корригируйте ее введением жидкости. Не используйте α-адреномиметики (метоксамин и фенилэфрин), поскольку они, вызывая сужение маточных сосудов, нарушают маточно-плацентарный кровоток. Эфедрин является средством выбора в данной ситуации, поскольку он прежде всего является β-агонистом и повышает АД, увеличивая сердечный выброс. Но тем не менее, при возникновении тяжелой гипотонии истинные вазопрессоры могут быть более эффективны для коррекции возникающей гипоперфузии матки.
Методика проведения эпидуральной блокады и выбор препаратов
Техника однократной инъекции или катетеризация эпидурального пространства
Методика однократного болюсного введения препарата в эпидуральное пространство без катетеризации последнего все еще широко используется для обеспечения интраоперационной анестезии или послеоперационной анальгезии. Основные недостатки данной методики это: 1) время послеоперационного обезболивания ограничено продолжительностью действия избранного препарата и не может быть увеличено, и 2) риск, связанный с одномоментным введением полной дозы препарата без предшествующей тест-дозы. При использовании данного варианта обезболивания крайне высок риск развития высокой блокады, проявлений токсичности местного анестетика и полного спинального блока. В связи с этим не допускается выполнение эпидуральной блокады по методике однократного болюсного введения при каких бы то ни было сложных ситуациях, особенно неопытными анестезиологами.
После установки эпидурального катетера, для исключения его субарахноидального введения инъецируется тест-доза местного анестетика (примерно 3,5 мл 0,5% бупивакаина). За пациентом наблюдают в течение некоторого времени. Данная доза, введенная в субарахноидальное пространство, вызовет полную хирургическую анестезию ниже уровня введения и будет сопровождаться характерным для спинальной анестезии снижением АД. Если же катетер установлен правильно (в эпидуральном пространстве), введение такой тест-дозы вряд ли вызовет колебания АД и развитие сенсорной блокады. После проведения теста характер введения препаратов в эпидуральное пространство будет зависеть от целей, поставленных перед анестезиологом. Важный принцип заключается в том, что формирование анестезии должно осуществляться постепенно, с введением небольших доз и под внимательным контролем за состоянием пациента. После формирования удовлетворительного блока, необходимого для хирургической анестезии, анальгезии в родах или после операции, его поддержание может осуществляться периодическим введением местных анестетиков (с опиоидами или без них) или в виде постоянной инфузии (при наличии необходимого оборудования).
| Таблица. Примерный выбор анестетика и техники эпидурального блока в зависимости от цели. | |||||
| | Обезболивание родов | Кесарево сечение | Хирургия нижних конечностей | Лапаротомия в условиях общей анестезии | Торакотомия или перелом ребер |
| Уровень пункции | L2-L4 | L2-L4 | L2-L4 | Th8-Th10 | В соответствующем промежутке, обычноTh5-Th7 |
| Рекомендуемый уровень блока | Th8-Th9 | Th6-Th7 | Th10 | От Th7 до Th10 | Соответствующая зона |
| Характер блока | Минимальный двигательный | Двигательный и сенсорный | Двигательный и сенсорный | Сенсорный и минимальный моторный | Сенсорный и минимальный моторный |
| Выбор местного анестетика | 0,1-0,25% бупивакаин | 15-20 мл 2% лидокаин + адреналин или 0,5% бупивакаин | 0,5% бупивакаин | 0,25-0,5% бупивакаин, в соответствии с зоной вмешательства | 0,25-0,5% бупивакаин, в соответствии с зоной вмешательства |
| Выбор опиоида | Фентанил 50 мкг | Фентанил 100 мкг | Морфин 1-2 мг или диаморфин 2-3 мг | Морфин 1-2 мг или диаморфин 2-3 мг | Морфин 1-2 мг или диаморфин 2-3 мг |
| Инфузия | 0,1% бупивакаин + фентанил 2 мкг/мл | После операции 0,166% бупивакаин + диаморфин 0,1мг/мл | Обычно нет необходимости | После операции 0,166% бупивакаин + диаморфин 0,1мг/мл | После операции 0,166% бупивакаин + диаморфин 0,1мг/мл |
| Скорость инфузии | 0-12 мл/час | 0-8 мл/час | - | 0-12 мл/час | 0-8 мл/час |
| Примечание: 0,166% бупивакаин готовится смешиванием 10 мл 0,5% бупивакаина с 20 мл 0,9% NaCl | |||||
Выбор препаратов.
Он зависит от целей проведения эпидуральной блокады.
- Хирургическая анестезия – требует мощного сенсорного блока без существенной моторной блокады. Обычно используемые в этой ситуации местные анестетики – 2% раствор лидокаина в дозе 10 – 20 мл (с адреналином 1:200 000 или без него) или 10 – 20 мл 0,5% бупивакаина. Последний характеризуется более продолжительным действием, но для формирования анестезии требуется больше времени.
- Для анальгезии в родах наибольшую популярность получил 0,1 – 0,25 % раствор бупивакаина в связи с незначительно выраженным моторным блоком. Дозировка: 5 – 10 мл.
- Для послеоперационной анальгезии используются анестетики низкой концентрации, такие как 0,1 – 0,166% раствор бупивакаина с опиоидами или без них. Введение может осуществляться дискретно (болюсами) или в виде постоянной инфузии. Показано, что эпидуральная анальгезия, контролируемая пациентом, не менее адекватна, но более безопасна.
Эпидуральные опиоиды
Добавление опиоидов к растворам местных анестетиков получило большую популярность. Опиоиды, взаимодействуя с опиатными рецепторами в спинном мозге, улучшают качество проводимой блокады. Различные опиоиды, такие как морфин (2-5 мг), фентанил (50-100 мкг) или диаморфин (2-4 мг) успешно используются изолированно или в комбинации с местными анестетиками для контроля боли в послеоперационном периоде или в родах, а также интраоперационно. Как было показано, постоянная инфузия комбинации местного анестетика с опиоидом более эффективна, чем периодическое введение для контроля болевого синдрома.
У пожилых, ослабленных больных и больных с ХОБЛ дозы опиоидов должны быть снижены из-за риска развития депрессии дыхания.
Осторожность должна быть и при назначении морфина эпидурально, поскольку может возникнуть отсроченная депрессия дыхания. Это является следствием его низкой липофильности, поэтому часть препарата, не связываясь с рецепторами спинного мозга, переходит в спинномозговую жидкость и перемещается ее током краниально к дыхательному центру. Такая отсроченная депрессия может возникнуть и по прошествии 24 часов от введения.
Опиоиды могут назначаться эпидурально и без местных анестетиков. Петидин (меперидин), к примеру, по своей структуре схож с местными анестетиками и в дозе 25-75 мг эффективен как для обеспечения интраоперационной анестезии, так и для послеоперационной анальгезии.
Все опиоиды, назначаемые эпидурально, потенциально опасны в отношении угнетения дыхания, что необходимо помнить анестезиологу, оставляющему таких пациентов без наблюдения. Пациенты должны находится под пристальным вниманием медсестер с тщательным контролем за ЧД и уровнем сознания. При невозможности осуществления такого контроля опиоиды эпидурально не назначаются. Среди других препаратов, вводимых эпидурально, следует отметить кетамин и α2-адреноагонисты (например, клофелин).
Осложнения и побочные эффекты
С эпидуральной анестезией связаны некоторые серьезные осложнения. При проведении эпидуральной анестезии обязательно должны быть под рукой оборудование и средства для проведения реанимационных мероприятий.
Гипотония как наиболее часто наблюдаемое побочное действие при формировании блокады выше пупка, обсуждалась ранее. Как правило, она возникает у беременных в родах и при кесаревом сечении. Гипотония должна быть корригирована быстрым введением жидкости и вазопрессоров. Характерным симптомом гипотонии является тошнота, возникающая, как правило, еще раньше, чем диагностируется снижение АД.
Чрезмерно высокий блок возникает из-за введения некорректно большой дозы местного анестетика в эпидуральное пространство. Проявляется гипотонией, тошнотой, снижением чувствительности или парестезиями в руках или затруднением дыхания вследствие блокады корешков, иннервирующих дыхательную мускулатуру. Данные симптомы могут быть крайне тягостными для пациента, и в наиболее тяжелых случаях наряду с лечением гипотонии может потребоваться индукция в анестезию с интубацией трахеи. При адекватном дыхании ограничиваются наблюдением и лечением гипотонии. При появлении сонливости и дизартрии, что свидетельствует о чрезмерно высоком блоке, лечение должно начинаться немедленно (см. полный спинальный блок).
Токсичность местных анестетиков может проявляться при введении больших доз в эпидуральное пространство. Даже небольшое количество местного анестетика, попавшего в кровеносный сосуд, может проявить токсичность. Как правило, это происходит при попадании катетера в одну из эпидуральных вен. Поэтому всегда, прежде чем вводить анестетик в катетер, выполняется аспирационная проба. В начале токсического действия, как правило, возникает головокружение, звон в ушах, покалывание вокруг рта; все это сопровождается чувством беспокойства или «страха смерти», появляются тремор, судороги, затем кома и, наконец, остановка дыхания и сердечной деятельности. Очень важно распознать ранние симптомы данного осложнения и прекратить дальнейшее введение местного анестетика. Лечение должно начинаться своевременно, с использованием при необходимости седативных препаратов и антиконвульсантов (тиопентал натрия, диазепам), и, если требуется, проведением СЛР.
Полный спинальный блок - это достаточно редкое осложнение, возникающее при попадании иглы или катетера по неведению анестезиолога в субарахноидальное пространство и введении 10 – 20 мл анестетика. У пациента возникает тяжелая гипотония, апноэ, как результат действия местного анестетика на головной мозг - потеря сознания и мидриаз. При использовании метода введения тест-дозы можно предупредить развитие полного спинального блока. Но были описаны случаи, где после контроля за действием тест-дозы повторно вводимые болюсы вызывали полный спинальный блок. Их связывали с миграцией катетера в субарахноидальное пространство, однако это не было доказано.
Лечение полного спинального блока
- Обеспечьте проходимость дыхательных путей и дайте кислород.
- Вентилируйте больного маской и интубируйте
- Контролируйте гемодинамику в/венным введением жидкости и вазопрессорами, например, эфедрином по 3-6 мг или, при необходимости, адреналином по 0,5-1 мг
- Продолжайте ИВЛ до полного регресса блока (2-4 часа)
- При регрессе блока к пациенту возвращается сознание, появляется спонтанное дыхание, движения рук и, в последнюю очередь, ног. В случае необходимости дальнейшей вентиляции у пациента с восстановившимся сознанием назначьте седативные препараты (диазепам по 5-10 мг в/в)
Прокол твердой мозговой оболочки
Случайный прокол твердой мозговой оболочки диагностируется при вытекании ликвора из эпидуральной иглы. Наиболее часто возникает у молодых и обучающихся анестезиологов. Прокол обуславливает возникновение вскоре характерной головной боли, которая может быть тягостной для пациента. Для нее характерна типичная лобная локализация, боль усиливается при движении и принятии вертикального положения, сопровождается светобоязнью, тошнотой и рвотой и уменьшается в положении лежа. Наиболее часто возникает у молодых пациентов и у беременных. Считается, что боль обусловлена истечением ликвора через дефект в твердой мозговой оболочке. Консервативные мероприятия направленные на лечение возникающей головной боли включают постельный режим, назначение жидкости, анальгетиков и кофеина. Если они не приводят к успеху, что бывает крайне редко, используется пломбирование эпидурального пространства аутокровью. Данная процедура эффективна у 90% пациентов. При сохранении головной боли после первой процедуры может быть выполнено повторное пломбирование, которое купирует боль в 96% оставшихся случаев. Кровь, вводимая в эпидуральное пространство, как считают, образует своеобразную пробку в дефекте твердой мозговой оболочки.
Процедура эпидурального пломбирования аутокровью
Показания:
- Установленный диагноз постпункционной головной боли.
- Боль сильная, причиняющая значительный дискомфорт пациенту.
- Не купируется в течение 2-3 дней консервативного лечения.
Противопоказания
- Необъяснимые неврологические симптомы.
- Активный неврологический процесс
- Воспаление в зоне пункции.
- Сепсис
- Коагулопатия
Техника процедуры
- Получите у пациента информированное согласие после подробного рассказа о технике процедуры, потенциальной опасности и ожидаемых результатах
- Проводится в операционной
- Анестезиолог и ассистент, соблюдая требования асептики и антисептики, облачаются в стерильное операционное белье.
- Положение пациента на боку либо сидя.
- Анестезиолог обрабатывает место укола, накрывает его стерильным бельем и выполняет пункцию эпидурального пространства на том же самом, что и предыдущая, уровне или на один промежуток ниже.
- Ассистент одновременно, с соблюдением правил асептики и антисептики, пунктирует вену, забирает 20 мл крови и передает шприц анестезиологу.
- Анестезиолог вводит кровь в эпидуральное пространство до появления у пациента тяжести в ягодицах или пояснице, или, если этого не происходит, то весь объем.
- Оставшуюся кровь отправляют в лабораторию для бактериологического исследования и определения чувствительности к антибиотикам.
- В течение 1 часа пациент лежит на спине под наблюдением медсестры.
Эпидуральная гематома – это редкое, но потенциально опасное осложнение эпидуральной анестезии. Эпидуральное пространство содержит богатую сеть венозных сплетений. Прокол этих вен с истечением крови в ограниченное эпидуральное пространство может привести к быстрому образованию гематомы и сдавлению спинного мозга, что может иметь катастрофические последствия, вплоть до развития параплегии. По этой причине коагулопатия или антикоагулянтная терапия с применением гепарина или пероральных антикоагулянтов должны быть абсолютными противопоказаниями для проведения эпидуральной блокады.
Инфекция – это другое редкое, но также потенциально опасное осложнение. Патогенные микроорганизмы попадают в эпидуральное пространство при несоблюдении правил асептики во время выполнения эпидуральной блокады. Чаще всего это St. aureus и Str. Были описаны случаи возникновения не только эпидуральных абсцессов, но и менингита. В дополнении к признакам компрессии спинного мозга у пациентов наблюдается лихорадка и изменения белой крови. При диагностике данного осложнения должно быть выполнено как можно более раннее вскрытие абсцесса.
Неудачи при выполнении эпидуральной блокады могут быть следствием многих причин. Наиболее частая из них – отсутствие необходимого опыта у анестезиолога. Ложная потеря сопротивления может привести к введению катетера не в эпидуральное пространство и невозможности сформировать адекватную блокаду. Мозаичность блока возникает по причинам, неясным до сих пор. Предполагают, что существуют определенные анатомические изменения, препятствующие распространению анестетика в эпидуральном пространстве равномерно. Как следствие, некоторые корешки остаются вне зоны действия анестетика, а соответствующие им дерматомы не обезболиваются. Иногда может возникнуть односторонняя блокада. Это возможно при наличии перемычки (перегородки) в эпидуральном пространстве и распространении анестетика по одной из его половин. Позиционирование пациента на неблокированном боку способствует «стеканию» анестетика и формированию полноценного двухстороннего блока.
Литература:
Sharrock NE, Haas SB, Hargett MJ et al. Effects of epidural analgesia on the incidence of deep vein thrombosis after total knee arthroplasty. Journal of Bone and Joint Surgery American Volume 1991;73:502-6.
- Dalldorf PG, Perkins FM, Totterman S, Pellegrini VD. Deep venous thrombosis following total hip arthroplasty. Effects of prolonged postoperative epidural analgesia. Journal of Arthroplasty 1994;9:611-6.
- Perler BA, Christopherson R, Rosenfeld BA et al. The influence of anaesthetic method on infrainguinal bypass graft patency: a closer look. American Journal of Surgery 1995;61:784-9.
- Bach S, Noreng MF, Tjellden NU. Phantom limb pain in amputees during the first 12 months following limb amputation, after preoperative lumbar epidural blockade. Pain 1988;33:297-301.
- Yeager MP, Glass DD, Neff RK, Brinck-Johnsen T. Epidural anaesthesia and analgesia in high-risk surgical patients. Anesthesiology 1987;66:729-36.
- Bromage PR. Continuous Epidural Analgesia. In "Epidural Analgesia" Bromage PR (ed) W.B. Saunders 1978 p. 237-8.
- Mulroy MF. Epidural opioid delivery methods: bolus, continuous infusion, and patient-controlled epidural analgesia. Regional Anaesthesia 1996;21:100-4.
- Ngan Kee WD. Epidural pethidine: pharmacology and clinical experience. Anaesthesia and Intensive Care 1998;26:247-55.
- Horlocker TT, Wedel DJ. Spinal and epidural blockade and perioperative low molecular weight heparin: smooth sailing on the Titanic (editorial). Anesthesia and Analgesia 1998;86:1153-6.
- Rodgers A, Walker N, Schug S et al. Reduction of postoperative mortality and morbidity with epidural or spinal anaesthesia: results from overview of randomised trials. British Medical Journal 2000;321:1493-7