И доречевой тугоухости
| Вид материала | Автореферат диссертации |
- Санитарные правила и нормы СанПиН 2 570-96, 1345.17kb.
Общая характеристика обследованных групп. Дети с неотягощенным семейным анамнезом были зарегистрированы в 69% случаев (1289/1863). Отягощенный семейный анамнез отмечался в 31% случаев (574/1863), включая 11,8% детей, имеющих слышащих родителей и тугоухих родственников 1 и 2 степени родства (219/1863). В ходе первичной обработки материала были выявлены 87 сибсов из 82 семей. Дети со слышащими родителями составили 80,9% (1508/1863). В 3,9% случаев (73/1863) потерей слуха страдал один из родителей. Оба родителя с нарушением слуха имели место в 15,1% (282/1863).
Согласно результатам исследования в первом контингенте двусторонней НСТ разной степени тяжести страдали 60,6% человек (403/665), глухотой - 15,8% (105/665), смешанной тугоухостью – 2,1% (14/665), односторонней тугоухостью/глухотой – 20,6% (137/665) человек. Среди обследованной группы кондуктивная тугоухость отмечалась только у 6 детей (0,9%).
В контингенте, прошедшем ДНК-диагностику, двусторонней НСТ разной степени тяжести страдали 86,45% человек (351/406), глухотой - 11,58% (47/406), смешанной тугоухостью - 0,98% (4/406), односторонней глухотой - 0,74% (3/406), односторонней тугоухостью - 0,25% (1/406) человек. Среди обследованной группы кондуктивной тугоухости не было ни у одного из пациентов. Неотягощенный семейный анамнез по нарушению слуха среди всех тестированных был выявлен у 57,1% детей (232/406). Отягощенные по тугоухости семьи составили 42,9% (174/406). Дети со слышащими родителями отмечались в 80,3% (326/406), а с тугоухими родителями - в 19,7% (80/406).
В результате проведенного анкетирования родителей была изучена структура 279 ядерных семей. Семьи I типа составили 179 семей (64%), II тип семьи имел место в 15 семьях (5%), к III типу относились 85 семей (31%). Число детей в ядерной семье во всех типах семей варьировало от 1 до 4. Общее число семей с одним и двумя детьми приближалось к 91%. При первом типе преобладали семьи с двумя детьми (54,2%), среди них число семей с первым глухими ребенком оказалось в 2 раза меньше числа семей с первым слышащим ребенком. Рождение глухого ребенка могло влиять на планы рождения второго.
Потребность в медико-генетическом консультировании подчеркнули только 35% опрошенных семей, в том числе 13% нуждались в ретроспективном и 22% в проспективном консультировании. Отрицательный ответ на вопрос о необходимости консультации генетика для семьи был получен в 55%.
В результате анализа происхождения проживающих в Санкт-Петербурге детей оказалось, что бабушек и дедушек родом из Санкт-Петербурга было всего 20,9%, по сравнению с 44,7% родителей детей. Только 8,6% бабушек и дедушек и 17,1% родителей родились в Ленинградской области. Следовательно, большинство семей происходят из других краев и областей, а знание места рождения ребенка и его родителей недостаточно для установления происхождения семьи.
Распространенность врожденной и доречевой стойкой тугоухости. В результате проведенного анализа распространенность врожденной и доречевой стойкой тугоухости у детей в возрасте от 0 до 16 лет в Санкт-Петербурге в 1994 г. составила 38 на 100 тысяч населения, включая 31 случай со слышащими родителями и 7 с тугоухими/глухими родителями. Распространенность несиндромальных форм среди врожденной и стойкой детской тугоухости составила 35 на 100 тысяч населения, синдромальные формы только 3 на 100 тысяч населения.
Таким образом, общее число случаев врожденной и доречевой тугоухости в значительной степени складывалось из нарушений слуха у детей со слышащими родителями и из несиндромальных форм, что согласуется с данными других исследований.
Наиболее распространенными этиологическими факторами врожденной и доречевой стойкой тугоухости среди детей в возрасте от 0 до 16 лет в Санкт-Петербурге на 1994 г.являлись наследственность, которая составила 7,2 случая на 100 тысяч населения, патология беременности и родов - 4,6 на 100 тысяч населения, тяжелые инфекции - 4 на 100 тысяч населения. Менингиты являлись причиной детской тугоухости в 1,8 случаях на 100 тысяч населения. В большом числе случаев этиология тугоухости оставалась неясна (15,3 на 100 тысяч населения), то есть медицинская документация не содержала никаких данных на этот счет.
Согласно поставленным задачам рассчитана частота врожденной и детской тугоухости среди новорожденных. Этот показатель определен для детей, рожденных в г. Санкт-Петербурге в период с 1980 по 1982 гг., и составил 3,4 на 1000 новорожденных. Двусторонняя нейросенсорная тугоухость/глухота была зарегистрирована в 2,6 случаях на 1000 новорожденных, включая двустороннюю тяжелую НСТ (IV степень) и глухоту - 0,8 на 1000, случаи среднетяжелой НСТ (III, III-IV степень) - 0,6 на 1000, случаи средней потери слуха (II и II-III степень) - 0,6 на 1000. Число случаев легкой двусторонней НСТ (I степень) составило 0,6 на 1000 новорожденных, а односторонняя нейросенсорная тугоухость/глухота - 0,7 на 1000. Редкие случаи асимметрии поражения органа слуха (НСТ I степени на одно ухо и глухота на другое) и стойкой кондуктивной или смешанной тугоухости вместе составили 0,1 на 1000 новорожденных. Таким образом, показатель значимых нарушений слуха (глухота, тугоухость тяжелой, среднетяжелой и средней степени) был равен 2 ребенка на 1000 новорожденных. К 10 годам на 10 тысяч новорожденных 6 детей страдали легкой формой тугоухости, которая также может отразиться на развитии ребенка.
Синдромальные нарушения слуха. В результате скрининга медицинской документации Городского детского сурдологического центра в 1994 г. зарегистрировано только 7,1% (132/1863) синдромальных форм тугоухости. В целом насчитывалось около 50 нозологических форм, зафиксированных врачом сурдологом как результат консультации генетика. Во втором контингенте в процессе совместного консультирования детского сурдолога и врача генетика выявлено 40 синдромов у 18% детей (103/573). В большинстве случаев диагноз был установлен впервые. Среди лиц, участвовавших в ДНК-диагностике, синдромальные формы тугоухости составили 7,9% (32/406).
Средний возраст первичной диагностики тугоухости при синдромальных формах в обоих контингентах составил 24 мес. Таким образом, почти все зарегистрированные синдромальные нарушения слуха имели врожденный характер.
Выявлены различия изученных контингентов по характеру тугоухости при синдромальных формах. По данным городского детского сурдоцентра среди синдромов зарегистрированы 81,1% (107/132) случаев с двусторонней НСТ и 8,3% (11/132) случаев глухоты (соотношение 10 к 1). Кондуктивная тугоухость не превышала 1%, смешанная тугоухость отмечена в 7,6% (10/132) случаев, односторонняя тугоухость – 3%.
При личном консультировании получена более разнообразная картина. Двусторонняя НСТ/глухота отмечались в 58,2% (54 и 6 случаев соответственно, 9:1). Кондуктивная тугоухость составила почти 12% (12/103), смешанная тугоухость 23,3% (24/103), односторонняя тугоухость 6,8%. Низкий уровень стойкой кондуктивной тугоухости в первом контингенте предположительно связан с тем, что такие дети не ставятся на диспансерный учет, не направляются или не обращаются в детский сурдоцентр.
Согласно полученным данным наиболее часто в практике врача сурдолога встречались синдромы лицевых дизморфий с пороками развития наружного, среднего и внутреннего уха (в сумме 13%, включая синдром Тричера Коллинза), врожденные пороки развития наружного уха без лицевых дизморфий (11,4%, включая синдром микротии-атрезии), врожденные расщелины твердого и мягкого неба (9%). Частота синдрома Ваарденбурга I типа среди других синдромальных нарушений слуха составила 11,4%, синдрома Ушера - 9%, синдрома Тричера Коллинза – 5%. Синдромы Пендреда, Альпорта, Стиклера, бранхио-ото-ренальный, Норри по полученным данным в общей структуре синдромов встречаются редко (не более 2,5%). В первом контингенте не встретилось ни одного диагноза распространенных синдромов Альпорта, Пендреда, Стиклера, бранхио-ото-ренального синдрома и ряда других, хотя при консультировании детей, включая тех, кто состоит на учете в сурдоцентре, эти синдромы были установлены.
Клинический диагноз синдрома Ваарденбурга I типа на молекулярном уровне подтвердился в 5 из восьми семей, участвовавших в поиске мутаций в РАХ3 гене. Из трех семей с признаками бранхио-ото-ренального синдрома только в одной была обнаружена мутация в гене EYA1.
В ходе анализа медицинской документации в 5% (94/1863) случаев имело место наличие сопутствующей патологии других органов, умственной отсталости, эписиндрома. Поскольку ряд симптомов характерен для некоторых моногенных синдромов, хромосомных нарушений и митохондриальных болезней, то можно предположить, что в первом контингенте присутствовали неустановленные синдромы.
Согласно нашим данным 60% синдромальных форм обладают наследственной этиологией. В 19% случаев этиология осталась неясна. 10% составили множественные врожденные пороки развития, которым часто предшествовала патология беременности и родов, применение тератогенных средств во время беременности, многократные оперативные вмешательства с приемом ототоксических средств. Исключительно приобретенный характер тугоухости (краснуха, цитомегаловирус) отмечался в 5% случаев.
Таким образом, наибольший процент синдромов (18%, 103/573) был получен только в контингенте лично обследованных детей. Зарубежная литература указывает, что синдромальные формы тугоухости в общей массе врожденной тугоухости составляют от 15% до 30%. В проведенном исследовании даже при целенаправленном обращении к врачу генетику число детей с синдромальными нарушениями слуха не превышало 20%.
Причинами таких низких цифр могло быть следующее: а) ряд синдромов оставались нераспознанными; б) некоторые синдромы имели более позднее начало или сопровождались легкими нарушениями слуха в детстве, поэтому дети не попадали в сурдоцентр; в) избирательный подход при направлении пациентов на консультацию к генетику; г) некоторые синдромы на практике встречались очень редко. Возможность распознать синдром является отправной точкой в правильном прогнозе потомства и профилактике тугоухости.
Таким образом, улучшить диагностику синдромальных нарушений слуха могла бы организация обязательного направления всех детей со стойким нарушением слуха невоспалительного характера к врачу генетику с концентрацией общей отчетности или базы данных по наследственной патологии у генетика городского сурдоцентра.
Несиндромальные нарушения слуха. Несиндромальные нарушения слуха в первом контингенте составили 93% (1731/1863 в общей группе или 620/665 в группе детей рожденных в 1980-1982 гг.), во втором контингенте – 82% (470/573). Среди лиц, прошедших ДНК-диагностику, несиндромальные формы имели место в 92,1% (374/406).
Нарушение слуха в исследованных контингентах в основном было представлено двусторонней НСТ. В первом контингенте она составила 75,8% (470/620), в том числе 15,6% (97/620) глухих детей. Среди лично обследованных детей двусторонняя НСТ охватывала 85,7% (403/470) детей, глухота 10% (47/470). В группе прошедшей ДНК-диагностику двустороннюю тугоухость имели 87,4% (327/374) детей и глухоту 11,8% (44/374). Данная группа отличалась значительным преобладанием тяжелой потери слуха. Двусторонняя НСТ IV степени составила 34% (127/374), НСТ III-IV - 23% (86/374). В первом контингенте эти степени тяжести не превышали 20%: двусторонняя НСТ IV степени 8,5% (53/620) и НСТ III-IV степени 9% (56/620).
Среднетяжелые потери слуха, НСТ III степени, в первом контингенте составили 7,4% (46/620). Двусторонняя НСТ II-III степени только в 4% (25/620). Средняя степень тяжести, НСТ II степени, отмечена в 5,2% (32/620) случаев, двусторонняя НСТ I-II степени в 7,1% (44/620). Второй контингент отличался отсутствием НСТ I-II, а среднетяжелых потерь слуха было в два раза больше. Двусторонняя НСТ III степени составила 18,2%. Двусторонняя НСТ II-III степени, как и в первом контингенте, не превышала 3,5% (13/374).
В первом контингенте были значительно представлены легкие потери слуха. Двусторонняя НСТ I степени 15,5% (96/620). Односторонняя НСТ и односторонняя глухота 21,6% (134/620). Во втором контингенте легкие потери слуха, включая односторонние нарушения, не превышали 2,5% (9/374).
Первый контингент также отличался наличием таких форм тугоухости как смешанная и кондуктивная в 2,6% случаев (16/620). Во втором контингенте в группе несиндромальной тугоухости этих нарушений слуха не было.
Таким образом, первый контингент отражал широкий спектр нарушений слуха, существующий на практике. Преобладание во втором контингенте тяжелых нарушений слуха соответствовало задачам поиска мутационных изменений в гене Сх26.
Средний возраст первичной диагностики двусторонней несиндромальной тугоухости в первом контингенте в целом был равен 3,3 года (40 мес.). Для второго контингента этот показатель не превышал 1,9 года (23 мес.). Средний возраст первичной диагностики изменялся в зависимости от степени тяжести нарушений. Так для двусторонней глухоты этот показатель составил 1,4 года (16,8 мес.) в первом и 1,1 года (13,2 мес.) во втором контингенте.
Изучение семейного анамнеза и анамнеза заболевания при несиндромальных формах приобретает особое значение, поскольку нет дополнительных клинических признаков, позволяющих поставить диагноз и определить причину тугоухости. В первом контингенте наличие тугоухих родственников отмечалось в 31,5% семей (545/1731), во втором в 45,3% (213/470). В группе с неотягощенным семейным анамнезом случаи с приобретенными факторами риска в анамнезе заболевания были зарегистрированы в 27,5% (477/1731) в первом контингенте и в 34,7%(163/470) во втором. Подгруппа с неотягощенным анамнезом заболевания в первом контингенте составила 41% (709/1731), а во втором - 20% (94/470). В 36% медицинских карт сурдоцентра анамнез заболевания отсутствовал или содержал краткое описание нормального развития ребенка.
Анализ структуры семей, имеющих одного и более тугоухих родственников показал, что доля семей IБ типа во втором контингенте составила 35,2% (75/213) против 21% (115/545) в первом. Эти данные косвенно могут указывать на недостаточность семейного анамнеза, собираемого сурдологом. При целенаправленном выяснении семейного анамнеза, составлении родословной генетик получает более точные сведения о других родственниках. Отягощенный семейный анамнез во втором контингенте преобладал именно за счет этой подгруппы семей. Доля семей III типа (ассортативные браки) в контингенте лиц, проконсультированных генетиком, была значительно меньше, 31,5% (67/213) против 50,8% (277/545) в первом контингенте, что могло говорить о низкой заинтересованности тугоухих родителей в консультации генетика.
Молекулярно-генетическое исследование несиндромальных форм тугоухости. По результатам ДНК-диагностики гена Сх26 нами выделены три группы пациентов (рис. 2). Группа гомозигот по мутации 35delG, генотип ∆/∆, составила 39% (146/374). Гетерозиготы по мутации 35delG, генотип ∆/N, обнаружены в 14% (51/374). Установлено 23 случая с биаллельным наследованием мутаций гена Сх26 и 1 случай дигенного наследования мутации 35delG гена Сх26 и крупной делеции гена Сх30. Группа пациентов с негативным генотипом по делеции, генотип N/N, составила 47% (177/374). В дальнейшем группы анализировались по общей схеме.
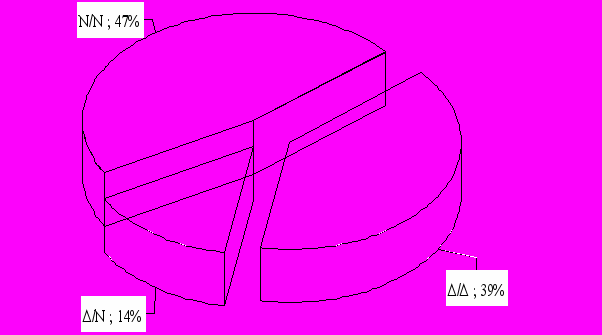
Рисунок 2. Доля наследственной тугоухости при несиндромальной тугоухости.
В результате исследования диагноз наследственной тугоухости был установлен в 53% (197/374) случаев несиндромальной НСТ, что соответствует доле генотипов ∆/∆ и ∆/N. В общей группе за счет присутствия синдромальных форм, в которых делеция не была обнаружена, измененные генотипы встретились в 48,5% (197/406).
Полученные результаты подтвердили аутосомно-рецессивный тип наследования тугоухости для семей, в которых были обнаружены мутации в гене Сх26. Высокая частота мутации 35delG оказалась в группе пробандов, проживающих в Санкт-Петербурге и в Ярославской области. Она составила 60,4% и 57,9% соответственно, что превышало данный показатель в обследованной группе в целом. Скорее всего, это было связано с высоким уровнем отягощенных по тугоухости семей в этих группах (почти 50%). В группе пробандов, проживающих в Ленинградской области, низкая частота мутации, только 29,2% соответствовала небольшой доле семей с отягощенной родословной (31%).
Согласно полученным данным среди всех обнаруженных и предполагаемых мутаций в гене Сх26 мутация 35delG составила 87% (343 на 394 хромосомы), частота мутации 310del14 - 2% (8 из 394 хромосомы), а мутации 235delC обнаружена в 0,5% измененных хромосом (2 из 394).
Скрининг крупной делеции 342-kb в гене Сх30 показал наличие ее только у одного ребенка, который был также гетерозиготой по мутации 35delG в гене Сх26. Таким образом, был выявлен случай дигенного наследования, то есть участия изменений двух генов в патогенезе тугоухости. Распространенность крупной делеции гена Сх30 составила 1% (1/95).
Мутация A1555G в гене 12S р-РНК митохондриальной ДНК была найдена в 3% (4/120), причем один ребенок был гомозиготой по делеции 35delG.
Как показали результаты исследования, в анамнезе детей с измененным генотипом отмечались следующие экзогенные факторы: патология беременности и родов (тяжелое течение, эклампсия, асфиксия и родовая травма), заболевания до 3-х лет, в том числе детские инфекции (грипп, скарлатина, ветряная оспа), пневмония, применение ототоксических антибиотиков не более одного курса.
Мутация не была обнаружена в тех случаях, когда экзогенные причины тугоухости строго соответствовали перечню приказа МЗ и МП РФ №108 от 29.03.1996. Сюда относились дети, перенесшие краснуху во время беременности матери, рожденные с весом до 1500 гр., перенесшие тяжелый резус-конфликт с гипербиллирубинэмией и обменным переливанием крови, гнойный менингит и менингоэнцефалит, органическое поражение головного мозга. В этих случаях выполнение генетического анализа рекомендуется для исключения случайных совпадений.
Результаты исследования подтвердили возможность наследственной патологии в семье слышащих родителей, когда первый ребенок здоров. Так, из 81 семьи с первым слышащими ребенком у 51% (41/81) пробандов обнаружена мутация 35delG. В группе семей с двумя глухими детьми у слышащих родителей мутация также обнаружена в половине случаев (9/18). Мутация 35delG идентифицирована в 45% семей I типа в целом (137/302), так же как и среди семей со слышащими родителями, имеющими двух детей, один из которых имеет нарушение слуха (63/140). Таким семьям до рождения первого ребенка в настоящее время возможно оказание необходимой консультативной помощи. Принимая во внимание, что современная семья ограничивается рождением одного или двух детей, то точный прогноз важен именно для первого ребенка.
Общая этиологическая структура врожденной и доречевой несиндромальной НСТ и глухоты. В соответствии с поставленной задачей изучения общей этиологической картины врожденной и доречевой несиндромальной НСТ сравнивали заключения о причине тугоухости, сделанные нами до проведения ДНК-диагностики с учетом мнения сурдологов и заключения по результатам тестирования.
После проведения ДНК-диагностики группа наследственной тугоухости составила 52,1%, а предположительно наследственные формы - 8,8%. Таким образом, наследственные формы тугоухости охватили 61% всех случаев врожденной и доречевой тугоухости/глухоты в обследованном контингенте. До ДНК-диагностики наследственные формы в этой группе были установлены лишь у 13,1%, хотя предположительно наследственный характер имели еще 16,6%.
В результате скрининга гена Сх26 на мутацию 35delG почти половина случаев тугоухости неясной этиологии и более половины случаев, ранее считавшихся приобретенными, оказались в группе наследственных нарушений слуха. До тестирования подгруппа неясной этиологии составляла 25,9%. После тестирования размеры данной подгруппы уменьшились до 13,4% (рис.3). Согласно полученным данным до ДНК-диагностики подгруппа тяжелых инфекций в среднем составляла 8,8%, включая 2,9% случаев после менингита, 3,2% случаев после пневмонии и 2,7% случаев после тяжелого течения других инфекций. После ДНК-диагностики размеры данной подгруппы уменьшились только на 1,3%. Это связано с тем, что в подгруппе нарушений слуха, связываемых с перенесенной пневмонией, были обнаружены мутации в гене Сх26. Подгруппа тугоухости вследствие перенесенного менингита не изменилась, что говорит о том, что данный фактор риска является одной из значимых приобретенных причин тугоухости. Тяжелое течение других инфекций также является значимым фактором риска, хотя не исключено, что потеря слуха при этом может быть связана с длительными курсами ототоксических препаратов.
Рисунок 3. Этиологическая структура врожденной и доречевой несиндромальной НСТ и глухоты по результатам ДНК-диагностики (n=374).
После ДНК-диагностики подгруппа патологии беременности и родов уменьшилась с 23,3% до 12,8%. Подгруппы с такими факторами риска как врожденные инфекции, недоношенность и гемолитическая болезнь новорожденных с обменным переливанием крови мало изменились. Иначе обстояло дело с патологией беременности и родов, которая не входит в перечень приобретенных факторов риска приказа МЗ и МП РФ №108 от 29.03.1996. Значительно изменились подгруппы с такими факторами риска в анамнезе, как родовая травма (от 2,4% до 0,3%), асфиксия в родах (от 2,1% до 0,5%), другая патология (анемия, гипертония, пиелонефрит, преэклампсия, тяжелые роды).

Рисунок 4. Спектр факторов, считавшихся причиной тугоухости, до проведения ДНК-диагностики в группе детей с измененным генотипом (генотипы ∆/∆ и ∆/N, n=197) и в группе, в которой мутация не обнаружена (генотип N/N, n=177).
Подгруппа причин, связанных с заболеваниями ребенка в первые годы жизни (отиты, грипп, детские инфекции) после ДНК-диагностики уменьшилась в 3 раза. Размеры подгруппы детей с другими факторами (черепно-мозговая травма, поражение ЦНС, реакция на прививки) изначально были очень малы, поскольку практически не участвовали в генетическом тестировании. В ряде случаев могло быть совпадение этих причин с тяжелым течением беременности, родов или инфекционных заболеваний, которые рассматривались как первичная причина.
В результате работы был определен спектр этиологических факторов, которые до проведения ДНК-диагностики считались причиной тугоухости в группе с мутацией 35delG в гене Сх26 (рис. 4). В качестве группы сравнения выступили дети, у которых данная мутация не была обнаружена. Обе группы отличались наличием в анамнезе патологии беременности и родов, 19,8% в группе с мутацией 35delG и 27,1% при негативном генотипе. При измененном генотипе в анамнезе заболевания в 2% случаях зарегистрировалась недоношенность (12% в контрольной группе), также в 2% отмечалась гемолитическая болезнь новорожденных (5% в контрольной группе). При детальном анализе выявлено, что анемия, гипертония беременных, родовая травма, асфиксия в родах чаще присутствовали в анамнезах детей с мутациями в гене Сх26. В группе с измененным генотипом заболевания первых лет жизни в 11,7% случае рассматривались в качестве причины тугоухости. В группе с негативным генотипом - только в 5,6% случаев. В группе с мутацией 35delG тяжелые инфекции в анамнезе отмечены только в 2,5%. При негативном генотипе размер данной подгруппы составил 15,8%. В группе детей с измененным генотипом полностью отсутствовала подгруппа с потерей слуха после перенесенного менингита. Тяжелое течение инфекций имело место только в 0,5%. Без проведения генетического анализа тугоухость в этих случаях могла считаться приобретенной, хотя в действительности являлась наследственной. Среди гомозигот и гетерозигот по делеции до проведения тестирования подгруппа неясной этиологии составила 23,9%.
Генетическая характеристика группы с неотягощенным семейным анамнезом (IА тип семьи). Эта группа семей при несиндромальных формах тугоухости составила 57% (213/374). Подгруппа детей с экзогенными факторами риска в анамнезе составила 33% (123/374). Тяжелые инфекции 7,2% (27/374), тяжелой патологией беременности и родов 17,1% (64/374), другие заболевания ребенка в первые годы жизни 23% 7,8% (29/374). Вторая подгруппа детей с неотягощенным анамнезом заболевания составила 24,1% (90/374), в этой подгруппе этиология тугоухости считалась неясной.
Согласно полученным данным частота мутации 35delG в этой группе составила 44% (93/213). В подгруппе детей с экзогенными факторами в анамнезе, которые сурдологами считались причиной тугоухости, встречаемость мутации составила 40% (49/123). Только гомозиготы по делеции составили 32% (39/123) (табл. 1). Случаи с первично наследственной причиной тугоухости до проведения ДНК-диагностики рассматривались сурдологами как приобретенные.
Самым важным представляется тот факт, что в подгруппе детей с неотягощенным анамнезом заболевания или неясной этиологией тугоухости мутация 35delG обнаружена в 49% (44/90). Такой высокий процент является дополнительным аргументом в пользу необходимости диагностики мутации в обследованном регионе среди тугоухих детей, имеющих слышащих родителей.
Таблица 1.
Распределение мутации 35delG в гене Сх26 в группе пробандов с неотягощенным семейным анамнезом (n=213).
| группа | Семьи IА типа | |||||
| Экзогенные факторы | Неотягощенный анамнез | всего | ||||
| n | % | n | % | n | % | |
| ∆/∆ | 39 | 32% | 32 | 36% | 71 | 33% |
| ∆/N | 10 | 8% | 12 | 13% | 22 | 11% |
| N/N | 74 | 60% | 46 | 51% | 120 | 56% |
| Всего | 123 | 100% | 90 | 100% | 213 | 100% |
Самый высокий процент мутации в неотягощенных семьях был обнаружен в подгруппе детей, проживающих в Ярославской области (50%), самый низкий - у детей из Ленинградской области (27,3%).
Если до проведения генетического тестирования в группе с неотягощенным анамнезом заболевания преобладала подгруппа, в которой причина была неясна, 42% (90/213), то после тестирования это место заняли наследственные причины, 44% (93/213), которые без проведения ДНК-диагностики полностью отсутствовали (рис. 5). Первоначально второе место занимала подгруппа патологии беременности и родов, 30% (64/213). После тестирования мутации 35delG она уменьшилась на 19%, немного уступив группе с неясной этиологией, которая в свою очередь уменьшилась наполовину (рис.6).

0%
0%
30%
13%
14%
1%
42%
Рисунок 5. Этиологическая структура несиндромальной тугоухости у детей из семей IA типа до проведения ДНК-диагностики (n=213).

44%
19%
11%
4%
1%
21%
Рисунок 6. Этиологическая структура несиндромальной тугоухости у детей из семей IA типа после проведения ДНК-диагностики (n=213).
Таким образом, в группе с неотягощенным семейным анамнезом без ДНК-диагностики наследственный характер можно было предполагать только теоретически, клинических доказательств в конкретной семье не было. Функцию точной генетической диагностики смогли выполнить только молекулярно-генетические анализы.
Генетическая характеристика группы с отягощенным семейным анамнезом. Группа детей, имеющих родственников с нарушением слуха составила 43% (161/374). Среди них был получен особенно высокий процент встречаемости мутации 35delG - 65% (104/161) (табл. 2). Семьи со слышащими родителями (IБ тип семьи) составили 23,7% (89/374), семьи с нарушением слуха только у сибсов - 5,6% (21/374), с тугоухими родственниками 2-3 степени родства - 16% (60/374), с нарушением слуха у сибсов и других родственников - 2,1% (8/374). Только один из родителей имел снижение слуха в 4,5% (17/374). Оба родителя страдали тугоухостью в 14,7% (55/374).
Высокая частота делеции 49% (44/89) отмечалась в подгруппе детей со слышащими родителями из семей IБ типа. В этой подгруппе число гомозигот по мутации почти в 4 раза превышало число гетерозигот по мутации.
Таблица 2.
Распределение мутации 35delG в гене Сх26 в группе пробандов
с отягощенным семейным анамнезом (n=161).
| группа | Отягощенный семейный анамнез | |||||||
| IБ тип семьи | II тип семьи | III тип семьи | всего | |||||
| n | % | n | % | n | % | n | % | |
| ∆/∆ | 35 | 39% | 3 | 18% | 37 | 67% | 75 | 47% |
| ∆/N | 9 | 10% | 4 | 23% | 16 | 29% | 29 | 18% |
| N/N | 45 | 51% | 10 | 59% | 2 | 4% | 57 | 35% |
| Всего | 89 | 100% | 17 | 100% | 55 | 100% | 161 | 100% |
В семьях III типа мутация 35delG в гомозиготном состоянии обнаружена у 67% (37/55), а в гетерозиготном состоянии у 29% (16/55). Таким образом, встречаемость мутации в этой подгруппе составила 96%. Эти данные свидетельствовали, что в изученной выборке нарушение слуха у детей из семей III типа связано практически только с мутацией 35delG в гене Сх26, исключение составили два случая (2/55).
В подгруппе детей с одним тугоухим родителем из семей II типа мутация была выявлена в 41% (7/17). В этих семьях благодаря ДНК-диагностике подтвержден аутосомно-рецессивный тип наследования. До проведения молекулярного анализа тугоухость в этих семьях рассматривалась как аутосомно-доминантная.
Результаты исследования показали, что соотношение числа гомозигот и гетерозигот по мутации мало отличалось в группах с отягощенным и неотягощенным семейным анамнезом (3:1 и 2,6:1 соответственно). Но при отягощенной по нарушению слуха родословной это соотношение меняется в зависимости от типа семьи. Для семей IБ типа отношение числа гомозигот и гетерозигот равно 4:1, при III типе - 2:1, при II типе – 0,8:1.
В подгруппе детей, проживающих в г. Санкт-Петербурге, уровень мутации достиг 76,3%. В Ярославской области частота мутации при отягощенном семейном анамнезе была равна 66,7%. Во всех подгруппах, отличающихся по месту проживания, частота мутации также оказалась значительно выше, чем в неотягощенных семьях. Исключение составили пробанды, проживающие в Ленинградской области и в г.Ярославле, где мутация 35delG обнаружена у 33,3% и 45,5% детей соответственно.
Генетическая структура семей со слышащими родителями без учета семейного анамнеза отличалась наличием измененного генотипа в 45% случаев (137/302). Каждая вторая семейная пара имела риск по наследственной тугоухости. Семьи с тугоухими родителями (типы II и III) имели измененный генотип в 83% (60/72).
Полученные результаты подтвердили, что возможна встреча в родительской паре лица со снижением слуха, обладателя двух разных рецессивных мутаций одного гена, и здорового лица, гетерозиготного носителя одной из этих мутаций. Тип наследования в такой семье клинически мог быть расценен как аутосомно-доминантный. В этом смысле ориентировка на тип наследования могла помешать точной генетической диагностике.

0%
75%
15%
4%
2%
4%
Рисунок 7. Этиологическая структура несиндромальной тугоухости при отягощенной родословной до проведения ДНК-диагностики (n=161).

65%
25%
6%
4%
2%
Рисунок 8. Этиологическая структура несиндромальной тугоухости при отягощенной родословной после проведения ДНК-диагностики (n=161).
Если бы отбирались только семьи с аутосомно-рецессивным типом наследования, то в данных семьях анализ гена Сх26 был бы не проведен. Интересно, что риск наследования тугоухости для такой пары равен 50%, то есть рекуррентный риск соответствует таковому при аутосомно-доминантном заболевании.
При оценке этиологической структуры тугоухости с отягощенным семейным анамнезом первоначально наследственная этиология предполагалась в 75% (рис. 7). В результате ДНК-диагностики наследственность подтверждена на молекулярном уровне в 65% (104/161), поскольку в этих семьях обнаружена мутация 35delG в гене Сх26 (рис. 8). В 25% (40/161) случаев тугоухость могла быть связана c другими изменениями в гене Сх26 или мутациями в других генах. Исследуемая делеция в этих случаях не обнаружена, но клинические данные позволяли сделать вывод о наследственном характере заболевания.
Таким образом, используя клинические и молекулярно-генетические критерии, наследственный характер тугоухости был установлен в 90% (144/161) семей с отягощенной родословной. Эти результаты свидетельствовали, что знание семейного анамнеза играло ключевую роль в диагностике причины тугоухости, поскольку наличие родственников с нарушением слуха позволяет в большинстве случаев правильно ориентироваться в наследственном характере заболевания.
Клинические характеристики нарушений слуха, связанных с мутациями в гене Сх26. В результате работы были выявлены следующие типы родословных среди детей с несиндромальной тугоухостью наследственной этиологии, связанной с мутациями в гене Сх26 (генотипы ∆/∆ и ∆/N):
- Спорадические случаи 47,2% (93 семьи IA типа). Ребенок с нарушением слуха мог быть как первым, так вторым или третьим в семье, другие дети имели нормальный слух.
- Аутосомно-рецессивный тип наследования 52,8% (104 семьи).
а) Нарушение слуха у сибсов 6,1% (12 семей IБ типа).
б) Тугоухость родственников II-III степени родства 16,2% (32 семьи IБ типа).
г) Тугоухость у одного из родителей 3,6% (7семей II типа).
д) Ассортативный брак 26,9% (53 семьи III типа).
У проживающих в Санкт-Петербурге и Ленинградской области детей с измененным генотипом только 16,1% (33/205) бабушек и дедушек родились в Санкт-Петербурге, а 9,8% (20/205) - в Ленинградской области. Остальные семьи происходили из других краев и областей: Псковской, Тверской, Вологодской, Новгородской, Ярославской, Украины.
Характеристика нарушений слуха при наследственной тугоухости, связанной с мутациями в гене Сх26. В обследованной группе все дети с мутацией в 35delG имели несиндромальную двустороннюю НСТ с преобладанием тяжелых нарушений слуха (75,7%). Двусторонняя глухота имела место в 13,2%, НСТ IV степени в 37,6%, НСТ III-IV степени в 24,9%. В группе с неизмененным по мутации генотипом эти формы тугоухости составили 10,1%, 30,5% и 19,8%, соответственно. Тугоухость III степени в группе гомо- и гетерозигот по делеции составила 16,7%. Только у 3% пробандов отмечалась НСТ II-III степени. Тугоухость II степени имели 3,6% пациентов, включая пять пробандов гомозигот по делеции и двух детей гетерозигот по делеции. Причем трое детей гомозигот имели обоих родителей с нарушением слуха. Тугоухость легкой степени (I и I-II) среди гомозигот по мутации 35delG не встретилась, а среди гетерозигот она отмечена в 1 случае (0,5%). Ребенок имел родителей с нарушением слуха и являлся носителем двух разных мутаций в гене Сх26. Со слов родителей ухудшение слуха на фоне простудных и других заболеваний имело место у 15% детей гомозигот по делеции и 25% гетерозиготных носителей. Не исключено, что прогрессирование могло быть обусловлено влиянием экзогенных факторов.
Поскольку изначально изучались тяжелые формы нарушения слуха, характерные для врожденной и доречевой тугоухости, то число детей с легкой степенью тугоухости в обследованной группе в целом было небольшим. Это не позволило судить о распространенности измененного генотипа при легких нарушениях слуха. Вопрос требует дальнейшего изучения. Тем не менее, результаты исследования показали, что мутация 35delG в гене Сх26 встречалась и при легких формах двусторонней НСТ, что соответствовало данным литературы. Другие мутации гена или их сочетание с мутацией 35delG также могут приводить к легким нарушениям слуха, что определяет необходимость проведения скрининга всего гена Сх26.
Согласно полученным данным почти у всех гомозигот по делеции тугоухость имеет врожденный или доречевой характер, поскольку возраст первичной диагностики нарушений слуха чаще всего относится к периоду с рождения до двух лет (87%). Средний возраст первичного выявления тугоухости среди гомозигот по делеции 14 месяцев, а среди гетерозигот 18,4 месяца. В группе пробандов с неизмененным по делеции генотипом средний возраст первичной диагностики нарушения слуха составил 24,2 месяца. Тугоухость у большинства гомозиготных носителей делеции (47,3%) выявлена до года, при этом преобладали тяжелые нарушения слуха. Среди гетерозиготных носителей только у 27,4% детей тугоухость была обнаружена до года. Среди гомозигот по мутации в возрасте одного года нарушение слуха заметили родители в 19,8% случаев, а от года до двух лет включительно также в 19,8% случаев. Половина детей с НСТ III степени выявлены в возрасте до года и в год, у остальных нарушение слуха замечено к двум, к трем и даже к пяти годам. Среди гомозигот по делеции с 2 до 3 лет тугоухость была обнаружена только у 9% детей. Возраст первичного выявления тугоухости для всех гетерозигот по делеции также распределился с рождения и до 3 лет включительно. Единичные случаи выявлены до 5 лет. Таким образом, нарушения слуха, связанные с изменениями в гене Сх26 были обнаружены на временном отрезке до 6 лет. Молекулярная диагностика позволит выявлять таких детей раньше.
Результаты исследования показали, что сочетание нарушения слуха с патологией других органов и систем в рамках известных синдромов в группе с делецией не выявлено. Другая сопутствующая патология отмечена среди 13,7% гомозигот по делеции. В группе с измененным генотипом имели место единичные случаи изолированных врожденных пороков развития лица (расщелина верхней губы и неба), конечностей (расщелина пальцев стопы), ангиопатии сетчатки, кривошеи, проляпса митрального клапана, гиперкератоза кистей и стоп и так далее. В трех случаях выявлены гемангиомы и пигментный невус. Диагноз перинатальной энцефалопатии имел место в 5,6% случаев, включая перинатальную энцефалопатию с синдромом двигательных нарушений (2%) и вертебробазилярной недостаточности (1,5%).
В результате анализа анамнестических данных оказалось, что в группе с измененным генотипом только в 24% случаев не было видимых причин для нарушения слуха. Почти 20% гомозигот по мутации 35delG в гене Сх26 имели в анамнезе патологию беременности и родов (врожденные инфекции, гемолитическую болезнь новорожденных, родовые травмы, асфиксию, недоношенность и другие), заболевания первых лет жизни, и тяжелые инфекции, за исключением менингитов. Применение ототоксических антибиотиков и других лекарственных средств довольно часто упоминалось при сборе анамнеза заболевания как основная или одна из причин тугоухости. Согласно полученным данным мутация 35delG в гене Сх26 была выявлена в половине случаев тугоухости/глухоты (47,3%) с использованием антибиотиков и других средств. Поэтому, ссылки на кратковременные курсы ототоксических антибиотиков, грипп, детские инфекции не исключают необходимость генетического обследования.
Медико-генетическое консультирование показано:
- Детям с нарушением слуха и сопутствующей патологией других органов и систем, а также их родственникам.
- Всем лицам с несиндромальной тугоухостью, включая детей, выявленных с помощью слуховых тестов, и особенно детям с тугоухостью неясной этиологии.
- Лицам с одним и более тугоухим родственником независимо от степени родства (брат, сестра, дядя, тетя, бабушка, дедушка и другие). В этом случае МГК и ДНК-диагностика строго обязательны, даже если сам пробанд имеет нормальный слух.
- Носителям мутаций при планировании семьи и прогнозе потомства.
ВЫВОДЫ
- При целенаправленном медико-генетическом консультировании врожденной и доречевой тугоухости доля несиндромальной двусторонней НСТ составила 82,2% среди, а доля синдромальных форм тугоухости -17,8%.
- Распространенность врожденной и стойкой детской тугоухости в Санкт-Петербурге в 1994 г. среди детей в возрасте от 0 до 16 лет составила 38 на 100 тысяч населения. Слышащих родителей имели 80,9% детей. Частота врожденной и стойкой детской тугоухости составила 3,4 на 1000 новорожденных, двусторонней тяжелой тугоухости и глухоты 0,8 на 1000 новорожденных.
- В общей группе с врожденной и доречевой стойкой тугоухостью после ДНК-диагностики наследственные нарушения слуха составили 52,1%.
- Среди детей с врожденной и доречевой несиндромальной тугоухостью в обследованной группе частота мутации 35delG составила 53%, в гомозиготном состоянии 39%, в гетерозиготном состоянии 14%. Среди всех обнаруженных и предполагаемых мутаций в гене Сх26 доля мутации 35delG 87%. Распространенность мутации 310del14 в обследованной группе 2% и 0,5% мутации 235delC. Частота мутации A1555G гена 12S p-РНК мт-ДНК составила 3%, крупной делеции гена Сх30 1%.
- Среди детей с врожденной и доречевой несиндромальной тугоухостью, имеющих слышащих родителей, мутацию 35delG можно ожидать в 45% случаях, или в каждой второй семье. В группе детей с нарушением слуха неясной этиологии измененный генотип был обнаружен в 49%.
- Показатели распространенности мутации 35delG зависят от ряда характеристик обследуемой группы: возраст первичной диагностики, степень тяжести тугоухости, анамнез заболевания, семейный анамнез, происхождение. При отягощенном семейном анамнезе имел значение тип семьи. В группе детей с нарушением слуха у обоих родителей мутация обнаружена в 96%.
- Клиника нарушений слуха при мутации 35delG характеризуется в основном двусторонней тяжелой и среднетяжелой, врожденной и доречевой стойкой тугоухостью, отягощенным и неотягощенным семейным анамнезом, разнообразием экзогенных факторов в анамнезе заболевания.
- Основной группой лиц, которым показаны консультация генетика и ДНК-диагностика являются родственники тугоухих детей и взрослых с измененным генотипом, носители мутаций, дети с синдромальной тугоухостью и их родственники. Обеспечение истинной профилактики наследственной тугоухости возможно только с помощью системного подхода к выявлению групп риска.
- Эффективность профилактики наследственных форм врожденной тугоухости и глухоты зависит от внедрения медико-генетического консультирования и ДНК-диагностики в практику сурдологических кабинетов крупных городов с курированием регионов по данной проблеме. Существующая в стране сеть сурдологических и медико-генетических центров является мощной базой способной обеспечить системный подход и взаимодействие между специалистами в решении вопросов профилактики.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- При сочетании тугоухости с патологией других органов в обязательном порядке необходима консультация генетика и более тщательное обследование ребенка, членов его семьи для установления правильного диагноза – синдромальной формы нарушения слуха.
- Исследование мутаций в гене Сх26 показано всем детям и взрослым с врожденной и доречевой нейросенсорной тугоухостью.
- Дети со стойкой кондуктивной тугоухостью невоспалительного генеза любой степени тяжести должны направляться на консультацию генетика.
- Случаи несиндромальной тугоухости неясной этиологии и случаи нарушения слуха, сопровождаемые любой сопутствующей патологией, следует активно направлять на консультацию к генетику. Методы молекулярной диагностики расширяют возможности врачей при выявлении наследственной тугоухости.
- Консультация генетика необходима не только семьям с отягощенной по нарушению слуха родословной, но и здоровым родителям при сознательном подходе к планированию семьи. Методы ДНК-диагностики позволяют проводить консультирование еще до рождения первого ребенка и при планировании второго, одновременно помогая преодолеть страх перед «наследственностью».
- При прогнозе потомства по поводу тугоухости необходимо учитывать число детей в семье и состояние слуха у них. Хотя риск наследования рецессивной мутации и риск рождения глухого ребенка в семье слышащих носителей патологической мутации одинаков для каждой беременности.
- Тяжелая двусторонняя несиндромальная НСТ является прямым показанием для ДНК-диагностики мутаций в гене Сх26. Родителям детей с двусторонней НСТ I-II, II, и II-III степени тяжести оправдана ДНК-диагностика всего гена Сх26 для исключения мутации 35delG и других изменений в данном гене.
- Молекулярные методы исследования, требующие небольшого количества материала для генетического анализа, помогают осуществлять высокоинформативное медико-генетическое консультирование в каждой конкретной семье независимо от места жительства. Само консультирование предполагает личный осмотр и беседу с семьей. Эта проблема может быть решена при развитии сурдологической и медико-генетической службы на местах, выполнении анализов в специализированных центрах.
- При изучении распространенности наследственных форм тугоухости следует учитывать не только обращаемость, но и активное выявление в ходе скрининговых осмотров. Единый регистр в рамках определенной территории может обеспечить преемственность в накоплении данных по группам риска и эффективность проводимых профилактических мероприятий.
- Для эффективной профилактики новых случаев наследственной тугоухости требуется системный подход к выявлению групп риска среди населения и взаимодействие между специалистами. Необходимо развивать следующие направления совместной деятельности сурдологов и врачей-генетиков:
- Универсальный скрининг новорожденных, включая генетические тесты.
- Скрининг гетерозиготных носителей среди здорового населения, изучение генетической структуры популяции в целом и тугоухих лиц в частности.
- Выявление и учет групп риска по врожденной тугоухости.
- Работа с семьями в консультациях «семья и брак».
- Просветительская деятельность среди населения.
Список сокращений.
НСТ - нейросенсорная тугоухость
ДНК - дезоксирибонуклеиновая кислота
GJB2 (Сх26), GJB6 (Сх30) - ген коннексина 26 и ген коннексина 30
∆/∆ - генотип гомозигот по мутации 35delG в гене Сх26
∆/N - генотип гетерозигот по мутации 35delG в гене Сх26
N/N - негативный генотип (мутация 35delG в гене Сх26 не обнаружена)
ПЦР - полимеразная цепная реакция
SSCP - полиморфизм конформации одноцепочечных фрагментов
