В отдаленном периоде
| Вид материала | Автореферат |
- Методические рекомендации для самостоятельной работы по элективной дисциплине, 41.54kb.
- Загрудинный зоб хирургическое лечение, 55.58kb.
- Клинические особенности, прогнозирование и дифференцированное лечение хронической головной, 332.77kb.
- Комплексная реабилитация больных в отдалённом периоде черепно-мозговой травмы на этапе, 71.66kb.
- Перинатальная патология актуальность проблемы, 275.94kb.
- Стно, любое осмысленное действие совершается человеком целенаправленно, то есть с целью, 192.55kb.
- Ейших банков сша, вполне серьезно говорят о возможности замены в не столь отдаленном, 654.95kb.
- О. В. Халецкая, В. В. Краснов, А. П. Обрядина, М. А. Суслова,, 24.57kb.
- Героям нужна память наша!, 37.18kb.
- Ii часть. Пояснительная записка к докладу Главы рабочего поселка Кольцово о достигнутых, 359.99kb.
На правах рукописи
АКСЕНОВА
Виктория Борисовна
ЭФФЕКТИВНОСТЬ ЭМБОЛИЗАЦИИ МАТОЧНЫХ
АРТЕРИЙ У ПАЦИЕНТОК С МИОМОЙ МАТКИ
В ОТДАЛЕННОМ ПЕРИОДЕ
14.01.01 – Акушерство и гинекология
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2011
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
^ Научные руководители:
доктор медицинских наук,
профессор Бреусенко Валентина Григорьевна
доктор медицинских наук,
профессор ^ Капранов Сергей Анатольевич
Официальные оппоненты:
доктор медицинских наук,
профессор Агаджанова Анна Арамовна
доктор медицинских наук,
профессор ^ Тихомиров Александр Леонидович
Ведущее учреждение:
Государственное учреждение здравоохранения Московский областной научно-исследовательский институт акушерства и гинекологии Министерства здравоохранения Московской области
Защита диссертации состоится «30» мая 2011 года в 14.00 часов на заседании диссертационного совета Д 208.072.12 при ГОУ ВПО РГМУ Росздрава
по адресу: 117997, Москва, ул. Островитянова, д.1.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ Росздрава по адресу: 117997, Москва, ул. Островитянова, д.1.
Автореферат разослан «25» апреля 2011 г.
Ученый секретарь диссертационного
совета доктор медицинских наук,
п
 рофессор Хашукоева Асият Зульчифовна
рофессор Хашукоева Асият Зульчифовна ^ ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования. Миома матки - одно из частых гинекологических заболеваний, которое до настоящего времени остается основным показанием для ее удаления. Внедрение в практику новых высокотехнологичных методов лечения, таких как ЭМА, явилось основанием для пересмотра вопроса относительно радикального хирургического вмешательства, отдав предпочтение альтернативным подходам, которые позволяют сохранить менструальную и репродуктивную функции [Бреусенко В.Г. и соавт., 2006; Капранов С.А. и соавт., 2007, Usadi R.S. et all., 2007, Yamagami T. et all., 2009].
Worthington-Kirsch R.(2003) создал реестр для сбора данных о безопасности и эффективности ЭМА. Технический успех по данным реестра составил 96-98%. Valenti D, Al-Fozano H, Torres CI, 2003, представили анализ стоимости ЭМА в сравнении с миомэктомией и гистерэктомией.,в котором продемонстрировали, что ЭМА требовала значительно меньшего времени нахождения в стационаре по сравнению с хирургическим лечением.
Все клиницисты, как отечественные, так и зарубежные, отметили, что ЭМА является безопасным, экономичным и клинически эффективным методом лечения миомы матки [Доброхотова Ю.Э., 2006, Бреусенко В.Г., 2007, Arleo E.K. et all., 2003, James Spies, 2003, Worthington-Kirsch, 2003].
Несмотря на значительное количество отечественных и зарубежных публикаций, посвященных эндоваскулярному лечению миомы матки, до сих пор остается ряд не полностью освещенных проблем, касающихся отдаленных результатов ЭМА. В их числе: оценка клинического течения миомы матки после операции с учетом топографо–анатомического расположения миоматозных узлов, влияние ЭМА на менструальную функцию и функцию яичников с учетом возрастных периодов жизни женщины, репродуктивное здоровье пациенток. Дискутабелен вопрос о проведении ЭМА как первого этапа лечения у больных с большими размерами миоматозных узлов, субмукозными узлами и об особенностях проведения вмешательства при перешеечной и шеечной локализации миомы. В доступной литературе отсутствует анализ причин неудовлетворительных результатов эндоваскулярного лечения. Все вышеперечисленное явилось основанием для проведения настоящей работы.
^ Цель исследования
Повысить эффективность ЭМА у пациенток с миомой матки, изучив отдаленный послеоперационный период.
Задачи исследования
- Изучить клинические проявления миомы матки у пациенток, перенесших ЭМА, в позднем послеоперационном периоде (через 6-12 месяцев), а также в отдаленные сроки (через 3-5 лет).
- Разработать алгоритм лечебных мероприятий после ЭМА у больных с интерстициальной и субмукозной миомой матки:
- механическая миомэктомия;
- гистерорезекция.
- Определить целесообразность и сроки проведения у пациенток с субсерозной миомой матки лапароскопической и лапаротомической миомэктомии после ЭМА.
- Оценить овариальную и менструальную функции у пациенток после ЭМА с учетом возраста в раннем, позднем репродуктивном периоде и в пременопаузе.
- Разработать тактику ведения больных с миомой матки после ЭМА при остаточной васкуляризации миоматозных узлов или их реваскуляризации.
^ Научная новизна
Впервые на основании анализа большого количества больных детально изучены клинические проявления ЭМА у пациенток с миомой матки в позднем постэмболизационном периоде (от 6 до 12 месяцев) и в отдаленные сроки (3-5 лет).
Разработан алгоритм лечебных мероприятий после ЭМА у больных с субмукозной и субсерозной локализацией узлов.
Впервые объективно оценена эффективность ЭМА у пациенток с миомой матки в различные возрастные периоды жизни женщины.
Подтверждено отсутствие отрицательного воздействия ЭМА на функцию яичников у пациенток репродуктивного возраста.
Впервые разработана тактика ведения больных с миомой матки и неудовлетворительными результатами ЭМА.
^ Практическая значимость работы
Разработан алгоритм ведения постэмболизационного периода у больных с миомой матки, что является чрезвычайно важным для пациенток репродуктивного возраста с нереализованной репродуктивной функцией. Отработанная тактика ведения пациенток помогает своевременно проводить мероприятия по оказанию помощи при субмукозной, субсерозной миоме матки, что позволяет избежать возможных осложнений у больных, перенесших ЭМА.
^ Основные положения, выносимые на защиту
- ЭМА имеет стойкий эффект относительно клинических проявлений миомы матки в течение 5 лет.
- Клиническую эффективность ЭМА необходимо оценивать после всех топографо-анатомических изменений, происходящих в течение года с момента операции.
- Проведение после ЭМА миомэктомии является не осложнением, а программированным этапом, позволяющим избавиться от узлов.
- Субсерозные и интерстициальные миоматозные узлы не требуют миомэктомии при уменьшении размеров матки после ЭМА меньше 12 недель.
- Абдоминальная миомэктомия показана при миоме матки после ЭМА свыше 14 недель, а также формировании ножки субсерозного узла.
- ЭМА приводит к нормализации менструальной функции и у большинства больных не оказывает угнетающего действия на яичники.
^ Внедрение полученных результатов исследования в практику
Результаты исследования внедрены в практику гинекологических отделений Центра планирования семьи и репродукции человека и городской клинической больницы №31 г. Москвы. Материалы диссертации используются в педагогическом процессе на кафедре акушерства и гинекологии педиатрического факультета ГОУ ВПО РГМУ Росздрава в лекционном курсе для студентов, клинических ординаторов и курсантов ФУВ.
^ Апробация диссертации
Основные положения диссертации доложены на совместной научно – практической конференции коллектива сотрудников кафедры акушерства и гинекологии педиатрического факультета РГМУ и сотрудников городской клинической больницы № 31 и Центра планирования семьи и репродукции человека г. Москвы 15 октября 2010 года, протокол №7.
Публикации
Основные положения диссертации отражены в 24 публикациях, из них 7 - в изданиях, рекомендуемых ВАК Минобрнауки.
^ ОБЪЕМ И СТРУКТУРА РАБОТЫ
Диссертация состоит из введения, обзора литературы (глава 1), клинической характеристики больных и описания методов исследования (глава 2), результатов собственных наблюдений (глава 3), обсуждения полученных результатов (глава 4), выводов, практических рекомендаций и библиографического указателя литературы.
Работа изложена на 138 страницах машинописного текста, иллюстрирована 19 таблицами, 5 графиками и 2 диаграммами.
Список литературы содержит 129 источников, из них 53 - отечественных, 76 - зарубежных.
^ МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Обследовано 180 пациенток с миомой матки с длительностью наблюдения до 5 лет после эмболизации маточных артерий. Возраст обследованных колебался от 20 до 55 лет, средний возраст составил 35,90,54 года [диаграмма №1].
Диаграмма №1.
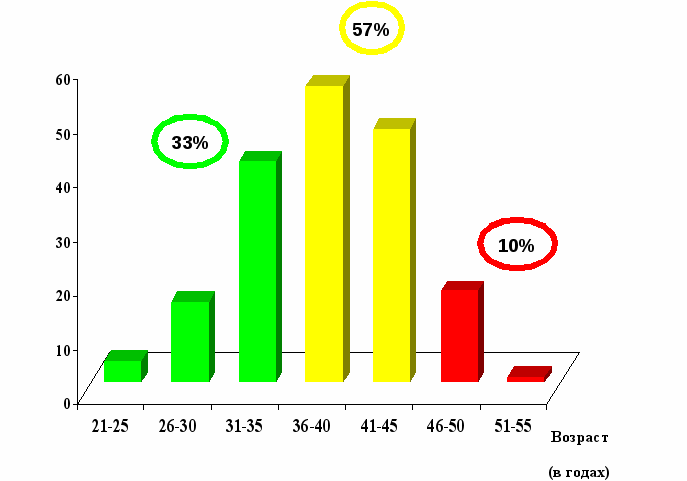
^ Ранний репродуктивный n-60
Количество пациенток
Поздний репродуктивный n-102
Пременопаузальный период n-18
Показаниями для ЭМА были: величина миомы матки свыше 14 недель беременности, мено– и метроррагии, анемизирующие пациентку, а также неэффективность других методов лечения миомы матки (консервативной терапии, хирургических вмешательств) [таблица №1].
Таблица №1.
^ Показания для проведения ЭМА (n -180)
| Показания | абс. | отн.(%) |
| Величина миомы матки более 14 недель беременности | 83 | 46,1 |
| Быстрый рост узлов | 21 | 11,7 |
| Мено-, менометроррагия, анемия II | 117 | 65,2 |
| Стойкий болевой синдром | 69 | 38,3 |
| Нарушение функции соседних органов | 59 | 32,8 |
| Неэффективность других методов лечения: 1. Гормональной терапии: -аГнРГ -прогестинами 2. Рост узлов после миомэктомии различными доступами: -лапаротомической -лапароскопической -трансцервикальной | 75 46 13 33 29 5 18 7 | 41,7 25,6 7,1 18,5 16,1 2,6 9,8 3,7 |
Нами установлено, что ЭМА проводилась пациенткам, имевшим показания для гистерэктомии, но отказавшимся от радикального хирургического лечения. На основании данных клинических и биохимических анализов крови у 148 наблюдаемых выявлена хроническая постгеморрагическая железодефицитная анемия. У 14 больных имелась сопутствующая выраженная экстрагенитальная патология, повышающая операционно-анестезиологический риск.
При анализе топографо-анатомического расположения миоматозных узлов выявлено, что единичные узлы были у 46,7% пациенток. Из них у 55,9% была диагностирована интерстициальная миома, субмукозная локализация - у 27,4% больных. У 4,8% ЭМА выполнялась при единичных субсерозных узлах 1-2 типа. Множественная миома матки была диагностирована у 53,3% больных.
В нашей работе, помимо общепринятых методов обследования, проводилась оценка гормонального профиля (ЛГ, ФСГ, эстрадиол), исследование свертывающей системы крови. При нарушении менструального цикла по типу метроррагии выполняли аспирационную биопсию эндометрия. При подозрении на патологию эндометрия - гистероскопию и раздельное диагностическое выскабливание слизистой матки с последующим гистологическим исследованием соскобов [таблица №2].
Таблица №2.
^ Методы диагностики и объем проведенных исследований
| Проведенные исследования | Сроки наблюдения | |
| За 1 год | За 5 лет | |
| Общеклинические исследования | 723 | 1719 |
| Гормональный профиль | 722 | 1768 |
| Кольпоскопия | 184 | 1078 |
| Мазки на онкоцитологию | 168 | 915 |
| УЗИ малого таза и ЦДК | 1073 | 2512 |
| МРТ малого таза | 18 | 26 |
| Гидросонография | 102 | 348 |
| Гистероскопия, РДВ слизистой матки | 51 | 97 |
| Всего | 3041 | 8463 |
На первом этапе, до проведения ЭМА, и в последующем, в сроки 1, 6, 9, 12, 18, 24, 30, 36 и 60 месяцев после операции всем больным выполнялось УЗИ органов малого таза при помощи серии продольных и поперечных сечений на аппаратах “Acuson” XP 128\10, “Technos MP” Esaote и Voluson 730, General Electric Medical Systems (Австрия), мультичастотными трансабдоминальным и трансвагинальным датчиками (3,5–7,0Мгц). Во время исследования детализировались топография миоматозных узлов, их структура, количество, локализация и размеры, толщина капсулы, тип, вычислялся объем матки, оценивалась ее форма и размеры, определялось состояние М-эхо. При ЦДК выявлялось наличие локусов васкуляризации, их количество, расположение (внутри миоматозного узла - интранодулярный кровоток, в капсуле узла - перинодулярный). Количественная оценка показателей кровотока в миоматозных узлах, маточных, аркуатных, радиальных, базальных, яичниковых артериях проводилась на основании показателей Vmax (максимальная скорость), Vmin (минимальная скорость), индекса резистентности (ИР), пульсационного индекса (ПИ), систоло-диастолического отношения (СДО). В отдаленном послеоперационном периоде оценивались динамика изменения показателей кровотока, размеров матки и миоматозных узлов, их локализация, дегенеративные изменения, состояние полости матки и яичников. Детально изучались особенности акустического строения яичников и состояние фолликулов на различных стадиях их развития. Для уточнения процентного соотношения итрамурального и субмукозного компонентов в предоперационном периоде 76 пациенткам была выполнена гидросонография.
При больших размерах миомы матки применялись компьютерная и магнитнорезонансная томография с использованием рентгеновского компьютерного томографа Sytec 200001 фирмы «General Electric».
Гистероскопия и лапароскопия производились при помощи эндоскопического оборудования фирмы Karl Storz.
Непосредственно перед ЭМА выполнялась двухсторонняя селективная и суперселективная ангиография сосудов бассейна внутренней подвздошной артерии. Ангиографические исследования проводилось в условиях рентгеноперационной с использованием цифровых ангиографических аппаратов с функцией дигитальной субтракции и с функцией «roadmap» OEC 98-00 фирмы General Electric, США и Philips Integris Allura производства фирмы Philips, Германия.
Эмболизация маточных артерий проводилась по стандартной методике. При селективной катетеризации маточных артерий использовались катетеры Cobra 4F, 5F (Cordis, J&J), а также катетеры Roberts Uterine Curve Catheter (William Cook Europe). В качестве эмболизирующих веществ для ЭМА нами использовались синтетический материал поливинилалкоголь - PVA (COOK), TruFill (Cordis, J&J) с размером микрочастиц - 355-500 и 500-710 µm, сферический PVA Сontour производства Boston Scientific, США, а также эмбосферы Bead Block (Terumo, Япония).
Статистическая обработка данных выполнена с применением электронных таблиц «Microsoft Excel» и «Statistica» (StatSoft, USA); вычисляли медиану, М, SD, значимость различий оценивали по критериям Стьюдента, Манна-Уитни и Фишера, Вилкоксона для независимых и парных выборок.
^ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Проведенный анализ наблюдений в позднем постэмболизационном периоде (от 6 до 12 месяцев) и в отдаленные сроки (3-5 лет) позволил нам выявить, что изменение характера кровоснабжения матки и миоматозных узлов приводит к взаимосвязанным последовательным анатомическим трансформациям: уменьшению объема матки и миоматозных узлов, изменению топографии узлов, и, как следствие, устранению клинических проявлений миомы матки. К 6 месяцам наблюдения размеры тела матки, в среднем, уменьшались на 45,2±3,8-50,4±4,6%, к 12 месяцам – еще на 10,3±1,9-15,8±2,1%. Через 2-5 лет мониторинга значимого изменения размеров матки не происходило. Однако у 27,2% (49) обследуемых при множественной миоме было зарегистрировано их уменьшение на 65,1±6,3-70, 5±8,1%. У 33,9% (61) пациенток матка стала нормальных размеров.
Уменьшение размеров миоматозных узлов приводило к сокращению волокон миометрия и закономерному изменению топографии миоматозных узлов. Феномен миграции миоматозных узлов делает доступной их полную энуклеацию: самопроизвольную (при экспульсии, миолизисе и фрагментации) или хирургическую (трансцервикальная миомэктомия, гистерорезекция, лапаротомическая или лапароскопическая миомэктомия). Лапаротомическая миомэктомия выполнялась для удаления субсерозных узлов на широком основании. При формировании «ножки» субсерозного узла его можно удалить лапароскопически.
Нормализация размеров матки, в основном, была характерна для пациенток, у которых отмечалась элиминация мигрировавших миоматозных узлов. У 25 больных матка достигла нормальных размеров при самопроизвольной экспульсии узлов, у 49 после проведения на 2 этапе лечения – трансцервикальной миомэктомии, из них у 36 - механическим способом у 13 - при помощи гистерорезекции. У 4 больных размер матки достиг нормы после выполнения миомэктомии субсерозных узлов лапаротомическим доступом, у 8 - лапароскопическим. Всего двухэтапное лечение было проведено 47,2% больных.
Миграция узлов происходит, в основном, в полость матки. О перемещении миоматозных узлов в полость матки и самопроизвольной экспульсии указывали в своих работах C.H.Toh et all., 2003, W.J.Hehenkamp et all., 2004, D.K. Rajan et all., 2004, H.R. Park et all., 2005. В отдаленном периоде, по данным Gabriel-Cox K. et all. (2007) после ЭМА гистерэктомии удалось избежать более 80,12% пациенток. Однако второй этап лечения - миомэктомию различными способами авторы смогли использовать лишь у 5,7%. Ни в одной из работ мы не нашли анализа предполагаемых сроков экспульсии. В доступной литературе мы также не встретили указаний на то, какие миоматозные узлы могут самопроизвольно выделиться из полости матки.
Нами установлено, что наибольшее изменение топографического расположения было характерно для субмукозных и интерстициальных узлов с центрипетальным направлением роста, независимо от их размеров. При единичной субмукозной миоме матки ЭМА производилась только при отсутствии условий для миомэктомии (23 больные). В полость матки мигрировало 60,1% миоматозных узлов, а в последующем самопроизвольной экспульсии подверглись 16,9%. Сроки миграции миоматозных узлов в полость матки зависели от первоначального их топографического расположения, исходных размеров миомы, наличия узлов другой локализации. Скорость миграции была обратно пропорциональна размерам узла и прямо пропорциональна толщине мышечного слоя между узлом и серозным покровом матки и сократительной способности миометрия. Узлы, подвергшиеся самопроизвольной экспульсии, изначально были субмукозными 0 типа у 8 больных, I – у 7 и II –у 5; интерстициальными с центральным направлением роста – у 2 или центрипетальным – у 3. Трансцервикальная миомэктомия произведена 18 больным с субмукозной миомой II типа, 8 – I типа, 3 - 0 типа, а также 14 пациенткам с интерстициальными узлами с центрипетальным ростом и 6 – с интерстициальной миомой с центральным направлением роста.
На 2 этапе после ЭМА, по данным гидросонографии, появились условия для проведения гистерорезекции у 15 больных. Но у 2 пациенток в возрасте 41 и 45 лет, у которых прошло после ЭМА 1,5 года и 5 лет, выполнение гистерорезекции субмукозных узлов биполярным электродом оказалось технически невозможным из-за выраженного кальциноза. Учитывая отсутствие у этих больных клинических признаков миомы матки и незаинтересованность в реализации репродуктивной функции, решено было ограничиться диагностической гистероскопией. Оптимальными для гистерорезекции узлов следует считать сроки от 3 до 12 месяцев после эндоваскулярного вмешательства.
Нами выявлено, что субсерозные миоматозные узлы подвержены миграции в меньшей степени. Однако важным проявлением структурной перестройки субсерозных узлов после ЭМА можно считать уменьшение глубины мышечного ложа как следствие уменьшения размеров миоматозных узлов. Экспульсии субсерозной миомы в брюшную полость ни в одном наблюдении отмечено не было. Лапароскопическое удаление субсерозных миоматозных узлов в сроки до 24 месяцев было произведено у 8 пациенток, учитывая формирование ножки узлов. У 3 пациенток с гигантскими миомами, соответствующими до ЭМА 24, 28 и 36 неделям беременности, через 6-9 месяцев после эндоваскулярного вмешательства, была проведена миомэктомия лапаротомным доступом, после которой размеры матки не превышали 6-8 недель беременности. Важно отметить, что все миоматозные узлы были заэмболизированы, миометрий у этих больных не изменен, органосохраняющие операции протекали с минимальной кровопотерей.
Считаем, что оптимальными для выполнения миомэктомии лапаротомическим доступом являются сроки 6-12 месяцев после ЭМА. Поскольку именно к этому времени достигается максимальное уменьшение узлов и, следовательно, размер мышечного ложа, восстанавливается кровообращение в миометрии, что способствует более полноценной регенерации тканей и формированию состоятельного рубца на матке. Эти два фактора имеют особое значение для пациенток, планирующих беременность.
Тактика ведения больных с субсерозными миомами матки должна быть строго индивидуальной и зависеть от возраста пациентки, репродуктивных интересов, характера и локализации узлов.
Применение ЭМА у пациенток с множественной миомой матки, низко расположенными перешеечными узлами, а также при большом размере интерстициальных и интерстициально-субсерозных узлов позволило нам избежать радикального хирургического вмешательства у большинства из них (97,2%).
Оценивая клинические проявления у больных с миомой матки, перенесших ЭМА, мы выявили, что клинические проявления, связанные с увеличением матки, купировались в первые 6 месяцев после ЭМА по мере уменьшения миоматозных узлов, их экспульсии, миолизиса и миомэктомии, что приводило к сокращению объема матки в целом, что согласуется с данными других исследователей [John C. et all., 1999, 2001, Burn P. et all., 2000, Malartic C. et all., 2010, Kim K.A. et all., 2011].
По нашим данным, через 6 месяцев после ЭМА все больные с альгоменореей до операции отмечали уменьшение или исчезновение болей во время менструации. Боли, связанные с нарушением функции соседних органов (чувство дискомфорта, тяжести внизу живота, давление на мочевой пузырь, болезненный акт дефекации), к 6 месяцу наблюдения исчезли у каждой третьей пациентки и значительно уменьшились - у каждой второй больной. Диспареуния не отмечалась уже через 3-6 месяцев. По мере уменьшения размеров, изменения локализации и эвакуации миоматозных узлов к 3-12 месяцу после ЭМА у всех больных нивелировалась альгоменорея. По результатам наших исследований, при наблюдении больных в сроки от 12 месяцев до 5 лет после эффективной ЭМА клинических симптомов миомы матки выявлено не было.
В течение 5 лет наблюдения из 180 пациенток нарушения менструального цикла по типу мено– и метроррагии были отмечены у 43 больных репродуктивного возраста: метроррагии - у 9, меноррагии - у 34. У этих пациенток маточное кровотечение сопровождало самопроизвольную экспульсию миоматозных узлов или их миграцию в полость матки. Кровотечение не было обильным, характеризовалось незначительной или средней кровопотерей, и купировалось после эвакуации миоматозных узлов.
Гипоменструальный синдром наблюдался у 23 больных после ЭМА. У 6 пациенток пременопаузального периода указанные изменения расценены как физиологические. У 17 больных репродуктивного периода гипоменструальный синдром возник у 5 вследствие формирования внутриматочных синехий после самопроизвольной экспульсии узлов и у 12 после 2 этапа лечения - трансцервикальной миомэктомии. Нормализация менструального цикла произошла у 16 больных после эндоскопического разрушения внутриматочных синехий с последующим проведением курсов циклической гормонотерапии, использованием ангиопротекторов, витаминотерапии и физиотерапевтического лечения. У 1 больной 37 лет разрушить синехии при полной облитерации полости матки не представилось возможным.
В наших наблюдениях, после ЭМА изменений гормонального статуса либо не происходило, либо они носили транзиторный характер. Исключение составили 4 больные в возрасте от 48 до 53 лет, у которых до операции имелось повышение ФСГ (от 14,80 до 61,70 мМE/мл), ЛГ (от 18,16 до 59,31 мМE/мл), снижение концентрации эстрадиола (от 18,10 до 35,20 пг/мл) во все фазы менструального цикла. В течение года у этих пациенток наступила физиологическая менопауза.
В нашей работе, в течение 5 лет наблюдения неполная редукция артериального кровотока в миоматозных узлах зарегистрирована у 12 больных, реваскуляризация – у 6. Полученные нами данные позволяют прогнозировать неудовлетворительные результаты ЭМА. Причинами кровоснабжения миоматозных узлов при неэффективности ЭМА, помимо наличия маточно–яичниковых артериальных анастомозов, были атипическая васкуляризация миоматозных узлов, техническая невозможность ЭМА, кровоснабжение из влагалищной ветви маточной артерии, а также неустановленные источники кровоснабжения. Аналогичные нашим данные приводит в своей работе James B. Spies (2003), в исследовании которого были определены основные теоретические причины неудовлетворительных результатов ЭМА. Помимо технических проблем, связанных непосредственно с методикой оперативного вмешательства, одной из наиболее вероятных причин неудач в своей работе автор выделяет кровоснабжение узлов миомы из дополнительных, нетипичных источников, чаще всего из яичниковой артерии.
При длительном наблюдении за больными с миомой матки после ЭМА (в течение 5 лет) ни у одной из них не выявлено появления новых миоматозных узлов.
Ravina J.H. et all. (2000), Christmas H.B. et all. (2002) в своих публикациях описывают ЭМА как предпочтительный метод лечения миомы матки при желании пациентки сохранить репродуктивную функцию. Mara M. et all., (2008), напротив, считая ЭМА эффективной относительно симптомов миомы и менее инвазивным вмешательством в сравнении с миомэктомией, считают, что репродуктивные результаты выше при миомэктомии без эмболизации. Нами установлено восстановление репродуктивной функции у 14 (56,0%) пациенток из 25 заинтересованных в беременности.
Таким образом, ЭМА является высокоэффективным органосохраняющим методом лечения миомы матки. Эффективность составляет 98,4%. ЭМА может быть выполнена как самостоятельный метод лечения, приводя к нормализации менструальной функции, восстановлению уровня сывороточного железа, купированию клинических проявлений миомы матки (боли, диспареунии, сдавления смежных органов и др.), и как подготовка к последующей миомэктомии различными доступами. После ЭМА возможно наступление беременности и рождение здоровых детей.
ВЫВОДЫ
- ЭМА является органосохраняющим методом лечения миомы матки, имеет стойкий эффект в отдаленном периоде и может быть использована как самостоятельный метод лечения миомы матки (66,1%), а также в качестве подготовки к проведению миомэктомий (33,9%). Уменьшение объема матки и миоматозных узлов на 59,2-83,4%, вне зависимости от их локализации, происходит в течение года после ЭМА. В последующие 2-5 лет размеры матки остаются без изменений. У обследованных больных новых зон роста за 5 лет не зарегистрировано.
- У большинства пациенток репродуктивного возраста, по данным УЗИ с ДГ и гормонального профиля, ЭМА не оказывает отрицательного влияния на менструальную и овариальную функции в течение 5 лет наблюдения. Физиологическая постменопауза наступила у 2,2% больных пременопаузального возраста через 2-5 лет.
- Нормализация менструальной функции, показателей красной крови, исчезновение альгодисменореи происходит в первые 3 месяца после ЭМА. В сроки от 4 до 18 месяцев в связи с миграцей в полость матки миоматозных узлов у 3,2% больных отмечена транзиторная мено– или метроррагия. Клинические проявления, сопряженные с большим объемом матки и множеством узлов, симптомами сдавления соседних органов, а также диспареуния у всех нивелируются постепенно по мере уменьшения объема матки к 6-12 месяцу наблюдения. Через 2-5 лет данные симптомы не рецидивируют. При субмукозной миоме матки после ЭМА в течение 6 месяцев может происходить самостоятельная эвакуация миоматозных узлов из полости матки (миолизис – в 2,7%, самопроизвольная экспульсия – в 16,9%). У 95,2 % больных с субсерозной миомой матки регистрируется уменьшение размеров узла без выделения в сторону брюшной полости, что исключает повторную интервенцию. У 4,8% пациенток формируется субсерозная миома на ножке в течение 6 месяцев. Этим больным может быть произведена лапароскопическая миомэктомия.
- Миомэктомию лапаротомическим доступом следует проводить при размерах матки после ЭМА свыше 14 недель беременности и наличии субсерозных узлов на широком основании. Оптимальный срок для выполнения миомэктомии – после 1 года постэмболизационного периода, так как к этому времени достигается максимальный эффект в виде уменьшения размера и глубины мышечного ложа, происходит восстановление микроциркуляции в миометрии, и, следовательно, создаются оптимальные условия для формирования полноценного рубца.
- У 6,7% больных была диагностирована остаточная васкуляризация, у 3,3% - реваскуляризация миоматозных узлов. У каждой второй пациентки с шеечной и перешеечной локализацией узлов остаточная васкуляризация была из влагалищной ветви маточной артерии, что исключает повторную эмболизацию.
^ ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Учитывая, что основной клинический эффект после ЭМА наступает в течение 1 года, все больные в этот период должны находиться под динамическим наблюдением с проведением через 1, 6, 12 месяцев УЗИ и ДГ, оценки гормонального профиля. Такой мониторинг позволяет своевременно выявить атипическую васкуляризацию, реваскуляризацию, дополнительные источники кровоснабжения миомы, оценить в динамике размеры миомы и функцию яичников.
- При регистрации остаточного кровотока в миоматозных узлах или их реваскуляризации необходимо установить их причину. Больным с маточно – яичниковыми артериальными коммуникациями следует произвести повторную эмболизацию с изменением доступа. При затромбированных восходящих сегментах маточных артерий и дополнительном источнике кровоснабжения из влагалищной ветви целесообразно динамическое наблюдение. При реваскуляризации после ЭМА с появлением патологического кровотока, росте миомы и отсутствии клинического эффекта показана гистерэктомия, ввиду невозможности исключить саркому матки.
- У больных с исходно субмукозной миомой матки, а также при миграции в полость интерстициальных узлов с центрипетальным и центральным направлением роста при появлении условий для трансцервикальной миомэктомии должна осуществляться своевременная эвакуация этих узлов, которая может быть проведена механическим способом или при помощи гистерорезекции. Это позволяет избежать осложнений в виде эндометрита и пиометры.
- При исходно больших и гигантских размерах миомы уменьшение матки до 14 недель беременности и отсутствие клинических проявлений свидетельствуют о достигнутом лечебном эффекте ЭМА и не требуют дополнительного хирургического вмешательства.
- С целью профилактики формирования внутриматочных синехий и маточной формы аменореи при двухэтапном лечении (ЭМА и трансцервикальной миомэктомии) показано проведение курса циклической гормональной терапии эстроген–гестагенными препаратами в течение 3-6 месяцев с обязательным УЗ контролем состояния эндометрия.
^ СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ:
- Бреусенко В.Г., Краснова И.А., Капранов С.А., Шевченко Н.А., Аксенова В.Б. / Эмболизация маточных артерий в лечении миомы матки //Материалы ХVII Международного конгресса «Современные технологии в диагностике и лечении гинекологических заболеваний», Тезисы докладов – Москва, июнь 2004. – С.53-54.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Шевченко Н.А., Бобров Б.Ю., Аксенова В.Б. / Эмболизация маточных артерий, современный метод лечения миомы матки //Материалы VI Российского форума «Мать и дитя», Тезисы докладов - Москва, 12-15 сентября 2004. - С. 304.
- Савельева Г.М., Бреусенко В.Г., Капранов С.А., Краснова И.А., Бобров Б.Ю., Шевченко Н.А., Аксенова В.Б., Алиева А.А. / Эмболизация маточных артерий у больных с миомой матки //«Акушерство и гинекология» № 5 - М., 2004. - С. 21-24.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Бобров Б.Ю., Шевченко Н.А., Аксенова В.Б. / Эмболизация маточных артерий в лечении больных с подслизистой миомой матки //«Вопросы гинекологии, акушерства и перинатологии», том 4 №1 - М., 2005. - С. 46-50.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Шевченко Н.А., Аксенова В.Б. / Эмболизация маточных артерий в лечение субмукозной миомы матки //Материалы ХII Российского национального конгресса «Человек и лекарство», Тезисы докладов - Москва, 18-22 апреля 2005. - С. 71.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Шевченко Н.А., Аксенова В.Б. / Оценка менструальной функции у пациенток с миомой матки, перенесших эмболизацию маточных артерий. //Материалы XVIII Международного конгресса «Современные технологии в диагностике и лечении гинекологических заболеваний», Тезисы докладов - Москва, 6-9 июня 2005. - С. 116.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Аксенова В.Б., Бобров Б.Ю., Шевченко Н.А. / Спорные вопросы ЭМА при миоме матки //«Вопросы гинекологии, акушерства и перинатологии», №4, том 4 –М., 2005. - С. 44-48.
- Бреусенко В.Г., Капранов С.А., Краснова И.А., Бобров Б.Ю., Аксенова В.Б., Шевченко Н.А., Арютин Д.Г. / Некоторые дискутабельные вопросы ЭМА у больных с миомой матки //Материалы на VII российского форума «Мать и дитя»: Тезисы докладов - Москва, 11-14 октября 2005. - С. 337-338.
- Капранов С.А., Бреусенко В.Г., Бобров Б.Ю., Краснова И.А., Шевченко Н.А., Алиева А.А., Аксенова В.Б. / Применение ЭМА при лечении миомы матки: анализ 258 наблюдений //Международный журнал интервенционной кардиоангиологии №7 - М., 2005. - С. 36.
- Бреусенко В.Г., Краснова И.А., Капранов С.А., Бобров Б.Ю., Аксенова В.Б., Шевченко Н.А., Арютин Д.Г. / Некоторые дискуссионные вопросы ЭМА при лечении миомы матки //«Акушерство и гинекология» №3 - М., 2006. - С. 23-26.
- Бобров Б.Ю., Капранов С.А., Доброхотова Ю.Э., Краснова И.А., Аксенова В.Б., Арютин Д.Г. / Эмболизация маточных артерий. Современный взгляд на проблему //«Диагностическая и интервенционная радиология», Журнал издательства «Радиология и Пресса», том 1, №2 - М., 2007. - С. 56-73.
- Краснова И.А., Капранов С.А., Бобров Б.Ю., Аксенова В.Б., Шевченко Н.А., Арютин Д.Г. / Некоторые дискутабельные вопросы эмболизации маточных артерий при миоме матки //Материалы XXI международного конгресса с курсом эндоскопии и роботохирургии «Технологии XXI века в в диагностике и лечении гинекологических заболеваний» - Москва, 2008. - С. 54-55.
- Краснова И.А., Калмыкова Н.В., Аксенова В.Б., Арютин Д.Г., Затонских Л.В. / Влияние особенностей кровоснабжения органов малого таза на эффективность эмболизации маточных артерий в раннем и отдаленном послеоперационном периодах у пациенток с симптомной миомой матки // Материалы XXI международного конгресса с курсом эндоскопии и роботохирургии «Технологии XXI века в диагностике и лечении гинекологических заболеваний» - Москва, 2008. - С. 55-56.
- Аксенова В.Б., Арютин Д.Г. / Менструальная и репродуктивная функция у пациенток с миомой матки после эмболизации маточных артерий //«Вестник Российского Государственного Медицинского Университета», №3 (62) - М., 2008. - С. 5-6.
- Аксенова В.Б., Арютин Д.Г., Краснова А.С. / Эффективность эмболизации маточных артерий при миоме матки у пациенток с различными вариантами кровоснабжения органов малого таза //«Вестник Российского Государственного Медицинского Университета», №3 (62) - М., 2008. - С.6-8.
- Краснова И.А., Бреусенко В.Г., Капранов С.А., Арютин Д.Г., Аксёнова В.Б., Калмыкова Н.В. / Клинические результаты эмболизации маточных артерий при различных вариантах кровоснабжения органов малого таза у пациенток с миомой матки //«Проблемы репродукции» специальный выпуск – М., 2009. - С. 233-234.
- Савельева Г.М., Бреусенко В.Г., Капранов С.А., Краснова И.А., Шиповский В.Н., Бобров Б.Ю., Арютин Д.Г., Аксенова В.Б., Ваганов Е.Ф. / Эмболизация маточных артерий в лечении миомы матки. Современное состояние вопроса //«Журнал Акушерства и Женских болезней», том LIX, выпуск 2 - М., 2010. - С. 81-86.
- Краснова И.А., Аксенова В.Б., Арютин Д.Г., Бреусенко В.Г. / Биполярная гистерорезекция в лечении миомы матки //XXIII Международный конгресс с курсом эндоскопии «Новые технологии в диагностике и лечении гинекологических заболеваний»: Тезисы докладов - Москва., 7-10 июня 2010. - С. 139.
- Арютин Д.Г., Аксенова В.Б., Калмыкова Н.В., Краснова А.С. / Результаты эндоваскулярного лечения миомы матки у пациенток с маточно-яичниковыми артериальными анастомозами. //Материалы 23-го Международного конгресса «Новые технологии в диагностике и лечении гинекологических заболеваний»: Тезисы докладов - Москва, 7-10 июня 2010.-С.37.
- Савельева Г.М., Бреусенко В.Г., Курцер М.А., Краснова И.А., Капранов С.А., Бобров Б.Ю. / Эндоваскулярные методы лечения в сохранении репродуктивного здоровья женщины. //Материалы V Международного конгресса по репродуктивной медицине. Проблемы репродукции, специальный выпуск – Москва, 2011. - С.189.
- Краснова И.А., Аксенова В.Б., Арютин Д.Г., Краснова А.С., Ваганов Е.Ф., Бреусенко В.Г. / Отдаленные результаты лечения пациенток с миомой матки методом ЭМА //Материалы V Международного конгресса по репродуктивной медицине. Проблемы репродукции, специальный выпуск – Москва, 2011г. - С.189.
- Saveljeva G.М., Breusenko V.G., Kapranov S.A., Krasnova I.А., Aksenova V.B., Aryutin D.G. / Uterine arteries embolization in treatment of fibroids: long-term outcome //«XVIII FIGO World congress of gynecology and obstetrics» - МА., 5-10 november 2006.- P. 117.
- Saveljeva G.М., Breusenko V.G., Krasnova I.А., Kapranov S.A., Aksenova V.B., Aryutin D.G. /Remote results of uterine artery embolization at the mioma of uteris. //«XVIII FIGO World congress of gynecology and obstetrics» – МА, 5-10 november 2006. book 4, - Р. 116.
- Saveljeva G., Kurcer M., Breusenko V., Kapranov S., Krasnova I., Aksenova V., Stepanov K. / Endovascular surgery in obstetrics and gynecology //«XIX FIGO World congress of gynecology and obstetrics» - SА., 4-9 october 2009.– Р. 329.
