Удк 004. 383. 3 Сравнительный анализ применения различных оценок энтропии ээг-сигнала для распознавания стадий наркоза
| Вид материала | Документы |
- Удк 004. 838: 004. 853: 004. 855. 5: 004. 738. 5 Анализ эффективности работы web-сайта, 146.96kb.
- С. Д. Кургалин, Я. А. Туровский,, 63.75kb.
- Темы курсовых работ по дисциплине «Макроэкономика» Сравнительный анализ методологических, 130.71kb.
- Сравнительный анализ различных систем адресации, используемых в мини и микроэвм, 240.23kb.
- Удк 004. 021+004. 81 Алгоритмы построения маршрута на карте по параметрам, 88.51kb.
- Сравнительный анализ методов активации процессов коагуляции и флокуляции, 35.43kb.
- На прошлой лекции было дано краткое введения в биоинформатику днк-биочип-экспериментов, 172.51kb.
- Удк 007. 5 Эмоции как аппарат оценок поведения интеллектуальных систем, 136kb.
- Е философских предпосылок, определивших возникновение и развитие различных дисциплинарных, 6956.59kb.
- Сравнительный анализ поисковой техники разных видов. Металлоискатели, магнитомеры,, 102.63kb.
УДК 004.383.3
Сравнительный анализ применения различных оценок энтропии ЭЭГ-сигнала для распознавания стадий наркоза1
Немирко А.П., Манило Л.А., Калиниченко А.Н., Волкова С.С.
Введение
Проблема контроля адекватности общей анестезии не теряет своей актуальности, начиная с момента становления анестезиологии как науки и до сегодняшнего дня. Еще в монографии 1847 года, посвященной применению эфира в анестезиологии, Джон Сноу пишет: "Главное, что требует максимального умения и знаний при проведении наркоза - это, несомненно, определение того уровня, когда глубина наркоза оптимальна". [1] Известно, что излишне глубокая анестезия, или, наоборот, интранаркозное пробуждение не может не сказаться на качестве оперативного лечения в целом. Общепринятая методика оценки влияния анестетиков на больного основана на изучении параметров центральной и периферической гемодинамики, которые в определенной ситуации могут быть малоинформативными.
Современная концепция анестезиологии базируется на основном принципе - создании максимально эффективной и в тоже время безопасной модели общей анестезии. Однако решение этого вопроса невозможно без применения отлаженной методики обратной связи между пациентом и врачом-анестезиологом во время проведения анестезии, что и привело к необходимости разработки автоматических мониторов глубины наркоза.
Способы оценки энтропии сигнала ЭЭГ
Известно, что степень активности мозга отражается в электроэнцефалографическом (ЭЭГ) сигнале. Во время анестезии преобладают медленные волны и чем глубже анестезия, тем ниже частота колебаний. Дальнейшее увеличение дозы анестетиков может привести к прогрессивному снижению ЭЭГ-активности вплоть до изоэлектрической линии. Доказано, что показатели, полученные путем обработки и анализа электроэнцефалограмм, применимы для оценки степени анестетического эффекта препаратов.
Обычно ЭЭГ-сигналы анализируются в частотной области с использованием быстрого преобразования Фурье. Тем не менее, было показано, что нейронные системы проявляют свойства нелинейного, хаотического поведения, поэтому к исследованию ЭЭГ-сигнала можно применить методы теории нелинейной динамики, одним из которых является энтропийный анализ. В теории информации и при анализе биомедицинских сигналов, энтропия отражает и описывает характеристики нерегулярности, сложности и непредсказуемости сигнала [4].
Рассмотрим основные подходы к оценке энтропии ЭЭГ-сигнала, которые легли в основу данного исследования.
Энтропия Шеннона
Клод Элвуд Шеннон впервые определил энтропию как единицу измерения в теории информации. Применительно к анализу ЭЭГ, энтропия Шеннона отражает степень предсказуемости значений амплитуды ЭЭГ-сигнала, основанную на оценках плотности вероятности амплитудных значений исследованной части сигнала. Было сделано наблюдение, что энтропия Шеннона амплитуды ЭЭГ-сигнала равномерно повышается с возрастанием концентраций десфлурана, и было сделано предположение, что энтропия Шеннона – это простая и устойчивая мера анестетического эффекта препарата по ЭЭГ [4].
Определение энтропии Шеннона предполагает выполнение следующей последовательности шагов: задается - число интервальных оценок дискретных отсчетов сигнала xi, i N в диапазоне xmin, xmax, затем формируется множество L-мерных последовательностей
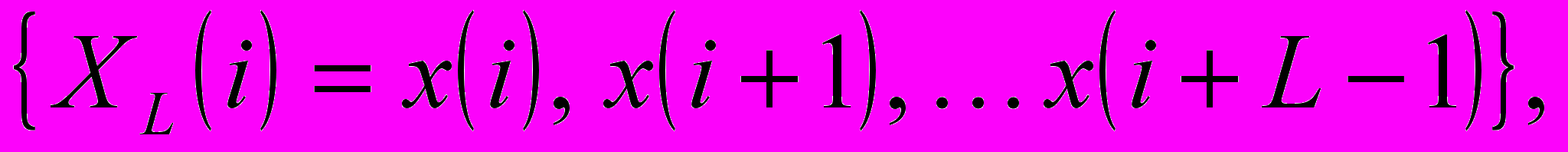
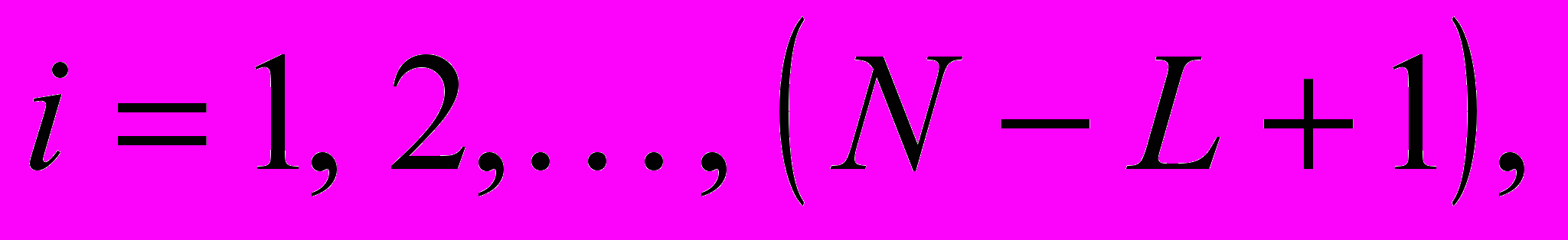 и оценивается вероятность появления каждой новой последовательности. При практических расчетах вероятности появления заменяются их оценками – частотами появления цепочек символов. Сумма этих частот и дает нам значение энтропии Шеннона
и оценивается вероятность появления каждой новой последовательности. При практических расчетах вероятности появления заменяются их оценками – частотами появления цепочек символов. Сумма этих частот и дает нам значение энтропии Шеннона 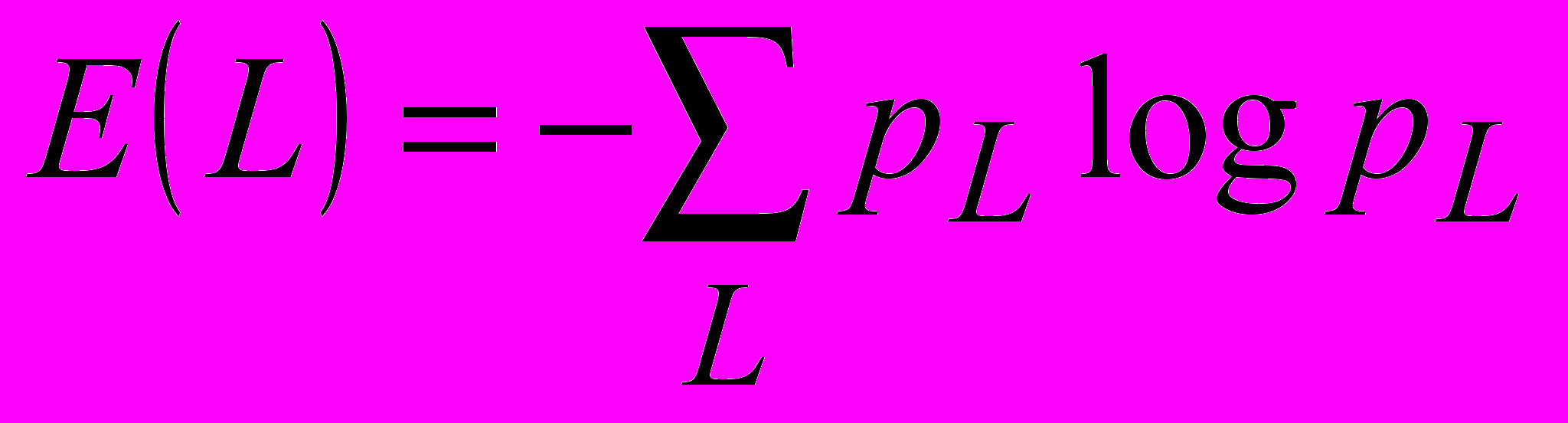 , где p L– вероятность (частота) появления конкретной цепочки событий длины L. Величина условной энтропии ELL определяется в виде приращения, получаемого безусловной энтропией EL при переходе от последовательности событий длины L1 к длине L:
, где p L– вероятность (частота) появления конкретной цепочки событий длины L. Величина условной энтропии ELL определяется в виде приращения, получаемого безусловной энтропией EL при переходе от последовательности событий длины L1 к длине L: 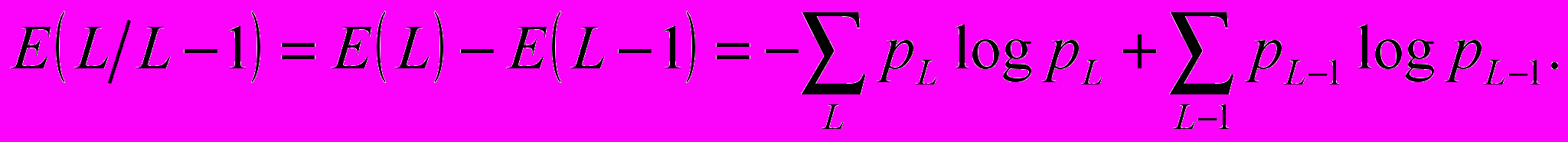
Аппроксимированная энтропия
Алгоритм расчета аппроксимированной энтропии был впервые опубликован в 1991 г. По сути, она является модификацией энтропии Колмогорова-Синая, специально разработанной для определения регулярности биологических сигналов при наличии белого шума. Аппроксимированная энтропия позволяет измерить предсказуемость будущих амплитудных значений ЭЭГ-сигнала, основываясь на известных предшествующих значениях [4].
Аппроксимированная энтропия вычисляется следующим образом: задаются значения двух параметров: m – длина анализируемых последовательностей отсчетов и R – величина порога, определяющего размеры ячеек фазового пространства (Rr∙SDx, r=0.05…0.3, где SDx – стандартное отклонение исходной выборки данных). Для дискретного сигнала xi, i N, осуществляются следующие преобразования: формируются последовательности длины m
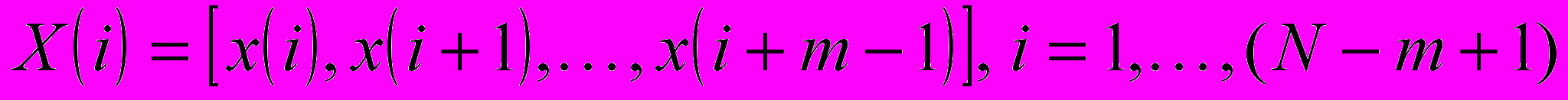 , причем каждая цепочка в этой последовательности интерпретируется как точка в m-мерном пространстве. Затем вокруг каждой такой точки строится гиперсфера радиусом R, и оценивается вероятность попадания точек в эти гиперсферы. Как и в случае энтропии Шеннона, оценкой вероятности являются частоты попадания в эти гиперсферы. Их сумма и дает нам безусловное значение аппроксимированной энтропии
, причем каждая цепочка в этой последовательности интерпретируется как точка в m-мерном пространстве. Затем вокруг каждой такой точки строится гиперсфера радиусом R, и оценивается вероятность попадания точек в эти гиперсферы. Как и в случае энтропии Шеннона, оценкой вероятности являются частоты попадания в эти гиперсферы. Их сумма и дает нам безусловное значение аппроксимированной энтропии 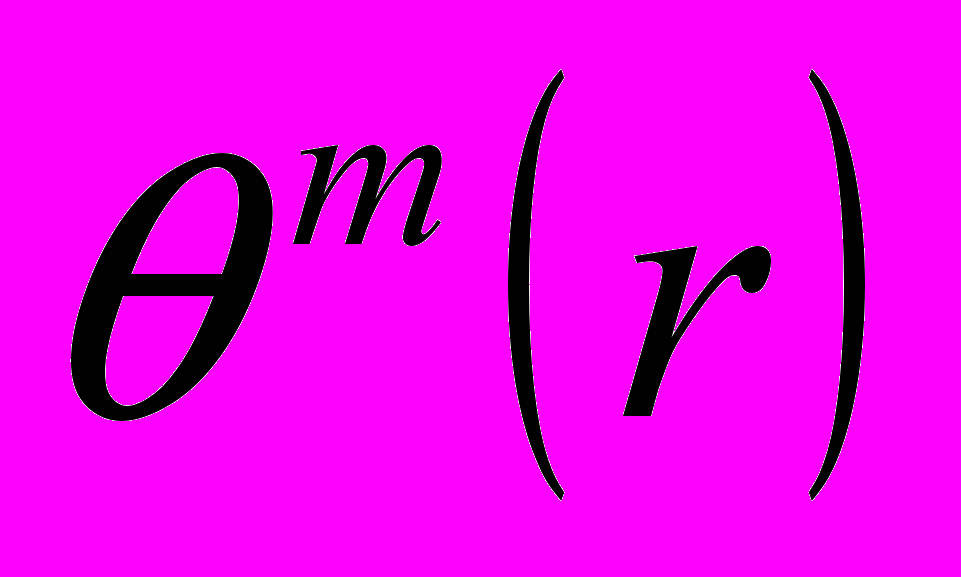 ,
, 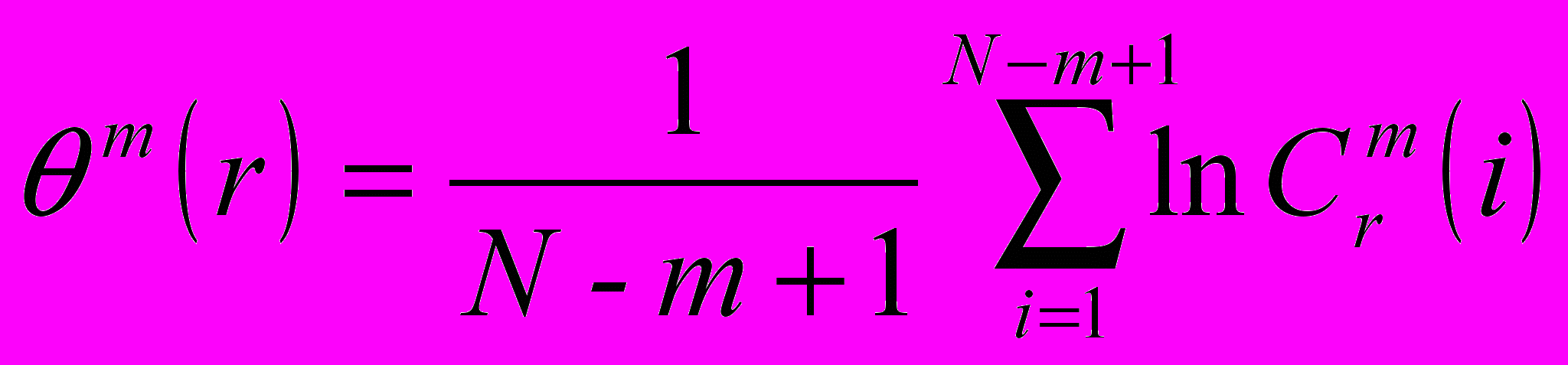 , где
, где 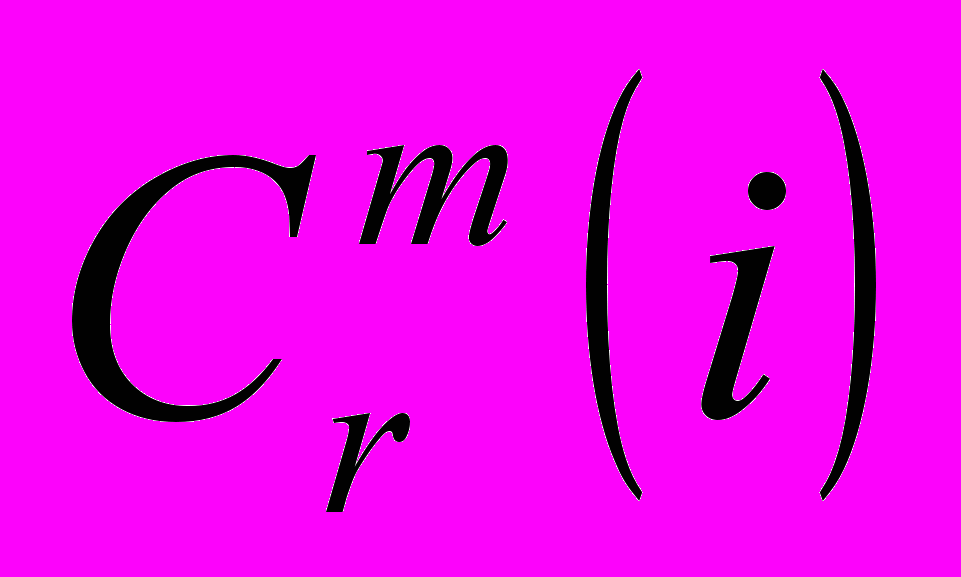 - частота попадания в данную гиперсферу. Аппроксимированная энтропия определяется в виде приращения, получаемого безусловной энтропией
- частота попадания в данную гиперсферу. Аппроксимированная энтропия определяется в виде приращения, получаемого безусловной энтропией 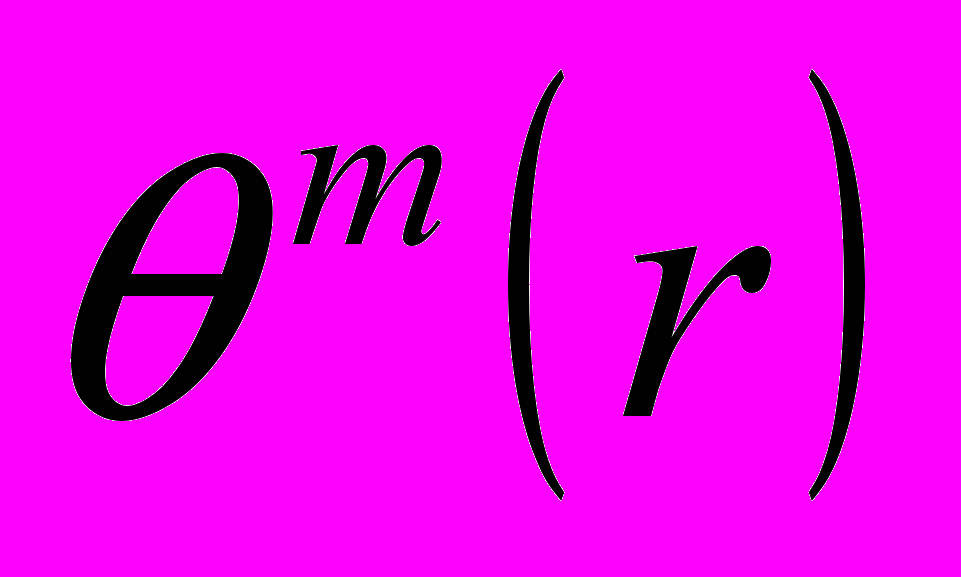 при переходе от последовательности событий длины m к длине m+1: ApEn(m)=[θm(r)- θm+1(r)].
при переходе от последовательности событий длины m к длине m+1: ApEn(m)=[θm(r)- θm+1(r)].Отметим следующие свойства энтропии Шеннона и аппроксимированной энтропии:
- энтропия принимает минимальные значения для абсолютно детерминированного сигнала и максимальное в случае хаотического сигнала;
- из-за повышения вероятности того, что с ростом длины L (или m) цепочки заданной длины будут представлять собой лишь однажды произошедшие события, значения энтропии резко падают при увеличении значений L и m,
- максимальное значение энтропия имеет при длине цепочки L или m равной единице.
Для исключения ложной регулярности, вносимой в оценку условной энтропии Шеннона одиночными цепочками, предложена следующая коррекция ее оценки:
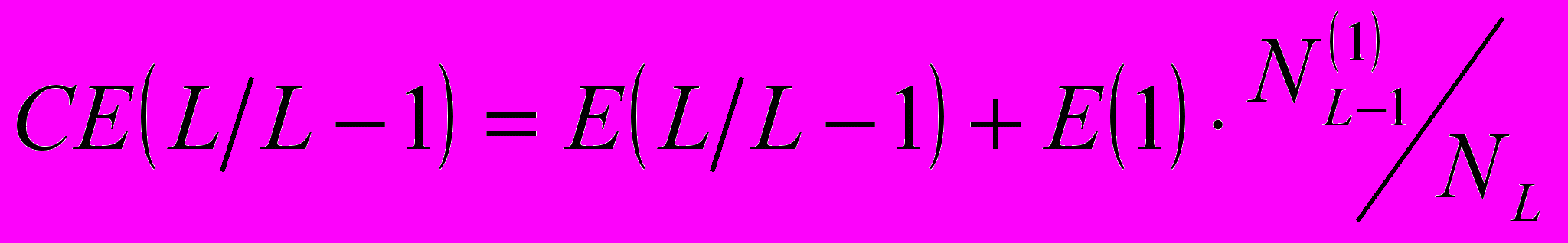 ,
, где
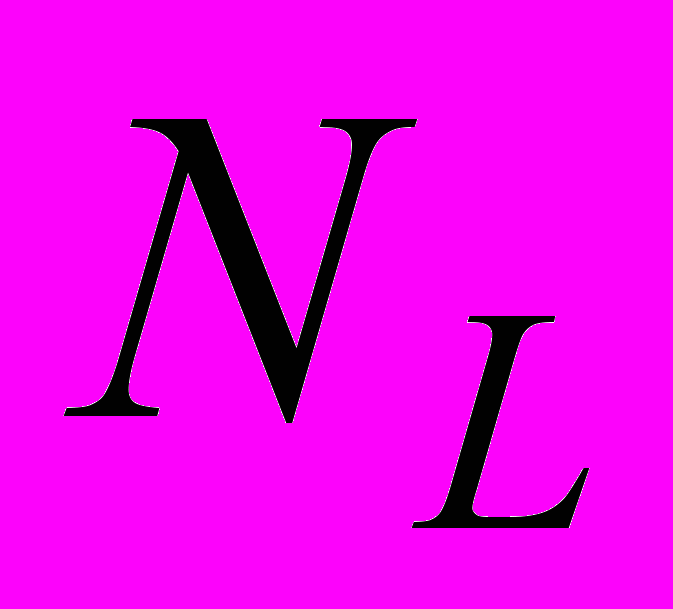 - число анализируемых цепочек символов длины
- число анализируемых цепочек символов длины 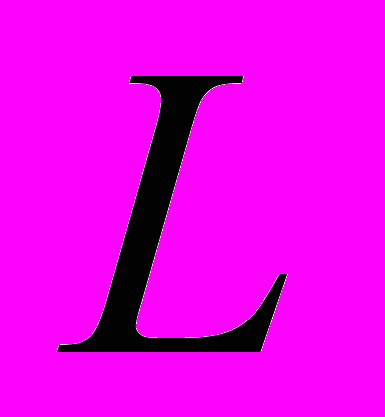 ,
, 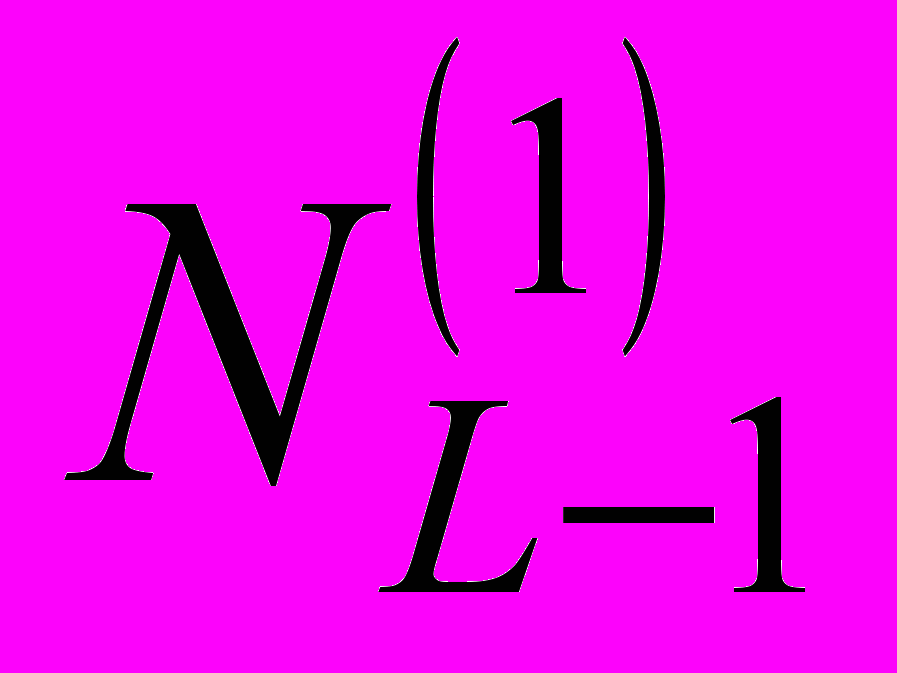 - число лишь однажды встретившихся цепочек символов длины
- число лишь однажды встретившихся цепочек символов длины 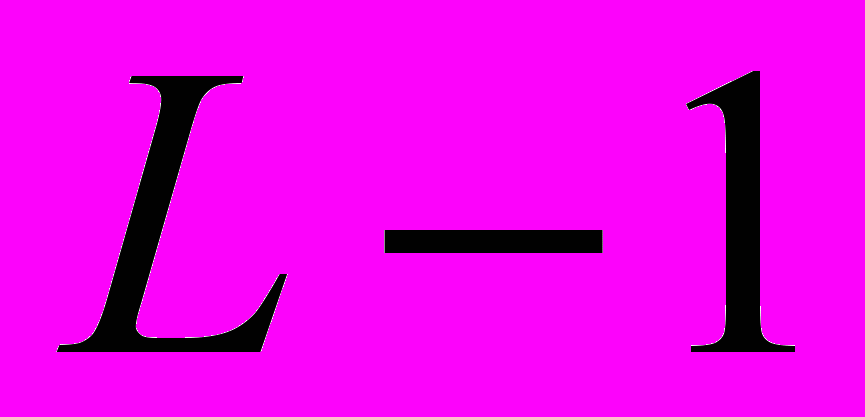 . Аналогичная коррекция вводится и для ApEn. В дальнейшем скорректированные оценки энтропии Шеннона и аппроксимированной энтропии будем обозначать соответственно CE и CApEn (сокращение от Corrected Entropy, Corrected Approximate Entropy). Максимальное значение скорректированные параметры принимают также при единичной длине исследуемой цепочки.
. Аналогичная коррекция вводится и для ApEn. В дальнейшем скорректированные оценки энтропии Шеннона и аппроксимированной энтропии будем обозначать соответственно CE и CApEn (сокращение от Corrected Entropy, Corrected Approximate Entropy). Максимальное значение скорректированные параметры принимают также при единичной длине исследуемой цепочки.Спектральная энтропия
Выше были рассмотрены способы оценки энтропии ЭЭГ-сигнала во временной области. Существует также сравнительно хорошо изученный метод определения спектральной энтропии (СЭ), который был реализован в анализаторе анестезии S/5TM фирмы GE Healthcare Finland (разработчик, Datex-Ohmeda, Хельсинки, Финляндия). Исходным описанием для расчёта спектральной энтропии является спектр сигнала, который может быть получен с использованием дискретного преобразования Фурье [7]. Для получения более устойчивых спектральных оценок в рамках данной работы также применялось усреднение спектра, основанного на использовании БПФ (быстрого преобразования Фурье), а также оценка его методом авторегрессии и скользящего среднего.
После вычисления спектра мощности с помощью функции Шеннона определяется набор величин, соответствующих полученным частотным компонентам. Сумма этих величин и дает значение спектральной энтропии. Спектр мощности ЭЭГ-сигнала в состоянии бодрствования включает более широкий диапазон частот в сравнении с состоянием анестезии. Таким образом результатом анализа спектра мощности с применением функции Шеннона будет низкое значение спектральной энтропии при наркозе, которое будет возрастать одновременно со снижением глубины анестезии и появлением новых частотных компонент. Вычислительный алгоритм позволяет получить число, которое будет масштабно-инвариантной величиной независимо от частоты и амплитуды сигнала [4]. Это достигается благодаря тому, что в процессе вычисления производится нормализация спектра.
ЭЭГ-сигнал, снятый с фронтальных электродов включает значительную электромиографическую (ЭМГ) составляющую, возникающую из-за активности лицевых мышц. Нижние частоты (примерно до 32 Гц) включают преимущественно сигнал ЭЭГ, на более высоких частотах мощность ЭЭГ-составляющей экспоненциально уменьшается. В отличие от этой составляющей, ЭМГ имеет широкий шумоподобный спектр, преобладающий на частотах выше 32 Гц. Как показано в работе [7], наиболее эффективным представляется использование двух частотных диапазонов, которые применимы для вычисления следующих параметров: энтропии состояния (SE) и энтропии отклика (RE). Энтропия состояния вычисляется по части спектра, в которой доминирует ЭЭГ-сигнал (0.8-32 Гц), энтропия отклика – в диапазоне частот от 0.8 до 47 Гц. Она включает область частот, в которой преобладает ЭЭГ-сигнал, а также ЭМГ-диапазон.
Идея применения двух отдельных показателей заключается в том, что каждый из них несет важную информацию о степени активности головного мозга пациента. Показатель SE дает оценку его текущего состояния, при этом кратковременные колебания исключаютя из обработки. Показатель RE реагирует на ЭМГ-активность, а значит, является косвенной оценкой адекватности анальгезии, поскольку ЭМГ-активность может увеличиваться в результате снижения степени анестезии. Исследование проведено отдельно для каждого из спектральных показателей.
Постановка задачи исследования
В работе проведен краткий обзор методов анализа ЭЭГ-сигнала, основанных на использовании показателей энтропии, вычисляемых во временной и частотной областях. Текущим «золотым стандартом» в оценке степени наркоза по ЭЭГ-сигналу является BIS-мониторинг, он используется в 160 странах мира. Значение BIS-индекса может меняться от 0 до 100; уровень 100 соответствует полному сознанию, уровень 0 - отсутствию активности мозга. Такой способ представления данных о глубине наркоза пациента наиболее удобен для врача, и, кроме того, уже опробован в клинической практике. Таким образом, можно сформулировать основные требования к разрабатываемому методу анализа:
- высокая чувствительность;
- низкая межиндивидуальная вариабельность;
- индекс глубины наркоза должен быть представлен в шкале от 0 до 100;
- метод неинвазивный и не должен требовать большого числа электродов.
На основе имеющихся записей электроэнцефалограмм необходимо отобрать наиболее информативные параметры сигнала, рассмотреть способы повышения чувствительности методов анализа, а также оценить возможности их совместного использования.
В данной работе исследовались следующие показатели хаотичности сигнала:
- значение энтропии Шеннона при L = 3, т.е. в той области, где вклад одиночных цепочек незначителен (E(3/2));
- относительный минимум скорректированной энтропии Шеннона (minCE);
- значение аппроксимированной энтропии при m = 2 (ApEn(2));
- относительный минимум скорректированной аппроксимированной энтропии (minCApEn);
- энтропия состояния (SE);
- энтропия отклика (RE).
Показатели с 1 по 4 ранжируются (в процентах) относительно энтропии одиночных событий. Полученные таким образом значения находятся в пределах от 0 (регулярный сигнал) до 100 (хаотический процесс).
Все исследования проводились на выборке данных, включающей 124 5-секундных записей ЭЭГ. Такой размер временного окна был выбран с учетом обеспечения устойчивости спектральных характеристик сигнала, с одной стороны, и достаточной скорости обновления индекса глубины наркоза, с другой. Исследовалось по 2 состояния каждого пациента – бодрствование и глубокий наркоз. В качестве показателя эффективности методов анализа ЭЭГ выбран критерий Фишера J, который принимает максимальное значение в условиях наилучшей классификации двух состояний, и определяется как:
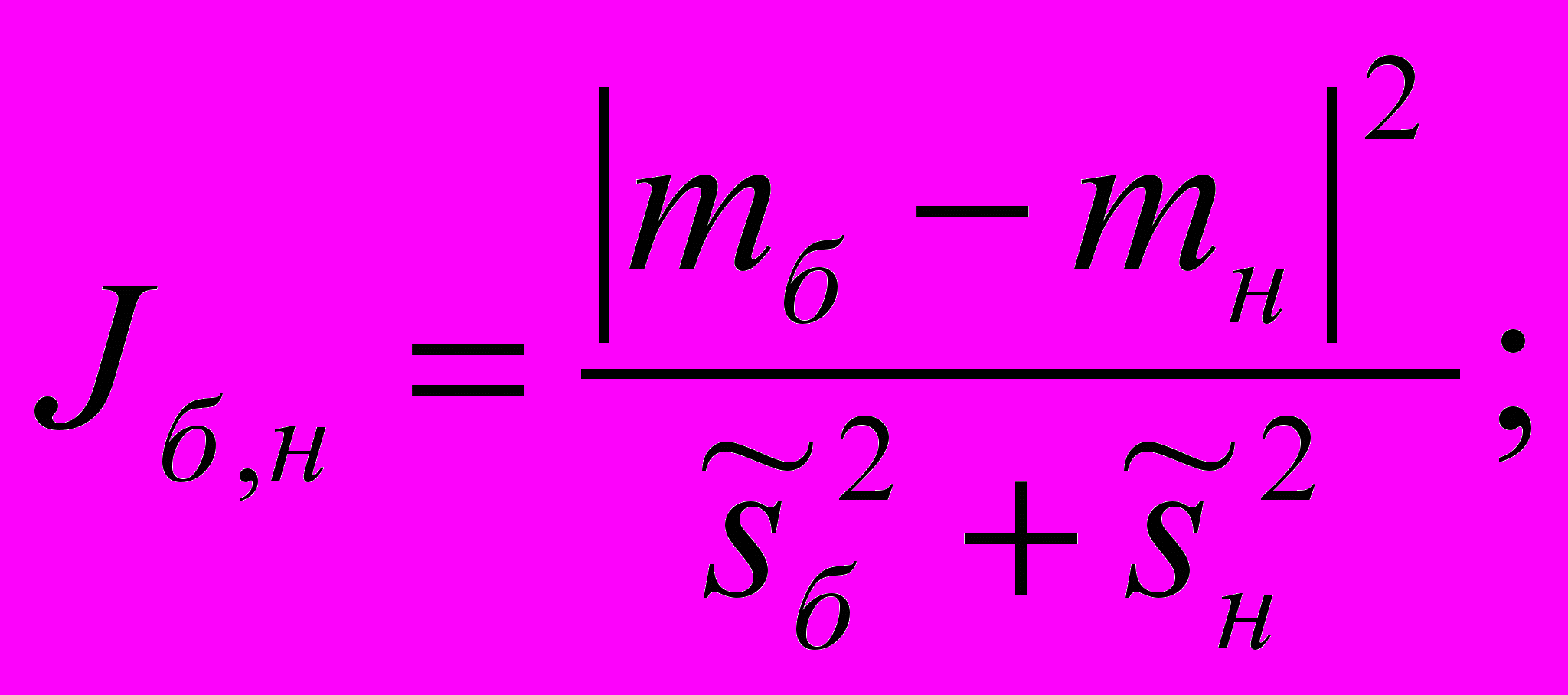
где mб и mн – средние значения вычисляемого параметра энтропии для состояний бодрствования и наркоза соответственно
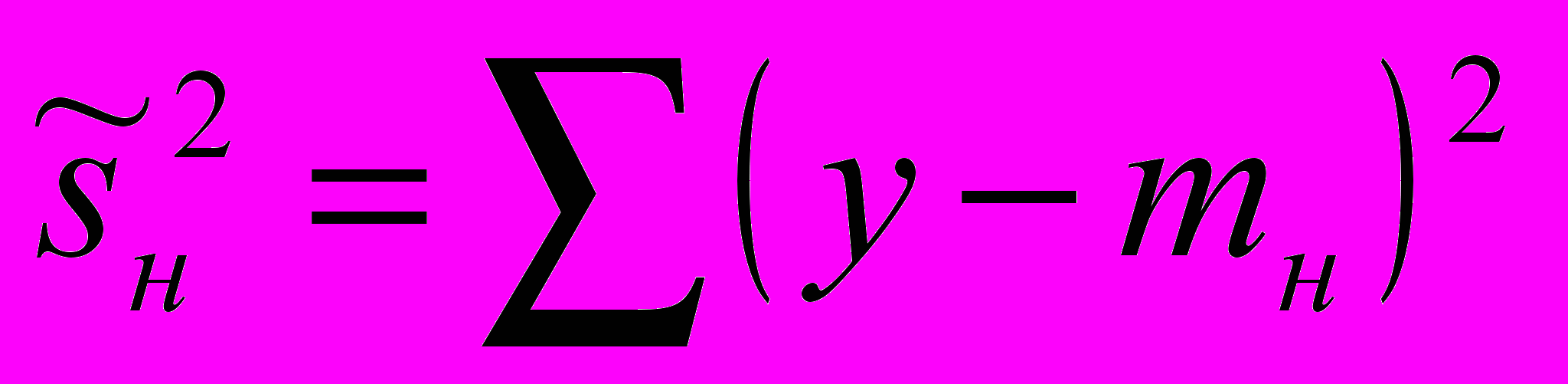 ,
, 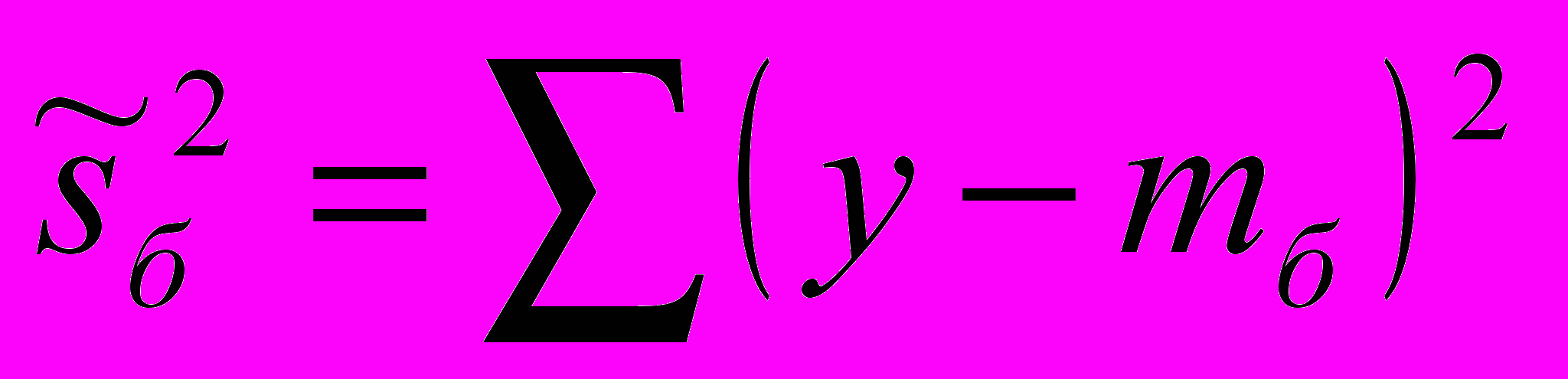 – величина разброса для спроецированных на ось решений выборок
– величина разброса для спроецированных на ось решений выборок 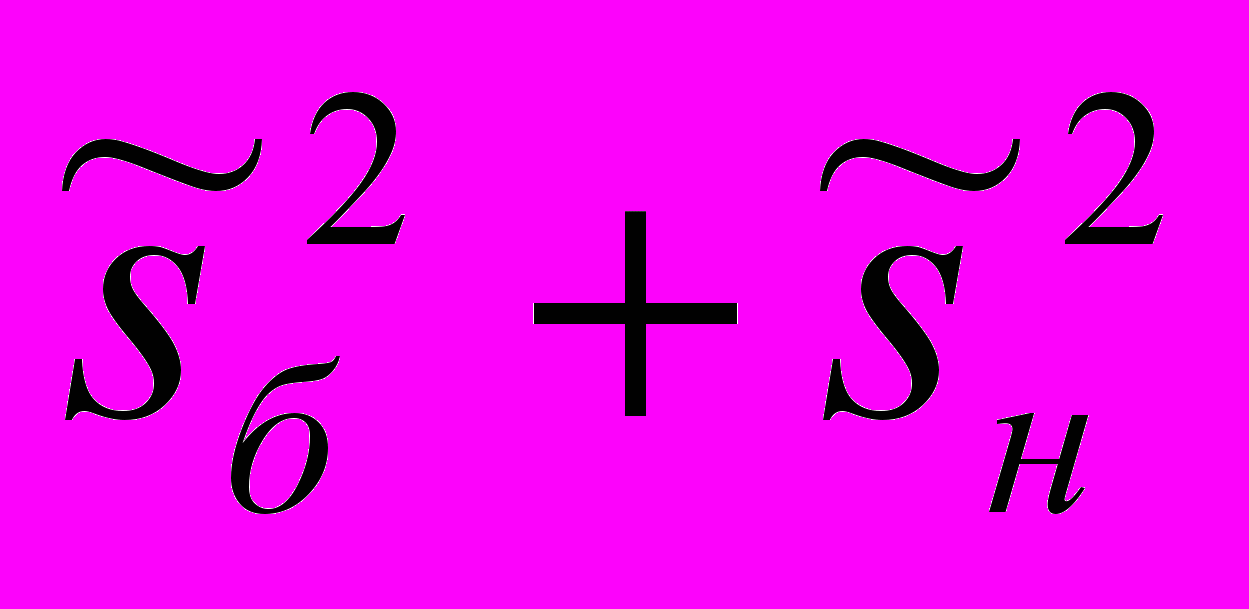 – полный разброс внутри классов [6].
– полный разброс внутри классов [6]. Сравнительный анализ методов оценки энтропии для распознавания стадии глубокого наркоза
В ходе предварительных экспериментов было установлено, что значения оценок энтропии, рассчитываемых во временной области, зависят от ряда параметров, изменение которых влияет на результат распознавания стадии глубокого наркоза. Для энтропии Шеннона это – число интервальных оценок дискретных отсчетов сигнала, а для аппроксимированной энтропии – r, величина порога, определяющего размеры ячеек фазового пространства (Rr∙SDx, r=0.05…0.3, где SDx – стандартное отклонение исходной выборки данных). Физический смысл изменения этих величин состоит в возможности управления размером ячеек фазового пространства. Зависимости коэффициента Фишера J при различных значениях и r представлены на рис. 1.
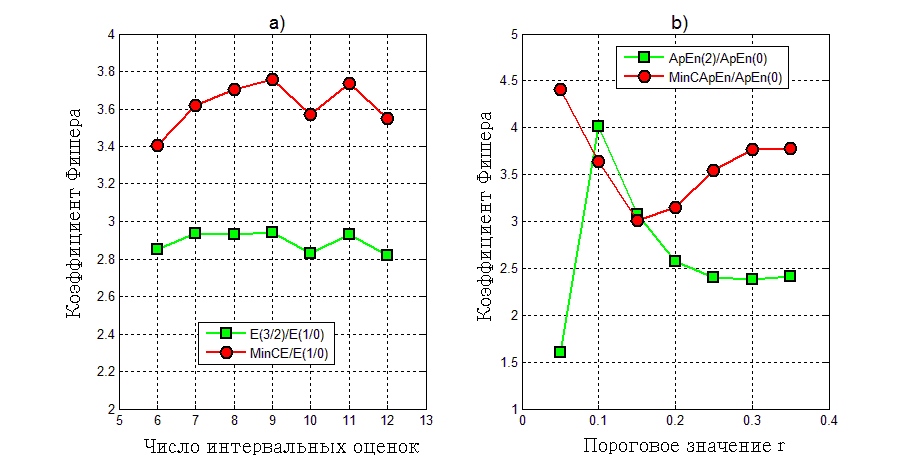
Рисунок 1. Зависимость коэффициента Фишера для временных оценок энтропии: a) энтропии Шеннона при различных значениях числа интервальных оценок ; b) аппроксимированной энтропии при различных значениях порога r
Как видно из графиков полученных зависимостей, в случае анализа энтропии Шеннона наилучший эффект достигается при числе интервальных оценок = 8 или 9, однако для минимума скорректированной энтропии Шеннона коэффициент J принимает большие значения. Анализ зависимости аппроксимированной энтропии позволил выбрать величину порога r=0.1, что обеспечивает наилучшие условия для классификации двух состояний.
Полученные значения коэффициентов J при = 8 и r = 0.1 представлены в таблице 1.
Таблица 1
Значения коэффициентов J для показателей энтропии, вычисляемых во временной области
| Параметр энтропии | E(3/2)/E(1/0) | MinCE/E(1/0) | ApEn(2)/ApEn(0) | MinCApEn/ApEn(0) |
| Значение коэффициента J | 2,85 | 3,78 | 4,07 | 3,74 |
Предварительные исследования показали, что критерии эффективности спектральной энтропии невысоки в сравнении с данными, полученными во временной области. С целью повышения качества оценок спектральной энтропии было проведено исследование в двух направлениях: поиск надежного метода вычисления спектра сигнала и изменение нижней граничной частоты при определении показателей SE и RE. Эти показатели рассчитывались в следующих частотных диапазонах: SE – от f1 до 32 Гц, RE – от f1 до 47 Гц, где f1=3…10 Гц. Рассматривались следующие способы отыскания спектральной плотности мощности (СПМ) (табл. 2, рис. 2):
- быстрое преобразование Фурье (БПФ);
- расчет СПМ по методу Уэлча;
- метод авторегрессии скользящего среднего (АРС).
Таблица 2
Значения коэффициентов J для показателей спектральной энтропии
-
Способ вычисления спектра
Показатель
Нижняя граничная частота f1
3
4
5
6
7
8
9
10
БПФ
SE
0,35
0,71
1,05
1,08
1,40
1,46
1,54
1,75
RE
1,54
2,56
3,24
3,17
3,81
3,98
3,93
4,12
метод Уэлча
SE
0,27
0,70
1,23
1,57
2,15
2,70
2,74
2,86
RE
1,19
2,42
3,49
3,98
4,63
5,59
5,42
5,38
АРС
SE
0,39
0,80
1,39
2,27
3,02
3,75
3,84
4,02
RE
1,52
2,53
3,66
5,10
6,21
6,67
6,82
6,70
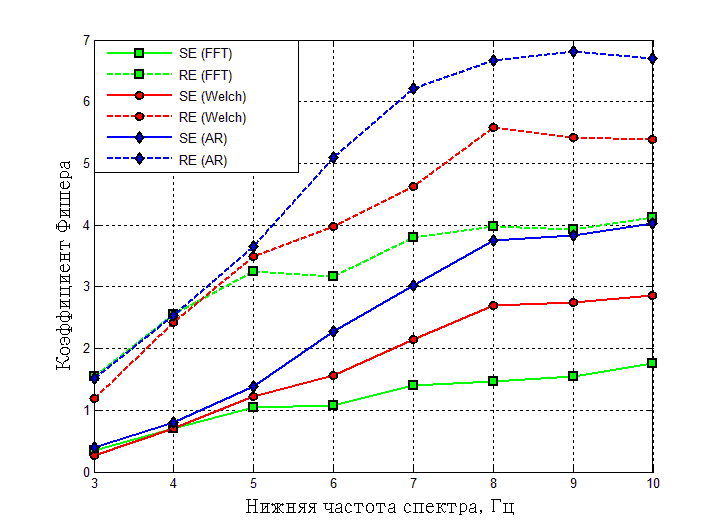
Рисунок 2. Зависимость коэффициента J для показателей спектральной энтропии (SE, RE) в зависимости от нижней частоты оцениваемой части спектра (f1)
Наиболее надежное разделение состояний наркоза и бодрствования получено в результате применения для вычисления СПМ метода авторегрессии скользящего среднего. Нижняя частота анализируемого спектра при этом должна быть равной 6-8 Гц. Во временной области наилучшее значение показателя J получено для нормированной величины аппроксимированной энтропии ApEn(2)/ApEn(0).
Помимо значения J оценкой качества распознавания стадий наркоза может служить величина рассеяния анализируемого показателя относительно некоторой идеальной точки. Согласно данному подходу состояние каждого отдельного пациента может быть представляем точкой на графике, где по оси абсцисс отложено значение индекса анестезии при наркозе, а по оси ординат – в состоянии полного сознания. Как указано выше, за идеальный метод принимается тот, который, при анализе ЭЭГ пациента в стадии глубокого наркоза показывает индекс, близкий к 0, а при бодрствовании близок к 100. Соответственно идеальная точка на полученном графике будет иметь координаты (0, 100).
Среднее рассеяние (СР) при этом будет определяться следующим образом:
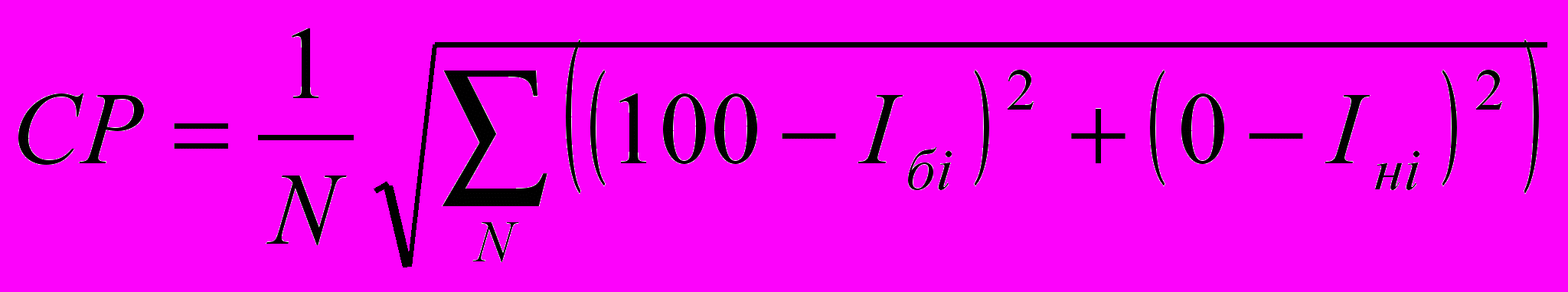 ,
,где N – число пациентов, Iбi и Iнi –значение оцениваемого показателя в состоянии бодрствования и наркоза, соответственно. Выражение
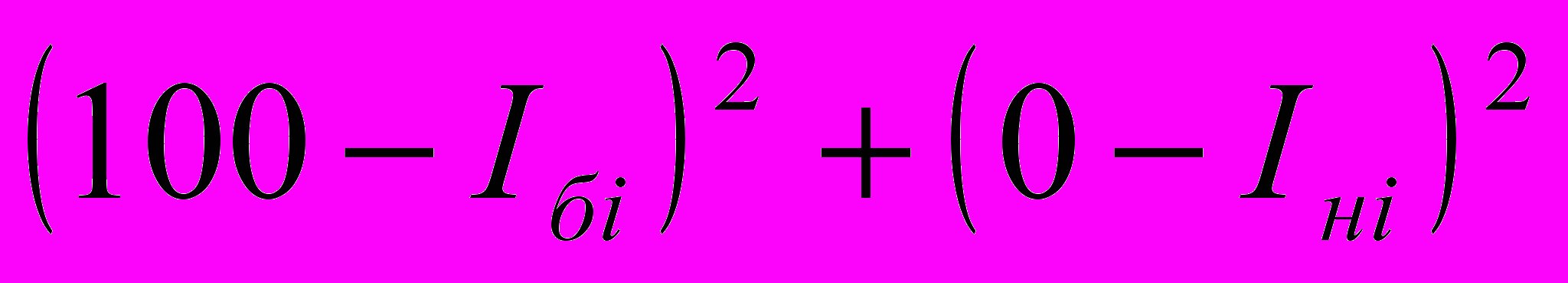 представляет собой квадрат евклидова расстояния от идеальной точки до i-го объекта. Значения СР для исследуемых показателей приведены в табл. 3,4.
представляет собой квадрат евклидова расстояния от идеальной точки до i-го объекта. Значения СР для исследуемых показателей приведены в табл. 3,4.Таблица 3
Значения среднего рассеяния для временных оценок энтропии
-
Метод оценки энтропии
E(3/2)/E(1/0)
MinCE/E(1/0)
ApEn(2)/ApEn(0)
MinCApEn/ApEn(0)
56,8
57,7
60,0
49,7
Таблица 4
Значения среднего рассеяния для спектральных оценок энтропии
| Метод оценки энтропии | |||||
| СЭ БПФ SE | СЭ БПФ RE | СЭ Уэлч SE | СЭ Уэлч RE | СЭ АР SE | СЭ АР RE |
| 81,2 | 76,1 | 87,1 | 81,1 | 88,5 | 82,2 |
Наилучшие результаты в данном исследовании получены для минимума скорректированной аппроксимированной энтропии, а спектральные методы наиболее далеки от «идеальной точки». Как видно из рисунка значения SE при наркозе преимущественно находятся в диапазоне 75-85, при бодрствовании – 85-99; RE при наркозе – 70-80, в сознании – 80-90, что далеко от идеального случая (Рис. 3). Однако, учитывая то, что спектральные методы дают хорошее межклассовое разделение, можно скорректировать получаемый индекс с помощью нелинейного преобразования шкалы отображения результатов.
По результатам анализа можно сделать вывод о том, что наилучшее разделение двух классов бодрствование-наркоз обеспечивают спектральные методы оценки энтропии. При этом нижняя граница оцениваемого спектра должна быть равной равной 6-8 Гц, а при нахождении СПМ сигнала в процессе вычисления спектральной энтропии целесообразно использовать алгоритм БПФ с усреднением по методу Уэлча или вычислять спектр сигнала на основе модели авторегрессии скользящего среднего. Однако для качественного их использование необходимо приведение получаемого индекса к шкале [0 100] с тем, чтобы состоянию наркоза соответствовал диапазон от 40 до 60, что важно для достижения единообразия с распространенным биспектральным индексом BIS.
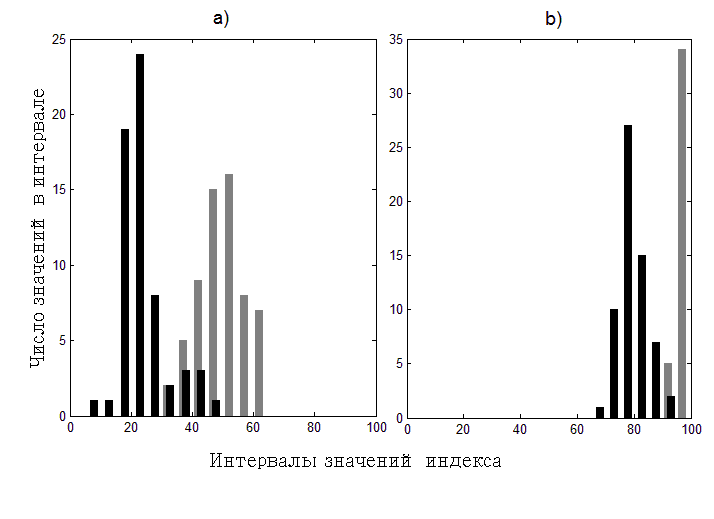
Рисунок 3. Гистограмма, отражающая распределение показателей энтропии: a) ApEn(2)/ApEn(0); b) СЭ АР RE. Черным цветом обозначено распределение для состоянии бодрствования, серым – при наркозе.
Оценки энтропии во временной области также показывают достаточно хорошие результаты, что открывает возможности для их совместного использования со спектральными оценками. Для определения степени статистической взаимосвязи величин, получаемых различными методами, использован коэффициент корреляции. Если для пары показателей он будет близок к единице, это значит, что величины имеют линейную взаимосвязь, и их совместное использование нецелесообразно, т.к. вся полезная информация содержится в значении лишь одной из них. Для оценки взаимозависимости временных и спектральных показателей найдены их попарные коэффициенты корреляции.
Таблица 5
Коэффиценты корреляции между спектральными и временными энтропийными показателями (в сознании;в глубоком наркозе)
| | CE(3/2)/CE(1/0) | MinCE/E(1/0) | ApEn(2)/ApEn(0) | MinCApEn/ApEn(0) |
| СЭ БПФ SE | 0,10; 0,51 | 0,10; 0,49 | 0,10; 0,47 | 0,11; 0,49 |
| СЭ БПФ RE | 0,25; 0,52 | 0,30; 0,52 | 0,29; 0,51 | 0,29; 0,55 |
| СЭ Уэлч SE | 0,27; 0,61 | 0,29; 0,59 | 0,30; 0,55 | 0,28; 0,56 |
| СЭ Уэлч RE | 0,33; 0,64 | 0,39; 0,64 | 0,39; 0,59 | 0,38; 0,62 |
| СЭ АРС SE | 0,35; 0,68 | 0,42; 0,67 | 0,39; 0,61 | 0,38; 0,61 |
| СЭ АРС RE | 0,43; 0,68 | 0,52; 0,70 | 0,50; 0,64 | 0,51; 0,66 |
Анализируя данные табл. 5, можно сделать вывод о том, что в состоянии глубокого наркоза корреляция показателей выше, что объяснимо, учитывая высокую упорядоченность сигнала в этом состоянии. Коэффициент корреляции порядка 0,5 – 0,7 показывает, что линейной или приближенно-линейной зависимости между временными и спектральными показателями не обнаружено, что открывает возможности для исследования возможностей их совместного использования.
Вывод
Понятие энтропии, изначально введенное Шенноном и адаптированное им в качестве меры количества информации, было успешно применено к анализу ЭЭГ. Разнообразные энтропийные алгоритмы были использованы в клинических исследованиях, однако в анализаторе глубины наркоза были применены только методы оценки спектральной энтропии [7]. Анализ временных показателей энтропии показал, что этот подход является перспективным. На выборке данных, состоящей из 124 5-секундных записей ЭЭГ пациентов (в состояниях бодрствования и глубокого наркоза), были проведены исследования эффективности различных энтропийных методик оценки степени хаотичности сигнала. Наилучшие результаты получены при анализе спектральных характеристик, однако при этом важно получать надежную оценку СПМ сигнала. Временные энтропийные характеристики обеспечивают получение устойчивых результатов, слабо коррелированных со спектральными оценками, что открывает возможности для их совместного использования.
Список литературы
- Snow J., On the inhalation of the vapour of either in surgical operations. Churchill, London, 1847.
- Галушка С.В., Лазарев К.В. Практические рекомендации по использованию BIS-монитора во время анестезии. Анналы анестезиологии. ссылка скрыта
- Зенков Л.Р. Клиническая электроэнцефалография (с элементами эпилептологии). – Таганрог: Изд. ТРТУ. – 1996. – 358 с.
- Entropy/ B. Bein. Best Practice & Research Clinical Anaesthesiology. Volume 20, No. 1 – 2006. – P. 101–109.
- Nonlinear Biomedical Signal Processing / Edited by Metin Akay. Volume 2, Dynamic Analysis and Modelling. New York: IEEE . – 2001. – 341 p.
- Немирко А.П., Манило Л.А., Калиниченко А.Н., Волкова С.С.. Энтропийные методы оценки уровня анестезии по ЭЭГ-сигналу. – «Информационно-управляющие системы», №3, 2010
- Description of the EntropyTM algorithm as applied in the Datex-Ohmeda S/5TM Entropy Module / H. Viertio-Oja, V. Maja, M. Sarkela, P. Talja, N. Tenkanen, H. Tolvanen-Laakso, M. Paloheimo, A. Vakkuri, A. Yli-Hankala, P. Merilainen // Acta Anaesthesiol. Scand. – 2004. – V. 48. – P. 154 – 161.
1 Работа выполнялась при финансовой поддержке Федерального агентства по науке и инновациям (госконтракт от 10.03.09 г. №02.522.11.2020) и РФФИ, проекты № 09-01-00501 и № 10-01-00604
