Теоретические и организационные основы управления эпидемическим процессом внутрибольничных инфекций в хирургии 14. 00. 30 эпидемиология 14. 00. 33 общественное здоровье и здравоохранение
| Вид материала | Автореферат |
- Медико-организационные аспекты внутрибольничных инфекций в стационарах хирургического, 378.76kb.
- Академия Кафедра «Общественное здоровье и здравоохранение», 807.94kb.
- Программа по дисциплине «Общественное здоровье и здравоохранение», 120.06kb.
- Примерная программа дисциплины общественное здоровье и здравоохранение Для студентов, 386.71kb.
- Рабочая программа дисциплины общественное здоровье и здравоохранение I. Цели и задачи, 1223.51kb.
- Создание унифицированной системы управления эпидемическим процессом кори, краснухи, 666.42kb.
- Клинико-экономические и организационные основы оказания кардиохирургической помощи, 587.11kb.
- Квалификационный тест по специальности «организация здравоохранение и общественное, 1347.84kb.
- Кафедра организации здравоохранения и управления сестринским делом, 78.62kb.
- Эпидемиология рака желудка в регионе сибири и дальнего востока и иркутской области, 372.04kb.
Таблица 1 - Количественная характеристика наблюдаемых эпидемических ситуаций, связанных с распространением госпитального штамма (1983-2006г.г.)
| Возбудитель | Количество ситуаций | Общее количество человек, вовлеченных в эпидемический процесс | Исследовано штаммов всего |
| Salmonella typhimurium | 5 | 32 | 79 |
| Salmonella infantis | 9 | 324 | 520 |
| Staphylococcus aureus | 44 | 528 | 2698 |
| Enterococcus spp. | 17 | 132 | 317 |
| Pseudomonas aeruginosa | 25 | 238 | 1458 |
| Klebsiella pneumoniae | 12 | 85 | 195 |
| Всего | 112 | 1339 | 5267 |
Самым высоким эпидемическим потенциалом обладала Salmonella typhimurium. Время от появления источника инфекции до колонизации возбудителем больничной среды и инфицированием контактных пациентов не превышало 1 суток. Salmonella infantis в хирургическом корпусе крупной больницы г. Новокузнецка, несмотря на систематические противоэпидемические меры циркулировала в течение десятилетнего периода и вызвала 9 эпидемических эпизодов, с вовлечением в эпидемический процесс 324 пациентов в возрасте старше 18 лет (исследование проведено совместно с И.А. Деминым). Период формирования госпитального штамма не превышал 14 дней с последующим образованием стойкого хронического очага. Самыми многочисленными эпидемическими ситуациями, связанными с формированием и распространением госпитального штамма, были ситуации, обусловленные Staphylococcus aureus, при этом в отдельные периоды заболеваемость стафилококковыми инфекциями области хирургического вмешательства достигала 746±2,34 на 1000 оперированных пациентов. Период формирования госпитального штамма в среднем составил 93 дня, продолжительность циркуляции достигала 8 месяцев и ограничивалась только тогда, когда стационар полностью освобождался от пациентов. Эпидемические ситуации, обусловленные распространением госпитального штамма энтерококков, до 2000 года практически не встречались. Доля энтерококков в общей структуре раневых инфекций в течение многих лет не превышала 2%. В последующие годы ситуация изменилась. Период формирования госпитального штамма составил всего 7 суток, максимальная продолжительность циркуляции - 4 месяца и была равна периоду наблюдения. Pseudomonas aeruginosa отличалась быстрым формированием госпитальных штаммов (средний период составлял 28 дней), циркуляцией в стационаре родственного штамма до 265 дней, высокой скоростью колонизации. Аналогичные характеристики для Klebsiella pneumoniae составили 67 и 35 суток. Кластерный анализ полученных данных выявил близость характеристик Salmonella typhimurium, Pseudomonas aeruginosa и Enterococcus spp. Ко второму кластеру были отнесены Staphylococcus aureus и Klebsiella pneumoniae, к третьему – Salmonella infantis .
Выявленные различия должны быть учтены при организации мониторинга циркулирующих возбудителей с высоким потенциалом формирования госпитальных штаммов, разработке профилактических и противоэпидемических мер.
Скорость формирования госпитальных штаммов зависела от следующих факторов:
- вида возбудителя;
- длительности пребывания пациента в стационаре;
- наличия резистентности к некоторым антибиотикам;
- интенсивности селекционных процессов, определяющихся количеством пациентов с гнойными процессами в стационаре;
- степени однородности пациентов по характеру основной патологии;
- типа стационара;
- вероятности обмена микрофлорой между пациентами.
С целью изучения закономерностей формирования госпитальных штаммов в течение 122-х-дневного периода в хирургическом стационаре Кемеровской областной клинической больницы проводили сплошное проспективное наблюдение за 292 пациентами, 55 из которых имели гнойные процессы преимущественно брюшной полости и подкожной клетчатки. Шестая часть наблюдаемых пациентов в процессе лечения переводились в реанимационное отделение на срок, превышающий 48 часов. Всего в период наблюдения изучен 241 штамм возбудителей.
Анализ структуры возбудителей гнойно-септических инфекций выявил преобладающую циркуляцию энтерококков и синегнойной палочки. Многолетняя динамика энтерококковых и синегнойных инфекций представлена на рис. 3, 4. Выявлена шестилетняя цикличность эпидемического процесса синегнойных инфекций и неблагоприятная тенденция к росту энтерококковых инфекций с 1999 года. Эти закономерности дали основание предполагать, что в наблюдаемом стационаре сформировались и циркулируют госпитальные штаммы именно этих возбудителей.
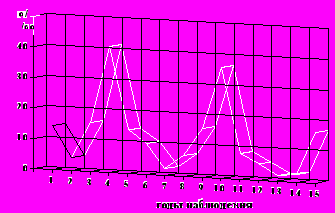
Рисунок 3 - Многолетняя динамика синегнойных инфекций в хирургическом стационаре (1991-2005гг.)
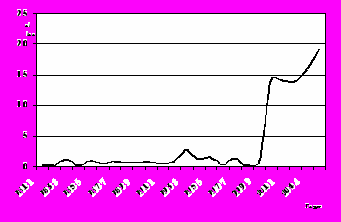
Рисунок 4 - Многолетняя динамика заболеваемости энтерококковыми инфекциями в хирургическом стационаре (1981-2005г.г.)
Изучение разнообразия циркулирующих в хирургическом стационаре госпитальных штаммов энтерококков проводили методом мультилокусного секвенирования-типирования. На протяжении наблюдаемого периода в стационаре циркулировало 5 различных резистенс-типов Enterococcus faecalis и единственный резистенс-тип Enterococcus faecium. Циркулирующие госпитальные штаммы Enterococcus faecium проявляли монотонное однообразие по резистенс-типу в течение наблюдаемого периода, несмотря на смену пациентов в стационаре. Госпитальные штаммы Enterococcus faecalis отличались достаточным разнообразием как по резистенс-типу (5 различных вариантов), так и по генотипу. Эпидемиологический анализ гнойных инфекций у пациентов с сопоставлением генотипов Enterococcus faecalis позволил проследить цепочки суперинфицирования от одного пациента к другому, установить место, время и процедуру, во время которой произошло суперинфицирование пациентов.
Основным источником инфекции являлись больные с гнойными процессами, дополнительным – внешняя среда хирургических стационаров. Инфицирование происходило преимущественно в период пребывания пациентов в реанимационном отделении через контаминированные руки персонала. Длительность циркуляции родственных штаммов энтерококков была равна периоду наблюдения, в то время как циркуляция невзаимосвязанных штаммов ограничивалась периодом пребывания в стационаре источника инфекции. Выявлено распространение родственных штаммов Enterococcus faecium в стационар, территориально не связанный с местом пребывания основного источника инфекции. Штаммы Enterococcus faecalis отличались меньшей контагиозностью, более короткой циркуляцией в стационаре.
Полученные данные свидетельствуют о более высокой эпидемической опасности Enterococcus faecium по сравнению с Enterococcus faecalis.
В качестве интегральных критериев, характеризующих состояние экологической системы, были выбраны 3 параметра:
- коэффициент видового разнообразия микроорганизмов;
- коэффициент разнообразия резистенс-и генотипов;
- средняя продолжительность циркуляции возбудителей.
На начальном этапе формирования экологической системы хирургического стационара, в момент, когда после ремонта произошло заполнение хирургических отделений, было изучено 108 штаммов микроорганизмов, циркулировавших в стационарах. Установлено во всех стационарах, исключая «чистый», высокое видовое разнообразие микроорганизмов (0,7 – 1) и разнообразие резистенс-типов (0,75-1,0). Видовое разнообразие в «чистом» стационаре на начальном этапе бедно (0,3), что объясняется отсутствием источников инфекции среди пациентов. Динамика коэффициентов видового разнообразия (0,33-0,6) и коэффициента разнообразия резистенс-типов микроорганизмов (0,73-0,91) на протяжении всего периода наблюдения оставалась стабильной. В «чистом» стационаре проблема формирования госпитального штамма не имела актуальности, а время циркуляции выделенных штаммов было коротким, при последующем исследовании через 28-30 дней не было зафиксировано ни одного повторения. Критическим параметром для управления эпидемическим процессом должна являться степень антиинфекционной защиты медицинских технологий.
В стационаре с преобладающим типом операций из категории «контаминированные» видовое разнообразие сокращалось только к восьмому периоду наблюдения, но не достигало критических значений. Основным циркулирующим возбудителем являлась Klebsiella pneumoniae, вызвавшая 29,9% всех гнойных инфекций ран и инфекций мочевыводящих путей. Формирование госпитального штамма Klebsiella pneumoniae происходило стремительно, уже к третьему периоду наблюдения разнообразие коэффициента резистенс-типов снижалось до критического уровня и колебалось от 0,1 до 0,28, сохраняясь на этих цифрах вплоть до десятого периода. Повторы идентичных по резистенс-типу микроорганизмов достигали 30% со сроком циркуляции более 90 дней.
В хирургическом отделении №1 (абдоминальная хирургия) выполнялись по классу асептичности «контаминированные» и «инфицированные» оперативные пособия. Наблюдалась интенсивная циркуляция трех возбудителей – энтерококков (14,15%), золотистого стафилококка (12,75%) и синегнойной палочки (13,72%). Конкурентная борьба за экологические ниши уже к седьмому периоду наблюдения привела к широкой циркуляции Enterococcus faecalis (коэффициент разнообразия резистенс-типов 0,44 -1,0) и стафилококков (0,4-1), однако именно этот фактор определял сдерживание скорости формирования госпитальных штаммов этих возбудителей. Параллельно с этими процессами обладающий более высоким эпидемическим потенциалом Enterococcus faecium госпитальный штамм сформировал к седьмому периоду наблюдения (0,25), циркуляция его сохранялась до 150 дней. Госпитальный штамм сформировала и Pseudomonas aeruginosa (0,25), циркуляция идентичного штамма продолжалась до 120 дней. Процессы снижения видового разнообразия и разнообразия резистенс-типов протекали синхронно.
В подобных типах стационаров управление эпидемическим процессом должно предусматривать мониторинг формирования госпитальных штаммов и предотвращение заносов в стационары эпидемических вариантов возбудителей из отделения реанимации и интенсивной терапии. Широко распространенная практика наблюдения больных в раннем послеоперационном периоде в реанимационном отделении в течение нескольких часов (до суток), подменяющего палаты постнаркозного наблюдения, является одним из важнейших условий, способствующих быстрому формированию и распространению госпитальных штаммов.
Реанимационное отделение характеризовалось интенсивной циркуляцией и разнообразием микроорганизмов, высокой скоростью обмена микрофлоры. Эти параметры по нашим данным были в 7 раз выше, чем в других типах отделений. Формирование госпитальных штаммов происходило значительно быстрее, и уже к четвертому периоду можно было наблюдать снижение разнообразия резистенс-типов у Enterococcus faecium (0,13-0,2), Pseudomonas aeruginosa (0,17-0,4). Циркуляция этих идентичных штаммов продолжалась до конца периода наблюдения. Была установлена ведущая роль рук медицинского персонала в поддержании этих процессов и доказано, что в реанимационном отделении происходит инфицирование подавляющего большинства пациентов, лечение которых осложнилось присоединением внутрибольничной инфекции. Снижение разнообразия резистенс-типов до критических значений (0,25-0,33) у Enterococcus faecalis происходило медленнее (к шестому периоду), однако циркуляция идентичных штаммов сохранялась также в течение всего последующего периода наблюдения. Процессы динамики видового разнообразия и разнообразия резистенс- и генотипов текли параллельно. Мониторинг разнообразия микрофлоры в реанимационном отделении, несомненно, должен лежать в основе системы управления эпидемическим процессом. Важнейшим звеном является обеспечение эффективной деконтаминации рук медицинского персонала и предупреждение обмена микрофлорой между реанимационными постами.
Изучение закономерностей распространения эпидемически значимых вариантов возбудителей в пространстве и времени имеет как теоретическое, так и практическое значение, поскольку позволяет прогнозировать интенсивность и характер проявлений эпидемического процесса и своевременно вмешиваться в его ход. Состояние резистентности этих микроорганизмов является критическим параметром для системы надзора и определяет управленческие решения.
Нами изучено на территории Кемеровской области состояние резистентности 12104 выделенных от пациентов штаммов Staphylococcus aureus к оксациллину (данные 2006г.); 3020 штаммов Enterococcus spp. к ванкомицину; 2172 штамма Pseudomonas aeruginosa к ципрофлоксацину; 3849 штаммов Klebsiella pneumoniae к цефтазидиму.
Установлен эпидемический характер распространения устойчивых к ципрофлоксацину штаммов Pseudomonas aeruginosa и Klebsiella pneumoniae к цефтазидиму – доля резистентных штаммов составила 45,72±1,07 и 45,23±0,80 соответственно, но эпидемическое распространение Pseudomonas aeruginosa носило мультифокальный характер в отличие от монофокального (на одной территории) распространения Klebsiella pneumoniae, где она вызвала инфекционный процесс у 1341 пациента. Распространение метициллинрезистентных штаммов стафилококков (MRSA) и ванкомицинрезистентных энтерококков (VRE) имело менее выраженный характер и составило 23,79±0,39и 30,83±0,84 соответственно (рис. 5).
Пятая часть изученных территорий имела эпидемический уровень распространения MRSA. Выявлено преимущественное распространение MRSA на южных территориях Кемеровской области (35,15% в сравнении с 14,98%).
Эпидемический уровень распространения VRE имела почти третья часть (31,38%) изученных территорий. Как и в случае MRSA, у VRE выявлено преимущественное распространение на южных территориях Кемеровской области (37,39% в сравнении с 26,34%).
Почти половина (47%) территорий Кемеровской области имела эпидемический уровень распространения резистентных к ципрофлоксацину Pseudomonas aeruginosa. Не установлено различий между южными и северными территориями Кемеровской области. Это утверждение справедливо и для резистентных к цефтазидиму штаммов Klebsiella pneumoniae, у которых наблюдалась относительная равномерность распространения с эпидемическим уровнем только на одной территории (5,26%).
Наблюдалось существенное различие в распространенности MRSA в различных типах стационаров. В крупных многопрофильных стационарах возбудители с высоким эпидемическим потенциалом были распространены значительно более широко, чем в стационарах общего профиля. Выраженная мозаичность в распространении этих возбудителей наблюдалась и между различными стационарами на одной территории, а также в различных функциональных подразделениях одного стационара.
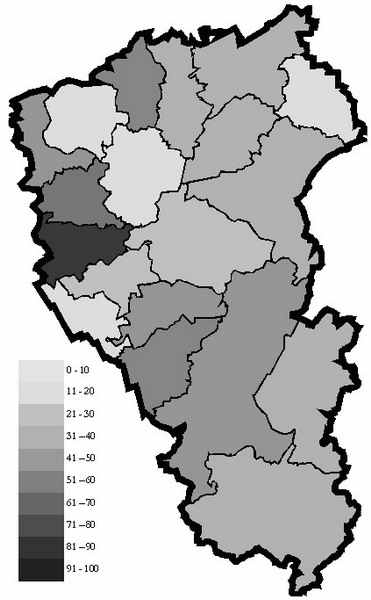
Рисунок 5 - Картограмма распространения устойчивых к метициллину/оксациллину Staphylococcus aureus в 2006г. в Кемеровской области (%)
Установлено преимущественное распространение MRSA в монопрофильных хирургических стационарах по сравнению с многопрофильными (71,54±3,15% и 17,67±0,43%, p<0,01). Аналогичная, но менее выраженная зависимость наблюдалась и у устойчивых к ципрофлоксацину Pseudomonas aeruginosa (58,5± 2,65% и 46,24±1,4%, p<0,01). Что же касается других возбудителей, то подобной зависимости у VRE (25,8±5,56% и 23,57±1,29%, p>0,05), и устойчивой к цефтазидиму Klebsiella pneumoniae (59,74±5,59% и 61,70±0,99%) не наблюдалось.
В существующей на настоящий момент системе эпидемиологического надзора в качестве информационных параметров, отражающих состояние эпидемического процесса внутрибольничных инфекций и используемых в цикле управления, приняты заболеваемость (инцидентность), летальность, частота нестерильных проб материалов, частота нестандартных проб смывов с объектов больничной среды и воздуха, частота нестандартных тестов и проб, контролирующих процесс дезинфекции.
Однако, совершенно очевидно, что показатели заболеваемости и летальность не могут удовлетворять требованиям, предъявляемым к информационным параметрам, т.к. они являются выходными параметрами. Цель управления – обеспечить стабильное поддержание выходных параметров в заданных пределах. Подтверждающими аргументами служат следующие положения:
- проявлениями эпидемического процесса являются не только манифестные, но и бессимптомные, и скрыто протекающие формы инфекции, в том числе и колонизация пациентов госпитальным штаммом, и суперинфицирование. По нашим данным соотношение манифестных и скрыто протекающих форм в хирургических стационарах достигала 1:30. При мониторировании хирургического стационара №1 были выявлены следующие закономерности: на 1 манифестную форму гнойной инфекции раны, вызванной Staphylococcus aureus, приходилось 30 случаев колонизации без клинических проявлений. Для Pseudomonas aeruginosa это соотношение составило 1:12; для Klebsiella pneumoniae – 1:20; для Enterococcus spp. – 1: 8. Соотношение вспышек и спорадических форм составляло 11:100. Таким образом, используя в качестве основного информационного параметра заболеваемость (инцидентность), и определяя в качестве базиса системы эпидемиологического надзора регистрацию манифестных форм, мы оставляем вне внимания 96,8% других проявлений эпидемического процесса (при соотношении манифестных и скрытых форм 1:30 на долю манифестных форм приходится в структуре 3,2%).
- Развитие манифестной формы происходит в среднем через 5-10 дней от момента инфицирования. По нашим данным самый короткий инкубационный период (от нескольких часов до двух суток) наблюдается при развитии гнойной инфекции, вызванной гемолитическим стрептококком и анаэробными бактериями. Средняя величина находится в интервале от пяти до десяти суток и типична для инфекции, вызванной золотистым стафилококком, кишечной палочкой, клебсиеллой и др. Продолжительный инкубационный период – до 45 суток мы наблюдали при гнойной инфекции области хирургического вмешательства, вызванной эпидермальным стафилококком. Развитие постимплантационной инфекции может быть отсрочено до года. Следует иметь в виду также и то обстоятельство, что раневая инфекция может быть вызвана ассоциацией микроорганизмов. Следовательно, регистрируемая манифестная форма отражает события, давность которых исчисляется в среднем 5-10 днями.
- Отсутствие нормативного документа, определяющего стандарт случая внутрибольничной инфекции, приводит к регистрации псевдослучаев с одной стороны и отсутствию регистрации части случаев (суперинфицирование, например), с другой стороны.
- Летальность отражает в большей степени качество оказания медицинской помощи, исходную тяжесть состояния пациента, и в меньшей – интенсивность проявлений эпидемического процесса. Как и заболеваемость (инцидентность), летальность относится к числу выходных параметров, стабильность и колебание уровня которых в заданных пределах должна обеспечивать система управления.
При обосновании и выборе информационных параметров учитывали, что:
- структура внутрибольничного инфицирования предполагает экзогенные, эндогенные инфекции и инфекции, обусловленные формированием госпитального штамма;
- интенсивность проявлений эпидемического процесса, его формы, закономерности развития определяются степенью агрессии и инвазии лечебно-диагностического процесса;
- в эпидемическом процессе внутрибольничных инфекций участвуют популяции микро- и макроорганизмов.
Процесс формирования госпитального штамма имеет протяженность во времени и начинается задолго до того, как появляются первые манифестные формы инфекций. Оптимальными информационными параметрами, отражающими состояние микробной популяции, и позволяющими упреждающе вмешиваться в эпидемический процесс по нашему убеждению являются
- коэффициент видового разнообразия микроорганизмов;
- коэффициент разнообразия резистенс-типов (генотипов) для микроорганизмов, имеющих высокий эпидемический потенциал (метициллин/оксациллинрезистентный Staphylococcus aureus, резистентные к ципрофлоксацину Pseudomonas aeruginosa, резистентные к цефтазидиму Klebsiella pneumoniae, резистентные к ванкомицину Enterococcus spp.);
Критическим значением параметра является коэффициент разнообразия менее 0,4. Основанием для вмешательства в ход эпидемического процесса является стабильная тенденция к снижению видового и типового разнообразия микроорганизмов, циркулирующих у пациентов.
Информационными параметрами, отражающими вероятность экзогенного инфицирования, могут служить
- стерильность применяемых материалов;
- степень антиинфекционной защиты медицинских технологий.
Степень антиинфекционной защиты медицинских технологий является интегральной величиной. Однако именно этот параметр наиболее точно отражает вероятность экзогенного инфицирования. Для введения этого параметра требуется предварительная разработка и утверждение на уровне органа управления здравоохранением субъекта РФ стандартов обеспечения антиинфекционной защиты медицинских технологий. Такого рода стандарт предусматривает детальный перечень применяемых материалов и порядок выполнения технологии, который, по мнению экспертов, максимально снизит риск экзогенного инфицирования. Наш опыт разработки и внедрения подобных стандартов подтверждает их эффективность. Так, частота суперинфицирования пациентов после внедрения стандарта антиинфекционной защиты при выполнении процедур в перевязочном кабинете не превышала 4,25±1,79 на 1000 перевязок, выполненных пациентам с гнойными ранами, до внедрения – 62,71±6,74 на 1000 (р<0,01). Методика оценки предусматривает наличие расчета необходимых материалов и инструментов при выполнении каждого вида процедур, операций, пособий и последующее сравнении суммарной фактической обеспеченности с расчетной, выраженное в процентах. Критическим значением параметра является отклонение от 100% на величину 10%.
Информационными параметрами, отражающими степень защиты медицинского персонала от инфицирования, могут служить
- степень антиинфекционной защиты медицинского персонала;
- охват вакцинацией против вирусного гепатита В, дифтерии и др. инфекций.
Критическое значение этих параметров – менее 99%.
Эндогенное инфицирование в большей степени отражено в показателе риска развития инфекции. Информационным параметром может служить величина предотвращенного риска развития инфекции. Критические значения для операций низкого риска – 100%, для операций среднего риска – 97%, для операций высокого риска – 93%.
Риск развития инфекции имеет прямую зависимость от степени агрессии лечебно-дигностического процесса. Информационным параметром, отражающим его, является удельный вес высоко агрессивных вмешательств в общей структуре применяемых медицинских технологий. Для каждого типа хирургического стационара перечень высоко агрессивных вмешательств индивидуален и определяется экспертами. Критическим значением является отсутствие снижения или возрастание агрессии.
Информационным параметром, отражающим риск развития манифестных форм внутрибольничной инфекции, являются сведения о температурящих больных (критическое значение – 380С и выше).
Основной целью аналитического цикла является своевременная диагностика формирования и распространения госпитального штамма, оценка степени антиинфекционной защиты медицинских технологий и агрессии лечебно-диагностического процесса, диагностика риска развития манифестных форм внутрибольничных инфекций.
Сведения об основных информационных параметрах поступают госпитальному эпидемиологу, основной функцией которого является эпидемиологическая диагностика и разработка профилактических и противоэпидемических мер, адаптированных к условиям конкретного стационара. Критические значения выходных параметров (инцидентность, плотность инцидентности, превалентность, летальность) по нашему опыту необходимо определять с помощью метода экспертных оценок. При этом при обработке материалов коллективной экспертной оценки используются методы теории ранговой корреляции. Для количественной оценки степени согласованности мнений экспертов применяется коэффициент конкордации.
Существующие различия стационаров как по медицинских технологиям, так и по структуре пациентов, условиям размещения и т.д. не позволяют задавать на данном этапе единые значения выходных параметров. Решаемые на каждом этапе цели и задачи должны быть индивидуальны для разного типа стационаров.
Формализованные сведения от госпитальных эпидемиологов поступают главному госпитальному эпидемиологу департамента здравоохранения субъекта РФ, анализируются, интегрируются в общую систему управления здравоохранением и служат основой для создания целевых долгосрочных программ, а также немедленных мер в случае необходимости. Механизмом управления служит включение критических параметров, влияющих на эпидемический процесс внутрибольничных инфекций в модель конечных результатов деятельности лечебно-профилактического учреждения. Выбор параметров при этом осуществляется экспертами.
Кроме того, в процессе сертификации ЛПУ экспертами на основании действующего законодательства и нормативных актов с применением соответствующей методики проводится оценка инфекционной безопасности больничной среды и санитарно-гигиенических условий в ЛПУ. Она включает экспертизу:
- заболеваемости внутрибольничными инфекциями;
- антиинфекционной защиты медицинских технологий;
- санитарно-гигиенических условий размещения пациентов;
- защиты медицинского персонала от инфицирования и вредного воздействия факторов больничной среды;
- системы сбора, хранения и удаления отходов лечебно-профилактического учреждения.
Важнейшими направлениями в управлении ситуацией по внутрибольничным инфекциям по нашему мнению являются:
- организация и обеспечение информационных потоков;
- внедрение современных информационных технологий системы сбора, учета, хранения и передачи информации, ориентированных как на сплошной учет случаев внутрибольничных инфекций, так и на проведение выборочной углубленной эпидемиологической оценки отдельных ее форм;
- эпидемиологический анализ заболеваемости;
- эпидемиологическая оценка медицинских технологий и минимизация риска инфицирования;
- организация системы мер, направленных на снижении агрессии лечебно-диагностического процесса;
- обеспечение высокого уровня антиинфекционной защиты медицинских технологий;
- мониторинг основных возбудителей внутрибольничных инфекций и надзор за резистентностью;
- рациональная стратегия и тактика применения антимикробных средств;
- внедрение принципа «индивидуальной изоляции» при выполнении медицинских технологий с высоким риском инфицирования;
- разработка и внедрение стандартов выполнения лечебно-диагностических манипуляций;
- экономический анализ и оптимизация финансовых затрат на обеспечение инфекционной безопасности;
- разработка и внедрение долгосрочных программ профилактики внутрибольничных инфекций.
Реализация этих направлений позволяет эффективно контролировать эпидемическую ситуацию в хирургических стационарах, значительно снизить заболеваемость и экономические потери от внутрибольничных инфекций.
Научно обоснованный нами и внедренный в практику новый концептуальный подход к управлению эпидемическим процессом внутрибольничных инфекций в хирургических стационарах, заключающийся в интеграции эпидемиологической оценки инфекционной безопасности больничной среды в общую систему управления обеспечением качества медицинской и лекарственной помощи населению доказал высокую эффективность.
Разработанная в Кемеровской области система управления обеспечением качества медицинской и лекарственной помощи с использованием стандартов медицинских технологий и стандартов материально-технического обеспечения с учетом уровней и этапов медицинского обслуживания позволяет учесть мнение пациентов, дать объективную оценку доступности медицинской помощи, профессионализму медицинских работников, состоянию материально-технической базы, инфекционной безопасности больничной среды и санитарно-гигиеническим условиям в лечебно-профилактическом учреждении, лекарственному обеспечению, соблюдению этических и деонтологических норм медицинским персоналом, адекватности медицинской помощи, деятельности ЛПУ на фоне объемов финансирования и эффективности использования ресурсов лечебно-профилактического учреждения.
Интегральная оценка эффективности управления системой обеспечения качества в лечебно-профилактических учреждениях включает оценку удовлетворенности пациента качеством медицинской помощи; углубленную объективную оценку качества медицинской помощи; оценку эффективности использования ресурсов и оценку финансирования.
Основной построения системы являются:
- унификация информационной системы;
- стандартизация информации (применение стандарта случая);
- создание регистра медицинских технологий;
- разработка стандартов антиинфекционной защиты медицинских технологий;
- определение критических (индикаторных) параметров эпидемического процесса и интегральных параметров оценки качества антиинфекционной защиты лечебно-диагностического процесса;
- интродукция в систему медицинского страхования параметров, характеризующих степень антиинфекционной защиты лечебно-диагностического процесса;
- интродукция в общую систему управления здравоохранением параметров, характеризующих степень антиинфекционной защиты лечебно-диагностического процесса;
- унификация обучения медицинского персонала созданием учебно-методического центра на базе государственных образовательных учреждений высшего и среднего профессионального образования
- дифференцированный подход к управлению эпидемическим процессом в различных типах ЛПУ;
- создание организационной основы управления, включающей главных специалистов регионального, муниципального, районного уровней, систему госпитальных эпидемиологов ЛПУ;
- наличие региональной программы профилактики, экспертного совета, внутриучрежденческих комитетов по профилактике внутрибольничных инфекций;
- экспертиза соответствия антиинфекционной защиты медицинских технологий, обеспечения безопасности пациентов и персонала в системе сертификации.
Согласно данным страховых медицинских организаций уровень качества лечения в пилотных лечебно-профилактических учреждениях стабилизировался на уровне 0,96-0,97. Затраты на оказание стационарной помощи сократились на 15,0-22,6%.
ВЫВОДЫ
1. Эпидемический процесс внутрибольничных инфекций в хирургических стационарах и его эволюция определяются медицинскими технологиями, их интенсивностью и агрессией, свойствами циркулирующих возбудителей, условиями функционирования стационаров, действующими моделями организации и управления качеством оказания медицинской помощи, эффективностью эпидемиологического надзора. Выявлена устойчивая тенденция к снижению заболеваемости с нерегулярными колебаниями. Тенденции проявлений эпидемического процесса в крупных специализированных многопрофильных стационарах определялись формированием и распространением эпидемических (госпитальных) штаммов возбудителей, а в стационарах общего профиля с числом хирургических коек до 60 - преимущественно экзогенным компонентом. Выявлена 6-летняя цикличность эпидемического процесса синегнойных инфекций и выраженная тенденция к росту энтерококковых инфекций.
2. Установлено, что в 92,2% всех случаев инфицирование происходило в высокотехнологичных специализированных и крупных многопрофильных стационарах. Максимальный риск внутрибольничных инфекций выявлен для монопрофильного хирургического специализированного стационара (28,37±0,08 на 1000 оперированных пациентов), достигающий 237,93±0,15 на 1000 оперированных пациентов с превалентностью 485,61±0,22. В многопрофильной хирургической клинике риск внутрибольничных инфекций в 2 раза ниже (15,18±0,06 на 1000 пациентов). В хирургических стационарах общего типа (уровень центральных районных больниц) - 6,09±0,04 на 1000 пациентов с колебаниями в пределах 2,65 – 9,52. Минимальные показатели инцидентности внутрибольничных инфекций зарегистрированы в амбулаторно - поликлинических учреждениях – 0,6 ± 0,07 на 1000 посещений. Соотношение инцидентности внутрибольничных инфекций в разных типах лечебно-профилактических учреждений хирургического профиля составило 48:26:10: 1.
3. Заболеваемость инфекциями медицинских работников в 25 раз выше официально зарегистрированной заболеваемости с временной утратой трудоспособности (144,20±9,46 на 1000), в 2,9 раза выше (p<0,05) по сравнению с основным населением. Превалентность вирусного гепатита В (16,04± 0,71) в 10 раз , а вирусного гепатита С (15,29±0,69) в 4,9 раза выше превалентности у населения. При сравнении инцидентности внутрибольничных инфекций у медицинского персонала и пациентов установлено, что эти инфекции у персонала встречаются как минимум в 9,5 раз чаще (p<0,05).
4. Молекулярно-генетическими исследованиями установлено, что инициация и первичное формирование госпитальных штаммов возбудителей преимущественно происходит в отделении реанимации и интенсивной терапии с последующим распространением в другие отделения. Выявлена гетерогенность возбудителей по эпидемическому потенциалу и скорости формирования госпитальных штаммов в зависимости от рода и вида. К кластеру с самым высоким эпидемическим потенциалом относятся Salmonella typhimurium, Pseudomonas aeruginosa и Enterococcus spp. При этом степень эпидемической опасности выше у Entercoccus faecium в сравнении с Enterococcus faecalis. По мере убывания эпидемического риска формирования госпитальных штаммов ко второму кластеру отнесены Staphylococcus aureus и Klebsiella pneumoniae. К третьему кластеру – Salmonella infantis.
5. В стационарах с преобладающим по асептичности типом «чистых» операций процессы снижения видового разнообразия и формирования госпитального штамма не синхронизированы. Критическим параметром для управления эпидемическим процессом является степень антиинфекционной защиты медицинских технологий. В хирургическом стационаре с преобладающим типом операций категории «контаминированные» на фоне медленного сокращения видового разнообразия типичен эксплозивный тип формирования и стремительного распространения госпитального штамма возбудителя. В хирургическом стационаре, выполняющем по классу асептичности одновременно «контаминированные» и «инфицированные» оперативные пособия, процессы снижения видового разнообразия и разнообразия резистенс-типов протекают синхронно. В подобных типах стационаров управление эпидемическим процессом должно предусматривать мониторинг формирования госпитальных штаммов и предотвращение заносов в стационары эпидемических вариантов возбудителей из отделения реанимации и интенсивной терапии.
6. Выявлена мозаичность территориального распространения эпидемических вариантов возбудителей внутрибольничных инфекций. Установлен эпидемический уровень циркуляции фторхинолонрезистентных штаммов Pseudomonas aeruginosa и β- лактамазопродуцирующих Klebsiella pneumoniae – доля резистентных штаммов составила 45,72±1,07 и 45,23±0,80 соответственно. Эпидемическое распространение Pseudomonas aeruginosa носило мультифокальный характер в отличие от монофокального распространения Klebsiella pneumoniae. Частота метициллинрезистентных штаммов стафилококков и ванкомицинрезистентных энтерококков составила 23,79±0,39 и 30,83±0,84 соответственно с преимущественным распространением на южных территориях Кемеровской области. Установлено преобладание MRSA в монопрофильных хирургических стационарах по сравнению с многопрофильными (71, 54 ± 3,15% и 17,67 ± 0,43%, p<0,01). Аналогичная, но менее выраженная зависимость наблюдалась и у устойчивых к ципрофлоксацину Pseudomonas aeruginosa (58,5± 2,65% и 46,24±1,4%, p<0,01).
7. Высоко чувствительными (97%) и специфичными (98%) информационными параметрами, отражающими состояние микробной популяции и позволяющими упреждающе вмешиваться в эпидемический процесс, являются коэффициент видового разнообразия микроорганизмов; коэффициент разнообразия резистенс-типов (генотипов) для микроорганизмов, имеющих высокий эпидемический потенциал (метициллин/оксациллинрезистентный Staphylococcus aureus, резистентные к ципрофлоксацину Pseudomonas aeruginosa, резистентные к цефтазидиму Klebsiella pneumoniae, резистентные к ванкомицину Enterococcus spp.), которые должны лежать в основе системы мониторинга. Критическим значением параметра является коэффициент разнообразия менее 0,4. Основанием для вмешательства в ход эпидемического процесса является стабильная тенденция к снижению видового и типового разнообразия микроорганизмов, циркулирующих у пациентов.
8. Информационными параметрами, отражающими вероятность экзогенного инфицирования, служат стерильность применяемых материалов и степень антиинфекционной защиты медицинских технологий. Стандартизация антиинфекционной защиты медицинских технологий является высоко эффективной мерой управления экзогенным компонентом эпидемического процесса внутрибольничных инфекций, позволяющим снизить риск инфицирования до 15 раз.
9. Разработана концептуальная модель управления эпидемическим процессом внутрибольничных инфекций. Механизмом управления служит включение критических параметров, влияющих на эпидемический процесс внутрибольничных инфекций в модель конечных результатов деятельности лечебно-профилактического учреждения.
10. Разработанная в Кемеровской области система управления обеспечением качества медицинской и лекарственной помощи с использованием стандартов медицинских технологий и стандартов материально-технического обеспечения с учетом уровней и этапов медицинского обслуживания позволяет учесть мнение пациентов, дать объективную оценку доступности медицинской помощи, профессионализму медицинских работников, состоянию материально-технической базы, инфекционной безопасности больничной среды и санитарно-гигиеническим условиям в лечебно-профилактическом учреждении, лекарственному обеспечению, соблюдению этических и деонтологических норм медицинским персоналом, адекватности медицинской помощи, деятельности ЛПУ на фоне объемов финансирования и эффективности использования ресурсов лечебно-профилактического учреждения. Согласно данным страховых медицинских организаций уровень качества лечения в пилотных лечебно-профилактических учреждениях стабилизировался на уровне 0,96-0,97. Затраты на оказание стационарной помощи сократились на 15,0-22,6%.
