Министерство образования и науки РФ московский государственный открытый университет Научно-образовательный материал
| Вид материала | Литература |
- Министерство образования и науки РФ московский государственный открытый университет, 705.26kb.
- Московский государственный открытый университет Научно-образовательный материал, 891.3kb.
- Московский государственный открытый университет Научно-образовательный материал, 695.01kb.
- Министерство образования и науки Российской Федерации государственное образовательное, 597.33kb.
- Министерство образования и науки российской федерации московский государственный университет, 75.5kb.
- Министерство образования и науки, 38.9kb.
- Министерство образования и науки РФ государственное образовательное учреждение высшего, 72.81kb.
- Дорожный Государственный Технический Университет (мади) Научно-образовательный материал, 127.07kb.
- Отчет по преддипломной практике гуп ппп «Типография «Наука», 3768.53kb.
- Программа 1-3 октября 2003 года Москва Организаторы и спонсоры Министерство образования, 141.3kb.
4.1. Фотохимический (сухой, Лос-анджелесского типа) смог
Возникает в больших городах с высокой плотностью транспорта. Формируется в атмосфере под действием солнечного света при отсутствии ветра и при низкой влажности из компонентов, характерных для выхлопных газов автомобилей.
Под действием ультрафиолетового излучения Солнца оксиды азота и углеводороды вступают между собой в фотохимические реакции и образуют агрессивный фотохимический смог (рис. 1), содержащий озон и другие сильные окислители – пероксиацетилнитраты (ПАН), альдегиды, кетоны и другие вредные вещества, характеризующиеся раздражающим (глаза, верхние дыхательные пути) и аллергическим действием.
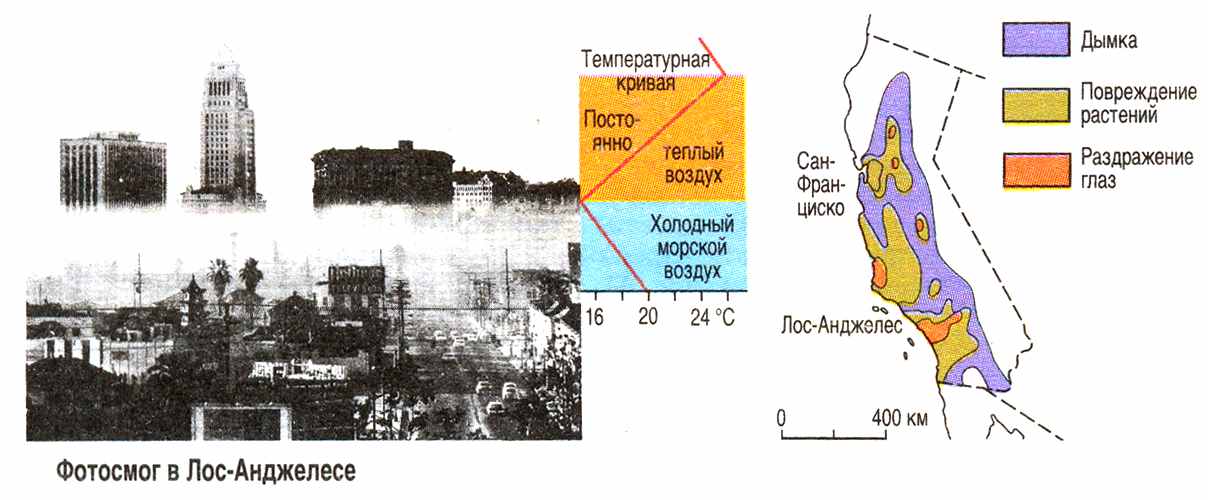
Рис. 1. Смог и его воздействие
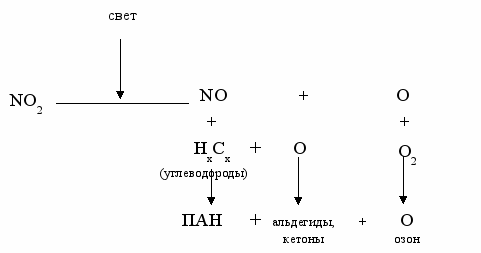
Рис. 2. Фотохимические реакции в воздухе в присутствии углеводородов
(Небел Б., 1943)
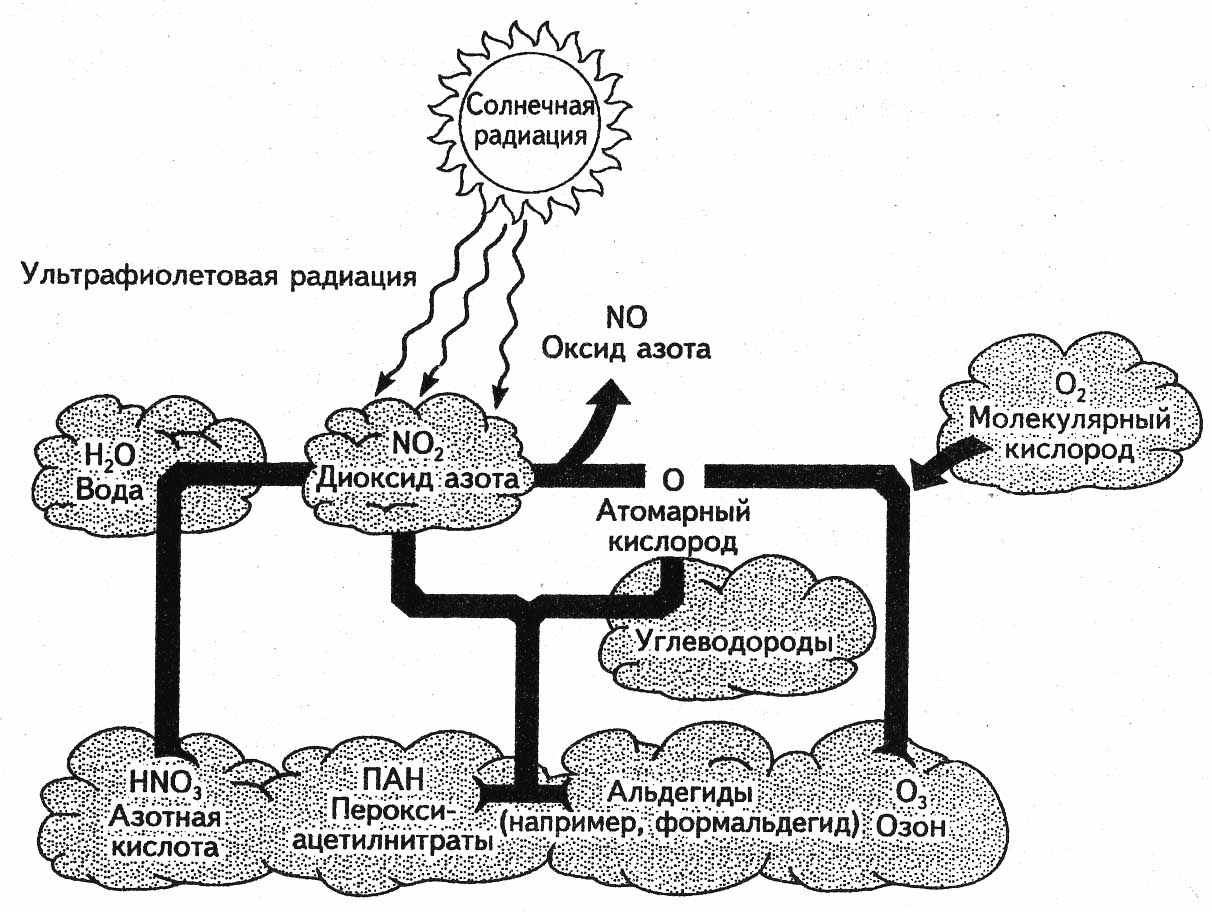
Рис. 3. Формирование фотохимического смога (Миллер Т., 1993)
4.2. Лондонский (влажный) смог
От англ. smoke – дым и fog – туман, что в переводе означает «смесь дыма и тумана» - это сочетание газообразных и твердых примесей с туманом, образующихся в результате сжигания большого количества угля (или мазута) при высокой влажности. Капли серной кислоты дополнительно адсорбируют воду и туман сгущается, достигая высокой степени кислотности.
Инверсионный слой изолирует приземный слой воздуха, приводя к скоплению пыли и SO2.
В отличие от «Лос-анджелесского смога», действующего как окислитель благодаря наличию пероксида, «лондонский смог» имеет восстановительный характер.
Оксид серы (SO2) возбуждается солнечным светом с образованием радикала SO2. Последний реагирует с кислородом до радикала SO4, который мгновенно распадается в присутствии атомарного кислорода. Атомарный кислород может окислять следующую молекулу SO2:
SO2 + O2 → SO4 → + O;
O + SO2 → SO3
Триоксид серы реагирует с водой до образования серной кислоты:
SO3 +H2O → H2SO4
H2SO4 и SO2 нейтрализуются в щелочной среде слизистой оболочки рта. Но поскольку SO2 абсорбируется на пылинках, а гигроскопичная серная кислота образует аэрозоли, оба соединения могут попасть в легкие и привести к защелачиванию кровеносных капилляров. Как следствие, возникает псевдокрупозное воспаление легких, астма и смертельный отек легких (в 1952 году причина гибели в Лондоне 4000 человек).
В табл. 1. приводится сравнительная характеристика фотохимического смога (Raiswell et al., 1980, цит. по Андруз Дж. и др., 1999, с дополнениями, 2006).
Таблица 1
| Характеристика | Фотохимический смог | «Лос-анджелесский смог» |
| Температура воздуха | 24-320С | (-1+4)0С |
| Влажность | 70% | 85% + туман |
| Изменения температуры | Падение на высоте 1000 м | Изменение на высоте нескольких сотен метров |
| Скорость ветра | 0,3 м*с-1 | Безветренно |
| Видимость | 0,8 – 1,6 км | 30м |
| Месяцы наиболее частого проявления | Август – сентябрь | Декабрь – январь |
| Основное топливо | Бензин | Уголь и мазут |
| Главные составляющие | О3, NO, NO2, CO | Частицы сажи, соединения серы, СО, пары |
| Тип химических реакций | Окислительное | Восстановительное |
| Время максимального проявления | Полдень | Раннее утро |
| Действие на здоровье | Раздражение глаз | Раздражение дыхательных путей, кашель |
| Повреждение материалов | Резина | Известняки, мрамор, железо, бетон |
| Внешний вид | Голубоватая дымка | Вид грязной ваты |
5. Кислотные осадки (кислотные дожди)
- Это продукт взаимодействия оксидов серы, азота и других соединений с водяными парами атмосферы, выпадающими на землю в виде кислотных осадков с дождями, снегом и туманами:
SO3 + H2O → SO3 + H2SO4;
2NO + O2 → 2NO2;
2NO2 + H2O → HNO3 + HNO2;
Явление – отчасти природного, отчасти – техногенного характера.
Основные техногенные источники кислотных осадков представлены в таблице 2.
Таблица 2
| Источники | Выбрасываемые соединения, % | |
| SO2 | NOx | |
| Теплоэнергетика Промышленность Транспорт | 55 44 1 | 37 13 50 |
В настоящее время объемы выбросов кислотообразующих осадков (и в первую очередь оксидов серы) в Европе настолько велико (табл. 3), что дают право признать в этом регионе экологическую ситуацию как критическую.
Таблица 3
Среднемесячное поступление в атмосферу оксидов серы
(по странам Европы)
| Страны | Общий объем, тыс.т. | Доля поступления из других стран, % |
| Норвегия | 25,5 | 92 |
| Швеция | 47,5 | 82 |
| Дания | 10,9 | 64 |
| Великобритания | 84,7 | 20 |
| Нидерланды | 17,3 | 77 |
| Германия | 207,9 | 53 |
| Польша | 133,0 | 58 |
| Швейцария | 14,1 | 90 |
| Австрия | 34,1 | 85 |
| Франция | 121,0 | 48 |
| Италия | 113,2 | 30 |
Соединения серы и азота с воздушными потоками переносятся на большие расстояния и могут выпадать на землю в виде кислотных осадков на расстоянии до 1000 – 2000 км от места выброса.
Максимальное количество кислотных осадков на территории России приходятся на регионы, граничащие с Западными странами, откуда они поступают на территорию РФ.
Если до техногенной эры кислотность выпадавших осадков приходилась в пределах 5,6 – 5,2 рН, то в настоящее время значения кислотности их увеличилось до 4 рН и менее (рис. 4).
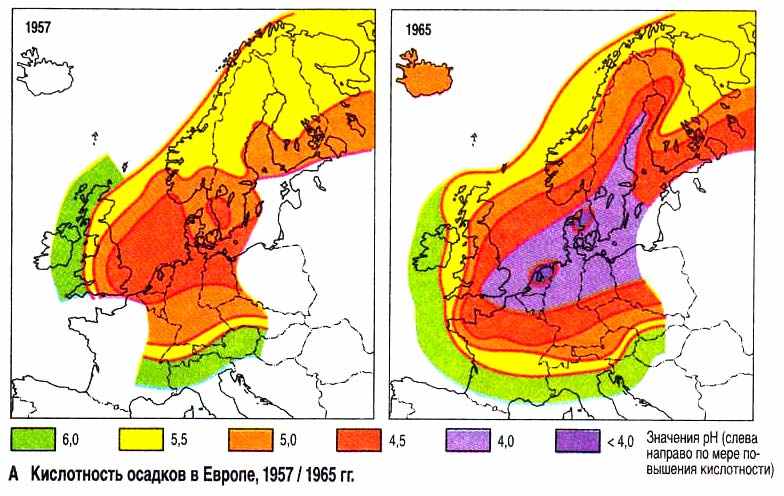
Рис. 4. Кислотность осадков в Европе в 1957/1965 гг.
Значения кислотности осадков над крупными городами России составляют:
в Санкт-Петербурге – 4,8 – 3,7;
в Красноярске – 4,9 – 3,8;
в Казани – 4,8 – 3,3;
В городах 70 – 90% загрязнителей атмосферы, в том числе и образующих кислотные осадки, поступают от автотранспорта.
Экологические последствия выпадения кислотных осадков
Первыми очевидными жертвами кислотных осадков стали озера и реки. Тысячи озер в Скандинавии, США, Канаде и Шотландии превратились в кислотные водоемы, особенно там, где местные почвы не способны нейтрализовать кислотные осадки.
Под влиянием кислотных осадков высвобождается из сложных почвенных соединений алюминий и вымывается в ближайшие ручьи и водоемы, в которых изменяется нормальный обмен веществ.
Повышенные концентрации алюминия в воде приводят к сокращению первичной продукции, от которой зависит жизнь всех обитателей водоемов. По мере увеличения кислотности воды быстро возрастает растворимость и других металлов, в частности кадмия, цинка, свинца и ртути. Некоторые из них являются высокотоксичными и могут по пищевым цепям передаваться гидробионтам.
В табл. 4 показана зависимость гибели гидробионтов от величины кислотности водной среды.
Таблица 4
| Величина pH | Виды гидробионтов |
| 6 5,9 5,8 5,6 5,1 4,5 | Ракообразные, улитки, моллюски Лосось, форель, плотва Фито- и зоопланктон Сиг, хариус Окунь, щук Угорь, голец |
Почвы обычно менее восприимчивы к подкислению, чем водоемы. В наибольшей степени реагируют на загрязнение маломощные почвы с низкими концентрациями нейтрализующих веществ. Кислотные осадки вымывают из почв питательные вещества, высвобождают алюминий, который попадает в корни деревьев и губит их.
Диоксид серы непосредственно повреждает зелень, нарушая процессы фотосинтеза. Из-за фонового влияния диоксида серы в Европе ежегодно теряется 520 тыс. тонн растительных продуктов.
Массовое высыхание лесов и падение жизнеспособности насаждений в западноевропейских странах является причиной выпадения кислотных осадков (рис. 5).
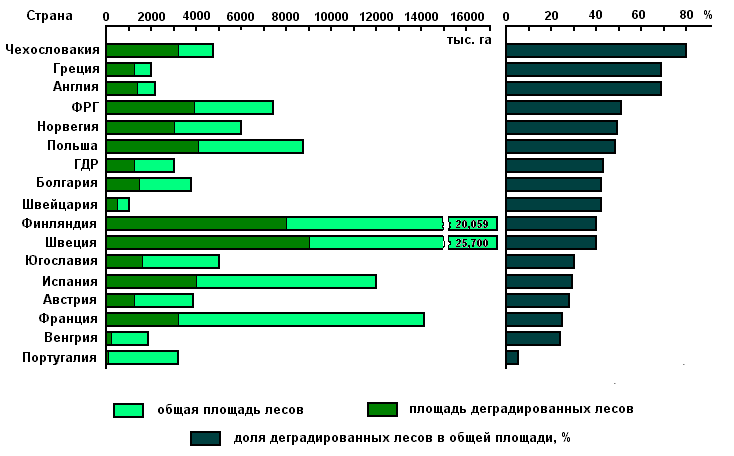
Рис. 5. Оценка деградации лесов Европы от “кислотных дождей”
На территории России большие площади погибших лесов имеются вокруг промышленных гигантов Мурманской области, Карелии, Норильска и других промышленных районов (рис. 6).

Рис. 6. Лес близ гиганта металлургии
Кислотные осадки наносят большой экономический ущерб, т.к. повышенная кислотность ускоряет коррозию большинства конструкционных материалов, используемых при строительстве и эксплуатации жилых зданий и промышленных объектов.
Серьезный ущерб кислотные осадки наносят памятникам архитектуры, многие из которых представляют величайшие сокровища мировой культуры.
6. «Парниковый эффект»
С середины 19 века средняя температура на Земле повысилась на 0,50С в результате усиления «парникового эффекта» (рис. 7, 7-а ). Это повышение температуры может показаться небольшим, однако, согласно имеющимся прогнозам, средняя температура на земном шаре может оказаться выше, чем когда-либо в течение последних 100.000 лет. Считают, что это связано, прежде всего, с увеличением содержания углекислого газа (СО2) в атмосфере (рис. 8). За последние 100 лет индустриального развития концентрация СО2 в атмосфере увеличилась на 13-16%.
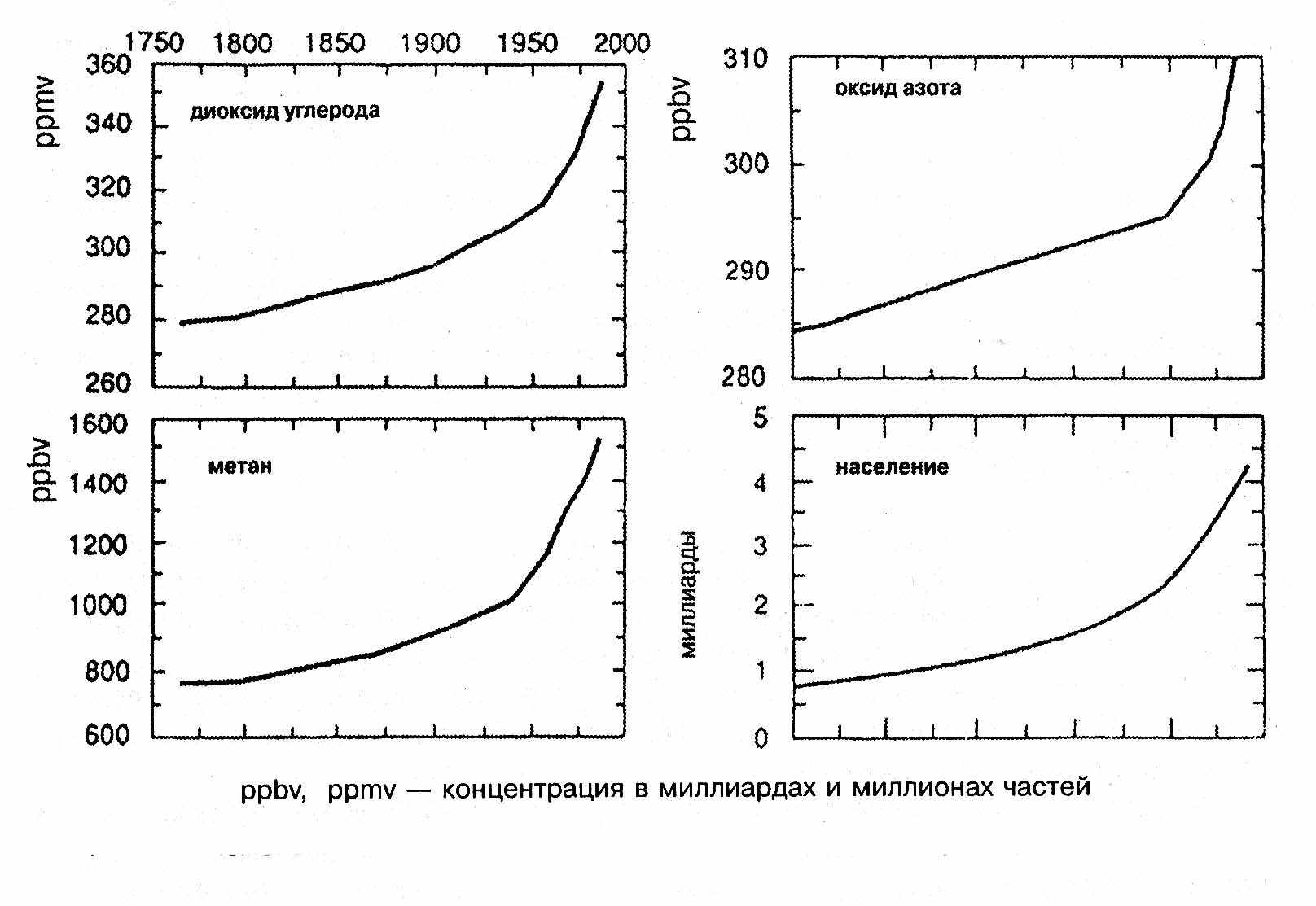
Рис. 7. Изменения концентрации парниковых газов в атмосфере
и населения Земли с 1750 года
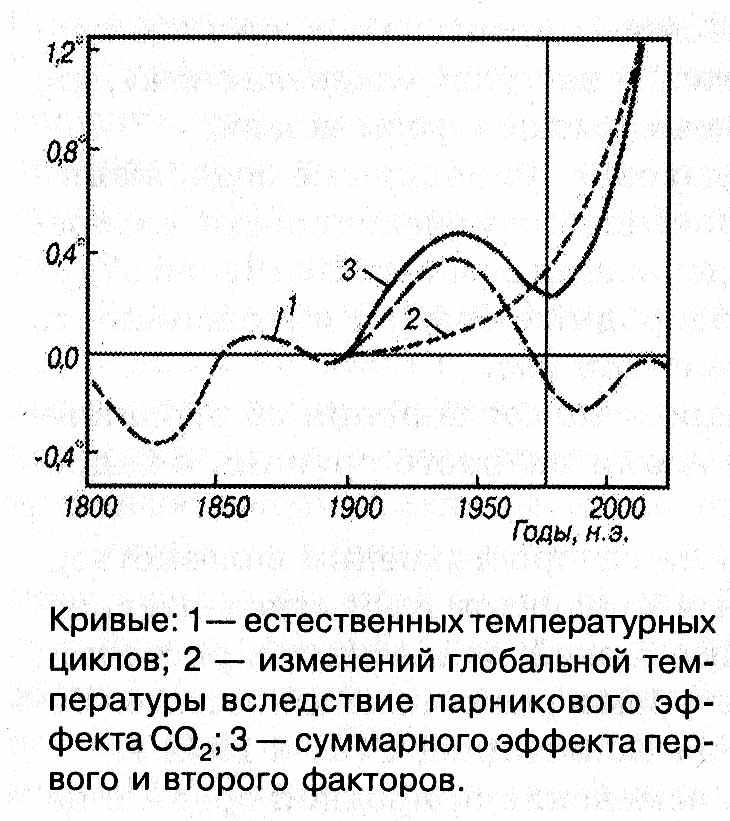
Рис. 7-а. Соотношение естественных температурных циклов с изменениями температур вследствие парникового эффекта
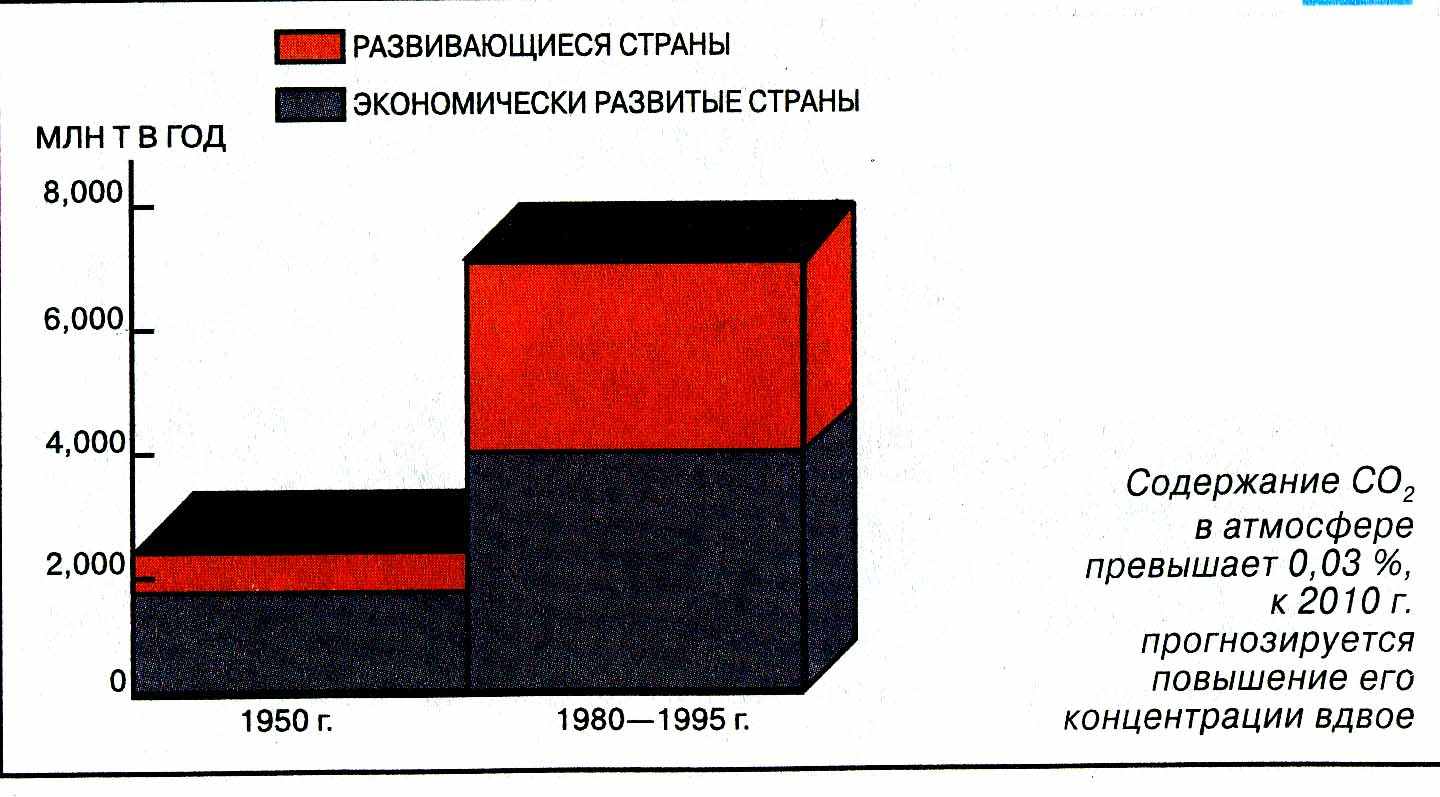
Рис. 8. Содержание диоксида углерода в 1950 – 1995 гг.
«Парниковый эффект» - это явление, связанное с накоплением в атмосфере над Землей СО2 и других, так называемых, «парниковых газов», которые, пропуская к Земле коротковолновую часть теплового излучения Солнца, препятствуют уходу в космос длинноволновой части излучения поверхности Земли, нагреваемой Солнцем (рис. 9).
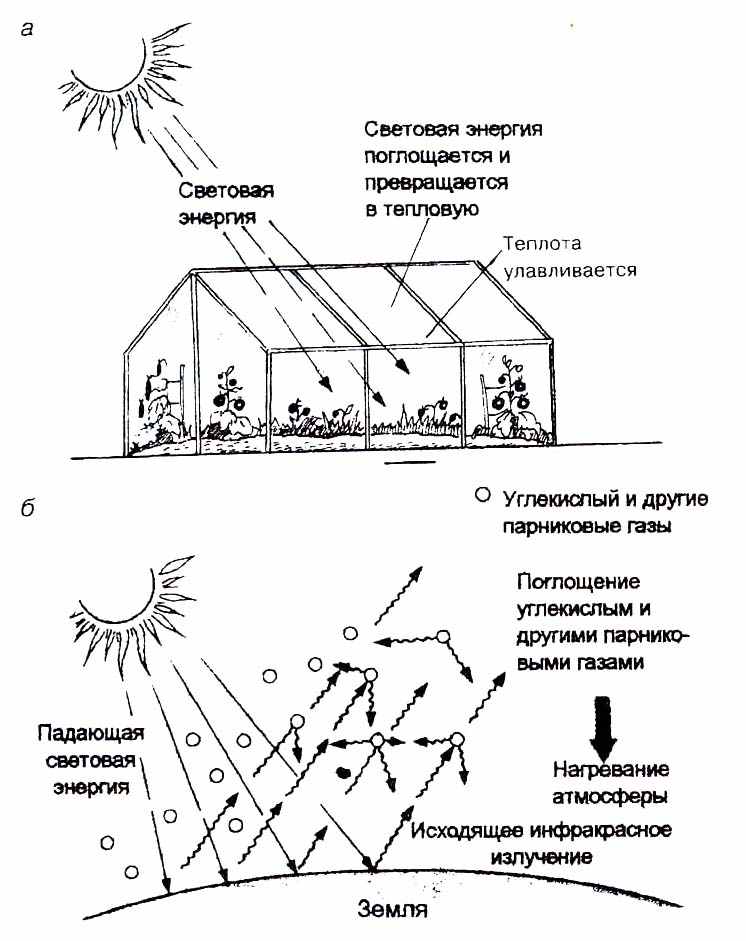
Рис. 9. Парниковый эффект.
(а) Парник нагревается на солнце, так как световая энергия, проникающая внутрь через стекло, поглощается и превращается в тепловую, т. е. в инфракрасное излучение, не проходящее через стекло. Когда теплота таким образом улавливается, температура поднимается. Аналогично нагревается атмосфера Земли (б): свет сквозь нее проникает, а инфракрасное излучение поглощается парниковыми газами. Чем выше концентрация этих газов, тем сильнее нагревается атмосфера
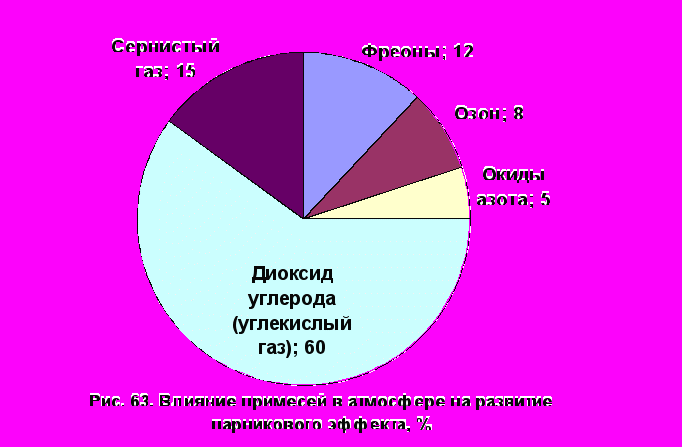
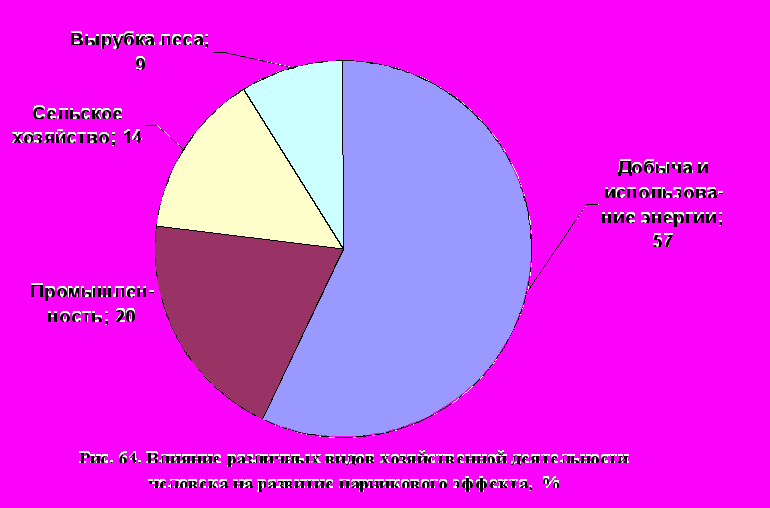
К «парниковым газам», кроме СО2, относят диоксид азота, метан, галогеноуглероды (фреоны) и тропосферный озон (рис. 9). Накопление углекислого газа (табл. 10) обусловлено выбросами тепловых электростанций, промышленными предприятиями, автомобильным транспортом; метан образуется в результате гниения органических отходов. Определенный вклад вносит сельское хозяйство и вырубка лесов (рис. 64). Тепловые электростанции – это главный источник поступления СО2 в атмосферу. В настоящее время увеличение концентрации СО2 происходит со скоростью 0,3 – 0,5% в год. По прогнозам в первой половине 21 века количество выбросов углекислого газа в атмосферу будет удвоено и достигнет 10 млрд. тонн в год, что, по мнению ученых, вызовет потепление климата.
Таблица 10
Изменение концентрации основных парниковых газов в атмосфере Земли, их динамика и свойства (К.Я.Кондратьев, 1990 г., с дополнениями)
| Показатели | Ед. измерения | Диоксид углерода | Метан | Фреон | Оксиды азота |
| Концентрация в доиндустриальный период | частей на млн | 280 | 0,79 | ничтожно мало | 0,288 |
| Концентрация в современный период | частей на млн | 354 | 1,72 | | |
| Ежегодный рост | % | 0,3-0,5 | 0,5-1,0 | | 0,2-0,3 |
| Время жизни | лет | 50-200 | 10 | 130 | 150 |
| Активность действия | на 1 молекулу | 1 | 25 | 11 000 | 165 |
| Доля в парниковом эффекте | % | 66 | 18 | 8 | 8 |
7. РАЗРУШЕНИЕ ОЗОННОГО ЭКРАНА
С конца 70-х годов прошедшего столетия, когда впервые с помощью космических спутников обнаружили нарушение озонного слоя над Антарктидой, проблема возникновения так называемых “озонных дыр” является предметом обсуждения и беспокойства специалистов всего мира.
Если в 1980 году содержание озона в атмосфере над Антарктидой по данным английских исследователей, уменьшилось на 20% по сравнению с нормой, то в 1983 году – на 30%, в 1984 году – на 35%, в 1985 году – на 40%. По данным японских исследователей “озонная дыра” над Антарктидой увеличилась с 1987 по 1997 г.г. в 13 раз, увеличив свою площадь с 8 до 17 млн. кв.км, причем количество озона в этой области сократилось более чем наполовину. В 1998 году площадь “озонной дыры” составила 25 млн.кв.км.
В первой половине марта 1997 года одна “озонная дыра” была обнаружена над северо-западом России – над Ленинградской, Псковской, Новгородской областями, вторая – над Восточной Сибирью, Якутией и центром Красноярского края. Над европейской частью отмечалось снижение стратосферного озона на 20-30%. В “сибирской “озонной дыре” содержание озона было снижено на 35%.
По оценочным данным, техногенное разрушение озонного слоя к 2050 г. может достигнуть 10%.
Что такое озоносфера, как она образуется и какую роль играет в жизни на нашей планете, почему образуются “озонные дыры”, какую опасность они представляют и какие меры, если это необходимо, следует предпринимать для восстановления целостности озонного слоя?
Озоносфера простирается в атмосфере от 10 до 50 км с максимумом концентрации в ней озона (O3) на высоте 20-25 км. При нормальном состоянии озонного слоя над каждым квадратным километром земной поверхности находится 5-6 т озона. Однако при нормальном атмосферном давлении (760 мм ртутного столба при 0оC) слой озона в среднем составил бы всего 3-4 мм.
Образуется озон из кислорода под действием жестких ультрафиолетовых квантов солнечного излучения, при этом картина реакций в озонном слое довольно сложная и пока до конца не понятая.
-
Роль озонного слоя в жизнедеятельности на Земле
Разрушение озонного слоя – наиболее масштабный глобальный процесс, способный нарушить ход развития всей биосферы.
Озоносфера, как щит предохраняет человека, а также растительный и животный мир от вредного влияния жесткой коротковолновой УФ-радиации Солнца.
В связи с тем, что содержание озона в земной атмосфере за последние десятилетия уменьшилось на 5-6%, а интенсивность ультрафиолетового облучения возросла на 10%, согласно прогнозам некоторых ученых к концу нынешнего столетия защитный озонный слой Земли может оказаться разрушенным на 1/3. Часть УФ-излучения, поглащаемая озонным слоем, лежит в диапазоне длин волн 290-320 нм и известна как биологически активное УФ-Б-излучение. Оно разрушает белки и ДНК – химические соединения, которые являются носителями генетической информации у живых организмов. Эти повреждения могут вызвать либо гибель клетки, либо изменения генетической информации, передаваемой ДНК, что является причиной возникновения рака кожи (меланомы). Только в США по данным Агентства по охране окружающей среды, число заболеваний раком кожи может увеличиться в следующем пятидесятилетии на 200 тысяч.
По данным американских исследователей, уменьшение озонного слоя на 50% приведет к возрастанию повреждений ДНК в 2,5 раза, что в свою очередь может повлечь за собой увеличение раком кожи в 7,5-8 раз.
Установлено, что УФ-излучение сильно снижает иммунитет, активизирует многие вирусы, включая вирус СПИДа. Исследователи опасаются, что у лиц, больных вирусными болезнями, болезнь будет протекать тяжелее.
От воздействия жесткого ультрафиолетового излучения у растений повреждается ДНК, кроме того, нарушается фотосинтез, рост и защита от паразитов. Разные виды растений затрагиваются в разной степени, поэтому усиление облучения может привести к изменению целых экосистем.
Ультрафиолетовое излучение диапазона Б проникает довольно глубоко в воду. Так, в чистых арктических водах оно доходит до глубины 65 метров. Поэтому может воздействовать на хромосомы и пигменты планктона. Между тем на фитопланктоне (микроскопических одноклеточных водорослях) держится вся экологическая пирамида в океане. Фитопланктоном питается зоопланктон (это в основном небольшие рачки), рачков едят рыбьи мальки и мелкие рыбы и т.д. Между тем 30% своей белковой пищи человечество получает сейчас из моря, не говоря уже о том, что роль фитопланктонов в производстве кислорода превосходит роль всех лесов планеты. Кислород высвобождается, когда фитопланктон поглощает и перерабатывает растворяющийся в океане атмосферный диоксид углерода. Сейчас его количество растет из-за сжигания ископаемого топлива, а это приводит к “парниковому эффекту” – средняя температура на всей планете медленно, но неуклонно повышается. Если в результате возникновения “озонных дыр” будет поврежден планктон, “парниковый эффект” возрастет.
Между тем, концентрация фитопланктона в антарктических водах обычно в тысячу-десять тысяч раз больше, чем в тропических. Но недавняя океанологическая экспедиция показала, что биомасса планктона в Антарктиде уменьшилась на 25%. Рассчитано: если количество фитопланктона по всему Мировому океану уменьшится на 10%, в атмосфере каждый год будут оставаться лишние 5 млн. тонн диоксида углерода.
7.2. Причины разрушения озоносферы
Главную роль в истощении озонного слоя играют хлорфторсодержащие (ХФУ) газы, особенно фреоны (хладоны), хотя принимают участие и такие примеси, как диоксид углерода, метан, оксиды азота.
Разрушительное действие хлорфторуглеродных соединений было обнаружено учеными-химиками Ш.Роулендом и М.Молина еще в 1974 году, а в 1996 году им за это открытие была присуждена Нобелевская премия. Однако бесспорным лидером в разрушении озонного слоя считается хлор. Молекула хлора способна уничтожить до ста тысяч молекул озона, в то время как молекула оксида азота – около 10 молекул озона.
Существует несколько синонимов хлорфторуглеродов: фреоны, хладоны, хлорфторметаны; ХФУ химически инертны, не вступают в химические реакции и поэтому нетоксичны для живых существ. Однако, попадая без изменений в стратосферу и подвергаясь там воздействию УФ-излучения, ХФУ распадаются с высвобождением атомов хлора, которые и разрушают молекулы озона:
Cl + O3 → ClO + O2
ClO + O → Cl + O2
Аналогичные реакции происходят с монооксидом азота NO:
NO + O3 → NO2 + O2
NO2 + O → NO + O2
O3 + O → 2O2
Монооксид азота присутствует в стратосферном слое как обязательный его компонент, но в небольшой концентрации.
ХФУ применяется как хладоагенты (фреоны) в холодильниках и кондиционерах, как пропелленты они содержатся в аэрозольных упаковках; их применяют при производстве вспененного полиуретана; используют при чистке электронной техники; их используют для изготовления теплоизоляционного и упаковочного материалов и ряда других целей.
Когда в конце 70-х годов специалисты с помощью спутников впервые обнаружили нарушение озонного слоя над Антарктидой, аномалию поначалу объяснили погрешностью приборов. Однако, когда это не подтвердилось, аномалию связали с испытаниями атомных и водородных бомб.
Наземные испытания запретили, но содержание озона в стратосфере возросло. Но потом кривая снова пошла вниз. Для объяснения этого в ход пошла вторая теория – природная.
Так, появление “озонных дыр” над Антарктидой связывают с отсутствием там растительного покрова, являющегося поставщиком озона в стратосферу. Аналогично – интенсивной вырубкой леса в бассейне реки Амазонки объясняют появление “озонной дыры” в Южном полушарии. Некоторые ученые связывают непостоянство размеров “озонных дыр” над Антарктидой с сезонными колебаниями уровня озона в атмосфере – максимумом концентрации в летнее время и снижением до минимума – в период полярной ночи.
Довольно распространенной является гипотеза о связи этого явления с характером солнечной активности. В годы так называемого активного солнца количество падающей на Землю радиации увеличивается. Это излучение возбуждает атомы атмосферного озона и они, обычно нейтральные, начинают вступать в реакцию с кислородом. В результате такой реакции образуются оксиды азота, которые являются разрушителями озона. Однако окончился очередной 11-летний период, а количество оксидов азота в средних широтах Южного полушария возросло на 30-60%, “дыра” над Антарктидой продолжает расширяться.
Возникла новая гипотеза о причастности в разрушении озоносферы самолетов типа “Конкорд”, “Боинг”, “МИГ”, высота полетов которых совпадает с высотой расположения озоносферы. Однако проведенные американскими учеными исследования в этом направлении, однозначных результатов не показали. Тем не менее, эта тема исследований, очевидно, будет нуждаться в реанимации, т.к. в последние годы созданы аэрокосмические системы, большинство из которых для озоносферы более опасны, чем самолеты указанных типов.
Космический “Шаттл” при одном запуске способен уничтожить десять миллионов тонн озона, или 0,3% от его общего содержания в земной атмосфере. Значительно менее опасны для озонного слоя отечественные ракеты-носители “Энергия”.
Проблема опасности, связанная с запуском космических кораблей, может получить серьезное развитие, если количество запусков достигнет нескольких десятков, или, вернее, сотен в год.
Уровни загрязнения атмосферы оксидами азота в результате пролетов ракет и летательных аппаратов сопоставимы с уровнями загрязнения ее в результате вулканической деятельности.
В состав вулканических газов входят соединения типа фреонов – хлор- и фтор- производные метана. Они практически непрерывно выделяются в атмосферу в Курило-Камчатском регионе, где количество действующих вулканов достигает 28. Активная вулканическая деятельность отмечается в Японии, на Филиппинах, в районе островных дуг и континентальных окраин Америки. Мощным источником фторхлорметанов являются вулканы Центральной Америки. Существует обширная цепь наземных и подводных вулканов в Антарктиде. Однако, приходится учитывать, что вулканическая деятельность на Земле продолжается не один миллион лет, а проблема “озонных дыр” возникла только сейчас.
Большинство специалистов в настоящее время полагают, что главный враг озонного слоя домашние и промышленные холодильники и аэрозольные баллончики, точнее содержащийся в них фреон. Счет таким холодильникам в мире идет на десятки миллионов, а баллончикам – на миллиарды. Содержащийся в них инертный, недорогой, нетоксичный газ фреон, попадая в стратосферу, становится сильнейшим разрушителем озона и сохраняет такое свойство в течение 70-80 лет.
Кроме того сотни тысяч тонн минеральных удобрений, ежегодно вносимых на поля, также являются поставщиками оксидов азота, неблагоприятно влияющих на озон, как и выхлопные газы автомашин.
7.3. Пути восстановления целостности озоносферы
Можно указать на три не исключающие друг друга пути.
Первый путь – удалить разрушающие озон катализаторы из атмосферы. Второй – наработать озон.
Удалить катализаторы очень трудно, поскольку их концентрация в атмосфере мала. Предлагается: 1). Использование лазера, излучение которого разрушает молекулы фреона. Недостаток этого метода – неэффективность использования энергии. Только небольшая ее часть разрушает фреоны, остальная рассеивается в космосе; 2).Вымораживание фреонов в специальных установках на поверхности Земли. Для этого надо будет пропустить значительную долю атмосферы через эти установки, что слишком дорого.
Все проекты этой группы дороги, энергоемки и чреваты образованием кислотных дождей и возможностью возникновения “парникового эффекта”.
Обсуждается несколько методов наработки озона. Наиболее заманчивым, на первый взгляд, является размещение на околоземной орбите отражателей солнечного света, увеличение количества которого должно способствовать наработке озона. Вопрос требует более подробного количественного анализа. Предлагается освещение верхней атмосферы ультрафиолетовым лазером с энергией кванта больше 5 эВ, который разрушает кислород, в результате чего генерируется озон. Однако располагать лазер на Земле нельзя – излучение пройдет через кислород плотных слоев атмосферы. Поэтому лазер должен быть расположен на борту космического аппарата и это вызывает большие энергетические трудности. Технически наиболее реально (и сравнительно дешево) создать с помощью радиоволн сверхвысоких частот разряд в верхней атмосфере (на высотах 15-30 км). Произойдет воздействие электронов на молекулы газа, в результате чего предполагается наработка озона.
Таким образом, возможности активного воздействия на “озонную дыру” имеются. Вопрос в том, сколько это будет стоить? Для этого нужны усилия всего человечества: четкие международные программы и их реализация в рамках международного сотрудничества.
И, наконец, третий путь – резкое ограничение выбросов в атмосферу наиболее активных озоноразрушающих веществ. 1 января 1989 года вступил в силу Международный (Монреальский) протокол о защите озонного слоя, выработанный 57 странами, согласно которому в течение 10 лет производство озоноразрушающих веществ будет сокращено на 50%, однако до сих пор во всем мире ежегодно производится около миллиона тонн газообразных веществ, способных разрушить озонный слой – и это, несмотря на то, что заменители фреонов, сравнительно быстро разрушающиеся в тропосфере, уже получены и применяются.
Производство бытовых холодильников уже переведено на нетрадиционный фреон и планируется сократить выбросы традиционного фреона путем его рекуперации при ремонте холодильных установок и кондиционеров.
Таким образом, названы основные вещества – заменители традиционных фреонов и интенсивно ведутся токсикологические исследования и разработки альтернативных веществ и технологий.
8. СИСТЕМА МОНИТОРИНГА ВОДЫ
ПЕРЕЧЕНЬ
КОНТРОЛИРУЮЩИХ СТВОРОВ ДЛЯ РАЗМЕЩЕНИЯ СТАЦИОНАРНЫХ
ПОСТОВ НАБЛЮДЕНИЯ ЗА КАЧЕСТВОМ ВОДЫ р. МОСКВЫ И ЕЁ
ПРИТОКОВ ОТ ИСТОЧНИКОВ ВОДОСНАБЖЕНИЯ ДО ВЫХОДА ИЗ ГОРОДА
I. Контрольные створы на участке от источников водоснабжения
города (тракт водоподачи) до Спасского моста
1. Створ - река Москва у п. Старая Руза. Характеризует качество воды, поступающей из Можайского, Рузского, Озернинского водохранилищ, рек Рузы, Озерны и части реки Москвы, где размещаются основные хозяйствующие объекты Можайского и Рузского районов.
2. Створ - река Москва у с. Успенское. Характеризует участок реки от впадения в нее р. Рузы, где расположены основные хозяйствующие объекты на площади водосбора р. Москвы.
3. Створ - устье р. Истры - с. Дмитровское. Характеризует качество воды основного притока р. Москвы, впадающего в нее в непосредственной близости от водозаборов водопроводных станций (время добегания воды в межень 11 часов), который подвержен наибольшей антропогенной нагрузке. Основные объекты сельского хозяйства, рекреации, дачное и коттеджное строительство сконцентрированы на водосборной площади реки Истры на территории Истринского района. Регулярный, оперативный контроль качества воды необходим для своевременного изменения технологического процесса на водопроводных станциях.
4. Створ - выше водозабора Западной водопроводной станции. Предлагается автоматизировать для оптимизации технологических процессов водоподготовки на водопроводных станциях и оперативного реагирования на загрязнения исходной воды.
5. Приплотинные створы Можайского, Рузского, Озернинского и Истринского водохранилищ. Характеризуют состояние водохранилищ, позволяют выбрать регламент их работы, определяющий долевое участие каждого водохранилища в формировании качества воды на водозаборах для оптимизации технологии водоподготовки на водопроводных станциях. Контроль качества в перечисленных створах необходимо осуществлять по следующим показателям:
1) температура, цветность, мутность, рН, окисляемость, электропроводность, растворенный кислород - общие физико - химические показатели, необходимые для оценки состояния водоема в целом и для выбора регламента работы водохранилищ.
2) хлориды, сульфаты, аммоний, нитраты, фосфаты, железо, БПК - для оценки степени антропогенной нагрузки, влияния деятельности человека на водоисточник и контроля поступления сточных вод.
3) щелочность, жесткость, кальций и магний - для подбора адекватной технологии очистки воды.
4) бактериологические показатели - для оценки уровня эпидемиологической безопасности водоисточников.
II. Контрольные створы наблюдения за качеством воды р. Москвы
и ее притоков в черте города
1. Створ - река Москва выше Спасского моста. Характеризует качество воды в реке на входе в город.
2. Створ - устье Сходни. Характеризует качество воды реки Сходни - приемника сточных вод Зеленоградской станции аэрации. По данным Государственного доклада Москомприроды за 1998 год состояние реки ухудшилось по сравнению с прошлыми годами. Возросло содержание азота нитритов, фосфатов, меди, железа, содержание которых превышает ПДК в 2,3; 7,0; 6,0; 3,0 раз соответственно. В р. Сходня сбрасывают поверхностные сточные воды 95 абонентов МП «Мосводосток». Расход воды в реке (с учетом обводнения волжской водой из канала им. Москвы) составляет порядка 23 куб. м/сек.
3. Створ - устье Сетуни. Характеризует качество воды реки Сетуни при впадении ее в р. Москву. По данным Государственного доклада Москомприроды за 1998 г., в устье реки значительно возросло содержание взвешенных веществ (119,5 мг/л - 1998 г., 23,4 мг/л - 1996 г.), сохраняется загрязнение реки ионами железа - 8 ПДК, меди - 12 ПДК, марганца - 19 ПДК. В реку Сетунь сбрасывают поверхностные сточные воды 189 абонентов МП «Мосводосток», впадают 6 притоков. Расход воды в реке составляет приблизительно 0,7 куб. м/сек.
4. Створ - устье Яузы. Характеризует качество воды реки Яузы при впадении ее в р. Москву. По данным Государственного доклада Москомприроды за 1998 год река Яуза сохраняет статус самого загрязненного притока р. Москвы в черте города. По сравнению с прошлыми годами в реке отмечается увеличение содержания взвешенных веществ, ХПК, БПК, фенолов, ПАВ. В концентрации выше ПДК обнаруживаются нитриты, нефтепродукты, железо, медь, цинк. Непосредственно в реку Яуза сбрасывают поверхностные сточные воды 162 абонента МП «Мосводосток», впадают 28 притоков, в которые сбрасывают свои стоки 28 абонентов МП «Мосводосток» . По данным инвентаризации река имеет 469 водовыпусков коллекторной сети поверхностного стока, в том числе с селитебной и промышленной территории города. Расход воды в реке с учетом обводнения составляет порядка 9,5 куб. м/сек.
5. Створ - устье Городни. Характеризует качество воды реки Городни при впадении ее в р. Москву. По данным Государственного доклада Москомприроды за 1998 год, несмотря на некоторое улучшение по ряду показателей, сохраняется высокое загрязнение аммонийным азотом (4 ПДК). В реку Городня сбрасывают поверхностные сточные воды 64 абонента МП «Мосводосток».
6. Створ - Бесединский мост. Характеризует качество воды в реке на выходе из города под влиянием стока со всей территории города. По данным инвентаризации в черте города река имеет 896 водовыпусков коллекторной сети поверхностного стока, в том числе с селитебной и промышленной территории города непосредственно в реку поступают стоки от 441 абонента МП «Мосводосток».
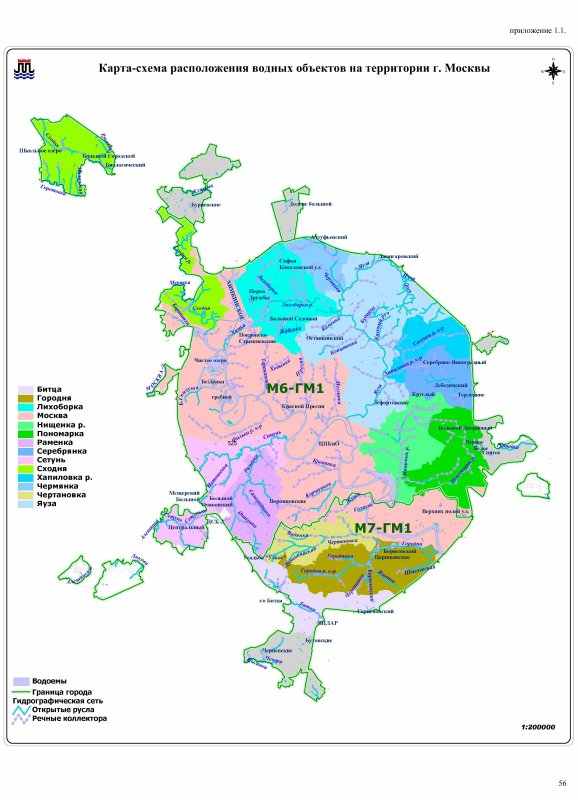
Карта-схема наблюдательной сети по состоянию водных объектов
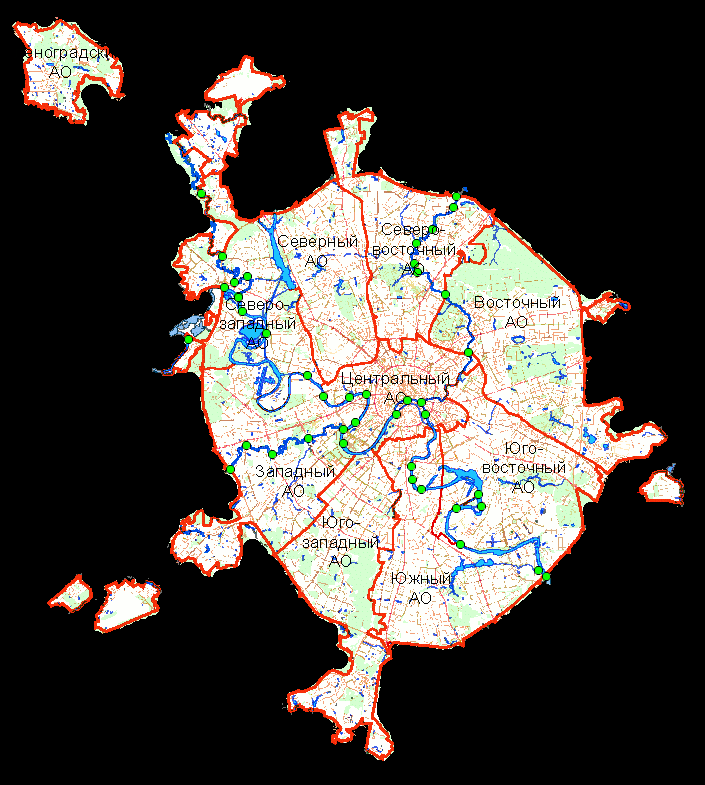
В черте города непосредственно по реке Москве предусмотрено 13 контрольных створов и 14 створов – в устьях малых рек, притоков реки Москвы.
Аналитический контроль предусмотрен по 29 показателям: рН, прозрачность, растворенный кислород, взвешенные вещества, БПК5, ХПК, сухой остаток, хлориды, сульфаты, фосфаты, ионы аммония, нитриты, нитраты, железо общее, марганец, медь, цинк, хром общий, никель, свинец, кобальт, алюминий, кадмий, нефтепродукты, фенолы, формальдегид, ПАВ анионоактивные, сероводород и сульфиды, токсичность.
Периодичность отбора проб установлена с учетом существующей практики контролирующих организаций, но не реже 1 раза в сезон.
В настоящее время контрольные створы распределены между различными организациями с учетом условий водопользования (например, устья малых рек – ГУП «Мосводосток»; выше и ниже ОКСА, а также на всем тракте водоподачи Москворецких водоисточников – МГУП «Мосводоканал» и т.д.). Утверждены единые методики количественного химического анализа поверхностных вод, контроль за качеством воды осуществляется аналитическими лабораториями, аккредитованными в соответствии с ГОСТ Р51000.4-96 «Система аккредитации в Российской Федерации. Общие требования к аккредитации испытательных лабораторий».
В дополнение к створам, утвержденным ППМ от 24.11.1998г № 911, Департаментом природопользования и охраны окружающей среды города Москвы периодически производится серийный отбор проб воды основных рек Москва, Яуза, Сетунь, Сходня последовательно по контрольным створам от входа в город до выхода из города.
В навигационный период контроль реки Москвы периодически осуществляет теплоход «Экопатруль», оборудованный автоматизированным аналитическим комплексом.
ГПУ «Мосэкомониторинг» осуществляет анализ и обобщение результатов контроля природных вод по створам, утвержденным ППМ от 24.11.1998г № 911 и дополнительным створам, контролируемым ДПиООС, а также производит оценку качества водных объектов на территории г.Москвы в соответствии с нормативами культурно-бытового и рыбохозяйственного водопользования.
ПДК веществ в водных объектах
В зависимости от хозяйственной цели использования водных объектов (по целевому назначению) выделяются следующие виды водопользования: для питьевого и хозяйственно-бытового водоснабжения; промышленности и энергетики; сельского хозяйства; лесного хозяйства, лесосплава; здравоохранения; строительства; пожарной безопасности; рыбного хозяйства; охотничьего хозяйства и иных целей. Для поверхностных водных объектов на территории г. Москвы установлены следующие предельно допустимые концентрации загрязняющих веществ.
| Анализируемые показатели | ПДКр-х | ПДКк-б | |
| | |||
| | |||
| Алюминий мг/л | 0.04 | 0.5 | |
| БПК5 мгО2/л | 2.0-3.0 | 4.0-6.0 | |
| Взвешенные вещества мг/л | Увеличение концентрации не более чем на 0.75 | Увеличение концентрации не более чем на 0.75 | |
| Железо общее мг/л | 0.1 | 0.3 | |
| Азот аммонийный мг/л | 0.39 | 2.0 по азоту | |
| Кадмий мг/л | 0.005 | 0.001 | |
| Растворенный кислород мг/л | не менее 4.0 | не менее 4.0 | |
| Хлориды мг/л | 300 | 350 | |
| Марганец мг/л | 0.01 | 0.1 | |
| Медь мг/л | 0.001 | 1.0 | |
| Нефтепродукты мг/л | 0.05 | 0.3 | |
| Никель мг/л | 0.01 | 0.1 | |
| Азот нитратов мг/л | 9.1 | 45.0 по нитратам (10.2 по N) | |
| Азот нитритный мг/л | 0.02 | 3.3 по нитритам (1.0 по N) | |
| Анионоактивные ПАВ мг/л | 0.5 | 0.5 | |
| Токсичность | Не должны оказывать хронического действия на тест-объект | Не должны оказывать хронического действия на тест-объект | |
| Водородный показатель рН | 6.5-8.5 | 6.5-8.5 | |
| Свинец мг/л | 0.1 | 0.03 | |
| Сульфаты мг/л | 100 | 500 | |
| Сульфиды мг/л | Отсутствие | Отсутствие | |
| Сухой остаток мг/л | 1000 | 1000 | |
| Фенолы мг/л | 0.001 | 0.001 | |
| Формальдегид мг/л | 0.01 | 0.05 | |
| Фосфаты мг/л | 0.2 | 3.5 по PO4 (1.2 по P) | |
| ХПК мгО/л | 30.0 | 30.0 | |
| Хром +3 мг/л | 0.07 | 0.5 | |
| Цинк мг/л | 0.01 | 1.0 | |
