Утверждаю
| Вид материала | Рабочая программа |
- Утверждаю утверждаю, 21.26kb.
- «утверждаю» «утверждаю», 262.03kb.
- Утверждаю утверждаю, 393.06kb.
- «Утверждаю» «Утверждаю» Председатель Совета доу заведующий мдоу №25, 113.74kb.
- Кикбоксинг против наркомании и детской преступности «Утверждаю» «Утверждаю», 78.29kb.
- Утверждаю: утверждаю, 156.74kb.
- «утверждаю» «утверждаю» Председатель республиканского Директор маоудод «цдтт №5» совета, 42.86kb.
- Утверждаю» «Утверждаю», 163.81kb.
- «Динамо», 49.89kb.
- Утверждаю: утверждаю: Председатель Глава администрация оо «Гомельский рыболовный клуб», 78.23kb.
 Рабочая программа учебной дисциплины | | Ф ТПУ 7.1 – 21/01 |
УТВЕРЖДАЮ
Декан ХТФ
________В.М. Погребенков
"____"____________ 2007 г.
МЕТОДЫ ОРГАНИЧЕСКОГО СИНТЕЗА
Рабочая программа
для направления 240100 «Химическая технология и биотехнология»
специальности 240901 (c) «Биотехнология»
Химико-технологический факультет (ХТФ)
Обеспечивающая кафедра – Кафедра органической химии и технологии органического синтеза
Курс – 4
Семестр – 8
Учебный план набора 2007 года с изменениями ______ года
Распределение учебного времени
Лекции 48 час.
Лабораторные занятия 32 час.
Всего аудиторных занятий 68
Самостоятельная (вне-
аудиторная) работа 112 час.
Общая трудоемкость 192 час.
Экзамен в 8-ом семестре
Зачет в 8-ом семестре
Томск 2007
Предисловие
1. Рабочая программа составлена на основе ГОС по направлению 655500 «Биотехнология», специальности 240901 (c) «Биотехнология», утвержденного 05.03.2000 г., РАССМОТРЕНА и ОДОБРЕНА на заседании обеспечивающей кафедры органической химии и технологии органической химии 7 сентября 2007 г., протокол № 2.
2. Разработчик
доцент кафедры ОХОС Т.А. Сарычева
3. Зав. обеспечивающей кафедрой ОХОС В.Д. Филимонов
4. Рабочая программа СОГЛАСОВАНА с факультетом, выпускающей кафедрой специальности, СООТВЕТСТВУЕТ действующему плану.
Зав. выпускающей кафедрой ОХОС В.Д. Филимонов
УДК 661.12.091.3 (075.8)
Ключевые слова: рабочая программа, методы органического синтеза, алкилирование, ацилирование, аминирование, галогенирование, нитрование, сульфирование, восстановление, окисление, механизм реакции.
МЕТОДЫ ОРГАНИЧЕСКОГО СИНТЕЗА
070100 (240901) (с)
Каф. ОХОС ХТФ
Доцент, к.х.н. Сарычева Тамара Александровна
Тел. (3822)563861
Цель: формирование основ и углубление знаний студентов в области методов органического синтеза, развитие у них химического мышления. Обучение студентов методам и приемам органического синтеза, методам выделения и очистки органических соединений.
Содержание: рассмотрены важнейшие методы промышленного и лабораторного органического синтеза, химизм процессов, механизмы изучаемых органических реакций. Для каждого процесса кратко рассматриваются наиболее важные случаи его практического применения в современной химической и химико-фармацевтической промышленности.
Курс 4 (8 сем. – экзамен, 8 сем. – зачет).
Всего 192 ч, в т.ч. Лк.- 48 ч, Лб.- 32 ч.
ЦЕЛИ И ЗАДАЧИ ДИСЦИПЛИНЫ
Курс «Методы органического синтеза» адресован студентам уже знакомым с основами органической химии, и желающим более основательно изучить органический синтез. Данный курс направлен, в основном, на изучение методов синтеза, используемых для получения биологически активных веществ. Материал в программе классифицирован по способам введения и взаимным превращениям функциональных групп. Кроме этого рассмотрены реакции конденсации и методы синтеза гетероциклических соединений.
Цель преподавания данной дисциплины – формирование основ и углубление знаний студентов в области методов органического синтеза, развитие у них химического мышления. При изучении дисциплины предусмотрен лабораторный практикум, целью которого является научить студентов методам и приемам органического синтеза, выделения и очистки органических соединений.
Задачи дисциплины:
- Научить студентов применять полученные теоретические знания для решения конкретных практических задач.
- Привить практические навыки по синтезу, выделению, очистке и идентификации органических веществ.
- Научить обрабатывать, анализировать и оформлять результаты эксперимента.
После изучения курса студент
должен знать:
- методы введения функциональных групп в органические молекулы;
- механизмы изученных органических реакций;
- о взаимных превращениях органических соединений;
должен уметь:
- на основе анализа литературы разработать методику синтеза органического соединения;
- собрать установку для синтеза и провести необходимые расчеты;
- синтезировать, выделить и очистить органическое вещество;
- определить степень его очистки;
СОДЕРЖАНИЕ ДИСЦИПЛИНЫ (лекции)
ВВЕДЕНИЕ (2 часа)
Цели и задачи курса. Краткая история развития органического синтеза. Общие методы получения промежуточных продуктов. Основные виды сырья.
1. СУЛЬФИРОВАНИЕ И СУЛЬФОХЛОРИРОВАНИЕ (6 часов)
1.1. Сульфирование (4 часа)
Цели введения сульфогруппы в органические соединения. Общая схема процесса сульфирования. Сульфирующие агенты. Механизм реакции сульфирования.
Влияние различных факторов на процесс сульфирования (концентрация кислоты, температура, время реакции). Значение концентрации отработанной кислоты («π-сульфирования»).
Правила размещения сульфогрупп в нафталиновом ядре (правило Армстронга – Винна). Сульфирование в присутствии катализаторов.
Основные способы сульфирования. Сульфирование в жидкой фазе серной кислотой или олеумом. Сульфирование газообразным серным ангидридом. Сульфирование в парах, технологические и экономические преимущества этого метода. Сульфирование аминов методом «запекания».
Методы выделения сульфокислот: высаливание, известкование. Разделение изомерных сульфокислот.
Сульфирование важнейших ароматических соединений: бензола, толуола, нитробензола, анилина, нафталина и его производных, антрахинона.
Характеристика получаемых продуктов.
1.2. Сульфохлорирование (2 часа)
Сульфохлорирование. Механизм реакции. Условия и способы проведения сульфохлорирования.
Техника безопасности при проведении процессов сульфирования и
сульфохлорирования.
Применение сульфокислот и их производных
2. НИТРОВАНИЕ И НИТРОЗИРОВАНИЕ (6 час.)
2.1. Нитрование (4 часа)
Общие сведения и схема процесса нитрования. Нитрующие агенты. Механизм реакции нитрования.
Влияние различных факторов на процесс нитрования (температура, время реакции, характер субстрата, характер нитрующего агента, катализаторы). Соотношение реагентов в реакции нитрования. Побочные процессы при нитровании.
Нитрование углеводородов. Способы разделения изомерных нитросоединений и их очистка. Нитрование хлорпроизводных и разделение продуктов реакции. Нитрование аминов. Нитрование сульфокислот и выделение нитросульфокислот. Технология кристаллизации, разгонки и очистки нитросоединений.
Основные способы нитрования. Получение динитробензола, нитротолуолов, динитрохлорбензола, нитросульфокислот нафталина. Нитрование водной азотной кислотой пирена, эфиров гидрохинона.
Методы контроля производства и характеристика продуктов.
Применение нитросоединений.
2.2. Нитрозирование (2 часа)
Схема реакции нитрозирования. Нитрозирование фенолов и аминов. Механизм нитрозирования вторичных и третичных жирно-ароматических аминов. Характерные свойства нитрозосоединений и их применение.
- 3. ГАЛОГЕНИРОВАНИЕ (4 часа)
Галогенирующие агенты. Галогенирование в ядро и в боковую цепь. Механизмы реакций галогенирования в ядро и боковую цепь. Влияние различных факторов на процесс галогенирования (температура, катализаторы, облучение).
Хлорирование ароматических углеводородов и их производных. Хлорирование фенолов и аминов. Получение галогенпроизводных антрахинонового ряда. Основные стадии промышленного хлорирования аренов. Технологические схемы хлорирования бензола и толуола (по кольцу и в боковую цепь). Требования, предъявляемые к аппаратуре.
Бромирование и иодирование. Получение фторпроизводных ароматических соединений.
- Диазотирование и превращение диазосоединений (4 часа)
Механизм реакции диазотирования. Условия проведения реакции. Влияние температуры и кислотности среды. Свойства солей диазония.
Превращение диазосоединений. Реакция азосочетания, её механизм. Азо- и диазосоставляющие. Замена диазогруппы на водород, гидроксил, галогены, цианогруппу. Восстановление солей диазония. Получение фенилгидразина.
5. алкилирование и ацилирование (6 часов)
Общие представления о реакциях алкилирования и ацилирования.
5.1. Алкилирование и ацилирование углеводородов (2 часа)
Алкилирование ароматических соединений. Реагенты и катализаторы, условия и механизмы реакций алкилирования аренов. Алкилирование по Фриделю-Крафтсу. Алкилирование спиртами и алкенами.
Алкилирование формалином, механизм реакции. Реакция хлорметилирования.
Алкилирование парафиновых углеводородов. Механизмы алкилирования алифатических соединений.
Ацилирование ароматических углеводородов. Катализаторы и реагенты реакций ацилирования. Механизм реакции ацилирования по Фриделю-Крафтсу. Использование реакций ацилирования для получения кетонов, карбоновых кислот, сложных эфиров, оксокислот, гетероциклических соединений. Формилирование. Реакции Гаттермана-Коха, Раймера-Тимана, Вильсмайера. Карбоксилирование фенолов по кольцу, реакция Кольбе-Шмидта.
Примеры промышленных синтезов. Их значение.
5.2. Алкилирование аминов и гидроксисоединений (2 часа)
Алкилирование фенолов и ароматических аминов по кольцу. Алкилирующие агенты. N-алкилирование аминов. Зависимость реакционной способности аминов и от их строения в реакциях алкилирования. О-алкилирование гидроксигруппы. Сравнение реакционной способности ариламинов и фенолов в реакциях алкилирования. Механизмы реакций алкилирования. Критерии выбора алкилирующих агентов.
5.3. Ацилирование аминов и гидроксисоединений (2 часа)
Ацилирование аминов и оксисоединений. Катализаторы и реагенты реакций ацилирования. Механизмы реакций. Сравнение реакционной способности ароматических аминов и фенолов, спиртов и фенолов в реакциях ацилирования.
6. гидрОксилирование и аминирование (6 часов)
общие представления о реакциях гидроксилирования и аминирования. Механизм реакции.
Нуклеофильное замещение сульфогруппы. Реакция щелочного плавления сульфокислот. Открытое и автоклавное щелочное плавление. Выделение гидроксисоединений. Замещение сульфогруппы на аминогруппу сплавлением сульфокислот с амидом натрия и при действии аммиака. Обработка щелочного плава. Аппаратура для проведения процессов щелочного плавления. Производство фенола, резорцина, -нафтола, аминоантрахинонов.
Замещение галогенов на гидрокси-, алкокси- и аминогруппу в ароматических и алифатических соединениях. Влияние природы субстрата и галогена на скорость реакции замещения. Механизмы реакций (SN1, SN2 и кине-замещение). Катализаторы в реакциях замещения хлора гидроксигруппой. Примеры промышленных синтезов. Замещение галогенов в активированных арилгалогенидах и гетероциклических соединениях. Механизм реакции.
Взаимные превращения амино- и гидроксисоединений. Кислотный гидролиз аминогруппы. Аминирование оксисоединений аммиаком или солями аммония. Реакция Бухерера.
Замещение нитрогруппы в ароматических соединениях.
Замещение амино- и аммониевых групп. Ариламинирование или араминирование. Получение дифениламина, N-арилнафтиламинов.
Нуклеофильное замещение атома водорода в гетероциклических и ароматических соединениях, содержащих электроноакцепторные заместители.
7. ВОССТАНОВЛЕНИЕ (5 часов)
Реакции восстановления. Классификация методов восстановления. Восстановление металлами и их солями. Восстановление карбонильных соединений, сложных эфиров, нитросоединений, органических галогенидов, азо - и диазосоединений. Механизмы реакций восстановления металлами и гидридами металлов.
Каталитическое восстановление молекулярным водородом. Достоинства и недостатки этого метода. Характеристика катализаторов. Никель Ренея, катализатор Линдлара. Механизм реакции. Восстановительное аминирование карбонильных соединений. Техника безопасности при проведении процессов восстановления на производстве.
8. ОКИСЛЕНИЕ (5 часов)
Реакции окисления. Окислители и катализаторы процессов окисления. Окисление бензола, нафталина и антрацена по ароматическому кольцу. Окисление боковых цепей алкиларенов и гетероциклических соединений до альдегидов и карбоновых кислот. Получение никотиновой кислоты. Автоокисление. Механизм реакции окисления кумола. Окисление серусодержащих соединений.
9. Методы образования углерод-углеродной связи.
Реакции конденсации (5 часов)
Конденсации арилгалогенидов с непредельными соединениями, катализируемые соединениями палладия. Механизмы реакций. Реакции конденсации карбонильных соединений: альдольная, Кляйзена-Шмидта, Перкина, Михаэля. Механизмы этих реакций. Реакции циклоприсоединения алкенов.
10. образование гетероциклов (5 часов)
Образование гетероциклических соединений. Получение 1,3-азолов циклизацией 1,4-дикарбонильных соединений. Получение бензимидазолов, бензтиазолов и бензоксазолов циклизацией N-ацилированных ароматических о-диаминов, о-аминофенолов, о-тиофенолов. Механизм получения хинолинов по Скраупу. Особенности реакций замещения в гетероциклических соединениях.
11. Защитные группы в синтезе (2 часа)
Защита спиртов образованием простых и сложных эфиров. Ацетальная и кетальная защита диолов. Защита карбоксильной и карбонильной групп. Защита аминогрупп (бензилоксикарбонильная, тритильная, ацетильная). Защита кратных связей. Выбор необходимой защиты и удаление защитных групп.
ЛАБОРАТОРНЫЕ ЗАНЯТИЯ (32 часа)
Теоретические знания, полученные на лекциях, закрепляются на лабораторных занятиях.
Во время лабораторных занятий студенты приобретают навыки работы с органическими соединениями и лабораторной посудой, а также закрепляют теоретический материал. Перед проведением эксперимента
они изучают методику синтеза, по справочникам находят характеристики соединений, участвующих и образующихся в данной реакции, проводят расчет синтеза и совместное обсуждение предстоящей работы с преподавателем. После окончания работы представляют отчет и защищают его.
Кроме этого на лабораторных занятиях студенты сдают коллоквиумы, на которых обсуждаются наиболее сложные теоретические вопросы, касающихся механизмов органических реакций, зависимости реакционной способности соединений от их строения.
Перечень лабораторных работ:
- Сульфирование. Получение бензолсульфокислоты, толуолсульфокислоты, 2-нафталинсульфокислоты, сульфаниловой кислоты.
- Нитрование. Получение нитробензола, 2,4-динитрохлорбензола, о- и п-нитротолуолов, нитробензолсульфокислоты.
- Галогенирование. Получение хлорбензола и о- и п-дихлорбензолов.
- Алкилирование и ацилирование. Получение диметиланилида, ацетанилида.
- Восстановление. Восстановление металлами. Получение анилина, о- и п-толуидинов, м-фенилендиамина, метаниловой кислоты (из нитробензола). Восстановление в щелочной среде. Получение бензидина, бензидинкарбоновой кислоты и бензидинсульфокислоты. Восстановление сернистыми щелочами. Получение м-нитроанилина, п-аминофенола, о-анизидина.
- Окисление. Получение бензойной, п-нитробензойной, антраниловой кислот.
- Конденсации. Получение салициловой кислоты, динитростильбендисульфокислоты, фенилметилпиразолона.
Каждый студент выполняет 3-4 синтетических задач (в зависимости от их сложности) или осуществляет многостадийный синтез заданного вещества, включающий 3-4 стадии. Лабораторный практикум охватывает основные разделы дисциплины и имеет необходимое методическое обеспечение.
САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ (112 часов)
Самостоятельная работа предусматривает изучение теоретического материала по лекциям и учебникам, выполнение домашних заданий, подготовку к лабораторным работам и контрольным работам, подготовку к сдаче коллоквиумов.
Планирование самостоятельной работы студентов
| Тема самостоятельной работы | Вид занятия | Технология организации самостоятельной работы | Контроль результатов самостоятельной работы | Бюджет времени, час. |
| Подготовка к многостадийному синтезу | Индивидуальное задание | Работа с литературой, Internet | Методики синтезов | 10 |
| Сульфирование и сульфохлорирование | Индивидуальное домашнее задание Подготовка к контрольной работе | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания. Контрольная работа №1 «Реакции SE ». | 10 |
| Нитрование, нитрозтрование, диазотирование | Индивидуальное домашнее задание Подготовка к контрольной работе | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания. Контрольная работа № 1 | 9 |
| Галогенирование. Алкилирование и ацилирование | Индивидуальное домашнее задание | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания. Контрольная работа №2 «Реакции SE». | 10 |
| Гидроксилирование и аминирование | Индивидуальное домашнее задание. Подготовка к колоквиуму | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания Коллоквиум «Гидроксилирование и аминирование» | 8 |
| Восстановление и окисление | Индивидуальное домашнее задание «Арены» | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания Контрольная работа №3 | 14 |
| Реакции конденсации | Индивидуальное домашнее задание «Спирты и фенолы» | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания Коллоквиум | 14 |
| Синтез гетероциклов | Индивидуальное домашнее задание «Гетероциклы» | Работа с конспектом, учебником. Выполнение домашнего задания. | Проверка домашнего задания Контрольная работа №4 | 12 |
| Все темы семестра | Подготовка к защите лабораторных работ | Работа с конспектом, учебниками, лабораторными практикумами, справочниками. | Отчет по лабораторной работе и её защита | 14 |
| Все темы курса | Подготовка к сдаче экзамена | Работа с конспектом, учебниками | Экзамен | 60 |
ТЕКУЩИЙ И ИТОГОВЫЙ КОНТРОЛЬ
Целью текущего и итогового контроля является не только проверка усвоения материала, но и оказание помощи студентам в вопросах, которые оказались для них сложными и не были поняты до конца. При изучении курса «Методы органического синтеза» используется рейтинговая система оценки знаний. В течение семестра студент может набрать 1000 баллов. Предусмотрены следующие виды контроля:
- выполнение домашних работ;
- контрольные работы и коллоквиумы;
- выполнение лабораторных работ с защитой.
Итоговый контроль результатов изучения дисциплины – зачет (10 семестр) и экзамен (11 семестр).
Общий рейтинг переводится в оценку следующим образом:
от 900 до 1000 баллов - "отлично"
от 780 до 900 баллов - "хорошо"
от 570 до 780 баллов - "удовлетворительно".
Состояние контролирующих материалов: имеются билеты входного контроля, текущего и рубежного контроля (самостоятельные и контрольные работы, коллоквиумы), экзаменационные билеты и билеты для зачета.
Образцы контролирующих материалов:
ВХОДНОЙ КОНТРОЛЬ
Билет № 1
- Даны три вещества: карбоновая кислота, альдегид и спирт. Молекулы всех веществ содержат одинаковое число атомов углерода. Выберите ряд, в котором вещества расположены в порядке увеличения температур кипения.
| 1) | кислота, альдегид, спирт |
| 2) | кислота, спирт, альдегид |
| 3) | альдегид, спирт, кислота |
| 4) | спирт, альдегид, кислота |
| Номер верного ответа: | |
- Какое из приведенных соединений не относится к классу фенолов?
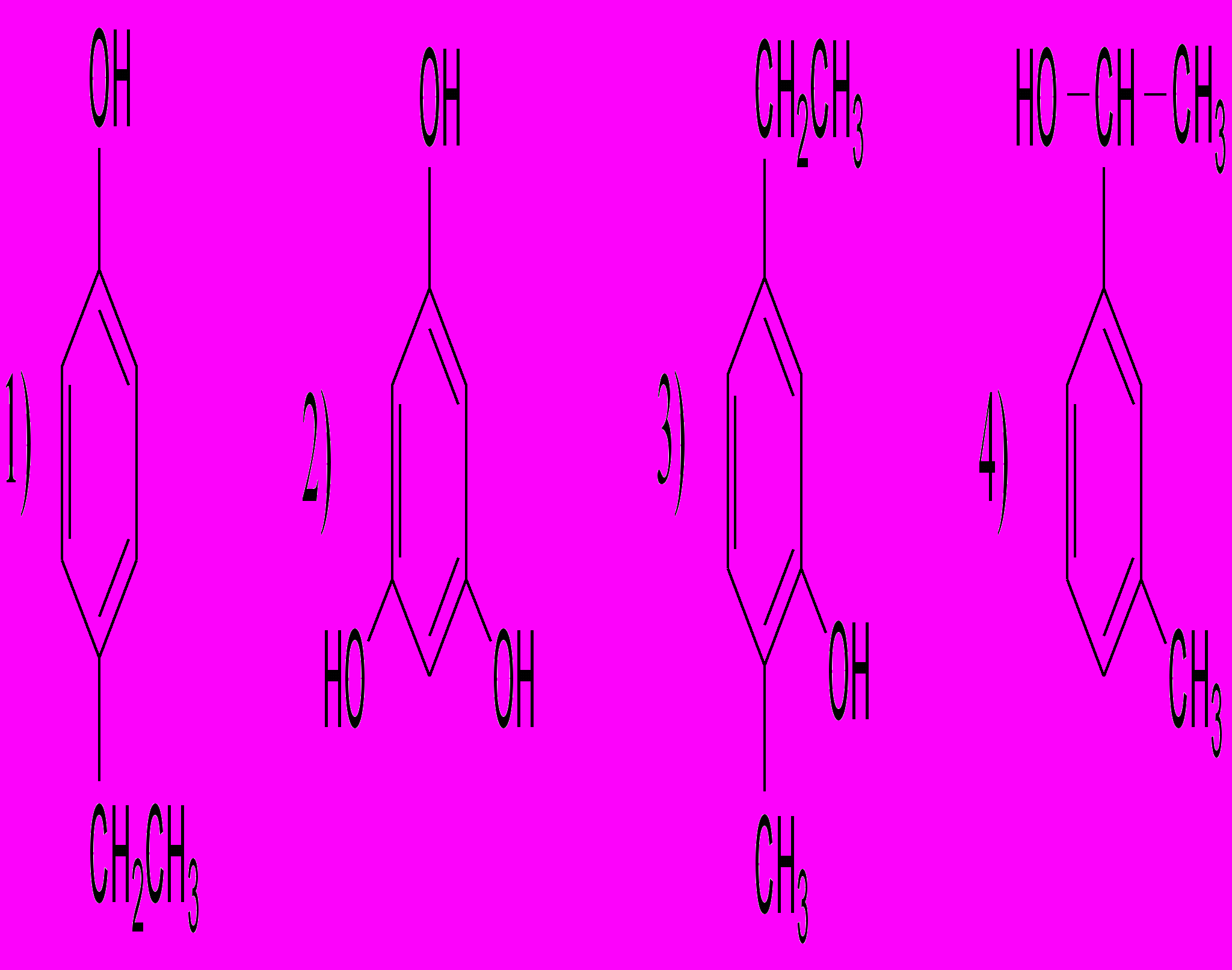
| Номер верного ответа: | |
- Для какого из приведенных соединений характерно явление оптической изомерии?
- 2-бромбутан
- 2-метилпропановая кислота
- 1-пропанол
- 2-хлорпропан
- Установите соответствие:
| | химическое превращение | | тип реакции |
| 1) | хлорирование этана | А) | нуклеофильное замещение |
| 2) | гидратация этилена | Б) | электрофильное замещение |
| 3) | гидролиз алкилгалогенида | В) | радикальное присоединение |
| 4) | алкилирование бензола | Г) | электрофильное присоединение |
| | | Д) | радикальное замещение |
| | 1) | 2) | 3) | 4) |
| Правильная последовательность элементов: | | | | |
5. Предскажите основной продукт (Б) в цепочке превращений:

-
1)

2)
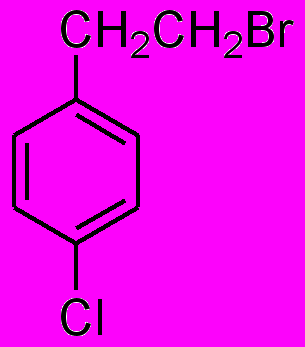
3)

4)

| Номер верного ответа: | |
6. Напишите структурную формулу соединения Х3 в цепочке превращений:

| Ответ: | |
7. Выберите последовательность реакций для рационального получения из бензола соединения, формула которого представлена на рисунке:
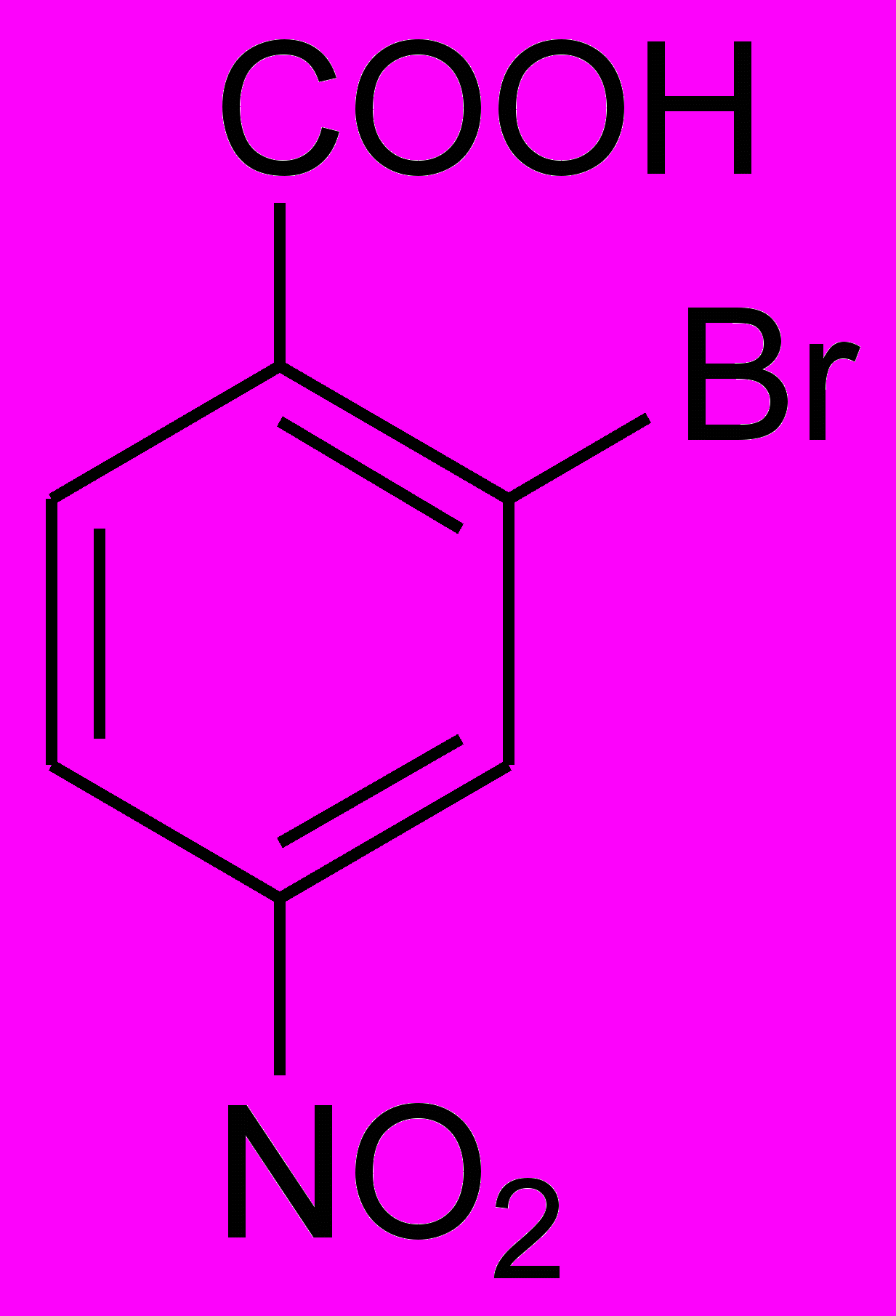
1) бромирование, нитрование, окисление, алкилирование
2) алкилирование, нитрование, бромирование, окисление
3) нитрование, алкилирование, окисление, бромирование
4) алкилирование, бромирование, окисление, нитрование
| Номер верного ответа: | |
8. Напишите реакцию альдольной конденсации бутаналя и отразите механизм реакции.
9. Используя реакцию азосочетания получите краситель:
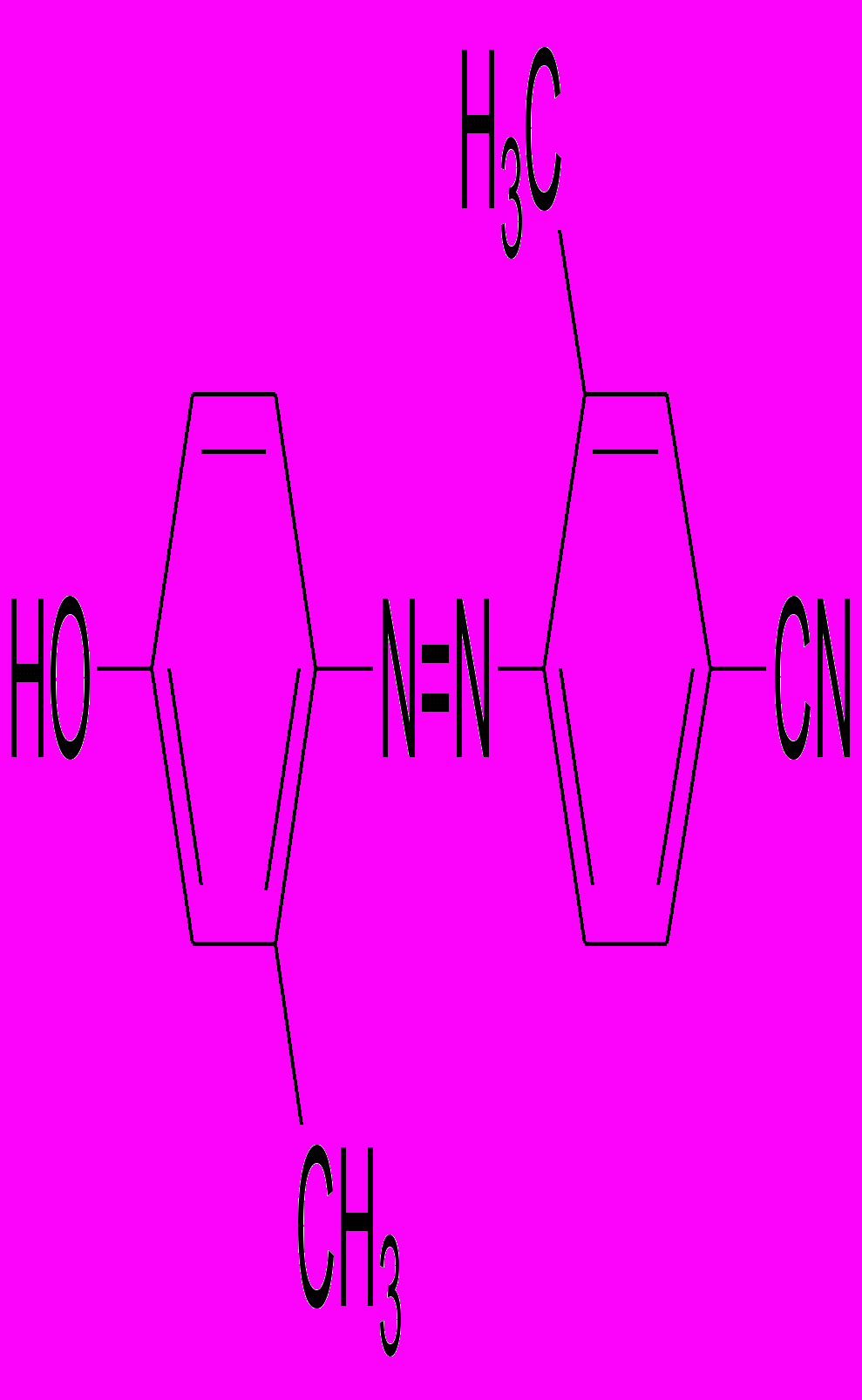
10. Какова структурная формула соединения С6Н6SO4, дающего окрашивание с хлорным железом, а при сплавлении с КОН и последующем подкислении образующего вещество состава С6Н6O2. При монобромировании конечного продукта образуется только один изомер. Напишите уравнения всех реакций.
ТЕКУЩИЙ КОНТРОЛЬ
КОНТРОЛЬНАЯ РАБОТА
“РЕАКЦИИ ЭлектофильноГО ароматичЕСКОГО замещениЯ”
билет № 1
- Нитрующие агенты и механизм реакции нитрования аренов в кольцо. Влияние различных факторов на процесс нитрования (температура, время реакции, характер субстрата, характер нитрующего агента, катализаторы).
- Для приведенного ниже соединение напишите реакцию внутримолекулярного алкилирования в присутствии H3РO4:
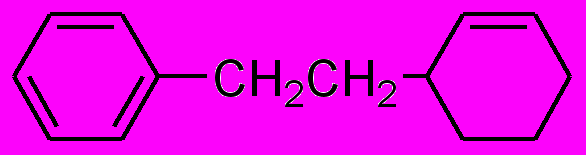
- В какое ядро и положение преимущественно вступает сульфогруппа при сульфировании следующих соединений:
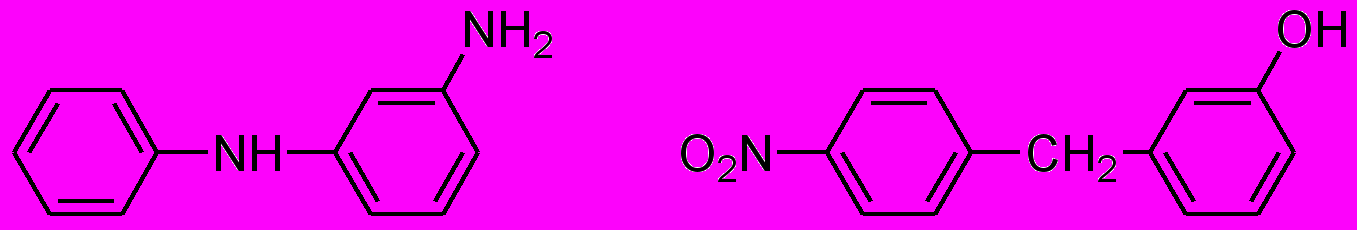
- Основные стадии промышленного хлорирования аренов. Требования, предъявляемые к аппаратуре в процессах хлорирования аренов.
КОЛЛОКВИУМ "ГИДРОКСИЛИРОВАНИЕ И АМИНИРОВАНИЕ"
Билет № 3
- Оксилирование и аминирование. Замещение галогенов на окси - алкокси - и аминогруппу в ароматических и алифатических соединениях. Механизмы реакций (SN1, SN2 и кине-замещение). Катализаторы в реакциях замещения хлора оксигруппой. Примеры промышленных синтезов.
- Осуществите превращение:
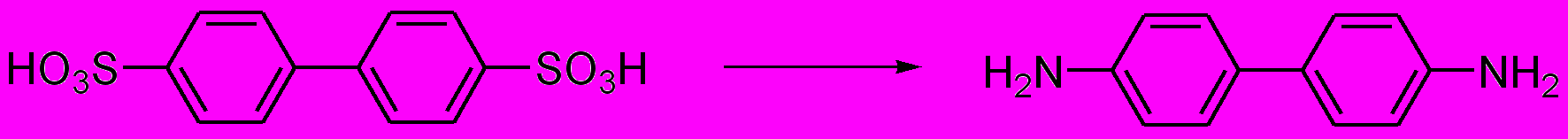
- Какие соединения образуются при нагревании с раствором щелочи следующих веществ:

Все соединения назовите.
РУБЕЖНЫЙ КОНТРОЛЬ
КОНТРОЛЬНАЯ РАБОТА № 2
Билет № 1
- Реакция диазотирования. Механизм реакции. Условия реакции диазотирования. Значение процессов диазотирования в синтезе.
- Осуществите следующие превращения:
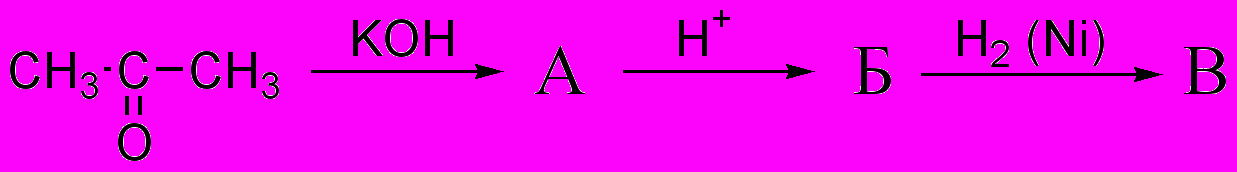
Приведите механизм первой стадии. Где находит применение конечный продукт В?
3. Напишите основные продукты реакции окисления:
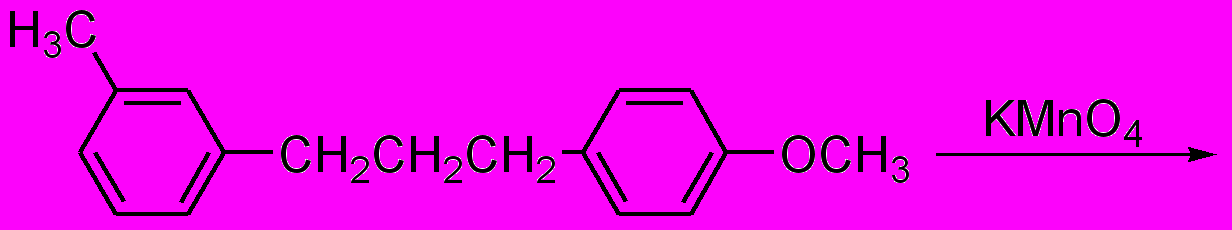
итоговЫЙ КОНТРОЛЬ
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ №1
- Сульфирование. Цели введения сульфогруппы в органические соединения. Сульфирующие агенты и механизм реакции сульфирования. Влияние концентрация кислоты, температура, времени реакции на процесс сульфирования. Характеристика методов сульфирования, их достоинства и недостатки. Требования к аппаратам для сульфирования. Выделение сульфокислот.
- Осуществите следующие превращения:

- Приведите механизм следующей реакции:

БИЛЕТ для зачета №2
- Ацилирование ароматических углеводородов, аминов и оксисоединений. Катализаторы и реагенты реакций ацилирования. Механизмы реакций. Сравнение реакционной способности ароматических аминов и фенолов, спиртов и фенолов в реакциях ацилирования.
- При нитровании ароматических соединений в присутствии ртути и её солей образуются полинитрофенолы:
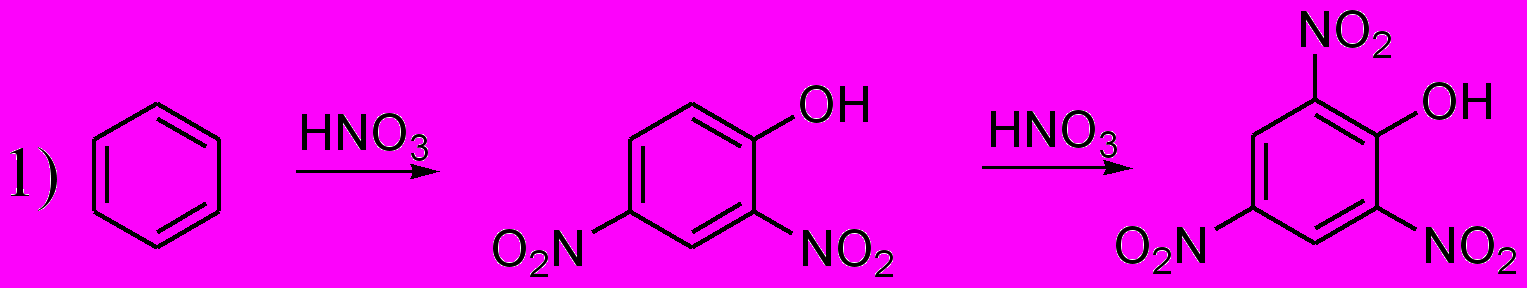
Объясните это явление.
- Расшифруйте следующую цепочку превращений и назовите продукты перечисленных реакций:

Учебно-методическое обеспечение дисциплины
Теоретическую часть курса студенты изучают по лекциям и используя литературу, рекомендованную в рабочей программе. Для закрепления изученного материала студенты решают задачи из сборника задач по методам органического синтеза.
Качество усвоения теоретической части курса оценивает преподаватель по результатам контрольных работ и коллоквиумов.
ПЕРЕЧЕНЬ РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
- Т.А. Сарычева. Методы органического синтеза. Томск: Изд-во Томского политехнического университета, 2009. – 98 с.
- Т.А. Сарычева. Сборник задач по методам органического синтеза. Томск: Изд-во Томского политехнического университета, 2009. – 17 с.
- Л.С.Эфрос, М.В. Горелик. Химия и технология промежуточных продуктов. Ленинград: Химия. 1980.
- Б.В. Пасет. Основные процессы химического синтеза биологически активных веществ. М.: Издательский дом «ГОЭТАР-МЕД». 2002.
- Б.В. Пассет, В.Я. Воробьева. Технология химико-фармацевтических препаратов и антибиотиков. М.: Медицина. 1977.
- Л.С. Эфрос, И.Я. Квитко. Химия и технология ароматических соединений в задачах и упражнениях. Ленинград: Химия. 1971.
- Р. Моррисон, Р. Бойд. Органическая химия. М.: Мир. 1974.
- Р. Маки, Д. Смит. Путеводитель по органическому синтезу. М.: Мир. 1985.
- П. Ласло. Логика органического синтеза. В 2-х т. М.: Мир. 1998.
- Защитные группы в органической химии./ Под ред. МакОми Дж. М.: Мир. 1979.
- Современные методы органического синтеза. Л. 1980.
- Пейн Ч., Пейн Л. Как выбирать путь синтеза органического соединения. М.: Мир. 1973.
- Матье Ж., Панико Р., Вейль-Рейналь Ж. Изменение и введение функций в органическом синтезе. М.: Мир. 1980.
- Г.Л. Мищенко, К.В. Вацуро. Синтетические методы органической химии. М.: Химия. 1982.
МЕТОДЫ ОРГАНИЧЕСКОГО СИНТЕЗА
Рабочая программа дисциплины
Разработчик Тамара Александровна Сарычева
Подписано к печати
Формат 60х84/16. Бумага офсетная
Печать RISO. Усл. печ. л. . Уч.-изд. л. .
Тираж экз. Заказ . Цена свободная.
Издательство ТПУ. 634050, Томск, пр. Ленина, 30.
Сарычева/ РП Методы органического синтеза - -
