Использование методов ик-фурье спектрометрии, масс-спектрометрии и газовой хроматографии для анализа фтора
| Вид материала | Документы |
- Методология анализа объектов различного происхождения методами газовой хроматографии-масс-спектрометрии, 1103.9kb.
- Масс-спектрометрия и резонансные методы. Часть I. Методы масс-спектрометрии, 397.85kb.
- Xii-е международное совещание проблемы прикладной спектрометрии и радиометрии ппср-2011, 133.02kb.
- Программа проведения Йошкар-Ола зао "скб, 56.45kb.
- Федеральная таможенная служба центральное экспертно-криминалистическое таможенное управление, 757.25kb.
- Курсовая работа по курсу " Химия и физико химические методы анализа" на тему " Методы, 218.07kb.
- Автоматизация измерений при масс-спектрометрии гексафторида урана на базе ми-1201 агм, 76.54kb.
- Физико-химические закономерности удерживания производных адамантана в высокоэффективной, 432.05kb.
- Программа обучения рассчитана на специалистов, которые не обладают достаточными знаниями, 3191.48kb.
- Определение содержания нефтепродуктов в пробах питьевых, природных и сточных вод методом, 73.13kb.
использование методов ИК-Фурье спектрометрии, масс-спектрометрии и газовой хроматографии для анализа фтора
Синкин И.М.1, Галата А.А.1, Волчков В.С.1, Матвеев А.А.1, Мурлышев А.П.1,
Буйновский А.С.2, Макасеев А.Ю.2
1ОАО «Сибирский химический комбинат», г. Северск
2ФГОУ ВПО «Северская государственная технологическая академия», г. Северск
E-mail: 1shk@seversk.tomsknet.ru, 2may@ssti.ru
Во второй половине 20 века в России были созданы мощнейшие производства молекулярного фтора. Необходимость в их создании была в использовании фтора в цикле переработки ядерных материалов и использовании в ракетной технике. В настоящее время фтор используется, помимо основного применения в производстве урановой продукции, в качестве одного из реагентов в производстве различных фторорганических соединений, хладонов, а также «электронных» газов, таких как гексафторид вольфрама, тетрафторид кремния, трифторид азота. Применение фторидов высокой чистоты в электронной промышленности предъявляет повышенные требования к содержанию примесей во фторе. Например, в гексафториде вольфрама, используемого в микроэлектронике, содержание примесей регламентируется на уровне 1…10 ppm (таблица 1).
Таблица 1 – Требования стандартов к концентрации примесей в гексафториде вольфрама
| Газ | Концентрация примесей, не более, ppmw | |||||||
| O2+Ar | N2 | CO2 | CO | CF4 | SF6 | SiF4 | HF* | |
| WF6 N30 [1] | – | – | – | 1 | 50 | | 50 | |
| WF6 N50 [1] | 1 | 1 | 1 | – | 5 | |||
| SEMI C3.52-0200 [2] WF6 99,996 % | 1 | 5 | 1 | 1 | 1 | 1 | 1 | 20 |
В требованиях спецификации на молекулярный фтор [3] в спецификации указаны только содержания азота и фтористого водорода.
Молекулярный фтор получают электролизом расплава KF×2HF c использованием графитовых электродов. Фтористый водород для получения электролита получают методом сернокислотного разложения плавикового шпата. Примеси определяются составом исходных продуктов – плавикового шпата, серной кислоты и материалом электродов. Таким образом, во фторе возможно присутствие таких примесей как фтористый водород, азот, кислород, монооксид углерода, диоксид углерода, карбонил-фторид, дифторид кислорода, тетрафторид кремния, гексафторид серы, трифторметан, тетрафторметан, гексафторэтан и октафторпропан, сульфурилфторид, фосфорилфторид.
Проблемой, решаемой в настоящее время, наряду с оптимизацией технологии очистки, является разработка методов анализа, позволяющих в полной мере проводить контроль производств.
При использовании получаемого фтора в производстве гексафторида вольфрама и для контроля систем очистки фтора от летучих примесей необходим количественный анализ фтора на содержание летучих примесей.
В настоящее время в России отсутствуют методики анализа всего спектра примесей во фторе. Для анализа фтора применимы различные методы – химический анализ, инфракрасная спектрометрия, газовая хроматография и масс-спектрометрия. Указанные методы наряду с их достоинствами имеют и ряд недостатков.
Метод инфракрасной спектрометрии позволяет анализировать фтор без предварительной пробоподготовки и определять вещества с высокой реакционной способностью при использовании кювет из никеля или монель-металла и оптических окон из лейкосапфира или фторидов кальция или бария. К недостаткам метода можно отнести невозможность определения полярных молекул, таких как кислород, азот, фтор и невозможность определения перфторалканов при их совместном присутствии из-за наложения спектров групп –CF2 и –CF3.
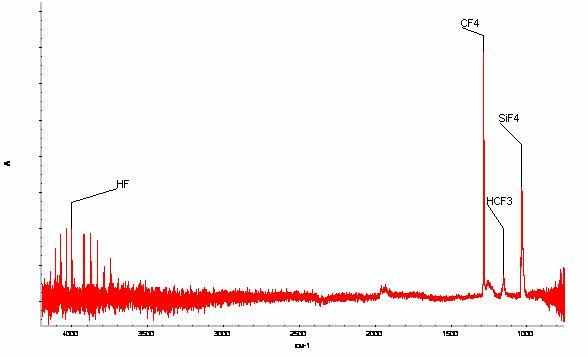
Рисунок 1 – Спектр поглощения (часть спектра) фтора на ИК-спектрометре «Nexus 5700» на кювете с l = 0,15 м и окнами из CaF2, диапазон измерений 4200…700 см–1, скорость зеркала – 0,6329, число сканирований – 20, апертура – 16, разрешение 0,5 см–1, давление пробы – 735 мм рт. ст.

Рисунок 2 – Спектр поглощения фтора на ИК-спектрометре «Nexus 5700» (часть спектра) на кювете с l = 10 м и окнами из AgCl, диапазон измерений 4200…700 см–1, скорость зеркала – 0,6329, число сканирований – 20, апертура – 16, разрешение 0,5 см–1, давление пробы – 5 мм рт. ст.
Для измерений использовали предварительно пассивированные фтором кюветы, изготовленные из никеля, с оптическими окнами из CaF2 и AgCl и длиной оптического пути 0,15 и 10 м.
Как видно из рисунков 1 и 2, на которых представлены ИК-спектры фтора на различных кюветах, в электролизном газе присутствуют такие примеси как фтористый водород, тетрафторметан, трифторметан, тетрафторид кремния, гексафторид серы, дифторид кислорода, диоксид углерода.
В таблице 2 указано минимальное и максимальное содержание определяемых ИК-методом соединений во фторе.
Таблица 2 – Результаты анализа фтора методом инфракрасной спектрометрии с Фурье преобразованием, % об.
| Диапазон содержания | HF | CF4 | SiF4 | SF6 | CHF3 | OF2 |
| Миним. | 3,6 | 0,0030 | 0,0030 | 0,0005 | 0,0005 | 0,0008 |
| Максим. | 9,7 | 0,0250 | 0,0112 | 0,0085 | 0,0075 | 0,0097 |
Масс-спектрометрический способ является универсальным способом анализа, позволяет анализировать примеси во фторе относительным методом. Трудности количественного определения состоят в сложности приготовления многокомпонентных смесей, аппаратурной сложности. Наряду с этим, масс-спектрометрия позволяет охватить практически весь спектр примесей во фторе. Анализ фтора проводили на масс-спектрометре МИ1201В с ионизацией электронным ударом.
Масс-спектрометрический способ не позволяет разделить вещества, дающие при ионизации ионы с одинаковыми массами. Так масс-спектрометрия не позволяет разделить азот и монооксид углерода. Возможно только их суммарное определение. В таблице 3 представлены анализируемые соединения и характеристические ионы.
Таблица 3 – Результат (усреднённый) масс-спектрометрического анализа фтора (с электролизёра), % об.
| Соединение | O2 | N2, CO | CO2 | CF4 | C2F6 | C3F8 | OF2 | COF2 | SO2F2 | POF3 | CHF3 | SiF4 | HF | |
| Определяе-мый ион | O2+ | N2+ | CO+ | CO2+ | CF3+ | C2F5+ | C3F7+ | OF2+ | COF+ | SO2F2+ | POF3+ | CHF2+ | SiF3+ | HF+ |
| m/e | 32 | 28 | 28 | 44 | 69 | 119 | 169 | 54 | 47 | 102 | 104 | 51 | 85 | 20 |
| Концентра-ция, % об. | 0,11 | 1,42 | 0,01 | 0,01 | 0,001 | 0,001 | 0,0005 | 0,017 | 0,0024 | 0,0012 | 0,0007 | 0,008 | 6,7 | |
Метод газовой хроматографии позволяет определять кислород, аргон, азот, перфторалканы, карбонилфторид с достаточной точностью и чувствительностью. Однако сложностью прямого хроматографирования является то, что фтор – самый активный и самый агрессивный химический элемент в природе. Большинство металлов взаимодействует с фтором при обычной температуре, но многие из них образуют стойкую защитную пленку, препятствующую дальнейшей реакции. Наилучшими материалами для конструирования хроматографической аппаратуры при работе с фтором и его соединениями является никель, не реагирующий с фтором даже при 600 °С, а также некоторые сплавы, например сплав платина-иридий и монель. Неорганические соединения фтора и многие межгалоидные соединения реагируют почти со всеми органическими веществами, в том числе и с политетрафторэтиленом (фторопласт-4) и политрифторхлорэтиленом (фторопласт-3).
Поэтому для хроматографического определения реакционноспособных галогенсодержащих неорганических газов используют два основных способа анализа:
- прямое хроматографирование агрессивных и реакционноспособных газов на полностью инертных сорбентах и на специальной хроматографической аппаратуре;
- превращение реакционноспособных газов в инертные (чаще всего органические) производные с последующим их определением на колонках с традиционными хроматографическими насадками и с использованием высокочувствительных ионизационных детекторов.
Пассивация системы осуществлялась трифторидом хлора до анализа фтора, обрабатывались все внутренние поверхности соединительных трубок, кранов, для образования на стенках устойчивых комплексов:
6NiO(тв) + 14ClF3(газ) → 6NiF3(тв) + 2Cl2(газ) + 3O2(газ).
Для исключения контакта газа с атмосферной влагой смонтирована вакуумная схема, позволяющая обеспечить представительность отбора газа, а также метод определения содержания лимитирующих примесей во фторе с использованием многомерной газовой хроматографии.
Для анализа фтора была разработана вакуумная система напуска, позволяющая проводить осушку и продувку газовых линий (рисунок 3).
На сегодняшний день проведены исследования газохроматографического метода анализа фтора на содержание кислорода и азота с использованием детектора по теплопроводности и многомерной газовой хроматографии и хроматографических колонок с цеолитами, углями, полисорбами и хромосорба Т с нанесенной жидкостью «Kel F № 10».

БПС – баллон с пробой или образцом; БПГ – баллон с продувочным газом
Рисунок 3 – Вакуумная система напуска для анализа фтора
Сорбенты на основе сополимера дивинилбензол стирола, используемые для анализа постоянных газов – это Porapak Q, Hayesep Q или российские аналоги – полисорбы, обладающие достаточной универсальностью и используемые для разделения различных газов – не стойки по отношению к основному компоненту. Колонки на основе дивинилбензол стирола разрушаются при контакте с молекулярным фтором.
Алюмосиликатные молекулярные сита поглощают F2 с образованием AlF3 и SiF4, что приводит к разрушению колонки с каждым вводом пробы.
Ввиду отсутствия специализированных хроматографов для работы с агрессивными фторсодержащими средами была разработана схема для стандартных детектирующих систем с использованием удаления пиков агрессивных веществ (многомерная газовая хроматография). Схема позволяет использовать обычные разделительные колонки и стандартное оборудование. Основой схемы является десятипортовый кран, основа схемы показана на рисунке 4.
Во время анализа кран обратной продувки переключается после элюирования примесей, при этом компонент, остается в тефлоновой колонке и не входит в контакт с обычными аналитическими колонками и детектором.
Для анализа примесей во фторе наиболее приемлемый детектор отечественных производителей – детектор по теплопроводности («Цвет», «Кристалл»), позволяющий определять примеси на уровне 5…10 ppmv.
Во фторе было определено содержание кислорода, азота и монооксида углерода. Также метод позволяет определить карбонилфторид, монооксид и диоксид углерода, перфторалаканы. Однако для этого требуется подбор разделительных колонок, поглотителя и режимов разделения.
Среди аналитических методов наиболее приемлемыми для анализа трифторида азота являются масс-спектрометрия, ИК-Фурье спектрометрия и газовая хроматография. Анализ всего спектра примесей во фторе возможно лишь комбинированием различных методов анализа.

Колонка 1 – предколонка с хромосорбом Т с НЖФ кель Ф № 10;
колонка 2 – хроматографическая колонка с порапак Q (цеолит NaX)
Рисунок 4 – Газовая схема разделения летучих примесей от гексафторида вольфрама
В таблице 4 показаны возможности аналитических методов по определению всего спектра примесей в молекулярном фторе.
Таблица 4 – Возможности методов по определению летучих примесей во фторе, % об.
| Соединение/ метод | O2 | N2 | CO | CO2 | CF4 | C2F6 | C3F8 | OF2 | COF2 | SO2F2 | POF3 | CHF2 | SiF4 | HF |
| МС | + | – | – | – | + | + | + | + | + | + | + | + | + | + |
| ГХ | + | + | + | + | + | + | + | + | + | – | – | + | – | – |
| ИК | – | – | + | – | – | – | – | + | + | – | – | + | + | + |
Таким образом, из проделанных экспериментов можно сделать вывод о возможности анализа всего спектра примесей во фторе лишь комбинацией аналитических методов. Одним из вариантов такого анализа является сочетание масс-спектрометрии, ИК-Фурье спектрометрии и многомерной газовой хроматографии с использованием селективных поглотителей.
Используемая литература
1 Спецификация на WF6 «AirLiquide».
2 Стандарт SEMI C3.52-0200. Гексафторид вольфрама.
3 Спецификация на молекулярный фтор F2 98 % «Boc Gases».
4 Анваер Б.И., Другов Ю.С. Газовая хроматография неорганических веществ. –М.: Химия, 1976. – С. 240.
5 Другов Ю.С., Родин А.Н. Газохроматографический анализ газов. – Санкт-Петербург, 2002.
