Алюмотермия: 3MnO 2 + 4Al 2Al
| Вид материала | Документы |


Электронная конфигурация валентного слоя

Получение
Природное соединение – ПИРОЛЮЗИТ MnO2
Алюмотермия: 3MnO2 + 4Al
 2Al2O3 + 3Mn
2Al2O3 + 3Mn Характерные степени окисления и соединения.
| +2 | +4 | +6 | +7 |
| MnO – основный оксид Mn(OH)2 Соли – с кислотами: MnCl2, MnSO4 (бесцветные) | MnO2 (пиролюзит) (бурый осадок) | Соли – манганаты K2MnO4 (зеленые) | Mn2O7 Кислотный оксид (зеленая жидкость) |
| Марганцевая кислота HMnO4 Соли – перманганаты KMnO4 (фиолетовые) |
Химические свойства
При нагревании марганец взаимодействует с кислородом, галогенами, серой. При взаимодействии марганца с кислородом образуется диоксид марганца:
Mn + O2 MnO2 Mn + S
 MnS
MnS Растворяется в кислотах-неокислителях:
Mn + 2HCl
 MnCl2 + H2
MnCl2 + H2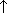
С концентрированной серной кислотой реакция идёт по уравнению:
Mn + 2H2SO4(конц.) → MnSO4 + SO2↑ + 2H2O
С разбавленной азотной кислотой реакция идёт по уравнению:
3Mn + 8HNO3(разб.) → 3Mn(NO3)2 + 2NO↑ + 4H2O
В щелочном растворе марганец устойчив.
Соединения Mn(II)
Оксид марганца (II) MnO получается восстановлением природного пиролюзита MnO2 водородом:
MnO2 + H2
 MnO + H2O
MnO + H2OГидроксид марганца (II) Mn(OH)2 - светло-розовое нерастворимое в воде основание: MnSO4 + 2NaOH
 Mn(OH)2
Mn(OH)2 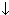 + Na2SO4
+ Na2SO4Гидроксид марганца (II) Mn(OH)2 в водных растворах проявляет основные свойства, то есть растворяется в кислотах, но не растворяется в щелочах: Mn(OH)2↓ + 2HCl = MnCl2+ 2H2O
В присутствии солей аммония Mn(OH)2 легко растворяется. Возможность протекания данной реакции обусловлена тем, что ее продукт — гидроксид аммония, гораздо более слабое основание, чем гидроксид марганца (II):
Mn(OH)2 + 2NH4Cl = MnCl2 + 2NH4OH
На воздухе Mn(OH)2 быстро темнеет в результате окисления:
2Mn(OH)2 + O2
 2MnO2 + 2H2O
2MnO2 + 2H2OМарганец (II) образует различные соли, в том числе сульфиды. Сульфид марганца (II) можно получить прямым синтезом или по обменным реакциям в растворах: MnSO4 + (NH4)2S = MnS↓+ (NH4)2SO4
Соединения Mn(IV)
Оксид марганца (IV) MnO2 - тёмно-коричневый порошок, нерастворимый в воде.
Образуется при термическом разложении нитрата марганца (II):
Mn(NO3)2 MnO2 + 2NO2
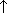
При сильном нагревании теряет кислород, превращаясь в Mn2O3 (при 6000C) или Mn3O4 (при 10000C).
Сильный окислитель в кислой среде, переходит в +2:
MnO2 + 4HCl MnCl2 + Cl2
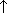 + 2H2O
+ 2H2O Под действием сильных окислителей в сплаве со щелочью переходит в степень окисления +6:
MnO2 + Na2CO3 + NaNO3 (спл) Na2MnO4 + NaNO2 + CO2
Соединения Mn(VI)
Степень окисления +6 у марганца наименее устойчива: существует только в сильнощелочном растворе в виде солей зеленого цвета – МАНГАНАТОВ.
Манганаты получаются при восстановлении перманганатов в щелочной среде:
Na2SO3 + 2KMnO4 + 2KOH Na2SO4 + 2K2MnO4 + H2O; или при окислении солей и оксидов марганца +2 и +4 сильными окислителями в присутствии щелочи:
3MnSO4 + 2KClO3 + 12KOH (спл) 3K2MnO4 + 2KCl + 3K2SO4 + 6H2O
Водой манганаты быстро разлагаются
(диспропорционируют на +7 и +4):
3K2MnO4 + 2H2O
 2KMnO4 + MnO2 + 4KOH
2KMnO4 + MnO2 + 4KOHМанганаты можно легко окислить хлором:
2K2MnO4 + Cl2 2KMnO4 + 2KCl
Соединения Mn(VII)
Оксид марганца (VII) Mn2O7 - тёмно-зелёная жидкость, кислотный оксид. Получают действием концентрированной серной кислоты на кристаллический KMnO4 (марганцевая кислота HMnO4 нестабильна):
2KMnO4 + H2SO4
 Mn2O7
Mn2O7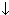 + K2SO4 + H2O
+ K2SO4 + H2OПри растворении в щелочах образует перманганаты:
Mn2O7 + 2KOH
 2KMnO4 + H2O
2KMnO4 + H2OПерманганат калия KMn+7O4 -тёмно-фиолетовое кристаллическое вещество, растворимое в воде. При нагревании разлагается с выделением кислорода: 2KMnO4 K2MnO4 + MnO2 + O2
При стоянии в растворе постепенно распадается:
4KMnO4 + 2H2O 4MnO2 + 4KOH + 3O2
Под действием серной кислоты (60%) и горячей щелочи перманганат также выделяет кислород:
4KMnO4 + 6H2SO4 4MnSO4 + 5O2 + 2K2SO4 + 6H2O
4KMnO4 + 4KOH –(t) 4K2MnO4 + O2+ 2H2O
Перманганат калия с восстановителями в разных средах:
 | KMnO4 (малиновый раствор) + восстановитель   | | ||
| кислая среда: Mn2+ (MnCl2, MnSO4) обесцвечивание | нейтральная среда: Mn +4 (MnO2↓ бурый осадок) | щелочная среда: Mn+6 (K2MnO4, зеленый раствор) | ||
Повышение степеней окисления марганца:
| Mn+2,+4 – оксид, гидроксид, соли | + очень сильные окислители: KNO3, кислородсодержащие соли хлора (в расплаве) | Щелочная среда: Mn+6 Образуется: K2MnO4 – манганат |
| Mn+2 – соли | + очень сильные окислители: PbO2, KBiO3 | Кислая среда: Mn+7 Образуется: KMnO4- перманганат HMnO4 - марганцевая кислота |
