Н. М. Эмануэля ран защита состоится 27 сентября 2011 г в 13
| Вид материала | Автореферат |
- Кинетика ферментативного гидролиза полипептидов и гидрофобные эффекты, 573.63kb.
- Автореферат диссертации на соискание ученой степени, 275.48kb.
- Трудовой потенциал пореформенной России: социально-демографические аспекты, 601.55kb.
- Которая состоится 8 сентября 2011 года в Москве, 15.37kb.
- Программа саратов, 12 15 сентября 2011 г. Научный совет ран по акустике Общественная, 576.97kb.
- Примерная программа конференции: Заезд участников конференции 12 сентября 2011 г. Регистрация, 91.77kb.
- Особенности биологии донных и придонных рыб, 1533.54kb.
- Онтология, эпистемология и диалектика Николая Кузанского, 335.03kb.
- Эволюция итальянской проповеди XIV-XV, 600.86kb.
- История и миф в операх Сергея Слонимского, 335.75kb.
Приведены результаты исследования спектров вторичного фотонного излучения, возникающего при облучении образцов костной ткани нейтронами, фотонами и протонами разной энергии. Исследование спектров, снятых в динамике после облучения разной продолжительности, заключалось в идентификации радионуклидов по энергии излучения и периоду полураспада, а также в оценке наличия и влияния интерференций. На основании полученных результатов было разработано 9 методик недеструктивного in vitro анализа образцов костной ткани. Разработка методик включала: 1) выбор оптимальных режимов облучения и измерения образца (время, геометрия, масса) на основе алгоритма оптимизации – максимальное число определяемых элементов при минимальном числе облучений и измерений; 2) подбор адекватных эталонных (калибровочных) образцов; 3) создание программы обработки спектров вторичного фотонного излучения образцов и эталонов с учётом интерференций, а также расчёта содержания элементов в исследуемом образце; 4) оценку статистической погрешности и предела определения элементов.
Глава 2. Метрологические характеристики и сопоставление возможностей разработанных методик in vitro анализа.
Проведена оценка внутрилабораторного контроля качества данных, получаемых с помощью разработанных методик in vitro анализа.
С этой целью для каждого метода в соответствии с ГОСТ Р ИСО 5725 – 2002 и Приказом Министерства здравоохранения Российской Федерации от 7 февраля 2000 года за № 45 «О системе мер по повышению качества клинических лабораторных исследований в учреждениях здравоохранения Российской Федерации» определялись все необходимые метрологические характеристики.
Показано, что разработанный комплекс из 9 методик позволяет надёжно определять содержание не менее 22 химических элементов и контролировать верхний уровень содержания ещё 19 элементов (табл. 2). При оценке точности использовали международные сертифицированные материалы сравнения для костной ткани - IAEA H-5 (Animal bone) и NIST SRM1486 (Bone Meal).
Таблица 2. Возможности разработанных методик определения содержания химических элементов в образцах костной ткани.
| Методика (Источник излучения, регистрирующий прибор) | Определяемые элементы (контролируемые элементы) | Количество образцов за 7 часовую смену | Количество элементо- определений за 7 часовую смену |
| NAA-SL Ядерный реактор, ППД | Ca, Cl, Mg, Na, P Ca, Cl, K, Mg, Mn, Na, P, Sr | 30 10 | 150 80 |
| NAA-LL Ядерный реактор, ППД | Ag, Co, Cr, Fe, Hg, Rb, Sb, Sc, Se, Tb, Zn (As, Au, Ba, Br, Cd, Ce, Cs, Eu, Gd, Hf, La, Lu, Nd, Sm, Ta, Th, U, Yb, Zr) | 1-2 | 30-60 |
| NAA 14 МэВ генератор, NaJ(Tl) | N, P | 40 | 80 |
| GAA ЛУЭ-25, γ-γ | F, N, P N, P | 4 10 | 12 20 |
| GAA ЛУЭ-25, ППД | Ca, Mg, Sr | 4 | 12 |
| PIGE Ускоритель протонов, ППД | F [Ca, Mg, Na, P] | 10-20 | 10-20 [50-100] |
| EDXRF 109Cd, ненасыщенный слой | Ca, Fe, Zn, Sr, (Pb) | 5-10 | 20-40 (25-50) |
| EDXRF 109Cd, насыщенный слой | Ca, Fe, Zn, Sr, (Pb) | 10-20 | 40-80 (50-100) |
| EDXRF 241Am, насыщенный слой | Ва | 6 | 6 |
NAA-SL – и NAA-LL – нейтронно-активационный анализ по коротко - и долгоживущим радионуклидам, соответственно, GAA – гамма активационный анализ (ППД - измерения на спектрометрической установке высокого разрешения, γ- γ - измерения на установке γ-γ–совпадений;), PIGE –индуцированный протонами гамма-эмиссионный анализ, [ ] –элементы, потенциально доступные определению методом PIGE, EDXRF – энерго-дисперсионный рентгенофлуоресцентный анализ, ( ) – элемент может быть определен, если его содержание превышает приведенный ПО.
Глава 3. Спектрометрическое исследование вторичных фотонов при in vivo облучении участков скелета и зубов с целью разработки методик определения содержания в них химических элементов.
Разработка in vivo методов анализа включала все этапы, необходимые при in vitro исследованиях, но с учётом ряда ограничений и дополнительных требований. Среди них: ограничения по времени обследования (комфортность процедуры); ограничения по поглощённой дозе (необходимость дозиметрических исследований); обеспечение равномерного флуенса тепловых нейтронов в исследуемом объёме (необходимость исследования пространственного распределения тепловых нейтронов); обеспечение равномерной вероятности регистрации используемых фотонов в исследуемом объёме (необходимость исследования пространственного распределения вероятности регистрации фотонов).
В ходе разработки in vivo нейтронно-активационного анализа (NAA) нами были сформулированы требования к источнику нейтронов, наиболее адекватному для парциальных вариантов метода: средняя энергия испускаемых нейтронов около 5 МэВ; достаточная интенсивность и высокая стабильность выхода нейтронов; возможность использования нескольких источников; портативность (малогабаритность); возможность погружения источников в воду. В наибольшей степени этим требованиям удовлетворяли ампулированные (α,n)-источники, среди которых наиболее оптимальными являлись 238Pu-Be-источники. Было показано, что для in vivo NAA содержания Са необходимо не менее пяти 238Pu-Be-источников с выходом 5·107 нейтронов·с-1.
Пространственное распределение поглощенной дозы от излучения 238Pu-Be-источника в «бесконечной» водной среде. Дозу нейтронов рассчитывали по показаниям соответствующих детекторов как дозу первого соударения (керму). Пространственное распределение тканевой кермы быстрых и промежуточных нейтронов определяли с помощью трековых детекторов с делящимся нуклидом 237Np [Крайтор С.Н., 1979]. Керму тепловых нейтронов рассчитывали по флуенсу тепловых нейтронов, измеренному фольгами из индия и 6Li-НЦ-детекторами [Зайчик В.Е. и др., 1973]. Кроме того, вклад в керму нейтронов различных энергетических групп оценивали с помощью радиометра КРАН-IН. Дозу гамма-излучения измеряли термолюминесцентными алюмофосфатными стеклами [Бочвар И.А. и соавт., 1972; 1977]. Изменения с расстоянием мощностей кермы нейтронов и поглощенной дозы гамма-излучения от 238Pu-Be-источника, расположенного в воде, представлены на рис 1.
Пространственное распределение эффективности регистрации вторичного фотонного излучения сцинтилляционными детекторами. Спектрометрические установки, предназначенные для in vivo нейтронно-активационного анализа, из-за ограничений по поглощенной дозе должны обладать как можно более высокой эффективностью регистрации гамма-излучения, наведенного в исследуемом участке тела человека при облучении нейтронами. Помимо этого, их разрешающая способность должна быть достаточной для прецизионного различения аналитических фотопиков на спектрах. Предстояло выяснить, с какой вероятностью γ-квант с энергией вплоть до 3085 кэВ будет зарегистрирован спектрометром в фотопике полного поглощения в зависимости от точки возникновения γ-кванта по отношению к кристаллу спектрометра. Эту вероятность обозначили как функцию отклика детектора Фотк (Еγ, H, R), где Еγ – энергия γ-кванта, H и R – координаты возникновения γ-кванта относительно кристалла детектора. Измерение Фотк проводили для трех энергий γ-квантов: 661, 1369 и 2754 КэВ. В качестве источника γ-квантов с энергией 661 КэВ использовали образцовый спектрометрический гамма-источник 137Cs из набора ОСГИ. Для получения γ-квантов с энергией 1369 и 2754 КэВ использовали источники с радионуклидом 24Na. В качестве примера Фотк, выраженная в %, при расположении источника на геометрической оси вращения кристалла детектора (R=0) для гамма-излучения с энергией 661 и 2754 КэВ представлена на рис. 2.
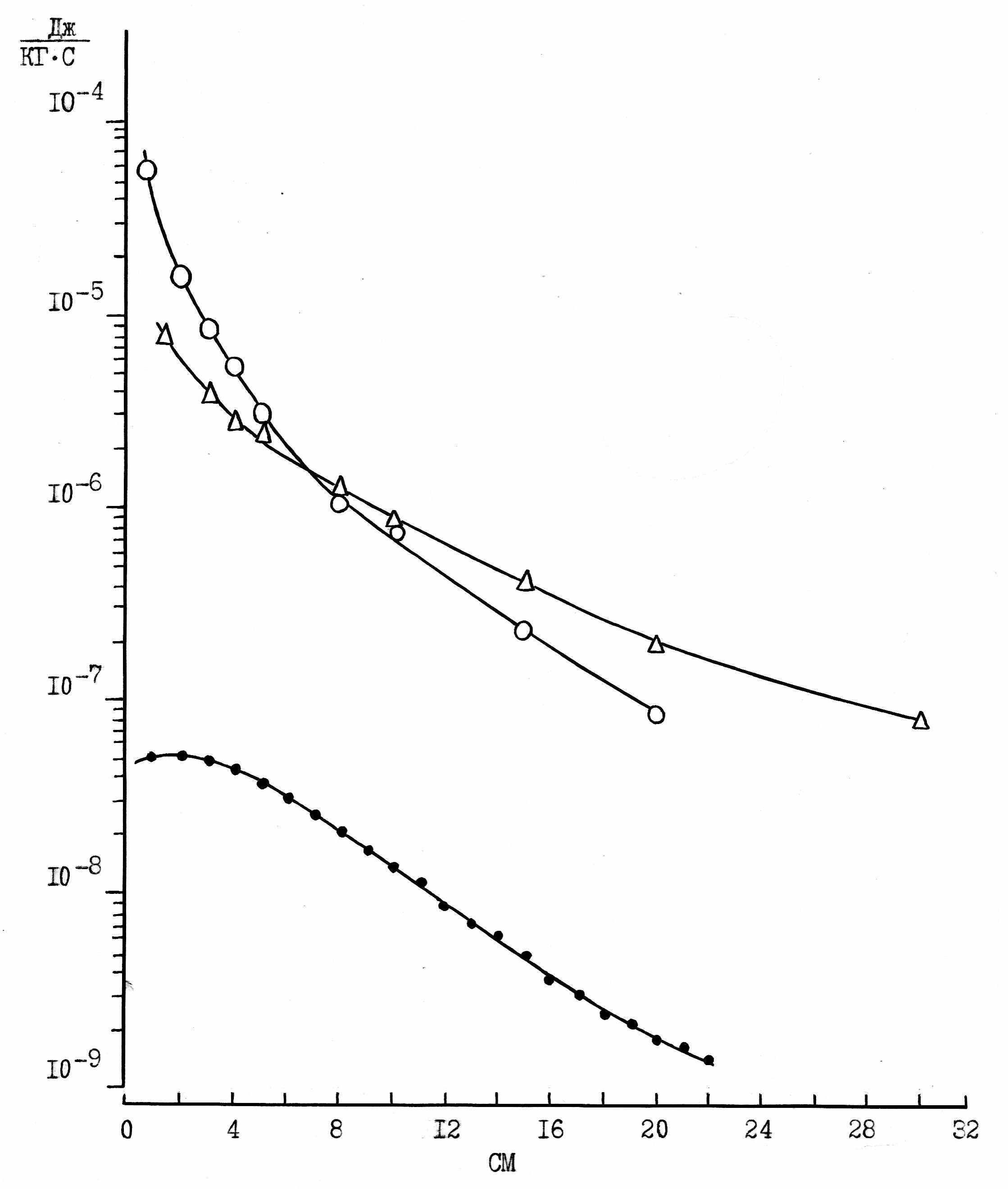
Рис. 1. Изменения мощности кермы быстрых и промежуточных нейтронов (○), тепловых нейтронов (•), а также мощности поглощенной дозы гамма-излучения (∆) с расстоянием от поверхности 238Pu-Be-источника с выходом 5·107 нейтрон·с-1, расположенного в воде
(Дж·кг-1·с-1 = Гр·с-1).
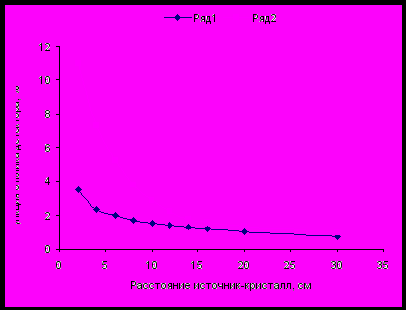
Рис. 2. Зависимость значение функция отклика детектора Фотк (Еγ, H, R) от расстояния H при R =0 и Еγ, равном 661 кэВ (ряд 2) и 2754 кэВ (ряд 1).
Полученные данные о пространственном распределении флуенса тепловых нейтронов и дозовых полях, создаваемых 238Pu-Be-источником с выходом 5·107 нейтронов·с-1 в водной среде, а также о полях эффективности регистрации γ-квантов с энергией до 3000 КэВ для детектора с кристаллом NaI(Tl) размером Ø150×100 мм, позволили разработать ряд установок для облучения и спектрометрического измерения, необходимых для реализации in vivo NAA содержания Ca, Na и Cl в участках тела человека.
По результатам исследования вторичного фотонного излучения, возбуждаемого в образцах костной ткани излучением от источника с радионуклидом 109Cd, были разработаны методика и устройство для in vivo определения содержания Zn, Sr и Pb в коронке зуба.
Таким образом, в главе 3 приведено описание трёх разработанных методов in vivo анализа: 1) In vivo NAA содержания Са в кисти, стопе и позвоночнике (поясничный, грудной и шейный отдел – вместе и порознь); 2) in vivo NAA содержания Са, Na и Cl, а также отношений Na/Ca, Cl/Ca и Na/Cl в очаге поражения костной ткани; 3) in vivo EDXRF содержания Ca, Sr, Zn и Pb в эмали зубов.
Глава 4. Результаты исследования содержания химических элементов в
образцах здоровой костной ткани и зубов.
Методом in vitro нейтронно-активационного анализа на нейтронах ядерного реактора с регистрацией излучения короткоживущих радионуклидов проведено определение содержания Ca, Cl, K, Mg, Mn, Na, P и Sr во всех образцах костей и зубов, взятых у здоровых людей. Помимо этого, в этих образцах методом in vitro нейтронно-активационного анализа на нейтронах ядерного реактора с регистрацией излучения долгоживущих радионуклидов проведено определение содержания Ag, As, Au, Ba, Br, Ca, Cd, Ce, Co, Cr, Cs, Eu, Fe, Gd, Hf, Hg, La, Lu, Nd, Rb, Sb, Sc, Se, Sm, Sr, Ta, Tb, Th, U, Yb, Zn и Zr, а в поперечных срезах ребра дополнительно методом PIGE – содержание F. Протокол содержания химических элементов в исследованных тканях представлен на примере анализа поперечного среза ребра в табл. 3.
Все приведенные в таблице 3 статистические параметры рассчитывали только для тех элементов, содержание которых было выше предела определения (ПО) в большинстве исследованных образцов. Для элементов, содержание которых в большинстве образцов было ниже ПО, рассчитывали средний наибольший из возможных уровень (≤M), включая в расчеты индивидуальные значения ПО. Помимо этого, для этих элементов приводили диапазон полученных величин – от минимального из достигнутых ПО до максимального определённого значения. Для элементов, содержание которых во всех образцах было ниже ПО, в таблицах указаны средние значения ПО.
Таблица 3. Основные статистические характеристики содержания некоторых химических элементов в поперечном срезе ребра здорового человека (женщины и мужчины вместе) в возрасте от 15 до 55 лет (мкг/г сухой ткани).
| Элемент | M | SD | SEM | min | max | Med | P0.025 | P0.975 |
| Ag | <0,02 (ПО) | - | - | - | - | - | - | - |
| As | <0,1 (ПО) | - | - | - | - | - | - | - |
| Au | <0,01 (ПО) | - | - | - | - | - | - | - |
| Ba | <100 (ПО) | - | - | - | - | - | - | - |
| Br | <10 (ПО) | - | - | - | - | - | - | - |
| Ca, мг/г | 193 | 44 | 4,9 | 95,9 | 306 | 199 | 103 | 269 |
| Cd | <2 (ПО) | - | - | - | - | - | - | - |
| Ce | <0,008 (ПО) | - | - | - | - | - | - | - |
| Cl | 993 | 453 | 50 | 131 | 2876 | 1003 | 189 | 2117 |
| Co | 0,0019 | 0,0010 | 0,0003 | 0,0004 | 0,0044 | 0,0019 | 0,0006 | 0,0039 |
| Cr | ≤0,9 | - | - | <0,8 (ПО) | 1,55 | - | - | - |
| Cs | ≤0,011 | - | - | <0,002 (ПО) | 0,11 | - | - | - |
| Eu | ≤0,001 | - | - | <0,0001 | 0,0051 | - | - | - |
| F | 1659 | 792 | 182 | 283 | 3230 | 1583 | 387 | 3151 |
| Fe | 115 | 73,9 | 9,4 | 23,4 | 429 | 101 | 34,4 | 282 |
| Gd | <0,25 (ПО) | - | - | - | - | - | - | - |
| Hf | <0,02 (ПО) | - | - | - | - | - | - | - |
| Hg | ≤0,008 | - | - | <0,001 (ПО) | 0,022 | - | - | - |
| K | 878 | 461 | 53 | 39 | 2111 | 808 | 144 | 1853 |
| La | <0,05 (ПО) | - | - | - | - | - | - | - |
| Lu | <0,003 (ПО) | - | - | - | - | - | - | - |
| Mg | 2110 | 713 | 79 | 579 | 3502 | 2155 | 606 | 3456 |
| Mn | 0,299 | 0,202 | 0,023 | 0,059 | 0,977 | 0,257 | 0,070 | 0,889 |
| Na | 4767 | 1224 | 136 | 1615 | 8594 | 4777 | 2043 | 6810 |
| Nd | <0,1 (ПО) | - | - | - | - | - | - | - |
| P, мг/г | 83,9 | 21,2 | 2,3 | 30,3 | 148 | 82,9 | 48,4 | 128 |
| Rb | 1,51 | 0,91 | 0,12 | 0,2 | 4,91 | 1,39 | 0,2 | 3,56 |
| Sb | ≤0,021 | - | - | <0,01 (ПО) | 0,074 | - | - | - |
| Sc | <0,001 (ПО) | - | - | - | - | - | - | - |
| Se | ≤0,03 | - | - | <0,02 (ПО) | 0,052 | - | - | - |
| Sm | <0,01 (ПО) | - | - | - | - | - | - | - |
| Sr | 289 | 177 | 19 | 28 | 1204 | 256 | 63 | 647 |
| Ta | <0,005 (ПО) | - | - | - | - | - | - | - |
| Tb | <0,03 (ПО) | - | - | - | - | - | - | - |
| Th | <0,05 (ПО) | - | - | - | - | - | - | - |
| U | <0,07 (ПО) | - | - | - | - | - | - | - |
| Yb | <0,03 (ПО) | - | - | - | - | - | - | - |
| Zn | 86,4 | 18,4 | 2,3 | 38,5 | 128 | 87,3 | 54,1 | 114 |
| Zr | <0,2 (ПО) | - | - | - | - | - | - | - |
M – среднее арифметическое, SD – стандартное отклонение среднего, SEM – стандартная ошибка среднего, min – минимальное значение, max – максимальное значение, Med – медиана значений, P0,025 – процентиль с уровнем 0,025, P0,975 – процентиль с уровнем 0,975, ПО – предел определения, Ca и Sr – среднее значение по данным NAA по коротко- и долгоживущим радионуклидам.
Помимо поперечного среза ребра информация о содержании ХЭ была получена также для крыла подвздошной кости (anterior-posterior биоптат), поперечного среза шейки бедра, кортикальной ткани крыла подвздошной кости, трабекулярной ткани крыла подвздошной кости, кортикальной ткани шейки бедра, трабекулярной ткани шейки бедра, кортикальной кости (крыло подвздошной кости и шейка бедра), трабекулярной кости (крыло подвздошной кости и шейка бедра), диафизов трубчатых костей, эпифизов трубчатых костей, коронки и корня зуба. При этом рассматривалось три группы лиц, разделённых по гендерному признаку – женщины, мужчины и объединённая группа женщин и мужчин, три группы лиц разделённых по возрасту – от 15 до 35 лет, от 36 до 55 лет и от 15 до 55 лет, а также две группы лиц в соответствии с местом проживания – г. Обнинск и г. Иркутск.
Показано, в частности, что содержание химических элементов зависит от вида (табл. 4) и типа (табл. 5) кости.
Показано также, что содержание химических элементов в зубах отличается от их содержания в костной ткани (табл. 6).
Таблица 4. Сопоставление средних значений (M ± SEM) содержания химических элементов в ребре, крыле подвздошной кости и шейке бедра здорового человека.
| Элемент | Ребро I | Крыло подвздошной кости II | Шейка бедра III | p (t-тест Стьюдента) | ||
| I-II | I-III | II-III | ||||
| Ca, мг/г | 193±5 | 169±3 | 153±3 | 0,001 | 0,001 | 0,01 |
| Cl | 993±50 | 1490±43 | 1188±48 | 0,001 | 0,01 | 0,001 |
| Co | 0,0019±0,0003 | 0,0073±0,0024 | 0,0039±0,0003 | 0,05 | 0,001 | Н.Р. |
| Eu | ≤0,001 | 0,0028±0,0010 | 0,0073±0,0019 | - | - | 0,05 |
| Fe | 115±9 | 177±24 | 55,5±8,8 | 0,05 | 0,001 | 0,001 |
| K | 878±53 | 1820±79 | 490±22 | 0,001 | 0,001 | 0,001 |
| Mg | 2110±79 | 1840±48 | 1938±48 | 0,01 | Н.Р. | Н.Р. |
| Mn | 0,299±0,023 | 0,316±0,013 | 0,385±0,015 | Н.Р. | 0,01 | 0,001 |
| Na | 4767±136 | 4970±87 | 3852±70 | Н.Р. | 0,001 | 0,001 |
| P, мг/г | 83,9±2,3 | 79,7±1,5 | 73,0±1,5 | Н.Р. | 0,001 | 0,01 |
| Rb | 1,51±0,12 | 1,89±0,22 | 0,39±0,05 | Н.Р. | 0,001 | 0,001 |
| Zn | 86,4±2,3 | 65,9±3,4 | 55,5±1,2 | 0,001 | 0,001 | 0,01 |
M – среднее арифметическое, SEM – стандартная ошибка среднего, Н.Р. – нет различия.
Таблица 5. Результаты сопоставления средних значений (M ± SEM)
содержания химических элементов в кортикальной и трабекулярной кости
здорового человека (образцы из крыла подвздошной кости и шейки бедра).
| Элемент | Кортикальная кость | Трабекулярная кость | p (t-тест Стьюдента) |
| Ca, мг/г | 216±3 | 120±2 | 0,001 |
| Co | 0,0081±0,0007 | 0,0037±0,0005 | 0,001 |
| Eu | 0,012±0,004 | 0,0016±0,0004 | 0,05 |
| Fe | 43±11 | 76±10 | 0,05 |
| K | 932±59 | 1436±109 | 0,001 |
| Mg | 2362±53 | 1556±37 | 0,001 |
| Mn | 0,391±0,016 | 0,325±0,018 | 0,01 |
| Na | 5372±81 | 3698±83 | 0,001 |
| P, мг/г | 101±2 | 58,8±1,3 | 0,001 |
| Sr | 350±16 | 277±16 | 0,01 |
| Zn | 74,0±3,1 | 50,4±2,9 | 0,001 |
M – среднее арифметическое, SEM – стандартная ошибка среднего.
Таблица 6. Сопоставление средних значений (M ± SEM) содержания химических элементов в кортикальной кости, коронке и корне зуба здорового человека.
| Элемент | Кортикальная кость I | Коронка зуба II | Корень зуба III | p (t-тест Стьюдента) | ||
| I-II | I-III | II-III | ||||
| Ca, мг/г | 216±3 | 350±5 | 278±6 | 0,001 | 0,001 | 0,001 |
| Cl | 1315±51 | 2924±152 | 978±77 | 0,001 | 0,001 | 0,001 |
| Co | 0,0081±0,0007 | 0,0030±0,0012 | - | 0,01 | 0,001 | - |
| Fe | 43±11 | 4,7±1,1 | - | 0,001 | - | - |
| Mg | 2362±53 | 4880±240 | 8127±46 | 0,001 | 0,001 | 0,001 |
| Mn | 0,391±0,016 | 3,20±0,30 | 1,22±0,10 | 0,001 | 0,001 | 0,001 |
| Na | 5372±81 | 6240±140 | 6925±220 | 0,001 | 0,001 | 0,01 |
| P, мг/г | 101±2 | 181±4 | 149±3 | 0,001 | 0,001 | 0,001 |
| Sb | ≤0,011 | 0,022±0,007 | - | - | - | - |
| Sr | 350±16 | 301±25 | 451±26 | Н.Р. | 0,01 | 0,001 |
| Zn | 74,0±3,1 | 136±11 | - | 0,001 | - | - |
M – среднее арифметическое, SEM – стандартная ошибка среднего, Н.Р. – нет различия.
Обнаружено, что во многих исследованных тканях костей скелета у женщин содержание Ca, Mg, Na, P, Sr и Zn выше, а содержание Fe несколько ниже, чем у мужчин. Для некоторых тканей это различие подтверждено статистически. Повышенное содержание Ca, Mg и P указывает на то, что костная ткань женщин более минерализована, т.е. более насыщена гидроксиапатитом. Более выраженная минерализация скелета у женщин может быть связана с особенностью репродуктивной функции женского организма – беременностью, во время которой Ca, Mg и P мобилизуются из скелета матери для нужд плода. Повышенное содержание Na и Sr, вероятно, связано с диетическими пристрастиями женщин на популяционном уровне – бóльшим потреблением поваренной соли (Na) и растительной пищи (Sr) по сравнению с мужчинами. В репродукционный период организм женщины находится в состоянии сдвига баланса Fe в сторону дефицита из-за дополнительных потерь элемента с менструальной кровью. В отличие от женщин, организм мужчины находится в состоянии сдвига баланса Zn в сторону дефицита из-за дополнительных потерь этого элемента с секретом предстательной железы, выделяемым при эякуляции и мочеиспускании. Соответственно, дефицит этих элементов в организме отражается на их уровне в одном из депо – костной ткани.
Гендерных различий в содержании ХЭ в зубах не выявлено, за исключением Mn в корне зуба.
Особое внимание было уделено исследованию возрастной зависимости содержания химических элементов в костной ткани и зубах от возраста, поскольку с ней связана проблема сенильного остеопороза. Детальный анализ возрастной зависимости с использованием 8 возрастных групп (от 15 до 55 лет с шагом 5 лет) позволил выявить возраст максимального содержания (пик накопления) Са и Р во всех исследованных видах образцов кости и зубов как у мужчин, так и у женщин (табл. 7).
Таблица 7. Возраст достижения максимума содержания Са и Р (годы).
| Костная ткань | Са | Р | |||
| мужчины | женщины | мужчины | женщины | ||
| Ребро (срез) | 26–30 | 26–30 | 26–30 | 26–30 | |
| Крыло П-кости (биоптат) | 20–25 | 15–20 | 20–25 | 15–20 | |
| Шейка бедра (срез) | 20–25 | 20–25 | 20–25 | 20–25 | |
| Крыло П-кости (корт.) | 26–30 | 15–20 | 26–30 | 15–20 | |
| Крыло П-кости (траб.) | 15–20 | 15–20 | 15–20 | 15–20 | |
| Шейка бедра (корт.) | 31–35 | 26–35 | 31–35 | 26–35 | |
| Шейка бедра (траб.) | 15–20 | 21–25 | 15–20 | 21–25 | |
| Кортикальная кость | 26–35 | 15–35 | 26–35 | 15–35 | |
| Трабекулярная кость | 15–20 | 15–25 | 15–20 | 15–25 | |
| Зуб (коронка) | 26–35 | 26–35 | 26–35 | 26–35 | |
| Зуб (корень) | 21–25 | 21–25 | 21–25 | 21–25 | |
Крыло П-кости – крыло подвздошной кости, корт. – кортикальная, траб. – трабекулярная.
После достижения максимума содержание Са и Р с возрастом медленно и равномерно уменьшается. Используя линейную аппроксимацию, представилось возможным определить среднегодовые потери Са и Р во всех исследованных видах образцов кости и зубов как у мужчин, так и у женщин (табл. 8). Как следует из данных, представленных в таблице 8, скорость потерь Ca и P в различных костях разная и, как правило, у женщин несколько выше, чем у мужчин. В возрасте до 55 лет трабекулярная ткань деминерализуется быстрее, чем кортикальная. Наибольшие среднегодовые потери Ca отмечены в поперечном срезе ребра и трабекулярной ткани шейки бедра у женщин.
Таблица 8. Среднегодовые потери Са и Р в костной ткани и зубах.
| Костная ткань | Са, % в год | Р, % в год | ||
| мужчины | женщины | мужчины | женщины | |
| Ребро (срез) | 0,39 | 0,72 | 0,57 | 0,56 |
| Крыло П-кости (биоптат) | 0,28 | 0,34 | 0,29 | 0,32 |
| Шейка бедра (срез) | 0,36 | 0,37 | 0,08 | 0,17 |
| Крыло П-кости (корт.) | 0,45 | 0,17 | 0,11 | 0,16 |
| Крыло П-кости (траб.) | 0,0 | 0,67 | 0,06 | 0,64 |
| Шейка бедра (корт.) | 0,28 | 0,42 | 0,20 | 0,0 |
| Шейка бедра (траб.) | 0,63 | 0,72 | 0,54 | 0,62 |
| Кортикальная кость | 0,18 | 0,09 | 0,0 | 0,0 |
| Трабекулярная кость | 0,17 | 0,70 | 0,30 | 0,64 |
| Зуб (коронка) | 0,20 | 0,36 | 0,76 | 0,32 |
| Зуб (корень) | 0,13 | 0,31 | 0,06 | 0,46 |
Крыло П-кости – крыло подвздошной кости, корт. – кортикальная, траб. – трабекулярная.
Показано, что содержание микроэлементов в костной ткани зависит от места жительства. Так, содержание Ag, Cr, Fe, Mn, Sb и Zn в костной ткани жителей г. Иркутска в 2–4 раза выше, чем у жителей г. Обнинска. Повышенное содержание этих элементов может быть связано с экологическим неблагополучием региона, вызванным интенсивным промышленным освоением Восточной Сибири. Почти в 10 раз более высокий уровень Sc и десятикратно сниженный уровень Sr в костной ткани жителей г. Иркутска возможно связан с биогеохимическими особенностями региона, однако этот вопрос требует специального исследования. Следует также отметить, что пониженный уровень стронция может быть отчасти обусловлен и особенностями структуры питания местного населения – превалированием в диете пищи животного, а не растительного происхождения.
Важное значение для оценки состояния костной ткани имеют не только абсолютные значения содержания элементов, но и их отношения. Особенно удобно использовать отношения химических элементов при проведении in vivo исследований. Для всех исследованных костных тканей и зубов рассчитывали отношения Ca/P, Ca/Mg, Ca/Na, Ca/Zn, Cl/Ca и Cl/Na. Выявлено, что в период жизни от 15 до 55 лет возраст не оказывает существенного влияния на величину отношений содержания химических элементов в костной ткани и зубах. Единственное исключение касается отношения Ca/P в поперечном срезе шейки бедра (p <0,01). Пол заметно влияет на величину многих из рассмотренных отношений химических элементов. Особенно это касается отношений Ca/Mg, Cl/Ca и Cl/Na в ребре, гребне крыла подвздошной кости и шейке бедра.
С помощью корреляционного анализа проведена оценка взаимосвязи уровней накопления одного и того же элемента во всех рассмотренных видах костной ткани и зубов. Показано, что уровни содержания Са в различных тканях кости и зубов слабо связаны между собой. Среди всех определённых химических элементов только для уровней содержания Sr в различных тканях кости и зубов наблюдалась положительная корреляция. В качестве иллюстрации в табл. 9. приведены значения коэффициентов корреляции для макроэлемента костной ткани Са и микроэлемента Sr.
Таблица 9. Коэффициенты корреляции содержания одного и того же элемента в различных тканях костей и зубов.
| Элемент | Ткань | № | 1 | 2 | 3 | 4 | 5 |
| Ca | Ребро (срез) | 1 | 1,00 | 0,25 | 0,22 | -0,02 | 0,34 |
| | Крыло П-кости (биоптат) | 2 | | 1,00 | 0,19 | -0,05 | 0,08 |
| | Шейка бедра (срез) | 3 | | | 1,00 | 0,01 | 0,20 |
| | Зуб (коронка) | 4 | | | | 1,00 | 0,04 |
| | Зуб (корень) | 5 | | | | | 1,00 |
| Sr | Ребро (срез) | 1 | 1,00 | 0,41 | 0,50 | 0,39 | 0,38 |
| | Крыло П-кости (биоптат) | 2 | | 1,00 | 0,55 | 0,23 | 0,20 |
| | Шейка бедра (срез) | 3 | | | 1,00 | 0,40 | 0,17 |
| | Зуб (коронка) | 4 | | | | 1,00 | 0,46 |
| | Зуб (корень) | 5 | | | | | 1,00 |
Подчёркнуто – p<0,05, жирный шрифт – p<0,01.
Из выявленного отсутствия значимых корреляций для макроэлементов вытекают важные выводы. Например о том, что по содержанию Са и Р в биоптате крыла подвздошной кости не представляется возможным сделать заключение о содержании этих элементов в шейке бедра или какой-либо другой кости. По той же причине и результаты определения содержания Са и Р в коронке зуба не могут быть использованы для оценки уровня минерализации костей скелета. Из наличия корреляции содержания Sr в костной ткани и зубах следует, что, определив содержание этого микроэлемента в любой кости или зубах, представляется возможным оценить уровень его содержания в скелете или во всём организме.
Межэлементные взаимосвязи были рассмотрены на примере ребра, крыла подвздошной кости, кортикальной и трабекулярной кости. Показано, что с содержанием Са имеется прямая связь уровней содержания таких элементов, как Mg, Mn, Na, P и Sr, с содержанием P – Ca, Mg, Mn, Na и Sr, с содержанием Mg – Ca, Mn, Na, P и Sr, с содержанием Na – Ca, К, Mg, Mn и P, с содержанием Cl – только К, с содержанием К – Cl и Na, с содержанием Mn – Ca, Na и P, с содержанием Sr – Ca, Mg, P и Zn, с содержанием Zn – только Sr. Уровень содержания Fe в кости находится в обратной зависимости от содержания Са, что понятно, т.к. железо связано, в основном, с органическим матриксом кости, а кальций - с минеральным.
