Утверждаю
| Вид материала | Рабочая программа |
- Утверждаю утверждаю, 21.26kb.
- «утверждаю» «утверждаю», 262.03kb.
- Утверждаю утверждаю, 393.06kb.
- «Утверждаю» «Утверждаю» Председатель Совета доу заведующий мдоу №25, 113.74kb.
- Кикбоксинг против наркомании и детской преступности «Утверждаю» «Утверждаю», 78.29kb.
- Утверждаю: утверждаю, 156.74kb.
- «утверждаю» «утверждаю» Председатель республиканского Директор маоудод «цдтт №5» совета, 42.86kb.
- Утверждаю» «Утверждаю», 163.81kb.
- «Динамо», 49.89kb.
- Утверждаю: утверждаю: Председатель Глава администрация оо «Гомельский рыболовный клуб», 78.23kb.
 Рабочая программа учебной дисциплины | | Ф ТПУ 7.1 – 21/01 |
УТВЕРЖДАЮ
Декан ХТФ
_______________В.М. Погребенков
"____"______________2007 г.
ОРГАНИЧЕСКАЯ ХИМИЯ
Рабочая программа
для направления 240100 «Химическая технология и биотехнология»
Факультет – Химико-технологический (ХТФ)
Обеспечивающая кафедра – Органической химии и технологии
органического синтеза (ОХОС)
Курс – второй, третий
Семестр – третий-пятый
Учебный план набора 2007 года
Распределение учебного времени
| Вид занятий | 3 семестр | 4 семестр | 5 семестр | Всего |
| Лекции Практические занятия Лабораторные занятия Всего аудиторных занятий Самостоятельная (внеаудиторная работа) Общая трудоемкость | 34 10 24 68 68 136 | 20 15 20 55 68 123 | 26 10 18 54 68 122 | 80 35 62 177 204 381 |
Экзамены в третьем и пятом семестрах, зачет в четвертом
Томск 2007
Предисловие
1. Рабочая программа составлена на основе ГОС по направлению 655500 «Биотехнология», специальности 240901 (c) «Биотехнология», утвержденного 05.03.2000 г., РАССМОТРЕНА и ОДОБРЕНА на заседании обеспечивающей кафедры органической химии и технологии органической химии «07» сентября 2007 г., протокол № 2.
2. Разработчик
проф. каф. ОХОС В.Д.Филимонов
3. Зав. обеспечивающей каф. ОХОС В.Д.Филимонов
4. Рабочая программа СОГЛАСОВАНА с факультетом, выпускающими кафедрами специальности; СООТВЕТСТВУЕТ действующему плану.
УДК 547. Ключевые слова: органическая химия, теория строения органических соединений, органический синтез, классы органических соединений, свойства и применение органических соединений
Аннотация
ОРГАНИЧЕСКАЯ ХИМИЯ
240100 (б) - 240901(c)
Каф. ОХОС ХТФ
Профессор, д.х.н. Филимонов Виктор Дмитриевич
Тел. (3822)563637, e-mail: filimonov@tpu.ru
Органическая химия - одна из учебных дисциплин, обеспечивающая фундаментальное химическое образование, и являющееся основой ряда дисциплин специальности 240100.
Цель данного курса - знакомство студентов с развитием, современным состоянием и достижениями органической химии, развитие у них химического мышления и экспериментальных навыков.
Содержание - материал в программе изложен на основе рассмотрения теории строения и реакционной способности органических соединений с последующей классификацией органических соединений по классам углеводородов и функциональным группам.
Разделы «Ароматические углеводороды», «Галогенорганические соединения», «Соли диазония и диазосоединения» включают материал для углубленного изучения: органический синтез и критерии «Зеленой химии», основы синтеза органических наноструктур, исследования Томской школы химиков-органиков.
Для полноценного усвоения данного курса важное значение имеют такие дисциплины, как «Общая и неорганическая химия» и «Физическая химия».
Курс 2,3 (3,5 сем. – экзамены; 4 сем. - зачет)
Всего 177 ч, в т. ч.: Лк 80 ч, Пр 35 ч., Лб. 62 ч.
Цели преподавания дисциплины
Органическая химия - одна из учебных дисциплин, обеспечивающая фундаментальное химическое образование, и являющееся основой многих дисциплин инженерного профиля направления «Химическая технология и биотехнология», а также ряда дисциплин подготовки магистрантов.
Цель данного курса - знакомство студентов с историей, современным состоянием и достижениями органической химии, развитие у них химического мышления и экспериментальных навыков.
Материал в программе изложен на основе рассмотрения теории строения и реакционной способности органических соединений с последующей классификацией органических соединений по классам углеводородов и функциональным группам.
Для полноценного усвоения данного курса важное значение имеют такие дисциплины, как «Общая и неорганическая химия» и «Физическая химия».
Цели и задачи дисциплины:
- Научить студентов понимать основные закономерности, лежащие в основе соединений углерода и применять полученные теоретические знания для решения конкретных практических задач.
- Освоение студентами основных методов получения органических соединений, их химических и физико-химических свойств и сфер практического применения.
- Привить практические навыки органического синтеза, методов выделения, очистки и идентификации органических веществ.
- Научить правильно обрабатывать, анализировать и оформлять результаты эксперимента.
После изучения курса органической химии студент
должен знать:
- теорию строения органических соединений и связь строения с реакционной способностью;
- основные классы органических соединений, их химические свойства и генетические взаимосвязи;
- методы синтеза важнейших классов органических соединений и способы трансформации функциональных групп; механизмы ключевых реакций органического синтеза;
- принципы влияния органических веществ на живые организмы и окружающую среду; их основные токсикологические характеристики и безопасные правила работы;
должен уметь:
- по структуре органического соединения предсказать его ключевые химические свойства и области практического использования;
- планировать и осуществлять синтез органического соединения с заданной структурой;
- эффективно пользоваться литературой по органической химии;
- осуществить синтез, начиная со сбора соответствующей установки и проведения необходимых расчетов;
Задачи изложения и изучения дисциплины
Для достижения целей при совместной и индивидуальной познавательной деятельности студентов в части овладения теоретическими знаниями и практическими умениями используются лекции, тесты и контрольные задания для проверки знаний студентов.
Для закрепления теоретических знаний, полученных на лекциях, в курсе предусмотрено проведение лабораторных и практических занятий в совместной и индивидуальной (самостоятельной) формах.
Содержание теоретического раздела дисциплины (лекции)
3 семестр
I. Введение (2 часа).
Предмет органической химии. Краткая история развития органической химии как науки. Значение органической химии для жизнедеятельности человека и промышленности, ее связь с другими науками. Сырьевые источники органических соединений. Органические вещества в живой природе, в организме человека. Проблема загрязнения окружающей среды органическими веществами. Историческая справка о работах выдающихся представителях Томской школы химиков-органиков: Кижнер А.М., Тронов Б.В., Кулев Л.П.
II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ (10 часов)
Современное состояние теории химического строения. Тетраэдрическая модель атома углерода, гибридизация электронных орбиталей. Понятие химической связи. Типы химической связи: ковалентная полярная и неполярная, водородная, семиполярная. Электронное строение простых и кратных углерод-углеродных связей: - и - связи. Классификация реагентов и реакций в органической химии. Электрофильные, нуклеофильные и радикальные реагенты. Классификация реакций по направлению (замещение, присоединение, отщепление, изомеризация, циклоприсоединение) и типу реагента. Термодинамическое и кинетическое описание химических реакций. Интермедиаты органических реакций (карбокатионы, карбанионы, свободные радикалы, карбены). Понятие о механизмах органических реакций. Описание органических реакций с помощью энергетических диаграмм. Электронные эффекты заместителей (индукционные, резонансные, сверхсопряжение) на реакционную способность. Теории кислот и оснований (Аррениус, Бренстед-Лоури, Льюис). Классификация органических соединений.
III. Углеводороды (22 часа)
Алканы (парафины) (4 ч)
Гомологический ряд алканов. Общая формула, строение, изомерия, номенклатура. Первичный, вторичный и третичный атомы углерода. Понятие об алкильных радикалах, их названия.
Природные источники алканов: нефть и природный газ.
Промышленные способы получения алканов: ректификация нефти, крекинг высших алканов, гидрогенизация углей, синтез Фишера-Тропша.
Синтетические методы получения алканов: реакция Вюрца-Шорыгина, гидрирование ненасыщенных углеводородов, восстановление алкилгалогенидов и кетонов по Кижнеру и Клеменсену. Получение предельных углеводородов из карбоновых кислот: пиролиз, электролиз (реакция Кольбе).
Физические свойства алканов: температуры кипения, растворимость в воде. Закономерности изменения физических свойств в гомологическом ряду.
Химические свойства алканов: реакции радикального замещения атомов водорода (галогенирование, сульфохлорирование, сульфоокисление, нитрование), механизмы этих процессов; изомеризации, как пример электрофильных превращений. Реакции, идущие с разрывом связей С-С: крекинг и окисление.
Использование предельных углеводородов и продуктов их переработки в органическом синтезе. Углеводороды как моторное топливо.
Алкены (олефины) (4 ч)
Гомологический ряд этиленовых углеводородов (олефинов). Общая формула, строение, изомерия, номенклатура.
Промышленные способы получения алкенов: крекинг и дегидрирование алканов.
Синтетические методы получения алкенов: дегидрогалогенирование, дегидратация спиртов, реакция Виттига.
Физические свойства алкенов.
Химические свойства. Реакции присоединения по двойной связи: каталитическое гидрирование, электрофильное присоединение галогенов, галогеноводородов, воды, серной и хлорноватистой кислот. Механизм электрофильного присоединения. Правило Марковникова. Механизм присоединения воды, кислотный катализ.
Свободнорадикальное присоединение, механизм радикального присоединения бромистого водорода.
Реакции окисления олефинов с разрывом и без разрыва углеводородной цепи. Реакция Вагнера. Реакция Прилежаева. Высокотемпературное окисление пропилена.
Озонирования и озонидное расщепление алкенов как метод установления их строения. Качественные реакции на наличие двойных связей.
Радикальная, катионная, анионная полимеризация алкенов.
Диены (3 ч)
Классификация диенов. Номенклатура. Электронное строение 1,3- или сопряженных диенов.
Реакции электрофильного 1,2- и 1,4 – присоединения к сопряженным диенам галогенводородов и галогенов. Кинетический и термодинамический контроль реакций присоединения. Реакции циклоприсоединения.
Важнейшие представители: 1,3-бутадиен и изопрен - мономеры для синтеза каучуков. Понятие о натуральном и синтетическом каучуках. Природные биологически важные соединения полиенового строения: каротин, витамин А.
Алкины (ацетилены) (3 ч)
Гомологический ряд ацетиленовых углеводородов. Общая формула, строение, изомерия, номенклатура. Вклад отечественных ученых в развитие химии ацетилена.
Электронное строение молекулы ацетилена.
Промышленные способы получения ацетилена: термическое разложение метана, карбидный метод.
Методы образования тройное связи: дегидрирование, дегидрогалогенирование органических дигалогенидов.
Физические свойства алкинов.
Химические свойства алкинов: каталитическое гидрирование. Реакции электрофильного и нуклеофильного присоединения галогенов, галогеноводородов, карбоновых кислот, воды, спиртов, синильной кислоты, реакции винилирования ацетиленом (реакции Кучерова, Реппе).
Кислотный характер терминальных алкинов. Замещение на металл (образование ацетиленидов - качественная реакция на концевую тройную связь). Синтезы производных ацетилена через ацетилениды и с использование палладиевого катализа (реакция Фаворского).
Окисление алкинов. Полимеризация ацетиленовых углеводородов, димеризация и тримеризация ацетилена и его гомологов.
Циклоалканы (нафтены) (2 ч)
Классификация и номенклатура. Теория напряжений и электронное строение связей С-С в низших циклоалканах. Пространственное строение циклоалканов, конформационная измерия.
Природные источники. Методы синтеза: реакции циклизации, гидрирования, реакции карбенов с олефинами.
Химические свойства циклоалканов: реакции с сохранением и раскрытием циклов.
Понятие о каркасных углеводородах. Адамантаны, фуллерены.
Ароматические углеводороды (арены) (6 ч)
Классификация ароматических углеводородов. Бензол и его гомологи. Изомерия и номенклатура. Нахождение в природе.
Электронное строение бензольного кольца. Понятие и критерии ароматичности.
Способы получения бензола и его гомологов: ароматизация алканов, тримеризация алкинов, алкилирование бензола, реакция Вюрца-Фиттига, выделение из нефти и каменноугольной смолы.
Физические свойства ароматических углеводородов.
Химические свойства аренов. Реакции электрофильного замещения: галогенирование, нитрование, сульфирование, алкилирование и ацилирование по Фриделю-Крафтсу. Механизмы этих реакций. Методы прямого иодирования органических соединений на базе разработок кафедры органической химии, в том числе метод Тронова-Новикова.
Влияние заместителей на направление реакций электрофильного замещения и на реакционную способность бензольного кольца. Ориентация при наличии двух заместителей: согласованная и несогласованная. Соотношение орто- и пара-изомеров. Объяснения правил замещения с точки зрения электронных и пространственных эффектов.
Радикальное галогенирование и нитрование алкилбензолов в боковую цепь.
Окисление бензола и его гомологов.
Реакции присоединения водорода, хлора, озона.
Главные представители: бензол, толуол, ксилолы, стирол (промышленные источники, применение).
Полициклические арены: классификация, номенклатура. Электронное строение и реакционная способность аннелированных производных (нафталин, антрацен, фенантрен, пирены). Термодинамический и кинетический контроль реакций на примере сульфирования нафталина. Современный органический синтез, отвечающий критериям «Зеленой химии». Основы синтеза органических наноструктур (нанотрубки, наноповерхности и др.)
4 семестр
IV. Галогенорганические соединения (6 ч)
Классификация, номенклатура.
Примеры наиболее практически важных галогенорганических соединений: растворители, мономеры, фреоны. Диоксины, как высокотоксичные соединения и загрязнители окружающей среды.
Алкил- и алкенилгалогениды. Методы получения: галогенирование алканов, гидрогалогенирование алкенов, алкинов, превращения спиртов и карбонильных соединений. Химические свойства алкил- и алкенилгалогенидов. Природа связи C-Hal, механизмы реакций дегидрогалогенирования и дегалогенирования. Значение реакций нулеофильного замещения и их механизмы (SN1, SN2).
Ароматические галогениды. Методы синтеза через реакции электрофильного замещения и соли диазония. Особенности реакций электрофильного иодирования, вклад Томской школы химиков-органиков в развитие методов иодирования, реакция Тронова-Новикова. Химические свойства арилгалогенидов, механизмы реакций нуклеофильного замещения в ароматическом ряду. Арилиодиды как универсальные синтоны для органического синтеза.
Особенности строения, синтеза, химических и физико-химических свойств фторорганических соединений, области их практического использования.
V. Понятие о металлорганических соединениях (2 ч)
Классификация, основы номенклатуры, физические и токсикологические свойства. Основные методы получения литий- и магнийорганических соединений. Химические свойства и применение в органическом синтезе (получение углеводородов, спиртов, карбоновых кислот).
VI. Кислородсодержащие органические соединения
Спирты и фенолы (6 ч)
Строение, классификация, изомерия, номенклатура.
Промышленные методы получения спиртов: гидратация алкенов, ферментативный гидролиз углеводов, получение метанола из синтез-газа. Методы синтеза спиртов: гидролиз алкилгалогенидов, восстановление карбонильных соединений. Получение первичных, вторичных и третичных спиртов методом Гриньяра.
Физические свойства спиртов. Растворимость в воде, высокие температуры кипения - как следствие образования водородных связей. Токсичность спиртов. Действие этанола и метанола на организм человека (практическое занятие под руководством преподавателя).
Химические свойства спиртов: влияние строения на кислотно-основные свойства, алкоголяты. Дегидратация спиртов, окисление первиных и вторичных спиртов до карбонильных соединений и карбоновых кислот. Образование простых и сложных эфиров. Механизм реакции этерификации. Замещение гидроксила на галоген. Многоатомные спирты и жиры.
Важнейшие представители: метанол, этанол, изопропиловый спирт, этиленгликоль, глицерин.
Получение фенолов из каменноугольной смолы, гидролизом арилгалогенидов и щелочным плавлением солей ароматических сульфокислот, окислением изопропилбензола (кумольный метод).
Физические свойства фенолов. Растворимость в воде, высокие температуры кипения - как следствие образования водородных связей. Токсичность.
Электронное строение и химические свойства фенолов: влияние строения на кислотность. Различия в кислотности спиртов и фенолов. Образование простых и сложных эфиров.
Реакции фенолов по ароматическому кольцу: галогенирование, нитрование. Реакция Кольбе. Взаимодействие с формальдегидом. Фенолформальдегидные смолы.
Многоатомные фенолы.
Карбонильные соединения (альдегиды и кетоны) (6 ч)
Строение, изомерия и номенклатура альдегидов и кетонов.
Получение альдегидов и кетонов: дегидрирование и окисление спиртов, гидратация алкинов, гидролиз геминальных дигалогенидов, озонолиз алкенов, декарбоксилирование солей карбоновых кислот. Вакер-процесс.
Химические свойства карбонилсодержащих соединений: восстановление (реакции Кижнера-Вольфа, Клеменсена). Нуклеофильное присоединение по карбонильной группе. Взаимодействие с синильной кислотой, реактивом Гриньяра, бисульфитом натрия, гидразином и его производными. Механизм реакций карбонильных соединений с первичными и вторичными аминами (азометины, енамины). Гидратация и образование ацеталей.
Кето-енольная таутомерия и реакции галогенирования. Галоформное расщепление. Реакции конденсации альдегидов и кетонов: Бородина, Клайзена, Перкина, Кневенагеля, Анри, Канниццаро, Зинина. Механизм альдольной конденсации. Окисление и восстановление альдегидов и кетонов. Реакции в бензольном кольце бензальдегида.
Важнейшие представители: формальдегид, ацетальдегид, бензальдегид, ацетон (промышленные методы получения, использование).
5 семестр
Карбоновые кислоты (6 ч)
Строение (насыщенные и ненасыщенные карбоновые кислоты), изомерия, номенклатура. Нахождение в природе.
Получение карбоновых кислот: окисление алкиларенов, спиртов и альдегидов; из органических галогенидов через присоединение металлорганических соединений и гидролизом нитрилов. Малоновый синтез.
Физические свойства. Влияние внутримолекулярных водородных связей на физико-химические свойства.
Электронное строение карбоксильной группы и органических карбоксилатов. Химические свойства: влияние строения на кислотность, образование и взаимопревращения производных карбоновых кислот (сложные эфиры, ангидриды, ацилгалогениды, амиды), механизмы этих реакций, декарбоксилирование. Реакции бензольного ядра бензойной кислоты.
Высшие предельные и непредельные карбоновые кислоты, жиры и масла.
Непредельные карбоновые кислоты (акриловая, метакриловая), методы их получения и практическое использование.
Дикарбоновые кислоты. Малоновая кислота.
Понятие об ионогенных поверхностно-активных веществах.
VII. Азотсодержащие органические соединения
Алифатические и ароматические нитросоединения (4 ч)
Строение, классификация, изомерия, номенклатура. Электронное строение нитрогруппы. Способы получения. Нуклеофильное замещение галоидалканов, нитрование алканов и ароматических углеводородов, .
Физические и химические свойства нитросоединений. Действие щелочей на алифатические нитросоединения, реакции нитроалканов с карбонильными соединениями. Восстановление нитросоединений в щелочной и кислой средах. Влияние нитрогруппы на реакционную способность фенильного ядра. Нитропарафины в качестве растворителей, добавок к ракетным топливам, промежуточных продуктов в синтезе красителей. Взрывчатые вещества. Тротил, пикриновая кислота, гексоген
Аминосоединения (6 ч)
Строение, классификация, изомерия, номенклатура. Первичные, вторичные, третичные амины. Соли аммония.
Способы получения аминов: восстановление нитросоединений, нитрилов и амидов карбоновых кислот, взаимодействие аммиака с алкилгалогенидами и спиртами. Реакция Гофмана. Синтез Габриэля.
Физические свойства аминов.
Химические свойства аминов: влияние строения на основность, образование солей с кислотами, алкилирование и ацилирование. Реакции первичных, вторичных, третичных алифатических и ароматических аминов с азотистой кислотой. Реакции ароматических аминов по кольцу: галогенирование, нитрование, сульфирование. Защита аминогруппы в реакциях электрофильного замещения и снятие защиты.
Применение аминов в синтезе красителей и лекарственных препаратов. Токсичность аминов.
Соли диазония и диазосоединения (3 ч)
Электронное строение диазониевой группы. Методы получения ароматических диазосоединений. Химические свойства солей диазония и их использование в органическом синтезе как наиболее универсальных синтонов. Реакция азосочетания. Практическое применение диазосоединений.
VIII. Гетероциклические соединения (6 ч)
Классификация, основы номенклатуры. Нахождение в природе. Пяти- и шестичленные гетероциклические соединения. Электронное строение, ароматический характер.
Методы получения и химические свойства фурана, тиофена, пиррола, индола, пиридина, хинолина и их производных. Применение и биологическое значение. Понятие об алкалоидах. Макроциклы: фталоцианины, порфирины.
IX. Аминокислоты (2 ч)
Классификация. Номенклатуры -аминокислот, их строение (цвиттер-ионные формы), заменимые и незаменимые, физико-химические свойства, методы получения через -галоидкарбоновые кислоты. Химические свойства (образование производных по карбоксильной и амино-группам, способность к синтезу пептидов). Понятие о полипептидах и белках, первичные и вторичные структуры, биологическое значение.
Содержание практического раздела дисциплины
Теоретические знания, полученные на лекциях, закрепляются во время практических занятий и лабораторных работ.
Практические занятия посвящаются решению задач и рассмотрению наиболее сложных теоретических вопросов, касающихся механизмов органических реакций, зависимости реакционной способности соединений от их строения. Предусмотрены следующие формы работы:
- Рассмотрение и обсуждение теоретических вопросов;
- Решение у доски типовых задач;
- Самостоятельная работа с использованием учебников, лекций и консультаций преподавателя по индивидуальным карточкам;
- Проведение контрольных работ.
Темы практических занятий (35 ч)
3 семестр
- Алканы. Строение, изомерия, номенклатура (2 ч)
- Теоретические основы органической химии (4 ч)
- Алканы. Алкены, алкины. Получение и свойства (2 ч)
- Контрольная работа №1 (2 ч)
4семестр
- Ароматические углеводороды. Правила ориентации (4 ч)
- Органические галогениды (2 ч)
- Спирты и фенолы (4 ч)
- Карбонильные соединения (3 ч)
- Контрольная работа №2 (2 ч)
5 семестр
- Карбоновые кислоты (2 ч)
- Амины. Методы синтеза и химические свойства (2 ч)
- Азо- и диазосоединения (2 ч)
- Гетероциклические соединения (2 ч)
- Контрольная работа №3 (2 ч)
Лабораторные занятия
Во время лабораторных занятий студенты приобретают навыки работы с органическими соединениями и лабораторной посудой, а также закрепляют теоретический материал. Перед проведением эксперимента
они изучают методику синтеза, технику безопасности, по справочникам находят характеристики соединений, участвующих и образующихся в данной реакции, проводят расчет синтеза и совместное обсуждение предстоящей работы с преподавателем. После окончания работы представляют отчет и защищают его.
Темы лабораторных занятий (64 часа):
3 семестр
- Введение в лабораторию органического синтеза: знакомство с методами работы, посудой, приборами. Техника безопасности при проведении лабораторных работ (2ч).
- Очистка растворителей методом простой перегонки и определение показателя преломления. Самостоятельная работа по теме «Номенклатура органических соединений». Коллоквиум по теме «Алканы». (6 ч).
- Получение этиленовых углеводородов. Качественные реакции на непредельные соединения. Самостоятельная работа по теме «Электронные эффекты заместителей». Коллоквиум по теме «Алкены, алкины» (8 ч).
- Использование метода тонкослойной хроматографии для идентификации органических соединений. Решение задач по теме «Арены». Расчет синтеза п-нитробромбензола (8 ч).
4 семестр
- Синтез п-нитробромбензола, его очистка перекристаллизацией и идентификация. Коллоквиум по теме «Арены» (8 ч).
- Синтез галоидных алкилов из спиртов; коллоквиум по теме «Галогенсодержащие органические соединения» (6 ч).
- Окисление алкилбензолов и синтез бензойной кислоты; коллоквиум по теме «Спирты и фенолы» (6 ч)
5 семестр
- Синтез сложных эфиров (4 ч)
- Синтез анилина восстановлением нитробензола. Самостоятельная работа по теме «Амины» «(6 ч)
- Получение дибензальацетона конденсацией Клайзена. Решение комплексных задач. (4 ч).
- Диазотирование-иодирование п-нитроанилина в водной пасте Самостоятельная работа по теме «Диазосоединения»(4 ч).
Лабораторный практикум охватывает основные разделы дисциплины и имеет необходимое методическое обеспечение.
Программа самостоятельной познавательной деятельности
Самостоятельная (внеаудиторная) работа студентов состоит в проработке лекционного материала, подготовке к практическим занятиям и лабораторным занятиям, выполнение домашних заданий. Для помощи студентам при подготовке ими домашних заданий, еженедельно проводятся консультации. В целом объем самостоятельной работы составляет 204ч часа и включает следующие пункты:
1) проработка курса лекций (80 ч)
2) подготовка к практическим занятиям (40 ч)
2) подготовка к лабораторным работам коллоквиумам (24 ч)
3) выполнение домашних заданий (60 ч).
Текущий и итоговый контроль результатов изучения дисциплины
При изучении курса “Органическая химия” используется рейтинговая система оценка знаний студентов. В течение семестра студент может набрать 1000 баллов. Целью текущего и итогового контроля является не только проверка усвоения материала, но и оказание помощи студентам в вопросах, которые оказались для них сложными и не были поняты до конца. В течение семестра студент может набрать 1000 баллов. Предусмотрены следующие виды контроля:
- Выполнение домашних работ по всем темам практических занятий (13 домашних работ).
- Контрольные, самостоятельные работы (9 работ) и коллоквиумы (5).
- Лабораторные работы (10 работ).
- Итоговый контроль результатов изучения дисциплины – экзамен, который оценивается в 400 баллов.
Общий рейтинг переводится в оценку следующим образом:
от 900 до 1000 баллов - "отлично"
от 780 до 900 баллов - "хорошо"
от 570 до 780 баллов - "удовлетворительно".
Если оценка экзамена менее 150 баллов, то экзамен считается не сданным, и студент теряет рейтинг семестра.
Контролирующие материалы
Состояние контролирующих материалов: имеются билеты входного и выходного контроля, экзаменационные билеты, билеты текущего контроля (самостоятельные и контрольные работы, вопросы к коллоквиумам). По каждому виду контроля имеется от 10 до 20 вариантов заданий, таким образом, каждый студент работает индивидуально.
Образцы контролирующих материалов:
Входной контроль
Билет № 1
- О

пределить класс соединений и назвать их:
- Дайте определение ионной и ковалентной связям. Приведите примеры соединений с такими связями.
- Сколько граммов KOH содержится в 50 мл 30%-го раствора щелочи с плотностью 1.33 г/мл?
Самостоятельная работа №1 "Номенклатура органических соединений"
Билет №1
- Назовите по систематической номенклатуре следующие соединения:
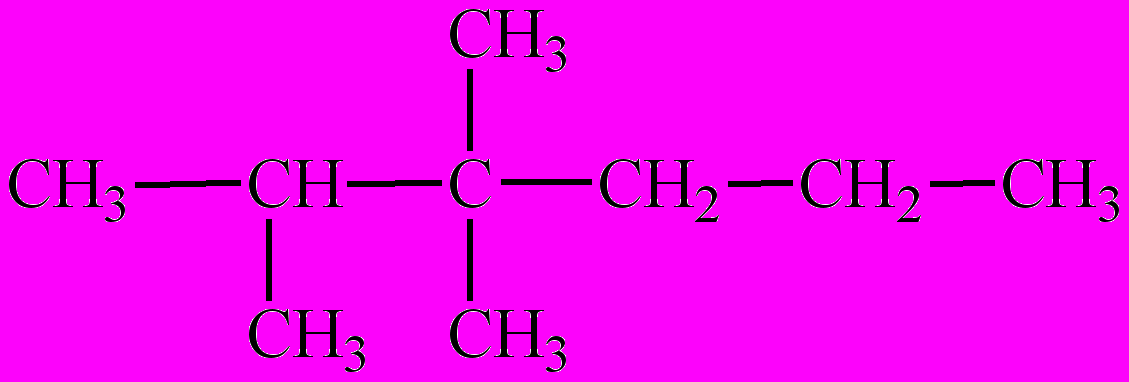
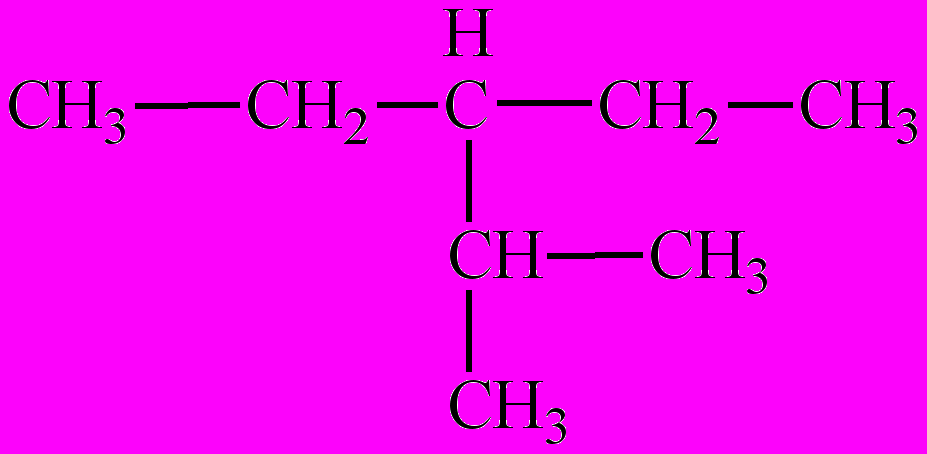
А Б
Сколько первичных, вторичных, третичных и четвертичных атомов содержит алкан А?
- Напишите структурные формулы следующих углеводородов:
А) 2,2,4,4-тетраметилпентан;
Б) 3-изопропил-2-метил-4,5-диэтилгексан.
Самостоятельная работа №2 «Электронные эффекты заместителей»
Билет №1
- Графическим методом показать распределение электронной плотности в молекуле бензальдегида и анизола (метоксибензол).
- Сравнить по устойчивости следующие интермедиаты:
 Ответ обоснуйте
Ответ обоснуйтеСпмостоятельная работа №3 «Органические галогениды» (выполняется в часы внеаудиторной работы).
Билет №1
1. Расположите в ряд по увеличению относительной реакционной способности в реакцииSN:
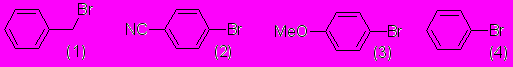
Ответ обоснуйте.
2. Предложите цепочку превращений из 5-6 стадий, при этом две из них должны быть реакции SN и/или Е.
3. Объясните результат следующих превращений:
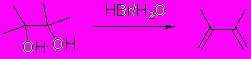 (55-60%)
(55-60%)Для ответа обдумайте следующие вопросы:
а) Тип реакции;
б) Возможный механизм реакции;
г) Селективность реакции;
д) Выбор условий проведения реакции (температура, растворитель и. проч).;
е) Стереохимия реакции
Самостоятельная работа №4 «Методы синтеза спиртов» (проводится в часы внеаудиторных занятий). При выполнении данной работы необходимо использовать базу данных органических соединений компании «Aldrich» ссылка скрыта. Исходные вещества для заданий 1-2 выбираются учащимся самостоятельно из каталога «Aldrich»
1. Синтезируйте первичный спирт, используя метод гидроборирования-окисления алкенов.
Необходимый алкен синтезируйте методом Виттига. Для всех реакций напишите синтетический протокол по следующей схеме:
- Цель;
- Схема реакции;
- Характеристика всех исходных реагентов: брутто-формула, структурная формула, название, молекулярная масса, Тпл/кип (для жидкостей указать плотность), CAS-№;
- Загрузка (г/мл, ммоль);
- Методика проведения синтеза, выделения продукта и очистки. Дайте ссылку на оригинальную работу (первоисточник).
2. Синтезируйте вторичный спирт методом Гриньяра. Работу выполните согласно указаниям, данным в задании №1.
Контрольная работа №1
Билет №1
1. Осуществите превращения:

2. Расположите в ряд по увеличению реакционной способности в реакциях AЕ следующие алкены:
 Ответ обоснуйте.
Ответ обоснуйте.3. Объясните, почему тринитрометан является более сильной кислотой, чем динитрометан, а метан вообще не проявляет кислых свойств?
4. Напишите структурную формулу углеводорода, если известно, что он реагирует с бромом, с аммиачным раствором оксида серебра, а при гидратации дает метилизопропилкетон. Все реакции напишите.
Контрольная работа №2
Билет №1
1. Расположите в ряд по увеличению относительной реакционной способности в реакциях SN1:
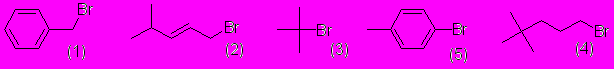
2. Соединение, формула которого приведена ниже, можно получить в результате реакции Дильса-Альдера. Какие диен и диенофил необходимы для получения этого вещества?

3. Исходя из бензола, получите метилфенилкетон. Предложите качественную реакцию для идентификации этого соединения.
4. Углеводород состава С10Н14 при окислении дает бензойную кислоту, при хлорировании на свету и при нагревании только первичное монохлорпроизводное, при хлорировании в присутствии кислот Льюиса два изомера в соотношении 10:1. Определите структурную формулу углеводорода, напишите все реакции.
Контрольная работа №3
Билет №2
- Напишите комбинацию реагентов и соответствующее уравнение реакции, которое приведет к образованию следующего соединения:
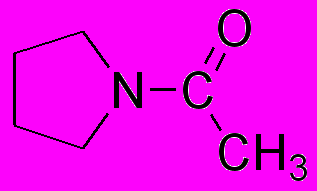
2. Приведите реагенты, из которых можно получить следующее соединение: СН3СОС(СН3)(СН2СН3)СООН. Напишите все реакции.
3. Сравните по кислотности: малеиновая кислота и фумаровая кислота (диссоциация по первой ступени). Ответ обоснуйте.
4. Какое строение имеет вещество состава C8H8O2, при хлорировании которого избытком хлора при нагревании без катализатора на свету образуется вещество состава C8H5O2Cl3, гидролиз которого приводит к фталевой кислоте.
Самостоятельная работа №5 "Азотсодержащие соединения»
1. Какие из приведенных соединений будут вступать в реакцию взаимодействия с водным раствором щелочи (без катализатора и нагрева)? Напишите реакции и дайте пояснения.
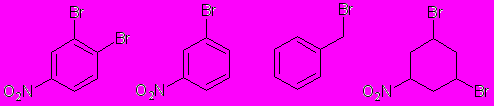
2. Осуществите следующие превращения, назовите типы химических реакций, которые Вы при этом используете:
Нитробензол → азобензол
3. Нижеприведенные амины расположите в ряд по увеличению их основности. Ответ обоснуйте.
п-броманилин, п-нитроанилин, п-метиланилин
4. Азотсодержащее вещество, растворимое в кислотах, было подвергнуто действию азотистой кислоты, причем образовалось соединение состава С3H8N2O. Напишите формулу исходного вещества, продукта реакции и реакцию растворения исходного вещества в кислотах.
Самостоятельная работа №6 "Диазосоединения»
1. Осуществите с использованием солей диазония и их химических превращений, а также различных свойств ароматических веществ следующие синтезы:
бензол: 1) м-дихлорбензол; 2) анисовая кислота; 3) п-фтортолуол
2. Ниже приведена формула азосоединения. Какая реакция лежит в основе получения этого соединения. Каков механизм этой реакции? Какие диазо- и азосотавляющие были взяты для реакции? Приведите синтез и название красителя, укажите в его составе хромофорные и ауксохромные группы.

3. Почему реакцию азосочетания обычно проводят в строгом интервале рН, а именно рН = 5-9? Объясните, какие осложнения могут произойти, если величину рН не поддерживать в указанных пределах?
Экзаменационный билет
| Экзаменационные б  илеты ХТФ илеты ХТФ | ЭБ ТПУ 8.4/СД.03/2006 |
| Томский политехнический университет | ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 6по дисциплине «Органическая химия» курс 2 |
2. Примеры и механизмы свободнорадикальных реакций замещения в алканах. | |
| Составитель, профессор ______________ /В.Д.Филимонов «_16_» декабря 2006 г. | |
Примеры задач к экзаменационным билетам:
1. Расположите в ряд по увеличению кислотных свойств следующие соединения:
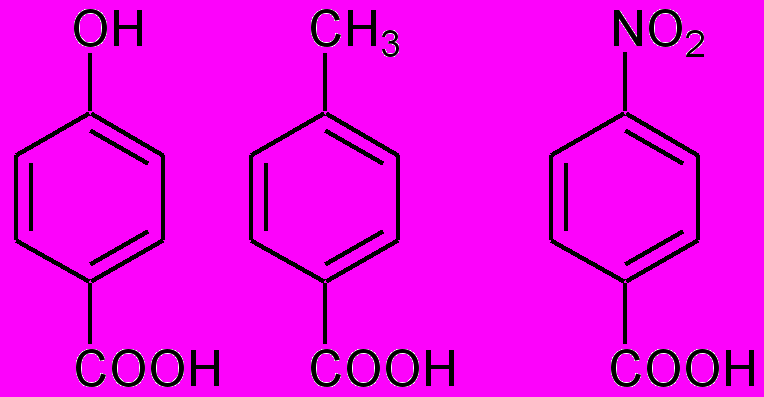 Ответ обоснуйте
Ответ обоснуйте2. Осуществите превращения:
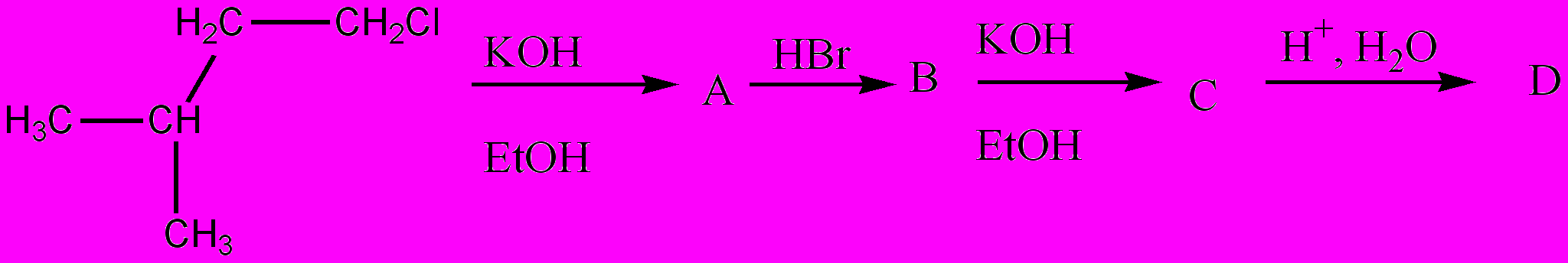
3. Напишите структурную формулу углеводорода, если известно, что он реагирует с бромом, с аммиачным раствором оксида серебра, а при гидратации дает метилизопропилкетон. Все реакции напишите.
Экзаменационный билет
| Экзаменационные б  илеты ХТФ илеты ХТФ | ЭБ ТПУ 8.4/СД.03/2006 |
| Томский политехнический университет | ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 15по дисциплине «Органическая химия» курс 3 |
| 1. Реакции карбоновых кислот: образование хлорангидридов, амидов. 2. Пятичленные гетероциклические соединения: электронное строение, ароматичность, методы синтеза пиррола, тиофена, фурана. | |
| Составитель, профессор ______________ /В.Д.Филимонов «_16_» декабря 2006 г. | |
Примеры задач к экзаменационным билетам:
1. Заполните следующую схему реакций, назовите промежуточные и конечные продукты:

2. Установите строение вещества C6H13NO, при гидролизе которого образуется диметиламин и соединение C4H8O2, последнее может быть получено окислением изобутилового спирта
3. Предложите методы получения м-фторхлорбензола из бензола
Учебно-методическое обеспечение дисциплины
Для изучения органической химии используются следующие пакеты прикладных программ: ChemWin, ChemOffice, Hyperchem. Эти программы позволяют, в частности, легко строить структуры химических соединений, наглядно показывают особенности строения и стереохимии, дают возможность наблюдать динамику химических реакций, что существенно облегчает усвоение материала и делает процесс обучения более занимательным. В научно-технической библиотеке ТПУ имеются в достаточном количестве учебники и учебные пособия, необходимые для изучения органической химии. Все они соответствуют программе курса и Государственному образовательному стандарту. Учебные пособия под номерами 5 и 6 разработаны на кафедре органической химии и ТОС ТПУ. На сайте кафедры ОХОС размещены электронный лекционный курс «Введение в основы теоретической органической химии», а также дополнительный материал по некоторым разделам дисциплины «Органическая химия».
Перечень рекомендуемой литературы
Основная литература:
- Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия.- М.: Высшая школа, 2002. - 591 с.
- Ким А.М. Органическая химия. Новосибирск: Сиб. унив. изд-во, 2004 -844 с.
- Терней А. Современная органическая химия. - М.: Мир, 1981. – Т.1-2.
- Моррисон Р., Бойд М. Органическая химия. – М.: Мир, 1974. – 1132 с.
- Сарычева Т.А., Тимощенко Л.В., Чайковский В.К. Сборник задач по органической химии с решениями. Часть 1 «Углеводороды». – Томск: ТПУ, 2006.
- Васильева В.П., Ковалева Л.Ф. и др. Сборник задач и упражнений по органической химии. – Томск: ТПУ, 1997. – Ч.1-2.
- Васильева В.П. и др. Лабораторный практикум по органической химии. – Томск: ТПУ, 1995.
- www.orgchem.chtj.tpu.ru
Дополнительная литература:
- Шабаров Ю.С. Органическая химия. – М.: Высшая школа, 1994.
- Сайкс П. Механизмы реакций в органической химии. – М.: Химия, 1991.
- Нейланд О.Я. Органическая химия. – М.: Высшая школа, 1989. – 750с.
стр. из
