Книга вторая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского
| Вид материала | Книга |
- Книга первая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского, 10010.77kb.
- А. Конан-Дойль новоеоткровени е перевод с английского Йога Рàманантáты, 2314.23kb.
- Copyright Сергей Александровский, перевод с английского Email: navegante[a]rambler, 619.61kb.
- "книга непрестанности осириса " 177, 7373.41kb.
- Н. М. Макарова Перевод с английского и редакция, 4147.65kb.
- Трудового Красного Знамени гупп детская книга, 2911.61kb.
- Трудового Красного Знамени гупп детская книга, 2911.77kb.
- Уайнхолд Б., Уайнхолд Дж. У 67 Освобождение от созависимости / Перевод с английского, 11462.2kb.
- Малиновской Софьи Борисовны Специальность: журналистика Специализация: художественный, 969.08kb.
- Духовные истины в психических явлениях перевод с английского 3-е издание Москва «Философская, 1557.75kb.
ветствии с этим, препаратами выбора считаются рокуроний, векуроний, доксакурий и пипекуро-ний. ^ Вместе с тем векуроний способен значительно потенцировать брадикардию, вызываемую опиои-дами. Панкуроний является препаратом выбора при высокодозной опиоидной анестезии, поскольку у него есть ваголитический эффект, который противодействует индуцированной опиоидами брадикардии. Сочетание панкурония и метокури-на (в соотношении 1:3) также обеспечивает стабильную гемодинамику, не вызывая тахикардии или гипотонии, опосредованной высвобождением гистамина (гл. 9). Если существует риск трудной интубации (гл. 5), применяют сукцинилхолин.
^ 3. ПРЕДПЕРФУЗИОННЫЙ ПЕРИОД
После индукции анестезии и интубации трахеи в течение некоторого времени не происходит сколько-нибудь значительной хирургической стимуляции (идет обработка кожи и подготовка операционного поля), что часто приводит, к артериальной гипотензии. Этот период вскоре сменяется дискретными эпизодами интенсивной хирургической стимуляции, когда возникают тахикардия и артериальная гипертензия. Перед началом интенсивной хирургической стимуляции, которая включает кожный разрез, стернотомию и ретракцию грудины, рассечение перикарда, а в ряде случаев и рассечение аорты, необходршо ввести дополнительную дозу анестетика (или увеличить скорость его инфузии).
Ретракция грудины и рассечение перикарда могут приводить к выраженной стимуляции блуждающего нерва, что сопровождается значительной брадикардией и артериальной гипотензией. Эта реакция сильнее проявляется у больных, получавших (3-адреноблокаторы, дилтиазем или верапа-мил. Глубокая анестезия часто приводит к прогрессирующему снижению сердечного выброса после вскрытия плевральной полости. Снижение сердечного выброса, вероятно, обусловлено уменьшением венозного возврата из-за выравнивания внутригрудного давления (в норме отрицательного) с атмосферным. Инфузия жидкости позволяет устранить снижение сердечного выброса, по крайней мере частично.
В предперфузионном периоде может возникнуть ишемия миокарда, при которой часто (но не всегда) наблюдается тахикардия, артериальная гипертензия или гипотония. Профилактическая интраоперационная инфузия нитроглицерина (1-2 мкг/кг/мин), необходимость которой признается не всеми, снижает вероятность развития ишемии.
Канюляция
Канюляция — это критический момент в ходе налаживания ИК. Обычно сначала канюлируют аорту, потому что канюляция вен способна привести к гемодинамическим нарушениям. Кроме того, через аортальную канюлю при необходимости можно быстро выполнить инфузию. Чаще всего используют восходящую аорту. Малый просвет аортальной канюли создает поток с кавитацией, что при ее неправильной установке чревато расслаиванием аорты или преимущественным сбросом крови в плечеголовной ствол. Снижение АД сред до 90-100 мм рт. ст. облегчает установку аортальной канюли. Перед началом ИК из канюли полностью удаляют все пузырьки воздуха и проверяют адекватность обратного тока крови из артерии в артериальную магистраль. Если не удалить все пузырьки, возникнет воздушная эмболия коронарных или церебральных артерий. При неправильной установке канюли существует риск расслаивания аорты. Полагают, что временное пережатие сонных артерий при канюляции аорты снижает риск воздушной эмболии мозговых артерий.
В правое предсердие (обычно через ушко) устанавливают одну или две венозные канюли. Для большинства операций КШ и вмешательств на аортальном клапане достаточно одной венозной канюли. Если устанавливают только одну венозную канюлю, то, как правило, применяют так называемые двухсекционные модели, в которых один порт для забора крови находится на уровне правого предсердия, а другой — на уровне нижней полой вены.
При операциях на открытом сердце устанавливают отдельные канюли для полых вен. ^ Манипуляции на полых венах и сердце часто нарушают наполнение желудочков, что проявляется артериальной гипотензией. Канюляция вен нередко провоцирует возникновение предсердных или, реже, желудочковых аритмий. Не исключены и предсерд-ные экстрасистолы и преходящие пароксизмы наджелудочковой тахикардии. Устойчивая паро-ксизмальная предсердная тахикардия или мерцательная аритмия приводят к гемодинамической декомпенсации, которую устраняют медикамен-тозно, кардиоверсией или же с помощью немедленной антикоагуляции и ИК. Неправильное положение венозных канюль нарушает венозный возврат или препятствует венозному оттоку от головы и шеи (синдром верхней полой вены). После начала ИК первое осложнение проявляется недостаточным поступлением крови в венозный резервуар, а второе — отеком головы и шеи. При этом ЦВД повышается только в том случае, когда наконечник катетера находится высоко в полой вене.
^ Профилактика кровотечения
После индукции анестезии и до введения антикоагулянтов необходимо оценить риск возникновения кровотечения и целесообразность назначения апротинина. Показания к применению апротини-на включают повторную операцию на сердце (особенно при КШ); отказ от гемотрансфузии по религиозным соображениям (например, у членов общины Свидетелей Иеговы); высокий риск развития послеоперационного кровотечения из-за недавнего приема аспирина или коагулопатии; особо длительные и сложные операции на сердце и аорте. Механизм действия апротинина до конца не изучен, но известно, что он является ингибитором сериновых протеаз — плазмина, калли-креина и трипсина. Наиболее важный эффект апротинина состоит в нормализации функции тромбоцитов (адгезивности и агрегации). Апро-тинин хорошо снижает объем интраоперацион-ной кровопотери и уменьшает потребность в трансфузии (на 40-80 %).
Апротинин представляет собой чужеродный белок, получаемый из легких телят, вследствие чего он способен вызывать аллергические реакции, включая анафилактические (распространенность < 0,5 %). Реакции чаще возникают при повторном введении, поэтому всегда вначале вводят тест-дозу (1,4 мг, или 10 000 КИЕ, калликреин-ингибирую-щих единиц). В отсутствие нежелательных реакций через центральный венозный катетер в течение 20-30 мин вводят нагрузочную дозу (280 мг, или 2 млн КИЕ). После этого на протяжении всей операции выполняют инфузию препарата в дозе 70 мг/ч (500 000 КИЕ/ч). Кроме того, 280 мг апротинина (2 млн КИЕ) добавляют в АИК. Если при измерении ABC в качестве контактного активатора используют целит, то апротинин в присутствие гепарина искажает результаты измерения. Эта ошибка может привести к неадекватной оценке состояния свертывающей системы во время ИК. При назначении апротинина рекомендуется в качестве контактного активатора для определения ABC применять каолин.
Вместо апротинина, хотя и с меньшим эффектом, используют транексамовую кислоту. Нагрузочная доза составляет 10 мг/кг, поддерживающая — 1 мг/кг/ч. Транексамовая кислота не влияет на ABC и реже вызывает аллергические реакции.
В некоторых клиниках перед ИК практикуют проведение тромбоцитофереза, в ходе которого получают обогащенную тромбоцитами плазму. Ее ре-инфузия после ИК уменьшает кровопотерю и снижает потребность в донорских препаратах крови.
^ Применение антикоагулянтов
Для предотвращения развития ДВ С-синдрома и образования сгустков в насосе АИК перед началом ИК необходимо ввести пациенту антикоагулянт. Для оценки эффекта его действия используют активированное время свертывания (ABC). B большинстве кардиохирургических центров безопасным уровнем считается ЛВС > 400-450 с. Гепарин в дозе 300-400 ЕД/кг обычно вводят во время наложения кисетных швов при канюляции аорты. Многие хирурги предпочитают сами вводить гепарин непосредственно в правое предсердие; или это делает анестезиолог через центральный венозный катетер. Через 3-5 мин после этого следует измерить ABC. Если ABC < 400 с, необходима дополнительная доза гепарина — 100 ЕД/кг. Когда используют апротинин, для оценки эффекта гепарина при определении ABC в качестве контактного активатора применяют каолин, а не целит. Если по техническим условиям не удается измерить каолиновое ABC, прибегают к режиму фиксированных доз гепарина, рассчитываемых на основе массы тела больного и продолжительности ИК. Концентрация гепарина в плазме (см. с. 97) — недостоверный показатель его антикоагулянтного эффекта. Высо-кодозное тромбиновое время не изменяется под влиянием апротинина, но определить его сложнее, чем каолиновое ABC. Кроме того, высокодозное тромбиновое время не позволяет оценить состояние свертывающей системы до введения гепарина; оно также не считается адекватным показателем нейтрализации гепарина протамином.
Иногда встречается резистентность к гепарину, которая в большинстве случаев сочетается с дефицитом антитромбина III (приобретенным или врожденным). Антитромбин III — это циркулирующая в крови сериновая протеаза, необратимо связывающая и инактивирующая тромбин (а также активированные факторы X, XI, XII и XIII). Когда гепарин связывается с антитромбином III, анти-коагулянтная активность последнего увеличивается в тысячу раз. При дефиците антитромбина III хороший аптикоагиляитный эффект наблюдается после инфузии двух доз свежезамороженной плазмы, концентрата антитромбина III или синтетического антитромбина III.
Особого подхода требуют больные с гепарино-вой тромбоцитопенией в анамнезе. У них гепарин вызывает образование антител, которые становятся причиной агглютинации тромбоцитов, что приводит к тромбоцитопении. Последняя в ряде случаев сопровождается тромбоэмболическими осложнениями. Если гепариновая тромбоцитопе-ния имела место в отдаленном прошлом и в крови
уже нет антител, то применение гепарина безопасно, но только при ИК. Если титр антител высокий, то плазмаферез обеспечивает их временную элиминацию, что позволяет ввести гепарин. При экстреннных операциях на сердце у больных с активной гепариновой тромбоцитопенией перед введением гепарина следует инактивировать тромбоциты аспирином и дипиридамолом (или аналогом простациклина).
^ 4. ПЕРФУЗИОННЫЙ ПЕРИОД Начало ИК
Начинать ИК можно, когда канюли правильно установлены и зафиксированы, ABC превышает критический уровень и перфузиолог готов к работе. Зажимы с канюль (наложенные при установке) удаляют (сначала с венозной, затем с артериальной), после чего запускают главный насос АИК. Очень важно обеспечить адекватный возврат крови в венозный резервуар. В норме уровень крови в резервуаре повышается, и нагнетаемый насосом поток постепенно увеличивается. Если венозный возврат мал, то уровень крови в резервуаре падает и в контур насоса может попасть воздух. Если уровень крови недостаточно высок, то нужно проверить, правильно ли установлены канюли, не оставлены ли зажимы, нет ли перегибов и воздушных пробок. При обнаружении вышеперечисленных проблем нагнетаемый поток замедляют до их устранения. Иногда возникает необходимость во внесении в резервуар дополнительного объема (крови или коллоидного раствора). При полном ИК сердце должно постепенно запустеть; если этого не наблюдается или же, наоборот, возникает прогрессирующее растяжение камер сердца, то причиной являются либо неправильная установка венозной канюли, либо регургитация крови через аортальный клапан. В последнем случае немедленно накладывают зажим на аорту и проводят кардиоплегию.
^ Потоки давление
При постепенном увеличении объемной скорости перфузии до 2-2,5 л/мин/м2 тщательно контролируют АД. С подключением АИК АД обычно резко снижается, так что начальное АДср в лучевой артерии может не превышать 30-40 мм рт. ст. Артериальная гипотония обусловлена резко возникающей гемодилюцией, которая уменьшает вязкость крови и значительно снижает ОПСС. Этот эффект частично компенсируется последующей гипотермией, при которой вязкость крови повышается.
При длительном снижении АДср до величины менее 30 мм рт. ст. необходимо исключить нераспознанное ранее расслаивание аорты. Если таковое обнаружено, ИК прерывают до повторной канюляции аорты дистальнее. Другие причины артериальной гипотонии включают низкий венозный возврат, неисправность насоса, ошибку датчика давления. Когда для мониторинга используют правую лучевую артерию, а аортальная канюля направлена к плечеголовному стволу, значения АД могут оказаться завышенными.
Зависимость между объемной скоростью перфузии, ОПСС и АДср выражается уравнением:
АДср = Объемная скорость перфузии х ОПСС.
Следовательно, если ОПСС постоянно, то АДср прямо пропорционально объемной скорости перфузии. Аналогично, при любой фиксированной объемной скорости перфузии АДср прямо пропорционально ОПСС. Главная задача при ИК состоит в поддержании адекватного АД и кровотока, что достигается изменением величин объемной скорости перфузии и ОПСС. В большинстве кардио-хирургических центров объемную скорость перфузии поддерживают на уровне 2-2,5 л/мин/м2 (50-60 мл/кг/мин), а АДср — в пределах между 50 и 80 мм рт. ст. Обычно необходимый кровоток прямо пропорционален центральной температуре тела. Установлено, что на фоне глубокой гипотермии (20-25 0C) даже при АДср = 30 мм рт. ст. мозговой кровоток остается адекватным. ОПСС можно поднять с помощью фенилэфрина или ме-токсамина.
Высокое АДср (> 150 мм рт. ст.) опасно, потому что повышает риск возникновения расслаивания аорты и геморрагического инсульта. ^ При АДср > 100 мм рт. ст. рекомендуется уменьшить объемную скорость перфузии или добавить изофлюран в оксигенатор через патрубок подачи газовой смеси. Если эти меры неэффективны или объемная скорость перфузии уже низкая, то вводят вазоди-лататор (нитропруссид).
Мониторинг
Дополнительный мониторинг при ИК включает определение объемной скорости перфузии, уровня крови в венозном резервуаре, давления в артериальной магистрали, температуры крови (перфуза-та и венозной), температуры миокарда, SO2 в артериальной и венозной крови. Используют также показания встроенных в аппарат датчиков рН, рСО2 и рО2. Значения рН, рСО2 и рО2 следует перепроверять с помощью прямых измерений. В отсутствие гипоксемии низкое SO2 венозной крови
(< 70 %), прогрессирующий метаболический ацидоз и низкий диурез свидетельствуют о низкой объемной скорости перфузии.
Во время И К давление в артериальной магистрали почти всегда выше, чем АД в лучевой артерии или даже в аорте. Разница обусловлена сопротивлением артериального фильтра, артериальной магистрали и узкого просвета аортальной канюли. Вместе с тем мониторинг этого давления позволяет выявить нарушения функционирования артериальной магистрали. Давление в артериальной магистрали должно быть ниже 300 мм рт. ст.; при более высоких значениях необходимо исключить засорение артериального фильтра, обструкцию артериальной магистрали или канюли, а также расслаивание аорты.
Во время ИК в динамике измеряют ABC, гематокрит и концентрацию калия. ABC определяют сразу после начала ИК, а затем каждые 20-30 мин. Охлаждение увеличивает время полусуществования гепарина и, соответственно, продолжительность его действия. Для облегчения расчета доз ге-
парина и протамина используют кривую 'доза-эффект" (рис. 21-3). Хотя имеющаяся зависимость не всегда линейна, но она применима в клинике. Гематокрит рекомендуется поддерживать в пределах 20-25 %. Иногда возникает необходимость в добавлении эритроцитарной массы в резервуар насоса. При выраженной гиперкалиемии (вызванной кардиоплегией) применяют фуросемид.
^ Гипотермия и кардиоплегия
В ходе большинства операций используют сред-неглубокую (26-31 0C) или глубокую (20-25 0C) гипотермию. Чем ниже температура, тем больше времени понадобится для охлаждения и последующего согревания. С другой стороны, низкие температуры позволяют уменьшить объемную скорость перфузии. Так, при 20 0C потребности организма удовлетворяет объемная скорость перфузии 1,2 л/мин/м2.
^ При охлаждении сердца до температуры ниже 28-29 0C часто возникает фибрилляция желудоч-
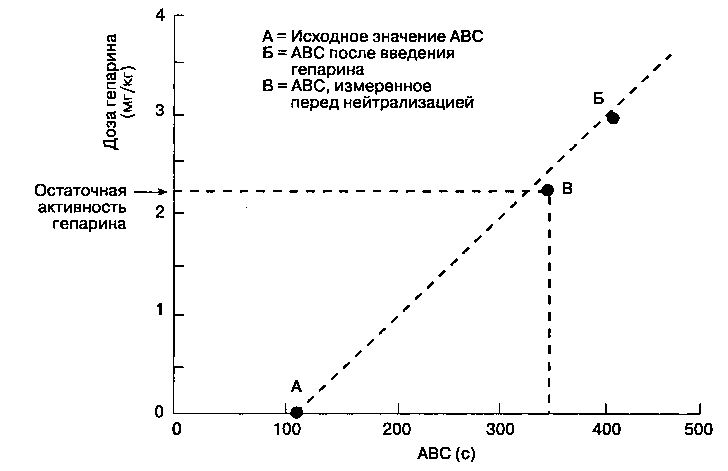
Рис. 21-3. Гепарин: кривая "доза-эффект". По горизонтальной оси активированное время свертывания (ABC) в секундах, по вертикальной — полная доза гепарина в мг/кг.
1. На оси .г отмечают исходное значение ABC.
2. Отмечают значение ABC после введения гепарина.
3. Проводят линию через эти две точки.
4. Если необходимо ввести дополнительную дозу антикоагулянта, находят желаемое значение ABC на этой линии. Дополнительная доза гепарина равна разнице между текущим значением ABC и желаемым ABC, спроецированной на ось у.
5. Если третья точка не лежит на первоначальной линии, проводят новую линию, начинающуюся от исходного значения ABC и проходящую посередине между двумя другими точками.
6. Для нейтрализации гепарина дозу протамина рассчитывают по остаточной активности гепарина, соответствующей последнему значению ABC на кривой "доза-эффект"
ков. Следует немедленно приступить к кардиопле-гии, потому что при фибрилляции быстро расходуются макроэргические соединения и нарушается защита миокарда. Для этого накладывают зажим на восходящую аорту проксимальнее аортальной канюли, после чего через небольшой катетер, установленный проксимальнее места пережатия, инфузируют кардиоплегический раствор. Альтернативный вариант — введение кардиоплегическо-го раствора непосредственно в устья коронарных артерий (если вскрыт просвет аорты). Во время КШ кардиоплегический раствор можно вводить через шунт, если хирург предпочитает вначале накладывать дистальный анастомоз. При выраженной обструкции коронарных артерий многие хирурги обычно используют ретроградную кардио-плегию через катетер, установленный в коронарном синусе.
ИВЛ
ИВЛ обычно продолжают до тех пор, пока не установится адекватная объемная скорость перфузии и пока сердце не перестанет перекачивать кровь. После перехода к полному ИК ЛЖ изгоняет кровь в течение короткого времени, пока его объем не достигнет критически низкого уровня. Преждевременное прекращение ИВЛ чревато шунтированием остаточного легочного кровотока справа налево, что провоцирует возникновение гипоксемии (гл. 22). Клиническая значимость такого шунта зависит от величины отношения остаточного легочного кровотока к объемной скорости перфузии. В некоторых кардиохирургических центрах после прекращения ИВЛ подают в контур наркозного аппарата кислород на фоне ПДКВ 5 см вод. ст., для предотвращения послеоперационных легочных осложнений. В большинстве центров отключают подачу всех газов или оставляют низкий поток кислорода (1-2 л/мин). По завершении ИК, когда сердце снова начинает перекачивать кровь, ИВЛ возобновляют.
^ Кислотно-основное состояние
Не существует общепринятого мнения, какие парциальные давления газов артериальной крови — скорректированные или нескорректированные по температуре — следует использовать при гипотер-мическом ИК. Причина разногласий заключается в том, что при гипотермии растворимость газов возрастает. Соответственно, при снижении температуры парциальное давление газа уменьшится, хотя его общее содержание не изменится (в закрытой системе). Проблема приобретает особое значе-
ние для величин PaCO2, от которого зависят рН артериальной крови и мозговой кровоток. При снижении температуры концентрация бикарбоната в плазме не меняется, но уменьшение PaCO2 обусловливает тенденцию к повышению рН и возникновению алкалоза (по нормотермическим критериям). Если при 37 0C PaCO2 составляет 40 мм рт. ст., а рН — 7,40, то при охлаждении крови до 25 0C PaCO2 составляет 23 мм рт. ст., а рН — 7,60.
В норме, независимо от температуры тела больного, образцы крови в газоанализаторах вначале нагревают до 37 0C и только после этого измеряют парциальные давления газов. Если нужно выполнить коррекцию величин парциальных давлений газов и р H по температуре тела, используют таблицу или программу в газоанализаторе. Если в условиях гипотермии реальные значения рН и PaCO2 поддерживают на уровне, который считают нормальным при нормотермии (7,40 и 40 мм рт. ст. соответственно),— то говорят, что регуляцию КОС проводят в режиме pH-stat. При проведении гипо-термического ИК в режиме pH-stat может потребоваться добавление CO2 в оксигенатор через патрубок подачи газовой смеси, что увеличивает общее содержание CO2B крови. В этих условиях мозговой кровоток становится более зависимым от PaCO2 и АДср, чем от потребления кислорода (гл. 25).
Чаще для регуляции КОС при гипотермии используют нескорректированные значения парциального давления газов, т. е. режим a-stat. В основе такого подхода лежит тот факт, что сохранение нормальной функции белков зависит от поддержания постоянства внутриклеточной электронейтральности (т. е. от равновесия зарядов белков). При физиологических значениях рН эти заряды расположены главным образом на имидазольном кольце гистидиновых остатков (называемых а-остатками). Кроме того, при уменьшении температуры снижается Kw (константа диссоциации воды), a pKw, соответственно, растет. Поэтому при низких температурах электронейтральность водных растворов, в которых [H+] = [ОН~], соответствует более низкой величине [H+] (т. е. более высокому значению рН). Гипотермический алкалоз, таким образом, необязательно отражает преобладание [OH"] над [H+], а скорее демонстрирует абсолютное снижение [H+]. При проведении гипотермического ИК в режиме
