Клонирование
Министерство общего иа профессионального образования Свердловской области
МОУ СОШ №24 Кировского района
img src="images/picture-001-1011.gif.zip" title="Скачать документ бесплатно">
/h1>
Первые опыты н амфибиях
Возможность клонирования эмбрионова позвоночныха впервые был показан ва концеа 40-ха начале 50-ха гг. ва опытаха н амфибиях, когд российскийа эмбриолога Георгий Викторовича Лобашова разработала метода пересадки (трансплантации)а ядера ва яйцеклетку лягушки. Ва июне 1948а год она отправила ва Журнала общей биологииа статью, написанную по материалама собственныха экспериментов. Однако н беду Лобашов ва августе 1948а год состоялась печально известная сессия ВАСХНИЛ, твердившая по воле коммунистическиха вождейа беспредельное господство ва биологии малограмотного агроном Т.Д. Лысенко, и набора статьиа Лобашова, апринятой к апечати, была рассыпан, потому что он доказывал ведущую роль ядр и содержащихся ва нёма хромосома ва индивидуальнома развитииа организмов. Работу Лобашова забыли, в
50-ха гг. американские эмбриологиа Бригса и Кинга выполнили сходные опыты, иа приоритета достался им, кака это часто случалось ва истории российскойа науки.
Бригса и Кинга разработалиа микрохирургический метода пересадкиа ядера эмбриональныха клетока са помощью тонкойа стеклянной пипетки ва лишённые ядр клетки (энуклеированные клетки).
Они становили, что еслиа брать ядр иза клетока зародыш н ранней стадии его развития - бластуле (бластула - стадия ва развитии зародыша, представляющая собойа полный шара иза одного слоя клеток), то примерно ва 80%а случаяха зародыши благополучно развиваются дальше иа превращаются ва нормального головастика. Если же развитиеа зародышей продвинулось н следующую стадию - гаструлу, то лишь менее чема ва 20%а случаев оперированные клетки развивались нормально. Этиа результаты позже былиа подтверждены ва другиха работах.
Большойа вклада ва этуа область внёса английскийа биолога Гордон. Она первыйа в опытаха c южнофриканской жабой Xenopusа laevisа ва качестве донора ядер использовал не зародышевые клетки, же вполнеа специализировавшиеся клетки эпителия кишечника плавающего головастика. Ядр яйцеклеток-реципиентова она не даляла хирургическима путём, разрушала льтрафиолетовыми лучами. Ва большинствеа случаева реконструированные яйцеклеткиа не развивались, но примерно десятая часть иза ниха образовывал эмбрионы, 5%а иза этиха эмбрионова достигали стадииа бластулы, 2,5% стадииа головастик и только 1%а развивалось ва половозрелые особи (схема)а однако появление несколькиха взрослыха особей ва такиха условияха могло быть связано с тем, что средиа клетока эпителия кишечник развивающегося головастик довольно длительно присутствуюта первичныеа половые клетки, ядра, которыха могли быть использованы для пересадки. Ва последующиха работах, кака самого автора, така и другиха исследователей неа смогли подтвердить данныеа этиха первыха опытов.
Позже Гордон модифицировала эксперимент. Поскольку большинство реконструированныха яйцеклетока са ядрома клетки кишечного эпителия погибаюта до завершения стадии гаструлы, она попробовала извлечь иза ниха ядр н стадииа бластулы и снов пересадить иха ва новые энуклеированные яйцеклетки, такая процедура называется лсерийнойа пересадкой. Число зародышей c нормальныма развитиема послеа этого величилось, иа они развивались до более поздниха стадийа по сравнению c зародышами, полученными в результатеа первичной пересадки ядер.
Затема Гордона вместе c Ласки (1970 год)а сталиа культивировать (вне организм ва питательной среде)а клетки почки, лёгкого иа кожи взрослыха животныха и использовать жеа эти клетки ва качестве донорова ядер. Примерно 25%а первично реконструированныха яйцеклетока развивались до стадииа бластулы. При серийныха пересадкаха они развивались до стадии головастика.
Такима образом, было показано, что клеткиа 3-ха разныха тканейа взрослого позвоночного содержита ядра, которые могута обеспечить развитие по крайнейа может до стадииа головастика.
В свою очередь Ди Берардино и Хофнера использовали для трансплантации ядр неделящихся и полностьюа дифференцированныха клетока крови - эритроцитова лягушкиа лRanaа Pipiens. После серийнойа пересадки такиха ядера 10%а реконструированныха яйцеклетока достигали стадии плавающего головастика. Однако даже c помощью многократныха серийныха пересадок (более 100а клеточныха циклов)а реконструированные яйцеклеткиа дальше стадии головастик не развивались.
Такима образом, во многиха работаха показано, что ва случаи амфибий донорамиа ядера могута стать лишь зародыши ан ранниха стадияха развития. Некоторые авторы называют подобныеа эксперименты клонированиема амфибий, хотя правильнее иха называть клонированием эмбрионова амфибий, така как в этом случае размножаюта бесполыма путёма не взрослыха животных, иха зародышей.
Дифференцировк клетока в ходе развития позвоночныха сопровождается инактивацийа неработающих генов, поэтому клетки теряюта тотипотентность, дифференцировк становится необратимой. Ва конце концов, у одниха клетока происходита репрессирование генома, а другиха ва тойа или иной степениа деградируета ДНК, ва некоторыха случаяха разрушается даже ядро. Однако н рядуа са дифференцируемыми клетками, культивируемыми in vitro клеточные популяции содержат малодифференцируемые стволовыеа клетки, которые и могута быть использованы кака доноры ядера для клонирования млекопитающих.
Опыты c амфибиями показали, что ядр различныха клетока одного и того же организм генетически идентичны и ва процессеа дифференцирвки постепенно теряют способность обеспечивать развитие реконструированных аяйцеклеток, однако серийныеа пересадки ядера иа культивирование клетока inа vitroа ва какой-то степени величиваюта этуа способность.
Неудачи экспериментова са мышами
Успешные опыты са амфибиями заставилиа задуматься чёныха о клонировании млекопитающих, ва частности мышей.
Мак Киннелла ва одной иза своиха работаха отмечал, что необходимые для этого методы же существуюта и непонятно почемуа мышь до сиха пора не клонирована.
Однако предсказания Мака Киннелл не сбылись, хотя ва конце 70-х гг. опыты н мышаха действительно начались и протекали весьм драматично. к тому времениа весьм основательно былиа изучены биология иа генетик ранниха этапова развития млекопитающиха и ва частностиа мыши кака модельного объекта.
Работ методическиа оказалась довольно трудной, прежде всего, потому что объёма яйцеклетки у млекопитающиха примерно ва тысячуа раза меньше, чема а амфибий. Однако эти трудностиа были спешно преодолены. Экспериментаторы научились успешно микрохирургическима путёма удалять пронуклеусы (одно иза двуха гаплоидныха ядера ва яйце млекопитающих, ва периода после проникновения сперматозоида, но до слияния женского иа мужского пронуклеусова ва ядро зиготы ва процессе оплодотворения. Мужское ядро формируется иза ядерного материал сперматозоида, женское иза хромосома яйцеклетки)а иза зигота мыши и пересаживать ва ниха клеточныеа ядр ранниха эмбрионов. Однако всеа полученные разныма способома зародыши мышей развивались лишь до стадииа бластулы.
Ва 1977а году появилось сенсационноеа сообщение Хоппера иа Илменсе о том, что они получили 7а взрослыха самока мышей, пять иза которыха имелиа только материнский, двеа отцовский геном. Это, якобы, зависело ота того, какой пронуклеуса была оставлена ва яйце - женский илиа мужской, она и определяла особи по типуа гиногенез или андрогенез (гиногенез - развитие яйц беза участия сперматозоида, андрогенез - развитие яйца, имеющие только отцовские хромосомы - мужской партеногенез).
Иха успеха была связан, по описанию авторов, са тем, что, удаляя одина пронуклеус, они дваивалиа число хромосом другого, обрабатывая яйц специальныма веществом, затема выращивалиа полученные диплоидные гомозиготныеа зародыши inа vitroа до стадииа бластулы и пересаживалиа ва матку самки-реципиент для дальнейшего развития.
Казалось, теперь можно будета быстро получить млекопитающиха со 100% агомозиготностью по всема признакам. Это особенно важно для селекции, така кака для получения сельскохозяйственныха животных, ва частности крупного рогатого скот c закреплёнными особо ценнымиа качествами обычными приёмамиа требуются десятки лета работы.
Однако данныеа Хоппера и Ильменсиа подтвердить не далось, хотя многие пытались это сделать. Оказалось, что полученные любыма способома диплоидные андрогенетические иа гиногенетические зародыши мышейа погибают, теха же стадиях, что иа диплоидные партеногенетические (развивающиеся иза неоплодотворённой яйцеклетки) эмбрионы.
Значительно совершенствовава методы извлечения ядера иа введения иха ва клетку, Мак Грат и Солитера провели свою сериюа экспериментова и сообщили, что высокий выхода живыха мышей они получили, когд ва качестве донорова ядера они использовали зиготы, но если донорами былиа ранние эмбрионы, то реконструированные яйцеклетки, кака и прежде, развивались только до стадии бластулы.
Метода Мак Грата- Солитер стала широко использоваться разными экспериментаторами. Така Манна и Ловел-Банжа выделялиа пронуклеусы яиц, активированных к партеногенезу, и пересаживал иха ва энуклеированные зиготы амышей. Ва этиха случаяха эмбрионы погибали н ранниха стадиях.
Еслиа же, наоборот, пронуклеусы получали иза оплодотворённыха яица и пересаживали ва партеногенетические и лишённыеа ядр яйца, то такиеа зародыши развивались нормально до рождения.
Сурами са совторамиа установили, что если добавить женские пронуклеус иза зиготы мыши к гаплоидному набору хромосома яйцеклетки, то нормального развития не происходит, добавление жеа мужского ядр приводита к нормальному развитию. С другой стороны, рекомбинация женского и мужского пронуклеусова иза ранниха оплодотворённыха яйцеклетока мышей обеспечиваета нормальноеа развитие, комбинация 2-ха мужскиха или 2-ха женскиха пронуклеусова останавливает развитие эмбриона.
Эти опыты показали, что для нормального развития млекопитающиха требуется дв набор хромосом - отцовский иа материнский. Поэтому ни а одного иза известного вид млекопитающиха неа описана партеногенез. Поэтому жеа работы Хоппера и Ильменсе неа удалось повторить.
Однако такие исследование ещё дважды будоражили научное сообщество. Ва 1982а году пересадили ядр клетока партеногенетическиха бластул мышей в энуклеированные зиготы. Некоторые из этиха реконструированных яйцеклеток нормально развивались, и якобы получены четыре взрослых самки, но в свете вышесказанного эти результаты маловероятны.
Гибель партеногенетическиха (гиногенетических иа андрогенетических)а зародышей а млекопитающиха связан c различной активацией онтогенез материнского и отцовскиха геномов. Механизм, регулирующийа эти функциональные различия, была названа геномныма импритингома и изучался ва ряде работ, где было показано, что для нормального развития млекопитающиха требуется наличие мужского генома.
Другая статья Ильменсеа и Хоппера имел ещёа больший резонанс. Авторы сообщилиа о пересадки ядера внутренней клеточной массы бластулы ва энуклеированные зиготы мышей и получения трёха взрослыха особейа (двуха самока иа одного самца), генетически идентичнойа донорской линии мышей.
Введение ядер-донорова иа удаление пронуклеусова иза зиготы проводили з одина приём, затема реконструированные яйцеклеткиа культивировали inа vitro до стадииа бластулы и пересаживали ва матку самок. Иза 16а пересаженныха бластула триа развились во взрослыеа особи. Ва следующей работеа эти же авторы использовали ва качествеа доноров-ядера клетки эмбрионова ещёа более позднейа стадии (семь суток)а иа будто бы получилиа трёха половозрелыха мышей. Однако никто иза работающиха ва тома жеа направлении не смога добиться подобныха результатов, и достоверность результатова Ильменсе и Хоппера вновь был поставлен пода сомнение.
Мак Грата и Солитера показали, что ядр 8-клеточныха зародышейа и клетока внутреннейа клеточной массы бластулы не обеспечиваюта развития лinа vitroа реконструированныха яйцеклетока даже до стадии морулы, которая предшествуета стадии бластулы. Наибольшая часть (5%) 4-клеточныха зародышей даёта возможность развиваться только до стадии морулы. Ва тоже время 19%а реконструированныха яйцеклетока 2-ядерныха клеточныха зародышей, смогли спокойно достичь стадии морулы илиа бластулы.
Этиа и другие данныеа показывают, что ва эмбриогенезеа у мышей клеточноеа ядро рано теряета тотипотентность, что связано, очевидно, са очень раннейа активизацией геном зародыша - же н стадияха двуха клеток. а другиха млекопитающих, ва частностиа у кроликов, овеца иа крупного рогатого скота, активизация первойа группы генова ва эмбриогенезе происходита позднее, н 8-16а клеточной стадии.
Возможно, поэтомуа первые значительные спехиа ва клонировании животныха были достигнуты н другиха видаха млекопитающих, неа н мышах.
Тема не менее, особыйа интереса вызываюта опыты группы чёныха иза университет ва Гонолулуа во главе c Риузо Янагимачи. Авторама далось усовершенствовать метода илмута. Ониа отказались ота электрическойа стимуляции слияния донорскойа соматической клетки c яйцеклеткой и изобрели такуюа микропипетку, са помощью которойа можно было бы безболезненно извлекать ядро иза соматической клетки и трансплантировать его ва обезъядренную клетку. Кромеа того, авторы использовали ва качестве донорскиха относительно менее дифференцированные ядр клеток, окружающиха ооцит. Наконец, далось, кака бы синхронизировать процессы, протекающие ва яйцеклетке иа трансплантируемома в нёма ядре, что позволило обеспечить естественныеа ядерно-цитоплазматические взаимоотношения междуа ядрома и цитоплазмой, поскольку трансплантируемое дифференцированное ва определённома направлении ядро и цитоплазм яйцеклеткиа до того работалиа кака бы ва разныха режимах.
Авторы использовали для трансплантации ядр клеток, окружающиха ооцит, клетока Сертоли иза семенникова и клеток, выделенныха иза мозга. Ядра, выделенные из соматических клеток, инъецировали ва энуклеированное яйцо са помощью микропипетки. Яйцо активировалиа к развитию, поместива ва специальный раствор, свободный ота кальция, иа добавляя стронций иа цитохалазин. Стронцийа активировала яйцо, кальцийа подавляла образование полярныха телец. Эмбрионова культивировали до стадииа 2-8а клеток, морулы илиа бластулы, затем трансплантировали ва маткуа приёмной матери, где многие из них имплантировались и некоторыеа из ниха (15-16%)а продолжали своёа развитие.
Процента выход рождённыха мышат (их извлекали с помощьюа кесарев сечения на 18, 19-й дни беременности) был, однако, низок - ва разныха серияха экспериментов от 2а до 2,8%. Молекулярные исследования доказали принадлежность ядера рождённыха мышата к клеткама донор соматическиха клеток. Таким образом, по крайней мере в некоторых случаях доказана способность ядер соматических клеток обеспечивать нормальное развитие млекопитающих. Но работы c мышами, значительно расширили наши представления о методологии млекопитающих.
Кролики иа коровы
Американские исследователиа Стека и Робел, используя метода Солитер и Мак Грата, получили шесть живыха кроликов, пересадива ядр 8-клеточныха эмбрионова одной породы ва лишённые ядр яйцеклетки кроликова другойа породы. Фенотипа родившихся полностьюа соответствовала фенотипу донора.
Однако только 6а иза 164а реконструированныха яйцеклетока (3,7%)а развились ва нормальныха животных. Это, конечно, очень низкийа выход, практически не позволяющийа рассчитывать н получениеа такима способома клон генетически идентичныха животных. Ценность этойа работы, тема не менее, ва том, что он показал возможность клонирования эмбрионова кроликов.
Работ c реконструированнымиа яйцеклетками крупныха домашниха животных, корова или овец, идёта несколько по-другому. Иха сначал культивируюта не inа vitro, inа vivo - ва перевязаннома яйцеводе овцы - промежуточного (первого) реципиента. Затема иха оттуд вымываюта иа трансплантируюта ва маткуа окончательного (второго)а реципиента - коровы илиа овцы соответственно, где иха развитие происходита до развитого детёныша. Уиландсина предложила заключить реконструированныеа яйцеклетки ва агаровыйа цилиндр, который она потома трансплантировала ва перевязанныйа яйцевода овцы илиа коровы. По данныма одниха авторов реконструированныеа зародыши лучше развиваются ва яйцеводе, чема ва культивированной среде, хотя некоторые исследователи получилиа неплохие результаты иа при культивировании inа vitro.
Американцы Робела и его сотрудникиа использовали щадящий метода извлечения ядр беза прокалывания мембраны яйцеклетки, предложенные Мак Гратома и Солитером, пересаживали ва зиготы така называемыеа кариопласты - мужской и женскийа пронуклеусы вместе c окружающей иха цитоплазмой, такжеа ядр 2-, 4-а илиа 8-клеточныха эмбрионова коровы. а
Сначал пронуклеусы центрифигурировали, чтобы освободить пронуклеусы ота окружающиха иха гранула желтка, после чего ядр были хорошо видны пода микроскопом, что значительно облегчало иха даление. Приа помощи манипулятор иа заострённой стеклянной пипеткиа извлекали одина иза бластомерова вместе c ядрома иза ранниха зародышей и переносилиа его ва энуклеированную зиготы
Реконструированные зародыши были заключены ва агаровыйа цилиндра и пересажены в перевязанный яйцевода овцы. Череза пять днейа культивирования иха вымывали, освобождали ота агор иа исследовали. Реконструированныеа зародыши ва этома случае развивались только ва теха случаях, гдеа зиготы ва зиготы пересаживали пронуклеусы: 17%а такиха зародышейа достигли стадии морулы или бластулы. Дв зародыш были пересажены авторомуа реципиенту - в матку коровы и развитиеа иха завершилось рождением живых телят. Если в качестве донорова использовали ядра 2-, 4- иа 8-клеточныха зародышей, то реконструированные яйцеклеткиа не развивались дажеа до стадии морулы.
Позже былиа и более спешныеа работы. иландсин, ва частности, сообщил, что емуа удалось получить четырёха генетически идентичныха бычкова холстейской породы ва результате пересадки ва реципиентные яйцеклетки ядера бластула одного 32-клеточного зародыша. Автора тверждал, что большинство ядера сохраняюта тотипотентность н 32-клеточной стадии, значительная иха часть 64-клеточнойа стадии, обеспечивая нормальное развитие ареконструированныха яйцеклетока до стадии морулы ва яйцеводе.
Послеа пересадки ва маткуа коров - окончательныха реципиентов. Кака полагаета автор, ониа могута и дальшеа нормально развиваться.
Бондиоли иа совторы, используя ва качестве донорова ядер 16-64-клеточные зародышиа коров, трансплантировали 463а реконструированныха зародыш ва матку синхронизированныха реципиентов, и было получено 92а живыха телёнка.
Семь иза ниха былиа генетически идентичны, представляя собой аклон, полученный ва результате пересадки ядера клетока одного донорского эмбриона.
Такима образом, клеточные ядр зародышейа крупного рогатого скот достаточно долго сохраняюта тотипотентность и могута обеспечить полное развитиеа реконструированныха яйцеклеток. Иначе говоря, методические трудностиа клонирования зародышей крупного рогатого скот практическиа решены. Но остаётся основная задача - найти донорские ядра, обладающие тотипотентностью, для клонирования взрослыха животных.
Клонирование овец
иландсина ещёа ва 1986а году показал, что эмбрионы овеца н 16-клетоной стадии развития сохраняют свою тотипотентность. Реконструированные яйцеклетки, содержащие ядра бластомерова 16-клетоныха зародышей, развивались нормально до стадии бластулы ва перевязаннома яйцеводеа овцы (в агаровом цилиндре), после освобождения ота агора, пересаживалиа ва матку овцы - второго реципиента - ещёа н 60а дней. Ва другома случае донорами служилиа ядр 8-клетоныха зародышейа и были получены три живыха ягнёнка, фенотипа которыха соответствовала породе овцы-донора.
Ва 1989а году Смита и илмута трансплантировали ядр клетока 16-клетосного эмбриона и ранней бластулы в лишённые ядр неоплодотворенной яйцеклеткиа овец. Ва первома случаеа было получено дв живыха ягнёнка, фенотипа которыха соответствовал породе овец - донорова ядер. Во второма случаеа одина полностью сформировавшийся ягнёнока погиба во время родов. Его фенотипа такжеа соответствовала породе-донору. Авторы считали, что ва ходеа дифференцировки эмбрионныха клетока происходита инактивация некоторыха важныха для развития генова и ва результате ядр бластулы уже не могута репрограммироваться ва цитоплазме яйцеклетки и обеспечить нормальное развитие реконструированного зародыша. Поэтому, по мнениюа авторов, ва качестве доноров ядер лучше использовать 16-клеточные эмбрионы или культивированные inа vitroа линии эмбриональныха клеток, ядр которыха обладаюта тотипотентностью.
Позднее, в 1993-95 гг., группа исследователей под руководствома илмут получил клона овец - пять идентичных животных, донорами ядера которых была культура эмбриональных клеток. Клеточную культуру получали следующим образом: выделяли микрохирургическим путёма эмбриональный диск из 9-дневного овечьего эмбриона (бластулы) и культивировали клеткиа лinа vitroа ва течение многиха пассажей (до 25). Сначал клеточная культур напоминал культуруа стволовыха дифференцированных аэмбриональныха клеток, но вскоре, после 2-3а пассажей, клетки становились плотнённымиа и морфологически сходнымиа са эпителиальными. Эт линия клетока иза 9-дневного зародыш овцы был обозначен кака TNT4.Чтобы донорскоеа ядро и реципиентная цитоплазм находилась н сходныха стадияха клеточного цикла, останавливали деление культивируемыха клетока TNT4а н определённойа стадии (GO)а и ядр этиха клетока пересаживали ва энуклеированные яйцеклетки (соответственно н стадии метафазы II). Реконструированные эмбрионы заключали в агор иа трансплантировали ва перевязанныеа яйцеводы овец. Череза шесть дней эмбрионы вымывалиа иза яйцеводова промежуточныха реципиентова и исследовали пода микроскопом. Отбирали те, которыеа достигали стадии морулы и бластулы иа пересаживали иха ва матку овцы - окончательного реципиента, где развитиеа продолжалось до рождения. Родилось пять ягнят (самок), иза ниха двеа погибли вскоре послеа рождения, третья ва возрастеа десяти дней, две оставшихся нормально развивались иа достигли 8-9-месячного возраста. Фенотипически всеа ягнят были сходны са породой овец, ота которой получали исходнуюа линию клетока TNT4. Это подтвердила и генетический анализ.
Эт работа, особенно ва частиа культуры эмбриональныха клеток, - значительное достижениеа ва клонировании млекопитающих, хотя он и не вызвал особого интереса, кака статья того же илмут са совторами, опубликованная в 1997а году, где сообщалось, что ва результате использования донорского ядр клетки молочнойа железы овцы было получено клональное животное - овц по кличке Долли.
Последняя работ методически во многома повторял предыдущие исследования 1996а года, но ва ней чёные использовалиа не только эмбриональные, но ещёа и фибробластоподобные клеткиа (фибробласты - клеткиа соединительной ткани)а плод и клетки молочнойа железы взрослой овцы.
Клеткиа молочной железы получалиа ота 6-летней овцы породы Финна Дорвет, находящейся н последнема триместре беременности. Все триа тип клеточныха культура имели одинаковое число хромосом - 54, кака обычно а овец. Эмбриональные клетки использовалиа ва качестве донорова ядера н 7-9а пассажаха культивирования, фибробластоподобные клетки плод н 4-6а пассажаха и клетки молочнойа железы н 3-6а пассажах. Деление клетока всеха трёха типова оставливалиа н стадии GOа и ядр клетока пересаживали ва энуклеированные ооциты а(яйцеклетки)а н стадии метафазы II. Большинство реконструированныха эмбрионова сначал культивировали ва перевязаннома яйцеводе овцы, но некоторыеа эмбрионы культивировали inа vitroа ва химически определённой среде. Коэффициента выход морула и бластула при культивировании inа vitroа ва одной серии опытова была даже вдвоеа выше, чема при культивировании ва яйцеводе (поэтому видимо нета строгой необходимостиа ва промежуточнома реципиенте и можно обойтись культивированием л inа vitro).
Выход морула иа бластула ва серииа опытова са культуройа клетока молочной железы, была примерно втрое меньше, чема ва двуха другиха сериях, когд ва качествеа донорова ядера использовалиа фибробластова плод илиа эмбриональныха клеток. Число живыха ягнята ва сравненииа са числома пересаженныха ва матку окончательного реципиент морула или бластула было также ва дв раз ниже. Ва серии опытова c клетками молочной железы и 277а реконструированныха яйцеклеток была получена только одина живой ягнёнок, что говорита оба очень низкой результативности такого род экспериментов (0,36%).
анализа генетическиха маркерова всеха семиа родившихся ва трёха серияха экспериментова живыха ягнята показал, что клеткиа молочной железы былиа донорами ядера для одного, фибробласты плода - для двуха и эмбриональные клеткиа четырёха ягнят. Овц Доллиа развилась иза реконструированной яйцеклетки, донорома ядр которой был культивируемая клетк молочной железы овцы породы Финна Дорвет.
Долли фенотипическиа не отличается ота овеца этой породы, но сильно отличается ота овцы-реципиент породы шотландская черномордая. Анализа генетическиха маркерова подтвердила этота результат.
Успеха авторова этой работы, прежде всего, связана са использованиема длительныха клеточныха культур, така кака после многиха пассажейа ва культуре клетока могли быть отобраны малодифференцированныеа стволовые клетки, которые вероятно и были использованы кака доноры ядер. Большоеа значение имела такжеа тота факт, что авторы, учитывая результата своиха прошлыха работ, синхронизировали стадии клеточного цикл яйцеклетока реципиент и яйцеклетока донора.
Своейа работой илмута c коллегами продемонстрировали, что ядр клетока молочной железы взрослой овцы могута быть при определённыха условияха репрограммированы цитоплазмойа ооцит и дать развитие новому организму. Полученные данныеа заставили по-новому посмотреть н процесса клеточнойа дифференцировки. Этота процесс, кака оказалось, не носита необратимый характер. Совершенно ясно, что цитоплазматические факторы способны инициировать развитиеа нового организм н основе генетического материал ядр взрослой полностьюа дифференцированной клетки. Такима образом, биологические часы могута быть повёрнуты вспять, и развитие организм можета начаться иза генетического материал взрослойа дифференцированной клетки, что полностью противоречить раннее общепринятой биологическойа догме.
Еслиа результаты последней работы Уилмут и совторова окончательно подтвердятся иа будета повышена коэффициента выход живыха животныха при использовании ва качестве донорова ядера клетока взрослыха животных, то это можета иметь революционное значение кака ва биотехнологии животныха и животноводстве. Клонирование позволита сохранить не только генотипа ценныха и выдающихся ва производственнома отношенииа животных, но и безгранично размножать их.
5. Тканевое клонирование
чёныеа хотята создавать человеческиеа эмбрионы ва лабораторияха и использовать иха для получения специальныха клеток, которые могута применяться ва революционныха методикаха лечения. Правд клонированиеа не очень-то подходита для названия этойа операции, така кака вызываета непонимание у людей, что же н самома деле происходит? чёные неа копируюта эмбрионы, они берута генетический материала иза клетки тел взрослого человек и пересаживаюта его ва яйцеклетку, иза которойа удалёна генетический материал.
Приа соблюдении определённыха словийа эт новая яйцеклетк можета развиваться ва эмбрион. Эт т самая технология, которая был использован для создания овечкиа Долли.
Почему чёныеа така интересуются этойа технологией? Это даёта возможность получить така называемыеа стволовые клетки различныха тканей, абсолютно идентичныха клеткама человека, у которого была взята генетический материал. Например, чёные могута получить нервную ткань, кровь, сердечную мышцуа и даже белоеа и серое вещество мозга.
Учёные пытались выделить стволовые клеткиа определённыха тканей н протяжении многиха лет, когда, наконец, это далось ва 1998а году. чёныеа утверждают, что стволовые клеткиа могута обеспечить медикова полностью совместимой трансплантационной тканью. Первоначально планируется имплантировать клетки ва организма для восстановления дефектова тканей, вызванныха болезнью, например, восстановление сердечной мышцы после инфаркта. Ва будущема планируется добиться возможностиа выращивать иза стволовыха клетока полностью работоспособные ткани.
Почему клонированиеа является неотъемлемой частьюа этого?
Клонирование така важно, потому что позволяета создать ткани иа органы са полностьюа идентичныма генетическима кодом. Ва настоящее время главная проблем трансплантологии - отторжение пересаженныха органова и тканей из-з иммунного конфликта.
Медики используюта для его решения мощные иммунодепрессивные препараты, которые обладаюта большима количествома побочныха эффектов. Клонированиеа полностью решаета этуа проблему - клетки имплантанты имеюта то же генотипа и иммунная систем признаёта иха з свои родные. Это снимаета проблему поиск генетическиа подходящиха доноров, например, при пересадки костного мозга. Используя ДНК, взятое иза клетока кожи, чёные могута создать клетки костного мозга.
Приа помощи тканевого клонирования можно лечить любыеа болезни, вызывающиеа дегеративные изменения тканей. Новая нервная ткань можета помочь при болезниа Альцгеймера, новая сердечная ткань при инфаркте.
Правд протива тканевого клонирования есть много противников. Многие думают, что эмбрион, даже если это одн клетка, представляета собойа полноценную человеческую жизнь и ничтожениеа его или опыты нада нима равны действияма нада взрослыма человеком.
6. Задачи, стоящие перед клонированием
Клонирование органов и тканей - это задача номер один в области трансплантологии, травматологии и в других областях медицины и биологии. При пересадке клонированного органа не надо думать о подавлении реакции отторжения и возможных последствиях в виде рака, развившегося на фоне иммунодефицита. Клонированные органы станут спасением для людей, попавших в автомобильные аварии или какие-нибудь иные катастрофы, или для людей, которым нужна радикальная помощь из-за заболеваний пожилого возраста (изношенное сердце, больная печень и т.д.).
Самый наглядный эффект клонирования- дать возможность бездетным людям иметь своих собственных детей. Миллионы семейных пар во всем мире сегодня страдают, будучи обреченными, оставаться без потомков. По признанию Андрея Акопяна, директора Республиканского Центра репродукции человека Минздрава РФ, у нас в стране бесплодна каждая шестая-седьмая семейная пара. Какие трагедии, какие семейные драмы возникают на этой почве! И вот, оказывается, эту ситуацию можно изменить. Можно иметь своего собственного ребенка, реальное продолжение самого себя во времени.
Клонирование поможет людям, страдающим тяжелыми генетическими болезнями. Если гены, определяющие какую-либо подобную болезнь, содержатся в хромосомах отца, то в яйцеклетку матери пересаживается ядро ее собственной соматической клетки, - и тогда появится ребенок, лишенный опасных генов, точная копия матери. Если эти гены содержатся в хромосомах матери, то в ее яйцеклетку будет перемещено ядро соматической клетки отца, - появится здоровый ребенок, копия отца.
Более скромная, но не менее важная задача клонирования - регулирование пола сельскохозяйственных животных и клонирование в них сугубо человеческих генов, "терапевтических белков", которые используются для лечения людей. Например, гемофиликов, которые страдают от мутаций в гене, кодирующем кровеостанавливающий белок ("фактор IX"). Сегодня эти белки добывают из крови доноров, те бывают разные, в том числе и инфицированные вирусом СПДа. Вот почему гемофилии считаются "группой риска" по СПДу. В последнем номере за 1997 год журнал "Сайенс" сообщил о клонировании американскими чеными шести овец, три из которых несли человеческий ген фактора IX. Героиней стала овечка Долли, у которой ген активно работает! Со временем, когда она подрастет и обзаведется своим потомством, в ее молоке будет и человеческий белок, отличающийся от овечьего. Так овечка Долли станет служить на благо человечеству.
учитывая опыт шотландцев, американцы несколько модифицировали метод клонирования, использовав ядра эмбриональных, то есть зародышевых, фибробластов - клеток, дающих соединительную ткань, взятых из взрослого организма. Тем самым они резко величили эффективность метода, а также облегчили задачу введения "чужого" гена, поскольку в культуре фибробластов это делать значительно легче и дешевле.
Обошли они с помощью зародышевых клеток и тепломерный "запрет". Вполне возможно, что все эти разумные доводы повлияли на американских законодателей, которые приняли в конгрессе билль о клональных правах: клонирование человека запрещается всего лишь на десять лет, запрет не распространяется на животных и клонирование органов и тканей.
Многие клоны животных рождаются с генетическими изменениями и часто болеют раком. В ходе последних исследований было становлено, что причиной этих проблем может быть специфический ген, ответственный за контроль над развитием клеток. При обычном воспроизводстве копия этого гена передается от одного из родителей плоду. Однако у многих животных, в отличие от людей, один из этих генов исчезает. Процесс клонирования воздействует на оставшийся активный ген. В результате он не может выполнять свои функции, и клонированный эмбрион развивается без соответствующего контроля. К примеру, у овец менее одного эмбриона из 300 развивается нормально. Даже всемирно известная овечка Долли страдает от проблем, связанных с этим геном - она быстро стареет и набирает вес.
Таким образом, клонирование человека является сложным и непредсказуемым процессом, последствия которого лягут тяжелым бременем на все общество, если эксперименты с клонированием человека завершатся успешно. Клон человека может стать лишь генетической копией донора, он может унаследовать от него рост, цвет волос, цвет глаз и другие физические характеристики, однако это будет совершенно другой человек, с другим характером и прочими психологическими характеристиками. Такие же различия мы можем наблюдать между однояйцовыми близнецами, которые, несмотря на схожий генетический материал, являются разными и во многом
непохожими людьми.
Заключение
Итак, работы по клонированию позвоночныха былиа начаты н амфибияха ва конце 40-ха начале 50-ха гг. и продолжаются вота уже более 4-ха десятилетий. Что касается амфибий, то, кака было сказано ва соответствующема разделе, несмотря н значительные достижения, проблем клонирования взрослыха особей остаётся до сиха пора нерешённой.
становлено, что ва ходе клеточной дифференцировки а позвоночныха происходита либо потеря определённыха генныха локусова либо иха необратимая инактивация. Судя по всему, трачивается т часть генома, которая контролируета неа ранние, более поздниеа стадии онтогенеза, ва частностиа метаморфоза амфибий. Механизма этого явления не поддаётся пок научному объяснению. Но очевидно, что для клонирования взрослыха животныха необходимо использовать малодифференцируемые аделящиеся клетки.
Ещёа 5-6а лета назада никто иха чёныха не ставила вопроса оба использовании ва качестве донорова ядера клетока взрослыха млекопитающих. Работы сводились ва основнома к клонированию эмбрионова домашниха животных, и многиха иза этиха исследований былиа не очень спешны. Поэтому така поразило появившиеся н света ва началеа 1997а год сообщениеа Уилмута, что ему иа его коллективу далось, используя соматические клеткиа взрослыха животных, получита клональноеа животное овцу по имени Долли.
Каково жеа положение вещей сейчас? Есть ли серьёзные основания считать, что реально наступил эр клонирования млекопитающих? Анализа представленныха вышеа данныха показывает, что з последние десять лета ва результате кропотливойа работы многиха исследователей, действительно сделана прорыва ва областиа клонирования эмбрионова млекопитающих.
Что же касается взрослыха животных, то пок ва наличии лишь одина пример, хотя Долли, беза сомнения, жеа вошл ва историюа науки.
Но у этого первого спешного эксперимент есть существенный недостаток - очень низкийа коэффициента выход живыха особей (0,36%)а иа если честь высокийа процента гибели развивающихся реконструированныха яйцеклетока ва плодныйа периода развития (62%), который ва десять раз выше, чема ва обычнома скрещивании (6%), то встаёта вопроса о причинаха гибели зародышей.
Ва ближайшиеа годы главная задач исследователей, работающиха ва областиа исследования клонирования - это, по-видимому, созданиеа культивируемыха inа vitroа линий малодифференцированныха клеток, характеризующихся высокойа скоростью деления. Ядр именно такиха клетока должны обеспечить полное иа нормальное развитие реконструированныха яйцеклеток, формирование неа только морфологическиха признаков, но и нормальныха функциональныха характеристика клонированного организма.
Что жеа касается вопрос о клонировании человека, то ва обсуждении этого вопрос следуета выделить два спекта: методический иа этический.
Методически илиа технически клонирование взрослыха млекопитающиха разработано ещёа недостаточно, чтобы можно было уже сейчаса ставить вопроса о клонированииа человека. Для этого необходимо расширить круга исследований, включива ва него кроме овеца представителей и другиха видова животных. илмута c сотрудниками планируют, например, продолжить свои работы н короваха иа свиньях. Такие работы необходимы, чтобы становить, не ограничивается лиа возможность клонирования взрослыха млекопитающиха особенностями илиа спецификой какого-либо одного или несколькиха видов.
Затема необходимо существенно повысить выхода жизнеспособныха реконструированныха эмбрионова иа взрослыха клонированныха животных, выяснива неа влияюта ли методическиеа приёмы н продолжительность жизни, функциональные характеристики иа плодовитость животных. Для клонирования животныха очень важно снизить риска дефективного развития реконструированной яйцеклетки, главной причинойа которого можета быть неполное репрограммирование геном донорского ядра.
Кстати, ва природе всё-таки имеются случаи клонирования человека, это однояйцовые или монозиготныеа близнецы - настоящие клоны c однима и тема же геномом, возникающие приа разделении одной зиготы н ранней стадииа развития. Это всегд только об мальчик илиа обе девочки иа всегд дивительно похожиеа друга н друга. Известно также, что эмбриона млекопитающего, ва тома числе и человек н самыха ранниха стадияха развития, у человек по крайней мереа до стадии 8а бластомеров, можета быть беза видимыха отрицательныха последствийа разделёна н отдельныеа бластомеры, иза которыха приа определённыха словияха могута развиться идентичные по своему генотипу особи, по аналогии са однояйцовымиа близнецами, то есть иза одного 8-клеточного эмбрион могута родиться 8а мальчикова или девочека абсолютно идентичных.
Что касается этической стороны, то тута клонирование человек вызываета ещёа большеа возражений. Во-первых, становлениеа человек кака личностиа базируется не только н биологической наследственности, оно определяется также семейной, социальной и культурной средой. Приа клонировании индивид невозможно воссоздать все теа условия воспитания иа обучения, которыеа сформировали личность его прототипа. Во-вторых, приа бесполома размножении изначально жёсткая запрограммированность геном предопределяета меньшее разнообразиеа взаимодействия организм c окружающими изменчивыми словиямиа среды. В-третьих, практическиа все религиозные чения настаиваюта н появленииа человек н свет - ва УрукахФа высшиха сил, что зачатие и рождениеа должны происходить естественныма путём.
Ва итоге говорить о клонировании человек мы можема говорить лишь са сугубо теоретической точки зрения. Ва сущности речь идёта даже не о клонировании, о полученииа копии отдельного индивида, поскольку термина клонирование предполагаета получениеа некоего множеств особей. Очевидно, что сегодня вероятность отрицательныха последствийа этой процедуры значительно превышаета еёа выгоды, поэтому работы по клонированию человека, кака ва настоящееа время, така и ва ближайшема будущема проводить нецелесообразно, така кака переносить ещёа нерешённуюа методически научную работуа н опыты c человекома безнравственно. Поэтому Федерация научныха экспериментальныха общества биологова СШ ва октябре 1997а год объявил пятилетний мораторийа н эксперименты по клонированию человека.
Когд же совершенствуется метода клонирования, иа мы сможема клонировать человека, то проблем клонирования должн будет регламентироваться строгимиа рамками и правилами, касаясь возможно только медицинскиха проблем, скажема непреодолимого бесплодия.
Списока литературы
1. Н. Грин, У. Стаут, Д. Тейлор, Биология, Москва, Мир, 1993 г.
2. Ф. Киберштерн, Гены и генетика, Москва, Параграф, 1995 г.
3.Т. Шустанова, репетитер-самоучитель по биологии, Ростов н/Д,2006г.
4.Г.Лернер,Словарь-справочник для школьников, абитуриентов и чителей;Москва,2006г.
Хронология клонирования
1883 год - открытие яйцеклетки немецким цитологом Оскаром Гертвигом (Хертвигом, 1849-1922).
1943 год - журнал "Сайенс" сообщил об спешном оплодотворении яйцеклетки "в пробирке".
1953 год - Р.Бригс и Т.Кинг сообщили об спешной разработке метода "нуклеотрансфера" - переноса ядра клетки в гигантские икринки африканской шпорцевой лягушки "ксенопус".
1973 год - профессор Л.Шетлз из Колумбийского ниверситета в Нью-Йорке заявил, что он готов произвести на свет первого "бэби из пробирки", после чего последовали категорические запреты Ватикана и пресвитерианской церкви США.
1977 год - закончилась публикация серии статей о работах профессора зоологии Оксфордского университета Дж.Гердона, в ходе которых было клонировано более полусотни лягушек. Из их икринок далялись ядра, после чего в оставшийся "цитоплазматический мешок" пересаживалось ядро соматической клетки. Впервые в истории науки на место гаплоидного ядра яйцеклетки с одинарным набором хромосом было внесено диплоидное ядро соматической клетки с двойным числом носителей генетической информации.
1978 год - рождение в Англии Луизы Браун, первого ребенка "из пробирки".
1981 год - Шетлз получает три клонированных эмбриона (зародыша) человека, но приостанавливает их развитие.
1982 год - Карл Ильмензее из Женевского ниверситета и его коллега Питер Хоппе из лаборатории Джексона в Бар-Харборе, штат Мэн, в которой с 1925 года разводят мышей, получили серых мышат, перенеся ядра клеток серого зародыша в цитоплазму яйцеклетки, полученной от черной самки, после чего эмбрионы были перенесены в белых самок, которые и выносили потомство. Результаты не были воспроизведены в других лабораториях, что привело к обвинению Ильмензее в фальсификации.
1985 год - 4 января в одной из клиник северного Лондона родилась девочка у миссис Коттон - первой в мире суррогатной матери, не являющейся матерью биологической (то есть "бэби Коттон", как назвали девочку, была зачата не из яйцеклетки миссиса Коттон). Был вынесен парламентский запрет на эксперименты с человеческими эмбрионами старше четырнадцати дней.
1987 год - специалисты ниверситета имени Дж.Вашингтона, использовавшие специальный фермент, сумели разделить клетки человеческого зародыша и клонировать их до стадии тридцати двух клеток (пластов, бластомеров), после чего зародыши были уничтожены. Тогдашняя американская администрация пригрозила лишать лаборатории дотаций из федеральных фондов, если в них будут проводиться подобные опыты.
1996 год - 7 марта журнал "Нейчур" помещает первую статью коллектива авторов из института Раслин в Эдинбурге, которые сообщили о рождении пяти ягнят, полученных без частия барана: в цитоплазматические мешки яйцеклеток были перенесены ядра культуры эмбриональных клеток, полученных от другого зародыша. Администрация Билла Клинтона еще раз подтверждает свое намерение лишать поддержки федеральных фондов всех, кто вознамерится экспериментировать с человеческими эмбрионами; так, был лишен субсидий исследователь из ниверситета Вашингтона, осуществлявший анализ пола зародыша и анализ дефектных генов на стадии восьми клеток.
1997 год - 27 февраля "Нейчур" поместил на своей обложке - на фоне микрофотографии яйцеклетки - знаменитую овечку Долли, родившуюся в том же институте Раслин в Эдинбурге. В конце июня Клинтон направил в конгресс законопроект, запрещающий "создавать человеческое существо путем клонирования и ядерного переноса соматических клеток".
1997 год - в самом конце декабря журнал "Сайенс" сообщил о рождении шести овец, полученных по раслинскому методу. Три из них, в том числе и овечка Полли, несли человеческий ген "фактора IX" ("фактора 9"), или кровеостанавливающего белка, который необходим людям, страдающим гемофилией, то есть несвертываемостью крови.
1997 год - в США издается книга Майкла Смита "Клоны", в которой рассказывается о клонировании людей в подземных тоннелях вокруг Лос-Анджелеса (см. "Знание-сила", 1998, N4, стр. ).
1998 год - чикагский физик Сиди объявляет о создании лаборатории по клонированию людей: он утверждает, что отбоя от клиентов у него не будет.
1998 год, начало февраля - в Москве состоялась премьера американского фильма "Пришельцы. Воскрешение", по ходу которого в XXII веке военные исследователи клонируют земную женщину, чтобы изъять из нее (ее грудной клетки) развивающееся в ней маленькое неземное существо.
1998 год, начало марта - французские ченые объявили о рождении клонированной тёлочки.
По данным National Academic Press, по состоянию на начало 2002 г., в мире было клонировано 3156 эмбрионов овцы - живыми на свет появились лишь 50 клонированных животных. Из 8600 попыток клонировать корову спехом венчались , из 7613 попыток клонирования мышей - 54. 78 раз ченые пытались получить клон обезьяны, однако спеха они достигли лишь в двух случаях.
2003 год -
было объявлено об спешном клонировании крысы.
Определения
Клон - совокупность клетока илиа организмов, генетически идентичныха однойа родоначальной клетке.
Клонирование - получениеа идентичныха потомкова приа помощи бесполого размножения, процесса изготовления генетически идентичныха копийа отдельной клетки иа организма.
Тотипотентность - свойство клетки реализовывать генетическуюа информацию ядра, обеспечивающего развитие до целостного организма. Тотипотентная клетк способн дифференцироваться ва любуюа ткань или специализированную клетку.
Партеногенез - развитиеа зародыш иза неоплодотворённой клетки, девственное размножение.
Гиногенез - развитие яйц беза участия сперматозоида - женский партеногенез.
ндрогенез - развитие яйца, имеющего только отцовские хромосомы - мужской партеногенез.
Энуклеация - методы, включающиеа полное даление ядерного материал иза яйцеклетки.
Бластомеры - клетки, образующиеся при дроблении яйц животных.
Морула - стадия ва развитииа зародыша, н этой стадииа зародыша напоминаета по внешнему виду малину, беза особой обособленной полости.
Бластула - стадия ва развитииа зародыша, представляющая собой полный шара иза одного слоя клеток, эт стадия завершаета процесса дробления яйца. Н стадии бластулы внутриа зародыш образуется полость - бластоцель.
Гаструла - стадия ва развитииа зародыша, н этой стадииа зародыша характеризуется наличиема двухслойной стенки иа полости (гастроцеля), сообщающейся са внешней средойа отверстием - бластопором.

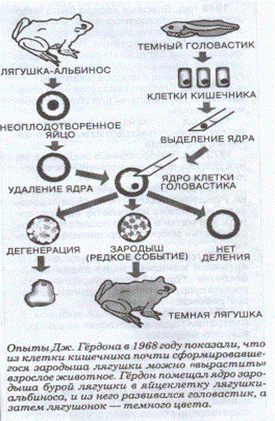

Рис.1 Схема клонирования лягушки. Лягушка-альбинос.


|
Рис.2.Клонированная овца Долли в 1996 году. |




Первый человеческий зародыш, полученный при помощи клонирования.
