Главная
/ Ответы на экзамены / химия - 9 класс
| Аммиак, состав его молекулы, физические и химические свойства (отношение к воде, кислороду, кислотам), применение.
Ответ можно начать с того, что для неметаллов характерно существование газообразных соединений с водородом. У азота таким соединением является аммиак NH3, который состоит из атома азота и трех атомов водорода. В молекуле аммиака три химических связи, образованных по ковалентному полярному механизму: 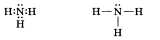 Далее можно перейти к описанию .физических свойств аммиака. Аммиак (NH3) — газ, без цвета, с резким запахом, легче воздуха (Мг = 17), хорошо растворим в в t°. «кип = -33,4 C° Рассматривая химические свойства аммиака, следует остановиться на следующих группах реакций, протекающих: 1. Без изменения степени окисления. а) Взаимодействие с водой: 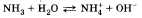 В результате растворения аммиака в воде образуются гидроксид-ионы ОН и ионы аммония NH. Раствор аммиака в воде называют аммиачной водой или гидроксидом аммония. Следует отметить также, что раствор аммиака в воде имеет щелочную реакцию среды, что говорит об основном характере гидроксида аммония. б) Взаимодействие с кислотами: 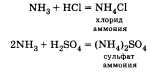 2. С изменением степеней окисления. Взаимодействие с кислородом (при этом продук ты реакции зависят от условий ее проведения): а) Горение в кислороде: 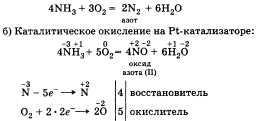 И в том и в другом случае аммиак за счет атома азота проявляет свойства восстановителя. При описании получения и применения аммиака важно подчеркнуть, что основной способ связывания азота воздуха — это соединение его с водородом — синтез аммиака: 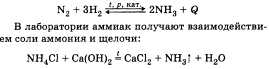 Используя аммиак, получают различные соединения, например азотные удобрения, азотную кислоту, нашатырный спирт. • Перейти к списку вопросов »
|
