Главная
/ Ответы на экзамены / химия - 9 класс
| Окислительно-восстановительные реакции. Окислитель и восстановитель.
Ответ можно начать с утверждения о том, что по изменению степени окисления химических элементов различают реакции окислительно-восстановительные и реакции, идущие без изменения степеней окисления (например, ионного обмена). Реакции, протекающие с изменением степени окисления, называются окислительно-восстановительными реакциями. Рассмотрим с точки зрения этого признака пример: 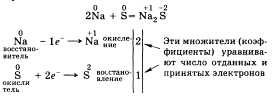 Частица (атом, ион), которая в ходе окислительно-восстановительного процесса отдает электроны, называется восстановителем. Процесс отдачи электронов — окисление. Восстановитель свою степень окисления повышает. В приведенном примере это натрий Na. Частица, принимающая электроны, — окислитель, он восстанавливается и понижает степень окисления. В нашем случае это сера S. Важно обратить внимание, что число электронов, отданных восстановителем, должно равняться числу электронов, принятых окислителем. В составе сложных веществ элементы могут иметь разные степени окисления. От этого зависит, окислителем или восстановителем является это вещество. Так, например, азотная кислота является окислителем. В состав азотной кислоты HNO3 входит азот, имеющий степень окисления +5, который в процессе окислительно-восстановительной реакции может только понижать свою степень окисления, принимая электроны. Сероводород H2S — восстановитель за счет атома серы со степенью окисления -2.  • Перейти к списку вопросов »
|
