|
< Предыдущая |
Оглавление |
Следующая > |
|---|
11.6. Мембранные процессы очистки сточных вод
Мембранный метод очистки сточных вод основан на свойствах пористых тел пропускать предпочтительнее одни вещества, чем другие. Способы мембранного разделения, используемые в технологии очистки воды, условно делятся на диализ, электродиализ, микрофильтрацию, ультрафильтрацию, обратный осмос. В соответствии с видом переноса вещества мембранные методы можно разделить на диффузионные, электрические и гидродинамические. Иногда один вид переноса вещества накладывается на другой для ускорения или улучшения разделения. К диффузионным методам относят газовую диффузию и диализ. При наложении электрического поля протекает электродиализ. Гидродинамическими методами являются фильтрация, ультрафильтрация и обратный осмос.
В технологии очистки сточных вод от растворенных и тонкодис-пергированных примесей чаще всего используют процессы обратного осмоса, ультрафильтрации и электродиализа. Обратный осмос применяют для обессоливания воды в системах водоподготовки, в системах локальной обработки сточных вод при небольших их расходах для концентрирования и выделения относительно ценных компонентов и для очистки природных и сточных вод.
В основе этих способов лежит явление осмоса - самопроизвольного перехода растворителя (воды) в раствор через полупроницаемую мембрану (рис. 11.6).
Наложение давления на систему, где мембрана разделяет два раствора, создает поле сил, порождающих потоки через мембрану (фильтрацию). Явление задержки растворенных молекул и ионов электролита при фильтрации через мембрану называется гиперфильтрацией или обратным осмосом (поскольку давление направлено навстречу возникающему осмотическому потоку).
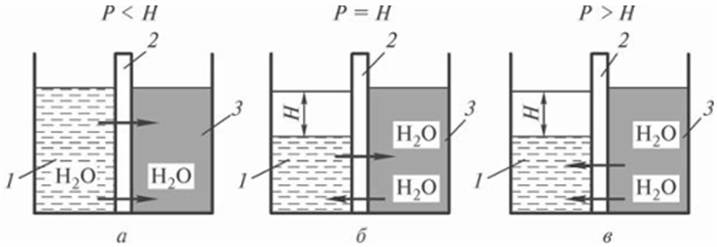 Рис. 11.6. Схемы осмоса (Я -осмотическое давление; Р- рабочее давление): а - прямой осмос; б - осмотическое равновесие; в - обратный осмос; 1 - чистая вода; 2- мембрана; 3 - раствор
Рис. 11.6. Схемы осмоса (Я -осмотическое давление; Р- рабочее давление): а - прямой осмос; б - осмотическое равновесие; в - обратный осмос; 1 - чистая вода; 2- мембрана; 3 - раствор
Обратный осмос - процесс фильтрования (концентрирования) растворов под давлением через микропористые мембраны с очень тонкими порами (радиус r ~ 10-7 см). Давление H в растворе, заставляющее растворитель переходить через мембрану, называют осмотическим давлением. Величина осмотического давления H (Па) для растворов определяется по уравнению Вант-Гоффа:
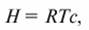 (11.35)
(11.35)
где R - газовая постоянная; Т - абсолютная температура раствора, К; с - молярная концентрация растворенного вещества.
Чем выше концентрация подлежащего очистке раствора (сточной воды), тем выше перепад осмотических давлений и тем больше гидродинамическое давление, необходимое для реализации очистки воды.
Кроме сопротивления мембраны рм надо преодолеть осмотическое давление π, направленное в другую сторону. Таким образом, перепад давления при обратном осмосе равен
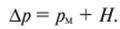 (11.36)
(11.36)
Создав над раствором давление pм равное осмотическому, осмос прекращается и наступает состояние равновесия. Если же над раствором создать избыточное давление π, превышающее осмотическое давление H на величину Δр, переход растворителя будет осуществляться в обратном направлении.
Механизм обратного осмоса состоит в том, что мембраны собирают воду, которая в поверхностном слое не обладает растворяющей способностью, и через поры мембраны будет проходить только чистая вода, несмотря на то, что размер многих ионов загрязнителей меньше, чем размер молекул воды. Это объясняется явлением адсорбции молекул воды у поверхности мембраны. Механизм гиперфильтрации при обратном осмосе через пористую мембрану объясняется тем, что поры такой мембраны достаточно велики, чтобы пропускать молекулы растворителя, но слишком малы, чтобы пропускать молекулы растворенных веществ. При обратном осмосе отделяются частицы (молекулы, гидратированные ионы), размеры которых не превышают размеров молекул растворителя, при этом мембраной задерживаются как высокомолекулярные вещества, так и большая часть низкомолекулярных веществ, а проходит через поры мембраны только почти чистый растворитель.
Обратный осмос принципиально отличается от обычного фильтрования. Если при обычном фильтровании образуется поток фильтрата в виде очищенного раствора (воды) и осадок откладывается на фильтровальной перегородке, то при обратном осмосе образуются два раствора, один из которых обогащен растворенным веществом. Механизм проницаемости при обратном осмосе значительно сложнее. При фильтрации водных растворов в порах лиофильной мембраны имеется слой связанной воды, которая уменьшает размеры пор и препятствует прохождению сильно гидратированных ионов. В то же время лиофильность мембраны способствует прохождению молекул воды.
Ультрафильтрация предназначена для концентрирования лиозолей при очистке сточных вод, растворов полимеров и их очистки от низкомолекулярных веществ. В процессе ультрафильтрации высокомолекулярные вещества задерживаются мембраной, так как размер их молекул больше, чем размер пор, или вследствие большого трения их молекул о стенки пор мембраны, а низкомолекулярные вещества и растворитель свободно проходят через ее поры.
От обычного фильтрования ультрафильтрация отличается отделением частиц меньших размеров и размером пор мембраны, которые при ультрафильтрации не должны превышать размеров частиц золя. Кроме того, в результате этого процесса получают более концентрированный лиозоль (суспензию), а не осадок, который образуется при обычном фильтровании. Перепады давлений при ультрафильтрации достигают 103 кПа и выше. Механизм ультрафильтрации близок к обычному фильтрованию.
На рис. 11.7 приведена схема применения процессов ультрафильтрации и обратного осмоса для разделения органических и неорганических веществ. Границы применения этих процессов поразмерам отделяемых веществ: обратный осмос - dч = 0,0001...0,001 мкм; ультрафильтрация - dч = 0,001...0,02 мкм. Давление, необходимое для проведения процесса обратного осмоса, 6... 10 МПа, для процесса ультрафильтрации - 0,1...0,5 М Па.
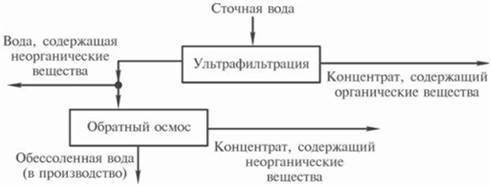
Рис. 11.7. Схема разделения органических и неорганических веществ
Эффективность процессов обратного осмоса и ультрафильтрации зависит от свойств мембран. В каждом методе применяют соответствующие мембраны. Различия в прохождении веществ через мембраны могут быть связаны как с равновесными, так и с кинетическими свойствами. По этим признакам мембраны подразделяют на фильтрационные (полупроницаемые) и диффузионные. Фильтрационные мембраны способны разделять вещества в равновесных условиях, размер их пор соизмерим с размерами проникающих частиц или молекул. Диффузионные мембраны обычно применяют для разделения газов методом газовой диффузии. Фильтрационные мембраны подразделяют на макро-, переходно- и микропористые (подобно адсорбентам). Микропористые мембраны могут быть нейтральными или ионитовыми.
Мембраны готовят из полимерных пленок, пористого стекла, керамики, металлической фольги, ионообменных материалов. Наибольшее применение получили мембраны на основе различных полимеров: ацетата целлюлозы, поливинилхлорида, полистирола, полиамидов и др.
Мембраны должны обладать высокой проницаемостью (удельной производительностью), хорошей селективностью (разделяющей способностью), стойкостью к действию среды, постоянством характеристик, достаточной механической прочностью.
Основными характеристиками процессов ультрафильтрации и обратного осмоса являются проницаемость и селективность мембран. Проницаемость (или удельная производительность) выражается количеством V фильтрата, отнесенным к единице времени t и единице поверхности S мембраны:
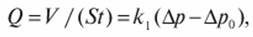 (11.37)
(11.37)
где k1 - коэффициент, зависящий от проницаемости мембраны; Δр - разность давлений раствора (воды) до и после мембраны; Δр0 - разность осмотических давлений.
Таким образом, скорость обратного осмоса прямо пропорциональна эффективному давлению (разности между приложенным давлением и осмотическим). Эффективное давление значительно превосходит осмотическое. Величина осмотического давления составляет: для соли Na2SO4 - 43 кПа, а для NaHCO3 - 89 кПа. Селективность определяют (в %) по следующей формуле:
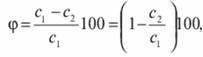 (11.38)
(11.38)
где с1 и с2 - концентрация растворенного вещества или дисперсной фазы соответственно в исходном растворе (сточной воде) и фильтрате (очищенной воде).
При 100%-й селективности мембрана пропускает только растворитель (очищенную воду).
Пористость β мембраны можно выразить соотношением
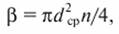 (11.39)
(11.39)
где dcр - средний диаметр пор, м; n - число пор на 1 м2 площади мембраны.
В процессе очистки некоторое количество растворимого вещества проходит через мембрану вместе с водой. Этот проскок S практически не зависит от давления:
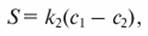 (11.40)
(11.40)
где k2 - константа мембраны.
Природа растворенного вещества оказывает влияние на селективность. При одинаковой молекулярной массе неорганические вещества задерживаются на мембране лучше, чем органические. С повышением давления удельная производительность мембраны увеличивается. Однако при высоких давлениях происходит уплотнение материала мембран, что вызывает снижение проницаемости, поэтому для каждого вида мембран устанавливают максимальное рабочее давление. Сростом температуры увеличивается проницаемость мембран, но при этом повышается осмотическое давление, которое уменьшает проницаемость; начинаются усадка и стягивание пор мембраны, что также снижает проницаемость; возрастает скорость гидролиза, сокращая срок службы мембран. Например, ацетатцеллюлозные мембраны при 50
Увеличение концентрации раствора приводит к росту осмотического давления растворителя, повышению вязкости раствора и росту концентрации поляризации, т.е. к снижению проницаемости и селективности. В тоже время проницаемость и селективность увеличиваются с повышением давления до определенного предела.
Так как через мембрану преимущественно проходит растворитель, то у ее поверхности значительно увеличивается концентрация растворенных или диспергированных веществ. Это явление называется концентрационной поляризацией. Оно может привести к снижению скорости процесса переноса, к осаждению растворенного вещества и коагуляции дисперсной фазы.
Для уменьшения влияния концентрации поляризации организуют рециркуляцию раствора и турбулизацию прилегающего к мембране слоя жидкости.
|
< Предыдущая |
Оглавление |
Следующая > |
|---|
