 Авторефераты по темам >>
Разные специальности - [часть 1] [часть 2]
Авторефераты по темам >>
Разные специальности - [часть 1] [часть 2]
Биохимические аспекты нарушений сосудисто-тромбоцитарного и плазменного гемостаза и методы их коррекции при метаболическом синдроме
Автореферат кандидатской диссертации
На правах рукописи
Хабарова Ольга Витальевна
Биохимические аспекты нарушений сосудисто-тромбоцитарного и плазменного гемостаза и методы их коррекции при метаболическом синдроме
03.01.04 - биохимия
АВТОРЕФЕРАТ
диссертации на соискание учёной степени
кандидата биологических наук
Ростов-на-Дону
2012
Работа выполнена на кафедре биохимии и микробиологии факультета биологических наук Федерального государственного автономного образовательного учреждения высшего профессионального образования Южный федеральный университет (г. Ростов-на-Дону)
Научный руководитель:а аа |
доктор биологических наук, профессор Внуков Валерий Валентинович |
Официальные оппоненты: |
доктор биологических наук,аа профессора Погорелова Татьяна Николаевна (г. Ростов-на-Дону) доктор медицинских наук, профессораа Франциянц Еленаа Михайловна (г. Ростов-на-Дону) |
Ведущая организация: |
ГОУ ВПО Нижегородскаяа государственная медицинскаяа академия (г. Нижний Новгород).а |
Защита диссертации состоитсяаа 28 амаяаа 2012 г. ва 13.00 часов на заседании диссертационного совета Д 212.208.07 в ФГАОУ ВПО Южный федеральный университет (г. Ростов-на-Дону, пр. Стачки 194/1, акт. зал).
С диссертацией можно ознакомится в библиотеке ФГАОУ ВПО Южный федеральный университет по адресу: г. Ростов-на-Дону, ул. Пушкинская, 148).
Автореферат разослан л_____________а 2012 г.
Ученый секретарь
диссертационного совета,
кандидат биологических наук, с.н.с. сланян Е.В.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Распространенность ожирения и метаболического синдрома (МС) приобретает глобальный характер среди населения практически всех развитых стран мира. В России лэпидемия МС достигает уровня 25-35% и более среди взрослого населения а(Балукова Е.В. и др., 2008). Высокий риск раннего развития ишемической болезни сердца (ИБС), сахарного диабета 2-го типа и атеросклероза у больных с МС придает этому синдрому особое медико-социальное значение. Доказано, что риск развития ИБС и/или инсульта у пациентов с МС повышен в 3Ц3,5 раза.а Как показывает статистика, наибольший процент инвалидизации и летальности в этой группе связан с сосудистыми осложнениями, нарушениями процессов свертывания крови с развитием внутрисосудистого тромбообразования. аПоказано, что смертность пациентов с МС от сердечно-сосудистых заболеваний в 23 раза выше, чем в общей популяции (Бутрова С.А., 2001). Развивающиеся на фоне МС нарушения тромбоцитарного иа плазменного гемостаза способны приводить к тромбозам различной локализации с тяжелыми последствиями (Ройтберг Г.Е. и др., 2007), при этом наличие гиперинсулинемии может усиливать тромбогенные осложнения (Lusher J.F., 1994).
Данные литературы, посвященные вопросам состояния системы гемостаза при МС, ограничиваются либо констатацией наличия гиперкоагуляционной направленности, либо содержат сведения об изменении уровня отдельных показателей. В опубликованных материалах имеются сведения о повышении содержания фибриногена, снижении фибринолиза, активации тромбоцитов при данной патологии. Несмотря на пристальное внимание к этой проблеме со стороны медико-биологических наук, многие вопросы патогенеза метаболического синдрома, в том числе и механизм развития гемостазиологических нарушений, связь этих изменений с эндотелиальной дисфункцией, остаются неразрешёнными. В этой связи изучение показателей сосудисто-тромбоцитарного и плазменного гемостаза, степени выраженности их изменений в зависимости от повреждения эндотелия, наличия воспалительного процесса при МС, а также поиск эффективной корригирующей терапии, направленнойа на максимальное снижение тромбогенного потенциала крови, а, следовательно, и риска развития сердечно-сосудистых заболеваний, представляется весьма актуальным.
Целью аработы явилось изучение биохимических показателей сосудисто-тромбоцитарного и плазменного гемостаза и обоснование методова коррекции выявленных нарушений при МС.
Для достижения поставленной цели решались следующие задачи:
1. Исследовать показатели функциональной активности сосудистого эндотелия.
2. Изучить состояние тромбоцитарного звена гемостаза.
3.а Исследовать состояние плазменного звена гемостаза.
4. Оценить состояние системы глутатиона.
5. Определить уровень маркеров воспалительного процесса.
6. Провести сравнительную оценку эффективности методов дието- и фармакотерапии МС с позиции их влияния на показатели сосудисто-тромбоцитарного и плазменного гемостаза, систему глутатиона, выраженность воспалительной реакции.
Научная новизна работы. В работе получены новые данные, свидетельствующие о наличии взаимосвязи изменений в системе гемостаза с активностью глутатионовой системы, развитием воспалительного процесса, нарушениями липидного, углеводного обменов, содержания мочевой кислоты при МС.
Впервые установлено, что комплексное использование сбалансированной по содержанию углеводов и жиров диеты в сочетании с физическими упражнениями приводит к стабилизации апоказателей функции сосудистого эндотелия, восстановлению системы глутатиона, снижению выраженности воспалительных процессов.
Впервые показано, что применение лекарственных средств, повышающих чувствительность тканей к инсулину (метформин) и содержащих ?-3- полиненасыщенные жирные кислоты (?-3-ПНЖК) (омакор), в разной степени приводит к снижению тромбогенного потенциала крови, восстановлению глютатионовой системыа у пациентов с МС.
Положения, выносимы на защиту
1. Развитие метаболического синдрома сопровождается ростом тромбогенного потенциала крови в результате нарушений сосудисто-тромбоцитарного и плазменного гемостаза, снижением активности ферментов глутатионовой системы и содержания восстановленного глутатиона.
2. Комплексное применение сбалансированной по содержанию жиров и углеводов диеты, индивидуально подобранной физической нагрузки, лекарственных средств - метформина, снижающего чувствительность тканей к инсулину и омакора, обладающего гиполипидемическим эффектом, способствует снижению у больных с аМС активации сосудисто-тромбоцитарного и плазменного гемостаза, восстановлению системы глутатиона, снижению содержания маркеров воспалительного процесса.
Научно-теоретическое и практическое значение результатов исследования. Выполненная работа позволяет расширить существующие представления о патогенезе метаболического синдрома, сформировать целостное представление о роли нарушений сосудисто-тромбоцитарного и плазменного гемостаза в развитии заболевания.
Проведена сравнительная оценка и дано теоретическое обоснование применения методов дието- и фармакотерапии при метаболическом синдроме для коррекции биохимических нарушений сосудисто-тромбоцитарного и плазменного гемостаза.
Показано, что важнейшими компонентами в развитии метаболического синдрома являются активация тромбогенного потенциала крови, снижение активности глютатионовой системы, развитие реакции воспаления. Нормализация функции эндотелия, показателей плазменного и тромбоцитарного звеньев гемостаза, глютатионовой системы, снижение содержания маркеров воспалительной реакции амогут абыть достигнуты при комплексном применении сбалансированной диеты в сочетании с физическими упражнениями и использовании лекарственных средств, снижающих инсулинрезистентность (ИР) (глюкофаж) и гиполипидемических, содержащих ?-3-ПНЖК (омакор).
Предложен перечень информативных биохимических показателей развития патологического процесса, характеризующийся простотой и оперативностью выполнения, который может быть использован для оценки степени тромбогенного риска у пациентов с МС.
Полученные в процессе проведенного исследования результаты могут использоваться в клинике как для диагностики состояния пациентов с метаболическим синдромом, так и для оценки эффективности проводимой терапии.
Апробация диссертационной работы. Материалы диссертации абыли представлены на ежегодной конференции ДиаМА (г. Ставрополь, 2009); Всероссийской научно-практической конференции Актуальные проблемы диагностики и лечения венозных и артериальных тромбозов (г. Санкт-Петербург, 2010); Всероссийской научно-практической конференции Модернизация науки и образования (г. Махачкала, 2011); Областной научно-практической конференции День специалиста клинической лабораторной диагностики (г. Ростов-на-Дону, 2012).
Публикации. По теме диссертации опубликовано 9 работ, из них 2 в журналах, рекомендованных ВАК РФ. Общий объем публикаций 0,83 п.л., личный вклад 63%.
Структура и объем диссертации. Диссертация изложена на 197 страницах машинописного текста и состоит из введения, обзора литературы, материалов и методов исследования, результатов и их обсуждения, выводов, списка литературы, включающего 112 отечественных и 97 зарубежных источников. Работа иллюстрирована 28 таблицами и 24 рисунками.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследуемая группа больных была сформирована из 57 пациентова обоего пола (33 женщины и 24 мужчин) в возрасте от 30 до 58 лет, которым впервые был установлен диагноз МС врачом-эндокринологом Ростовского эндокринологического центра городской больницы № 4. Лабораторное обследование больных отобранной группы апроводилось на базе клинико-диагностического лабораторного комплекса ГБУа РО ОКДЦ. аВ качестве контроля использовали данныеа обследования 20 здоровых доноров соответствующего пола (11 женщин и 9 мужчин) аи возраста, худощавого телосложения, без вредных привычек. Обследуемая группа больных согласно критериям диагностики МС (Всемирнойа организации здравоохранения, 1998а и Международной диабетической организации, а2005) имела: индекс массы тела (ИМТ) 37,422,8 кг/м2; отношение объёма талии к объёму бёдер (ОТ/ОБ) 0,940,03; уровень глюкозы натощак 6,120,05 ммоль/л; уровень иммунореактивного инсулина (ИРИ) 19,641,0 мкМЕ/л; индекс Caro 0,310,02; коэффициент атерогенностиа (Ка) 3,150,16;а артериальное давление (АД)а 14510/ 955. Пациенты с МС были аразделеныа на 3 группы в зависимости ота выраженностиа метаболических нарушенийа иа назначенной врачом-эндокринологом терапии:
- первую группу составилиа 20 пациентов (11 женщин и 9 мужчин), которыма в качестве анемедикаментозной терапии была назначенаа гипокалорийная диета с пониженным содержанием жиров и рациональная физическая нагрузка в виде ежедневной 30-минутнойа аэробной гимнастики.
- вторую группуа составили 18 пациентов (10 женщин и 8 мужчин) са наиболее выраженными изменениями со стороны углеводного обмена, которым было назначено лечение апрепаратома глюкофаж (метформин ) в дозе 1000 мг/в сут;
- третью группу составили 19 пациентов (12 женщин и 7 мужчин), имеющих наиболее выраженные изменения со стороны липидногоа обмена, которым было назначено алечение апрепаратом омакора в дозе 1000 мг/в сут.а Исследования осуществлялись исходно, через 3 и 6 месяцев после начала терапии.аа
аа Получение биологического материала. Кровь собирали утром натощак путем пункции локтевой вены, используя вакуумные системы для забора кровиа без антикоагулянтов для получения сыворотки и с антикоагулянтами а(гепарин, ацитрат натрия) для получения плазмы. Забор крови проводили в 3 этапа: до лечения (исходно), через 3 и 6 месяцев после начала терапии.
Методы определения показателей системы гемостаза. Содержание эндотелина-1 (Эн-1) в сыворотке крови определяли методом иммуноферментного анализа (ИФА) наборами Biomedica Gruppe (Австрия), оксид азота (NO)а - колориметрическима методом наборами RD Systems (США) на автоматическом анализаторе Labsystems Eims (Финляндия); концентрацию гомоцистеина - энзиматическим методом наборами фирмы DyaSis (Германия) на автоматическом анализаторе Сапфир 400 (Япония).а Регистрацию скорости и степени агрегации проводили на оптическом агрегометре Chrono Log 490D (США); протромбиновое время (ПВ), активированное частично тромбопластиновое время (АЧТВ), тромбиновое время (ТВ), активность плазминогена (Пл), антитромбина III (АнтIII), активность системы протеина С, афакторов свертывания кровиа (FVIII, FIX, FXIII), фактора Виллебранда (FW), ингибитора активатора плазминогена (PAI-1),а содержание Д-димера определяли в цитратнойа бедной тромбоцитами плазме стандартными клиническими наборами фирмыа Dade Behringа (Германия)а на автоматическом коагулометре BCT Dade Behring; фибринолитическую активность плазмы (фибринолиз) определяли с помощью наборов фирмы Технология Стандарт методом Kowarzyk, Buluk (1954); содержание растворимых фибрин-мономерных комплексов (РФМК) - ортофенантролиновым методом с помощьюа наборов Технология Стандарт.
Методы определенияа показателей аглутатионовой системы. Активность глутатионпероксидазы (GPox) определяли поа методуа Моин а(1986); активность глутатионредуктазы (GRe) - по методу Юсупова (1989); содержание восстановленного глутатиона (GSH) -а по методу Ellman (1959).
Методы определения маркеров воспаления. Содержание С-реактивного белка а(shСРБ) определяли высокочувствительным нефелометрическима методом наборами фирмы Siemensа на лазерном автоматическом нефелометреа Siemens BN Pro Spec; содержание фибриногена - наборами фирмы Dade Behring на автоматическом коагулометре BCT Dade Behring.
Методы определения показателей углеводно-инсулинового, липидного, пуринового обменов, содержания магния. аОпределение содержания глюкозы проводили натощак в венозной кровиа аглюкозооксидазным методом стандартными наборами фирмы Ольвекс (С.-Петербург); содержание иммунореактивного инсулина а(ИРИ) - наборами IRI наа автоматической иммунофлюоресцентном анализаторе закрытого типа Tosoh AIA -1800 (Япония); показатели липидного обмена: содержание общего холестерина (ОХС), триглицеридов (ТГЛ), ахолестерина липопротеинов очень низкой плотности (ХС-ЛПВ) определяли ферментативными колориметрическими методами наборами Dade Behring на автоматическом анализаторе Dimension (Германия); содержание аполипопротеинов А-1 и В (АПО-А-1, АПО-В) - наборами фирмы Siemensа на лазерном автоматическом нефелометреа Siemens BN Pro Spec ; свободных жирных кислот (СЖК) - ферментативным методом наборами фирмыа Diasys (Германия) на полуавтоматическома анализаторе BS 3000; асодержание мочевой кислоты и концентрацию ионов магния (Mg) определялиа колориметрическим методом анаборами фирмы Randox (Англия) на автоматическом анализаторе Сапфир 400 (Япония).
Статистическую обработку результатов проводили с помощью программ Exel 8,0 и Statistica 5. аЗначимость различий между изучаемыми величинами определяли по t-критерию Стьюдента. Различия считали достоверными при p<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Показателиа сосудисто-тромбоцитарного и плазменного гемостазаа приа метаболическом синдроме
Прежде всего, был проведен анализ метаболических нарушений, развивающихся при МС. Для этого показатели всех больных с МС, полученные до лечения, сравнивали с аналогичными показателями контрольной группы, которую составляли здоровые (в эндокринологическом плане) доноры.
Функциональное состояние сосудистого эндотелияа у больных с МСа
В результате проведенного нами исследования было установлено, что у больных с МС содержание Эн-1, FW, PAI-1 превышало аналогичные показатели здоровых аадоноров на 218, 47 и 30%, соответственно, т.е. в значительной степени был повышен уровень вазоконстрикторов. В то же время наблюдалось снижение основного вазодилататора - NO - на 32% (Рис. 1). Анализ содержания маркеров повреждения эндотелия позволяет заключить, что у обследованных нами пациентов с МС имеет место эндотелиальная дисфункция. Повышение уровня FW и PAI-1 свидетельствует о росте прокоагулянтного потенциала. Наличие гипергомоцистеинемии, выявленное у больных с МС, является дополнительным фактором риска развития атеротромбоза.
Состояние тромбоцитарного гемостазаа у больных с МС
Полученные результаты свидетельствовалиа о повышенной агрегационной активности тромбоцитов по сравнению с данными практически здоровых лиц контрольной группы. Зарегистрированная чувствительность рецепторов тромбоцитов у пациентов с МС к различным видам индукторов агрегации абыла различна (Рис. 2). Наиболее выраженные изменения наблюдались в отношении адгезивной активности под действием коллагена. В исследуемой группе пациентов с МСа степень и скорость агрегации тромбоцитов в присутствии коллагена адостоверно возрастали относительно контроля на 22% и 17%, соответственно, степень агрегации при действии ааденозиндифосфата (АДФ) - на 18% (скорость АДФ-агрегации при этом достоверно не менялась). При использовании в качестве индуктора эпинефрина достоверных изменений агрегационной активности тромбоцитов азарегистрировано не было (Рис. 2).
Усиление коллаген-индуцированной агрегации свидетельствует о возрастании способности тромбоцитов высвобождать содержимое своих гранул, в том числе и АДФ, что у больных с МС проявляется в виде усиления степени АДФ-зависимой агрегации.
а а а
а
Рис. 1. Изменения биохимических показателейа функционального состоянияа сосудистого эндотелияаа у больных с МС по сравнению с контрольной группой. Обозначения: * - аадостоверные различия ( р ? 0,05)
Рис. 2. Изменения показателей функциональной активности тромбоцитов у пациентов с МС по сравнению с контрольной группой. Обозначения как на Рис.1.
Состояниеа плазменного гемостаза у больных с МС
В плазме крови больных с МС был выявлен дисбаланс протромбогенных и антитромбогенных факторов ав пользу первых, что выражалось в достоверном увеличенииа уровня фибриногена на 19%, Пл - 12%, РФМК - 59%, FW - 49%, FVIII - 21%, FIX - 19%, аPAI-1 - 30% (Рис. 3). Достоверных изменений параметров ПВ, АЧТВ, ТВ, а также показателей противосвертывающей системы - АнтIII иа активность системы протеина С, маркера тромбинемии -а Д-димера авыявлено не было.
Cогласно новой концепцииа реакции активации свертывания крови (Spronk H., 2003; Добровольский А.Б, 2009), FVIII иа FIX факторы свертывания крови являются одними иза лотправных элементов запускающего каскада.а Фаза распространения обеспечиваетсяа теназой внутреннего пути - комплексом FVIIIа иа FIXа + FX, формирующимся на поверхности активированных тромбоцитов. Наличие увеличенной активности FVIII, FIXа в плазме крови больных с МС на фоне выраженной дисфункции эндотелия свидетельствует о серьёзном напряжении внутрисосудистого свертывания.

Рис. 3.а Изменения показателей плазменного гемостаза у больных с МС по сравнению с контрольной группой. Обозначения как на Рис.1.
Показатели системы глутатиона уаа больных с МС
В эритроцитах больных с МС по сравнению са контрольной группой наблюдалось достоверное снижение активности ферментов глутатионовой системы GRe , GPoxа и уровня восстановленного глутатиона GSH на 26%, 25%а и 28%, соответственно (Рис. 4).
Полученные результаты позволяют предположить, что снижение активности ферментов глутатионового цикла можета быть связано с функциональным использованием данных ферментов в эритроцитах. Нельзя также исключать вероятность свободнорадикального повреждения активного центра при окислительном стрессе, наличие которого у пациентов с МС доказано (Попова Т.П., 2009).
Показатели воспалительного процесса у больных с МС
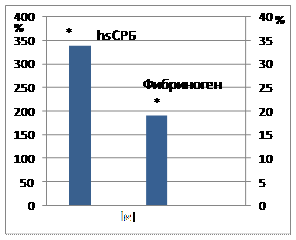
Проведенные исследования показали, что содержание hsСРБ на 338% превышало уровень, наблюдаемый у доноров. Содержание фибриногена превышало уровень здоровых людей на 19% (Рис. 5).а
 а
а
Рис. 4. Изменения показателей системы глутатиона уаа больных с МС по сравнению с контрольной группой. Обозначения как на Рис.1.
 а
а
Рис. 5. Изменения содержания hsСРБ и аафибриногена у больных с МС по сравнению с контрольной группой. Обозначения как на Рис.1.
Можно предположить, что повышенный синтез hsCRP инициируетсяа метаболитами висцеральной жировой ткани - интерлейкином-6 и фактором некроза опухоли-?, которые и запускают сосудистое воспаление. При воспалении образуется и накапливается большое разнообразие биологически активных агентов, с одной стороны, обеспечивающих защитную функцию, а с другой - являющихся триггерами процесса коагуляции.
Содержание Мg у пациентов с МС
Сегодня в литературе широко обсуждается роль Мg в метаболических нарушениях, имеющих место при МС. Указывается, что дефицит Мg вызывает инсулинорезистентность (Haenni A., 2001), способствует развитию оксидативного стресса (FreedmanA.M., et al., 1990, 1991), эндотелиальной дисфункции, оказывает проагрегантное влияние на форменные элементы крови (Шилов А.М. и др., 2010). Проведенные исследования показали, что в группе пациентов с МС содержание Мg было достоверно ниже (на 11%), чем в группе здоровых доноров.
Таким образом, полученные результаты свидетельствуют, о том, что у больных с МС до лечения имеет место выраженная эндотелиальная дисфункция, нарушения тромбоцитарного и плазменного гемостаза, характеризующиеся смещением баланса про- и анти-тромботических факторов в сторону первых.а Данные нарушения, развиваясь на фоне гиперлипидемии, гипергликемии, гиперинсулинемии, факторов системного воспаления, гипергомоцистеинемии и дефицита системы глутатиона, формируют сложную тромбогенерирующую систему, находящуюся в состоянии напряжения.
Показатели сосудисто-тромбоцитарного и плазменного гемостаза при лечении метаболического синдрома
В процессе проводимой терапии во всех обследуемых группах наблюдались достоверные положительныеа изменения функционального состояния сосудистого эндотелия разной степени выраженности (Рис. 6). Так, у первой группы больных с МС на фоне индивидуально подобранного диетического питания и регулярных физических нагрузок регистрировалась положительная динамика по большему (чем во второй и третьей группах) числу показателей, особенно после 6 месяцев лечения. Происходило достоверное снижение уровня Эн-1 на 50%, увеличение уровня NO на 58%,а снижениеа активностиа РАI-1 на 21 % и 22% (после 3-ха и 6-ти месяцев), снижение уровня гомоцистеина на 27% по сравнению с их значениями до лечения (Рис. 6).
Во 2 группе пациентов, которые получали метформин, отмечалось достоверное увеличениеа NO на 64% через 3 месяца терапии (которое после 6-и месяцев лечения нивелировалось) и достоверноеа снижение Эн-1 на 62% через 6 месяцев по сравнению с начальным периодом наблюдения (Рис. 6).
В 3 группе пациентов, которые получали омакор,а наблюдалось снижение Эн-1 на 59% и 64% через 3 и 6 месяцев, соответственно, и снижение активностиа РАI-1 на 57% через 6 месяцев лечения по отношению к исходным значениям.

Рис. 6. Изменения биохимических маркеров функционального состояния сосудистого эндотелия пациентов с МС на фоне терапии апо сравнению с начальным периодом наблюдения. Обозначения как на Рис.1.
На фоне проведения терапии в обследуемых группах наблюдали измененияа функциональной активности тромбоцитов у пациентов с МС. Так диетотерапия и регулярные физические нагрузки приводили к незначительной положительной динамике, проявляющейся в достоверном снижении скорости агрегации тромбоцитова при действии коллагенаа (на 8% через 6 месяцев) и АДФ-индукторов (скорости и степени агрегации - на 7% и 5%, соответственно через 3 месяца, а ттакже степени агрегации на 9% через 6 месяцев) (Рис. 7). Наблюдаемая положительная динамика стабилизации тромбоцитарного гемостаза может быть связана со снижением FW, регистрируемыма у больных данной группы.
Ва группе больных, получавших метформин, было выявлено достоверное уменьшение степени и скорости агрегационной активности тромбоцитов, наиболее выраженное под действием эпинефрина, соответственно, на 27% и 16% через 3 месяца иа на 29% и 19% - через 6 месяцев лечения. Полученные данные можно объяснить доказанным влиянием метформина на снижение периферической инсулинорезистентности (Wiernsperger N.F. et al., 1999), благодаря чему не развивается гипергликемияа и соответствующие процессы гликирования мембран клеток (возможно и тромбоцитов), способствующие образованию агрегатов.
Исследование показателейа тромбоцитарного гемостазаа в группе пациентов, получавших омакор, показало, что данная терапия приводилаа к достоверному снижению степени и скорости агрегационной активности тромбоцитов. Наиболее чувствительными к этому воздействию оказались эпинефрин (через 3 месяца - на 33% и 15% и через 6 месяцев - на 35% и 18%, соответственно) и АДФ (через 3 месяца - на 30% и 13% и через 6 месяцев - на 30% и 15%, соответственно).

Рис. 7. Изменения показателей функциональной активности тромбоцитов у пациентов с МС на фоне терапии по сравнению с начальным периодом наблюдения. Обозначения как на Рис.1.
Проводимая терапия в обследуемых группах больных с МС способствовала измененияма показателей плазменного гемостаза. На фоне диетотерапии и регулярных физических нагрузок наблюдалась достоверная положительная динамика после 3 месяцев лечения только по активности PAI-1 (снижение на 21% относительно начального периода наблюдения), а после 6-ти месяцев - аснижение концентрации фибриногена на 13%, активности PAI-1 - на 22%, увеличение активности Пл на 12% (Рис. 8 и 9). Изменения показателей гемостаза в результате лечения были проанализированы, также, в сравнении с их значениями в группе здоровых доноров. Так было зарегистрировано снижение активности FW на 14% и активация фибринолиза на 8% по отношению к контрольной группе.

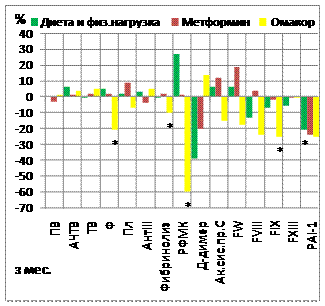 Зарегистрированная активация фибринолиза, может быть связана со снижением активности PAI-1, которое, в свою очередь, может быть результатом снижения уровня инсулина, также наблюдаемого в исследовании. а
Зарегистрированная активация фибринолиза, может быть связана со снижением активности PAI-1, которое, в свою очередь, может быть результатом снижения уровня инсулина, также наблюдаемого в исследовании. а
аа В
Рис. 8.а Изменение показателей плазменного гемостаза у больных с МС на фоне терапии аапо сравнению са начальным периодом наблюдения (А - через 3, В - через 6 месяцев лечения, соответственно). Обозначения как на Рис.1
После проведения терапии метформином также были получены положительные изменения: после 6 месяцев лечения наблюдалось достоверное увеличение ТВ на 7% и снижение активности FXIII на 20% по отношению к начальному периоду наблюдения. Это даёт основание предполагать, что метформин, вызывая снижение активности FXIII, осуществляющего перекрёстное сшивание фибрина, влияет на процессы конечного образования фибрина, его полимеризацию и агрегацию, что ведет к нарушению его структуры и функции. Всеа выше сказанное может приводить ак удлинению времени конечного пути образования фибрина - ТВ, регистрируемому в исследовании, а также свидетельствовать о снижении прокоагулянтной активности плазмы. Кроме того, в данной группе пациентов была отмечена следующая динамика показателей плазменного гемостаза (по отношению к контрольной группе): снижение активности FIX, увеличение активности системы протеина С (до лечения данный показатель не был изменен), увеличение активности Пл, незначительное снижение содержания фибриногена и активности FW, что расценивалось кака благоприятные факты ва условиях повышенного риска тромбообразования.
Исследование показателей плазменного гемостаза на фоне терапии омакором у пациентов с МС показало, чтоа трех- и шестимесячная терапия приводили к снижению активности FIX на 25% и 24%, активации афибринолиза на 10% и 8%, аснижению содержания фибриногена на 21% (только через 6 месяцев лечения), РФМК - на 60% и 54%, соответственно, что может расцениваться как положительная динамика.а Кроме того, к 6-му месяцу терапии наблюдалось улучшение всеха исследуемых показателей фибринолитической системы. Полученные результаты можно объяснить антитромботическима эффектом ?3-ПНЖК,а а именно,а увеличением фибринолитической активности вследствие снижения активности PAI-1, что согласуется с данными других авторов (Leaf A. et al., 1988).
Результаты исследования показали, что все три вида применяемой терапии априводили к достоверным положительным изменениям показателей системы глутатиона у больных с МС. Так в группе, находящейся на диетотерапии и физической нагрузке, наблюдали достоверную положительную динамику всех исследованных параметров данной системы (увеличение содержания GSH на 32%, активности аGReа - 45%, GPox - 25% относительно их исходных значений). В конце лечения показатели системы глутатиона ау больных данной группы практически соответствовали таковым ау здоровых доноров (Рис. 10).
В группе пациентов с МС, получающих метформин, наблюдали достоверное аувеличение содержания GSH на 29% и активности GRe - на 52% относительно фоновых значений. аИзменений активности GPox ана фоне терапии метформином неа наблюдалось. В группе пациентов с МС, принимающих омакор, аотмечались наиболее выраженные аизменения: асодержание аGSН увеличилось на 134%, аа активности GRe и GPox - на 106% и 12%, соответственно. Возможно, одним из факторов, влияющих наа восстановление GSН, может являтьсяа установленное в исследовании увеличение на фоне терапии омакором содержания Mg (на 20% и 24% после 3-х и 6-ти месяцев терапии, соответственно, относительно начального периода наблюдения), так кака последний являетсяа кофактором образованияа глутатиона (Шилов А.М. и др., 2010).
 а
а
Рис.10.а Изменения показателей системы глутатиона у больных с МС на фоне терапии по сравнению са начальным периодом наблюдения. Обозначения как на Рис.1
Наиболее выраженный противовоспалительный эффект наблюдался в группе пациентов, которым были назначены диетотерапия и рациональные физические нагрузки.а У них происходило снижение содержания маркеров воспаления - hsCRP и фибриногенаа на 50% и 13%, соответственно, после 6 месяцев терапии.а Снижение в результате проведенных процедур массы тела и доли жировой ткани как основного поставщика провоспалительных адипокинов, оказалось очень значимым на пути коррекции МС.
В группе пациентов, получавших метформин, достоверных измененийа показателей hsCRPа и фибриногена ав процессе лечения не наблюдалось (Рис. 11). Однако данные показатели достоверно изменились относительно значений, зарегистрированных в контрольной группе: их содержание снижалось на 61% и 4%, соответственно. В литературе отмечается, что противоспалительный эффект метформина не зависит от влияния на гипергликемию, а заключается в дозозависимом угнетении факторов транскрипции (NF-?B, активность IKK?-киназы и экспрессию адгезивных молекул, индуцированных фактором некроза опухоли-?) (Hannori Y. et al., 2006; Bullkao C. et al., 2007).
В группе пациентов с МС, получающих омакор,аа противовоспалительный эффект анаблюдался уже через 3 месяца лечения, что выражалось в достоверном снижением фибриногена на 21%, а через 6 месяцев - в снижении уровня hsCРБ на 78%. Антивоспалительный эффект омакора связан с вмешательством ?3-ПНЖК (путем превращений с участием 5Цлипоксигеназы в менее активные лейкотриены, например В5) в состав лейкотриенов - модуляторов воспаления (Оганов Р.Г. и др., 2011).

Рис. 11. Изменение содержания биохимических маркеров воспалительного процесса у больных с МС на фоне терапии по сравнению са начальным периодом наблюдения. Обозначения как на Рис.1.
Все проанализированные нами способы лечения МС оказывали тот или иной эффект на основные показатели углеводно-инсулинового, липидного обменов, содержание мочевой кислоты. Так, в группе пациентов, получавших немедикаментозное лечение, достоверноа снижались уровни инсулина и глюкозы, коэффициента атерогенности, увеличивался уровень ХС-ЛПВП, соотношения АПО-А-1/АПО-Б. В группе пациентов, получавших метформин, регистрировались достоверные положительные изменения асодержания глюкозы уже через 3 месяца терапии, снижение инсулина, более выраженное после 6-ти месяцев терапии, что подтверждает теорию о положительном влиянии на углеводный обмен бигуанидов. Также, было зарегистрировано достоверное увеличение ХС-ЛПВП и снижение уровня мочевой кислоты (относительноа контрольной группы). При исследовании пациентов с МС, принимающих омакор, была обнаружена положительная динамика содержания инсулина. Что же касается концентрации глюкозы, то у данной группы пациентов этот показатель находился в референтных пределах до начала лечения и не претерпевал достоверных изменений на фоне приема омакора. Влияние омакора на липидный обмен, в силу его основного назначения как гиполипидемического препарата, было достаточно эффективным: наблюдалось достоверное снижение,а в основном после 6 месяцев терапии,а ХС-ЛПОНП, ХС-ЛПНП,а ТГЛ, ОХС, СЖК, Ка, мочевой кислоты и увеличение холестерина липопротеинов высокой плотности (ХС-ЛПВП).
Таким образом, все проанализированные нами методы коррекции оказывали в той или аиной степени выраженное нормализующее действие на аанарушения сосудисто-тромбоцитарного, плазменного гемостаза, системы глутатиона,а показатели инсулиново-углеводного, липидного обменов, содержание мочевой кислоты и магния, а также наличие воспаления приа МС.а Сравнительный анализа эффективности использованных методов коррекции нарушений при МС, оцениваемой по количеству показателей достоверно улучившихся на фоне лечения по сравнению с начальным периодом наблюдения показал (Табл. 1), чтоа в схему лечения больных с МС целесообразно включать все 3 исследуемыха метода коррекции, но наиболее полный терапевтический эффект снижения выраженности нарушений системы гемостаза, а, следовательно, и прогрессирования сердечно-сосудистых осложнений при МС, можно получить путем применения комплексной терапии, состоящей из сочетанияа немедикаментозных методов (диеты и дозированных аэробных нагрузок) и препарата аомакор.а Одной из важных проблем остается проведение эффективного дозоподбора препарата метформина, поскольку он обладает важнейшим адля лечения МС патогенетическим свойством - улучшением чувствительности тканей к инсулину.
Таблица 1.
Сравнительный анализ влиянияа различных методов коррекции биохимических нарушений у пациентов с МС.
а Изменения |
Диетотерапияа и физическая нагрузка |
Метформин |
Омакор |
|||
3 мес |
6мес |
3 мес |
6мес |
3 мес |
6мес |
|
Углеводного обмена |
- |
-/+ |
+ |
аа + |
0 |
0 |
Инсулинового обмена |
+ |
+ |
- |
+ |
- |
+ |
ипидного обмена |
- |
-/+ |
- |
-/+ |
-/+ |
+ |
Пуринового обмена |
- |
- |
-/+ |
-/+ |
- |
-/+ |
Сосудистого эндотелия |
-/+ |
+ |
-/+ |
-/+ |
- |
-/+ |
Тромбоцитарногоа гемостаза |
-/+ |
-/+ |
-/+ |
+ |
+ |
+ |
Плазменного гемостаза |
- |
-/+ |
-/+ |
-/+ |
+ |
+ |
Системы глутатиона |
-/+ |
+ |
- |
+ |
-/+ |
+ |
Показатели воспаления |
-/+ |
+ |
- |
-/+ |
-/+ |
-/+ |
Содержанияа магния |
- |
- |
- |
- |
+ |
+ |
Содержания гомоцистеина |
-/+ |
+ |
- |
- |
- |
- |
Обозначения: - неэффективное воздействие терапии; -/+ малоэффективное воздействие терапии; + эффективное воздействие терапии; а0 не были изменены.
ВЫВОДЫ
1. Развитие метаболического синдрома сопровождается ростом тромбогенного потенциала крови (нарушением сосудисто-тромбоцитарного и плазменного гемостаза). аЭто проявляется в достоверном увеличении содержанияа вазоконстрикторов (Эн-1, FW, PAI-1, гомоцистеина) на фоне снижения содержания вазодилятатора - NO), повышении способности тромбоцитов к адгезии и агрегации, увеличении активности плазменных факторов свертывания (FVIII, FIX, FW), снижении активности фибринолитической системы (PAI-1), а также в увеличении содержания маркеров тромбинемии (фибриногена,а РФМК).
2. В крови больных с МС наблюдается снижение активности ферментов глютатионовой системы (глютатионредуктазы, глютатионпероксидазы) и содержания восстановленного глютатиона.
3. Применение рациональной диеты и индивидуально подобранной физической нагрузки у больных ас МС способствует стабилизации функции сосудистого эндотелия, восстановлению системы глутатиона, снижению выраженности воспалительных процессов.
4. аПрименение метформина способствует снижению у больных с МС активации тромбоцитарного гемостаза, восстановлению системы глутатиона на фоне улучшения чувствительности тканей к инсулину, нормализации углеводного обмена.
5. Применение омакора способствует снижению у больных с МС активации тромбоцитарного и плазменного гемостаза,а восстановлениюа системы глутатиона и содержания Mg на фоне нормализации инсулинового и липидного обменов.
Список работ, опубликованных по теме диссертации в изданиях,
рекомендованных ВАК РФ:
1. Хабарова О.В. Активность факторов свертывания у пациентов с метаболическим синдромом / Хабарова О.В., Крайнова Н.Н. Внуков В.В. // Валеология. 2010. № 3. С. 36-42 (0,24 п.л., личн. вк. 80%).
2. Хабарова О.В. Состояние сосудисто-тромбоцитарного звена гемостаза у больных с метаболическим синдромом / Внуков В.В., Крайнова Н.Н., Хабарова О.В. // Валеология. 2012. № 1. С35-38 (0,12 п.л., личн. вк. 50 %).
Список работ, опубликованных по теме диссертации
3. Хабарова О.В. Оценка липидного состава сыворотки крови у больных с сердечно-сосудистыми заболеваниями / Хабарова О.В., Вагнер В.П., Бутолина Л.Н., Назарова Л.Л. // Опыт деятельности диагностических центров, Москва, 1998. С. 102-103 (0,04 п.л., личн. вк. 70%).
4. Хабарова О.В. Метаболические нарушения у больных с синдромом инсулинрезистентности /Агеева В.Г., Бутолина Л.Н., Задерина В.А., Кивва В.Н., Фомичева Н.Г., Хабарова О.В., Черкашина. СФ. // Материалы научно-практической конференции к 10-летию клинико-диагностического центра Тульской областной больницы. Тула, 1998. С. 8-10 (0,08 п.л., личн. вк. 40%).
5. Хабарова О.В. Антиоксидантный статус у больных с хроническими заболеваниями печени / Ковалев Н.А., Хабарова О.В. // Сборник тезисов I Cъезда терапевтов Юга России, Ростов-на-Дону, 2000. С. 232-233 (0,04 п.л., личн. вк. 50%).
6. Хабарова О.В. Содержание магния в сыворотке крови у больных с патологией сосудистой и нервнойа систем / Хабарова О.В., Полторацкая Т.Э., Нехай Н.А. а// Материалыа III-й Межвузовской конференции молодых ученых, специалистов и студентов Обмен веществ при адаптации и повреждении, Ростов-наЦДону, 2004. С. 62-63 (0,04 п.л., личн. вк. 70%).
7. Хабарова О.В. Содержание молекул средней массы в плазме крови пациентов с метаболическим синдромом / Крайнова Н.Н., Попова Т.П., Внуков В.В., Хабарова О.В. // Сборника материалова ежегоднойа конференции ДиаМА, Ставрополь, 2009. С. 178-180 (0,08 п.л., личн. вк. 40%).
8. Хабарова О.В. Гемостазиологические нарушения у больных с метаболическим синдромом // Сборник материалов Всероссийской научно-практической конференции Актуальные проблемы диагностики и лечения венозных и артериальных тромбозов, Санкт-Петербург, 2010. С. 60-62 (0,08 п.л., личн. вк. 100%).
9. Хабарова О.В. Изучение показателейа глутатион-зависимого звена антиоксидантной системы при метаболическом синдроме / Хабарова О.В., Крайнова Н.Н. Внуков В.В. // Сборник материалов Всероссийской научно-практическойа конференции Модернизация науки и образования, Махачкала, 2011. С. 80-82 (0,08 п.л., личн. вк. 70%).
ПЕРЕЧЕНЬ ИСПОЛЬЗОВАННЫХ СОКРАЩЕНИЙ
АД - артериальное давление
АДФ - аденосиндифосфат
АнтIII - антитромбин
АПО-А-1, АПО-В - аполипопротеин - А-1 и -В
АЧТВ - активированное частично тромбопластиновое время
СРБ - С- реактивный белок
ИМТ Циндекс массы тела
ИР - инсулинорезистентность
ИРИ - иммунореактивный инсулин
ИФА - иммуноферментный анализ
Ка - коэффициент атерогенности
МС - метаболический синдром
ОТ/ОБ - отношение объёма талии к объёму бедер
ОХС - общий холестерин
ПВ - протромбиновое время
Пл - плазминоген
РФМК-растворимые фибринмономерные комплексы
СЖК - свободные жирные кислоты
ТВ - тромбиновое время
ТГЛ - триглицериды
Ф - фибриноген
ХС - (ЛПОНП, -ЛПНП,-ЛПВП) - холестерин липопротеинов очень низкой, - низкой, и высокой плотности (соответственно)
Эн -1-эндотелин-1
FVIII, FIX, FXIII, FXа, - факторы свертывания (а - активированный фактор свертывания)
FW - фактор Виллебранда
GSH - восстановленный глутатион
GPox - глутаионпероксидаза
GRe - глутатионредуктаза
NO - оксид азота
PAI-1- ингибитора активатора плазминогена-1
?3-ПНЖК - ?3- полиненасыщенные жирные кислоты
 Авторефераты по темам >>
Разные специальности - [часть 1] [часть 2]
Авторефераты по темам >>
Разные специальности - [часть 1] [часть 2]
